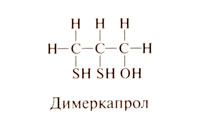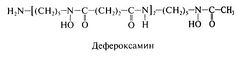Антидоты тяжелых металлов и железа
Источник:
Клиническая фармакология по Гудману и Гилману, том 4.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Железо
Соли железа, используемые для лечения железодефицитной анемии, — распространенная причина отравлений у детей младшего возраста. Отравление железом рассматривается в статье приведены общие сведения о деферокс-амине.
Радиоактивные тяжелые металлы
В связи с крупномасштабной добычей радиоактивных тяжелых металлов и их широким использованием в атомной энергетике, производстве ядерного оружия, научных исследованиях и медицинской диагностике случайные отравления этими веществами представляют серьезную опасность. Токсическое действие радиоактивных металлов почти полностью обусловлено ионизирующим излучением, поэтому цель лечения состоит не только в связывании этих металлов комплексобразующими средствами, но и в скорейшем и как можно более полном удалении радиоактивных веществ из организма.
Острую лучевую болезнь лечат главным образом симптоматически. Попытки использовать органические восстановители (например, меркаптамин) для предотвращения образования свободных радикалов особого успеха не имели.
При авариях ядерных реакторов и использовании ядерного оружия образуются в основном изотопы 239Pu, l37Cs, 144Се и 90Sr. Изотопы стронция и радия с трудом удаляются из организма с помощью комплексобразующих средств. Тому есть несколько причин. Во-первых, эти металлы обладают низким сродством к комплексобразующим средствам. Во-вторых, стронций и радий, откладываясь в костях, разрушают близлежащие капилляры. В результате нарушается кровоснабжение костей, и радиоактивные металлы не выводятся из них. Предпринимались попытки использовать разные комплексобразуюшие средства. Кальциево-тринатриевая сольдиэтилентриаминпентауксусной кислоты — ДТПА (см. ниже) — оказалась эффективной при отравлении M9Pu (Jones et al., 1986). Применение этого препарата вдозе 1 г в/в медленно 3 раза в неделю через день усиливает выведение некоторых радиоактивных металлов у животных и человека в 50—100 раз. Как и при отравлении нерадиоактивными тяжелыми металлами, с увеличением времени, прошедшего после контакта с радиоактивным металлом, эффективность лечения быстро падает.
Антидоты тяжелых металлов и железа
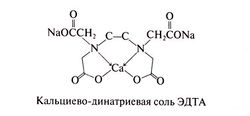
Кальциево-динатриевая соль ЭДТА
ЭДТА (этилендиаминтетрауксусную кислоту), ее динатриевую соль и другие родственные соединения уже много лет используют в промышленности и науке, поскольку эти вещества образуют хелатные комплексы со многими двух- и трехвалентными металлами. Побочное действие водорастворимых солей ЭДТА зависит от того, какой катион их формирует. Так, динатриевая соль ЭДТА вызывает гипокальциемическую тетанию. Однако использовать вместо динатриевой соли ЭДТА кальциево-динатриевую соль можно только при отравлениях теми металлами, которые имеют большее сродство к комплексобра-зующему средству, чем кальций.
Химические свойства и механизм действия
Фармакологические эффекты кальциево-динатриевой соли ЭДТА вытекают из ее способности образовывать хелатные соединения с двух- и трехвалентными металлами. Металлы (как экзогенные, так и эндогенные) с более высоким, чем у кальция, сродством к препарату образуют с ЭДТА хелатные комплексы, которые мобилизуются из тканей и выводятся. По данным экспериментов на мышах, кальциево-динатриевая соль ЭДТА связывает катионы некоторых эндогенных металлов, включая цинк, марганец и железо (Cantilena and Klaassen, 1982b). Основное показание к ее применению — отравление металлами, в первую очередь — свинцом.
При в/м введении кальциево-динатриевая соль ЭДТА хорошо всасывается, но инъекции болезненны, поэтому ее часто применяют в смеси с местным анестетиком или вводят в/в. В последнем случае препарат разводят в 5% глюкозе или физиологическом растворе и вводят путем в/в инфузии. Разведение необходимо для уменьшения риска тромбофлебита. Во избежание нефротоксического действия до начала терапии и во время нее необходимо поддерживать высокий диурез. Однако при свинцовой энцефалопатии и повышенном внутричерепном давлении поступление жидкости ограничивают, поэтому кальциево-динатриевую соль ЭДТА рекомендуется вводить в/м.
Свинцовое отравление
Эффективность кальциево-динатриевой соли ЭДТА при свинцовом отравлении объясняется способностью свинца вытеснять кальций из хелатных комплексов и доступностью токсичного металла для комплексобразующего средства. Доказательством тому служит усиление мобилизации и экскреции свинца. При отравлении ртутью кальциево-динатриевая соль ЭДТА неэффективна: хотя ртуть и вытесняет кальций из комплекса с ЭДТА in vitro, в организме она недоступна для препарата. Возможно, это обусловлено слишком прочной связью ртути с сульфгидрильными группами эндогенных лигандов или депонированием металла в тканях, в которые ЭДТА не проникает.
Кальциево-динатриевая соль ЭДТА мобилизует свинец, содержащийся в костях (Hammond, 1971). По окончании лечения металл из мягких тканей вновь постепенно перераспределяется в кости.
В 1980-х гг. в средствах массовой информации появились сведения о том, что ЭДТА уменьшает риск образования атеросклеротических бляшек, связывая находящийся в них кальций, однако подобное использование препарата не обосновано и неэффективно (Guldageret al., 1992; Elihuetal., 1998). Фармакокинетика. В ЖКТ всасывается менее 5% препарата. После в/в введения все вещество находится в плазме; Т1/2 составляет 20—60 мин. В организме кальциево-динатриевая соль ЭДТА присутствует в ионизированной форме, а потому плохо проникает через клеточные мембраны и распределяется преимущественно во внеклеточной жидкости (объем распределения препарата приблизительно равен объему внеклеточной жидкости). Концентрация препарата в СМЖ составляет всего лишь 5% его концентрации в плазме. В течение часа с мочой выводится около 50% препарата, в течение 24 ч — более 95%, поэтому необходимым условием успешного лечения служит нормальная работа почек. Выведение осуществляется только путем клубочковой фильтрации; почечный клиренс кальциево-динатриевой соли ЭДТА у собак соответствует клиренсу инулина. Ни изменение pH мочи, ни изменение скорости тока канальцевой жидкости не влияют на экскрецию препарата. ЭДТА почти не метаболизируется.
Побочные эффекты
Быстрое в/в введение динатриевой соли ЭДТА вызывает гипокальциемическую тетанию. При медленной инфузии (со скоростью менее 15 мг/мин) это осложнение обычно не развивается благодаря поступлению кальция из депо. В отличие от динатриевой соли, кальциево-динатриевую соль ЭДТА можно вводить в/в в относительно больших дозах, не опасаясь гипокальцие-мии, поскольку ни концентрация кальция в плазме, ни его общее содержание в организме при этом почти не изменяются.
Нефротоксическое действие. Это наиболее опасный из побочных эффектов кальциево-динатриевой соли ЭДТА. Повторное применение препарата в больших дозах вызывает гидропиче-скую дистрофию эпителия проксимальных канальцев и утрату щеточной каемки (Catsch and Harmuth-Hoene, 1979). В дистальных канальцах и клубочках патологические изменения не столь заметны. На ранних стадиях поражение почек обычно обратимо и после отмены препарата быстро проходит.
Один из предполагаемых механизмов нефротоксического действия кальциево-динатриевой соли ЭДТА — прохождение через канальцы большого количества хелатных комплексов с металлами за относительно короткий промежуток времени. Часть этих комплексов может диссоциировать из-за конкуренции ЭДТА с биологическими лигандами или изменения pH (внутри клеток либо в просвете канальцев). Другой, более вероятный механизм — взаимодействие комплексобразующего средства с эндогенными металлами в проксимальных канальцах.
Прочие побочные эффекты. К менее тяжелым побочным эффектам относятся недомогание, утомляемость и сильная жажда, сопровождаемые внезапным ознобом и лихорадкой. Впоследствии могут появиться сильная миалгия, головная боль в лобной области, снижение аппетита. Иногда наблюдаются тошнота и рвота; изредка возникают учащенное мочеиспускание и императивные позывы на мочеиспускание. Возможны чихание, заложенность носа, слезотечение, глюкозурия, анемия, дерматит напоминающий поражение кожи при авитаминозе В6, преходящее снижение систолического и диастолического АД, увеличение ПВ, а также инверсия зубца Т на ЭКГ.
ДТПА
ДТПА (диэтилентриаминпентауксусная кислота), как и ЭДТА, относится к многоосновным карбоновым кислотам, но отличается более высоким сродством ко многим тяжелым металлам. По данным многочисленных исследований на животных, по эффективности ДТПА не отличается от ЭДТА. Благодаря большему сродству к металлам ДТПА пытались применять при отравлениях тяжелыми металлами (особенно радиоактивными), не поддающихся лечению ЭДТА. К сожалению, эти попытки не имели особого успеха, возможно, потому, что ДТПА не проникает во внутриклеточные депо тяжелых металлов. ДТПА легко связывается с кальцием, поэтому ее используют в виде кальциево-тринатриевой соли. Применение ДТПА пока ограничено рамками клинических испытаний.
Димеркапрол
Историческая справка
Во время Второй мировой войны предпринимались многочисленные попытки разработать антидот люизита — содержащего мышьяк боевого отравляющего вещества кожно-нарывного действия. Поскольку мышьяк реагирует с сульфгидрильными группами, Стокен и Томпсон из Оксфордского университета стали систематически изучать тиолы, пытаясь обнаружить вещество, которое конкурировало бы с эндогенными лигандами за связывание с мышьяком. Оказалось, что мышьяк образует очень устойчивый и малотоксичный хелатный комплекс с димеркапролом — соединением, содержащим две сульфгидрильные группы (2,3-димеркаптопропанол). Присоединившиеся к исследованиям своих английских коллег американские ученые назвали димеркапрол британским антилюизитом. Фармакологические исследования показали, что димеркапрол эффективен и при отравлениях тяжелыми металлами. Химические свойства. Структурная формула димеркапрола следующая:
Димеркапрол — маслянистая жидкость со свойственным ти-олам резким, неприятным запахом. Поскольку водные растворы этого соединения неустойчивы, используется раствор димеркапрола в арахисовом масле. Димеркапрол и родственные ему тиолы легко окисляются.
Механизм действия
Фармакологические эффекты димеркапрола обусловлены формированием координационных связей между его сульфгидрильными группами и ионами металла. Эффективность лечения в значительной мере зависит от химических свойств образующихся хелатных комплексов. Выведение токсичных веществ (ртуть, золото, мышьяк) усиливается только в том случае, если эти комплексы стабильны. Однако in vivo комплекс димеркапрол—металл может диссоциировать, а сам димеркапрол — окисляться. К тому же в кислой среде канальцевой жидкости связь между серой и металлом становится неустойчивой, диссоциация хелатных комплексов усиливается, и высвободившийся металл оказывает токсическое действие на почки. Более стабильны хелатные комплексы, в которых две молекулы димеркапрола связаны с одним ионом металла. Следовательно, концентрация препарата в плазме должна быть достаточной для образования таких комплексов и их быстрого выведения, но не чрезмерно высокой, так как димеркапролу свойственны дозозависимые побочные эффекты. Поэтому дозу димеркапрола вводят дробно, следя за экскрецией токсичного металла.
Терапию димеркапролом нужно начинать как можно раньше, так как предотвратить с его помощью ингибирование содержащих сульфгидрильные группы ферментов легче, чем реактивировать эти ферменты. Димеркапрол служит антидотом веществ, которые реагируют с сульфгидрильными группами эндогенных лигандов, в первую очередь мышьяка, золота и ртути. Кроме того, в сочетании с кальциево-динатриевой солью ЭДТА препарат применяют при свинцовом отравлении, особенно при свинцовой энцефалопатии. При отравлении селенитами, которые окисляют ферменты, содержащие сульфгидрильные группы, димеркапрол неэффективен.
Фармакокинетика
Димеркапрол применяют только в/м. Препарат вводят глубоко в мышцу в виде раствора в арахисовом масле (100 мг/мл), поэтому при аллергии к арахису димеркапрол противопоказан. Максимальная концентрация в крови достигается через 30—60 мин. Препарат быстро элиминируется; его метаболизм и выведение почти полностью завершаются в течение 4 ч.
Побочные эффекты
Димеркапрол вызывает разнообразные побочные эффекты, но большинство из них скорее неприятны, чем опасны. У больных, получающих препарат в дозе 5 мг/кг, их частота составляет примерно 50%. Если интервал между инъекциями не меньше 4 ч, кумулятивного действия не наблюдается. Один из самых распространенных побочных эффектов — увеличение систолического и диастолического АД, сопровождающееся тахикардией. При повторном введении в дозе 5 мг/кг с интервалом 2 ч АД может повыситься на 50 мм рт. ст. АД повышается сразу после инъекции и возвращается к норме в течение 2 ч.
К другим побочным эффектам относятся (в порядке убывания частоты) тошнота и рвота; головная боль; чувство жжения на губах, во рту и в горле; ощущение сжатия, а иногда и боли в горле, груди и руках; конъюнктивит, блефароспазм, слезотечение, насморк и слюнотечение; покалывание в кистях; жжение в области полового члена; потливость лба, ладоней и других частей тела; боль в животе; болезненный асептический абсцесс в месте инъекции. Перечисленные симптомы часто сопровождаются тревогой и беспокойством. Многие из побочных эффектов возникают одновременно с артериальной гипертонией, а их выраженность соответствует степени повышения АД- Поскольку комплекс димеркапрола с металлом в кислой среде легко диссоциирует, для предотвращения токсического действия металла на почки во время лечения ощелачивают мочу. У детей помимо указанных побочных эффектов возможны лихорадка (в 30% случаев), исчезающая после отмены препарата. Возможно преходящее уменьшение числа нейтрофилов. У больных с недостаточностью Г-6-ФД димеркапрол может вызвать гемолитическую анемию. При печеночной недостаточности препарат противопоказан, за исключением тех случаев, когда она обусловлена отравлением мышьяком.
Сукцимер
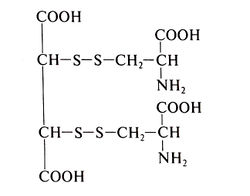
Сукцимер (2,3-димеркаптоянтарная кислота) — недавно разработанное комплексобразующее средство для приема внутрь. По химической структуре он близок к димеркапролу, но содержит две карбоксильные группы, которые влияют на распределение препарата и его способность образовывать комплексы с теми или иными веществами. Структурная формула сукцимера следующая:
Сукцимер взаимодействует с цистеином, образуя смешанный дисульфид (Aposhian and Aposhian, 1990):
Сукцимер усиливает выведение свинца с мочой, вследствие чего снижается концентрация металла в крови и исчезают вызванные свинцовым отравлением биохимические нарушения, в частности нормализуется активность аминолевулинатдегидратазы(Grazianoetal., 1992). Кроме того, комплекс сукцимера со свинцом выводится с желчью и подвергается кишечно-печеночному кругообороту.
Преимущество сукцимера в том, что он почти не повышает экскрецию микроэлементов, таких, как цинк, медь и железо. По данным экспериментов на животных, сукцимер эффективен при отравлениях кадмием, ртутью, другими металлами, а также мышьяком (Aposhian and Aposhian, 1990).
Сукцимер менее токсичен, чем димеркапрол, вероятно, благодаря меньшей растворимости в липидах, препятствующей его проникновению в клетки. Тем не менее при лечении сукцимером наблюдается преходящее повышение активности печеночных ферментов в сыворотке. Наиболее распространенные побочные эффекты — тошнота, рвота, понос и снижение аппетита. Возможна сыпь, которая иногда требует прекращения приема препарата.
В США сукцимер разрешено применять у детей с концентрацией свинца в крови выше 45 мкг%.
Пеницилламин
Историческая справка
Пеницилламин был впервые выделен в 1953 г. из мочи больных с поражением печени, получавших пенициллин. После того как было обнаружено, что пеницилламин способен образовывать хелатные комплексы, его стали использовать для лечения болезни Вильсона и отравлений тяжелыми металлами.
Химические свойства
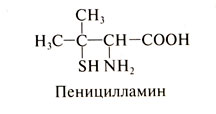
Структурная формула пеницилламина (3,3-диметилцистеина) следующая:
В клинической практике применяют d-пеницилламин, хотя l-пеницилламин тоже образует хелатные комплексы. Пеницилламин связывает медь, ртуть, цинк и свинец и усиливает выведение этих металлов с мочой.
Фармакокинетика
Несомненное преимущество пеницилламина перед другими комплексобразующими средствами — высокая степень всасывания в ЖКТ (40—70%). При приеме пищи, антацидных средств и препаратов железа всасывание пеницилламина ухудшается. Максимальная концентрация в крови достигается через 1—3 ч после приема (Netteret al., 1987). В отличие от своего неме-тилированного предшественника, цистеина, пеницилламин в меньшей степени подвержен действию цистатионин-у-лиазы и оксидазы L-аминокислот и потому относительно устойчив in vivo. При отравлении ртутью N-аце-тилпеницилламин эффективнее пеницилламина (Apos-hian and Aposhian, 1959), возможно, благодаря еще большей устойчивости к действию ферментов. Основной путь элиминации пеницилламина — печеночный метаболизм; в неизмененном виде выводится лишь незначительное количество препарата. Продукты метаболизма пеницилламина обнаруживают как в моче, так и в кале (Perrett, 1981).
Применение
Пеницилламин выпускают в таблетках и капсулах. Стандартные дозы для взрослых — 1—1,5 г/сут в 4 приема (см. разделы, посвященные отдельным металлам). Препарат следует принимать натощак, чтобы избежать взаимодействия с металлами, содержащимися в пище. Помимо отравлений медью, ртутью и свинцом пеницилламин используют при болезни Вильсона (гепатолентикулярная дегенерация), цистинурии и ревматоидном артрите. При болезни Вильсона пеницилламин, как правило, назначают в дозе 1—2 г/сут в 4 приема. Чтобы убедиться, что доза пеницилламина достаточна, следят за экскрецией меди.
Пеницилламин вступает в реакцию тиол-дисульфид-ного обмена с малорастворимым цистеином с образованием более растворимого смешанного дисульфида. Благодаря этому свойству препарат применяют при цистинурии. Стандартная доза — 2 г/сут в 4 приема; при необходимости дозу изменяют, ориентируясь на экскрецию цистина с мочой.
Механизм действия пеницилламина при ревматоидном артрите остается неясным. Возможно, терапевтический эффект обусловлен выраженным уменьшением концентрации ревматоидного фактора, представленного аутоантителами IgM (Wernick et al., 1983). Примечательно, что уровень других иммуноглобулинов в сыворотке при этом не снижается. Предлагались разные схемы лечения ревматоидного артрита пеницилламином. Начальная доза обычно составляет 125—250 мг 1 раз в сутки. При необходимости каждые 1—3 мес дозу увеличивают. До наступления заметного улучшения может пройти 2—3 мес. Во многих случаях эффект достигается при использовании доз, не превышающих 500—750 мг/сут.
Предпринимались попытки применять пеницилламин при первичном билиарном циррозе печени и системной склеродермии. Терапевтический эффект препарата при этих заболеваниях, возможно, тоже обусловлен уменьшением концентрации иммуноглобулинов и иммунных комплексов (Epstein et al., 1979).
Побочные эффекты
Основной побочный эффект кратковременной терапии пеницилламином — аллергические реакции, особенно при аллергии к пенициллинам (Bell and Graziano,1983). Риск аллергических реакций, обусловленных примесью пенициллина, сведен к нулю, так как современные препараты пеницилламина не содержат пенициллин. При длительном приеме пеницилламин вызывает поражения кожи, как легкие (сухость и шелушение), так и более выраженные (крапивница, пятнистая, папулезная или буллезная сыпь, волчаночный синдром, дерматомиозит). Кроме того, пеницилламин нарушает образование коллагена. Наблюдающаяся у трети больных крапивница или пятнисто-папулезная сыпь, сопровождающиеся отеком, зудом и лихорадкой, может быть следствием перекрестной реакции с пенициллинами (Bell and Graziano, 1983). Подробно поражения кожи, вызванные пеницилламином, описаны в работе Levy et al. (1983).
Пеницилламин способен вызвать тяжелые гематологические нарушения — лейкопению, эгоистическую анемию и агрануло-цитоз. Эти нарушения могут возникнуть в любые сроки после начала лечения и привести к смерти. Поэтому больные должны находиться под тщательным наблюдением.
Пеницилламин вызывает поражение почек, которое может ограничиться обратимыми протеинурией и гематурией или прогрессировать вплоть до развития нефротического синдрома вследствие мембранозной нефропатии. Зарегистрированы редкие случаи смерти от синдрома Гудпасчера (Hill, 1979).
Хотя органы дыхания поражаются редко, может развиться облитерирующий бронхиолит, сопровождающийся тяжелой одышкой. Длительный прием пеницилламина вызывает миастению (Gordon and Burnside, 1977). К менее опасным побочным эффектам относятся тошнота, рвота, понос, диспепсия, снижение аппетита, временная утрата вкусовых ощущений (сладкого и соленого). Последняя устраняется добавлением к пище меди. Противопоказания к терапии пеницилламином — беременность, почечная недостаточность, а также обусловленные приемом пеницилламина агранулоцитоз или эгоистическая анемия ванзмнезе.
Триентин
Пеницилламин — препарат выбора при болезни Вильсона. Однако из-за побочных эффектов (см. выше) некоторые больные его не переносят. В таких случаях используют триентин (триэтилентетрамин). Триентин усиливает экскрецию меди, хотя и в меньшей степени, чем пеницилламин. Препарат назначают внутрь в 2—4 приема натощак; максимальная суточная доза для взрослых — 2 г, для детей — 1,5 г. Триентин может вызвать дефицит железа; в этом случае помогает короткий курс лечения препаратами железа. Интервал между приемом триентинаи препаратов железа должен составлять не менее 2 ч.
Дефероксамин
Дефероксамин получают из Streptomyces pilosus в виде хелатного комплекса с железом, а затем химическими методами выделяют в чистом виде. Дефероксамин обладает чрезвычайно высоким сродством к трехвалентному железу (константа ассоциации КА = 1031) при очень низком сродстве к кальцию (КА = 102). По данным исследований in vitro, дефероксамин способен извлекать железо из гемосидерина и ферритина и, в меньшей степени, из трансферрина. Железо, входящее в состав гемоглобина и цитохромов, с помощью этого препарата не выводится.
Дефероксамин плохо всасывается в ЖКТ и в большинстве случаев применяется парентерально. При тяжелом отравлении железом (уровень железа в сыворотке выше 500 мкг%) предпочтительно в/в введение. Препарат вводят путем длительной в/в инфузии со скоростью 10-15 мг/кг/ч. Иногда скорость введения увеличивают до 45 мг/кг/ч. Быстрое в/в введение чревато падением дД. При умеренном отравлении (уровень железа в сыворотке 350—500 мкг%) дефероксамин можно применять в/м в дозе 50 мг/кг (максимальная доза — 1 г). Артериальная гипотония возможна и при в/м введении.
При гемосидерозе (например, у больных талассемия-ми) дефероксамин рекомендуется вводить в/м в дозе 0.5-1 г/сут. Возможно также п/к и в/в введение. Длительная п/к инфузия в дозе 1—2 г/сут почти столь же эффективна, как и в/в введение (Propper et al., 1977). При переливании крови больным талассемиями дефероксамин вводят путем в/в инфузии со скоростью не более 15 мг/кг/ч через отдельный катетер (по 2 г на каждую дозу перелитой крови). При гемохроматозе дефероксамин не применяют; методом выбора служит кровопускание. Дефероксамин назначают также для связывания алюминия у больных, находящихся на диализе (Swartz, 1985).
Дефероксамин метаболизируется в основном ферментами плазмы (хотя пути его метаболизма пока не изучены) и легко выводится с мочой.
Препарат вызывает разнообразные аллергические реакции, в том числе крапивницу и анафилактический шок. К другим побочным эффектам относятся болезненное мочеиспускание, неприятные ощущения в животе, понос, лихорадка, мышечные спазмы в ногах, тахикардия. Описаны случаи катаракты. Длительное лечение высокими дозами дефероксамина (при большой талассемии, требующей постоянных переливаний крови) приводит к поражению нервной системы с нарушениями зрения и слуха (Olivieri et al., 1986). В высоких дозах (10—25 мг/кг/ч) препарат вызывает поражение легких (Freedman et al., 1990; Castriota-Scanderbeg et al., 1990), проявляющееся тахипноэ, гипоксемией, лихорадкой и эозинофилией. Противопоказания к лечению дефероксамином — почечная недостаточность и анурия; при беременности препарат назначают только в случае крайней необходимости.
В настоящее время проходят испытания деферипрона (1,2-диметил-3-гидроксипиридин-4-он) — антидота железа для приема внутрь. Возможно, этот препарат станет приемлемой альтернативой для больных большой талассемией, которые не хотят или не могут лечиться дефероксамином (Olivieri et al., 1995).