Этапы разработки лекарственных препаратов — различия между версиями
Zabava (обсуждение | вклад) (→Этапы разработки лекарственных средств) |
Dormiz (обсуждение | вклад) |
||
| Строка 2: | Строка 2: | ||
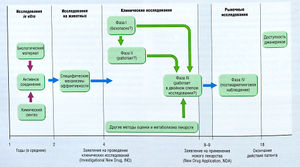
[[Image:Ph_3_1.jpg|300px|thumb|right|Рис. 3.1 Процесс разработки и оценки лекарства для вывода на рынок США.]] | [[Image:Ph_3_1.jpg|300px|thumb|right|Рис. 3.1 Процесс разработки и оценки лекарства для вывода на рынок США.]] | ||
| − | Между моментами создания нового лекарства и демонстрации его клинической эффективности и адекватной безопасности можно выделить несколько этапов (рис. 3.1). Этап первоначальной разработки обычно состоит в определении терапевтической дели (заболевание или состояние) или целевой молекулы, например рецептора, фермента и др., и последующем обнаружении основного химического соединения, т.е. вещества с характерным эффектом, необходимым для нового лекарства. В современных программах разработки лекарств чаще определяется целевая молекула, которая является ключевым звеном патологического процесса, и осуществляется поиск синтетических и природных соединений, действующих на эту молекулу. В дальнейшем пытаются разработать более подходящие соединения. Получение таких соединений — многократный процесс, включающий синтез похожих химических производных основного соединения. При разработке новых аналогов, чтобы получить требуемую эффективность, используют анализ взаимосвязи структура-активность (SAR или QSAR при количественной оценке). | + | Между моментами [[Создание лекарств|создания нового лекарства]] и демонстрации его клинической эффективности и адекватной безопасности можно выделить несколько этапов (рис. 3.1). '''Этап первоначальной разработки''' обычно состоит в определении терапевтической дели (заболевание или состояние) или целевой молекулы, например рецептора, фермента и др., и последующем обнаружении основного химического соединения, т.е. вещества с характерным эффектом, необходимым для нового лекарства. В современных программах разработки лекарств чаще определяется целевая молекула, которая является ключевым звеном патологического процесса, и осуществляется поиск синтетических и природных соединений, действующих на эту молекулу. В дальнейшем пытаются разработать более подходящие соединения. Получение таких соединений — многократный процесс, включающий синтез похожих химических производных основного соединения. При разработке новых аналогов, чтобы получить требуемую эффективность, используют анализ взаимосвязи структура-активность (SAR или QSAR при количественной оценке). |
| − | '''''Описание к рис. 3.1''' Процесс разработки и оценки лекарства для вывода на рынок США. Некоторые требования для препаратов, | + | '''''Описание к рис. 3.1''' Процесс разработки и оценки лекарства для вывода на рынок США. Некоторые требования для препаратов, используемых для лечения жизнеугрожающих заболеваний, могут отличаться [Katzung ВС. Basic and Clinical Pharmacology, 6th ed. New York: I Appleton & Lange]'' |
| − | Некоторые аналоги препаратов становятся объектами крупномасштабных фармакологических и токсикологических исследований для определения характеристик лекарств, которые могут получить одобрение для клинических исследований с участием пациентов. После серии клинических наблюдений полученные данные подаются в регулирующий орган для получения разрешения на реализацию нового лекарства. После этого с помощью различных методов собирают результаты клинического применения препарата. Этот процесс называют постмаркетинговыми наблюдениями (см. | + | Некоторые [[Препараты дженерики (аналоги)|аналоги препаратов]] становятся объектами крупномасштабных фармакологических и токсикологических исследований для определения характеристик лекарств, которые могут получить одобрение для клинических исследований с участием пациентов. После серии клинических наблюдений полученные данные подаются в регулирующий орган для получения разрешения на реализацию нового лекарства. После этого с помощью различных методов собирают результаты клинического применения препарата. Этот процесс называют постмаркетинговыми наблюдениями (см. [[Принятие фармакотерапевтического решения]]), которые регулируют менее строго, чем процедуры, необходимые до получения регистрации. |
'''Эксперименты на животных обеспечивают основу клинических наблюдений''' | '''Эксперименты на животных обеспечивают основу клинических наблюдений''' | ||
| − | Сведения о фармакологических эффектах лекарства in vitro и in vivo используют для предварительного заключения о его терапевтической ценности. Эти данные нужны для обоснования исследований на людях, поскольку без них не будет базы для оценки ожидаемой пользы и приемлемого риска нежелательных эффектов. Доклиническими исследованиями называют эксперименты in vitro и на животных, используемые для определения действия лекарства на уровне молекулы, клетки, определенной ткани или органа, оценки фармакологических свойств и изучения потенциальных терапевтических эффектов на животных моделях заболеваний человека. Исследования на животных также помогают изучить метаболизм и распределение лекарства в организме и разработать основные показания. Клинические исследования не могут быть продолжены, если не доказана безопасность лекарства. Для оценки возможной токсичности нового лекарства необходимы следующие исследования на животных: | + | Сведения о фармакологических эффектах лекарства in vitro и in vivo используют для предварительного заключения о его терапевтической ценности. Эти данные нужны для обоснования исследований на людях, поскольку без них не будет базы для оценки ожидаемой пользы и приемлемого риска нежелательных эффектов. Доклиническими исследованиями называют эксперименты in vitro и на животных, используемые для определения действия лекарства на уровне молекулы, клетки, определенной ткани или органа, оценки фармакологических свойств и изучения потенциальных терапевтических эффектов на животных моделях заболеваний человека. Исследования на животных также помогают изучить [[Метаболизм лекарственных средств|метаболизм]] и [[Распределение лекарственных средств|распределение лекарства в организме]] и разработать основные показания. Клинические исследования не могут быть продолжены, если не доказана безопасность лекарства. Для оценки возможной токсичности нового лекарства необходимы следующие исследования на животных: |
| − | *токсикологические исследования in vitro для оценки генетической и биохимической токсичности; | + | *токсикологические исследования in vitro для оценки генетической и биохимической [[Токсические эффекты|токсичности]]; |
*оценка острой токсичности с изучением физиологических систем (сердечно-сосудистая, центральная нервная, желудочно-кишечный тракт), кожи и слизистых (острое раздражение и возбуждение); | *оценка острой токсичности с изучением физиологических систем (сердечно-сосудистая, центральная нервная, желудочно-кишечный тракт), кожи и слизистых (острое раздражение и возбуждение); | ||
| Строка 32: | Строка 32: | ||
Клинические исследования начинаются после того, как собрано достаточное количество данных после исследований на животных в качестве обоснования для оценки нового лекарства в клинике и получения необходимого официального разрешения. Этапы разработки лекарства обозначают как фаза I, фаза II и фаза III. Фаза IV является этапом пост-маркетинговых наблюдений и других пострегистрационных клинических исследований (см. рис. 3.1). | Клинические исследования начинаются после того, как собрано достаточное количество данных после исследований на животных в качестве обоснования для оценки нового лекарства в клинике и получения необходимого официального разрешения. Этапы разработки лекарства обозначают как фаза I, фаза II и фаза III. Фаза IV является этапом пост-маркетинговых наблюдений и других пострегистрационных клинических исследований (см. рис. 3.1). | ||
| − | Фаза I включает первые клинические исследования с участием людей. Эти исследования проводят под очень строгим наблюдением, обычно они являются открытыми или одинарными слепыми (табл.3.2) и определяют наименьшую допустимую дозу по токсичности. Дальнейшие исследования проводят с меньшими дозами. Обычно в таких исследованиях участвуют молодые здоровые мужчины. В дальнейшем их заменяют группой больных. Также в эту фазу получают первичные данные о фармакокинетике. | + | ''Фаза I включает первые клинические исследования с участием людей''. Эти исследования проводят под очень строгим наблюдением, обычно они являются открытыми или одинарными слепыми (табл.3.2) и определяют наименьшую допустимую дозу по токсичности. Дальнейшие исследования проводят с меньшими дозами. Обычно в таких исследованиях участвуют молодые здоровые мужчины. В дальнейшем их заменяют группой больных. Также в эту фазу получают первичные данные о фармакокинетике. |
| − | Фаза II начинается после определения диапазона допустимых доз и рассматривается как доказательство концепции. Этот этап проходит с участием больных, у которых новое лекарство должно проявить свой потенциальный эффект. Основная цель состоит в получении доказательств того, что новое лекарство эффективно, т.е. обладает эффектами, полученными в доклинических исследованиях. Иногда конечной точкой клинических наблюдений фазы II является собственно терапия, в других случаях используют заместительные конечные точки исследований. Заместительная конечная точка прогнозирует или предположительно прогнозирует истинную конечную точку. Например, изучение лекарства при сердечной недостаточности может иметь истинную конечную точку при увеличении толерантности к нагрузке или выживаемости. Заместительная конечная точка для того же лекарства может быть уменьшением периферического сопротивления сосудов и улучшением сердечного выброса. Для лекарства, которое может предотвращать тромбообразование при ангиопластике, заместительной конечной точкой может быть ингибирование агрегации тромбоцитов, а истинной конечной точкой — уменьшение рестеноза. | + | ''Фаза II начинается после определения диапазона допустимых доз и рассматривается как доказательство концепции''. Этот этап проходит с участием больных, у которых новое лекарство должно проявить свой потенциальный эффект. Основная цель состоит в получении доказательств того, что новое лекарство эффективно, т.е. обладает эффектами, полученными в доклинических исследованиях. Иногда конечной точкой клинических наблюдений фазы II является собственно терапия, в других случаях используют заместительные конечные точки исследований. Заместительная конечная точка прогнозирует или предположительно прогнозирует истинную конечную точку. Например, изучение лекарства при сердечной недостаточности может иметь истинную конечную точку при увеличении толерантности к нагрузке или выживаемости. Заместительная конечная точка для того же лекарства может быть уменьшением периферического сопротивления сосудов и улучшением сердечного выброса. Для лекарства, которое может предотвращать тромбообразование при ангиопластике, заместительной конечной точкой может быть ингибирование агрегации тромбоцитов, а истинной конечной точкой — уменьшение рестеноза. |
Заместительная конечная точка наиболее удобна, когда она тесно связана с истинной конечной точкой. Так, например, заместительной конечной точкой является снижение артериального давления. Целью лечения гипертензии является снижение неблагоприятных сердечно-сосудистых реакций организма и почечной недостаточности как последствий гипертензии. Таким образом, снижение артериального давления — это заместительная конечная точка для уменьшения последствий гипертензии. | Заместительная конечная точка наиболее удобна, когда она тесно связана с истинной конечной точкой. Так, например, заместительной конечной точкой является снижение артериального давления. Целью лечения гипертензии является снижение неблагоприятных сердечно-сосудистых реакций организма и почечной недостаточности как последствий гипертензии. Таким образом, снижение артериального давления — это заместительная конечная точка для уменьшения последствий гипертензии. | ||
| − | Другие цели фазы II состоят в определении фармакокинетики лекарства и связи между эффектом и концентрацией вещества в плазме, если это возможно. Также изучается влияние заболеваний печени и почек на выведение лекарства из организма, фармакокинетические и фармакодинамические взаимодействия нового лекарства с другими средствами, с которыми их могут назначать совместно. | + | Другие цели фазы II состоят в определении [[Фармакокинетика: биодоступность, экскреция, клиренс, распределение|фармакокинетики]] лекарства и связи между эффектом и концентрацией вещества в плазме, если это возможно. Также изучается влияние заболеваний печени и почек на выведение лекарства из организма, фармакокинетические и фармакодинамические [[Взаимодействие лекарственных средств|взаимодействия нового лекарства с другими средствами]], с которыми их могут назначать совместно. |
Исследования в фазу II могут быть одинарными или двойными слепыми, параллельными или перекрестными, с использованием случайных выборок пациентов. В этнически разнородных популяциях, например в США, в фармакокинетических исследованиях иногда изучают особенности метаболизма лекарств у разных этнических групп. Этническая однородность является грубым усреднением генетической классификации. Возможно, в будущем более корректный подход к оценке путей метаболизма и клинических результатов будет состоять в классификации пациентов по их генетической предрасположенности к метаболизму лекарств. Тогда будет возможно предсказать, для какого генотипа лекарство будет более полезно, а для какого — токсично. Этот раздел фармакологии называют фармакогенетикой. | Исследования в фазу II могут быть одинарными или двойными слепыми, параллельными или перекрестными, с использованием случайных выборок пациентов. В этнически разнородных популяциях, например в США, в фармакокинетических исследованиях иногда изучают особенности метаболизма лекарств у разных этнических групп. Этническая однородность является грубым усреднением генетической классификации. Возможно, в будущем более корректный подход к оценке путей метаболизма и клинических результатов будет состоять в классификации пациентов по их генетической предрасположенности к метаболизму лекарств. Тогда будет возможно предсказать, для какого генотипа лекарство будет более полезно, а для какого — токсично. Этот раздел фармакологии называют фармакогенетикой. | ||
| − | В фазу III устанавливают эффективность и безопасность нового лекарства. Если возможно, проводят контролируемые рандомизированные двойные слепые исследования, которые всегда параллельны. Планируемая модель и размер всех клинических наблюдений, особенно фазы III, основывают на статистических действиях, например рандомизации процедур, чтобы после окончания исследования получить веское заключение. Кроме того, популяционные исследования фазы III должны усреднять целевую популяцию для данного лекарства. В исследовании должны участвовать пациенты с различными проявлениями изучаемого заболевания. Распределение по этническим группам и полу должно отражать таковое в популяции. Наибольшее внимание уделяют изучению детей, за исключением случаев, когда это нецелесообразно, например при изучении лекарств для лечения таких заболеваний у пожилых, как болезнь Альцгеймера. | + | ''В фазу III устанавливают эффективность и безопасность нового лекарства''. Если возможно, проводят контролируемые рандомизированные двойные слепые исследования, которые всегда параллельны. Планируемая модель и размер всех клинических наблюдений, особенно фазы III, основывают на статистических действиях, например рандомизации процедур, чтобы после окончания исследования получить веское заключение. Кроме того, популяционные исследования фазы III должны усреднять целевую популяцию для данного лекарства. В исследовании должны участвовать пациенты с различными проявлениями изучаемого заболевания. Распределение по этническим группам и полу должно отражать таковое в популяции. Наибольшее внимание уделяют изучению детей, за исключением случаев, когда это нецелесообразно, например при изучении лекарств для лечения таких заболеваний у пожилых, как болезнь Альцгеймера. |
'''Разработка лекарств является длительным процессом''' | '''Разработка лекарств является длительным процессом''' | ||
| Строка 54: | Строка 54: | ||
<table border="1"> | <table border="1"> | ||
<tr><td> | <tr><td> | ||
| − | <p>Термин</p></td><td> | + | <p>'''Термин'''</p></td><td> |
| − | <p>Определение</p></td></tr> | + | <p>'''Определение'''</p></td></tr> |
<tr><td> | <tr><td> | ||
<p>Контрольная группа</p></td><td> | <p>Контрольная группа</p></td><td> | ||
| Строка 84: | Строка 84: | ||
<p>Результат лечения, который прогнозирует истинную цель терапии, не являясь этой целью (например, снижение размера опухоли в качестве заместителя выживаемости)</p></td></tr> | <p>Результат лечения, который прогнозирует истинную цель терапии, не являясь этой целью (например, снижение размера опухоли в качестве заместителя выживаемости)</p></td></tr> | ||
</table> | </table> | ||
| + | |||
| + | == Читайте также == | ||
| + | |||
| + | *[[Создание лекарств]] | ||
| + | *[[Разработка новых лекарственных средств]] | ||
| + | *[[Этапы разработки лекарственных средств]] | ||
| + | *[[Регламенты и одобрение новых лекарственных средств]] | ||
| + | *[[Принятие фармакотерапевтического решения]] | ||
Текущая версия на 07:34, 17 октября 2014
Этапы разработки лекарственных средств[править | править код]
Между моментами создания нового лекарства и демонстрации его клинической эффективности и адекватной безопасности можно выделить несколько этапов (рис. 3.1). Этап первоначальной разработки обычно состоит в определении терапевтической дели (заболевание или состояние) или целевой молекулы, например рецептора, фермента и др., и последующем обнаружении основного химического соединения, т.е. вещества с характерным эффектом, необходимым для нового лекарства. В современных программах разработки лекарств чаще определяется целевая молекула, которая является ключевым звеном патологического процесса, и осуществляется поиск синтетических и природных соединений, действующих на эту молекулу. В дальнейшем пытаются разработать более подходящие соединения. Получение таких соединений — многократный процесс, включающий синтез похожих химических производных основного соединения. При разработке новых аналогов, чтобы получить требуемую эффективность, используют анализ взаимосвязи структура-активность (SAR или QSAR при количественной оценке).
Описание к рис. 3.1 Процесс разработки и оценки лекарства для вывода на рынок США. Некоторые требования для препаратов, используемых для лечения жизнеугрожающих заболеваний, могут отличаться [Katzung ВС. Basic and Clinical Pharmacology, 6th ed. New York: I Appleton & Lange]
Некоторые аналоги препаратов становятся объектами крупномасштабных фармакологических и токсикологических исследований для определения характеристик лекарств, которые могут получить одобрение для клинических исследований с участием пациентов. После серии клинических наблюдений полученные данные подаются в регулирующий орган для получения разрешения на реализацию нового лекарства. После этого с помощью различных методов собирают результаты клинического применения препарата. Этот процесс называют постмаркетинговыми наблюдениями (см. Принятие фармакотерапевтического решения), которые регулируют менее строго, чем процедуры, необходимые до получения регистрации.
Эксперименты на животных обеспечивают основу клинических наблюдений
Сведения о фармакологических эффектах лекарства in vitro и in vivo используют для предварительного заключения о его терапевтической ценности. Эти данные нужны для обоснования исследований на людях, поскольку без них не будет базы для оценки ожидаемой пользы и приемлемого риска нежелательных эффектов. Доклиническими исследованиями называют эксперименты in vitro и на животных, используемые для определения действия лекарства на уровне молекулы, клетки, определенной ткани или органа, оценки фармакологических свойств и изучения потенциальных терапевтических эффектов на животных моделях заболеваний человека. Исследования на животных также помогают изучить метаболизм и распределение лекарства в организме и разработать основные показания. Клинические исследования не могут быть продолжены, если не доказана безопасность лекарства. Для оценки возможной токсичности нового лекарства необходимы следующие исследования на животных:
- токсикологические исследования in vitro для оценки генетической и биохимической токсичности;
- оценка острой токсичности с изучением физиологических систем (сердечно-сосудистая, центральная нервная, желудочно-кишечный тракт), кожи и слизистых (острое раздражение и возбуждение);
- оценка подострой и хронической токсичности;
- оценка канцерогенности;
- оценка репродуктивной токсичности;
- оценка генетической токсичности.
При изучении острой токсичности оценивают эффекты, возникающие через несколько часов или дней после однократного введения. При изучении хронической токсичности рассматривают эффекты после введения повторных доз в течение нескольких недель или месяцев.
Однако надежность данных, полученных на животных, для прогнозирования клинических результатов зависит от уровня клинической релевантности модели. Например, модель пневмонии, вызванной золотистым стафилококком, хорошо прогнозируема. Инфицирование организма одинаково и у людей, и у животных. Иммунологический ответ против бактерий и легочная патология у животных и человека очень схожи. Напротив, животные модели других заболеваний только косвенно имитируют заболевания человека и менее предсказуемы. Обычно возможность разработки животной модели связана с пониманием патофизиологии конкретного заболевания. В указанном примере непосредственная причина пневмонии хорошо известна, в то время как точная этиология многих заболеваний не определена.
Изучение лекарства в клинике состоит из нескольких этапов
Клинические исследования начинаются после того, как собрано достаточное количество данных после исследований на животных в качестве обоснования для оценки нового лекарства в клинике и получения необходимого официального разрешения. Этапы разработки лекарства обозначают как фаза I, фаза II и фаза III. Фаза IV является этапом пост-маркетинговых наблюдений и других пострегистрационных клинических исследований (см. рис. 3.1).
Фаза I включает первые клинические исследования с участием людей. Эти исследования проводят под очень строгим наблюдением, обычно они являются открытыми или одинарными слепыми (табл.3.2) и определяют наименьшую допустимую дозу по токсичности. Дальнейшие исследования проводят с меньшими дозами. Обычно в таких исследованиях участвуют молодые здоровые мужчины. В дальнейшем их заменяют группой больных. Также в эту фазу получают первичные данные о фармакокинетике.
Фаза II начинается после определения диапазона допустимых доз и рассматривается как доказательство концепции. Этот этап проходит с участием больных, у которых новое лекарство должно проявить свой потенциальный эффект. Основная цель состоит в получении доказательств того, что новое лекарство эффективно, т.е. обладает эффектами, полученными в доклинических исследованиях. Иногда конечной точкой клинических наблюдений фазы II является собственно терапия, в других случаях используют заместительные конечные точки исследований. Заместительная конечная точка прогнозирует или предположительно прогнозирует истинную конечную точку. Например, изучение лекарства при сердечной недостаточности может иметь истинную конечную точку при увеличении толерантности к нагрузке или выживаемости. Заместительная конечная точка для того же лекарства может быть уменьшением периферического сопротивления сосудов и улучшением сердечного выброса. Для лекарства, которое может предотвращать тромбообразование при ангиопластике, заместительной конечной точкой может быть ингибирование агрегации тромбоцитов, а истинной конечной точкой — уменьшение рестеноза.
Заместительная конечная точка наиболее удобна, когда она тесно связана с истинной конечной точкой. Так, например, заместительной конечной точкой является снижение артериального давления. Целью лечения гипертензии является снижение неблагоприятных сердечно-сосудистых реакций организма и почечной недостаточности как последствий гипертензии. Таким образом, снижение артериального давления — это заместительная конечная точка для уменьшения последствий гипертензии.
Другие цели фазы II состоят в определении фармакокинетики лекарства и связи между эффектом и концентрацией вещества в плазме, если это возможно. Также изучается влияние заболеваний печени и почек на выведение лекарства из организма, фармакокинетические и фармакодинамические взаимодействия нового лекарства с другими средствами, с которыми их могут назначать совместно.
Исследования в фазу II могут быть одинарными или двойными слепыми, параллельными или перекрестными, с использованием случайных выборок пациентов. В этнически разнородных популяциях, например в США, в фармакокинетических исследованиях иногда изучают особенности метаболизма лекарств у разных этнических групп. Этническая однородность является грубым усреднением генетической классификации. Возможно, в будущем более корректный подход к оценке путей метаболизма и клинических результатов будет состоять в классификации пациентов по их генетической предрасположенности к метаболизму лекарств. Тогда будет возможно предсказать, для какого генотипа лекарство будет более полезно, а для какого — токсично. Этот раздел фармакологии называют фармакогенетикой.
В фазу III устанавливают эффективность и безопасность нового лекарства. Если возможно, проводят контролируемые рандомизированные двойные слепые исследования, которые всегда параллельны. Планируемая модель и размер всех клинических наблюдений, особенно фазы III, основывают на статистических действиях, например рандомизации процедур, чтобы после окончания исследования получить веское заключение. Кроме того, популяционные исследования фазы III должны усреднять целевую популяцию для данного лекарства. В исследовании должны участвовать пациенты с различными проявлениями изучаемого заболевания. Распределение по этническим группам и полу должно отражать таковое в популяции. Наибольшее внимание уделяют изучению детей, за исключением случаев, когда это нецелесообразно, например при изучении лекарств для лечения таких заболеваний у пожилых, как болезнь Альцгеймера.
Разработка лекарств является длительным процессом
- Время от подачи заявки на регистрацию до его получения составляет от 6 мес до нескольких лет, чаще 1-2 года
- Процесс разработки лекарства до регистрации обычно занимает 6-10 лет
Таблица 3.2 Клинические исследования, терминология
|
Термин |
Определение |
|
Контрольная группа |
Стандартная терапия (или плацебо при отсутствии стандартов), с которой сравнивают эффективность нового препарата |
|
Рандомизированное исследование |
Пациенты, участвующие в исследовании, имеют одинаковую возможность быть включенными в опытную или контрольную группу, а факторы, которые могут повлиять на результаты, одинаково распределены между двумя группами |
|
Двойное слепое исследование |
Ни врач, ни пациент не знают, получает ли данный пациент опытное или контрольное средство, что помогает избежать субъективизма |
|
Одинарное слепое исследование |
Врач знает, какой препарат назначен данному пациенту, но пациент не знает |
|
Открытое исследование |
Противоположно двойному слепому: и врач, и пациент знают, какое средство (опытное или контрольное)назначено и в какой дозе |
|
Параллельные исследования |
Одновременно оценивают как минимум две схемы, но пациенту назначают только один вид терапии |
|
Перекрестные исследования |
Пациенты получают каждый вид лечения последовательно и таким образом выступают в качестве контрольной группы для самих себя. Например, если лечение А оценивают относительно лечения В, то некоторые пациенты получают сначала А, потом В, а другие наоборот — сначала В, потом А. Так оценивают эффекты лекарственной терапии, а не порядка назначений |
|
Конечная точка |
Измеряют для оценки эффекта лекарства (например, нормализация артериального давления — конечная точка для оценки антигипертензивных средств, уменьшение боли — конечная точка для оценки анальгетиков) |
|
Заместительная конечная точка |
Результат лечения, который прогнозирует истинную цель терапии, не являясь этой целью (например, снижение размера опухоли в качестве заместителя выживаемости) |