Паратиреоидин (паратгормон) — различия между версиями
Febor (обсуждение | вклад) (Новая страница: «== Паратиреоидин (паратгормон, ПТГ) == === Историческая справка === Открытие паращитовидных …») |
Zabava (обсуждение | вклад) (→Физиология) |
||
| (не показана 1 промежуточная версия 1 участника) | |||
| Строка 14: | Строка 14: | ||
=== Синтез, секреция и методы иммунологического анализа === | === Синтез, секреция и методы иммунологического анализа === | ||
| − | + | Паратиреоидин (паратгормон) синтезируется в виде полипептида-предшественника. Вначале образуется так называемый препроПТГ, состоящий из 115 аминокислот. При переносе внутрь эндоплазматического ретикулума от этого полипептида отщепляется 25 N-концевых аминокислотных остатков, и он превращается в проПТГ Последний переносится в аппарат Гольджи, где от него отщепляются еще 6 аминокислотных остатков. В результате образуется ПТГ, который хранится в секреторных гранулах и из них высвобождается в кровь. В норме большая часть ПТГ разрушается путем протеолиза еще до секреции. При гипокальциемии интенсивность протеолиза снижается и секретируется больше паратгормона. Этот механизм позволяет быстро усилить секрецию гормона без активации белкового синтеза, требующего достаточно большого времени. При длительной гипокальциемии активируется и синтез ПТГ, что сопровождается гипертрофией паращитовидных желез. Ни препроПТГ, ни проПТГ в кровь не попадают. Синтез и процессинг паратиреоидина подробно описаны, например, в обзоре Кгоnenberg et al. (1994). | |
| − | T1/2 зрелого паратгормона в плазме составляет 2—5 мин; его элиминация примерно на 90% осуществляется печенью и почками При распаде ПТГ образуются фрагменты, продолжающие циркулировать в крови. Часть фрагментов образуется и в самих паращитовидных железах при протеолизе ПТГ. Фрагменты не обладают биологической активностью, но реагируют с | + | T1/2 зрелого паратгормона в плазме составляет 2—5 мин; его элиминация примерно на 90% осуществляется печенью и почками При распаде ПТГ образуются фрагменты, продолжающие циркулировать в крови. Часть фрагментов образуется и в самих паращитовидных железах при протеолизе ПТГ. Фрагменты не обладают биологической активностью, но реагируют с антителами к ПТГ. Тем не менее существуют иммунологические методы определения ПТГ, достаточно надежные для клинических целей. РИА с использованием двух видов моноклональ ных антител (одно — к N-концевому, а другое — к С-концевому участку молекулы) обладает высокой чувствительностью и позволяет точно определять содержание зрелого ПТГ. Этот метод теперь используется вместо старых вариантов РИА (Nus-sbaum and Potts, 1994). |
=== Физиология === | === Физиология === | ||
| − | Основная функция ПТГ — обеспечение постоянства концентрации кальция в крови. | + | Основная функция ПТГ — обеспечение постоянства концентрации кальция в крови. Паратиреоидин (паратгормон) влияет на всасывание кальция в кишечнике, мобилизацию кальция из костной ткани, экскрецию кальция с мочой, калом, потом и молоком. Действие ПТГ на ткани-мишени опосредуется мембранным рецептором, сопряженным с G-белком (гл. 2). Методами клонирования установлены аминокислотная последовательность рецептора и расположение семи его трансмембранных доменов (Juppner et al., 1991).[[Image:Gm62_3.jpg|250px|thumb|right|Рисунок 62.3. Регуляция обмена кальция.]] |
| − | |||
| − | Рисунок 62.3. Регуляция обмена кальция. | ||
=== Регуляция секреции === | === Регуляция секреции === | ||
| − | Самый мощный регулятор активности паращитовидных желез — концентрация ионизированного кальция в плазме. При низкой его концентрации секреция ПТГ возрастает и, если гипокальциемия сохраняется длительное время, развивается гипертрофия и гиперплазия паращитовидных желез. При высокой концентрации секреция ПТГ снижается. Исследования in vitro показали, что низкая концентрация ионизированного кальция в среде надолго стимулирует транспорт аминокислот в клетки паращитовидных желез, синтез нуклеиновых кислот и белка в них, ведет к увеличению объема цитоплазмы и усилению секреции ПТГ. Высокая концентрация кальция оказывает противоположное действие. Таким образом, кальций непосредственно регулирует состояние паращитовидных желез, равно как и синтез и секрецию ПТГ. | + | Самый мощный регулятор активности паращитовидных желез — концентрация ионизированного кальция в плазме. При низкой его концентрации секреция ПТГ возрастает и, если [[Гипокальциемия (недостаток кальция) - лечение|гипокальциемия]] сохраняется длительное время, развивается гипертрофия и гиперплазия паращитовидных желез. При высокой концентрации секреция ПТГ снижается. Исследования in vitro показали, что низкая концентрация ионизированного кальция в среде надолго стимулирует транспорт аминокислот в клетки паращитовидных желез, синтез нуклеиновых кислот и белка в них, ведет к увеличению объема цитоплазмы и усилению секреции ПТГ. Высокая концентрация кальция оказывает противоположное действие. Таким образом, кальций непосредственно регулирует состояние паращитовидных желез, равно как и синтез и секрецию ПТГ. |
| − | Колебания концентрации ионизированного кальция в крови воспринимаются специфическим мембранным рецептором, расположенным на поверхности клеток паращитовидных желез (Brown et al., 1993). Связывание кальция с рецептором подавляет секрецию ПТГ. Гиперкальциемия приводит к снижению внутриклеточного содержания цАМФ и активности | + | Колебания концентрации ионизированного кальция в крови воспринимаются специфическим мембранным рецептором, расположенным на поверхности клеток паращитовидных желез (Brown et al., 1993). Связывание кальция с рецептором подавляет секрецию ПТГ. [[Гиперкальциемия - лечение|Гиперкальциемия]] приводит к снижению внутриклеточного содержания цАМФ и активности протеинкиназы С, а гипокальциемия — к активации этого фермента. Однако связь между этими изменениями и сдвигами в секреции ПТГ выяснена не до конца. Другие факторы, которые повышают содержание цАМФ в клетках паращитовидных желез (например, p-адреностимуляторы и дофамин), также стимулируют секрецию ПТГ, но в гораздо меньшей степени, чем гипокальциемия. Активный метаболит [[витамин D|витамина D]] — кальцитриол — подавляет экспрессию гена ПТГ. Колебания уровня фосфата в крови в физиологическом диапазоне, по-видимому, не влияют на секрецию ПТГ (если, разумеется, эти колебания не приводят к существенным изменениям концентрации ионизированного кальция). При выраженных гипер- и гипомагниемии секреция ПТГ может снижаться (Rude et al., 1976). |
Таким образом, концентрация кальция в крови регулируется по механизму обратной связи: регуляторная система воспринимает уровень ионизированного кальция в крови, и в ответ на это меняется секреция ПТГ; последний действует на различные ткани-мишени, увеличивая поступление кальция в кровь. | Таким образом, концентрация кальция в крови регулируется по механизму обратной связи: регуляторная система воспринимает уровень ионизированного кальция в крови, и в ответ на это меняется секреция ПТГ; последний действует на различные ткани-мишени, увеличивая поступление кальция в кровь. | ||
| Строка 34: | Строка 32: | ||
=== Влияние на кости === | === Влияние на кости === | ||
| − | + | Паратиреоидин (паратгормон) увеличивает поступление кальция из костей в кровь, ускоряя процесс резорбции костной ткани, в ходе которой высвобождаются как органические, так и минеральные компоненты межклеточного вещества. Клетками-мишенями ПТГ в костях являются, вероятно, остеобласты. Рецепторы ПТГ на остеокластах обнаружены только у птиц. В отсутствие других клеток ПТГ не увеличивает активность остеокластов, нанесенных на поверхность кости. Реакция на гормон появляется, если остеокласты культивируются в среде, в которой до того находились остеобласты, подвергнувшиеся действию ПТГ. Это свидетельствует о важной роли остеобластов в стимуляции резорбции костной ткани под действием ПТГ (McSheehy and Chambers, 1986; Perry et al., 1987; Takanashi et al., 1988). | |
Под влиянием ПТГ предшественники остеокластов образуют новые единицы костного обновления. При длительном повышении уровня ПТГ происходят характерные гистологические изменения в костях: увеличивается число очагов резорбции и, соответственно, площадь костной поверхности, покрытой неминерализованным органическим матриксом. В данном случае это указывает не на нарушение минерализации, а на общее увеличение площади остеогенеза вследствие активации процессов обновления кости. | Под влиянием ПТГ предшественники остеокластов образуют новые единицы костного обновления. При длительном повышении уровня ПТГ происходят характерные гистологические изменения в костях: увеличивается число очагов резорбции и, соответственно, площадь костной поверхности, покрытой неминерализованным органическим матриксом. В данном случае это указывает не на нарушение минерализации, а на общее увеличение площади остеогенеза вследствие активации процессов обновления кости. | ||
| − | При инкубации ПТГ с изолированными остеобластами он обычно подавляет их функцию: снижаются образование коллагена I типа, щелочной фосфатазы и остеокальцина. Однако действие ПТГ in vivo включает не только влияние на отдельные клетки, но и увеличение общего количества активных остеобластов, поскольку возникают новые единицы костного обновления. В результате уровень остеокальцина и активность щелочной фосфатазы в плазме могут возрастать. Простой модели, которая полностью объясняла бы молекулярный механизм действия ПТГ на костную ткань, не существует. | + | При инкубации ПТГ с изолированными остеобластами он обычно подавляет их функцию: снижаются образование коллагена I типа, щелочной фосфатазы и остеокальцина. Однако действие ПТГ in vivo включает не только влияние на отдельные клетки, но и увеличение общего количества активных остеобластов, поскольку возникают новые единицы костного обновления. В результате уровень остеокальцина и активность щелочной фосфатазы в плазме могут возрастать. Простой модели, которая полностью объясняла бы молекулярный механизм действия ПТГ на костную ткань, не существует. Паратиреоидин (паратгормон) стимулирует образование цАМФ в остеобластах, но имеются данные и о роли внутриклеточного кальция в опосредовании некоторых эффектов этого гормона. |
=== Влияние на почки === | === Влияние на почки === | ||
| Строка 46: | Строка 44: | ||
=== Влияние на обмен фосфата === | === Влияние на обмен фосфата === | ||
| − | + | Паратиреоидин (паратгормон) увеличивает почечную экскрецию фосфата за счет снижения его реабсорбции, поэтому для гиперпаратиреоза характерна гипофосфатемия. | |
| − | Действие ПТГ на почки опосредуется цАМФ (Aurbach, 1988). В клетках коркового вещества почек найдена аденилатциклаза, активность которой возрастает под действием ПТГ. Это приводит к усилению синтеза цАМФ, который и влияет на канальцевую реабсорбцию. Часть цАМФ из клеток канальцев попадает в мочу, поэтому по содержанию цАМФ в моче судят об активности паращитовидных желез и чувствительности почек к ПТГ. Влияние на обмен других ионов. ПТГ снижает почечную экскрецию магния, увеличивая его реабсорбцию, и усиливает его мобилизацию из костной ткани (MacIntyre et al., 1963). | + | Действие ПТГ на почки опосредуется цАМФ (Aurbach, 1988). В клетках коркового вещества почек найдена аденилатциклаза, активность которой возрастает под действием ПТГ. Это приводит к усилению синтеза цАМФ, который и влияет на канальцевую реабсорбцию. Часть цАМФ из клеток канальцев попадает в мочу, поэтому по содержанию цАМФ в моче судят об активности паращитовидных желез и чувствительности почек к ПТГ. Влияние на обмен других ионов. ПТГ снижает почечную экскрецию магния, увеличивая его реабсорбцию, и усиливает его мобилизацию из костной ткани (MacIntyre et al., 1963). Паратиреоидин (паратгормон) повышает почечную экскрецию воды, аминокислот, цитрата, К+, бикарбоната, Na+, СГ и SOj~, но тормозит экскрецию Н+. Влияние ПТГ на почечную экскрецию кислот и оснований сходно с действием ацетазоламида, однако оно не опосредовано влиянием на карбоангидразу. |
=== Влияние на синтез кальцитриола === | === Влияние на синтез кальцитриола === | ||
| Строка 56: | Строка 54: | ||
=== Прочие эффекты === | === Прочие эффекты === | ||
| − | + | Паратиреоидин (паратгормон) снижает концентрацию кальция в молоке и слюне, несмотря на одновременное повышение его концентрации в плазме. Таким образом, постоянство концентрации кальция в крови обеспечивается также ингибирующим влиянием ПТГ на транспорт этого катиона в молоко и слюну. | |
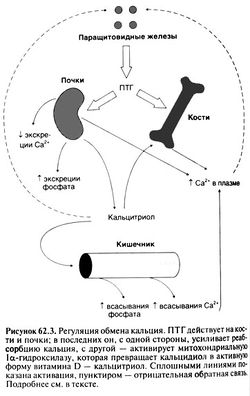
Общая схема регуляции концентрации кальция в крови (рис. 62.3). Реакция клеток паращитовидных желез даже на небольшое снижение концентрации ионизированного кальция возникает очень быстро (в течение минут). Коррекция кратковременных колебаний концентрации кальция в крови обеспечивается влияниями ПТГ на реабсорбцию кальция в почках. При более длительной гипокальциемии в почках активируется 1а-гидроксилаза, что приводит к увеличению образования кальцитриола; последний стимулирует всасывание кальция в кишечнике. Кроме того, в кровь поступает кальций из лабильной фракции костей. При длительной и тяжелой гипокальциемии ускоряются процессы обновления костей (возрастает количество единиц костного обновления); это также приводит к выходу кальция в кровь, но уже за счет снижения массы костной ткани. | Общая схема регуляции концентрации кальция в крови (рис. 62.3). Реакция клеток паращитовидных желез даже на небольшое снижение концентрации ионизированного кальция возникает очень быстро (в течение минут). Коррекция кратковременных колебаний концентрации кальция в крови обеспечивается влияниями ПТГ на реабсорбцию кальция в почках. При более длительной гипокальциемии в почках активируется 1а-гидроксилаза, что приводит к увеличению образования кальцитриола; последний стимулирует всасывание кальция в кишечнике. Кроме того, в кровь поступает кальций из лабильной фракции костей. При длительной и тяжелой гипокальциемии ускоряются процессы обновления костей (возрастает количество единиц костного обновления); это также приводит к выходу кальция в кровь, но уже за счет снижения массы костной ткани. | ||
| Строка 86: | Строка 84: | ||
== Применение ПТГ == | == Применение ПТГ == | ||
| − | В прошлом ПТГ применяли для повышения концентрации кальция в плазме, однако того же эффекта с большей безопасностью можно достичь введением кальция и витамина D. В списке разрешенных ФДА лечебных средств ПТГ отсутствует, но в ближайшем будущем может быть одобрено использование ПТГ или его аналогов при | + | В прошлом ПТГ применяли для повышения концентрации кальция в плазме, однако того же эффекта с большей безопасностью можно достичь введением кальция и витамина D. В списке разрешенных ФДА лечебных средств ПТГ отсутствует, но в ближайшем будущем может быть одобрено использование ПТГ или его аналогов при [[остеопороз]]е. Показано, что ежедневное введение ПТГ(1—34) больным с остеопорозом значительно увеличивает массу костной ткани позвоночника (см. «[[Остеопороз]]»). ПТГ(1—34) можно использовать для дифференциальной диагностики гипопаратиреоза и псевдогипопаратиреоза. Поскольку для псевдогипопаратиреоза характерна резистентность органов-мишеней к ПТГ, введение препарата не повышает экскрецию цАМФ с мочой. Эта проба позволяет выявить характер нарушений у отдельных больных и их родственников, однако диагноз обычно устанавливают путем определения уровня зрелого ПТГ в плазме. |
Текущая версия на 00:10, 15 августа 2013
Паратиреоидин (паратгормон, ПТГ)[править | править код]
Историческая справка[править | править код]
Открытие паращитовидных желез обычно приписывают Сендстрему, статья которого, опубликованная в 1880 г., прошла почти незамеченной. Десятилетием позже эти железы были вторично открыты Глеем, описавшим последствия их удаления вместе со щитовидной железой. Затем Вассале и Дженерали показали, что избирательное удаление паращитовидных желез быстро приводит к тетании, эпилептическим припадкам и смерти.
Мак-Каллем и Фегглин в 1909 г. первыми описали влияние паратиреоэктомии на концентрацию кальция в плазме. Довольно быстро была установлена связь между низкой концентрацией кальция и возникающими при этом симптомами, и начали формироваться представления о функции паращитовидных желез. Активные вытяжки из этих желез ослабляли гипокальциемическую тетанию у подвергнутых паратиреоэктомии животных, а у контрольных повышали концентрацию кальция в плазме (Berman, 1924; Collip, 1925). Эти данные впервые позволили связать клинические нарушения с гиперфункцией паращитовидных желез.
В то время как американские и английские физиологи изучали функцию паращитовидных желез, немецкие и австрийские патологоанатомы обнаружили фиброзно-кистозный остит у больных с опухолями этих желез. Олбрайт (Albright, 1948) в своем прекрасном историческом обзоре проследил, каким образом этими двумя разными путями удалось прийти к одинаковым заключениям.
Химические свойства[править | править код]
Молекулы паратиреоидина у человека, быка и свиньи представляют собой одноцепочечные полипептиды с молекулярной массой около 9500, состоящие из 84 аминокислот. Их аминокислотная последовательность полностью расшифрована. Биологической активностью обладают N-концевые участки цепи. Для связывания с рецепторами и проявления гормональной активности необходимы аминокислотные остатки с 1 по 27. Производные, лишенные первого или второго остатка, хотя и взаимодействуют с рецепторами, но почти не активны (Aur-bach, 1988). ПТГ быка и свиньи различаются семью аминокислотными остатками, а N-концевой участок ПТГ человека отличается от соответствующих участков бычьего и свиного гормонов только четырьмя и тремя остатками соответственно. Три этих гормона обладают почти одинаковой биологической активностью, но различаются иммунологически.
Синтез, секреция и методы иммунологического анализа[править | править код]
Паратиреоидин (паратгормон) синтезируется в виде полипептида-предшественника. Вначале образуется так называемый препроПТГ, состоящий из 115 аминокислот. При переносе внутрь эндоплазматического ретикулума от этого полипептида отщепляется 25 N-концевых аминокислотных остатков, и он превращается в проПТГ Последний переносится в аппарат Гольджи, где от него отщепляются еще 6 аминокислотных остатков. В результате образуется ПТГ, который хранится в секреторных гранулах и из них высвобождается в кровь. В норме большая часть ПТГ разрушается путем протеолиза еще до секреции. При гипокальциемии интенсивность протеолиза снижается и секретируется больше паратгормона. Этот механизм позволяет быстро усилить секрецию гормона без активации белкового синтеза, требующего достаточно большого времени. При длительной гипокальциемии активируется и синтез ПТГ, что сопровождается гипертрофией паращитовидных желез. Ни препроПТГ, ни проПТГ в кровь не попадают. Синтез и процессинг паратиреоидина подробно описаны, например, в обзоре Кгоnenberg et al. (1994).
T1/2 зрелого паратгормона в плазме составляет 2—5 мин; его элиминация примерно на 90% осуществляется печенью и почками При распаде ПТГ образуются фрагменты, продолжающие циркулировать в крови. Часть фрагментов образуется и в самих паращитовидных железах при протеолизе ПТГ. Фрагменты не обладают биологической активностью, но реагируют с антителами к ПТГ. Тем не менее существуют иммунологические методы определения ПТГ, достаточно надежные для клинических целей. РИА с использованием двух видов моноклональ ных антител (одно — к N-концевому, а другое — к С-концевому участку молекулы) обладает высокой чувствительностью и позволяет точно определять содержание зрелого ПТГ. Этот метод теперь используется вместо старых вариантов РИА (Nus-sbaum and Potts, 1994).
Физиология[править | править код]
Основная функция ПТГ — обеспечение постоянства концентрации кальция в крови. Паратиреоидин (паратгормон) влияет на всасывание кальция в кишечнике, мобилизацию кальция из костной ткани, экскрецию кальция с мочой, калом, потом и молоком. Действие ПТГ на ткани-мишени опосредуется мембранным рецептором, сопряженным с G-белком (гл. 2). Методами клонирования установлены аминокислотная последовательность рецептора и расположение семи его трансмембранных доменов (Juppner et al., 1991).
Регуляция секреции[править | править код]
Самый мощный регулятор активности паращитовидных желез — концентрация ионизированного кальция в плазме. При низкой его концентрации секреция ПТГ возрастает и, если гипокальциемия сохраняется длительное время, развивается гипертрофия и гиперплазия паращитовидных желез. При высокой концентрации секреция ПТГ снижается. Исследования in vitro показали, что низкая концентрация ионизированного кальция в среде надолго стимулирует транспорт аминокислот в клетки паращитовидных желез, синтез нуклеиновых кислот и белка в них, ведет к увеличению объема цитоплазмы и усилению секреции ПТГ. Высокая концентрация кальция оказывает противоположное действие. Таким образом, кальций непосредственно регулирует состояние паращитовидных желез, равно как и синтез и секрецию ПТГ.
Колебания концентрации ионизированного кальция в крови воспринимаются специфическим мембранным рецептором, расположенным на поверхности клеток паращитовидных желез (Brown et al., 1993). Связывание кальция с рецептором подавляет секрецию ПТГ. Гиперкальциемия приводит к снижению внутриклеточного содержания цАМФ и активности протеинкиназы С, а гипокальциемия — к активации этого фермента. Однако связь между этими изменениями и сдвигами в секреции ПТГ выяснена не до конца. Другие факторы, которые повышают содержание цАМФ в клетках паращитовидных желез (например, p-адреностимуляторы и дофамин), также стимулируют секрецию ПТГ, но в гораздо меньшей степени, чем гипокальциемия. Активный метаболит витамина D — кальцитриол — подавляет экспрессию гена ПТГ. Колебания уровня фосфата в крови в физиологическом диапазоне, по-видимому, не влияют на секрецию ПТГ (если, разумеется, эти колебания не приводят к существенным изменениям концентрации ионизированного кальция). При выраженных гипер- и гипомагниемии секреция ПТГ может снижаться (Rude et al., 1976).
Таким образом, концентрация кальция в крови регулируется по механизму обратной связи: регуляторная система воспринимает уровень ионизированного кальция в крови, и в ответ на это меняется секреция ПТГ; последний действует на различные ткани-мишени, увеличивая поступление кальция в кровь.
Влияние на кости[править | править код]
Паратиреоидин (паратгормон) увеличивает поступление кальция из костей в кровь, ускоряя процесс резорбции костной ткани, в ходе которой высвобождаются как органические, так и минеральные компоненты межклеточного вещества. Клетками-мишенями ПТГ в костях являются, вероятно, остеобласты. Рецепторы ПТГ на остеокластах обнаружены только у птиц. В отсутствие других клеток ПТГ не увеличивает активность остеокластов, нанесенных на поверхность кости. Реакция на гормон появляется, если остеокласты культивируются в среде, в которой до того находились остеобласты, подвергнувшиеся действию ПТГ. Это свидетельствует о важной роли остеобластов в стимуляции резорбции костной ткани под действием ПТГ (McSheehy and Chambers, 1986; Perry et al., 1987; Takanashi et al., 1988).
Под влиянием ПТГ предшественники остеокластов образуют новые единицы костного обновления. При длительном повышении уровня ПТГ происходят характерные гистологические изменения в костях: увеличивается число очагов резорбции и, соответственно, площадь костной поверхности, покрытой неминерализованным органическим матриксом. В данном случае это указывает не на нарушение минерализации, а на общее увеличение площади остеогенеза вследствие активации процессов обновления кости.
При инкубации ПТГ с изолированными остеобластами он обычно подавляет их функцию: снижаются образование коллагена I типа, щелочной фосфатазы и остеокальцина. Однако действие ПТГ in vivo включает не только влияние на отдельные клетки, но и увеличение общего количества активных остеобластов, поскольку возникают новые единицы костного обновления. В результате уровень остеокальцина и активность щелочной фосфатазы в плазме могут возрастать. Простой модели, которая полностью объясняла бы молекулярный механизм действия ПТГ на костную ткань, не существует. Паратиреоидин (паратгормон) стимулирует образование цАМФ в остеобластах, но имеются данные и о роли внутриклеточного кальция в опосредовании некоторых эффектов этого гормона.
Влияние на почки[править | править код]
В почках ПТГ оказывает двоякое действие. Во-первых, он усиливает реабсорбцию кальция и подавляет реабсорбцию фосфата; это приводит к повышению концентрации в крови кальция и снижению — фосфата. Во-вторых, ПТГ стимулирует превращение витамина D в его активную форму — кальцитриол (см. ниже). Последний связывается с рецепторами в кишечнике и стимулирует всасывание кальция, что также способствует повышению концентрации кальция в крови. Влияние на обмен кальция. ПТГ усиливает реабсорбцию кальция в дистальных отделах нефрона (Agus et al., 1973). Удаление паращитовидных желез при исходно нормальной концентрации кальция в плазме приводит к снижению его канальцевой реабсорбции и тем самым к увеличению его экскреции с мочой. Когда концентрация этого иона в плазме падает ниже 7 мг% (1,75 ммоль/л), его экскреция уменьшается: фильтруемое в клубочках количество кальция оказывается настолько малым, что он почти полностью реабсорбируется, несмотря на сниженную реабсорбционную способность канальцев. При введении ПТГ животным или человеку с гипопаратиреозом канальцевая реабсорбция кальция увеличивается, а экскреция уменьшается. Наряду с поступлением кальция из костей и усилением его всасывания в кишечнике это приводит к повышению концентрации кальция в крови. Когда она оказывается выше нормы, количество отфильтровавшегося кальция начинает превышать возможности канальцевой реабсорбции (даже усиленной под действием ПТГ) и возникает гиперкальциурия.
Влияние на обмен фосфата[править | править код]
Паратиреоидин (паратгормон) увеличивает почечную экскрецию фосфата за счет снижения его реабсорбции, поэтому для гиперпаратиреоза характерна гипофосфатемия.
Действие ПТГ на почки опосредуется цАМФ (Aurbach, 1988). В клетках коркового вещества почек найдена аденилатциклаза, активность которой возрастает под действием ПТГ. Это приводит к усилению синтеза цАМФ, который и влияет на канальцевую реабсорбцию. Часть цАМФ из клеток канальцев попадает в мочу, поэтому по содержанию цАМФ в моче судят об активности паращитовидных желез и чувствительности почек к ПТГ. Влияние на обмен других ионов. ПТГ снижает почечную экскрецию магния, увеличивая его реабсорбцию, и усиливает его мобилизацию из костной ткани (MacIntyre et al., 1963). Паратиреоидин (паратгормон) повышает почечную экскрецию воды, аминокислот, цитрата, К+, бикарбоната, Na+, СГ и SOj~, но тормозит экскрецию Н+. Влияние ПТГ на почечную экскрецию кислот и оснований сходно с действием ацетазоламида, однако оно не опосредовано влиянием на карбоангидразу.
Влияние на синтез кальцитриола[править | править код]
В клетках почечных канальцев осуществляется конечный этап активации витамина D — превращение его в гормональную форму, то есть в кальцитриол (см. ниже). Активность la-гидроксилазы, катализирующей это превращение, регулируется тремя основными факторами: фосфатом, ПТГ и кальцием. Снижение концентрации фосфата в крови или тканях быстро увеличивает образование кальцитриола. Мощным стимулятором образования кальцитриола является и ПТГ, тогда как гиперкальциемия и гиперфосфатемия подавляют этот процесс. Таким образом, когда гипокальциемия приводит к повышению секреции ПТГ, концентрация кальцитриола в крови возрастает не только из-за ПТГ -зависимого снижения концентрации фосфата, но и в силу прямого влияния гормона на активность 1а-гидроксилазы.
Прочие эффекты[править | править код]
Паратиреоидин (паратгормон) снижает концентрацию кальция в молоке и слюне, несмотря на одновременное повышение его концентрации в плазме. Таким образом, постоянство концентрации кальция в крови обеспечивается также ингибирующим влиянием ПТГ на транспорт этого катиона в молоко и слюну.
Общая схема регуляции концентрации кальция в крови (рис. 62.3). Реакция клеток паращитовидных желез даже на небольшое снижение концентрации ионизированного кальция возникает очень быстро (в течение минут). Коррекция кратковременных колебаний концентрации кальция в крови обеспечивается влияниями ПТГ на реабсорбцию кальция в почках. При более длительной гипокальциемии в почках активируется 1а-гидроксилаза, что приводит к увеличению образования кальцитриола; последний стимулирует всасывание кальция в кишечнике. Кроме того, в кровь поступает кальций из лабильной фракции костей. При длительной и тяжелой гипокальциемии ускоряются процессы обновления костей (возрастает количество единиц костного обновления); это также приводит к выходу кальция в кровь, но уже за счет снижения массы костной ткани.
Когда концентрация ионизированного кальция в плазме увеличивается, секреция ПТГ падает и канальцевая реабсорбция кальция уменьшается. Кроме того, снижение уровня ПТГ в крови способствует реабсорбции фосфата в почках. Как само по себе снижение уровня ПТГ, так и гиперфосфатемия подавляют образование кальцитриола, что, в свою очередь, приводит к уменьшению всасывания кальция в кишечнике. Наконец, замедляется и процесс обновления костей.
Схема регуляции концентрации кальция в крови приведена на рис. 62.3. Видно, что в этой регуляции участвуют 2 гормона (ПТГ и кальцитриол) и 3 эффекторных органа (почки, ЖКТ и кости). В приведенной схеме не учитывается роль других гормонов (например, кальцитони-на), но у человека они, по всей вероятности, не регулируют концентрацию кальция в крови самостоятельно, а лишь модулируют деятельность основной регуляторной системы, включающей ПТГ и витамин D.
Гипопаратиреоз[править | править код]
Это довольно редкое состояние, являющееся лишь одной из многих причин гипокальциемии (см. выше). Чаще всего гипопаратиреоз возникает после операций на щитовидной или паращитовидных железах. Реже он бывает обусловлен генетическими или аутоиммунными нарушениями. При псевдогипопаратиреозе биохимические нарушения такие же, как при гипопаратиреозе, но уровень ПТГ в крови повышен Это состояние обусловлено резистентностью органов-мишеней к ПТГ — обычно вследствие дефекта рецептора, G-белка или аденилатциклазы (Levine, 1999).
И при гипопаратиреозе, и при псевдогипопаратиреозе наблюдаются гипокальциемия и сопутствующие ей симптомы. Самый ранний симптом гипокальциемии — парестезия в конечностях. Постукивание молоточком по нервам вызывает сокращение соответствующих скелетных мышц (например, симптом Хвостека — сокращение мышц лица в ответ на удар молоточком по точке выхода лицевого нерва). Вслед за этим может развиться тетания — тонические судороги мышц (особенно судороги мышц кистей и стоп и ларингоспазм). Наконец, возникают генерализованные эпилептические припадки и другие центральные нарушения. Возможны симптомы со стороны гладкомышечных органов — спазмы ресничной мышцы (спазм аккомодации), мышц радужки, пищевода, кишечника, мочевого пузыря и бронхов. Изменения ЭКГ и выраженная тахикардия свидетельствуют о поражении сердца. Часто возникают спазмы сосудов пальцев рук и ног. При хроническом гипопаратиреозе встречаются изменения тканей эктодермального происхождения: выпадение волос, слоистость и ломкость ногтей, дефекты зубной эмали и катаракта; при рентгенографии головы можно обнаружить обызвествление базальных ядер. Нередко возникают психические симптомы: эмоциональная лабильность, тревога, депрессия и бред.
Для лечения гипопаратиреоза и псевдогипопаратиреоза применяют главным образом витамин D (см. ниже). Могут потребоваться также кальциевые добавки.
Гиперпаратиреоз[править | править код]
Первичный гиперпаратиреоз обусловлен гиперсекрецией ПТГ одной или несколькими парашитовидными железами. Концентрация кальция в плазме при гиперпаратиреозе иногда остается нормальной, но обычно повышена. Концентрация фосфата — на нижней границе нормы или снижена. Экскреция кальция с мочой, как правило, возрастает, отражая преобладание его фильтрации над канальцевой реабсорбцией (даже усиленной под влиянием ПТГ). Однако экскреция кальция при гиперпаратиреозе все же меньше, чем при гиперкальциемии иного происхождения (при одинаковой концентрации кальция в плазме). Вторичный гиперпаратиреоз развивается как компенсаторная реакция на снижение уровня кальция в крови и не сопровождается гиперкальциемией. При этом концентрация фосфата особенно мала (если только одновременно нет почечной недостаточности), а активность щелочной фосфатазы в сыворотке резко повышена.
При тяжелом первичном или вторичном гиперпаратиреозе может наблюдаться особое поражение костей — фиброзно-кистозный остит. Однако у большинства больных с первичным гиперпаратиреозом изменения костей выражены очень слабо. Обычно они включают умеренное снижение общей плотности костной ткани за счет компактного вещества; плотность губчатого вещества уменьшается мало (Bilezikian et al., 1994).
Диагностику гиперпаратиреоза упростило появление методов РИА, позволяющих определять уровень зрелого ПТГ. Сочетание гиперкальциемии с повышенным уровнем зрелого ПТГ позволяет поставить правильный диагноз более чем в 90% случаев.
Лечение[править | править код]
Удаление одиночной аденомы паращитовидной железы (примерно 80% случаев гиперпаратиреоза) или удаление либо субтотальная резекция нескольких гиперплазированныхжелез (около 15% случаев гиперпаратиреоза), проведенная опытным хирургом, приводит к излечению гиперпаратиреоза. Преходящая послеоперационная гипокальциемия может быть связана с временным нарушением кровоснабжения оставшейся железистой ткани или с усиленным поглощением кальция костной тканью. Постоянный гипопаратиреоз, требующий пожизненного лечения витамином D и кальциевыми добавками, — тяжелое, но редкое осложнение операций на паращитовидных железах.
Применение ПТГ[править | править код]
В прошлом ПТГ применяли для повышения концентрации кальция в плазме, однако того же эффекта с большей безопасностью можно достичь введением кальция и витамина D. В списке разрешенных ФДА лечебных средств ПТГ отсутствует, но в ближайшем будущем может быть одобрено использование ПТГ или его аналогов при остеопорозе. Показано, что ежедневное введение ПТГ(1—34) больным с остеопорозом значительно увеличивает массу костной ткани позвоночника (см. «Остеопороз»). ПТГ(1—34) можно использовать для дифференциальной диагностики гипопаратиреоза и псевдогипопаратиреоза. Поскольку для псевдогипопаратиреоза характерна резистентность органов-мишеней к ПТГ, введение препарата не повышает экскрецию цАМФ с мочой. Эта проба позволяет выявить характер нарушений у отдельных больных и их родственников, однако диагноз обычно устанавливают путем определения уровня зрелого ПТГ в плазме.