Противомалярийные средства (препараты) — различия между версиями
Zabava (обсуждение | вклад) (→Историческая справка) |
Zabava (обсуждение | вклад) (→Историческая справка) |
||
| Строка 141: | Строка 141: | ||
==== Историческая справка ==== | ==== Историческая справка ==== | ||
| − | Некоторые гидроксинафтохиноны обладают антипротозойной активностью, что и легло в основу создания синтетического препарата атоваквона, высокоактивного в отношении Plasmodium spp. и ряда условно-патогенных микроорганизмов (Hudson et al., 1991). Позже клинические испытания показали, что при лечении неосложненной тропической малярии атоваквоном улучшение наступает быстро, но и число рецидивов остается высоким (Looareesuwan et al., 1996). В то же время при назначении атоваквона вместе с прогуанилом доля выздоровевших велика, рецидивы возникают редко, а побочные эффекты незначительны (Looareesuwan et al., 1996, 1999а). В США выпускается комбинированный препарат атоваквон/прогуанил (Looareesuwan et al., 1999а). Атоваквон активен также в отношении Pneumocystis carinii и Toxoplasma gondii, которые вызывают тяжелые оппортунистические инфекции у больных СПИДом (Hughes et al., 1990). В 1992 г. после нескольких клинических испытаний ФДА одобрило этот препарат для лечения легкой и среднетяжелой пневмонии, вызванной Pneumocystis carinii, у больных с непереносимостью триметоприма/сульфаметоксазола (гл. 44). Атоваквон отчасти эффективен при поражениях головного мозга и глаз, вызванных Toxoplasma gondii, и применение его совместно с другими антипаразитарными препаратами еще изучается. Структурная формула атоваквона следующая: | + | Некоторые гидроксинафтохиноны обладают антипротозойной активностью, что и легло в основу создания синтетического препарата атоваквона, высокоактивного в отношении Plasmodium spp. и ряда условно-патогенных микроорганизмов (Hudson et al., 1991). Позже клинические испытания показали, что при лечении неосложненной тропической малярии атоваквоном улучшение наступает быстро, но и число рецидивов остается высоким (Looareesuwan et al., 1996). В то же время при назначении атоваквона вместе с прогуанилом доля выздоровевших велика, рецидивы возникают редко, а побочные эффекты незначительны (Looareesuwan et al., 1996, 1999а). В США выпускается комбинированный препарат атоваквон/прогуанил (Looareesuwan et al., 1999а). Атоваквон активен также в отношении Pneumocystis carinii и Toxoplasma gondii, которые вызывают тяжелые оппортунистические инфекции у больных СПИДом (Hughes et al., 1990). В 1992 г. после нескольких клинических испытаний ФДА одобрило этот препарат для лечения легкой и среднетяжелой пневмонии, вызванной Pneumocystis carinii, у больных с непереносимостью триметоприма/сульфаметоксазола (гл. 44). Атоваквон отчасти эффективен при поражениях головного мозга и глаз, вызванных Toxoplasma gondii, и применение его совместно с другими антипаразитарными препаратами еще изучается. Структурная формула атоваквона следующая:[[Image:Gm824.jpg|250px|thumb|right|Структурная формула атоваквона]] |
==== Антипаразитарная активность ==== | ==== Антипаразитарная активность ==== | ||
Версия 11:52, 31 августа 2013
Источник:
Клиническая фармакология по Гудману и Гилману том 3.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
- 1 Противомалярийные средства
- 2 Этиология и патогенез малярии
- 3 Классификация противомалярийных средств
- 4 Противомалярийные средства
- 5 Антибактериальные средства
- 6 Принципы профилактики и лечения малярии
- 7 Перспективы
Противомалярийные средства
Малярию вызывают четыре вида простейших рода Plasmodium, самый опасный из которых — Plasmodium falciparum. Из всех паразитарных заболеваний малярия наносит наибольший ущерб здоровью населения. В этой главе мы рассмотрим фармакологические свойства и применение основных препаратов, используемых для лечения и профилактики этого заболевания. Приступы малярии возникают при бесполом размножении возбудителей — эритроцитарной шизогонии. Наибольшей активностью в отношении плазмодиев на этой стадии развития обладают хлорохин, хинин, хинидин, мефлохин, атоваквон и производные артемизинина. Медленнее и не столь эффективно действуют на этой стадии прогуанил, пириметамин, сульфаниламиды, сульфоны и некоторые антибиотики. На дремлющие формы паразита (гипнозоиты), которые служат причиной рецидивов при малярии, вызванной Plasmodium vivax и Plasmodium ovale, действует только примахин. Ни один из противомалярийных препаратов при монотерапии не может сдержать распространение штаммов Plasmodium falciparum, которые приобретают устойчивость ко все большему числу лекарственных средств. Поэтому лучшим на сегодня подходом к лечению тропической малярии считают комбинированную терапию.
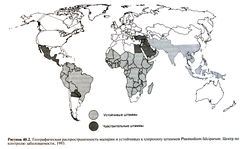
Малярия остается одним из самых опасных паразитарных заболеваний — поданным ВОЗ (1997 г.), каждый год во всем мире малярией заболевают более 500 млн человек, из них 1,7—2,5 млн — погибают. Большая часть смертельных исходов приходится на тропическую малярию (вызванную Plasmodium falciparum). Чаше умирают беременные, дети до 5 лет и неиммунные больные. К настоящему времени малярию удалось почти полностью искоренить в Северной Америке, Европе и в России, но в тропиках, особенно в Западной, Экваториальной и Южной Африке, она встречается все чаше и чаше, угрожая коренному населению и представляя опасность для путешественников.
Для борьбы с малярией нужны недорогие, эффективные и безопасные лекарственные средства, инсектициды и вакцины. В 1950-х гг. справиться с малярией не удалось в основном из-за появления устойчивости к инсектицидам и противомалярийным препаратам. С I960 г. в большинстве эндемических районов заболеваемость малярией возросла, распространились штаммы Plasmodium falciparum, устойчивые к хлорохину и другим препаратам, возросла степень лекарственной устойчивости. Не так давно устойчивые к хлорохину штаммы Plasmodium vivax обнаружены в Океании.
Почти все противомалярийные средства разрабатывались с целью воздействия на бесполые эритроцитарные формы возбудителей, которые служат причиной клинических проявлений. К препаратам этой группы, действующим быстро и эффективно, относятся хлорохин, хинин, хинидин, мефлохин, атоваквон и производные артемизинина. Прогуанил, пириметамин, сульфаниламиды, сульфоны и антибиотики, например тетрациклины, действуют медленнее и слабее. Гипнозоитов Plasmodium vivax и Plasmodium ovale, вызывающих рецидивы малярии, уничтожает только примахин. Все шире распространяются полирезистентные штаммы Plasmodium falciparum, и при монотерапии с ними не справится ни один препарат. Поэтому при тропической малярии рекомендуют назначать не менее двух препаратов, дополняющих друг друга по свойствам (White, 1997, 1999).
Метод выращивания Plasmodium falciparum in vitro (Тгаger and Jensen, 1976) позволил определять их чувствительность к противомалярийным средствам; близится к концу расшифровка генома Plasmodium falciparum (24,6 млн нуклеотидов) (Su et al., 1999) — эти и другие открытия, несомненно, помогут выявить новые молекулярные мишени противомалярийных препаратов, прояснят механизмы формирования устойчивости и будут способствовать созданию вакцины.
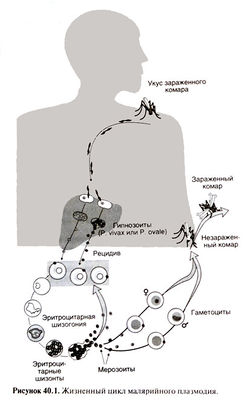
Чтобы понять, как действуют противомалярийные средства и по каким схемам их следует применять, необходимо рассмотреть жизненный цикл возбудителя малярии.
Этиология и патогенез малярии
Почти все случаи малярии и у человека вызываются четырьмя видами облигатных внутриклеточных паразитов — простейших рода Plasmodium. Малярия может передаваться при переливании крови и при использовании общих игл и шприцев, но чаще всего заражение происходит при укусе, когда спорозоиты из слюнных желез самки комара (рода Anopheles) попадают в кровь человека. С кровотоком спорозоиты быстро заносятся в печень и проникают в гепатоциты, где они размножаются и превращаются в тканевых шизонтов (рис. 40.1). Эта первичная стадия называется тканевой, или экзоэритроцитарной, шизогонией, протекает бессимптомно и длится у разных видов Plasmodium от 5 до 15 сут. Тканевые ши-зонты затем делятся, и из каждого образуются тысячи мерозоитов, которые попадают в кровь и внедряются в эритроциты. Начинается эритроцитарная шизогония. Plasmodium falciparum и Plasmodium malariae по окончании экзоэритроцитарной шизогонии полностью покидают печень. Напротив, при малярии, вызванной Plasmodium vivax или Plasmodium ovale, в гепатоцитах сохраняются дремлющие формы паразитов (гипнозоиты), которые могут вызывать рецидивы через несколько месяцев или лет после первого приступа. Как и почему образуются гипнозоиты, не ясно. Как только плазмодии вступают в стадию эритроцитарной шизогонии, они уже не могут проникнуть в другие ткани; поэтому при заражении во время переливания крови тканевой шизогонии не бывает. В эритроцитах большая часть плазмодиев превращается сначала в молодых (кольцевидных) шизонтов, затем в растущих и, наконец, в зрелых шизонтов. Вслед за этим содержащий шизонтов эритроцит разрушается, и в кровь выходят от 6 до 24 мерозоитов (у разных видов Plasmodium число мерозоитов различно). В этот момент у больного возникает лихорадка. Мерозоиты внедряются в другие эритроциты, и шизогония начинается вновь. Такие циклы повторяются до гибели больного, до приобретения им частичного иммунитета или до начала лечения противомалярийными препаратами. Периодичность паразитемии и лихорадки зависит от продолжительности эритроцитарной шизогонии. У Plasmodium falciparum, Plasmodium vivax и Plasmodium ovale последняя занимает около 48 ч. Одновременное разрушение эритроцитов и выход в кровь мерозоитов вызывает типичные приступы лихорадки через два дня на третий — отсюда название «трехдневная малярия*. При тропической малярии мерозоиты высвобождаются из эритроцитов неодновременно, к тому же зараженные эритроциты могут скапливаться в микроциркулятор-ном русле, поэтому зачастую периодичность лихорадки не столь выражена. При малярии, вызванной Plasmodium malariae, шизогония длится около 72 ч, поэтому приступы возникают через три дня на четвертый («четырехдневная малярия»).
Часть эритроцитарных шизонтов дают начало половым формам плазмодия — гаметоцитам. При попадании с кровью в желудок самки комара мужские гаметоциты делятся, образуя мужские гаметы (эксфлагелляция), которые затем сливаются с женскими гаметами. В результате оплодотворения возникает зигота. Проникнув в стенку желудка, она превращается в ооцисту. По мере созревания ооциста делится и дает начало спорозоитам, которые поступают в слюнные железы комара. С этого момента комар становится заразным для человека.
Каждый вид малярийного плазмодия вызывает болезнь с характерными симптомами и морфологическими изменениями в мазках крови.
- Plasmodium falciparum вызывает тропическую (трехдневную) малярию, самую опасную из всех форм малярии у человека. Внедряясь в эритроциты любого возраста, плазмодии этого вида могут вызывать очень высокий уровень паразитемии, секвестрацию пораженных эритроцитов в микроциркуляторном русле, гипогликемию, гемолиз, шок и полиорганную недостаточность. Позднее начало лечения (с появлением паразитемии) может стоить больному жизни, даже если удалось уничтожить всех паразитов в крови. При раннем начале лечения и правильном подборе препарата улучшение обычно наступаете течение 48 ч. При неправильном лечении паразиты остаются в крови, и их размножение может привести к рецидивам.
- Plasmodium vivax также вызывает трехдневную малярию, но протекает она легче тропической, так как пораженные эритроциты не секвестрируются в микроциркуляторном русле. Даже в отсутствие лечения смертность при этой форме малярии низкая, но нередко возникают рецидивы, вызванные гипнозоитами.
- Реже малярию вызывает Plasmodium ovale — периодичность приступов и частота рецидивов при этом такая же, как и при малярии, вызванной Plasmodium vivax, но болезнь протекает еще легче и быстрее поддается лечению.
- Plasmodium malariae вызывает четырехдневную малярию, которая распространена в отдельных районах тропиков. Рецидивы менее характерны, чем для малярии, вызванной Plasmodium vivax, однако они могут возникать даже через несколько лет после первого приступа.
Классификация противомалярийных средств
Противомалярийные средства можно классифицировать по стадиям жизненного цикла плазмодия, на которые они действуют, а также по показаниям к применению. Некоторые препараты действуют на малярийного плазмодия за счет нескольких механизмов.
Гистошизотропные препараты
Эти средства активны в отношении тканевых шизонтов в печени, готовых приступить к эритроцитарной шизогонии в течение ближайшего месяца. Эти препараты предотвращают внедрение плазмодия в эритроциты и дальнейшее его распространение. Прогуанил, первый препарат из этой группы, широко использовали для медикаментозной профилактики тропической малярии. Однако из-за роста устойчивости профилактика одним прогуанилом стала ненадежной. Примахин также активен в отношении Plasmodium falciparum, но этот препарат токсичен и применяется по другим показаниям (см. ниже).
Гистошизотропные препараты для профилактики рецидивов
Эти средства активны в отношении гипнозоитов Plasmodium vivax и Plasmodium ovale, которые остаются в гепатоцитах после окончания тканевой шизогонии, когда образовавшиеся мерозоиты уже поступили в кровь. В печени гипнозоиты созревают, чтобы спустя несколько месяцев или лет после первого приступа малярии перейти к эритроцитарной шизогонии и вызвать рецидив заболевания. Препараты, действующие на гипнозоитов, применяют для радикального лечения и профилактики рецидивов после возвращения из района, где распространены Plasmodium vivax и Plasmodium ovale. Прием для профилактики рецидивов начинают незадолго до или сразу после отъезда из эндемического района. Для радикального лечения эти средства применяют как в латентном периоде, когда гипнозоиты еще покоятся в печени, так и во время приступов. При лечении во время приступа препарат данной группы назначают вместе с противомалярийным препаратом, действующим на эритроцитарных шизонтов Plasmodium vivax и Plasmodium ovale. Примахин — основной препарат, который предотвращает рецидивы малярии, вызванные активацией гипнозоитов и повторным поражением эритроцитов.
Гематошизотропные препараты
Эти средства активны в отношении бесполых эритроцитарных форм малярийного плазмодия. Они нарушают эритроцитарную шизогонию и тем самым прерывают череду приступов. Кроме того, их можно использовать для полного уничтожения паразитов в эритроцитах. При неправильном лечении гематошизотропными препаратами эритроцитарная шизогония может возобновиться, что приводит к рецидиву.
За исключением примахина, все противомалярийные препараты были созданы для уничтожения бесполых эритроцитарных форм малярийного плазмодия. Эти средства можно разделить на две группы. К быстродействующим гематошизотропным препаратам относятся классические противомалярийные средства хлорохин, хинин (алкалоиды хины) и их производные, хинидин и мефлохин, а также атоваквон и производные артемизинина (эндопероксиды). Слабее и медленнее действуют антагонисты фолиевой кислоты и тетрациклины. И те, и другие чаше используют в сочетании с быстродействующими препаратами.
Гамотропные препараты
Эти средства действуют на половые формы малярийного плазмодия, предотвращая тем самым заражение комаров. Хлорохин и хинин действуют на гаметоциты Plasmodium vivax, Plasmodium ovale и Plasmodium malariae, а примахин особенно активен в отношении гаметоцитов Plasmodium falciparum. Однако для лечения приступов малярии гамотропные препараты не применяют, так как на бесполые эритроцитарные формы они не действуют.
Споронтоцидные препараты
Эти средства прерывают распространение малярии, угнетая образование ооцист и спорозоитов в организме комара. Хлорохин и ряд других противомалярийных препаратов также нарушают развитие плазмодия в организме комара, но в качестве споронтоцидных средств они не используются.
Рекомендуемые схемы медикаментозной профилактики у неиммунных лиц представлены в табл. 40.1, схемы лечения малярии у неиммунных больных — в табл. 40.2. Фармакологические свойства отдельных препаратов подробно рассмотрены ниже.
Противомалярийные средства
Артемизинин и его производные
Историческая справка
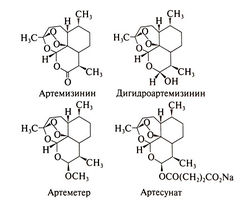
Артемизинин — сесквитерпен, в cocтaв которого входит эндопероксидный мостик и лактонное кольцо, — был выделен из растения цинхао, то есть полыни однолетней (Artemisia annua). В Китае уже более 2000 лет знают о целебных свойствах этого растения (Klayman, 1985). В 340 г. Гэ Xyн-прописывал чай из полыни однолетней при лихорадках, a i 1596 г. Ли Шичжэнь назначал эту траву для облегчения приступов малярии. К 1972 г. китайские ученые выделили из полыни и установили структуру цинхаосу — основного вещества, обладающего противомалярийным действием. Нам оно известно под названием артемизинин. Они же синтезировали три произвольных артемизинина с еще большей активностью, чем у исходного вещества: дигидроартемизинин (восстановленный артемизинин), артеметер (жирорастворимый метиловый эфир артемизинина) и артесунат (водорастворимый гемисукцинат дигид роартемизинина). В 1979 г. из Китая сообщили, что артемизинин и его производные безопасны и действуют быстро и эффективно при малярии, вызванной Plasmodium vivax и Plasmodiun falciparum. С тех пор в Китае, Юго-Восточной Азии и Африки более 2 млн больных малярией получали артемизинин или его производные, при этом тяжелых побочных эффектов и устойчивости возбудителей не отмечалось. В США эти препараты пока не выпускают, но они находят применение в других странах. Противомалярийные эндопероксиды, особенно в сочетании гематошизотропными препаратами длительного действия (мефлохин), значительно улучшают прогноз при тяжелой малярии вызванной штаммами Plasmodium falciparum, устойчивыми к многим противомалярийным препаратам (Meshnick et al., 1996 Newton and White, 1999). Структурные формулы артемизинина и его производных следующие:
Схемы медикаментозной профилактики и самостоятельного лечения малярии у неиммунных лица
Профилактика малярии, вызванной чувствительными к хлорохину штаммами Plasmodium falciparum, Plasmodium vivax, Plasmodium malariae и Plasmodium ovale
Хлорохин. Взрослым назначают 500 мг хлорохина фосфата (300 мг в пересчете на основание) внутрь 1 раз в неделю. Детям — 8,3 мг/кг (5 мг/кг в пересчете на основание) внутрь 1 раз в неделю. Прием начинают за 1 нед до въезда в эндемический район и продолжают еще 4 нед после возвращения. Примечание: для искоренения гипнозоитов Plasmodium vivax и Plasmodium ovale и полного излечения после отъезда из района, где эти виды широко распространены, используют примахин (см. текст и табл. 40.2).
Профилактика малярии, вызванной устойчивыми к хлорохину и полирезистентными штаммами Plasmodium falciparum. Примечание: выбор схемы зависит от чувствительности возбудителей к препаратам в данной местности и от других факторов (см. текст) Рекомендуемые схемы:
Мефлохин. Выпускают только для приема внутрь. Взрослым и детям весом > 45 кг назначают по 1 таблетке (250 мг мефлохина гидрохлорида, 228 мг в пересчете на основание) 1 раз в неделю. Детям весом 5—9 кг назначают по 1/8 таблетки; 10— 19 кг — 1/4 таблетки; 20—30 кг — 1/2 таблетки; 31—45 кг — 3/4 таблетки 1 раз в неделю. Прием начинают за 1 нед до въезда в эндемический район и продолжают еще 4 нед после возвращения. Примечание: мефлохин не рекомендуется назначать при эпилептических припадках, тяжелых неврологических и психических нарушениях, аллергических реакциях на производные аминохинолина в анамнезе, а также детям весом до 5 кг.
Доксициклин. Выпускают в капсулах, таблетках, покрытых оболочкой, и в виде растворов для приема внутрь. Взрослым назначают 100 мг/сут внутрь. Детям старше 8 лет — 2 мг/кг/сут внутрь с постепенным повышением дозы до 100 мг/сут. Прием начинают за 1 сут до въезда в эндемический район и продолжают еще 4 нед после возвращения. Эту схему применяют в районах, где преобладают полирезистентные штаммы Plasmodium falciparum. Примечание: прием доксициклина для профилактики малярии не должен длиться более 4 мес; препарат не следует назначать детям до 8 лет и беременным. Доксициклин противопоказан при аллергии к тетрациклинам. Профилактику доксициклином можно сочетать с приемом хлорохина (по такой же схеме, как и для профилактики малярии, вызванной чувствительными к хлорохину плазмодиями). Так часто поступают в местностях, где высока вероятность заражения сразу несколькими видами плазмодия.
Другие схемы:
Самостоятельный прием сульфадоксина/пириметамина на фоне одной из описанных выше схем для мефлохина, доксициклина или хлорохина. Сульфадоксин/пириметамин выпускают в таблетках, содержащих по 25 мг пириметамина и 500 мг сульфадоксина. Принимают однократно при подозрении на малярию (лихорадка), когда медицинская помощь недоступна. Вслед за этим следует немедленно обратиться к врачу. Взрослые принимают 3 таблетки. Детям до 1 года дают 1/4 таблетки, детям 1—З лет(вес 5— 10кг)— 1/2 таблетки, 4—8 лет(11— 20 кг)— 1таблетку, 9—14лет(31—45 кг) —2 таблетки, 15летистар-ше (> 45 кг) — 3 таблетки. Примечание: сульфадоксин/пириметамин не рекомендуется детям до 2 мес, в III триместре беременности и при аллергии к сульфаниламидам. Там, где распространена устойчивость к хлорохину и сульфадоксину/пириметамину (в некоторых областях Юго-Восточной Азии, Африки и Южной Америки), эта схема неэффективна.
Прогуанил + хлорохин по схеме для профилактики тропической малярии, вызванной чувствительными к хлорохину штаммами (см. выше). Взрослым и детям старше 10 лет прогуанил назначают по 200 мг/сут внутрь. Детям до 2 лет назначают 50 мг/сут; 2—6 лет — 100 мг/сут; 7—10 лет — 150 мг/сут. Прием начинают с первых суток пребывания в эндемическом районе и продолжают еще 4 нед после возвращения. Эта схема работает в некоторых областях Западной, Экваториальной и Южной Африки, но устойчивость к прогуанилу встречается все чаще. Отсутствие эффекта от профилактики может быть также обусловлено низкой скоростью метаболизма прогуанила и недостаточным образованием его активного метаболита циклогуа-нила (см. текст). В США прогуанил не выпускается, но его можно приобрести в Канаде и в других странах. Атоваквон/прогуанил признан эффективным средством профилактики тропической малярии (Shanks et al., 1999), однако целесообразней приберечь его для лечения этого тяжелого заболевания
- Ни одна из перечисленных схем не дает полной гарантии от заражения тропической малярией — лучше использовать их в сочетании с индивидуальными средствами зашиты от комаров (см. текст).
- В настоящее время такие штаммы сохранились только в Мексике, Центральной Америке к западу от Панамского канала, странах Карибского бассейна и в некоторых районах Южной Америки и Ближнего Востока.
Антипаразитарная активность
Часть молекулы артемизинина и его производных, содержащая эндопероксидный мостик, определяет их противомалярийную активность, которая значительно увеличивается при замещениях в карбонильной группе лактонного кольца. Эти препараты быстро действуют на бесполые эритроцитарные формы Plasmodium vivax и на штаммы Plasmodium falciparum — как чувствительные, так и устойчивые к хлорохину и другим средствам. Активность артемизинина и его производных in vivo в 10—100 раз выше, чем других противомалярийных препаратов (White, 1997). Артемизинин и его производные действуют и на гаметоциты, но в отношении тканевых форм и гипнозоитов неактивны, поэтому для медикаментозной профилактики и предотвращения рецидивов малярии, вызванной Plasmodium vivax, эти препараты не используют. По современным представлениям, механизм действия артемизинина складывается из двух этапов. Первый этап — расщепление эндопероксидного мостика — происходит внутри плазмодия, катализатором этой реакции служит железо гема пораженного эритроцита. Затем внутри молекулы артемизинина происходит перегруппировка, в ходе которой образуются свободные радикалы. Они вступают в ковалентную связь с белками малярийного плазмодия и повреждают их (Meshnick et al., 1996). Артемизинин и его производные действуют и на других простейших in vitro (Leishmania major и Toxoplasma gondii), а также на шистосом in vivo, но для лечения заболеваний, вызванных этими паразитами, данные препараты не применяют.
Схемы лечения малярии у неиммунных лиц
Лечение тяжелой малярии
Тропическая малярия у неиммунных лиц — неотложное состояние, так как тяжесть ее может быстро нарастать вплоть до смертельного исхода. Лечение необходимо начинать сразу, не дожидаясь микробиологического подтверждения диагноза. Тяжелым больным, которые не могут принимать препараты внутрь, вводят в/в хинидина глюконат по схеме, которая подходит для лечения малярии, вызванной любыми видами плазмодия. При уровне паразитемии выше 10% может потребоваться обменное переливание крови.
Рекомендуемые схемы:
И взрослым, и детям в/в введение хинидина глюконата начинают с насыщающей дозы 10 мг/кг в 300 мл физиологического раствора. Вводят ее в течение 1—2 ч, причем максимальная доза не должна превышать 600 мг. В дальнейшем проводят длительную инфузию со скоростью 0,02 мг/кг/мин до тех пор, пока больной не сможет принимать препарат внутрь. При введении хинидина необходимо постоянно следить за АД и ЭКГ и периодически определять уровень глюкозы плазмы. При появлении артериальной гипотонии, расширении комплекса QRS, удлинении интервала QT или гипогликемии скорость инфузии снижают. Если же эти изменения сильно выражены, препарат следует отменить.
Как только больной будет в состоянии принимать пищу, его переводят на прием хинина внутрь. Взрослым назначают по 650 мг хинина сульфата, детям — по 10 мг/кг 3 раза в сутки. Лечение хинином (хинидином) длится 3—7 сут в зависимости от вида и чувствительности возбудителей в данной местности. Если состояние больного не улучшается в течение 48 ч от начала приема хинина, дозу снижают на 30—50%. Если ранее больной получал мефлохин, дозу хинина, возможно, придется снизить.
Дополнительное лечение:
Для повышения эффективности к любой из следующих схем добавляют хинин (внутрь). Выбор схемы зависит от чувствительности возбудителей в данной местности к препаратам.
Доксициклин. Взрослым назначают по 100 мг доксициклина внутрь 2 раза в сутки в течение 7 сут. Детям старше 8 лет — начинают с 2 мг/кг внутрь, увеличивают до дозы у взрослых, применяют 7 сут. Вместо доксициклина можно использовать тетрациклин: взрослым по 250 мг, детям — по 5 мг/кг 4 раза в сутки в течение 7 сут. Примечание: из-за побочного действия на кости и зубытетрациклины не назначают детям до 8 лет и беременным. Оба препарата противопоказаны при аллергии к тетрациклинам.
Сульфадоксин/пириметамин. Назначают внутрь однократно в последний день приема хинина (взрослым 3 таблетки, детям — меньше, см. табл. 40.1).
Другие схемы лечения малярии, вызванной штаммами Plasmodium vivax и Plasmodium falciparum, устойчивыми к хлорохину, или полирезистентными штаммами Plasmodium falciparum
Мефлохин. Назначают внутрь: взрослым и детям весом > 45 кг 750 мг мефлохина гидрохлорида, затем спустя 12 ч еще 500 мг внутрь; детям весом < 45 кг — 15 мг/кг и еще 10 мг/кг спустя 12 ч (дозы для детей не одобрены ФДА). Если в течение часа после приема препарата возникла рвота, то первую дозу назначают повторно. В терапевтических дозах мефлохин может вызвать нарушения со стороны ЖКТ, неврологические и психические нарушения. Из-за длинного Т1/2 и выраженного взаимодействия с другими препаратами назначать алкалоиды хины (хинин, хинидин) одновременно и вскоре после приема мефлохина нужно с большой осторожностью.
Артесунат + мефлохин. Назначают внутрь. В 1 -й день 4 мг/кг/сут артесуната, со 2-го по 5-й дни — по 2 мг/кг/сут (общая доза на курс — 12 мг/кг — одинакова для взрослых и детей). На 2-й день приема артесуната однократно назначают 25 мг/кг мефлохина. Примечание: в США артесунат не выпускают.
Атоваквон/прогуанил. Таблетки, содержащие 250 мг атоваквона и 100 мг прогуанила. В США не выпускают. Назначают внутрь. Для взрослых доза атоваквона составляет 1000 мг, доза прогуанила — 400 мг. Детям весом 11 —20 кг назначают 250 мг атоваквона и 100 мг прогуанила, 21—30 кг — 500 мг атоваквона и 200 мг прогуанила, 31—40 кг — 750 мг атоваквона и 300 мг прогуанила. Препараты принимают 1 раз в сутки в течение 3 сут. Чтобы увеличить биодоступность, таблетки измельчают перед приемом или разжевывают и принимают после употребления жирной пищи.
Лечение малярии, вызванной Plasmodium vivax, Plasmodium malariae, Plasmodium ovale и чувствительными к хлорохину штаммами Plasmodium falciparum
Хлорохин. Выпускают в таблетках по 250 или 500 мг хлорохина фосфата. Дозы для взрослых и детей в расчете на вес одинаковы. Назначают 16,7 мг/кг хлорохина фосфата (10 мг/кг в пересчете на основание) сразу, затем по 8,3 мг/кг (5 мг/кг в пересчете на основание) через 6,12,24 и 36 ч. К концу 2-х суток общая доза должна составить 50 мг/кг (30 мг/кг в пересчете на основание). При малярии, вызванной Plasmodium vivax и Plasmodium ovale, дополнительно назначают по 8,3 мг/кг хлорохина фосфата (5 мг/кг в пересчете на основание) на 7-е и 14-е сутки.
Профилактика рецидивов:
Примахин. Выпускают в таблетках по 13,2 и 26,3 мг примахина фосфата (соответственно 7,5 и 15 мг в пересчете на основание). Для искоренения гипнозоитов Plasmodium vivax и Plasmodium ovale, которые служат причиной рецидивов, взрослым назначают по 26,3 мг/сут, детям — 0,5 мг/кг/сут (0,3 мг/кг/сут в пересчете на основание) в течение 2 нед, начиная с 4-х суток после приступа малярии. По той же схеме примахин можно назначать в последние 2 нед профилактики хлорохином (после поездки в район, где распространены штаммы Plasmodium vivax или Plasmodium ovale). Или же примахин добавляют к хлорохину (табл. 40.1) сразу после возвращения из эндемического района и принимают 500 мг/нед хлорохина фосфата (300 мг/нед в пересчете на основание) и 78,9 мг/нед примахина фосфата (45 мг/нед в пересчете на основание) в течение 8 нед.
Фармакокинетика
Распределение производных артемизинина изучено не полностью из-за трудностей при хранении биологических образцов и отсутствия надежных методов оценки концентрации препарата в них. Опубликованы результаты нескольких исследований фармакокинетики (Barradell and Fitton, 1995; de Vries and Dien, 1996). Сывороточная концентрация производных артемизинина достигает максимальной через несколько минут или часов, в зависимости от препарата и пути введения. Различны также характер и степень связывания с белками. Артеметер и артесунат в организме превращаются в активный дигидроартемизинин. Гидролиз артесуната до дигидроартемизинина может происходить еще во время всасывания. При распаде артемизинина образуются по крайней мере четыре неактивных метаболита, но является ли дигидроартемизинин промежуточным продуктом метаболизма, не ясно (de Vries and Dien, 1996). Противомалярийное действие производных артемизинина обусловлено главным образом дигидроартемизинином, который быстро выводится из плазмы (Т1/2 около 45 мин). Ни дигидроартемизинин, ни другие производные артемизинина в моче не обнаруживаются. Артемизинин может усиливать синтез изофермента I1C19 цитохрома Р450 (Svensson et al., 1998), но сколько-нибудь важных взаимодействий между артемизинином и другими лекарственными средствами пока не выявлено.
Применение
При тяжелой малярии, в том числе вызванной устойчивыми к хлорохину и полирезистентными штаммами Plasmodium falciparum, производные артемизинина действуют быстрее и сильнее других препаратов и оказывают мало побочных эффектов (White, 1999). Для профилактики и при легких формах малярии эти препараты не применяют (Meshnick et al., 1996). Производные артемизинина действуют быстрее и менее токсичны, чем алкалоиды хины, в то время как эффективность тех и других при малярийной коме одинакова. Артемизинин и его производные можно назначать в виде монотерапии, но продолжительность ее должна быть не менее 5—7 сут, иначе может возникнуть рецидив. Короткие курсы этих , препаратов допустимы при назначении их вместе с аминохинолинами длительного действия (например, мефлохином) или с антибиотиками с противомалярийным действием (например, доксициклином) — такой подход помогает избежать рецидивов и может замедлить развитие устойчивости (White, 1997,1999). Схемы лечения еще не отработаны, но одна из них предусматривает курс артесуната, чтобы быстро снизить уровень паразитемии, а затем — одно- или двукратный прием мефлохина, чтобы искоренить возбудителей (White, 1999; Price et al., 1999; табл. 40.2). Преимущество этой схемы в том, что риск побочных эффектов снижается без потери противомалярийной активности. Производные артемизинина выпускаются в виде различных лекарственных форм и применяются они по-разному. Так, дигидроартемизинин можно назначать только внутрь. Артеметер принимают внутрь и вводят в/м. Артемизинин эффективен при приеме внутрь или введении в ректальных свечах. Артесунат, по-видимому, самый удобный из производных артемизинина, так как его можно назначать и внутрь, и в/м, и в/в, и рек-тально. Возможность вводить артесунат в/в особенно важна при лечении малярийной комы, а свечи имеют большие преимущества при лечении тяжелой малярии в труднодоступных районах.
Побочные эффекты и противопоказания. При назначении производных артемизинина в терапевтических дозах в течение недели эти препараты выглядят на удивление безопасными (de Vries and Dien, 1996). Сообщается о преходящей АВ-блокаде 1-й степени, обратимой дозозависимой ретикулоцитопении и нейтропении, временном повышении активности АсАТ, но клиническое значение этих эффектов не определено. В ряде исследований на добровольцах отмечена кратковременная лихорадка. В опытах на животных высокие дозы производных артемизинина оказывали нейротоксическое действие, вызывали удлинение интервала QT, угнетение кроветворения и внутриутробную гибель плода. При длительном лечении этими препаратами можно ожидать подобных побочных эффектов и у людей (de Vries and Dien, 1996). Но на сегодня производные артемизинина следует признать самым безопасным средством неотложной помощи при тяжелой малярии, вызванной полирезистентными штаммами плазмодия, — даже у беременных (McGready et al., 1998) и у детей (Price et al., 1999).
Атоваквон
Историческая справка
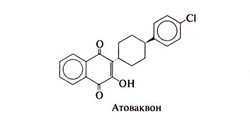
Некоторые гидроксинафтохиноны обладают антипротозойной активностью, что и легло в основу создания синтетического препарата атоваквона, высокоактивного в отношении Plasmodium spp. и ряда условно-патогенных микроорганизмов (Hudson et al., 1991). Позже клинические испытания показали, что при лечении неосложненной тропической малярии атоваквоном улучшение наступает быстро, но и число рецидивов остается высоким (Looareesuwan et al., 1996). В то же время при назначении атоваквона вместе с прогуанилом доля выздоровевших велика, рецидивы возникают редко, а побочные эффекты незначительны (Looareesuwan et al., 1996, 1999а). В США выпускается комбинированный препарат атоваквон/прогуанил (Looareesuwan et al., 1999а). Атоваквон активен также в отношении Pneumocystis carinii и Toxoplasma gondii, которые вызывают тяжелые оппортунистические инфекции у больных СПИДом (Hughes et al., 1990). В 1992 г. после нескольких клинических испытаний ФДА одобрило этот препарат для лечения легкой и среднетяжелой пневмонии, вызванной Pneumocystis carinii, у больных с непереносимостью триметоприма/сульфаметоксазола (гл. 44). Атоваквон отчасти эффективен при поражениях головного мозга и глаз, вызванных Toxoplasma gondii, и применение его совместно с другими антипаразитарными препаратами еще изучается. Структурная формула атоваквона следующая:
Антипаразитарная активность
Атоваквон — жирорастворимый аналог убихинона. В опытах на животных и in vitro атоваквон проявил высокую активность в отношении эритроцитарных шизонтов Plasmodium spp., эндозоитов и цист Toxoplasma gondii, Babesia spp., а также Pneumocystis carinii (Hughes etal., 1990; Hudson etal., 1991; Hughes and Oz, 1995). Атоваквон высокоактивен в отношении Plasmodium spp., вызывающих малярию у грызунов, и Plasmodium falciparum, как in vitro (в концентрации 0,7—4,3 нмоль/л подавляет 50% штаммов), так и в опытах на обезьянах рода Aotus (Hudson et al., 1991). У чувствительных микроорганизмов он нарушает транспорт электронов в дыхательной цепи митохондрий и связанные с ним процессы синтеза АТФ и пиримидиновых оснований. У малярийного плазмодия атоваквон избирательно действует на комплекс III дыхательной цепи (цито-хромы b и с,); в результате наступает деполяризация митохондриальной мембраны, тканевое дыхание прерывается, и клетка погибает (Vaidya, 1998). Прогуанил (бигуа-нид) усиливает действие атоваквона на мембранный потенциал митохондрий (Srivastava and Vaidya, 1999). Аналогичное действие оказывал атоваквон на митохондрии эндозоитов Toxoplasma gondii после обработки веществами, повышающими проницаемость мембран для мелких молекул (Vercesi et al., 1998).
Фармакокинетика
Атоваквон плохо растворяется в воде, биодоступность его зависит от лекарственной формы. При приеме внутрь в виде мелкодисперсной суспензии биодоступность вдвое выше, чем при приеме в таблетках. При однократном приеме внутрь атоваквон всасывается медленно, причем характер всасывания непостоянен. Так, при приеме с жирной пищей всасывание улучшается, но при приеме более чем 750 мг атоваквона за один раз — ухудшается. Более 99% препарата связывается с белками плазмы, и его концентрация в СМЖ составляет менее 1% сывороточной. Фармакокинетическая кривая атоваквона часто имеет две фазы, однако время их наступления непостоянно: первый подъем возникает через 1—8 ч, второй — через 1—4 сут после однократного введения. Вместе с д линным Т |/2 (1,5—3 сут) это говорит об участии атоваквона в кишечно-печеночном кругообороте. У людей метаболизм атоваквона незначителен. Выводится препарат с желчью, более 94% принятой дозы обнаруживают в кале в неизмененном виде, в мочу попадают лишьследы атоваквона (Rolan et al., 1997). При лечении тропической малярии клиренс атоваквона может различаться у представителей разных этнических групп (Hussein etal., 1997).
Применение
Для того чтобы достичь наилучших результатов и одновременно избежать появления устойчивости, атоваквон назначают вместе с бигуанидами. Упомянутый выше комбинированный препарат атоваквон/ прогуанил (в одной таблетке 250 мг атоваквона и 100 мг прогуанила) при приеме в течение 3 сут весьма эффективен и безопасен в случае нетяжелой тропической малярии, возбудители которой устойчивы к хлорохину и другим противомалярийным препаратам (Looareesuwan et al., 1999а; табл. 40.2). Эта же схема с последующим приемом примахина давала отличные результаты при малярии, вызванной устойчивыми к хлорохину штаммами Plasmodium vivax (Looareesuwan et al., 1999b). Несмотря на высокую эффективность атоваквона/прогуа-нила при лечении малярии у детей и взрослых, для профилактики его использовать не рекомендуется, чтобы замедлить развитие устойчивости. При назначении каждого из препаратов по отдельности устойчивые штаммы появляются очень быстро. Атоваквон эффективен при инфекциях, вызванных Pneumocystis carinii и Toxoplasma gondii, которые наиболее тяжело протекают у больных с иммунодефицитами, в том числе у ВИЧ-ин-фицированных. Если такой больной может принимать препараты внутрь, но не переносит триметоприм/суль-фаметоксазол или пентамидин для в/в введения, атоваквон может с успехом заменить эти препараты при лечении и профилактике пневмоцистной пневмонии (гл. 41, 44 и 49). При инфекциях, вызванных Toxoplasma gondii, особенно с поражением головного мозга, длительный прием атоваквона давал лишь умеренный дозозависимый эффект (Torres et al., 1997). У больных токсоплаз-менным хориоретинитом при нормальном иммунитете атоваквон действовал лучше (Pearson et al., 1999). Этот препарат можно применять и при бабезиозе (Hughesand Oz, 1995).
Побочные эффекты
При тропической малярии у ослабленных больных с иммунодефицитом (в частности, при СПИДе) побочные эффекты атоваквона трудно отличить от проявлений основной болезни. Но осложнения, требующие отмены препарата, возникают редко. Чаще всего встречаются сыпь, лихорадка, рвота, понос и головная боль. Рвота и понос уменьшают всасывание препарата и могут снизить его эффективность. Однако при повторном назначении в течение часа после рвоты препарат все же может оказать лечебное действие (Looareesuwan et al., 1999а). Пятнисто-папулезная сыпь возникает у 20% больных (дозозависимый побочный эффект), но протекает она обычно легко и не усиливается, даже если продолжать прием атоваквона. Однако из осторожности его не следует назначать больным, у которых ранее уже отмечались аллергические реакции при приеме этого препарата. Изредка у больных, получающих атоваквон, повышается активность аминотрансфераз и амилазы сыворотки. Действие атоваквона на бактерии, вирусы и большинство возбудителей оппортунистических инфекций, которые часто развиваются на фоне иммунодефицитов, не доказано, поэтому эти инфекции следует лечить отдельно. Не исключено, что атоваквон может вызывать и другие, редкие и необычные, побочные эффекты, особенно при длительном приеме, но этот вопрос еще требует изучения. Так, полагают, что обратимая вихревидная кератопатия (cornea verticillata) может быть вызвана приемом жирорастворимых антипаразитарных средств, таких, как атоваквон (Shah et al., 1995).
Меры предосторожности и противопоказания
На первый взгляд атоваквон кажется удивительно безопасным препаратом, но его действие и возможные побочные эффекты у детей, пожилых, беременных и кормящих еще предстоит изучить. В этих группах препарат следует назначать с осторожностью. Стандартные исследования не выявили ни канцерогенного, ни мутагенного, ни тератогенного эффектов, но у кроликов терапевтические дозы атоваквона оказывали токсическое действие при беременности и нарушали развитие плода. Атоваквон может конкурировать с некоторыми препаратами за связывание с белками плазмы. Назначение его одновременно с рифампицином (мощным индуктором микросомальных ферментов печени) может намного снизить сывороточную концентрацию атоваквона, при этом концентрация самого рифампицина повышается. До тех пор пока действие атоваквона на печеночный метаболизм и выведение с желчью других препаратов не изучено, больным с тяжелыми поражениями печени атоваквон следует назначать с осторожностью.
Галофантрин
Производное фенантренметанола галофантрин относится к ге-матошизотропным препаратам и по фармакологическим свойствам сходен с аминохинолинами. Этот препарат создавался как альтернатива хинину и мефлохину при лечении приступов тропической малярии, вызванной устойчивыми к хлорохину и другим препаратам штаммами. Биодоступность галофантрина непостоянна; он оказывает кардиотоксическое действие, которое может стать причиной смерти; кроме того, широко распространена перекрестная устойчивость к галофантрину и мефлохину — поэтому в настоящее время галофантрин почти не применяют. История создания, фармакологические и токсические свойства галофантрина подробно изложены в 9-м издании этой книги.
Диаминопиримидины
Историческая справка
Диаминопиримидины — антагонисты фолиевой кислоты. Сначала их использовали при выращивании Lactobacillus casei, затем была исследована способность этих соединений угнетать рост патогенных микроорганизмов. Ряд производных 2,4-диаминопиримидина, в том числе пириметамин и антибактериальный препарат триметоприм, в опытах на животных обнаружили мощное противомалярийное действие. Позже выяснилось, что пириметамин особенно эффективен при лечении малярии у людей (Symposium, 1952). Комбинированный препарат из двух антагонистов фолиевой кислоты сульфадоксин/пириметамин (сульфадоксин — сульфаниламид длительного действия) широко применяли для профилактики и лечения малярии, особенно вызванной устойчивыми к хлорохину штаммами Plasmodium falciparum. Впервые возникнув в Индокитае, устойчивость к этому препарату быстро распространилась повсюду, где встречается малярия, кроме некоторых областей Африки, где его используют главным образом у коренного населения для лечения тропической малярии, вызванной устойчивыми к хлорохину штаммами. Из-за токсичности (см. ниже) сульфадоксин/пириметамин больше не рекомендуют для длительной профилактики малярии. Структурная формула пириметамина следующая:
Противомалярийное действие
Пириметамин, медленно действующий гематошизотропный препарат, по активности в отношении малярийного плазмодия in vivo напоминает прогуанил (см. ниже). Но пириметамин — более мощное противомалярийное средство, так как не требует перехода в активную форму, а Т|/2 у него намного больше, чем у циклогуанила, активного метаболита прогуанила. В отличие от прогуанила, пириметамин почти не действует на стадии тканевой шизогонии Plasmodium falciparum. В терапевтических дозах пириметамин не уничтожает гипнозоитов Plasmodium vivax и не действует на гаметоцитов всех видов плазмодия. Противомалярийному действию пириметамина и прогуанила посвящен ряд исследований (Davey and Hill, 1963).
Действие на других простейших
При токсоплазмозе, протекающем особенно тяжело у детей и больных с иммунодефицитом, наиболее эффективна комбинация из пириметамина в высокой дозе и сульфадиазина (гл. 41). Механизм действия и устойчивость. Ряд исследований показал, что 2,4-диаминопиримидины угнетают дигидро-фолатредуктазу малярийного плазмодия в концентрациях, намного бсшее низких, чем необходимые для угнетения этого фермента у млекопитающих (Ferone et al., 1969). В отличие от млекопитающих, у плазмодиев дигидрофолатредукгаза выполняет также функции тимидилатсинтазы. Синергичное действие пириметамина и сульфаниламидов (или сульфонов) объясняется тем, что они угнетают синтез фолиевой кислоты на двух разных этапах (гл. 44). Сульфаниламиды действуют на этапе образования дигидроптероевой кислоты из парааминобен-зойной при участии дигидроптероатсинтазы. Пиримета-мин подавляет восстановление дигидрофолиевой кислоты до ТГФК при участии дигидрофолатредуктазы. Действие антагонистов фолиевой кислоты проявляется на поздних стадиях жизненного цикла паразита — нарушается деление ядра во время эритроцитарной и тканевой шизогонии. Этим объясняется более медленное действие данных препаратов по сравнению с ам инохи ноли нами. Но там, где пириметамин применяется широко, а также в течение длительного времени, устойчивость к нему все равно развивается. Клонирован и расшифрован ген дигидрофолатредуктазы у штаммов Plasmodium falciparum — как чувствительных, так и устойчивых к пири-метамину. Выявлено несколько мутаций, приводящих к замене одной аминокислоты и вызывающих устойчивость к пириметамину. В результате мутации уменьшается сродство пириметамина к активному центру той части фермента, которая у плазмодия выполняет функцию дигидрофолатредуктазы. Для развития устойчивости достаточно уже одной замены Асн108 дигидрофолатредуктазы на серин. Это основная мутация. Дополнительные мутации повышают устойчивость за счет замен в положениях 50,51,59 и 164. Замена в положении 164всочета-нии с основной мутацией резко увеличивает устойчивость к пириметамину. У устойчивых штаммов эти и другие мутации гена дигидрофолатредуктазы встречаются в различных сочетаниях. У плазмодиев, устойчивых к циклогуанилу, происходят замены других аминокислот, однако возможно появление перекрестной устойчивости за счет структурного сходства пириметамина и циклогуанила (см. ниже, Прогуанил; а также Cowman, 1998; Corteseand Plowe, 1998).
Фармакокинетика
При приеме внутрь пириметамин медленно, но полностью всасывается; сывороточная концентрация достигает максимальной примерно через 4—6 ч. Препарат связывается с белками плазмы и накапливается в почках, легких, печени и селезенке. Выводится он также медленно, Т1/2 составляет 80—95 ч. Сывороточная концентрация пириметамина, достаточная для уничтожения чувствительных возбудителей, сохраняется в течение 2 нед. Однако при сравнении с данными, полученными при испытании препарата на здоровых добровольцах, у больных малярией его сывороточная концентрация оказалась ниже (Winstanley et al., 1992). С мочой выводятся несколько метаболитов пириметамина, но их строение и противомалярийные свойства изучены не полностью. Пириметамин проникает в молоко.
Применение
Пириметамин не относится к противомалярийным препаратам первого ряда. Почти всегда его назначают в комбинации с сульфаниламидами или сульфо-нами, чтобы усилить действие на метаболизм фолиевой кислоты, но пириметамин все равно действует медленнее, чем аминохинолины, а его длительное выведение способствует появлению устойчивых плазмодиев. Пириметамин следует назначать только для поддерживающей терапии при тропической малярии, вызванной устойчивыми к хлорохину штаммами, и только в тех районах (например, Африки), где устойчивость к антагонистам фолиевой кислоты сформировалась еше не полностью. Выезжающим в эти районы рекомендуется иметь при себе сульфадоксин/пириметамин в дозах, достаточных для лечения, с тем, чтобы начать прием при подозрении на малярию. Одновременно следует как можно скорее обратиться к врачу. Пириметамин совместно с сульфаниламидом короткого действия (например, сульфадиазином) и хинином можно использовать при лечении приступов малярии. Схемы лечения представлены в табл. 40.1 и 40.2. Из-за токсичности сульфадоксина сульфадоксин/пириметамин больше не назначают для профилактики малярии (см. ниже). Этот комбинированный препарат совместно с мефлохином применяли для профилактики и лечения малярии, вызванной полирезистентными штаммами Plasmodium falciparum, но такая комбинация высокотоксична, а преимуществ перед монотерапией мефлохином почти не имеет (Palmer et al., 1993).
Высокие дозы пириметамина в сочетании с сульфадиазином весьма эффективны при токсоплазмозе у больных с иммунодефицитами. Без лечения такие больные быстро погибают (Kasper, 1998; гл. 41). Лечение начинают с приема пириметамина внутрь (насыщающая доза 200 мг, в дальнейшем 50—75 мг/сут) в сочетании с сульфадиазином внутрь (4—6 г/сут в 4 приема). Одновременно, чтобы предотвратить угнетение кроветворения (см. ниже), на весь период лечения назначают 10—15 мг/сут фолината кальция внутрь. В дальнейшем для длительной поддерживающей терапии достаточно 25—50 мг/сут пириметамина и 2—4 г/сут сульфадиазина. Во избежание токсического действия сульфадиазина пириметамин часто назначают совместно с клиндамицином, спирамицином и другими макролидами (Kasper, 1998). При врожденном токсоплазмозе назначают пириметамин (0,5—1 мг/кг/сут) и сульфадиазин (100 мг/кг/сут) в течение 1 года.
Побочные эффекты, меры предосторожности и противопоказания
В дозах, необходимых для лечения малярии, пириметамин почти не дает побочных эффектов, за исключением редких случаев сыпи и угнетения кроветворения. Передозировка приводит к мегалобластной анемии, напоминающей фолиеводефицитную, которая быстро исчезает при отмене препарата или назначении фолината кальция. У животных очень большие дозы пириметамина оказывают тератогенное действие, в отношении людей таких данных нет.
При назначении комбинированных препаратов побочные эффекты обычно бывают вызваны не пириметамином, а сульфаниламидами и сульфонами (гл. 44). Сульфадоксин/пириметамин (соответственно S00 и 25 мг) больше не рекомендуют для профилактики малярии, так как в одном из 5000—8000 случаев этот комбинированный препарат вызывает тяжелые и даже смертельные реакции: полиморфную экссудативную эритему, синдром Стивенса—Джонсона, синдром Лайелла. Отмечены также сывороточная болезнь, крапивница, эритродермия и гепатит. Сульфадоксин/пириметамин противопоказан при аллергических реакциях на сульфаниламиды в анамнезе, кормящим матерям и детям младше 2 мес. Комбинированный препарат пириметамин/дапсон (в США не выпускается) может в отдельных случаях вызывать агранулоцитоз. Более высокие дозы пириметамина (75 мг/сут), применяемого вместе с сульфадиа-зином (4—6 г/сут) при лечении токсоплазмоза у больных с иммунодефицитами, вызывают сыпь, угнетение кроветворения и поражение почек примерно в 40% случаев. Однако эти побочные эффекты обусловлены в основном сульфадиазином (Kasper, 1998; гл. 44).
Мефлохин
Историческая справка
Мефлохин был создан в 1963 г., когда Во-енно-медицинский Центр Уолтера Рида (г. Вашингтон) основал программу по созданию новых препаратов для борьбы с устойчивыми штаммами Plasmodium falciparum. Из многих производных 4-хинолинметанола, отобранных для исследований за химическое сходство с хинином, именно мефлохин проявил высокую противомалярийную активность в опытах на животных, а при клинических испытаниях оказался безопасным и высокоактивным в отношении устойчивых штаммов Plasmodium falciparum (Schmidt et al., 1978). Впервые мефлохин применили в Таиланде для лечения малярии, вызванной такими штаммами. Чтобы задержать появление устойчивых плазмодиев, его назначали в виде комбинированного препарата с сульфадоксином/пириметамином. Но устойчивость все равно развивалась, так как из-за медленного выведения мефлохина его сывороточная концентрация долго удерживалась на уровне ниже терапевтической, что способствовало отбору устойчивых штаммов (While, 1999). Сейчас мефлохин рекомендуют только для профилактики и лечения малярии, вызванной штаммами Plasmodium falciparum, устойчивыми к хлорохину и другим препаратам. Мефлохин наиболее эффективен при лечении неосложненной тропической малярии, вызванной полирезистентными штаммами, при назначении через 48 ч после того, как лечение одним из производных артемизинина (см. выше) значительно снизит уровень паразитемии (White, 1997, 1999). Подробно о противомалярийной активности, фармакокинетике, об эффективности и о побочных эффектах препарата см., например, в обзорах Palmer et al. (1993), Schlagenhauf (1999). Структурная формула мефлохина следующая:
Противомалярийное действие
Мефлохин представляет собой рацемическую смесь четырех оптических изомеров с почти одинаковой противомалярийной активностью. Мощный гематошизотропный препарат, мефлохин особенно активен в отношении зрелых шизонтов. Препарат не действует на стадии тканевой шизогонии, неактивен в отношении гаметоцитов Plasmodium falciparum и гипнозоитов Plasmodium vivax. Мефлохин оказывает некоторое споронтоцидное действие, но это его свойство не нашло применения.
Механизм действия и устойчивость
Механизм действия мефлохина точно не установлен, возможно, он действует аналогично хлорохину (см. ниже). Как гематошизотропный препарат мефлохин во многом сходен с хинином, но, в отличие от него, не взаимодействует с ДН К. Оба препарата вызывают сходные морфологические изменения у кольцевидных шизонтов Plasmodium falciparum и Plasmodium vivax (Schmidt et al., 1978) и конкурируют с хлорохином за накопление в клетке и связывание с ге-матином (Fitch et al., 1979). Под действием мефлохина пищеварительные вакуоли Plasmodium falciparum набухают. Низкие концентрации мефлохина (как и хлорохина) вне клетки повышают pH внутри пищеварительной вакуоли в большей степени, чем можно было бы ожидать исходя из динамики пассивного распределения слабых оснований. Это предполагает существование какого-то механизма, посредством которого мефлохин проникает в клетку и накапливается в ней. Мефлохин не только угнетает кристаллизацию гематина, но и образует токсичные соединения со свободным гемом, повреждающие мембраны и другие структуры плазмодия (Palmer et al., 1993; Sullivan et al.,1998). Взаимное расположение гидроксильных и аминогрупп в молекуле мефлохина играет важную роль в образовании водородных связей и может определять противомалярийную активность препарата (Karle and Karle, 1991).
Устойчивые к мефлохину штаммы Plasmodium falciparum чаще всего выделяют от людей, лечившихся этим препаратом. Для лечения малярии, вызванной устойчивыми плазмодиями, обычно требуются более высокие дозы мефлохина. Многие штаммы Plasmodium falciparum обладают полирезистентностью — это зависит от района, где они распространены, и противомалярийных препаратов, которые там применялись. Эго заставляет задуматься о существовании общих механизмов природной и приобретенной устойчивости к мефлохину и сходным с ним по строению противомалярийным препаратам (Palmer et al., 1993). В формировании устойчивости Plasmodium falciparum к мефлохину может участвовать генный комплекс mdr, отвечающий за полирезистентность у бактерий. Продукты этих генов — мембранные белки-переносчики — снижают внутриклеточную концентрацию препаратов, увеличивая их выведение по механизму активного транспорта. Такое выведение угнетают некоторые антагонисты кальция. У устойчивых к мефлохину и гало-фантрину in vivo штаммов Plasmodium falciparum представитель этого комплекса — ген pfindrl — обычно (но не всегда) ампли-фицирован, то есть количество копий гена увеличено (Wilson et al., 1993; Limetal., 1996). Сдругой стороны, четкой зависимости между устойчивостью к хлорохину и амплификацией pjmdrl нет (Mungthin et al., 1999). Устойчивые к мефлохину плазмодии обычно, но не всегда устойчивы и к хинину. Таким образом, в развитии устойчивости к этим сходным по строению препаратам помимо гена pfmdrl могут играть роль и другие генетические механизмы (Zalis et al., 1998). Устойчивость к стереоизомерам мефлохина и их механизм действия еще требуют изучения. Фармакокинетика. Мефлохин назначают внутрь, так как при парентеральном введении он вызывает тяжелые местные реакции. Препарат хорошо всасывается, особенно при приеме во время еды. Сывороточная концентрация достигает максимальной через 17 ч. Ее динамика описывается двухфазной кривой, что, по-видимому, отражает активное всасывание мефлохина в ЖКТ, а затем — участие в кишечно-печеночном кругообороте. Препарат проникает во многие ткани и биологические жидкости, на 98% связывается с белками плазмы и медленно элиминируется с конечным Т1/2 около 20 сут. Метаболизм мефлохина у человека изучен недостаточно, известно лишь, что при распаде препарата образуется несколько метаболитов. Сывороточная концентрация неактивного метаболита мефлохина — 2,8-бис-трифторметил-4-хинолинкарбоновой кислоты — превышает концентрацию самого мефлохина. В дальнейшем концентрация обоих соединений снижается почти с одинаковой скоростью. Выводится мефлохин в основном с калом, лишь 10% препарата в неизмененном виде обнаруживают в моче. Это согласуется с данными (полученными в опытах на животных) о том, что мефлохин выводится с желчью и участвует в кишечно-печеночном кругообороте. Фармакокинетические свойства право- и левовращающих стереоизомеров мефлохина, в том числе их распределение в организме, различны (Hellgren et al., 1997). Но при приеме в виде рацемической смеси особенности фармакокинетики мефлохина, связанные с возрастом или этнической принадлежностью, беременностью или возникающие при заболевании малярией, не требуют существенного пересмотра схемы лечения (Palmer etal., 1993; Schlagenhauf, 1999). Применение. Мефлохин следует использовать только для профилактики и лечения малярии, вызванной устойчивыми к хлорохину и другим препаратам штаммами Plasmodium falciparum. Препарат особенно эффективен для профилактики малярии у неиммунных лиц, выезжающих в эндемические районы на короткие сроки (табл. 40.1). Во избежание отбора устойчивых штаммов людям, проживающим в эндемических районах длительное время, для профилактики мефлохин не назначают. В настоящее время только мефлохин и галофантрин способны справиться с тропической малярией, вызванной полирезистентными штаммами. Однако оба препарата можно назначать только внутрь — это большой недостаток при лечении больных в тяжелом состоянии. Таким больным лучше всего вводить препараты хинидина или хинина для парентерального применения. Из-за возможной перекрестной устойчивости неправильное лечение мефло-хином или галофантрином может привести к появлению штаммов Plasmodium falciparum, устойчивых к обоим препаратам, а возможно, и к хинину (Wilson et al., 1993). С устойчивостью можно бороться, увеличивая дозу — ценой повышения токсичности препарата. При лечении приступов малярии высокими дозами мефлохина часто возникает рвота. Поэтому после приема мефлохина за больным наблюдают в течение часа и, если рвота возникла, снова дают полную дозу препарата. Обычные схемы монотерапии тропической малярии мефлохином приведены в табл. 40.2. При необходимости их можно менять; так, частично иммунным больным можно назначать дозы ниже указанных в таблице. Более полную информацию по этому вопросу можно найти в обзоре Palmer et al. (1993).
Недавно показано, что неосложненную малярию, вызванную полирезистентными штаммами Plasmodium falciparum, лучше всего лечить мефлохином в сочетании с производным артемизинина, например артесунатом (см. выше) (White, 1997, 1999). Сначала — чтобы снизить уровень паразитемии — назначают артесунат, затем проводят лечение мефлохином, чтобы искоренить возбудителя и предупредить рецидивы. Исследования показали, что между мефлохином и производными артемизинина не возникает неблагоприятных лекарственных взаимодействий, и эти препараты не влияют на фармакокинетические свойства друг друга при условии, что мефлохин назначают спустя 36—48 ч после производного артемизинина. Дозу мефлохина (1250 мг) обычно делят на 2 приема: 750 мг после еды и еще 500 мг через 12 ч. Так же поступают и при тропической малярии у детей — отличные результаты давало назначение 25 мг/кг мефлохина (однократно или дробно) на вторые сутки лечения артесунатом (Price et al., 1999).
Побочные эффекты
Побочное действие мефлохина подробно описаны в обзорах Palmer etal. (1993), Schlagenhauf (1999). При приеме в дозе до 1500 мг однократно или 250—500 мг раз в неделю мефлохин обычно хорошо переносится. Побочные эффекты — тошнота, рвота, боль в животе, понос, дисфория и дурнота — встречаются редко. Они зависят от дозы, не требуют лечения, и временами их трудно отличить от проявлений малярии. Примерно у 50% больных, получающих мефлохин, возникают нарушения со стороны ЦНС. К ним относятся дурнота, атаксия, головная боль, двигательные нарушения, угнетение сознания, нарушение зрения и слуха. Протекают они обычно нетяжело и проходят самостоятельно. Изредка возникают тяжелые неврологические и психические нарушения: дезориентация, эпилептические припадки, энцефалопатия. Они проходят после отмены препарата или на фоне симптоматического лечения. Несмотря на то что эти осложнения чаше отмечаются при лечении, чем при профилактике мефлохином, сывороточная концентрация препарата, похоже, не влияет на частоту их появления. Противопоказания и лекарственные взаимодействия. Очень высокие дозы мефлохина оказывают тератогенное действие у грызунов. Однако профилактические дозы мефлохина во II и в III триместрах беременности практически безопасны и даже могут оказывать благоприятное воздействие на плод (Schlagenhauf, 1999). Но пока информации по этому вопросу недостаточно, мефлохин во время беременности (особенно в I триместре) лучше не назначать при условии, что риск малярии не слишком высок. Препарат не следует назначать детям весом до 5 кг. Мефлохин противопоказан при эпилептических припадках, тяжелых неврологических и психических нарушениях и побочных эффектах аминохинолинов (хинина, хинидина или хлорохина) в анамнезе. Последние лучше не назначать совместно с мефлохином, поскольку при этом повышается риск эпилептических припадков и кардиотоксического действия. Мефлохин можно принимать уже через 12 ч после хинина, но — поскольку мефлохин выводится очень медленно — назначение хинина вскоре после мефлохина небезопасно. Мефлохин может повышать риск припадков у больных эпилепсией, получающих вальпроевую кислоту. Кроме того, он может уменьшать иммуногенность живой брюшнотифозной вакцины. До появления новых данных о сочетаемости мефлохина с препаратами, нарушающими проводимость миокарда, назначать их совместно нужно с осторожностью. Последние исследования показали, что мефлохин не вызывает нарушения координации движений, таким образом, вождение или управление оборудованием на производстве при приеме мефлохина не противопоказано (Schlagenhauf, 1999).
Примахин
Историческая справка
Открытие Эрлихом в 1891 г. слабого противомалярийного действия метиленового синего послужило толчком к использованию производных 8-аминохинолина для лечения малярии. Из множества синтезированных производных 8-аминохинолина с метоксильными группами и замещенными 8-аминогруппами первым в медицине стали применять памахин. Поиск более мощных и менее токсичных производных во время Второй мировой войны привел к созданию пента-хина, изопентахина и примахина (см. предыдущие издания книги). В отличие от препаратов других групп, они действуют на тканевые формы Plasmodium vivax и Plasmodium ovale и, таким образом, подходят для профилактики и лечения рецидивов малярии, вызванной этими видами плазмодия. Сегодня из трех препаратов широко применяется лишь примахин, прошедший клинические испытания во время войны в Южной Корее. К сожалению, у больных с недостаточностью Г-6-ФД примахин вызывает гемолиз, а значит, нужно искать замену этому важному препарату. Многообещающим представляется производное 8-аминохинолина тафенохин, но его фармакологические свойства еще требуют изучения (Walsh et al., 1999). Структурная формула примахина следующая:
Противомалярийное действие
Примахин действует на поздние тканевые формы и гипнозоитов Plasmodium vivax и Plasmodium ovale и потому весьма эффективен при лечении рецидивов малярии, вызванной этими возбудителями. Монотерапия примахином не помогает при лечении приступов малярии, вызванной Plasmodium vivax, хотя он и обладает активностью в отношении эритроцитарных форм этого вида плазмодия. Препарат действует и на тканевые формы Plasmodium falciparum, но в отношении эритроцитарных форм этого вида он неактивен и для лечения тропической малярии не применяется. Производные 8-аминохинолина вызывают гибель гаметоци-тов всех четырех возбудителей малярии у человека. Особенно ярко это действие проявляется в отношении Plasmodium falciparum. Некоторые штаммы Plasmodium vivax частично устойчивы к примахину (Smoak et al., 1997). Это лишний раз подчеркивает необходимость правильно применять препарат и разрабатывать новые препараты с подобными свойствами.
Механизм действия
Методы выращивания Plasmodium vivax in vitro пока не найдены, поэтому о противомалярийном действии производных 8-аминохинолина известно немного. В частности, не ясно, почему они намного активнее в отношении тканевых форм и гаметоцитов и не действуют на бесполые эритроцитарные формы плазмодиев. Метаболиты примахина могут участвовать в окислительно-восстановительных процессах (см. ниже; Таг-lov et al., 1962), в ходе которых образуются свободные радикалы, и нарушать транспорт электронов в клетке плазмодия (Bates et al., 1990).
Фармакокинетика
При парентеральном введении примахин дает выраженную артериальную гипотонию, поэтому назначают его только внутрь. Всасывается он почти полностью. При однократном приеме сывороточная концентрация примахина достигает максимальной через 3 ч, а затем начинает снижаться с Т1/2, равным 6 ч (Fletcher et al., 1981). Объем распределения в несколько раз выше общего объема жидкости в организме.
Примахин быстро метаболизируется, лишь небольшая часть препарата выводится в неизмененном виде. Все три метаболита примахина активны. Основной из них — карбоксипримахин. При однократном приеме его сывороточная концентрация более чем в 10 раз превышает концентрацию примахина. Выводится карбоксипримахин медленнее исходного вещества и при длительном приеме способен накапливаться в организме (Symposium, 1987). Противомалярийная активность метаболитов примахина значительно ниже, чем у самого препарата. Карбоксипримахин не токсичен, но другие два метаболита являются более сильными метгемоглобинобразователями, чем примахин (Fletcher etal., 1981).
Применение
Примахин высокоактивен в отношении гипнозоитов Plasmodium vivax и Plasmodium ovale, поэтому его применяют в основном для радикального лечения и профилактики рецидивов после возвращения из эндемического района. Чтобы воздействовать на эритроцитарные формы Plasmodium vivax и Plasmodium ovale и замедлить появление устойчивости, препарат назначают совместно с гематошизотропным средством (обычно с хлорохином). Для профилактики рецидивов примахин назначают незадолго до или сразу после отъезда из эндемического района (табл. 40.1 и 40.2). Для радикального лечения примахин применяют как в латентном периоде, когда гипнозоиты еще покоятся в печени, так и во время приступов. Схемы для радикального лечения представлены в табл. 40.2. Длительный прием примахина не рекомендуется, так как при этом повышается риск аллергических реакций и других побочных эффектов.
Побочные эффекты
При назначении белым людям в терапевтических дозах примахин почти не дает побочных эффектов. Повышение дозы иногда вызывает легкие и умеренные нарушения со стороны ЖКТ, в том числе боль в эпигастрии, — эти проявления уменьшаются, если примахин принимают во время еды. Реже отмечаются легкая анемия, цианоз (из-за метгемоглоби-немии) и лейкоцитоз. При приеме высоких доз примахина (60—240 мг/сут) усиливаются нарушения со стороны ЖКТ и метгемоглобинемия, а у некоторых бальных возникает лейкопения. У больных с недостаточностью НАДН-метгемоглобин-редуктазы метгемоглобинемия протекает тяжелее, и ее могут вызвать даже обычные дозы примахина, хлорохина и дапсона (Coleman and Coleman, 1996). Функция печени не нарушается. Изредка возникают нейтропения и агранулоцитоз (обычно это признак передозировки), артериальная гипертония, аритмии и нарушения со стороны ЦНС.
У больных с недостаточностью Г-6-ФД метаболиты примахина (при приеме его в любой дозе) могут вызвать острый гемолиз и гемолитическую анемию. Недостаточность Г-6-ФД наследуется сцепленно с Х-хромосомой и обусловлена заменой аминокислот в молекуле Г-6-ФД. Во всем мире этим заболеванием страдают более 200 млн человек. Описано свыше 400 вариантов строения Г-6-ФД с разной чувствительностью к свободнорадикальному окислению. Около 11% американских темнокожих имеют так называемый вариант А—, который делает их уязвимыми для гемолитического действия окислителей, в том числе примахина. У людей со смуглой кожей (выходцев из Греции, Сардинии, Ирана и у евреев-сефардов) эритроциты могут быть еще более чувствительны к действию примахина. Так как ген, кодирующий Г-6-ФД, расположен на Х-хромосоме, то в крови гетерозиготных женщин есть два вида эритроцитов — нормальные и с недостаточностью Г -6-ФД. При введении примахина таким больным гемолиз зачастую выражен умеренно и, благодаря неполной пенетрантности, развивается не всегда. Помимо примахина еще более 50 препаратов (в том числе сульфаниламиды, применяемые при лечении малярии) и ряд других веществ вызывают гемолиз у больных с недостаточностью Г-6-ФД.
Меры предосторожности и противопоказания
Прежде чем назначить примахин, больному проводят обследование на недостаточность Г-6-ФД. При назначении более 30 мг/сут, а больным из группы риска — более 15 мг/сут примахина (в пересчете на основание) необходимы повторные общие анализы крови и хотя бы макроскопическое исследование мочи.
Примахин противопоказан при обострениях системных заболеваний, протекающих с нейтропенией, например ревматоидного артрита и системной красной волчанки. Примахин не следует назначать больным, получающим другие препараты, способные вызвать гемолиз или угнетение костного мозга.
Прогуанил
Историческая справка
Производное бигуанида прогуанил был создан в 1945 г. в Великобритании в ходе поиска и исследования новых противомалярийных средств. Противомалярийную активность прогуанила приписывают его активному метаболиту циклогуанилу (циклическое производное триазина), который избирательно подавляет дигидрофолатредуктазу плазмодия. Изучение веществ, химически сходных с циклогуанилом, привело к появлению ингибиторов дигидрофолатредуктазы, в том числе пириметамина. Эффект прогуанила не ограничивается угнетением дигидрофолатредуктазы под действием циклогуа-нила. Все больше данных говорят за то, что сам прогуанил также обладает некоторой противомалярийной активностью (Fidock and Wellems, 1997).
Строение
Структурные формулы прогуанила и циклогуанила следующие:
Из множества изученных бигуанидов с противомалярийным действием прогуанил имеет самый высокий порог токсического действия. Более мощный препарат — хлорпрогуанил — содержит атомы хлора в положениях 3 и 4 бензольного кольца. Циклогуанил сходен по строению с пириметамином. Противомалярийное действие. Прогуанил действует на тканевые формы Plasmodium falciparum и эффективен при лечении и профилактике тропической малярии. Препарат улучшает состояние больного во время приступа и обычно позволяет полностью искоренить возбудителя. Прогуанил подавляет приступы малярии, вызванной Plasmodium vivax, но на гипнозоитов этого вида он не действует, поэтому вскоре после отмены препарата часто возникают рецидивы. В отношении гаметоцитовон неактивен, но способен нарушать развитие ооцист в желудке комара.
Механизм действия и устойчивость
Циклогуанил избирательно угнетает дигидрофолатредуктазу чувствительных плазмодиев, что приводит к нарушению синтеза ДНК и дефициту кофер-ментных форм фолиевой кислоты. Этим объясняется медленное противомалярийное действие антагонистов фолиевой кислоты по сравнению с производными аминохинолина. Как уже упоминалось, ген дигидрофолатредуктазы клонирован и расшифрован у чувствительных и устойчивых к пириметамину штаммов Plasmodium falciparum. Обнаружено, что замена соответствующих аминокислот вблизи центра связывания дигидро-фолатредуктазы придает возбудителю устойчивость к циклогуанилу, пириметамину или обоим препаратам сразу. Устойчивость к циклогуанилу (и хлорциклогуанилу) может быть обусловлена одновременной заменой Вал16 и Тре10* дигидрофолат-редуктазы соответственно. Дополнительная замена Лей усиливает устойчивость. У штаммов, устойчивых к пириметамину, происходят другие замены: в основе лежит замена Асп10* на серии' устойчивость возрастает за счет дополнительных замен Apr и Apr59, Иле51 и Лей164. При замене Лей164 многократно усиливается устойчивость к обоим препаратам. При перекрестной устойчивости к циклогуанилу и пириметамину мутации гена, кодирующего дигидрофолатредуктазу, зачастую складываются в сложный узор. Генетический анализ устойчивых штаммов Plasmodium falciparum и современные методы оценки экспрессии генов будут способствовать разработке новых противомалярийных препаратов, зашиты от которых у плазмодия еше нет (Fidock and Wellems, 1997; Cowman, 1998; Cortese and Plowe, 1998).
Противомалярийное действие прогуанила и хлорпрогуанила не ограничивается угнетением дигидрофолатредуктазы плазмодия (Fidock and Wellems, 1998), однако другие механизмы действия этих препаратов пока не изучены. Будучи бигуанидом. прогуанил усиливает деполяризацию митохондриальной мембраны Plasmodium falciparum под действием атоваквона, носам по себе такой активностью не обладает (см. выше, «Атоваквон») (Srivastava and Vaidya, 1999). В отличие от ситуации с циклогуанилом, штаммы, устойчивые к собственному действию прогуанила (при назначении отдельно или в комбинации с атовакво-ном), пока не выявлены.
Фармакокинетика
Прогуанил медленно, но почти полностью всасывается при приеме внутрь. При однократном приеме сывороточная концентрация достигает максимальной через 5 ч. Т1/2 составляет около 20 ч или дольше и зависит от скорости метаболизма. У млекопитающих метаболизм прогуанила, мефе-нитоина и ряда других препаратов протекает при участии изофермента IID6 цитохрома P450. Скорость метаболизма препаратов зависит от активности этого изофермента, которая подвержена индивидуальным колебаниям (Ward et al., 1991). Примерно у 3% белых и у 20% азиатов и кенийцев активность изофермента IID6 низка, и указанные препараты окисляются медленно. При окислении прогуанила образуются два основных метаболита, один из них — циклогуанил, второй — неактивный 4-хлорфенилбигуанид. При назначении 200 мг/сут прогуанила людям с высокой активностью изофермента 1106 сывороточная концентрация циклогуанила может превысить терапевтическую. У людей же с низкой активностью изофермента IID6, напротив, концентрация циклогуанила может оказаться недостаточной для лечебного эффекта (Helsby ct al., 1993). Сам прогуанил при длительном приеме почти не накапливается в тканях, за исключением эритроцитов, где его концентрация примерно в 3 раза превышает сывороточную. Высокая концентрация прогуанила в эритроцитах существенна, когда речь идет о собственной активности препарата (в том числе в комбинации с атовак-воном) в отношении плазмодия. У больных с низкой активностью изофермента IID6 неактивный 4-хлорфенилбигуанид почти не определяется в плазме, но в больших количествах попадает в мочу. От 40 до 60% прогуанила выводится с мочой — либо в неизмененном виде, либо в виде активного метаболита. Применение. В комбинации с хлорохином прогуанил служит безопасной заменой мефлохину и другим препаратам при профилактике тропической малярии или смешанной малярии, вызванной Plasmodium vivax и Plasmodium falciparum, в Восточной, Южной или Центральной Африке (табл. 40.1). В США прогуанил не выпускают, но в Англии и других европейских странах его назначают белым людям, выезжающим в эти области Африки. В местах, где применяют только прогуанил, быстро появляются устойчивые к нему штаммы Plasmodium falciparum, однако неэффективность профилактики можно объяснить и недостаточным образованием циклогуанила у людей с низкой активностью изофермента IID6. Прогуанил не действует на полирезистентные штаммы Plasmodium falciparum в Таиланде и Папуа—Новой Гвинее. Прогуанил может оказаться эффективным для профилактики тропической малярии, вызванной устойчивыми к хлорохину и сульфадоксину/пириметамину штаммами Plasmodium falciparum, которые встречаются в Западной, Экваториальной и Южной Африке.
При приеме внутрь 1 раз в сутки в течение 3 сут в комбинации с атоваквоном (атоваквон/прогуанил) прогуанил хорошо переносится и эффективен при лечении приступов малярии, вызванной устойчивыми к хлорохину и другим противомалярийным препаратам штаммами Plasmodium falciparum и Plasmodium vivax (см. выше, «Атоваквон») (Looareesuwan et al., 1999а, b). Атоваквон/прогуанил оправдал себя при применении в Юго-Восточной Азии, где преобладают полирезистентные штаммы Plasmodium falciparum (Kremsner et al., 1999). Несмотря на эффективность, для профилактики этот комбинированный препарат обычно не применяют, чтобы замедлить развитие устойчивости. При монотерапии прогуанилом или атоваквоном Plasmodium falciparum приобретает устойчивость очень быстро. Устойчивость к комбинированному препарату встречается редко, если только штамм изначально не был устойчивым к атоваквону. Напротив, малярия, вызванная устойчивыми к прогуанилу штаммами, поддается лечению атоваквоном/прогуанилом. Побочные эффекты. В профилактических дозах 200—300 мг/сут прогуанил почти не дает побочных эффектов, лишь иногда могут возникать тошнота и понос. Большие дозы (1 г/сут и более) могут вызывать рвоту, боль в животе, понос, гематурию, преходящее появление спущенного эпителия и эпителиальных цилиндров в моче. При случайной или намеренной передозировке (до 15 г прогуанила) в конце концов наступало полное выздоровление. Прием 700 мг прогуанила 2 раза в сутки в течение более 2 нед не вызывал тяжелых осложнений. Прогуанил безопасен при беременности; хорошо сочетается с другими антагонистами фолиевой кислоты, а также с хлорохином, атоваквоном и тетрациклинами. Это позволяет использовать прогуанил в сочетании с атоваквоном и производными артемизинина, чтобы снизить уровень паразитемии, ограничить распространение паразита и как можно дольше сдерживать развитие устойчивости (van Vugt et al., 1999).
Хинин
Историческая справка
Важнейший из алкалоидов хины — хинин — используют в медицине более 350 лет. Его получают из коры растущих в Южной Америке деревьев рода Cinchona. В 1633 г. монах-августинец Каланча изЛимы (Перу) впервые записал, что «питье из коры дерева цинхона излечивает лихорадку и трехдневную малярию». К 1640 г. кору цинхоны применяли для лечения лихорадки в Европе. В европейской медицинской литературе кора цинхоны впервые упоминается в 1643 г. В Европе основными ее поставщиками были иезуиты, отсюда и произошло название этого лекарственного средства — иезуитский порошок. Еще одним названием — пудра Луго — кора цинхоны обязана кардиналу де Луго: выдающийся философ, живший в Риме, он способствовал распространению чудесного порошка. Однако врачи того времени не спешили признать новый препарат, и лишь в 1677 г. он был внесен в Лондонскую фармакопею под названием cortex peruanus, или перуанская кора (Jarcho, 1993).
Почти 200 лет кору цинхоны использовали в виде порошка, экстракта, настоя или настойки, пока в 1820 г. Пеллетье и Ка ванту не выделили из нее хинин и цинхонин и эти алкалоиды не нашли, наконец, широкое применение. И до сих пор хинин в сочетании с антагонистами фолиевой кислоты или тетрациклинами остается основным препаратом при лечении тропической малярии, вызванной полирезистентными штаммами (табл. 40.2). Однако комбинации из других противомалярийных препаратов грозят вытеснить семидневный курс лечения хинином из-за его токсичности и распространения устойчивых штаммов Plasmodium falciparum (см. ниже, «Перспективы»),
Строение
Хотя хинин удалось синтезировать, процесс этот сложен, поэтому вместе с другими алкалоидами коры цинхоны его получают из природного сырья. Кора цинхоны содержит более 20 алкалоидов. Важнейшие из них — две пары стереоизомеров: хинин и хинидин и цинхонин и цинхонидин. Хинин и цинхо-нидин — левовращающие изомеры. Структурная формула хинина следующая:
Молекула хинина состоит из хинолинового и хинуклидино-вого ядер, соединенных через остаток вторичного спирта. От хинолинового ядра отходит метоксильная группа, а от хинукли-динового — винильная. Хинидин имеет такое же строение, как и хинин, единственное отличие — пространственная конфигурация спиртового остатка. Эти стереоизомеры обладают почти одинаковой активностью: хинидин сильнее хинина действует на малярийного плазмодия, но он же и более токсичен (Krishna and White, 1996). Многие природные алкалоиды, близкие по строению к хинину, а также созданные на его основе полусин-тетические соединения отличаются от хинина главным образом заместителями в боковых цепях. Эти отличия отражаются на количественных, но не качественных характеристиках фармакологического действия. Изучение алкалоидов хины с точки зрения структурно-функциональной зависимости привело к созданию более активных и менее токсичных противомалярийных препаратов, в том числе мефлохина.
Фармакологические эффекты
Противомалярийное действие. Основное действие хинина — гематошизотропное, в отношении спорозоитов и тканевых форм он почти неактивен. Препарат уничтожает гаметоцитов Plasmodium vivax и Plasmodium ovale, но не действует на гаметоцитов Plasmodium falciparum. Такой спектр противомалярийного действия делает хинин непригодным для профилактики малярии. По сравнению с хлорохином хинин более токсичен и менее эффективен при лечении и предупреждении рецидивов малярии, вызванной чувствительными к обоим препаратам штаммами. Однако хинин и его стереоизомер хинидин весьма ценны при лечении тяжелой малярии, вызванной полирезистентными штаммами Plasmodium falciparum, несмотря на то что в некоторых областях Юго-Восточной Азии и Южной Америки такие штаммы становятся все более устойчивыми и к этим двум препаратам.
Механизм действия хинина и сходных с ним аминохинолинов рассмотрен в разделе «Хлорохин». Хинин накапливается в кислой среде пищеварительных вакуолей Plasmodium falciparum — отчасти это можно объяснить тем, что хинин представляет собой слабое основание. Препарат нарушает неферментативную кристаллизацию химически активного и токсичного для плазмодия гематина в нетоксичный малярийный пигмент. Этот процесс протекает в 2 этапа: сначала аминохинолин связывается с гематином, а затем комплексы из препарата и гематина встраиваются в кристалл малярийного пигмента, препятствуя дальнейшей кристаллизации (Sullivan et al., 1996, 1998). Что именно вызывает гибель плазмодия — отложение токсичного гема, действие комплексов из гематина и аминохинолина или и то, и другое — остается неясным.
Механизм устойчивости Plasmodium falciparum к хинину не известен, но, по-видимому, довольно сложен. Как уже упоминалось в разделе «Хлорохин», устойчивые к хинину штаммы Plasmodium falciparum чаще устойчивы к мефлохину и галофантрину, чем к хлорохину. Амплификация гена pfrndrl, с которым связывают устойчивость Plasmodium falciparum к мефлохину и галофантрину, in vitro придает возбудителю устойчивость и к хинину. Однако существуют штаммы, устойчивые к мефлохину, но чувствительные к хинину, и наоборот (Meshnick, 1998; Zalis etal., 1998).
Действие на скелетные мышцы. В клинической практике используется также действие хинина и других алкалоидов хины на скелетные мышцы. Хинин усиливает сокращение мышцы в ответ на одиночное прямое или непрямое раздражение. В то же время препарат удлиняет рефрактерный период мышцы, и в результате снижается амплитуда тетануса при высокочастотном раздражении. Кроме того, уменьшается возбудимость постсинаптической мембраны нервно-мышечных синапсов, что также снижает ответ мышцы на ритмическое раздражение нерва и на действие ацетилхолина. Таким образом, хинин не хуже миорелаксантов устраняет действие физостигмина. У больных миастенией хинин может вызвать тяжелое нарушение дыхания и дисфагию. Препарат может дать временное облегчение при врожденной миотонии. По клинической картине это заболевание — противоположность миастении, поэтому средства, помогающие при миастении, ухудшают состояние при миотонии, и наоборот.
Фармакокинетика
Хинин и сходные с ним аминохинолины быстро всасываются при приеме внутрь ив/м введении. При приеме внутрь всасывание происходит главным образом в верхних отделах тонкой кишки, и даже при сильном поносе всасывается более 80% препарата. Сывороточная концентрация достигает максимальной через 3—8 ч, объем распределения у здоровых людей составляет около 1,5 л/кг, а после отмены препарата сывороточная концентрация снижается сТ1/2 около 11ч. Фармакокинетика хинина зависит от тяжести малярии (Krishna and White, 1996). При тяжелой малярии объем распределения хинина снижается, еще больше снижается клиренс, и Т1/2 возрастает до 18 ч. При назначении терапевтических доз хинина взрослым с тяжелыми приступами сывороточная концентрация препарата может достигать 15—20 мг/л, но выраженного токсического действия при этом не наблюдается (см. ниже). Однако при намеренном приеме больших доз препарата (например, с целью самоубийства) сывороточная концентрация более 10 мг/л вызывает тяжелое отравление. Предположительно, при тяжелой малярии вырабатывается много кислого аггликопротеида, который, связываясь с хинином, уменьшает его свободную фракцию на 5— 10% общей сывороточной концентрации, тем самым предотвращая токсическое действие препарата (Krishna and White, 1996). По мере выздоровления сывороточная концентрация сц-гликопротеида уменьшается, объем распределения и клиренс хинина растут, а сывороточная концентрация снижается. Концентрация хинина в эритроцитах составляет 33—40%, в СМЖ — 2—5% сывороточной; препарат легко проходит через плаценту.
Алкалоиды хины активно метаболизируются, главным образом, под действием изофермента IIIA4 цитохрома Р450 (Zhaoet al., 1996), и лишь около 20% введенного препарата попадает в мочу в неизмененном виде. Метаболиты алкалоидов хины выводятся с мочой, поэтому даже при длительном лечении они не накапливаются. В то же время основной метаболит хинина 3-гидроксихинин, обладающий некоторой противомалярийной активностью, может накапливаться и оказывать токсическое действие у больных с ХПН (Newton et al., 1999). Выведение хинина почками ускоряется при закислении мочи. Применение. Малярия. Несмотря на токсичность, хинин остается основным гематошизотропным средством для лечения малярии, вызванной устойчивыми к хлорохину и другим препаратам штаммами Plasmodium falciparum. Тяжелое течение малярии требует срочного в/в введения насыщающей дозы хинина (или хинидина) — иногда только это может спасти жизнь неиммунным больным. Как только больной будет в состоянии принимать пищу, хинин назначают внутрь. Для поддержания терапевтических концентраций препарата курс лечения должен составлять 5—7 сут. При тропической малярии, вызванной полирезистентными штаммами, в дополнение к хинину назначают гематошизотропные препараты медленного действия (сульфаниламиды или тетрациклины). Лекарственные формы хинина и хинидина и схемы лечения тропической малярии с использованием этих средств представлены выше.
Схемы в табл. 40.2 подобраны эмпирически, и при необходимости их можно и нужно менять. За последние 20 лет разработаны схемы лечения тропической малярии в Юго-Восточной Азии с учетом оптимальных насыщающих доз для хинина и хинидина (Krishna and White, 1996). Как уже говорилось, при назначении хинина в полных терапевтических дозах взрослым с тяжелыми приступами сывороточная концентрация его достигает 15—20 мг/л, но токсическое действие не наступает. Терапевтический диапазон свободного хинина составляет 0,2—2 мг/л. Такой сывороточной концентрации можно добиться с помощью различных схем лечения, в зависимости от возраста больного, тяжести состояния и чувствительности Plasmodium falciparum к хинину. Так, лечение тропической малярии у детей в Африке требует более низкихдоз хинина, чем лечение взрослых в Юго-Восточной Азии, — различна не только чувствительность плазмодия в этих двух районах, но и фармакокинетика препарата у разных групп населения (Krishna and White, 1996). Если в течение 48 ч от начала лечения улучшение не наступает, дозу хинина нужно снизить на 30—50%, чтобы предупредить накопление и токсическое действие препарата (Krishna and White, 1996). Схемы для хинидина и хинина почти одинаковы, но хинидин в меньшей степени связывается с белками плазмы, обладает большими объемом распределения и клиренсом и меньшим конечным Т1/2,чем хинин (Milleretal., 1989; Krishna and White, 1996). Ночные судороги ног. Прием 200—300 мг хинина внутрь перед сном уменьшает ночные судороги ног. У одних улучшение наступает уже после короткого курса лечения, другим не помогают и большие дозы препарата. До 1995 г. хинин можно было купить без рецепта, но позднее ФДА запретило безрецептурную продажу препарата, ссылаясь на недостаток данных, подтверждающих его безопасность и эффективность при этом заболевании.
Побочные эффекты
Смертельная доза хинина для взрослых составляет 2—8 г. При назначении полных терапевтических доз или передозировке хинин может вызвать триаду дозозависимых побочных эффектов: симптомы отравления, гипогликемию и артериальную гипотонию. Легкое отравление хинином проявляется шумом в ушах, тугоухостью на звуки высоких частот, нарушением зрения, головной болью, дисфорией, тошнотой, рвотой и ортостатической гипотонией, встречается часто и быстро проходит при отмене препарата. Гипогликемия — также достаточно частое осложнение и может угрожать жизни больного, если вовремя не ввести в/в глюкозу. Реже развивается артериальная гипотония — она может быть тяжелой и чаще возникает при слишком быстром в/в введении больших доз хинина или хинидина. При длительном лечении или однократном назначении высокой дозы препарата могут возникнуть нарушения со стороны ЖКТ, сердечно-сосудистой системы и поражение кожи. Эти и другие проявления токсического действия хинина подробнее описаны ниже.
Больше всего страдают слух и зрение. Нарушение функции VIII пары черепных нервов проявляется шумом в ушах, снижением остроты слуха и головокружением. Со стороны глаз могут возникать нечеткость зрения, нарушение цветового зрения, светобоязнь, диплопия, гемералопия, сужение полей зрения, скотомы, мидриаз и даже слепота (Bateman and Dyson, 1986). Нарушения зрения и слуха, по-видимому, вызваны прямым нейро-токсическим действием хинина, хотя может играть роль и поражение сосудов. Из-за сильного спазма сосудов нарушается кровообращение в сетчатке, диск зрительного нерва бледнеет, может развиться отек сетчатки и, в тяжелых случаях, наступить атрофия зрительного нерва.
Еще один признак отравления хинином — нарушения со стороны ЖКТ. Хинин обладает местным раздражающим действием и вызывает тошноту, рвоту, боль в животе и понос, но тошнота и рвота могут быть и центрального происхождения. Кожа часто гиперемирована и горячая на ощупь, усиливается потливость. Нередко появляется сыпь. Иногда возникает отек Квинке, особенно на лице.
Лаже в терапевтических дозах хинин и хинидин сильно стимулируют р-клетки поджелудочной железы и могут вызывать гиперинсулинемию и тяжелую гипогликемию. Несмотря на срочное введение глюкозы в/в, это состояние может угрожать жизни, особенно при беременности и при длительном и тяжелом течении малярии.
Если сывороточная концентрация хинина не превышает терапевтическую, нарушения со стороны сердечно-сосудистой системы возникают редко (Krishna and White, 1996). Однако слишком быстрое в/в введение препарата может вызвать тяжелую артериальную гипотонию. Передозировка может привести к тяжелым и даже смертельным аритмиям, в том числе остановке синусового узла, АВ-узловому ритму, АВ-блокаде, желудочковой тахикардии и фибрилляции желудочков (Bateman and Dyson, 1986). У хинидина кардиотоксическое действие выражено сильнее, чем у хинина (гл. 35).
Если признаки отравления возникают даже при введении низких доз алкалоидов хины, то это может указывать на аллергию к препарату. Отравление — обычно легкое — иногда возникает уже при первом приеме хинина. Аллергические реакции проявляются зудом, приливами, сыпью, повышением температуры, болью в эпигастрии, одышкой, звоном в ушах и нарушением зрения; чаще всего наблюдаются сильные приливы и генерализованный зуд. Возможны приступы бронхиальной астмы. Изредка при тропической малярии аллергическая реакция на хинин проявляется массивным гемолизом с гемоглобинеми-ей и гемоглобинурией; последняя может привести к анурии, ОПН и смерти. Иногда хинин вызывает не столь тяжелый гемолиз, особенно у лиц с недостаточностью Г-6-ФД. Другой редкий побочный эффект — тромбоцитопеническая пурпура: при этом комплексы антитело—хинин активируют комплемент, что ведет к разрушению тромбоцитов. Такое состояние может развиться даже при питье напитков, содержащих хинин («коктейльная пурпура»). Прочие редкие осложнения — гипопротромбинемия, лейкопения и агранулоцитоз. Высокие дозы хинина, применяемые для возбуждения и усиления родовой деятельности, могут оказать неблагоприятное влияние на плод.
Меры предосторожности, противопоказания и лекарственные взаимодействия
Больным с аллергической реакцией на хинин в анамнезе, особенно если она проявлялась поражением кожи, отеком Квинке, нарушениями зрения или слуха, препарат если и назначают, то с большой осторожностью. При появлении признаков гемолиза хинин немедленно отменяют. Противопоказаниями служат шум в ушах и неврит зрительного нерва. При назначении хинина больным с аритмиями следует соблюдать те же предосторожности, что и при назначении хинидина (гл. 35).
Препараты хинина для парентерального введения обладают сильным раздражающим действием, поэтому п/к хинин не вводят. Концентрированные растворы могут вызвать абсцесс при в/м введении или тромбофлебит — при в/в введении. Всасывание хинина при приеме внутрь может замедляться под действием антацидных средств, содержащих алюминий. В свою очередь, хинин и хинидин могут замедлять всасывание и приводить к увеличению сывороточной концентрации дигоксина и сходных с ним сердечных гликозидов (гл. 34 и 35). Хинин и хинидин могут также увеличивать сывороточную концентрацию варфарина и других непрямых антикоагулянтов. За счет действия на нервно-мышечные синапсы хинин усиливает эффект миорелаксантов и ослабляет эффект ингибиторов АХЭ (см. выше). Клиренс хинина уменьшается под действием циметидина и увеличивается при закислении мочи.
Хлорохин
Историческая справка
Хлорохин был открыт в ходе обширного исследования по поиску противомалярийных препаратов, которое проводилось в США в годы Второй мировой войны. С 1943 г. были синтезированы и изучены тысячи производных 4-аминохинолина, хлорохин оказался самым активным из них и был допущен к клиническим испытаниям. После окончания войны выяснилось, что тот же препарат под названием резохин был получен и исследован немецкими учеными еще в 1934 г. Строение. Структурная формула хлорохина следующая:
Хлорохин по строению близок к устаревшим противомалярийным препаратам — производным 8-аминохинолина памахину и пентахину. Хлорохин содержит такую же боковую цепь, как и мепакрин, но отличается от него наличием хинолинового ядра вместо акридинового и отсутствием метоксильной группы. Правовращающий и левовращающий изомеры хлорохина, а также рацемическая смесь одинаково активны при малярии у уток, но у млекопитающих правовращающий изомер оказался менее токсичен, чем левовращающий. Атом хлора в положении 7 хинолинового ядра увеличивает активность хлорохина при малярии как у птиц, так и у человека. Продолжается изучение зависимости между химическим строением и активностью хлорохина и сходных с ним алкалоидов в надежде найти новые эффективные и безопасные средства для лечения тропической малярии, вызванной устойчивыми к хлорохину и другим препаратам штаммами (см. ниже, а также Goldberg et al., 1997; O'Neill et al.. 1998: Raynes, 1999).
Близкий по строению к хлорохину амодиахин может оказывать гепатотоксическое действие и вызывать агранулоцитоз, поэтому для профилактики тропической малярии его больше не используют. Сходный с ним пиронаридин (создан в Китае в 1970-х гг.) эффективен при малярии, вызванной Plasmodium vivax и Plasmodium ovale, и хорошо переносится больными. Но для широкого применения его рекомендовать нельзя, так как схемы лечения еще не отработаны и не до конца изучены отдаленные побочные эффекты (Naisbitt et al., 1998). Гидроксихлрохин отличается от хлорохина тем, что у него одна из N-этильных групп гидроксилирована в p-положении. По активности в отношении Plasmodium falciparum гидроксихлорохин сходен с хлорохином. При нетяжелом ревматоидном артрите и системной красной волчанке лучше назначать гидроксихлорохин, поскольку в высоких дозах, необходимых для лечения, он реже, чем хлорохин. вызывает поражение глаз (Easterbrook, 1999).
Фармакологические эффекты
Противомалярийное действие. Хлорохин высокоактивен в отношении бесполых эритроцитарных форм Plasmodium vivax, Plasmodium ovale, Plasmodium malariae и чувствительных штаммов Plasmodium falciparum. Действует он и на гаметоцитов (за исключением Plasmodium falciparum). На гипнозоитов Plasmodium vivax и Plasmodium ovale хлорохин не действует. Другие эффекты. Хлорохин и его аналоги применяют не только для лечения малярии. Использование этих средств при амебном абсцессе печени описано в гл. 41. Хлорохин и гидроксихлорохин используют в качестве препаратов второго ряда при различных хронических заболеваниях, поскольку оба алкалоида накапливаются в лизосомах и оказывают противовоспалительное действие. Так, высокие дозы этих препаратов, часто назначаемых совместно с другими средствами, эффективны при ревматоидном артрите, системной и дискоидной красной волчанке, саркоидозе и фотодерматозах, таких, как поздняя кожная порфирия и полиморфный фотодерматоз (Danning and Boumpas, 1998; Fritschetal., 1998; Baltzanetal., 1999).
Механизм действия и устойчивость
Находясь в эритроцитах, бесполые формы малярийного плазмодия питаются гемоглобином. В кислой среде пищеварительных вакуолей плазмодия гемоглобин распадается на гем и глобин. При распаде железо в молекуле гема окисляется, и гем переходит в гематин. Образующиеся при окислении свободные радикалы обладают высокой химической активностью. И гем, и свободные радикалы могут повреждать клеточные мембраны, поэтому плазмодий стремится любым способом избавиться от этих соединений. Так, гем (гематин) подвергается кристаллизации. Сначала при участии богатых гистидином белков и, возможно, липидов образуются димеры гематина (ядра кристаллизации), а затем димеры собираются в кристаллы нерастворимого и химически неактивного малярийного пигмента. Накапливаясь в пищеварительных вакуолях плазмодия, аминохинолины (слабые основания) повышают pH, подавляют разрушение гема перекисью водорода и нарушают кристаллизацию гематина. В результате гем откладывается в клетке, и плазмодий погибает вследствие окисления мембран, протеаз пищеварительной вакуоли и других молекул, необходимых для его жизнедеятельности (Foley and Tilley, 1998). Подавление кристаллизации гематина, вероятно, является ключевым механизмом действия аминохинолинов. Недавние исследования показали, что меченые хлорохин, хинидин и мефлохин сначала связываются с гематином, а затем в виде комплексов из гематина и препарата встраиваются в кристаллы малярийного пигмента, препятствуя дальнейшей кристаллизации. По-видимому, также действуют амодиахин, мепакрин и хинин, но не примахин (Sullivan etal., 1996; Mungthinetal., 1998). Предстоит еще выяснить, ограничивается ли противомалярийное действие аминохинолинов только нарушением кристаллизации гематина, или есть и другие — неизученные пока — механизмы (Ginsburg et al., 1998; Bray et al., 1998; Loria et al., 1999).
Сама по себе устойчивость бесполых эритроцитарных форм Plasmodium falciparum к аминохинолинам, особенно хлорохину, развивается медленно, но сейчас устойчивые штаммы распространены повсеместно, особенно там, где аминохинолины используются чаще всего (рис. 40.2). Механизмы развития устойчивости к разным аминохинолинам различны (см. ниже), здесь мы рассмотрим только устойчивость к хлорохину. Более 20 лет назад было показано, что устойчивые штаммы Plasmodium falciparum накапливают хлорохин в меньшей степени, чем чувствительные (Fitch et al., 1979). Причины такой избирательности до конца не выяснены. Возможно, с появлением устойчивости нарушаются процессы захвата и транспорта хлорохина в пищеварительную вакуоль, или же препарат начинает быстро вы водиться из вакуоли, не задерживаясь в ней (Goldberg et al., 1997; Brayet al., 1998; Foley and Tilley, 1998).
Верапамил привлек внимание исследователей способностью подавлять опосредуемое Р-гликопротеидом выведение лекарственных средств полирезистентными опухолевыми клетками. Оказалось, что сходное действие верапамил оказывает и на хлорохин, уменьшая его выведение из пищеварительной вакуоли Plasmodium falciparum, тем самым частично восстанавливая чувствительность возбудителя (Foley and Tilley, 1998). Позже у Plasmodium falciparum были открыты два гена, гомологичных генам mtr, отвечающим за полирезистентность к антимикробным средствам у бактерий — pfmdrl и pfmdr2(Wilson et al.. 1989; Foote et al., 1989). Однако генетические исследования показали, что ни один из этих генов не связан с устойчивостью к хлорохину (Wellems et al., 1990). Ген pfmdrl кодирует белок Pgh I, подобный Р-гликопротеиду. При избыточной экспрессии этого гена плазмодий может приобрести относительную чувствительность к хлорохину, сохраняя устойчивость к таким препаратам, как мефлохин, галофантрин и хинин (Cowman et al., 1994). Популяционные испытания не обнаружили связи между устойчивостью к хлорохину и изменениями гена pfmdr/ (von Scidlein et al., 1997; Povoa et al., 1998; Zaliset al., 1998). He удалось доказать и эффективность совместного назначения хлорохина и ингибиторов опосредуемого Р-гликопротеидом транспорта при лечении малярии, вызванной устойчивыми к хлорохину Plasmodium falciparum. Данные, полученные при изучении штаммов плазмодия, как лабораторных, так и выделенных от больных, — позволяют предположить, что устойчивость к хлорохину, мефлохину, гапофантрину и хинину обусловлена по крайней мере гремя различными механизмами (Zaliset al., 1998; Reed el al., 2000).
Недавно получила подтверждение гипотеза о существовании переносчика хлорохина в пищеварительную вакуоль плазмодия (Sanchez et al., 1997). В одном из исследований было установлено, что ген устойчивости Plasmodium falciparum к хлорохину расположен на 7-й хромосоме, на участке длиной 36 000 нуклеотидов (Su et al., 1997). В этом участке находится ген cg2 со сложным полиморфизмом, кодирующий белок с молекулярной массой 330 000. У 20 из 21 штамма определенный набор аллелей был связан с устойчивостью к хлорохину. Однако один штамм из 20 с таким набором аллелей оказался чувствительным, то есть наличие указанного набора аллелей было необходимым, но не достаточным условием устойчивости к хлорохину. Это исследование подтвердило клинические данные о различной природе устойчивости Plasmodium falciparum к хлорохину в Южной Америке, Азии и Африке. Белок Cg2, кодируемый геном cg2, обнаружен и в пищеварительной вакуоли, где он связан с малярийным пигментом, и в цитоплазме плазмодия, что также говорит об участии этого белка в переносе хлорохина (Su et al., 1997). Дальнейшие исследования подтвердили связь полиморфизма гена cg2 и устойчивости к хлорохину у штаммов, выделенных от людей, вернувшихся из эндемических районов (Durand et al., 1999). Уже выделены вещества, которые могут служить маркерами для выявления штаммов, устойчивых к хлорохину за счет наличия гена cg2(Goldberg et al., 1997). Таким образом, за различные механизмы устойчивости к хлорохину отвечает сложная система, состоящая из целого ряда генов.
Фармакокинетика
Хлорохин хорошо всасывается при приеме внутрь, в/м и п/к введении. Распределяется он относительно медленно, объем распределения очень велик — более 100 л/кг (Krishna and White, 1996). Это объясняется способностью хлорохина накапливаться в тканях, особенно в печени, селезенке, почках, легких, тканях, содержащих меланин, и, в меньшей степени, в головном и спинном мозге. Хлорохин на 60% связывается с белками плазмы и метаболизируется в печени с участием микросомальных ферментов. При этом образуются два основных метаболита: N-дезэтилхлорохин и N,N-дидезэтилхлорохин (Ducharmeand Farinotti, 1996). Их сывороточные концентрации достигают соответственно 40 и 10% концентрации хлорохина. Правовращающий стереоизомер хлорохина в большей степени, чем левовращающий, связывается с белками плазмы и быстрее выводится из организма (Krishna and White, 1996). Почечный клиренс хлорохина составляет примерно половину его суммарного клиренса. Среди соединений хлорохина, обнаруживаемых в моче, 50% приходится на неизмененный препарат и 25% — на его основной метаболит N-дезэтилхлорохин. Выведение обоих соединений почками усиливается при закислении мочи.
Фармакокинетика хлорохина сложна: сывороточная концентрация сразу после введения зависит больше от особенностей распределения, чем от элиминации (Krishna and White, 1996). Препарат в значительной степени накапливается в тканях, поэтому, чтобы достигнуть необходимой сывороточной концентрации, начинают с насыщающей дозы. Хлорохин медленно распределяется, и при быстром парентеральном введении его сывороточная концентрация может временно стать слишком высокой или даже смертельной. Поэтому препарат вводят медленно путем длительной в/в инфузии или дробно небольшими дозами п/к или в/м (Foley and Tilley, 1998). Но все же безопаснее назначать хлорохин внутрь, так как скорость всасывания и распределения препарата при этом больше соответствуют друг другу. Сывороточная концентрация достигает максимальной через 3—5 ч после приема внутрь. По мере ее снижения Т1/2 хлорохина увеличивается от нескольких дней до нескольких недель, отражая сначала медленное распределение, а затем медленное выведение препарата из тканевых депо. Конечный Т1/2, хлорохина составляет 30—60 сут, а следы препарата в моче можно обнаружить спустя годы после лечения.
Применение
Хлорохин — самый универсальный из противомалярийных препаратов, но с появлением устойчивых (частично или полностью) штаммов Plasmodium falciparum ценность его снизилась. Хлорохин действует сильнее хинина и менее токсичен, а для поддерживающей терапии его достаточно назначать лишь раз в неделю. Хлорохин не годится ни для профилактики, ни для радикального лечения малярии, вызванной Plasmodium vivax и Plasmodium ovale. Однако он высокоэффективен при лечении приступов малярии, вызванной этими видами, кроме районов (например, Океании), где обнаружены относительно устойчивые штаммы Plasmodium vivax (Newton and White, 1999). После отмены хлорохина могут возникать рецидивы малярии, вызванной Plasmodium vivax, но интервалы между приступами удлиняются. Для искоренения плазмодия можно применять хлорохин совместно с примахином или назначить примахин после того, как больной покинет эндемическую зону. Хлорохин весьма эффективен для профилактики и лечения малярии, вызванной Plasmodium malariae и чувствительными штаммами Plasmodium falciparum, которые все еще встречаются в отдельных эндемических районах (рис. 40.2). На фоне лечения приступ быстро стихает, исчезает пара-зитемия. У большинства больных температура нормализуется через 24—48 ч от начала приема препарата, а через 48—72 ч паразит не обнаруживается в толстой капле. Если на второй день лечения состояние больного не улучшается, малярия, скорее всего, вызвана устойчивым штаммом Plasmodium falciparum и хлорохин следует заменить хинином или другим быстродействующим гема-тошизотропным препаратом. При рвоте или коме хлорохин можно вводить парентерально до тех пор, пока больной не сможет принимать его внутрь. Но чаще в таких случаях переходят на введение хинидина глюконата. У детей в коме хлорохин хорошо всасывается и эффективен при введении через назогастральный зонд. В табл. 40.1 и 40.2 приведены схемы лечения и профилактики малярии. в том числе с применением хлорохина. В зависимости от состояния больного и от наличия устойчивых к хлорохину штаммов схемы могут меняться. Так, у лиц, проживающих в эндемических районах, нередко развивается частичная устойчивость к малярии. Таким больным может подойти сокращенная схема или будет достаточно симптоматического лечения.
Побочные эффекты
При правильном подборе дозы хлорохин почти не дает побочных эффектов. Тем не менее быстрое парентеральное введение хлорохина — даже в терапевтических дозах — может привести к отравлению (см. выше). Побочные эффекты затрагивают главным образом сердечно-сосудистую систему и ЦНС. Осложнения со стороны сердечно-сосудистой системы включают артериальную гипотонию, расширение сосудов, снижение сократимости миокарда, аритмии и остановку кровообращения. К побочным эффектам со стороны ЦНС относятся спутанность сознания, судороги и кома. Парентеральное введение более 5 г хлорохина за один раз смертельно. Спасти жизнь больному может И BJ1, введение адреналина и диазепама.
В дозах для лечения приступов малярии хлорохин (внутрь) может вызвать нарушения со стороны ЖКТ, головную боль, нарушения зрения и крапивницу. Иногда возникает зуд, особенно у темнокожих. При длительной поддерживающей терапии возможны головная боль, нечеткость зрения, диплопия, спутанность сознания, судороги, сыпь, похожая на красный плоский лишай, поседение, расширение комплекса QRS, изменения зубца Т. Эти нарушения обычно быстро проходят после отмены препарата. Изредка отмечаются гемолиз и угнетение кроветворения. Хлорохин может вызвать изменение цвета ногтей и слизистых и влиять на иммуногенность некоторых вакцин (Brachman et al., 1992; Horowitz and Carbonaro, 1992; Pappaioanouetal., 1986).
Высокие дозы хлорохина (> 250 мг/сут) или гидроксихлорохина при лечении других заболеваний могут оказывать тяжелое ототоксическое действие и вызывать необратимую ретинопатию, которая, по-видимому, связанас накоплением препарата в тканях, богатых меланином. При назначении менее 250 мг хлорохина в сутки ретинопатия не развивается (Rennie, 1993). Длительное лечение высокими дозами любого из производных 4-аминохинолина иногда приводит к нейропатии и миопатии с поражением скелетных мышц и миокарда. Эти проявления исчезают, если препарат сразу отменить (Estes et al., 1987). В редких случаях при передозировке могут возникать неврологические и психические нарушения, вплоть до самоубийства.
Меры предосторожности и противопоказания
Хлорохин не рекомендуется назначать больным эпилепсией и миастенией (Griffin. 1999). При сопутствующих заболеваниях печени, тяжелых поражениях ЖКТ, нервной системы и болезнях крови препарат назначают с большой осторожностью. Если такие состояния развиваются уже во время лечения, хлорохин следует отменить.
У больных с недостаточностью Г-6-ФД хлорохин может вызвать гемолиз (см. выше, «Примахин»), Не следует назначать одновременно с хлорохином препараты золота и фенилбутазон, поскольку все эти лекарственные средства вызывают дерматит. Больным с псориазом и эксфолнативной эритродермией хлорохин не назначают, так как он может вызвать резкое ухудшение состояния. Хлорохин вступает во взаимодействие с множеством разных препаратов. Его нельзя назначать совместно с мефлохином. поскольку при этом повышается риск эпилептических припадков. Важно помнить, что хлорохин сводит на нет действие противосудорожных средств, а при совместном назначении с амиодароном или галофантрином увеличивает риск возникновения желудочковых аритмий. Хлорохин увеличивает сывороточные концентрации дигоксина и циклоспорина, тем самым повышая риск побочных эффектов этих препаратов. При длительном лечении высокими дозами хлорохина раз в 3—6 мес следует проводить офтальмологическое и неврологическое обследование.
Антибактериальные средства
Вскоре после начала применения сульфаниламидов выяснилось, что они обладают противомалярийной активностью; это свойство активно изучалось во время Второй мировой войны. Тогда же было выявлено противомалярийное действие сульфонов — в 1943 г. дапсон был впервые использован для лечения тропической малярии. При тропической малярии, вызванной устойчивыми к хлорохину штаммами (особенно в Африке), сульфаниламиды применяют совместно с пириметамином и хинином. Гематошизотропное действие тетрациклинов развивается медленно, их используют для кратковременной профилактики малярии и — в сочетании с хинином — для лечения малярии, вызванной полирезистентными штаммами Plasmodium falciparum.
Сульфаниламиды и сульфоны
Эти лекарственные средства относятся к гематошизотропным препаратам медленного действия и более активны в отношении Plasmodium falciparum, чем Plasmodium vivax. Сульфаниламиды — структурные аналоги парааминобензойной кислоты — конкурентно ингибируют дигидро птероатсинтазу Plasmodium falciparum. Чтобы усилить противомалярийное действие сульфаниламидов, их применяют вместе с ингибиторами дигидрофолатредуктазы. Так, сульфадиазин в сочетании с ингибитором дигидрофолатредуктазы пириметамином и хинином с успехом используется в Африке при лечении приступов тропической малярии, вызванной устойчивыми к хлорохину штаммами. В отдельных районах Африки комбинированный препарат сульфадоксина и пириметамина (сульфадоксин/пириметамин, см. выше) начинают принимать при приступе малярии еше до осмотра врачом. В состав еще одного комбинированного препарата, применяемого в Африке и действующего на устойчивых к хлорохину Plasmodium falciparum, входят дапсон и хлорпрогуанил.
Антагонисты фолиевой кислоты действуют медленно, и потому их лучше назначать вместе с быстродействующими и более эффективными препаратами, например производными артемизинина. Из-за высокой токсичности сульфадоксина длительный прием сульфадоксина/пиримстамина для профилактики тропической малярии больше не рекомендуют (см. выше и гл. 44) (Bjorkman and Phillips-Howard, 1991). Многие штаммы Plasmodium falciparum уже устойчивы к антагонистам фолиевой кислоты, и такая устойчивость быстро возникает в ходе лечения, что делает эти препараты все менее эффективными. Мутации, приводящие к замене аминокислот в разных участках гена дигидроптероатсинтазы Plasmodium falciparum, вызывают устойчивость к сульфадоксину, а также увеличивают К{ других сульфаниламидов и дапсона, снижая тем самым активность этих препаратов. В свою очередь, мутации гена дигидрофолатредуктазы вызывают устойчивость к пириметамину и циклогуанилу. Накапливаясь, мутации могут значительно снизить эффективность лечения тропической малярии комбинированными препаратами, в состав которых входят антагонисты фолиевой кислоты (Cowman, 1998).
Тетрациклины
При лечении приступов малярии, вызванной полирезистентными штаммами Plasmodium falciparum, которые отчасти устойчивы и к хинину, тетрациклины представляют особую ценность (Chongsuphajaisiddhi et al., 1986). Действуют тетрациклины медленно, и потому, чтобы быстро снизить уровень паразитемии, к ним обязательно добавляют хинин. Назначать можно любой из препаратов, но обычно предпочтение отдаюттетрациклину или доксициклину. Тетрациклин высокоактивен в отношении тканевых шизонтов Plasmodium falciparum, устойчивых к хлорохину, но применять его для длительной профилактики малярии не рекомендуют. Доксициклин же назначают людям, выезжающим в эндемические районы, для кратковременной профилактики малярии, вызванной полирезистентными штаммами. Схемы приема тетрациклинов приведены в табл. 40.1 и 40.2. Тетрациклины оказывают побочное действие на кости и зубы, поэтому эти препараты нельзя назначать беременным и детям до 8 лет. При лечении тетрациклинами может возникнуть фотосенсибилизация или суперинфекция устойчивыми к ним микроорганизмами — это прямое показание к отмене препаратов как при лечении, так и при профилактике (гл. 47).
Принципы профилактики и лечения малярии
Борьба с малярией сложна. Более 85% случаев малярии вызывает Plasmodium falciparum, и именно на тропическую малярию приходится большинство летальных исходов. Устойчивость Plasmodium falciparum к имеющимся лекарственным средствам продолжает расти. К счастью, малярию, вызванную Plasmodium ovale, Plasmodium malariae и большинством штаммов Plasmodium vivax, пока еще удается вылечить хлорохином (Newton and White, 1999), и в отдельных районах еще встречаются чувствительные к нему штаммы Plasmodium falciparum. Однако, за исключением Мексики, Центральной Америки к западу от Панамского канала, стран Карибского бассейна и некоторых районов Южной Америки и Ближнего Востока, во всех эндемических районах преобладают штаммы Plasmodium falciparum, устойчивые к этому препарату (рис. 40.2). Кроме некоторых областей Африки, возбудители, устойчивые к хлорохину, устойчивы и к су-льфадоксину/пириметамину, недорогому комбинированному препарату из двух антагонистов фолиевой кислоты, который широко используется для лечения тропической малярии. Тропическая малярия, вызванная полирезистентными возбудителями, протекает тяжело и чаше всего встречается в Юго-Восточной Азии и Океании, но теперь она захватила и Южную Америку и угрожает Африке. При монотерапии, например мефлохином или хинином, такая форма малярии может не поддаться лечению даже токсическими дозами препаратов.
Генетические исследования показывают, что в эндемических районах каждый штамм Plasmodium falciparum содержит множество клонов паразита с разной степенью устойчивости к противомалярийным препаратам (Druil-he et al., 1998). Каждый клон может быть устойчив к целому ряду препаратов, и разные клоны по-разному отвечают на лечение. С другой стороны, устойчивость клона к определенному препарату может быть опосредована несколькими, подчас неоднородными, мутациями. Таким образом, монотерапия тропической малярии способствует отбору и распространению устойчивых штаммов, что в конце концов делает такое лечение неэффективным и даже опасным для больного. Паразиты, устойчивые к нескольким препаратам, могут быстрее вырабатывать устойчивость к новым противомалярийным средствам (Rathod etal., 1997). Наряду с данными фармакокинетических и фармакодинамических исследований это наблюдение подчеркивает, насколько важно при лечении тропической малярии, вызванной устойчивыми плазмодиями, использовать не менее двух препаратов, дополняющих друг друга по механизму действия (White, 1997, 1999). Обнадеживающие результаты получены при использовании таких схем: производное артемизинина, а затем мефлохин; производное артемизинина, хлорпрогуанил и дапсон; атоваквон/прогуанил. Рекомендованные схемы профилактики и лечения малярии у неиммунных лиц представлены в табл. 40.1 и 40.2. Схемы эти ориентировочные, со временем устаревают и требуют поправок, учитывающих состояние и место проживания больного, происхождение, вид и устойчивость возбудителя, а также противомалярийные препараты, применяемые в данной местности.
Здесь мы рассмотрим лишь общие принципы профилактики и лечения малярии. Подробнее о каждом препарате и его применении можно узнать из предыдущих разделов этой главы и из дополнительной литературы (Zucker and Campbell, 1993; Newton and White, 1999). Последние сведения о районах с повышенным риском заражения малярией и о ее профилактике можно получить в Центре по контролю заболеваемости, либо на странице Центра в интернете (www.cdc.gov/travel/travel.html), либо по бесплатному факсу (888-232-3299). Срочную консультацию по лечению круглосуточно предоставляют в Отделе паразитологии Центра по контролю заболеваемости (тел. 770-488-7760).
Медикаментозная профилактика не должна заменять простые и недорогие меры предупреждения малярии. Так, находясь в эндемических районах, нужно пользоваться индивидуальными средствами защиты от укусов — особенно утром и вечером, когда комары наиболее активны. Одежду лучше выбирать темную и с длинными рукавами, использовать репелленты на основе 30% диэ-тилтолуамида (ДЭТА), спать в хорошо защищенных от комаров помещениях (оконные сетки или пологи, пропитанные перметрином или другими пиретринами) (Zucker and Campbell, 1993).
В эндемических районах лучший препарат для профилактики — мефлохин. При непереносимости мефлохина назначают доксициклин. Если противопоказаны оба эти препарата, остается только рассчитывать на менее эффективные схемы. Так, в некоторых областях Африки южнее Сахары для профилактики малярии, вызванной устойчивыми к хлорохину штаммами Plasmodium falciparum, используют хлорохин в сочетании с прогуанилом. Там, где эти штаммы широко распространены, сульфадоксин/пириметамин больше не рекомендуют для профилактики из-за высокого риска побочных эффектов. Но при подозрении на приступ малярии, когда медицинская помощь недоступна, следует начать профилактику хлорохином и однократно принять терапевтическую дозу сульфадоксина/пириметамина. В то же время при приступах малярии, вызванной полирезистентными штаммами Plasmodium falciparum (например, в Юго-Восточной Азии) антагонисты фолиевой кислоты могут оказаться бесполезными. Случается, что не помогает и профилактика мефлохином или доксициклином — тогда не остается ничего, как бороться с приступами малярии, повторяя при необходимости курсы лечения (см. ниже). В тех немногих районах, где Plasmodium falciparum все еще чувствительны к хлорохину, этот препарат вполне годится для профилактики. Он же остается лучшим средством для лечения и профилактики малярии. вызванной Plasmodium vivax, Plasmodium ovale и Plasmodium malariae. Назначать примахин для искоренения Plasmodium vivax следует лишь после того, как больной покинет эндемический район.
Лечение приступов малярии, вызванной разными видами плазмодия, начинается одинаково, за исключением случаев, обусловленных устойчивыми штаммами Plasmodium falciparum. От вида зависит лишь дальнейшее лечение. Приступ малярии требует неотложной помощи, особенно у самых уязвимых групп населения: неиммунных лиц, беременных и детей младшего возраста. При подозрении на тропическую малярию (по сведениям о поездках и клинической картине) сразу же назначают быстродействующие гематошизотропные препараты. При этом не стоит дожидаться подтверждения диагноза, так как состояние таких бальных может ухудшаться очень быстро. К тому же картина заболевания может быть атипичной, а на ранних стадиях малярийные плазмодии в толстой капле обнаруживаются не всегда. Для лечения малярии, вызванной Plasmodium vivax, Plasmodium ovale, Plasmodium malariae и чувствительными к хлорохину штаммами Plasmodium falciparum, лучше всего подходит хлорохин. Назначают его, по возможности, внутрь, но при соблюдении соответствующих предосторожностей (см. выше) хлорохин можно вводить в/м и даже в/в. В течение 48—72 ч от начала лечения состояние больных должно значительно улучшиться, а уровень паразитемии (оценивают ежедневным исследованием толстой капли) — снизиться. Если этого не происходит либо паразитемия не исчезает в течение 7 сут, то, скорее всего, возбудитель устойчив к хлорохину. В подобном случае, а также в тех случаях, когда сведения о поездках позволяют предположить устойчивость Plasmodium falciparum к хлорохину, — препаратом выбора, несмотря на токсичность, становится хинин. При тропической малярии, вызванной полирезистентными плазмодиями, хинин назначают в сочетании с гематошизот-ропными препаратами медленного действия, например антагонистами фолиевой кислоты или тетрациклинами, — выбор конкретного препарата определяется многими факторами (см. выше и табл. 40.2). Опять же, хинин лучше всего назначать внутрь (хинина сульфат), но до тех пор, пока больной не сможет принимать пишу, препарат вводят в/в (хинина дигидрохлорид). Правда, во многих больницах США вместо хинина ди гидрохлорида применяют сейчас хинидина глюконат. При тяжелой тропической малярии с высоким уровнем паразитемии может потребоваться обменное переливание крови (Miller et al., 1989).
Приступы малярии могут возникать вновь во время и после курса лечения, даже в отсутствие повторного заражения. Рецидивы, вызванные Plasmodium vivax, Plasmodium ovale или Plasmodium malariae, обычно хорошо поддаются повторному курсу лечения хлорохином, причем в случае малярии, вызванной Plasmodium vivax или Plasmodium ovale, одновременно с хлорохином или после него назначают примахин. Иногда при малярии, вызванной Plasmodium vivax, для полного искоренения возбудителя приходится назначать повторный курс примахина. Рецидивы тропической малярии или паразитемия, сохраняющаяся после лечения хлорохином, обычно указывают на устойчи-вость возбудителя к хлорохину (с клинической классификацией лекарственной устойчивости можно ознакомиться по дополнительной литератур», см. World Health Organization, 1981). С устойчивостью Plasmodium falciparum к хлорохину удалось справиться назначением хинина в сочетании с противомалярийным препаратом медленного действия (например, доксициклином) в Юго-Восточной Азии или с антагонистом фолиевой кислоты (например, сульфадоксином/пириметамином) — в Африке (табл. 40.2); Но ценность таких схем снижается из-за высокого риска побочных эффектов при приеме хинина в течение 7 сут' тем более что растущая устойчивость Plasmodium falciparum требует все большего повышения дозы. К тому же больные часто не соблюдают предписания врачей. Там, где отсутствует устойчив вость к обоим препаратам, хинин можно заменить на мефлохин. Однако мефлохин нельзя вводить парентерально и нельзя принимать вместе с хинином. Кроме того, для полного искоренения паразита, который in vitro проявляет перекрестную устойчивость к хинину, могут потребоваться токсические дозы мефлохина. Что касается лечения тропической малярии, вызванной полирезистентными штаммами, — здесь большие надежды возлагают на производные артемизинина, которые еще проходят клинические испытания. Эти препараты действуют быстрее и сильнее других гематошизотропных средств, значительно снижают уровень паразитемии и отлично сочетаются с мефлохином или хлорпрогуанилом и одним из сульфонов. Устойчивость паразитов к этим относительно безопасным препаратам минимальна. По-видимому, это объясняется быстрым действием и очень коротким Т|/2 производных артемизинина (см. выше). Малярия, вызванная полирезистентными штаммами Plasmodium falciparum, с успехом лечится атоваквоном в сочетании с противомалярийным бигуанидом (прогуанилом или хлорпрогуанилом). Однако эти комбинации довольно дороги, и, вероятно, к ним также вскоре разовьется устойчивость — штаммы Plasmodium falciparum, устойчивые к каждому из препаратов в отдельности, существуют уже сейчас.
Малярия, особенно тропическая, представляет серьезную угрозу для детей и беременных. У детей применяют в целом те же схемы, что и у взрослых, лишь уменьшают дозы в соответствии с возрастом и принимают необходимые меры предосторожности. Однако назначение тетрацикпинов детям до 8 лет допустимо только по экстренным показаниям. Беременным по возможности лучше отказаться от поездки в эндемические районы. Если хлорохин, прогуанил и производные артемизинина признаны безопасными, то антагонисты фолиевой кислоты, тетрациклины и примахин беременным противопоказаны (см. выше и табл. 40.1 и 40.2).
Перспективы
На противомалярийные средства некогда возлагали большие надежды в плане борьбы с этим опасным и нередко смертельным заболеванием. Но будущее их представляется туманным, если дальнейшие исследования и разработка новых мощных препаратов не получат должного финансирования и не окажутся в руках умелых и грамотных специалистов. Существующие сегодня противомалярийные препараты повторяют историю других антимикробных средств — возникают и распространяются все более устойчивые штаммы Plasmodium falciparum, а эффективные ранее препараты, например хлорохин, быстро устаревают. Разработка же и выпуск новых препаратов, способных спасти жизнь многим больным (например, производных артемизинина), идет слишком медленно, не поспевая за растущими потребностями.
Тем не менее именно в последнее время в области патогенеза и лечения малярии сделаны важнейшие открытия. Так, найдены методы выделения из организма человека и животных и выращивания чувствительных и устойчивых клонов Plasmodium falciparum, что предоставило материал, необходимый для изучения биологических свойств и механизмов устойчивости плазмодия, а также для поиска молекулярных мишеней новых препаратов. Не за горами полная расшифровка генома Plasmodium falciparum. Вместе с достижениями в других областях науки это открытие, несомненно, послужит толчком к созданию новых противомалярийных средств.
Клинические испытания противомалярийных средств должны идти в ногу с разработкой новых препаратов. Рациональный подход к борьбе с малярией означает, что нужны активные исследования фармакодинамики и фармакокинетики, которые помогут разработать схемы лечения и выявить показания к применению противомалярийных препаратов у разных групп населения при заболеваниях, вызванных разными видами плазмодия.