Лечение тромбозов — различия между версиями
Dormiz (обсуждение | вклад) (Новая страница: «{{Шаблон:Наглядная фарма}} == Профилактика и лечение тромбозов == При повреждении сосуда а…») |
(нет различий)
|
Версия 22:33, 31 октября 2014
Источник: «Наглядная фармакология».
Автор: X. Люльман. Пер. с нем. Изд.: М.: Мир, 2008 г.
Содержание
Профилактика и лечение тромбозов
При повреждении сосуда активируется система свертывания крови, в результате чего из тромбоцитов и молекул фибрина образуется сгусток, закрывающий повреждение и останавливающий кровотечение. Патологии тромбообразования или тромбоз сосудов опасны для жизни: если тромб образуется на атеросклеротически измененной коронарной артерии, то может развиться инфаркт миокарда; при тромбозе глубоких вен нижних конечностей тромб может оторваться, попасть в легочную артерию с током крови и вызвать тромбоэмболию легочной артерии.
Для профилактики тромбозов применяют препараты, уменьшающие свертываемость крови, т. е. препятствующие агрегации тромбоцитов и действующие в основном на тромбообразование в артериях. Для лечения тромбозов используются средства, растворяющие фибриновую сеть: фибринолитики.
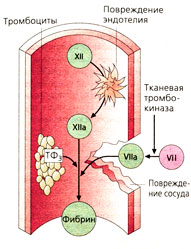
Каскад свертывания крови активируется двумя путями (А):
- Если внутри сосуда есть участок, не покрытый эндотелием, то фактор XII превращается в активированный фактор ХНа (внутренний путь).
- Под воздействием фосфолипопротеинов тканей (тромбокиназа, или тромбопластин) фактор VII превращается в VIla (внешний путь).
Оба пути приводят к одному и тому же заключительному этапу каскада свертывания с участием фактора X.
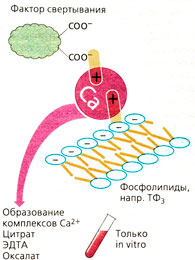
Факторами свертывания являются белковые молекулы. Для многих факторов «активация» означает отщепление белкового фрагмента и превращение их (кроме фибрина) в ферменты, расщепляющие белок (протеазы). Некоторым факторам необходимо также присутствие фосфолипидов (ФЛ) и ионов Са2+. Возможно, ионы Са2+ влияют на присоединение фактора свертывания к фосфолипиду (Б). Фосфолипиды входят в состав тромбоцитарного фактора 3 (ТФ3), который высвобождается из тромбоцитов, а также тромбопластина (А). Включение в каскад одного за другим множества ферментов направлено на то, чтобы количество продуктов вышеназванных реакций лавинообразно увеличивалось (на рис. В показано в виде увеличения количества частиц) и в конечном итоге приводило бы к массивному образованию фибрина.
Связывание кальция (Б) нарушает ферментативную активность Са-зависимых факторов. Связывать ионы Са2+ способны вещества, содержащие СОО~-группу. Цитрат и EDTA (этилендиаминтетрауксусная кислота) образуют с Са2+ растворимые комплексы, оксалат переходит в нерастворимый оксалат кальция. Комплексообразование с кальцием нельзя использовать в терапевтических целях, поскольку концентрация кальция резко снижается, что опасно для жизни (гипокальциемическая тетания). Эти соединения (например, в виде солей натрия) используются вне организма (in vitro) для предотвращения свертывания крови. Такой эффект можно сделать обратимым путем дополнительного введения Са2+-ионов.
На механизм свертывания крови in vivo можно воздействовать с помощью следующих препаратов (В):
1. Производные кумарина снижают концентрацию в крови неактивированных факторов II, VII, IX, X, блокируя их синтез в печени.
2. Комплекс гепарина с антитромбином III блокирует протеолитический эффект активированных факторов. В противоположность обычному гепарину низкомолекулярные гепариновые фрагменты, например обладающий минимальной гепариновой активностью фондапарин, в комплексе с антитромбином ингибируют только активированный фактор Ха.
3. Гирудин и его производные блокируют активный центр тромбина.
Витамин К и его антагонисты
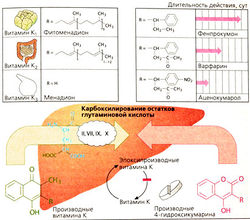
Витамин К способствует присоединению карбоксильных групп к остатку глутаминовой кислоты в печени при образовании факторов II, VII, IX, X; карбоксильные группы необходимы для Са2+-зависимого связывания с фосфолипидами. Существует несколько различных по происхождению производных витамина: витамин К {фитоменадион) образуется в клетках растений, витамин К2 продуцируется бактериями кишечника, витамин Кз (менадион) синтезирован химическим путем. Все виды витамина гидрофобны, и для их всасывания необходимы желчные кислоты.
Пероральные антикоагулянты
4-Гидроксикумарины имеют структурное сходство с витамином К и вступают в реакции в качестве «ложного» витамина К. Витамин К по реакции карбоксилирования превращается в эпоксид. Гидроксикумарины вступают в реакцию восстановления витамина К из эпоксидов и вызывают дефицит активной формы витамина К.
Кумарины хорошо всасываются при пероральном приеме. Длительность действия кумаринов очень сильно различается. Синтез факторов свертывания зависит от концентрации витамина К и кумаринов в печени. Для каждого пациента подбирается индивидуальная доза кумаринов (контроль с помощью международного нормализованного отношения INR, ранее применялся показатель QUICK).
Показания: профилактика тромбоэмболии, например при трепетании предсердий или у пациентов с искусственными клапанами сердца.
Наиболее опасный побочный эффект от использования пероральных антикоагулянтов — кровотечение. В этом случае в качестве естественного антидота назначают витамин К. Однако свертываемость крови при этом нормализуется не сразу, а в течение часов или дней, на протяжении которых в печени вновь восстанавливается синтез соответствующих факторов свертывания. При неотложных состояниях проводят заместительную терапию факторами свертывания, например переливание свежей крови или факторов крови (концентрат протромбина).
Другие побочные действия: геморрагический некроз кожи, выпадение волос; при назначении беременным у ребенка может происходить нарушение скелетообразования и повреждение ЦНС (вследствие кровоизлияний), а также существует опасность ретроплацентарного кровотечения.
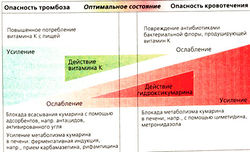
Взаимодействия
Назначение кумаринов подразумевает постоянное балансирование на грани между двумя опасностями: кровотечение и тромбоз. Даже при удачной дозировке можно не учесть внешние факторы. Если больной изменяет рацион питания и употребляет много зеленых овощей, то соотношение витамина К и антагонистов изменяется в пользу витамина К. Если на фоне антибактериальной терапии продукция витамина К в кишечнике снижается, то превалируют антагонисты витамина К. Лекарства, повышающие микросомальное окисление в печени, могут усилить выведение гидроксикумарина и понизить его концентрацию в крови. Блокаторы биотрансформации в печени (например, Н2-антигистаминный препарат циметидин) повышают активность кумаринов. Следует учитывать не только фармакокинетические, но и фармакодинамические взаимодействия. Например, при приеме антикоагулянтов противопоказана ацетилсалициловая кислота, так как, вопервых, она замедляет агрегацию тромбоцитов, во-вторых, повреждает слизистую желудка и может вызывать эрозию стенок сосудов.