Третичная и четвертичная структура белка — различия между версиями
Nico (обсуждение | вклад) (Новая страница: «== Третичная и четвертичная структура белка. Коллаген == Рис. 8.1. Третичная структура. β-Скл…») |
Django (обсуждение | вклад) |
||
| Строка 1: | Строка 1: | ||
| − | == Третичная | + | == Третичная структура белка == |
| − | |||
| − | |||
| − | |||
| − | |||
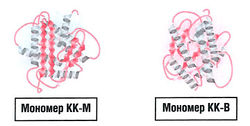
'''Третичная структура белка''' — это взаимное расположение в пространстве β-цепей, β-складчатых слоев и а-спиралей. Примеры различных способов укладки — мономеры креатинкиназы КК-М и КК-В (рис. 8.1). | '''Третичная структура белка''' — это взаимное расположение в пространстве β-цепей, β-складчатых слоев и а-спиралей. Примеры различных способов укладки — мономеры креатинкиназы КК-М и КК-В (рис. 8.1). | ||
| − | + | [[Image:Bio_wiki_8_1.jpg|250px|thumb|right|Рис. 8.1. Третичная структура. β-Складчатые слои и а-спирали сворачиваются в пространстве с образованием двух разных мономеров креатинкиназы (КК-М и КК-В)]] | |
=== Четвертичная структура белка === | === Четвертичная структура белка === | ||
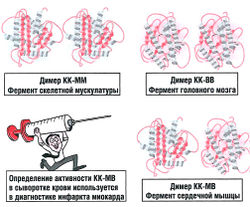
Многие белки состоят из нескольких полипептидных цепей, которые связаны нековалентными связями. '''Мономером''' называется один отдельный белок, состоящий из одной полипептидной цепи. Когда мы говорим о четвертичной структуре белка, это означает, что в его состав входят несколько мономеров: 2 мономера образуют димер (рис. 8.2), три — '''тример''', четыре — '''тетрамер''' и т.д. '''Олигомеры''' состоят из большого числа мономеров. | Многие белки состоят из нескольких полипептидных цепей, которые связаны нековалентными связями. '''Мономером''' называется один отдельный белок, состоящий из одной полипептидной цепи. Когда мы говорим о четвертичной структуре белка, это означает, что в его состав входят несколько мономеров: 2 мономера образуют димер (рис. 8.2), три — '''тример''', четыре — '''тетрамер''' и т.д. '''Олигомеры''' состоят из большого числа мономеров. | ||
| − | + | [[Image:Bio_wiki_8_2.jpg|250px|thumb|none|<small>Рис. 8.2. Четвертичная структура. Два разных мономера креатинкиназы — КК-М и КК-В — связываются с образованием трех вариантов димеров. Это гомодимер КК-ММ (фермент скелетной мускулатуры), гомодимер КК-ВВ (фермент головного мозга) и гетеродимер КК-МВ (характерен для ткани сердечной мышцы)</small>]] | |
=== Коллаген === | === Коллаген === | ||
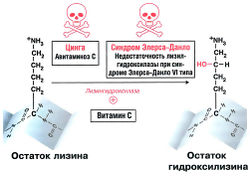
При кипячении соединительная ткань превращается в желатин, который можно использовать как клей. Отсюда и возникло название «[[коллаген]]» (по-гречески «kola» значит «клей»). На настоящий момент известно 19 разных типов коллагена. '''Коллагены''' — структурные белки соединительной ткани, самые многочисленные белки человеческого организма. Коллагены по-разному распределены в организме: так, коллаген I типа содержится главным образом в связках, сухожилиях и коже, а коллаген II типа — в хрящевой ткани. Структурные единицы коллагена — '''а-спирали''', которые скручиваются в '''тройную спираль'''. В первичной последовательности коллагена повторяется мотив '''-Гли-X-Y-'''. В этой последовательности X обычно представлен пролином. На месте Y чаще всего находится остаток пролина, гидроксилированный в витамин С-зависимой реакции: таким образом, Y представляет собой остаток '''гидроксипролина'''. В других случаях Y может быть представлен остатком '''гидроксилизина''' (рис 8.3). '''[[Глицин]]''' — необходимый компонент коллагена. Это самая маленькая аминокислота: ее радикал R представлен лишь одним атомом водорода. Пространство в тройной спирали ограничено, и другие, более крупные, молекулы аминокислот просто не могли бы там поместиться. | При кипячении соединительная ткань превращается в желатин, который можно использовать как клей. Отсюда и возникло название «[[коллаген]]» (по-гречески «kola» значит «клей»). На настоящий момент известно 19 разных типов коллагена. '''Коллагены''' — структурные белки соединительной ткани, самые многочисленные белки человеческого организма. Коллагены по-разному распределены в организме: так, коллаген I типа содержится главным образом в связках, сухожилиях и коже, а коллаген II типа — в хрящевой ткани. Структурные единицы коллагена — '''а-спирали''', которые скручиваются в '''тройную спираль'''. В первичной последовательности коллагена повторяется мотив '''-Гли-X-Y-'''. В этой последовательности X обычно представлен пролином. На месте Y чаще всего находится остаток пролина, гидроксилированный в витамин С-зависимой реакции: таким образом, Y представляет собой остаток '''гидроксипролина'''. В других случаях Y может быть представлен остатком '''гидроксилизина''' (рис 8.3). '''[[Глицин]]''' — необходимый компонент коллагена. Это самая маленькая аминокислота: ее радикал R представлен лишь одним атомом водорода. Пространство в тройной спирали ограничено, и другие, более крупные, молекулы аминокислот просто не могли бы там поместиться. | ||
| + | [[Image:Bio_wiki_8_3.jpg|250px|thumb|none|Рис. 8.3. Гидроксилирование остатков лизина при образовании коллагена]] | ||
==== Биосинтез коллагена ==== | ==== Биосинтез коллагена ==== | ||
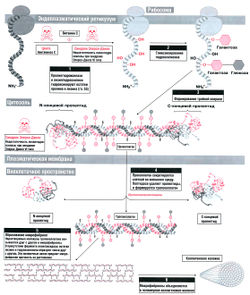
| − | + | [[Image:Bio_wiki_8_4.jpg|250px|thumb|right|Рис. 8.4. Биосинтез коллагена]] | |
Коллаген — нерастворимый гликопротеин внеклеточного матрикса. Каким же образом фибробласты — клетки, синтезирующие коллаген, образуют нерастворимый внеклеточный белок? Все дело в том, что синтез коллагена осуществляется в 2 '''стадии''': внутриклеточной и внеклеточной (рис. 8.4). | Коллаген — нерастворимый гликопротеин внеклеточного матрикса. Каким же образом фибробласты — клетки, синтезирующие коллаген, образуют нерастворимый внеклеточный белок? Все дело в том, что синтез коллагена осуществляется в 2 '''стадии''': внутриклеточной и внеклеточной (рис. 8.4). | ||
| Строка 25: | Строка 22: | ||
Проколлаген секретируется клеткой во внеклеточную жидкость. Фермент проколлагенпептидаза удаляет глобулярные пропептиды с N- и С-концевых участков молекул проколлагена, и образуется нерастворимый тропколлаген. Молекулы тропоколлагена объединяются в микрофибриллы, причем они располагаются в шахматном порядке так, что каждая молекула тропоколлагена перекрывается с соседними на четверть своей длины. Наконец, в присутствии лизиноксидазы остатки лизина и гидроксилизина реагируют друг с другом, формируя поперечные связи, что придает микрофибрилле прочность на растяжение, и микрофибриллы объединяются в одно полимерное коллагеновое волокно. | Проколлаген секретируется клеткой во внеклеточную жидкость. Фермент проколлагенпептидаза удаляет глобулярные пропептиды с N- и С-концевых участков молекул проколлагена, и образуется нерастворимый тропколлаген. Молекулы тропоколлагена объединяются в микрофибриллы, причем они располагаются в шахматном порядке так, что каждая молекула тропоколлагена перекрывается с соседними на четверть своей длины. Наконец, в присутствии лизиноксидазы остатки лизина и гидроксилизина реагируют друг с другом, формируя поперечные связи, что придает микрофибрилле прочность на растяжение, и микрофибриллы объединяются в одно полимерное коллагеновое волокно. | ||
| − | |||
| − | |||
== Читайте также == | == Читайте также == | ||
*[[Вторичная структура белка]] | *[[Вторичная структура белка]] | ||
Текущая версия на 21:39, 15 мая 2016
Содержание
Третичная структура белка[править | править код]
Третичная структура белка — это взаимное расположение в пространстве β-цепей, β-складчатых слоев и а-спиралей. Примеры различных способов укладки — мономеры креатинкиназы КК-М и КК-В (рис. 8.1).
Четвертичная структура белка[править | править код]
Многие белки состоят из нескольких полипептидных цепей, которые связаны нековалентными связями. Мономером называется один отдельный белок, состоящий из одной полипептидной цепи. Когда мы говорим о четвертичной структуре белка, это означает, что в его состав входят несколько мономеров: 2 мономера образуют димер (рис. 8.2), три — тример, четыре — тетрамер и т.д. Олигомеры состоят из большого числа мономеров.
Коллаген[править | править код]
При кипячении соединительная ткань превращается в желатин, который можно использовать как клей. Отсюда и возникло название «коллаген» (по-гречески «kola» значит «клей»). На настоящий момент известно 19 разных типов коллагена. Коллагены — структурные белки соединительной ткани, самые многочисленные белки человеческого организма. Коллагены по-разному распределены в организме: так, коллаген I типа содержится главным образом в связках, сухожилиях и коже, а коллаген II типа — в хрящевой ткани. Структурные единицы коллагена — а-спирали, которые скручиваются в тройную спираль. В первичной последовательности коллагена повторяется мотив -Гли-X-Y-. В этой последовательности X обычно представлен пролином. На месте Y чаще всего находится остаток пролина, гидроксилированный в витамин С-зависимой реакции: таким образом, Y представляет собой остаток гидроксипролина. В других случаях Y может быть представлен остатком гидроксилизина (рис 8.3). Глицин — необходимый компонент коллагена. Это самая маленькая аминокислота: ее радикал R представлен лишь одним атомом водорода. Пространство в тройной спирали ограничено, и другие, более крупные, молекулы аминокислот просто не могли бы там поместиться.
Биосинтез коллагена[править | править код]
Коллаген — нерастворимый гликопротеин внеклеточного матрикса. Каким же образом фибробласты — клетки, синтезирующие коллаген, образуют нерастворимый внеклеточный белок? Все дело в том, что синтез коллагена осуществляется в 2 стадии: внутриклеточной и внеклеточной (рис. 8.4).
На внутриклеточной стадии происходит синтез проколлагена
Сначала внутриклеточный белковый аппарат синтезирует полипептидные а-спирали (длиной примерно в 1000 аминокислот). Некоторые из остатков пролина и лизина гидроксилируются в ходе реакций, для которых необходим витамин С. Некоторые остатки гидроксилизина гликозилируются. Потом а-спирали объединяются, сплетаясь друг с другом, и образуют тройную спираль проколлагена, который является растворимым белком.
На внеклеточной стадии формируются коллагеновые волокна
Проколлаген секретируется клеткой во внеклеточную жидкость. Фермент проколлагенпептидаза удаляет глобулярные пропептиды с N- и С-концевых участков молекул проколлагена, и образуется нерастворимый тропколлаген. Молекулы тропоколлагена объединяются в микрофибриллы, причем они располагаются в шахматном порядке так, что каждая молекула тропоколлагена перекрывается с соседними на четверть своей длины. Наконец, в присутствии лизиноксидазы остатки лизина и гидроксилизина реагируют друг с другом, формируя поперечные связи, что придает микрофибрилле прочность на растяжение, и микрофибриллы объединяются в одно полимерное коллагеновое волокно.