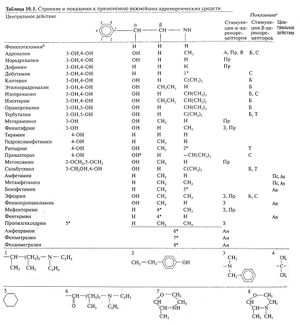
Бета-адреностимуляторы
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Бета-адреностимуляторы
Препараты этой группы использовали при многих состояниях, но сегодня их основное применение — устранение бронхоспазма у больных с бронхиальной астмой и ХОЗЛ.
Адреналин стали впервые использовать в качестве бронходилататора в начале XX века. Эфедрин вошел в западную медицину в 1924 г., хотя в Китае он применялся до этого в течение нескольких тысяч лет (Chen and Schmidt, 1930). Следующим крупным шагом стала разработка в 1940-х гг. избирательного β-адреностимулятора изопреналина: появилась возможность применять при бронхиальной астме лекарственное средство, не обладающее а-адреностимулирущей активностью и соответствующими побочными эффектами. Наконец, были получены избирательные β2-адреностимуляторы — еще более ценные в терапевтическом отношении препараты. К их достоинствам относится высокая биодоступность при приеме внутрь, отсутствие а-адреностимулирущей активности и низкий риск побочных эффектов на сердечно-сосудистую систему.
Бета-адреностимуляторы применяют для повышения частоты и силы сердечных сокращений. Их хронотропное действие важно для экстренного купирования таких аритмий, как пируэтная тахикардия, резкая брадикардия и АВ-блокада (гл. 35), а инотропное — в ситуациях, когда важно повысить сократимость сердца. Клиническое применение препаратов этой группы рассматривается ниже.
Изопреналин
Этот препарат (табл. 10.1) представляет собой мощный неизбирательный β-адреностимулятор с очень низким сродством к а-адренорецепторам.
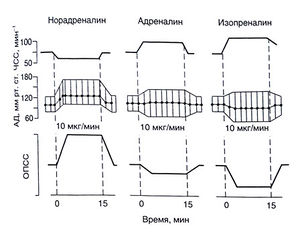
Фармакологические свойства. На рис. 10.2 приведены изменения некоторых показателей гемодинамики, возникающие у человека в ответ на в/в инфузию изопреналина. ОПСС снижается, прежде всего за счет расширения мышечных сосудов, но также — почечных и брыжеечных сосудов. Диастолическое АД уменьшается, систолическое может оставаться прежним или повышаться, среднее — обычно снижается. Сердечный выброс повышается в связи с положительным инотропным и хронотропным эффектом изопреналина, с одной стороны, и со снижением посленагрузки — с другой. При введении изопреналина возможны сердцебиение, синусовая тахикардия и аритмии. У животных высокие дозы изопреналина вызывают некроз миокарда.
Изопреналин вызывает расслабление почти всех гладких мышц (особенно если они находятся в состоянии высокого тонуса), однако наиболее выражено его действие на бронхи и ЖКТ. Он предупреждает или устраняет бронхоспазм; кроме того, его эффект при бронхиальной астме может быть обусловлен и подавлением вызванного антигенами высвобождения гистамина и других медиаторов воспаления. Такое действие свойственно и избирательным β2-адреностимуляторам.
Фармакокинетика. Изопреналин легко всасывается при приеме внутрь или ингаляции в виде аэрозоля. Он инактивируется КОМТ — прежде всего в печени, но также и в других тканях. МАО на него действует слабо, а симпатическими нейронами он не захватывается в такой степени, как адреналин и норадреналин. В связи со всеми этими особенностями длительность действия изопреналина несколько больше, чем адреналина, но все равно невелика.
Побочные эффекты. Часто наблюдаются сердцебиение, тахикардия, головная боль, приливы. Возможны нарушения ритма сердца, особенно у больных ИБС.
Применение. Изопреналин применяют при экстренных состояниях для повышения ЧСС у больных с резкой брадикардию или полной АВ-блокадой — особенно как временную меру це ред установкой электрокардиостимулятора или при пируэтной тахикардии. При бронхиальной астме и шоке вместо изопреналина в настоящее время используют другие препараты (гл. 28)
Добутамин
По химической структуре добутамин сходен с дофамином, однако у него имеется крупный ароматический радикал при аминогруппе (табл. 10.1). Физиологические эффекты добутамина обусловлены его прямым действием на а- и β-адренорецепторы, а не повышением высвобождения норадреналина из симпатических окончаний и не влиянием на дофаминовые рецепторы. Вначале считали, что добутамин — это сравнительно избирательный β1-адреностимулятор, однако теперь доказано, что механизмы его действия сложнее. У молекулы добутамина имеется хиральный центр, и поэтому существуют его оптические изомеры. Используемый в клинике препарат представляет собой рацемическую смесь из лево- и правовращающего изомеров (Ruffolo et al., 1981): /-добутамин — мощный а1-адреностимулятор, способный вызвать резкое повышение АД (Ruffolo and Yaden, 1983V напротив, d-добутамин — мощный а1-адреноблокатор подавляющий реакцию на /-добутамин. Таким образом конечная реакция на добутамин обусловлена влиянием обоих изомеров на β-адренорецепторы; d-добутамин примерно в 10 раз более активный бета-адреностимулятор,чем /-добутамин. Бета-адреноблокирующей активностью,видимо, не обладает ни один из изомеров.
Фармакологические свойства. Сердечно-сосудистая система. Как уже говорилось, применяемый в клинике добутамин — это рацемическая смесь, и поэтому его влияния на сердечно-сосудистую систему складываются из эффектов обоих изомеров. В отличие от изопреналина, добутамин обладает более выраженным инотропным, чем хронотропным действием. Причина этого не известна. Возможно, дело в том, что ОПСС под действием добутамина не изменяется; не исключено также, что в инотропном эффекте добутамина участвуют а1-адренорецепторы. В дозах, оказывающих одинаковый инотропный эффект, добутамин меньше влияет на частоту разрядов синусового узла, чем изопреналин. На АВ- и внугри-желудочковое проведение оба препарата действуют одинаково.
Инфузия животным добутамина со скоростью 2,5— 15 мкг/кг/мин приводит к повышению сократимости миокарда и сердечного выброса. ОПСС меняется маловидимо, из-за того, что обусловленное а1-адренорецеп-торами сужение сосудов компенсируется опосредованным β2-адренорецепторами расширением (Ruffolo, 1987), При скоростях инфузии меньше 20 мкг/мг/мин ЧСС возрастает незначительно. Инфузия добутамина на фоне β-адреноблокаторов не вызывает повышения сердечного выброса, но приводит к росту ОПСС. Это еще раз подтверждает, что добутамин оказывает некоторое стимулирующее влияние на сосудистые а-адренорецепторы.
Побочные эффекты. У некоторых больных добутамин вызывает резкое повышение АД и ЧСС, требующее снижения скорости инфузии. Вероятность повышения АД выше у больных с артериальной гипертонией в анамнезе. Поскольку добутамин улучшает АВ-проведение, при мерцательной аритмии он может привести к чрезмерному повышению частоты сокращений желудочков. Для профилактики этого осложнения назначают, например, дигоксин. Иногда добутамин вызывает желудочковые экстрасистолы. Как и другие инотропные средства, он может привести к увеличению зоны инфаркта из-за повышения потребности миокарда в кислороде; это всегда надо учитывать при принятии решения о назначении добутамина. Не известно, насколько эффективно применять добутамин на протяжении более нескольких суток. Есть данные о развитии к нему устойчивости (Unverferth et al., 1980).
Показания и применение. Добутамин применяют коротким курсом при декомпенсированной сердечной недостаточности I после операций на сердце, на фоне тяжелой хронической сердечной недостаточности, при инфаркте миокарда. В таких случаях он повышает ударный объем и сердечный выброс, как правило, без выраженного увеличения ЧСС и существенных изменений АД и ОПСС (впрочем, как уже говорилось, у некоторых больных возможен резкий подъем ЧСС и АД). Данных о его влиянии на долгосрочный прогноз мало. При ИБС по строгим показаниям применяют добутаминовую стресс-ЭхоКГ (Madu et al. 1994): вызванная добутамином повышенная нагрузка на миокард позволяет выявить очаги нарушений.
Т1/2 добутамина составляет примерно 2 мин. Основные пути метаболизма — конъюгация и превращение в З-О-метилдобутамин. Эффект развивается быстро, поэтому насыщающая доза не нужна, а стационарная концентрация достигается через 10 мин после начала инфузии. Для повышения сердечного выброса обычно проводят инфузию со скоростью 2,5—10 мкг/кг/мин, хотя иногда требуется и большая скорость. В целом скорость и длительность инфузии индивидуальны и зависят от клинического состояния и параметров гемодинамики.
Бета2-адреностимуляторы
Некоторые из основных побочных эффектов, возникающих при назначении β-адреностимуляторов больным бронхиальной астмой, обусловлены стимуляцией β1-ад-ренорецепторов сердца. В связи с этим были разработаны препараты, действующие преимущественно на β2-адренорецепторы. Однако избирательность их не абсолютна, и в высоких дозах они действуют на оба подтипа β-адренорецепторов.
Еще один подход к повышению эффективности β2-адреностимуляторов при бронхиальной астме — это получение препаратов с меньшей скоростью метаболизма и большей биодоступностью при приеме внутрь (по сравнению с катехоламинами). Это достигается путем гидроксилирования в положениях 3 и 5 бензольного кольца или замены гидроксильной группы в положении 3 на иную группу. Так были получены орципреналин, сальбутамол и тербуталин. Все эти препараты не инактивируются КОМТ. Замены на крупные радикалы в аминогруппе катехоламинов приводят к повышению активности в отношении β-адренорецепторов, снижению активности в отношении а-адренорецепторов и уменьшению чувствительности к МАО (Nelson, 1982).
Наконец, для преимущественной стимуляции β2-адренорецепторов бронхов используют ингаляцию малых доз упомянутых препаратов в аэрозолях. Обычно это приводит к выраженному действию на данные рецепторы при очень низких сывороточных концентрациях препаратов (Newhouse and Dolovich, 1986). При этом в меньшей степени стимулируются β1-адренорецепторы сердца и β2-адренорецепторы скелетных мышц (активация последних приводит к тремору, что ограничивает прием препаратов внутрь).
Ингаляция β-адреностимуляторов обычно дает очень быстрый (в течение минут) эффект. Есть и препараты с замедленным действием, например сальметерол. При п/к введении бета-адреностимуляторов расширение бронхов также наступает быстро, но при приеме внутрь максимальный эффект может быть достигнут лишь через несколько часов. Действие ингалируемых препаратов зависит от попадания их в дистальные отделы дыхательных путей — что, в свою очередь, определяется размерами частиц и параметрами дыхания (скоростью воздушного потока на вдохе, дыхательным объемом, временем задержки дыхания, сопротивлением дыхательных путей и др.; Newhouse and Dolovich, 1986). Лишь 10% ингалируемых препаратов попадает в легкие, остальная часть заглатывается и затем всасывается из ЖКТ. Для эффективности ингаляционной терапии необходимо, чтобы больной был обучен правильно ее проводить. Многие же больные, особенно старики и дети, этого не умеют — часто из-за того, что недостаточное внимание уделяют их обучению (Kelly, 1985; Newhouse and Dolovich, 1986). В таких случаях могут помочь буферные насадки (гл. 28).
Считается, что основной механизм действия β-адреностимуляторов при бронхиальной астме — это активация бета-адренорецепторов бронхов, бронходилатация и снижение сопротивления дыхательных путей. Однако есть данные о том, что бета-адреностимуляторы подавляют также высвобождение лейкотриенов и гистамина из тучных клеток легких (Hughes et al., 1983), усиливают восходящий ток слизи, снижают проницаемость сосудов микроциркуляторного русла и, возможно, ингибируют фосфолипазу Ц (Seale, 1988). Вклад всех этих механизмов в терапевтический эффект p-адреностимуляторов уточняется, но уже сейчас ясно, что воспаление бронхов играет роль в их повышенной реактивности (гл. 28). Значит, важную роль в лечении бронхиальной астмы могут играть противовоспалительные средства (например, ингаляции глюкокортикоидов). Применение β-адреностимуляторов при этом заболевании подробнее рассматривается в гл. 28.
Орципреналин. Орципреналин, тербуталин, фенотерол — это резорцинолы, имеющие гидроксильные группы в положениях 3 и 5 бензольного кольца (катехолы — в положениях 3 и 4; см. табл. 10.1). Поэтому они устойчивы к КОМТ, и их биодоступность при приеме внутрь достаточно высока — 40%. Элиминация происходит путем конъюгирования с глюкуроновой кислотой и последующим выведением почками. Орципреналин считается избирательным β2-адреностимулятором, хотя эта избирательность у него, видимо, меньше, чем у сальбутамола и тербуталина. Эффект развивается через несколько минут и длится несколько часов после ингаляции. После приема внутрь эффект развивается медленнее, а длится 3—4 ч. Орципреналин используют при приступах бронхиальной астмы и для длительного лечения при ХОЗЛ (гл. 28).
Тербуталин. Это избирательный β2-адреностимулятор, используемый в качестве бронходилататора. Будучи производным резорцинола, он устойчив к КОМТ и поэтому эффективен при введении не только п/к и путем ингаляции, но и внутрь. После ингаляции или парентерального введения эффект развивается быстро; он длится в течение 3—6 ч после ингаляции. При приеме внутрь эффект может наступить лишь через 1—2 ч. Тербуталин используют при приступах бронхиальной астмы и для длительного лечения при ХОЗЛ. Препараты тербуталина для парентерального введения применяют в экстренных ситуациях при астматическом статусе (гл. 28).
Сальбутамол. Это также избирательный β2-адреностимулятор, по фармакологическим свойствам и показаниям сходный с тербуталином. Его вводят путем ингаляции или внутрь. При ингаляции он в пределах 15 мин вызывает значительное расширение бронхов, и его эффект длится 3—4 ч. Сальбутамол значительно меньше влияет на сердечно-сосудистую систему, чем изопреналин (при ингаляции в дозах, вызывающих одинаковое расширение бронхов).
Изоэтарин. Эго первый из бета2-адреностимуляторов, который начали широко применять при обструктивных заболеваниях легких. В то же время его избирательность меньше, чем более современных средств, и он, будучи катехоламином (табл. 10.1), метаболизируется КОМТ (хотя и устойчив к МАО). Поэтому его назначают только в ингаляциях для купирования острого бронхоспазма.
Пирбугерол. Это относительно избирательный β2-адреностимулятор, отличающийся отсальбутамола только заменой бензольного кольца на пиридиновое (Richards and Brogden, 1985). Его назначают в ингаляциях, обычно каждые 4—6 ч.
Битолтерол. Это новый β2-адреностимулятор, у которого катехоловые гидроксильные группы защищены от действия КОМТ путем этерификации с 4-метилбензоатом. Эстеразы легких и других тканей гидролизуют его до активной формы (колтерола, или тербутилнорадреналина; табл. 10.1). На животных показано, что в легких активность таких эстераз выше, чем в других тканях, например в сердце (Nelson, 1986; Friedel and Brogden, 1988). Длительность эффекта битолтерола после ингаляции составляет 3—6 ч.
Фенотерол. Эффект этого β2-адреностимулятора развивается после ингаляции быстро и длится 4—6 ч. В США он не выпускается. Данные о возможной связи приема фенотерола с повышенной смертностью от бронхиальной астмы, полученные в Новой Зеландии, противоречивы (Pearce et al., 1995; Suissa and Ernst, 1997).
Формотерол. Это препарат длительного действия: через несколько минут после ингаляции он вызывает выраженное расширение бронхов, сохраняющееся до 12 ч (Faulds et al., 1991). В этом его главное преимущество перед другими бета2 - адреностимуляторами — особенно при ночных приступах бронхиальной астмы. В США он не выпускается.
Прокатерол. Эффект этого β2-адреностимулятора развивается после ингаляции быстро и длится около 5 ч. В США он не выпускается.
Сальметерол. Это препарат длительного (около 12 ч) действия. Однако эффект его после ингаляции развивается сравнительно медленно, и поэтому для быстрого купирования приступов бронхиальной астмы он не подходит (Lotvall and Svedmyr, 1993; Brogden and Faulds, 1991).
Ритодрии. Этот избирательный β-адреностимулятор был разработан как средство для расслабления мускулатуры матки, однако по своим фармакологическим свойствам он во многом сходен с другими препаратами данной группы. При приеме внутрь он всасывается быстро, хотя и недостаточно полно (на 30%), и на 90% выводится с мочой в виде неактивных конъюгатов. При в/в введении 50% препарата выводится с мочой в неизмененном виде. Фармакокинетика его сложна и изучена недостаточно, особенно у беременных.
Применение. Ритодрин и некоторые другие β2-адреностимуляторы вводят в/в по строгим показаниям при угрозе преждевременных родов (King et al., 1988). Однако существенного снижения перинатальной смертности при их применении не выявлено, а материнская смертность может даже возрастать (The Canadian Preterm Labor Investigators Group, 1992; Higby et al., 1993; Johnson, 1993). Впрочем, учитывая современные достижения в ведении недоношенных детей, можно полагать, что имеющиеся статистические методы недостаточно чувствительны для того, чтобы выявить небольшие, но все же важные положительные эффекты. При угрозе преждевременных родов применяют и некоторые другие средства (Bossmar, 1998; Norwitz et al., 1999), например препараты магния. Есть данные о токолитическом действии индометацина, однако для него пока не установлено соотношение пользы и риска (Panter et al., 1999). Такое действие оказывают и антагонисты кальция, но их влияние на долгосрочный прогноз также не выяснено (Carret al., 1999; гл. 32). Побочные эффекты β2-адреностимуляторов. Основные из этих эффектов связаны с чрезмерной активацией β-адренорецепторов. Особенно велик их риск при сердечно-сосудистых заболеваниях, но его можно снизить путем назначения препаратов в виде ингаляций.
Сравнительно частый побочный эффект бета2-адреностимуляторов — тремор. Со временем он обычно уменьшается (то есть развивается привыкание); пока не известно, связано ли это с десенситизацией бета2-адреноре-цепторов скелетных мышц или с адаптацией на уровне ЦНС. Тремор можно облегчить, начиная прием препаратов внутрь с малых доз и постепенно увеличивая их по мере развития привыкания. Бета2-адреностимуляторы, особенно при приеме внутрь или парентеральном введении, могут вызвать тревожность и беспокойство, что ограничивает их применение.
Частый побочный эффект при системном введении β2-адреностимуляторов — тахикардия. В то же время известно, что положительный хронотропный эффект катехоламинов опосредован активацией β1-адренорецепторов, и поэтому механизм вызываемой β2-адреностимуляторами тахикардии пока не ясен. Возможно, активация сердечных β2-адренорецепторов тоже может приводить к повышению ЧСС. Не исключено также, что тахикардия обусловлена рефлексами, возникающими в ответ на опосредованное β2-адренорецепторами снижение ОПСС. При тяжелом приступе бронхиальной астмы β2-адреностимуляторы могут, напротив, вызвать снижение ЧСС -предположительно благодаря улучшению показателей дыхания и, как следствие, снижению симпатических тонических влияний на сердце. У больных без заболеваний сердца β2-адреностимуляторы редко вызывают аритмию или ишемию миокарда, однако риск этих осложнений гораздо выше у больных ИБС или с уже имеющейся аритмией. Кроме того, вероятность сердечно-сосудистых осложнений повышена у принимающих ингибиторы МАО.
При начале лечения β2-адреностимуляторами приступа бронхиальной астмы возможно снижение Ра02. Оно может быть обусловлено вызванным этими препаратами расширением сосудов легких, приводящим к еще большему нарушению вентиляционно-перфузионного отношения. Обычно этот эффект выражен незначительно и вскоре проходит, но при необходимости можно назначить ингаляцию кислорода. У женщин, получающих ритодрин или тербуталин в связи с угрозой преждевременных родов, описан тяжелый отек легких.
Данные ряда эпидемиологических исследований свидетельствуют о возможной связи между длительный приемом β-адреностимуляторов и риском смерти или критических состояний при бронхиальной астме (Suissa et al., 1994). Делать из этих исследований однозначные выводы трудно, однако вопрос о постоянном приеме β2-адреностимуляторов при бронхиальной астме явно не прост. Известно и хорошо изучено, как in vivo, так и in vitro, привыкание к адренергическим средствам (гл. 6). Длительное системное применение β-адреностимуляторов во многих органах сопровождается снижением плотности β-адренорецепторов, а следовательно, и уменьшением реакций на данные препараты. Впрочем, у большинства больных бронхиальной астмой такое привыкание не приводит к снижению терапевтического эффекта — если, конечно, они не используют чрезмерно высокие дозы β-адреностимуляторов в течение длительного времени (Jenne, 1982; Tattersfield, 1985).
Есть данные о том, что постоянное употребление β2-адреностимуляторов может еще больше повышать реактивность бронхов, тем самым затрудняя лечение бронхиальной астмы (Lipworth and McDevitt, 1992; Hancox et al., 1999). He известно, повышается ли риск такого осложнения при использовании препаратов длительного действия или высоких доз (Beasley et al., 1999). Как бы то ни было, при решении вопроса о назначении β2-адреностимуляторов на длительный срок необходимо подумать о дополнительной или иной терапии (например, об ингаляциях глюкокортикоидов).
У животных высокие дозы β-адреностимуляторов вызывают некроз миокарда. Их парентеральное введение может также приводить к повышению концентраций в плазме глюкозы, молочной кислоты и свободных жирных кислот и к понижению концентрации К+. Последний эффект очень важен при заболеваниях сердца, особенно у принимающих сердечные гликозиды и диуретики. При сахарном диабете β-адреностимуляторы могут усугублять гипергликемию, и порой бывает необходимым повышать дозу инсулина. Риск всех этих побочных эффектов гораздо ниже при ингаляциях, чем при парентеральном введении или приеме внутрь.