Центральная нервная система
Содержание
- 1 Центральная нервная система
- 2 Получение и обработка стимулов
- 3 Сенсорные функции кожи
- 4 Проприоцепция, рефлекс растяжения
- 5 Ноцицепция и боль
- 6 Полисинаптические рефлексы
- 7 Проведение сенсорного импульса в ЦНС
- 8 Движение
- 9 Функции базальных ганглиев
- 10 Функции мозжечка
- 11 Двигательный контроль осанки
- 12 Гипоталамус, лимбическая система
- 13 Кора головного мозга, электроэнцефалограмма (ЭЭГ)
- 14 Цикл сна-бодрствования, циркадные ритмы
- 15 Сознание. Сон
- 16 Обучение, память, язык
- 17 Глия
- 18 Читайте также
Центральная нервная система
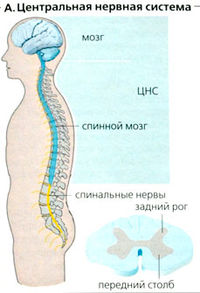
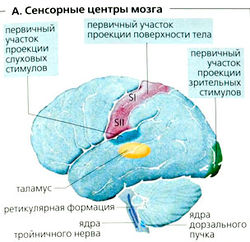
Центральную нервную систему составляют головной и спинной мозг (ЦНС) (рис. А). Спинной мозг делится на сегменты, но он на 30% короче позвоночника. Спинальные нервы выходят из позвоночного канала на уровне соответствующего позвонка и содержат афферентные соматические и висцеральные волокна дорзальных (задних) корешков, которые проецируются на спинной мозг, и эфферентные соматические (и частично вегетативные) волокна передних корешков, которые проецируются на периферию. Таким образом, нерв представляет собой пучок нервных волокон, которые имеют различные функции и проводят импульсы в разных направлениях.
Спинной мозг (А). У спинного мозга в сечении имеется темный внутренний участок в форме бабочки (серое вещество), окруженный более светлым участком (белое вещество). Четыре крыла серого вещества называются рогами (в поперечном сечении) или столбами (в продольном сечении). Передний рог содержит мотонейроны (проецируются на мышцы), а задний рог содержит интернейроны. Клеточные тела большинства афферентных волокон лежат внутри спинальных ганглиев вне спинного мозга. Белое вещество содержит аксоны восходящих и нисходящих путей (трактов).
Головной мозг (Г). Главные области: продолговатый мозг (Г7), варолиев мост (Гб), средний мозг (Г5), мозжечок (Д), промежуточный мозг и конечный мозг (Е). Продолговатый мозг, варолиев мост и средний мозг вместе называются стволом мозга. Структурно ствол мозга аналогичен спинному мозгу, но содержит также клеточные тела (ядра) черепных нервов - нейронов, контролирующих дыхание и кровоток и т. д. Мозжечок является важным центром контроля двигательных функций. Варолиев мост и мозжечок составляют метэнцефалон (задний мозг).
Промежуточный мозг. Таламус (ВБ) промежуточного мозга действует как передающее устройство для большинства чувствительных (афферентных) нервов, например от глаз, ушей и кожи, а также от других частей мозга. Гипоталамус (В9) - это высший вегетативный центр, он также играет доминантную роль в работе эндокринных желез, поскольку контролирует высвобождение гормонов из близлежащего гипофиза (ГА).
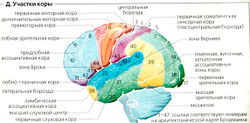
Конечный мозг состоит из коры и ядер, важных для двигательных функций, базальных ганглиев, т. е. хвостатого ядра (В5), скорлупы (В7), бледного шара (В8) и частей миндалевидного тела (В10). Миндалевидное тело и краевая извилина (Г2) относятся к лимбической системе. Кора головного мозга состоит из четырех долей, разделенных щелями (бороздами) - центральной бороздой (И, Д) и латеральной бороздой (ВЗ, Д). Согласно карте Бродманна кора головного мозга делится на гистологически различные участки (Д, курсив), которые имеют разные функции (Д). Полушария мозга тесно соединены нервными волокнами мозолистого тела (В1, ВЗ).
Спинномозговая жидкость
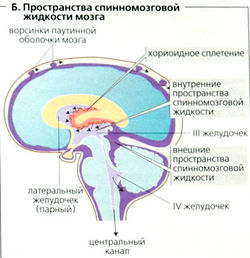
Мозг окружен внешними и внутренними пространствами, заполненными спинномозговой жидкостью (СМЖ) (Б). Внутренние пространства спинномозговой жидкости называются желудочками. Два боковых желудочка I и II (Б, В2) соединены с желудочками III и IV и с главным каналом спинного мозга (Б). Примерно 650 мл СМЖ каждый день образуется в хориоидном сплетении (Б, В4) и просачивается через паутинную оболочку мозга (Б). Барьер проницаемости между кровью и спинномозговой жидкостью, между кровью и мозгом (гематоэнцефалический барьер) предотвращает прохождение большинства веществ, кроме СО2, О2. воды и липофильных соединений. (Исключением являются циркумвентрикулярные органы мозга, такие как сосудистая сеть терминальной пластинки (OVLT) и самое заднее поле ромбовидной ямки, обладающие менее плотными гематоэнцефалическими барьерами.) Некоторые вещества, такие как глюкоза и аминокислоты, могут проходить гематоэнцефалический барьер при помощи переносчиков, тогда как белки - нет. Способность или неспособность лекарства пересекать гематоэнцефалический барьер является важным фактором фармакотерапии.
Повреждения, затрудняющие отток СМЖ (например, опухоли), приводят к компрессии мозга; у детей это приводит к аккумуляции жидкости (гидроцефалия, водянка головного мозга).
Получение и обработка стимулов
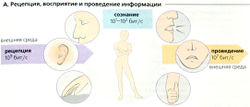
Из окружающего мира мы получаем при помощи органов чувств огромное количество информации (109 бит/с). Лишь незначительная часть этой информации (10—100 бит/с) воспринимается сознательно; а остальная либо обрабатывается подсознанием, либо не воспринимается вовсе. В то же время мы передаем в среду примерно 107 бит/с информации посредством речи и двигательной активности, особенно через выражение лица (А).
Бит (двоичный знак) - единица информации (1 байт = 8 бит). В среднем страница книги содержит примерно 1000 бит, а телевизионное изображение — более 106 бит/с.
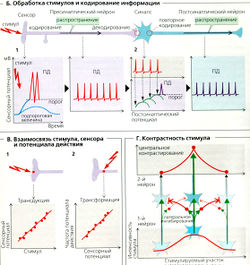
Стимулы достигают тела в виде различных форм энергии, например в виде электромагнитной (зрительные стимулы) или механической (тактильные стимулы). Разнообразные сенсорные рецепторы (сенсоры этих стимулов) локализованы в пяти «классических» органах чувств (глаза, уши, кожа, язык, нос) как на поверхности тела, так и внутри тела (например, проприорецепторы, вестибулярный орган). (В этой книге сенсорные рецепторы иногда называются сенсорами, чтобы отличить их от центров связывания гормонов и медиаторов.) Сенсорная система получает сигнал, имеющий четыре элемента стимуляции: модальность, интенсивность, продолжительность и локализацию. Каждый тип сенсора является специфичным для уникального раздражителя, вызывающего определенные сенсорные модальности, такие как образ, звук, тактильное ощущение, вибрация, температура, боль, вкус, запах, а также положение тела и его движения и т. д. Каждая модальность имеет несколько субмодальностей, например вкус может быть сладким или горьким, и т. д.
Во вторичных сенсорах (например, во вкусовых и слуховых рецепторах) сенсор и афферентные волокна разделены синапсом, тогда как первичные сенсоры (например, обонятельные и болевые) имеют свои собственные афферентные волокна.
Стимул индуцирует изменение сенсорного потенциала (трансдукция), что приводит к деполяризации сенсорных клеток (большинства типов; Б1), или гиперполяризацию, как в сетчатке. Чем сильнее стимул, тем больше амплитуда сенсорного потенциала (В1). Как только сенсорный потенциал превышает некоторый порог, он преобразуется в потенциал действия, ПД (Б1, с. 52 и ел ).
Кодирование сигнала. Стимул кодируется частотой потенциала действия (импульс/с = Гц), т. е. сенсорный потенциал тем выше, чем выше частота потенциала действия (ПД) (В2). Информация декодируется в следующем синапсе: чем выше частота приходящего ПД, тем выше возбуждающий постсинаптический потенциал (ВПСП). Новый ПД создается постсинаптическим нейроном в тот момент, когда ВПСП превышает некоторый пороговый уровень (Б2).
Кодирование частоты ПД служит более надежным способом передачи информации на большие дистанции, чем кодирование амплитуды, поскольку амплитуда более чувствительна и подвержена более сильным изменениям, что может исказить передаваемую сигналом информацию. В синапсе, однако, сигнал должен быть либо усилен, либо ослаблен (другими нейронами), что легче достигается путем кодирования амплитуды.
Адаптация. При постоянной стимуляции большинство сенсоров «привыкает» к стимулу (адаптируется), т. е. их потенциал понижается. Потенциал медленно адаптирующихся сенсоров становится пропорциональным интенсивности стимула (Р-сенсоры, или тонические сенсоры). Быстро адаптирующиеся сенсоры отвечают только на начало и конец стимула. Они ощущают дифференциальные изменения интенсивности стимула D-сенсоры, или фазические сенсоры). У PD-сенсоров проявляется и то, и другое.
Обработка в ЦНС. В первую очередь, ингибиторные и возбуждающие импульсы, проводимые в ЦНС, интегрируются, например, с тем чтобы увеличить контрастность стимула (Г. В этом случае возбуждающие импульсы от близлежащего сенсора ослабляются (латеральное ингибирование). На втором этапе сенсорное ощущение от стимула (например, «зеленый» или «сладкий») принимается низкоуровневыми сенсорными участками коры головного мозга. Это начальный этап субъективной физиологии чувств. Сознание является предпосылкой для данного процесса. За ощущением следует его интерпретация. Результат интерпретации называется восприятием; последнее основано на опыте и рассуждениях, причем интерпретация индивидуальна. Ощущение «зеленый», например, может вызвать восприятие: «Это дерево» или «Это луг».
Абсолютный порог, пороговая разница, пространственная и временная суммация, пределы чувствительности, обучаемость и возбуждение - все это другие важные понятия физиологии чувств. Два последних механизма играют важную роль в процессе обучения.
Сенсорные функции кожи
Соматовисцеральная чувствительность - это общий термин для всех типов сенсорной информации от рецепторов, или сенсоров тела (в противоположность сенсорным органам головы), включающий в себя проприорецепторы, болевые рецепторы, а также кожную, или поверхностную, чувствительность.
Тактильные ощущения необходимы для восприятия формы, очертаний и пространственных свойств объектов (стереогностика). Тактильные рецепторы расположены преимущественно на ладонях, в особенности на кончиках пальцев, а также на языке и в ротовой полости. Стереогностическое восприятие объекта требует интеграции в ЦНС сигналов от близлежащих рецепторов в пространственное изображение и координации их с тактильной двигательной функцией.
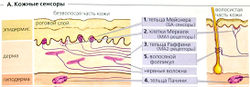
Механорецепторы. Безволосые участки тела содержат следующие механорецепторы (А), которые афферентно иннервированы миелинизированными нервными волокнами класса ll/Aβ:
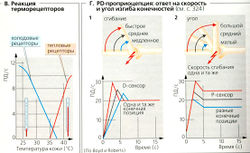
- Веретенообразные чувствительные нервные окончания (тельца Руффини) (АЗ) частично инкапсулируют афферентные ветви аксонов. Этот комплекс называется медленно адаптирующимся (МА) сенсорами давления типа МА2. Это Р-сенсоры. Таким образом, чем больше давление на кожу (глубина вмятины или масса объекта), тем выше частота ПД (Б1).
- Клетки Меркеля (А2) находятся в местах контактов синапсов с менискообразными терминалями аксонов. Эти комплексы называются барорецепторами типа МА1 и относятся к PD-сенсорам (сочетание Б1 и Б2), поскольку частота их потенциала действия зависит не только от величины давления, но также от скорости его изменения (dp/dt).
- Тельца Мейснера (А1) состоят из пластинчатых клеточных слоев, между которыми заканчиваются булавовидные аксоны. Этот комплекс представляет собой быстро адаптирующийся барорецептор (БА-сештд), который реагирует только на изменения давления, dp/dt [D-сенсор, или рецептор скорости). БА-сенсоры специфичны для касания (вдавливание кожи на 10-100 мкм) и низкочастотной вибрации (10-100 Гц). Рецепторы волосяных фолликулов (А5), которые отвечают на изгиб волоса, принимают на себя данную функцию на участках кожи с волосяным покровом.
- Тельца Пачини (А4) иннервируются аксоном ЦНС. Они адаптируются очень быстро и таким образом отвечают на изменения скорости изменения давления, т. е. на ускорение (d2p/dt2) и ощущают высокочастотную вибрацию (100-400 Гц;глубина вдавливания <3 мкм). Частота ПД пропорциональна частоте вибрации (БЗ). Такое усиление сигнала также играет роль в проприорецепции.
Разрешение. БА- и МА1 -рецепторы локализованы с большой плотностью во рту, на губах и кончиках пальцев, особенно на указательном и среднем пальцах (примерно 100 см-2). Они могут отдельно различать очень близкие стимулы, т. е. каждый афферентный аксон имеет узкий участок восприятия. Поскольку сигналы при их проведении в ЦНС не сходятся, сенсоры рта, губ и кончиков пальцев имеют очень хорошую способность к различению близких соседних тактильных стимулов, т. е. очень высокое разрешение.
Пространственный порог дифференциации двух точек, т. е. дистанция, с которой два одновременных стимула могут восприниматься как отдельные, используется в качестве меры тактильного различения. Пространственный порог на пальце, губах и кончике языка составляет примерно 1 мм, на ладони 4 мм, на предплечье 15 мм и на спине более 60 мм.
МА2-рецепторы и тельца Пачини имеют широкий участок восприятия (при этом точная функция МА2-рецепторов не известна). Тельца Пачини, следовательно, хорошо адаптированы для определения вибрации, например дрожания земли.
На коже локализованы два типа терморецепторов: холодовые рецепторы для температур <36 °С и тепловые рецепторы для температур >36 °С. Чем ниже температура (в пределах 20-36 °С), тем выше частота потенциала действия холодовых рецепторов. Для тепловых рецепторов при температурах 36-43 °С применим обратный принцип (В). Температура 20-40 °С подлежит быстрой адаптации термосенсорами (PD-сенсорами). Например, вода, нагретая до 25 °С, вначале ощущается как прохладная. Но крайние температуры этого интервала воспринимаются как холодная или горячая вода (это помогает поддерживать постоянную поверхностную температуру тела и предотвратить повреждение кожи - ожоги и обморожения). Плотность холодовых и тепловых рецепторов на большинстве участков кожи низкая по сравнению с высокой плотностью таких рецепторов во рту или на губах. (Вот почему мы используем губы или щеки для определения температуры.)
При температуре выше 45 °С за восприятие тепла отвечают терморецепторы. Раздражителями для них являются также острые (жгучие) вещества, такие как капсаицин, активный компонент острого перца. Стимуляция VR1-рецепторов капсаицина (ваниллоидных рецепторов типа 1) вызывает открывание катионных каналов ноцицептивных (болевых) нервных окончаний, что ведет к их деполяризации.
Проприоцепция, рефлекс растяжения
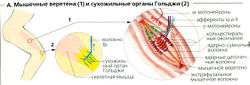
Проприоцепция - это механизм, посредством которого мы ощущаем силу, развиваемую нашими мышцами, а также позу и движение нашего тела и конечностей. Вестибулярный аппарат и кожные механорецепторы помогают при этом проприосенсорам мышечных веретен, суставов и сухожилий. Близ мышечно-сухожильного соединения находятся сенсоры сухожильных органов Гольджи.
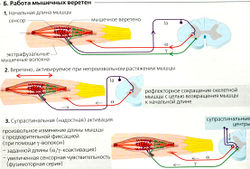
Мышечные веретена (А1) содержат тонические (Р) и дифференциальные (D) рецепторы для определения позиции конечностей и их движения. Скорость изменения позиции отражается в кратковременном повышении частоты импульсов (D-сенсор), а конечная позиция конечностей - как постоянная частота импульсов (Р-сенсор). Мышечные веретена функционируют, регулируя длину мышцы. Они расположены параллельно скелетным мышечным волокнам (экстрафузальные мышечные волокна) и содержат свои собственные мышечные волокна (интрафузальные мышечные волокна). Существуют два типа интрафузальных мышечных волокон: (1) ядерно-цепочечные волокна (Р-сенсоры) и (2) ядерно-сумчатые волокна (D-сенсоры). Окончания афферентных нейронов типа 1а обвивают волокна обоих типов, а нейроны типа II - только ядерно-цепочечные волокна. Эти аннулоспиральные окончания определяют продольные сокращения интрафузальных мышечных волокон и передают в спинной мозг их длину (афференты типа 1а и II) и изменения длины (афференты 1а). Эфферентные у -мотонейроны (фузимоторные волокна) иннервируют оба типа интрафузальных волокон, допуская вариации в их длине и чувствительности к растяжению (А1, Б1).
Сухожильные органы Гольджи (А2) организованы последовательно с мышцей и отвечают на сокращения лишь нескольких двигательных единиц. Их основной функцией является регуляция мышечного напряжения. Импульсы из сухожильных органов Гольджи (проводимые афферентами типа lb), кожи, суставов и мышечных веретен (некоторые из них принадлежат к афферентным волокнам типа 1а и II), а также нисходящие импульсы все вместе интегрируются в интернейронах типа lb спинного мозга; это называется мультимодальной интеграцией (Г2). Интернейроны типа lb ингибируют а-мотонейроны той мышцы, из которой выходят афференты типа lb (аутогенное ингибирование), и активируют антагонистические мышцы при помощи возбуждающих интернейронов (Г5).
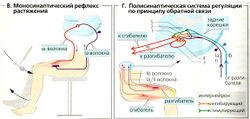
Моносинаптический рефлекс растяжения (В). На мышечные веретена также могут действовать неожиданные растяжения скелетной мышцы, например, через ответвления прикрепляющих ее сухожилий. Сокращение мышечных веретен запускает активацию афферентных импульсов типа 1а (Б2, В), которые поступают в спинной мозг через дорзальные корешки и заканчиваются в брюшном роге у а-мотонейронов той же мышцы. Таким образом, входной сигнал от афферента типа 1а вызывает сокращение той же самой мышцы при помощи единственного синаптического соединения, и рефлекторное время этого моносинаптического рефлекса очень мало (около 30 мс). Он классифицируется как проприоцептивный рефлекс, поскольку и стимуляция, и ответ возникают в том же самом органе. Моносинаптический рефлекс растяжения необходим для быстрой коррекции «непроизвольных» изменений длины мышц и позиций суставов.
Супраспинальная активация (БЗ). Произвольное мышечное сокращение характеризуется коактивацией а- и у-нейронов. Последние корректируют мышечные веретена (сенсоры длины) до некоторой заданной длины. Все отклонения от этого заданного значения, например, по причине неожиданного поднятия тяжести, компенсируются перекорректировкой а-иннервации [рефлекс компенсации нагрузки). Ожидаемые изменения мышечной длины, особенно во время сложного движения, также могут корректироваться более точно активностью у-волокон (центрально регулируемых) путем увеличения преднагрузки и чувствительности к растяжению интрафузальных мышечных волокон (фузимоторная серия).
Рефлекс Гофмана может быть использован для тестирования путей рефлекса растяжения. Это может быть выполнено путем помещения электродов на кожу поверх (смешанных) мышечных нервов и последующей записи мышечного сокращения, индуцируемого электростимуляцией разной интенсивности.
Полисинаптический контрольный механизм, также начинающийся от афферентов типа II, дополняет рефлекс растяжения. Если рефлекс растяжения (например, коленный) происходит на мышце-разгибателе, то а-мотонейроны антагонистической мышцы-сгибателя для достижения эффективного растяжения должны быть ингибированы при помощи ингибиторных интернейронов 1а (Г1).
Дезактивация рефлекса растяжения достигается путем ингибирования мышечного сокращения следующим образом: 1) мышечные веретена расслабляются, тем самым осуществляя дезактивацию волокон типа la; 2) сухожильный орган Гольджи ингибирует а-мотонейроны при помощи интернейронов lb (Г2); 3) а-мотонейроны ингибируются интернейронами (клетками Реншоу, Г4), которые они сами стимулируют при помощи аксонных коллатералей (рецидивирующее ингибирование, Г3).
Ноцицепция и боль
Боль - это неприятное сенсорное ощущение, ассоциирующееся с дискомфортом. Боль служит защитным механизмом, поскольку сигнализирует о том, что организм подвергается повреждению. Ноцицепция - это восприятие боли при помощи болевых рецепторов, нейронального проведения болевого стимула и обработки центральной нервной системой. Боль переживается как субъективное ощущение и может развиваться и без стимуляции болевых рецепторов, а возбуждение болевых рецепторов не всегда вызывает боль.
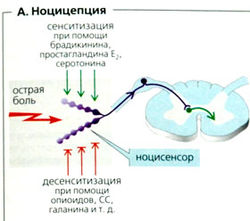
Все ткани организма, кроме мозга и печени, содержат болевые рецепторы, т. е. ноцисенсоры, или ноцицепторы (А). Это похожие на бусинки окончания периферических аксонов, тела которых расположены в ганглиях дорзальных корешков и в ядре тройничного нерва. Большинство этих волокон - медленно проводящие С-волокна (< 1 м/с); а остальные -миелинизированные Аδ-волокна (5-30 м/с).
При травме человек чувствует сначала резкую «быструю боль» (Аδ-волокна), а потом - тупую «медленную боль» (С-волокна), которая чувствуется дольше и на более широких участках. Поскольку болевые рецепторы не адаптируются, боль может продолжаться сутками. Сенситизация может даже понизить порог стимула.
Большинство ноцицепторов являются полимодальными сенсорами (С-волокна), активирующимися механическими стимулами, химическими медиаторами воспаления, а также интенсивными тепловыми или холодовыми стимулами. Однородные ноцицепторы, менее распространенный тип, состоят из термоноцицепторов (Аδ-волокна), механоно-цицепторов (Аδ-волокна) и «дремлющих (дормантных) ноцицепторов». Термоноцицепторы активируются очень горячими (>45 °С) или очень холодными (<5 °С) стимулами. Дормантные ноцицепторы в основном локализованы во внутренних органах и «просыпаются» после длительного воздействия (сенситизации), например при воспалении.
Ноцицепторы могут быть ингибированы опиоидами (десенсибилизация) и стимулированы простагландином Е2 или брадикинином, которые высвобождаются в результате воспаления (сенсибилизация; А). Эндогенные опиоиды (например, динорфин, энкефалин, эндорфин) и экзогенные опиоиды (например, морфин), а также ингибиторы синтеза простагландинов (например, ацетилсалициловая кислота [аспирин]) способны облегчать боль (анальгетическое действие).
Сенсибилизация в результате воспаления (например, эритемы от воздействия солнечных лучей) понижает порог болевых стимулов, что ведет к повышенной чувствительности (гиперальгезии) и боли, происходящей от неболевой стимуляции кожи (аллодинии), например от прикосновения или от теплой воды (37 °С). Когда ноцицепторы стимулируются, они начинают высвобождать нейропетиды, такие как вещество Р или пептид, связанный с геном кальцитонина, которые вызывают воспаление окружающих сосудов (нейрогенное воспаление) Проецируемая боль. Повреждение ноцицептивных волокон порождает боль (нейрогенную или нейропатическую), которая часто проецируется и воспринимается как идущая с периферии. Выпадающий диск, сдавливающий спинномозговые нервы, может, например, вызывать боли в ноге. Ноцицептивные волокна могут быть блокированы холодом или местной анастезией.
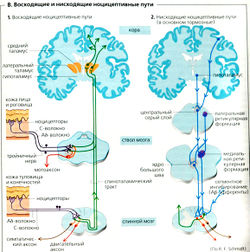
Ноцицептивный тракт (В1). Центральные аксоны ноцицептивных соматических нейронов и ноцицептивные афференты внутренних органов оканчиваются на нейронах дорзального рога спинного мозга. Во многих случаях они оканчиваются на тех же нейронах, что и афференты кожи.
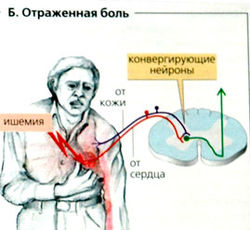
Отраженная боль (Б). Конвергенция соматических и висцеральных ноцицептивных афферентов, вероятно, является основной причиной отраженной боли. При этом виде боли болезненные висцеральные стимулы вызывают восприятие боли в некоторых участках кожи, называемых зонами Геда. Для сердца, например, они расположены в основном в районе груди. Миокардиальная ишемия, следовательно, воспринимается как боль на поверхности грудной клетки (стенокардия, грудная жаба) и часто также в предплечье и верхней части брюшной полости.
В спинном мозге нейроцептивные афференты переходят на противоположную сторону (перекрест) и проводятся в пучки переднелатерального канатика - в основном в спиноталамический тракт - и продолжаются по центру в стволе мозга, где присоединяются к ноцицептивным афферентам головы (в основном к тройничному нерву) и идут в таламус (В1). Из вентролатерального таламуса сенсорное выражение боли проецируется на участки S1 и S2 коры головного мозга. Пути из средних таламических ядер проецируются на лимбическую систему и другие центры.
Компоненты боли. Боль имеет сенсорно-дискриминативный компонент, включая сознательное восприятие (ощущение) участка боли, ее продолжительность и интенсивность; двигательный компонент (например, защитная поза и рефлекс отдергивания), вегетативный компонент (например, тахикардия) и аффективный (эмоциональный) компонент (например, отвращение). Кроме того, оценка боли, основанная на воспоминаниях опыта переживания боли, может вести к связанному с болью поведению (например, стоны).
В таламусе и спинном мозге ноцицепция может быть ингибирована нисходящими путями при помощи различных медиаторов (в основном опиоидов). Ядра этих путей (В2, синий цвет) расположены в стволе головного мозга и в основном активируются при помощи ноцицептивного спиноретикулярного пути (петля отрицательной обратной связи).
Полисинаптические рефлексы
В отличие от проприоцептивных рефлексов, полисинаптические рефлексы активируются сенсорами, которые пространственно отделены от эффекторного органа. Такой тип рефлекса называется полисинаптическим, поскольку рефлекторная дуга включает в себя много последовательных синапсов. Это приводит к относительно большому времени развития рефлекса. Интенсивность ответа зависит от продолжительности и интенсивности стимула, который подлежит пространственной и временной суммации в ЦНС . Например: ощущение зуда в носу - чихание. Ответ распространяется, если интенсивность стимула возрастает (например, кашель - захлебывающийся кашель). Защитные рефлексы (например, рефлекс отдергивания, роговичный и слезный рефлексы, кашель и чихание), рефлексы, связанные с питанием (например, глотание, сосание), локомоторные рефлексы, а также различные вегетативные рефлексы являются полисинаптическими. Некоторые рефлексы, например подошвенный, кремастерный и брюшной, используются в диагностических целях.
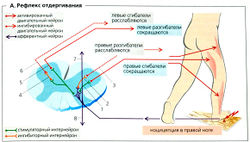
Рефлекс отдергивания (А). Пример: болезненный стимул в подошве правой ноги (например, если наступить на кнопку) ведет к сгибанию всех суставов этой ноги (сгибательный рефлекс). Ноцицептиные афферентные сигналы проводятся при помощи возбуждающих интернейронов (А1) спинного мозга к двигательным нейронам мышц-сгибателей тол же стороны тела, а также при помощи ингибиторных интернейронов (А2) к двигательным нейронам мышц-разгибателей той же стороны тела (АЗ), что ведет к их релаксации; это называется антагонистическим ингибированием. Одна часть ответа - перекрестный разгибательный рефлекс, обеспечивающий отдергивание конечности от повреждающего стимула путем увеличения дистанции между ноцицептивным стимулом (например, от кнопки) и болевым рецептором и тем самым предохраняющий организм. Этот рефлекс состоит из сокращения мышцы-разгибателя (А5) и релаксации мышцы-сгибателя другой ноги (А4, А6). Ноцицептивные афферентные сигналы проводятся и к другим сегментам спинного мозга (восходящим и нисходящим; А7, А8), поскольку разные сгибатели и разгибатели иннервируются разными сегментами. Болезненный стимул может также запускать сгибание той же руки и разгибание другой руки (двойной перекрестный разгибательный рефлекс). Болезненный стимул вызывает восприятие боли в мозге.
В отличие от моносинаптического рефлекса растяжения полисинаптические рефлексы происходят путем коактивации двигательных а- и у-нейронов. Рефлекторное возбуждение двигательных а-нейронов в основном контролируется супраспинальными (надостными) центрами через посредство многочисленных интернейронов. Мозг, таким образом, может сократить время рефлекса спинного мозга, если ожидается болевой стимул.
Надостные повреждения или прерывание нисходящих путей (например, у страдающих параличом нижних конечностей) могут привести к увеличению рефлекса (гиперрефлексии) и стереотипическим рефлексам. Отсутствие рефлекса (арефлексия) соответствует специфическим расстройствам спинного мозга или периферического нерва.
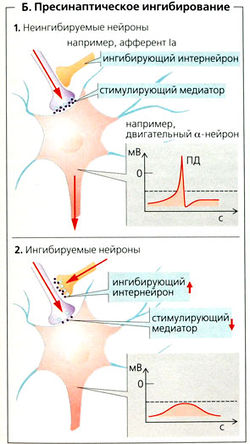
Синаптическое ингибирование ГАМК (у-аминомасляная кислота) и глицинфункционируют в качестве ингибиторных медиаторов спинного мозга. Пресинаптическое ингибирование (Б) часто происходит в ЦНС, например в синапсах между афферентными волокнами типа la и двигательными а-нейронами, а также включает ак-соаксональные синапсы ГАМК-ергических интернейронов пресинаптических нервных окончаний. ГАМК оказывает ингибиторный эффект на нервные окончания посредством увеличения мембранной проводимости ионов Cl- (ГАМКд рецепторы) и К+ (ГАМКв рецепторы) и путем уменьшения проводимости Са2+ (ГАМКв рецепторы). Это снижает высвобождение медиаторов из нервных окончаний нейрона-мишени (Б2), таким образом уменьшая амплитуду возбуждающего постсинаптического потенциала (ВПСП). Целью пресинаптического ингибирования является снижение некоторых влияний на мотонейрон без уменьшения общей возбудимости клетки.
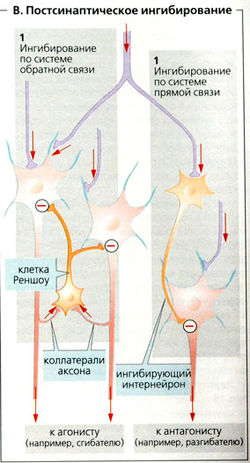
При постсииаптическом ингибировании (В) ингибиторные интернейроны увеличивают мембранную проводимость постсинаптического нейрона к Cl~ или К+, особенно вблизи аксонального бугорка, таким образом замыкая деполяризующие электрические токи от возбуждающего постсинаптического потенциала.
Интернейроны, ответственные за постсинаптическое ингибирование, либо активируются по механизму обратной связи от аксональных коллатералей нейрона-мишени (рецидивирующее ингибирование мотонейронов при помощи глицинергических клеток Реншоу; В1), либо активируются непосредственно другим нейроном при помощи управления по типу прямой связи (В2). Ингибирование одноименного разгибателя (А2, АЗ) в сгибательном рефлексе является примером ингибирования по типу прямой связи.
Проведение сенсорного импульса в ЦНС
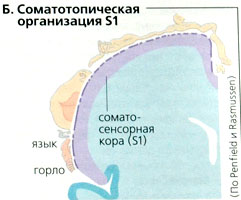
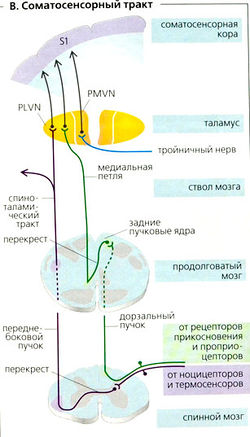
Задние пучковые ядра (В, зеленый цвет) - основной путь, при помощи которого соматосенсорная кора S1 [постцентральная извилина) получает сенсорные сигналы от рецепторов кожи и проприорецепторов. Импульсы от кожи [поверхностная чувствительность) и локомоторной системы [проприоцептивная чувствительность) достигают спинного мозга через дорзальные корешки. Часть этих в основном афферентных волокон проецируется на тракт задних пучков без синапсов к ядрам задних пучков каудального отдела продолговатого мозга (тонкое и клиновидное ядра). Тракты задних пучков демонстрируют соматотропную организацию, т. е. чем более черепным является происхождение волокон, тем более латерально их расположение. У медиальной петли вторичные афферентные соматосенсорные волокна делают перекрест на контрлатеральную сторону и продолжаются в заднелатеральное брюшное ядро (PLVN) таламуса, где также организованы соматотопически. Вторичные афферентные волокна тройничного нерва (петля тройничного нерва) заканчиваются в постеромедиальном брюшном ядре (PMVN) таламуса. Третичные афферентные соматосенсорные волокна заканчиваются в четвертичных соматосенсорных нейронах соматосенсорной коры S1. Основная функция заднего пучково-петельного пути заключается в том, чтобы транслировать информацию о тактильных стимулах (давление, прикосновение, вибрация), а также о положении и движении суставов (проприоцепция) в кору головного мозга, в основном через его особенно быстро проводящие волокна, с большим пространственным и временным разрешением.
Как и в двигательной коре, каждая часть тела соотносится с соответствующим участком проекции в соматосенсорной коре S1 (А) с последующей соматотропной организацией (Б). Три особенности организации S1 следующие: (1) каждое полушарие мозга получает информацию от контрлатеральной части тела (тракты пересекаются в медиальной петле; В); (2) большинство нейронов S1 получают афферентные сигналы от тактильных сенсоров пальцев и рта; и (3) афферентные сигналы обрабатываются в коре головного мозга, которые активируются специфическими стимулами (например, касанием).
Переднелатеральный спиноталамический путь (В; фиолетовый цвет). Афферентные сигналы от ноцицепторов, термосенсоров и второй части афферентных нейронов давления и прикосновения транслируются (частично через интернейроны) на разных уровнях спинного мозга. Вторичные нейроны образуют перекрест на противоположную сторону соответствующих сегментов спинного мозга, образуют латеральный и вентральный спиноталамический тракт в переднелатеральном пучке и проецируются в таламус. Третичные афферентные волокна далее попадают в соматосенсорную кору S1.
Нисходящие тракты (от коры) могут тормозить сенсорный поток в кору на всех участках передачи (спинной мозг, продолговатый мозг, таламус). Основная функция этих трактов заключается в модификации воспринимающего участка и достижении порога стимула. Когда импульсы от разных источников проводятся в одном афферентном волокне, они также помогают подавлению несущественного сенсорного входа и селективно обрабатывают наиболее важные и интересные сенсорные модальности и стимулы (например, при подслушивании).
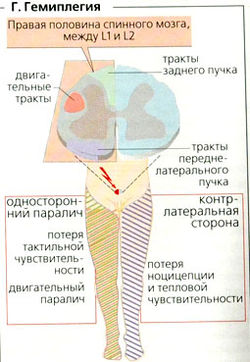
Гемиплегия (Г). Синдром Броуна-Секара развивается из-за повреждения половины поперечника спинного мозга, приводящего к одностороннему параличу и потере различных функций ниже повреждения. Поврежденная сторона демонстрирует двигательный паралич (вначале слабый, затем спастический) и потерю сенсорных ощущений (например, ослабленное различение двух точек). При этом происходит дополнительная потеря болевой и тепловой чувствительности на контрлатеральной стороне [диссоциированный паралич).
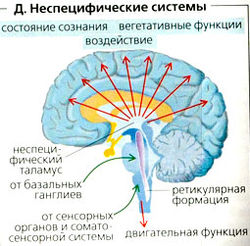
Ретикулярная активирующая система (Д). Сенсорный вход, описанный выше, как и вход от сенсорных органов, специфичен, тогда как ретикулярная активирующая система (РАС) является неспецифической системой. РАС - это комплексная обрабатывающая и интегрирующая система клеток ретикулярной формации ствола головного мозга. Эти клетки получают сенсорный вход от всех сенсорных органов и восходящих путей спинного мозга (например, от глаз, ушей, поверхностная чувствительность, ноцицепция), базальных ганглиев и т. д. Холинергический и адренергический выход от РАС проводится по нисходящему пути в спинной мозг и вдоль восходящих «неспецифических» таламических ядер и «неспецифических» таламокортикальных трактов почти во все участки коры, лимбическую систему и гипоталамус. Восходящая РАС, или ВРАС, контролирует состояние сознания и степень бодрствования [показатель возбудимости).
Движение
Координированные мышечные движения (пешая прогулка, хватание, бросание и т. д.) функционально зависят от статической (постуральной) двигательной системы, которая ответственна за поддержание вертикального положения тела, равновесия, а также пространственной интеграции движений тела. Поскольку контроль за статической моторной функцией и мышечной координацией требует одновременного и непрерывного потока сенсорных импульсов от периферии, это называют сенсомоторной функцией.
а-Мотонейроны переднего рога спинного мозга и ядер черепных нервов являются терминальными трактами активации скелетной мускулатуры. Только некоторые части кортикоспинального тракта и афферентных волокон типа la моносинаптически соединяются с а-мохонейронами. Другие афферентные волокна от периферии (проприоцепторы, ноцицепторы, механорецепторы), другие сегменты спинного мозга, моторной коры, мозжечка, а также моторные центры ствола мозга соединены с а-мотонейронами при помощи сотен тормозных и возбуждающих интернейронов на один мотонейрон.
Произвольная двигательная функция
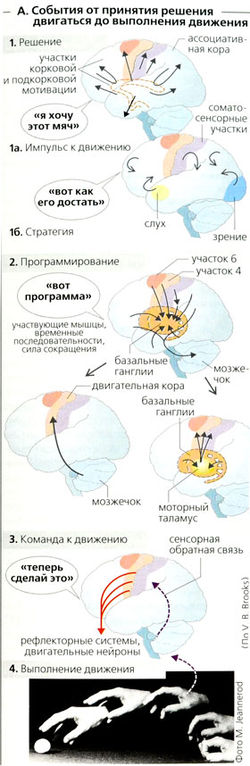
Произвольные движения требуют серии действий: решение начать движение → планирование (воспоминание о хранящихся стандартных программах) →команда к началу движения → выполнение движения (А1-4). Обратная связь от афферентных волокон двигательных подсистем и информация от периферии постоянно включается в процесс. Это позволяет совершать коррекцию как до, так и во время произвольного движения.
Нейронная активность, ассоциируемая с первыми двумя фазами произвольного движения, активирует многочисленные двигательные участки коры. Эта электрическая активность мозга отражается в виде отрицательного потенциала ожидания коры головного мозга, который наилучшим образом может быть измерен в ассоциированных участках или на темени. Чем более сложным является движение, тем выше потенциал ожидания и тем раньше его начало (примерно 0,3-3 с).
Двигательная кора состоит из трех основных участков (В, вверху):
- первичный моторный участок, М1 (участок 4);
- премоторный участок, РМА (латеральный участок 6);
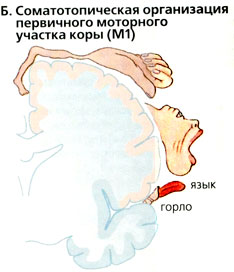
- дополнительный моторный участок, SMA (средний участок 6). Моторные участки коры обнаруживают соматотопическую организацию по отношению к мышцам-мишеням их волокон (показано на Б для М1) и их взаимосвязь.
Кортикальные афферентные волокна
Кора головного мозга получает двигательные сигналы от
- периферии организма (через таламус → S1 → сенсорную ассоциативную кору → РМА);
- базальных ганглиев (через таламус→ М1, РМА, SMA [А2] → предлобную ассоциативную кору);
- мозжечка (через таламус → М1, РМА; А2);
- сенсорных и задних париетальных участков коры (участки 1-3 и 5-7 соответственно).
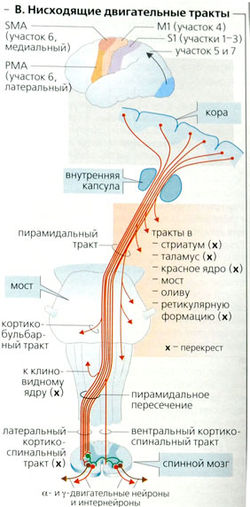
Кортикальные эфферентные волокна (В, Г, Д, Е). Двигательные импульсы от коры в основном проецируются на (а) спинной мозг; (б) подкорковые двигательные центры, и (в) контрлатеральную кору через комиссуральные (соединительные) пути.
Пирамидный тракт включает в себя кортикоспинальный тракт и часть кортикобульбарного тракта. Более 90% пирамидального тракта состоит из тонких волокон, но об их функции мало что известно. Толстый быстро проводящий кортикоспинальный тракт (В) проецируется на спинной мозг от 4 и 6 и от 1-3 участков сенсорной коры. Некоторые волокна моносинаптически соединены с а- и у-мотонейронами, ответственными за движение пальцев (точный захват). Большая их часть образует синапсы с интернейронами спинного мозга, где они влияют на вход периферических афферентных нейронов, а также на моторные выходы (через клетки Реншоу) и, таким образом, на спинальные рефлексы.
Функции базальных ганглиев
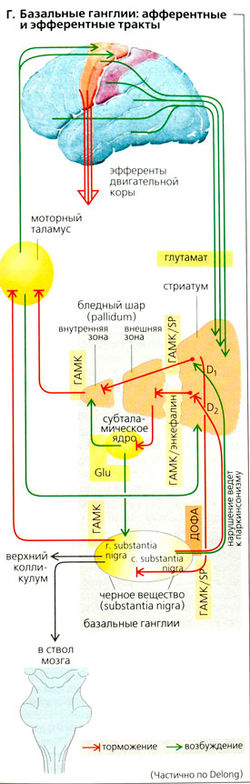
Строение. Базальные ганглии являются частью многочисленных параллельных кортикокортикальных сигнальных петель. Ассоциативные петли, начинающиеся в лобной и лимбической коре, играют роль в таких видах ментальной активности, как оценка сенсорной информации, адаптация поведения к эмоциональному контексту, мотивация, долговременное планирование действий. Функция скелетодвигательных и глазодвигательных петель (см. далее) состоит в координации и контроле скорости последовательных движений. Эфферентные проекции базальных ганглиев контролируют проведение таламокортикальных сигналов при помощи; (а) ослабления торможения (растормаживающий эффект, прямой способ) таламических моторных ядер и верхнего колликулума, соответственно, или (б) путем интенсификации их торможения, (непрямой способ).
Основной вход информации в базальные ганглии происходит из скорлупы и хвостатого ядра стриатума (полосатого тела). Нейроны стриатума активируются трактами из всех участков коры и в качестве медиатора используют глутамат [Г). При активации нейроны стриатума высвобождают ингибиторный медиатор (у-аминомасляную кислоту, ГАМК) и комедиатор - вещество Р (SP) или энкефалин (Г).
Основной исходящий импульс базальных ганглиев проходит через ретикулярную (сетчатую) зону черного вещества (substantia nigra) или через внутреннюю зону бледного шара (globus pallidus). Обе зоны ингибируются substantia nigra/ГАМК-ергическими нейронами стриатума (Г).
Как substantia nigra, так и i. pallidus ингибируют (при помощи ГАМК) вентролатеральный таламус с большим уровнем спонтанной активности. Активация стриатума, следовательно, ведет к растормаживанию таламуса прямым путем. Однако, если активируются нейроны стриатума, высвобождающие энкефалин и ГАМК, то они ингибируют внешнюю зону бледного шара, что, в свою очередь, тормозит (при помощи ГАМК) субталамическое ядро. Субталамическое ядро индуцирует глутаминергическую активацию substantia nigra и globus pallidus. Конечным результатом этого непрямого пути является увеличение торможения таламуса. Поскольку таламус проецируется на двигательную и предлобную кору, кортикоталамокортикальная петля (скелетодвигательная петля), влияющая на движение скелетных мышц проходит через базальные ганглии в области пугамена (скорлупного ядра). Глазодвигательная петля проецируется на хвостатое ядро, ретикулярную зону и верхний колликулум и участвует в контроле за движением глаз. Нисходящий тракт из substantia nigra проецируется на крышу среднего мозга и ядро ножки моста.
Тот факт, что компактная зона (compacts) черной субстанции (с. substantia nigra) снабжает дофамином весь стриатум (дофаминэргические нейроны) - важная физиологическая функция, возможна патология (Г). Дофамин связывается с D1-рецепторами (увеличивая уровень цАМФ), тем самым активируя substantia nigra/ГАМК-нейроны стриатума - прямой путь активации (см. ранее). Дофамин же реагирует с D2-рецепторами (снижая уровень цАМФ), ингибируя при этом энкефалин/ГАМК-нейроны -непрямой путь активации. Эти эффекты дофамина важны для работы стриатума в норме. Дегенерация более чем 70% дофаминергических нейронов компактной зоны приводит к избыточному ингибированию участков таламуса, управляющих мотонейронами, что влияет на произвольные движения. Это происходит при болезни Паркинсона и может быть результатом генетической предрасположенности, травмы (например, у боксеров), мозговой инфекции и других причин. Характерные симптомы болезни: бедность движений [акинезия), замедленные движения [брадикинезия), семенящая походка, мелкий почерк (микрография.I, маскоподобное выражение лица, гипертонус мышц (ригор, окоченение), изогнутая поза, а также мышечный тремор в покое (характерные движения пальцев, как при пересчитывании денет).
Функции мозжечка
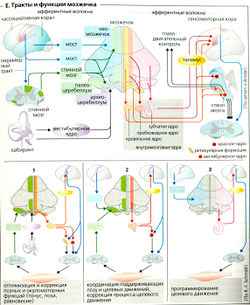
Мозжечок содержит столько же нейронов, сколько и весь остальной мозг. Он является важным контрольным центром двигательных (моторных) функций, имеющим афферентное и эфферентное соединение с корой мозга и периферическими нейронами (Е, вверху). Мозжечок участвует в планировании, выполнении и контроле движений и отвечает за адаптацию к новым последовательностям движений (двигательное научение). Он также взаимодействует в высшими центрами контроля внимания и т. д.
Анатомия (Е, вверху). Архицеребеллум (старый мозжечок состоит из клочков и узелка) и палеоцеребеллум (древний мозжечок состоит из пирамиды, язычка, червя, внеклочковых долек и частей передней доли) - это все филогенетически наиболее древние части мозжечка. Эти структуры и промежуточная зона (интермедиа) образует срединный мозжечок. Неоцеребеллум (новый мозжечок состоит из задней доли и тела мозжечка) - это филогенетически новые части мозжечка; латеральный мозжечок. На основе происхождения эфферентных волокон старый мозжечок и червь мозжечка иногда называют вестибулоцеребеллумом (вестибулярным мозжечком), древний мозжечок -спиноцебеллум, а новый мозжечок - мостоцеребеллумом (мостовым ядром мозжечка). Кора мозжечка представлена складчатой (бороздчатой) поверхностью из серого вещества - внешнего молекулярного слоя дендритов клеток Пуркинье и их афферентов, среднего слоя клеток Пуркинье (телец Пуркинье) и внутреннего слоя гранулярных клеток. На внешнем слое мозжечка видны маленькие параллельные извилины, называемые листками.
Срединный мозжечок и зона интермедиа мозжечка в основном контролируют позные и поддерживающие двигательные функции (Е1, 2) и глазодвигательные функции. Входящие сигналы: срединный мозжечок получает афферентные копии спинальных, вестибулярных и зрительных стимулов и эфферентные копии нисходящих двигательных сигналов к скелетной мускулатуре. Выходящие сигналы из срединного мозжечка проходят через внутримозжечковые верхушечное, сферическое и эмболиформное ядра к двигательным центрам спинного мозга и ствола мозга, а также к вне-мозжечковым вестибулярным ядрам (главным образом к ядру Дейтерса). Эти центры контролируют глазодвигательную функцию и воздействуют на локомоторную функцию и поддержание осанки (позные функции) через вестибулоспинальный тракт.
Латеральный мозжечок (полушария) в основном участвует в программируемых движениях (ЕЗ), но его пластичность также способствует двигательной адаптации и научению двигательным последовательностям. Полушария мозжечка имеют двухстороннюю связь с корой головного мозга. Входящие сигналы: а) через мостовое ядро и гранулярные волокна; латеральный мозжечок получает входящие сигналы от кортикальных центров для планирования движения (например, от париетальной, предлобной и премоторной ассоциативной коры; сенсомоторного и зрительного участков); б) мозжечок также получает входящие сигналы из кортикальных и подкорковых двигательных центров через нижнюю оливу и извитые волокна. Выходящие сигналы: из латерального мозжечка проецируются через двигательные участки таламуса от зубчатого ядра к двигательным участкам коры.
Повреждения срединного мозжечка ведут к нарушению равновесия и глазодвигательного контроля (головокружение, тошнота, маятниковый нистагм] и вызывают атаксию туловища и походки. Повреждения латерального мозжечка ведут к нарушениям начала, координации и окончания направленных движений и ухудшают быстрое перепрограммирование диаметрально противоположных движений [диадохокинез). Типичный пациент: тремор при попытке произвольных координированных движений (тремор усилия), затруднения при определении расстояния при мышечных движениях (дисметрия), маятникообразные движения с отскоком после остановки (феномен отскока), а также неспособность к выполнению быстрых возвратно-поступательных движений (адиадохокинез).
Кора мозжечка имеет однородную ультраструктуру и строение. Все исходящие импульсы от коры мозжечка проводятся аксонами клеток Пуркинье, количество которых примерно 15 • 106. Эти ГАМК-ергические клетки проецируются на верхушечное, эмболиформное, зубчатое и латеральное вестибулярное ядра (ядро Дейтерса; Е, справа) и оказывают на них тормозное воздействие.
Входящие импульсы и строение: входящие импульсы от спинного мозга (спинально-церебеллярные тракты) транслируются через нижнюю оливу и переносятся через возбуждающие извитые волокна (рассеивание 1:15), которые оканчиваются на полоске клеток Пуркинье, протягивающейся через листки мозжечка, образуя сагиттальные возбудительные очаги. Извитые волокна используют в качестве медиатора аспартат. Серотонинергические волокна из шовных ядер и норадренергические волокна из локуса церулеус также заканчиваются в возбудительных очагах. Гранулярные волокна (мостовые, ретикулярные и спинальные афференты) стимулируют гранулярные клетки. Их аксоны образуют Т-образные ответвления (параллельные волокна). В молекулярном слое они плотно сходятся (примерно 105: 1) на полосках клеток Пуркинье, проходящих рядом с листками; эти участки называются продольными возбудительными очагами. Считают, что система извитых волокон (на пересечении перпендикулярных возбудительных очагов) усиливает относительно слабые сигналы афферентных гранулярных волокон клеток Пуркинье. Многочисленные интернейроны (Гольджи, звездчатые и корзинчатые нейроны) усиливают контраст возбуждающего действия коры мозжечка за счет латерального рецидивного ингибирования.
Двигательный контроль осанки
Простые рефлексы растяжения, а также более сложные сгибательные и перекрестные экстензорные рефлексы контролируются на уровне спинного мозга.
Рассечение спинного мозга (параплегия) ведет к начальной потере периферических рефлексов ниже уровня повреждения (арефлексия, спинальный шок), но позже рефлексы могут восстановиться, даже несмотря на продолжающуюся параплегию.
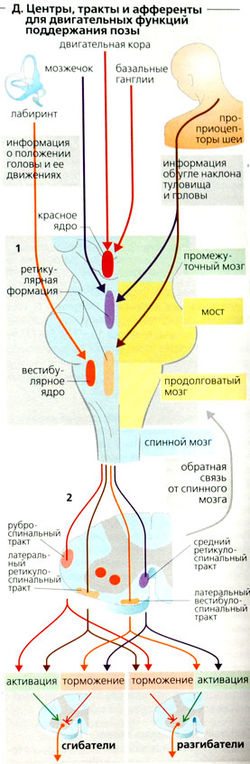
Спинальные рефлексы в основном подчинены супраспинальным центрам (Д). Двигательная функция поддержания осанки в основном контролируется моторными центрами ствола мозга (Д1), т. е. красным ядром, вестибулярным ядром (в основном латеральным вестибулярным ядром), и частью ретикулярной формации. Эти центры функционируют как места переключения, передающие информацию, относящуюся к статическому и лабиринтному рефлексам, требующимся для поддержания позы и равновесия (без участия воли). Осаночные рефлексы регулируют мышечный тонус и адаптационные движения глаз. Входящие сигналы поступают от органов равновесия [тонический лабиринтный рефлекс) и от проприоцепторов шеи (тонический шейный рефлекс). В осаночные рефлексы (тонический и шейный) вовлечены те же самые афференты, которые помогают поддерживать тело в нормальном положении. Туловище приводится к нормальной позе в ответ на сигналы от проприоцепторов шеи. Афферентная проекция от мозжечка, двигательной коры головного мозга (В), глаз, ушей и органа обоняния, а также рецепторов кожи также воздействует на осаночный рефлекс. Статокинетические рефлексы играют важную роль также в контроле за положением тела и осанкой. Они участвуют, например, в нистагме и рефлексе испуга.
Нисходящие тракты спинного мозга, начинающиеся от красного ядра и медуллярной ретикулярной формации [руброспинальный и латеральный ретикулоспинальный тракты), оказывают общий тормозной эффект на а и у-мотонейроны мышцы-разгибателя и возбуждающий эффект но мышцу-сгибатель (Д2). И наоборот, тракты из ядра Дейтерса и мостовых участков ретикулярной формации (вестибулоспинальный и медиальный ретикулоспинальный тракты) ингибируют сгибатель и возбуждают а- и у-волокна разгибателя.
Рассечение ствола мозга ниже красного ядра ведет к децеребрационной ригидности, поскольку разгибательный эффект ядра Дейтерса при этом доминирует.
Интегрирующую и координирующую функции сенсомоторной системы можно проиллюстрировать на примере двух игроков в теннис. Когда один из игроков подает, тело другого перемещается навстречу мячу [целенаправленное движение), используя при этом правую ногу для поддержки и левую руку для поддержания равновесия (двигательный контроль осанки). Игрок следит глазами за мячом (глазодвигательный контроль), и зрительный участок коры оценивает траекторию и скорость движения мяча. Ассоциативная кора головного мозга инициирует движение возвращения мяча, принимая во внимание мяч, сетку, другую сторону корта и положение партнера. Для возврата мяча может быть необходима корректировка позиции. Моторная часть коры выполняет направленное действие возврата мяча, используя план движения, запрограммированный мозжечком и базальными ганглиями. При выполнении этого действия игрок может «подрезать» мяч, чтобы придать ему дополнительное вращение (приобретенное быстрое управляемое движение).
Гипоталамус, лимбическая система
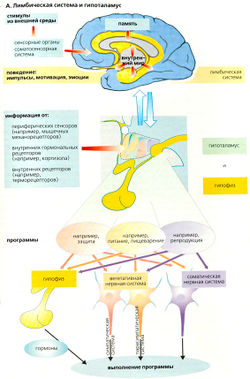
Гипоталамус координирует все вегетативные и большинство эндокринных процессов и интегрирует сигналы, контролирующие внутреннюю среду, цикл сна-бодрствования, рост, умственное и психическое развитие, процесс репродукции и другие функции. Гипоталамус получает многочисленные сенсорные и гуморальные сигналы (А). Пептидные гормоны могут преодолевать гемато-энцефалический барьер при помощи циркумвентрикулярных органов.
Афференты. Термосенсоры, осуществляющие контроль за температурой тела, осмосенсоры, регулирующие осмоляльность и водный баланс, и рецепторы глюкозы, обеспечивающие поддержание минимальной концентрации глюкозы, расположены в гипоталамусе. Информация о текущем состоянии внутреннего пространства проецируется в гипоталамус от дистальных сенсоров, например от термосенсоров кожи, осмосенсоров печени и рецепторов растяжения предсердий. Гипоталамические/цир-кумвентрикулярные органы также содержат рецепторы различных гормонов [например, кортизола и ангиотензина II), некоторые из них формируют часть контрольных цепей метаболизма энергии и метаболического гомеостаза (например, рецепторы кортизола, АКТГ, КРГ, лептина и ХСК). Для выполнения функций, связанных с ростом и репродукцией, гипоталамус получает регуляторные сигналы от гонад и входящие сигналы от нейронных афферентов, которые оповещают, помимо прочего, о расширении шейки матки в начале родов и стимуляции груди (рефлекс сосания).
Лимбическая система (А) и другие участки мозга воздействуют на функцию гипоталамуса. Лимбическая система контролирует врожденное и приобретенное поведение («выбор программы») и является местонахождением инстинктивного поведения, эмоций и мотиваций («внутренний мир»). Она контролирует выражение эмоций, проводя в среду важные сигналы (например, страх, гнев, ярость, дискомфорт, радость, счастье). И наоборот, сигналы из среды (например, запах) сильно связаны с поведением.
Лимбическая система включает корковые компоненты (гиппокамп, извилина гиппокампа, мозолисто-краевая извилина, часть обонятельного участка мозга) и подкорковые компоненты (миндалевидное тело, перегородочные ядра, передние ядра таламуса). Лимбическая система имеет взаимосвязь с латеральной частью гипоталамуса (в основном используемую для вспоминания программ, см. далее), а также височной и лобной долями коры головного мозга. Связь лимбической системы с корой в основном используется для восприятия и оценки сигналов из «внешнего мира» и из воспоминаний. Обработка обоих типов входящей информации важна для поведения.
Программируемое поведение (А). Латеральная часть гипоталамуса имеет различные программы контроля низших гормональных, вегетативных и моторных процессов. Это отражается внутри за счет многочисленных вегетативных и гормональных процессов и выражается наружу в различных видах поведения.
Для разных поведенческих реакций существуют различные программы.
- Защитное поведение («нападение или бегство»). Эта программа имеет соматическую (отталкивающее выражение лица и поза, нападающее поведение или бегство), гормональную (адреналин, кортизол) и вегетативную (симпатическая нервная система) компоненты. Активация защитного поведения приводит к высвобождению богатых энергией жирных кислот, ингибированию высвобождения инсулина и снижению кровотока в желудочно-кишечном тракте, а также к увеличению минутного сердечного выброса, частоты дыхания и кровотока в скелетных мышцах.
- Физические упражнения. Компоненты этой программы сходны с таковыми для защитного поведения.
- Пищевое поведение, целью которого является обеспечение адекватного снабжения едой и напитками, их переваривания и усвоения. Включает в себя поиск еды, например, в холодильнике, активацию парасимпатической системы с увеличением желудочно-кишечной секреции и подвижности в ответ на поглощение пищи, уменьшение скелетной мышечной активности после еды и т. д.
- Половое поведение, т. е. ухаживание за партнером, нейронные механизмы сексуального ответа, гормональная регуляция беременности и т. д.
- Терморегуляторное поведение, которое позволяет нам поддерживать относительно постоянную температуру даже при экстремальных температурах окружающей среды или при высоком уровне выделения тепла при интенсивной физической работе.
Моноаминергическая нейронная система содержит нейроны, высвобождающие моноаминные нейромедиаторы норадреналин, адреналин, дофамин и серотонин. Эти нейронные тракты тянутся от ствола почти во все части мозга и играют важную роль в общей регуляции поведения. Экспериментальная активация норадренергических нейронов, например, приводила к положительному подкреплению (симпатии, вознаграждения), тогда как серотонинергические нейроны считаются ассоциированными с антипатией. Многие психотропные лекарства направлены на моноаминергические нейронные системы.
Кора головного мозга, электроэнцефалограмма (ЭЭГ)
В норме функции коры головного мозга необходимы при сознательном восприятии, планировании действий и целенаправленных движениях.
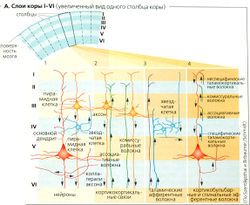
Ультраструктура коры мозга и строение нейронов (А). Кора головного мозга состоит из шести слоев (I—VI], расположенных параллельно поверхности мозга. Вертикально кора мозга разделена на столбы и модули (диаметром 0,05-0,3 мм, глубиной 1,3-4,5 мм), которые тянутся через все шесть слоев.
Входные сигналы от специфических и неспецифических участков таламуса заканчиваются в основном в слое IV и в слоях I и II соответственно (АЗ); входные сигналы от других участков коры заканчиваются в основном в слое II (А2). Большие и малые пирамидные клетки (А1) составляют 80% всех клеток коры, они расположены в слоях V и III соответственно (в качестве медиатора обычно выступает глутамат, например, в стриатуме). Аксоны пирамидных клеток покидают VI слой соответствующего столба и являются единственным источником выходных сигналов коры. Большинство аксонов проецируется на другие участки той же стороны коры (ассоциативные волокна) или на контрлатеральные участки коры (комиссуральные волокна) (А2); и лишь небольшое количество тянется на периферию (А4 ). Пирамидные клетки в некоторых местах соединены друг с другом коллатералями аксонов. Главный дендрит пирамидной клетки проецируется на верхние слои своих столбов и имеет множество шипообразных отростков (остей), где заканчиваются многие таламокортикальные, комиссуральные и ассоциативные волокна. Афферентные волокна используют разнообразные медиаторы, например глутамат, норадреналин, дофамин, серотонин, ацетилхолин и гистамин. Внутри коры информация обрабатывается многочисленными морфологически различающимися звездчатыми клетками (А1), некоторые из них имеют возбуждающий эффект (ВИП, ХСК и другие пептидные медиаторы), тогда как другие имеют тормозящий эффект (ГАМК). Дендриты пирамидных и звездчатых клеток проецируются на соседние столбы, и таким образом столбы соединены тысячами нитей. Пластичность синапсов пирамидных клеток, т. е. тот факт, что они могут быть модифицированы в соответствии с их действием, играет важную роль при обучении.
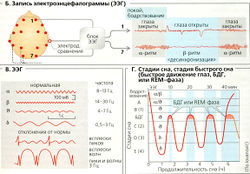
Потенциал коры. По аналогии с методом электрокардиографии, совокупные флуктуации электрических потенциалов (мозговые волны) в коре могут быть записаны методом электроэнцефалографии с использованием электродов, налагаемых на кожу головы (Б). Возбуждающий постсинаптический потенциал (ВПСП) дает основной вклад в электроэнцефалограмму (ЭЭГ) по сравнению с ингибирующим постсинаптическим потенциалом (ИПСП), генерируемым у синапсов дендритов пирамидных клеток. Лишь часть ритмов, регистрируемых при помощи ЭЭГ, производится непосредственно в коре (а- и у-волны у находящего в сознании человека; см. далее). Волны более низкой частоты из других участков мозга, например a-волны из таламуса и 0-вол-ны из гиппокампа, «нагнетаются» в кору (увеличение мозговых волн).
По договоренности, нисходящие отклонения ЭЭГ считаются положительными. В общем деполяризация (возбуждение) более глубоких слоев коры и гиперполяризация поверхностных слоев вызывают нисходящие отклонения (+) и наоборот.
Типы мозговых волн. Уровень электрической активности коры в основном определяется степенью бодрствования и может различаться на основе амплитуды (з) и частоты (А волн (Б, В). а-Волны [f =10 Гц; a« 50 мкВ), преобладающие во время бодрствования здорового человека в расслабленном состоянии (с закрытыми глазами), обычно определяются несколькими электродами (синхронизированная активность). Когда глаза открыты, или если стимулируются другие сенсорные органы, или испытуемый решает математическую задачу, a-волны затухают (а-блокада), и появляются β-волны (f= 20 Гц). Амплитуда β-волн ниже, чем a-волн, и при открытых глазах в основном они обнаруживаются в затылочной (Б) и теменной областях. Частота и амплитуда β-волн сильно отличается при разных отведениях [десинхронизация). β-Волны отражают повышенное внимание и активность (активность возбуждения) восходящей ретикулярной активационной системы (ВРАС). у-Волны (>30 Гц) появляются во время обучения. Низкочастотные 6-волны появляются при переходе дремоты в сон (стадии сна А/В/С; Г), во время глубокого сна они могут трансформироваться в еще более медленные d-волны (В, Г).
ЭЭГ используется при диагностике эпилепсии (локальные или генерализованные параксимальные потенциалы; В), при оценке степени зрелости мозга, при контроле анестезии, а также как критерий констатации смерти мозга [изоэлектрическая ЭЭГ).
Магнитоэнцефалография (МЭГ), т. е. запись магнитных сигналов, индуцированных токами кортикальных ионов, в сочетании с ЭЭГ используется для точной локализации участка активности коры (разрешение в несколько мм).
Цикл сна-бодрствования, циркадные ритмы
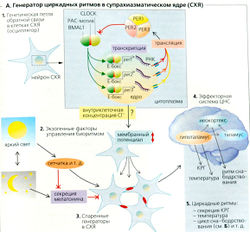
Суточный цикл сна-бодрствования и другие циркадные (суточные) ритмы контролируются эндогенными генераторами ритма. Регулируют эти процессы центральные биологические часы (циркадный осциллятор) в супрахиазматическом ядре (СХЯ) гипоталамуса (А). Эндогенный циркадный ритм в виде циклов происходит примерно за 24-25 часов, но он таков только тогда, когда человек полностью изолирован от внешних влияний (например, находится в подвале без окон, в темной пещере и т. д.). Экзогенные сигнальные стимулы синхронизируют биологические часы к точному 24-часовому циклу. Раздражающий стимул или замедляет, или ускоряет ритм в зависимости от его фазы. Для того чтобы заново установить биологические часы (например, после долгого путешествия с востока на запад) требуется несколько дней (расстройство биоритмов).
Основным экзогенным раздражающим стимулом 24-часовой синхронизации цикла сна-бодрствования является световой день (световой раздражитель). Световые стимулы воспринимаются непосредственно небольшой меланопсинсорержащей фракцией ганглионарных клеток сетчатки, и проводятся в супрахиазматическое ядро по ретиногипоталамическому тракту (А2, 3).
Сигналы достигают также эпифиза (шишковидное тело, шишковидная железа), где ингибируют секрецию мелатонина, обычно высокую ночью. Поскольку эффект оказывается в основном на СХЯ, введение мелатонина перед отходом ко сну может сильно уменьшить время, требующееся для «переустановки» биологических часов. Основная причина состоит в том, что мелатонин временно «дезактивирует» через М2-рецепторы СХЯ, благодаря чему большинство ночных входящих сигналов (кроме световых стимулов) исключаются (не проводятся).
Недавно были открыты важные генетические «зубцы» центральных биологических часов млекопитающих (А1). Нейроны СХЯ содержат специальные белки (CLOCK и BMAL1), домены РАС которых связываются с образованием гетеродимеров. Образующиеся в результате комплексы CLOCK/BMAL1 входят в клеточное ядро, где их промоторные последовательности (Е-бокс) связываются с генами периодического [per)-осциллятора per1, рег2 и реrЗ, активируя тем самым их транскрипцию. После латентного периода, экспрессия этих генов дает продукты PER1, PER2 и PER3, которые все вместе функционируют в виде тримера и блокируют эффект CLOCK/BMAL1, завершая петлю отрицательной обратной связи. Механизм, при помощи которого этот цикл активирует последующие нейрональные эффекты (мембранные потенциалы), не известен.
Спаренные клетки СХЯ (АЗ) осуществляют циркадные ритмы гормональной секреции, внутренней температуры тела и циклов сна-бодрствования (А5, Б) при помощи различных эффектоных систем ЦНС (А4).
Стадии сна можно различить при помощи ЗЗГ. Когда здоровый человек, находящийся в состоянии бодрствования, отдыхает и его глаза закрыты (a-волны), он начинает погружаться в сон; сознание сначала переходит в фазу сна А (дремота), при которой на ЭЭГ могут быть обнаружены только несколько изолированных a-волн. Далее дремота переходит в фазу засыпания В (стадия 1), на которой появляются a-волны, затем в фазу поверхностного сна С (стадия 2) - вспышки быстрых волн (сонные веретена) и изолированных волн (К-комплексы), и, в конечном итоге, в стадию глубокого сна (фазы D/E = стадии 3/4) - появление δ-волн. Их амплитуда возрастает, тогда как частота падает до минимума во время фазы Е.
Таким образом, эта фаза называется медпенновопновым сном (МВС). Порог возбуждения является самым высоким примерно через 1 час после того, как человек заснул. Затем сон становится менее глубоким, и происходит первый эпизод быстрого движения глаз (БДГ, или REM-фаза). Этим завершается первый цикл сна. Во время быстрого движения глаз большинство скелетных мышц становятся расслабленными (торможение двигательных нейронов), тогда как дыхание и сердечный ритм увеличиваются. Лицо и пальцы неожиданно начинают подергиваться, может происходить эрекция пениса (у мужчин), можно наблюдать быстрые движения глаз. Все другие стадии сна совместно называются стадиями небыстрого движения глаз (НБДГ). Спящие, разбуженные во время стадии с БДГ, чаще способны рассказать о своих снах, чем разбуженные на других стадиях. Цикл сна обычно длится 90 мин и повторяется 4-5 раз в течение ночи.
К утру стадии сна с НБДГ становятся короче и более поверхностными, тогда как длительность эпизодов сна с БДГ возрастает примерно от 10 до 30 минут.
Младенцы спят дольше (примерно 16 часов в сутки, 50% - сон с БДГ), 10-летние дети спят примерно 10 часов в сутки (20% - с БДГ), молодые люди спят 7-8 часов в сутки, а люди старше 50 лет спят около 6 часов (в обоих группах 20% - с БДГ). Пропорция МВС снижается в пользу фазы С (стадии 2).
Когда человек лишается фазы сна с БДГ (бывает разбужен во время этой фазы), продолжительность следующей фазы с БДГ увеличивается для компенсации дефицита. Первые два-три цикла сна (основной сон) являются необходимыми. Полное лишение сна ведет к смерти, но причина этого пока не ясна, поскольку слишком мало известно о физиологической роли сна.
Сознание. Сон
Сознание. Избирательное внимание, абстрактное мышление, возможность выразить словами свой жизненный опыт, способность планировать свою деятельность, опираясь на опыт, самоанализ и систему ценностей - вот некоторые из многих характеристик сознания. Сознание позволяет нам иметь дело с трудными условиями среды (адаптация). О мозговой активности, ассоциированной с сознанием и контролируемой вниманием (СКОВ, см. далее), известно так немного, однако мы знаем, что подкорковые активационные системы, такие как ретикулярная формация и кортикостриарные системы, тормозящие афферентные сигналы к коре и таламусу, играют в этом важную роль.
Внимание. Сенсорные стимулы, поступающие в сенсорную память, оцениваются и сравниваются с содержимым долговременной памяти в течение долей секунды. В обычных ситуациях, таких как вождение автомобиля в уличном потоке транспорта, эти стимулы обрабатываются бессознательно (автоматическое внимание) и не взаимодействуют с другими последовательностями стимулами, например беседа с пассажиром. Наше сознательное, избирательное (управляемое) внимание стимулируется новыми или неопределенными стимулами, реакции на которые (например, установление приоритетов) контролирует обширная часть мозга, называемая системой контроля с ограниченными возможностями (СКОВ). Однако наша способность к избирательному вниманию ограничена, и обычно данная система используется только в стрессовых ситуациях.
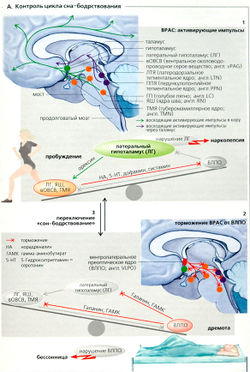
Сознание и внимание связаны с состоянием бодрствования и поддерживается ретикулярной формацией ствола мозга с помощью сложного ансамбля нейронов, которые передают неспецифические восходящие активационные импульсы через таламус в обширные области переднего мозга: восходящая ретикулярная активирующая система (ВРАС, А1). Медиатором в этой системе является ацетилхолин (АХ) из медиального парабрахиального ядра (ядра Кёлликера-Фузе), латеродорзального и педункулопонтийного тегментальных ядер (А1, ЛТЯ, ППЯ). Наряду с холинергической системой существует также моноаминергическая система, образованная голубым пятном с медиатором норадреналином (НА), ядрами шва с медиатором серотонином (= 5-гидрокситриптамин, 5-ГТ), центральным серым веществом (А) с дофамином и туберомаммиллярным ядром (ТМЯ) с гистамином в роли медиатора. Во время бодрствования эта система высокоактивна (см. таблицу) и переход между сном и пробуждением осуществляется в гипоталамусе (ЛГ), где медиатор орексин (= гипокретин) активирует аминергическую систему (А).
Сон - это физиологический процесс восстановления, регулярно повторяющийся ночью. Суточный ритм ассоциирован с изменением уровня сознания. Так, парадоксальный сон (сон с БДГ, или REM-фаза) существенно отличается от медленного сна (сон без БДГ, NREM-фаза) . Эти формы сна являются взаимоисключающими, например спящий мозг способен либо обрабатывать ощущения, поступающие из эндогенных источников (сон с БДГ, REM-фаза, с галлюцинаторными иллюзиями; экзогенная чувствительность блокирована), либо воспринимать и (непрерывно) «обдумывать» внешнюю информацию (см. таблицу), но не способен к выполнению обеих этих функций одновременно.
|
Бодрствование |
Без БДГ (NREM) |
БДГ(REM) | |
|
Восприятие |
Активное (внешняя стимуляция) |
Вялое |
Активное (внутренняя стимуляция) |
|
Мышление |
Логическое, прогрессивное |
Логическое, устойчивое |
Алогичное |
|
Активность двигательной системы |
Непрерывная, произвольная |
Периодическая, непроизвольная |
Мозговые тракты активны, но а-мотонейроны заторможены |
|
Активность ВРАС |
Холинергическая и аминергическая активность ↑↑↑ |
Холинергическая и аминергическая активность ↑ |
Холинергическая ↑↑↑ и аминергическая активность 0 |
|
ЭЭГ |
а, β: высокая частота, низкая амплитуда |
θ, δ: низкая частота, высокая амплитуда |
β: высокая частота, низкая амплитуда |
Сон - это регулируемый процесс. Центральные биологические часы, находящиеся в супрахиазматическом (СХЯ) ядре гипоталамуса, могут синхронизировать его. Во время быстрого сна выключается только аминергическая активирующая система (в то время как холинэргическая система остается активной), однако в фазу медленного сна центральные биологические часы ингибируют обе системы в равной степени (таблица; A, внизу). Ночью СХЯ контролирует нейроны вентролатерального преоптического ядра (ВЛПО). Активация ВЛПО приводит к переключению в состояние сна вследствие ингибирования, а также стабилизации ЛГ и амино-эргической активирующей системы (ГП, ЯШ, вОВСВ, ТМЯ) с помощью медиаторов галанина и гамма-аминобутирата (ГАМК; А, внизу).
Основное значение сна для организма- это сохранение гомеостаза (возобновление энергетических резервов при значительном парасимпатическом влиянии) и консолидация (закрепление) усвоенных процедурных навыков (разговорная речь, двигательные функции, см. далее). Сновидения при этом могут быть включены в процессы консолидации. Сны представлены фрагментарными, эпизодическими воспоминаниями, которые отражают события предшествующих 1-6 дней и эмоционально оформлены. Высокая скорость фазы быстрого сна у детей позволяет предположить, что эта фаза играет немаловажную роль при развитии мозга. У взрослых в течение ночи продолжительность фаз быстрого сна обычно возрастает, и без будильника мы просыпаемся, как правило, во время БДГ (REM-фазы). Общая активность значительно выше при пробуждении из быстрого, а не из глубокого сна, таким образом, еще одно значение REM-фазы состоит в подготовке к пробуждению (стимуляция активности ствола мозга).
Расстройства сна включают (в дополнение к аномалиям ритма сна) гиперсомнию, т.е. сильно повышенную утомляемость днем, несмотря на нормальный сон ночью. Нарколепсия - один из примеров такого нарушения, при котором (как последствие энцефалита или врожденного синдрома Желино) стабилизация ВРАС посредством ЛГ отсутствует (А, внизу). В течение дня случаются внезапные промежутки сна длительностью в несколько минут, если дестабилизированный «переключатель» сон-бодрствование внезапно переключается на сон. Бессонница может быть вызвана многими причинами, включая нарушение ВЛПО (в частности, из-за энцефалита; А, вверху). К парасомниям относят такое поведение во сне, как хождение во сне (сомнамбулизм) или недержание мочи (ночной энурез).
Легкость пробуждения зависит от того, в какую фазу сна оно происходит, и, как правило, мы можем легко вспомнить, что происходило незадолго до того, как мы заснули. Напротив, в бессознательном состоянии, кратковременном (обморок) или длительном (кома), но вызывающем повреждения мозга, дефицит О2 и глюкозы, отравление и т.д., пациента невозможно разбудить, и часто наблюдается ретроградная амнезия (см. далее).
Обучение, память, язык
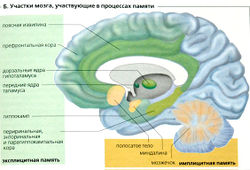
Когнитивная память (имплицитная; Б, коричневый цвет) хранит информацию, связанную с навыками, а также информацию, необходимую для ассоциативного научения (приобретенные, или условные, рефлексы) и неассоциативного научения (активизация рефлекторных путей и безусловные рефлексы). В когнитивной памяти задействованы базальные ганглии (процедурная память, т.е. научение навыкам и приемам), мозжечок (моторные рефлексы, сопряженные с научением), неокортекс (предварительная подготовка, например способность заканчивать фрагменты текстов основана на ранее приобретенных знаниях), моторную (двигательную) кору, миндалевидное тело (эмоциональные реакции) и другие структуры мозга.
Нейрональная циркуляция когнитивной памяти (Б), по-видимому, не зависит от путей сенсорной памяти. Последняя страдает при нарушениях гиппокампа (например, ретроградная амнезия), тогда как имлицитная память продолжает нормально функционировать. И наоборот, атрофия амигдалы, например при болезни Урбаха-Вите, приводит к дефициту эмоциональной памяти (проблемы с интерпретацией и проявлением эмоций).
Декларативная (эксплицитная) память (эрудиция) хранит факты (семантические знания) и опыт (эпизодическая память, особенно при участии селективного внимания) и сознательно их представляет. За хранение информации, обрабатываемой в уни- и полимодальных ассоциативных участках, отвечает височная доля (гиппокамп, околоносовая, внутриносовая и парагиппокампальная кора, и т. д.; Б, зеленый цвет). Там обеспечиваются временной и пространственный контексты опыта; информация повторно откладывается в корешках кортикальных дендритов ассоциативных участков (Г). Частичного повторения опыта бывает достаточно для возвращения содержимого памяти.
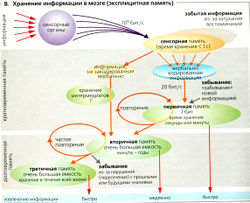
Научение (В) начинается в сенсорной памяти, которая автоматически сохраняет сенсорные сигналы в течение менее чем 1 с. Небольшая часть информации достигает первичной памяти (кратковременной памяти), которая может удерживать около 7 единиц информации (например, серию цифр) в течение нескольких секунд. В большинстве случаев информация также переводится в словесную форму. Длительное хранение информации во вторичной памяти (долговременной памяти) достигается путем повторения (закрепление). Третичная память хранит часто повторяемые впечатления (например, навыки чтения, письма, имя самого человека); эта информация никогда не забывается и легко вспоминается в течение всей жизни.
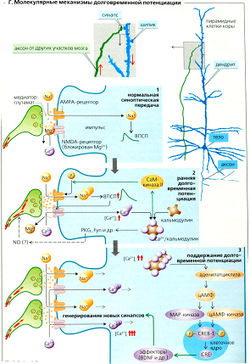
Механизм первичной (кратковременной) памяти, возможно, обеспечивается стимулами, циркулирующими в нервных трактах, а биохимические механизмы принимают участие преимущественно в долговременной памяти. Повторяющееся возбуждение приводит к усилению в течение часов или дней прочности синаптических контактов [долговременная потенциация) на шипиках дендритов коры (Г, вверху). Долговременные геномные перестройки в конечном счете являются результатом этого усиления (поздняя фаза долговременной потенциации). Таким образом в отдельных синапсах синаптическая передача настолько усиливается, что изучаемая информация закрепляется.
Механизмы долговременной потенциации. Ионотропные рецепторы для АМПА (альфа-аминометилизокса-золпропионовая кислота) проницаемы для Na+, но не для Са2+, и активируются глутаматом, высвобождаемым из глутаматэргических аксодендритных синапсов пирамидных клеток коры. Вход Na+ приводит к деполяризации постсинаптической мембраны и происходит нормальный ВПСП (Г1). Глутамат также связывается с ионотропными NMDA (N-methyl-aspartic acid - N-метиласпар-гиновая кислота) рецепторами. Ионные каналы NMDA-рецепторов проницаемы преимущественно для Са2+, но при нормальном ВПСП блокируются Мg2+. Если нейрон дополнительно деполяризован из-за повышенной активности дендритных синапсов, Мд2+ отщепляется, и Са2+ может свободно проникать в клетку. Концентрация Са2+ в цитозоле [Ca2+]j при этом возрастает. Если это происходит достаточно часто, кальмодулин вызывает аутофосфорилирование СаМ-киназы II (Г2), которое происходит даже после того как [Ca2+]j снизится до нормы. СаМ-киназа II фосфорилирует АМРА рецепторы (увеличивает их проводимость) и вызывает их встраивание в постсинаптическую мембрану, тем самым увеличивая синаптическую передачу на более длительный период (ранняя долговременная потенциация). Частые, выраженные изменения в концентрации [Ca2+]j приводят к долговременной пролонгации (поздняя долговременная потенциация), поскольку происходит активация аде-нилатциклазы и повышение уровня сАМР (ГЗ). Киназы сАМР и МАР (белок, активируемый митозом) далее активируют и фосфорилируют факторы транскрипции (CREB = сАМР response element binding protein) в клеточном ядре. В свою очередь они активируют промоторы (CRE) и тем самым синапсы, находящиеся в неактивном состоянии, мобилизуются, и синтезируются новые необходимые белки.
Речь служит способом коммуникации (1) для получения информации через зрительные и слуховые каналы (и через тактильные каналы у слепых) и (2) для передачи информации в письменной и устной форме. Речь также необходима для образования вербальных понятий и стратегий на основе сознательно обрабатываемого сенсорного восприятия. Таким образом, воспоминания могут эффективно сохраняться. Центры образования и обработки понятий и речи распределены по полушариям мозга неравномерно. У праворуких людей [«доминирующее» полушарие, большая височная поверхность) центр речи находится обычно в левом полушарии, тогда как правое полушарие является доминантным у 30-40% всех левшей. Недоминантное полушарие играет важную роль для распознавания слов, напевания мелодии, а также для множества невербальных способностей (например, музыкальных, к пространственному мышлению, распознаванию лиц).
Это можно проиллюстрировать на примере пациентов, у которых два полушария хирургически разделены из-за таких причин, как неизлечимая другим способом тяжелая эпилепсия. Если такой пациент с расщепленным мозгом касается объекта правой рукой (что передается левому полушарию), то он может назвать этот объект. Если, однако, он касается объекта левой рукой (правое полушарие), то не может назвать объект, но может указать на картинку, изображающую данный объект. Поскольку полное разделение полушарий ведет к множеству других нарушений, этот тип хирургического вмешательства используется только для пациентов с очень тяжелыми приступами, с которыми нельзя справиться другим способом.
Амнезия (потеря памяти). Ретроградная амнезия (потеря памяти о последних событиях) характеризуется потерей первичной памяти и временными затруднениями при припоминании информации, сохраняемой во вторичной памяти, что может развиться по различным причинам (контузия, электрошок и т. д.). Антероградная амнезия характеризуется неспособностью к усвоению новой информации, т. е. к ее хранению в доступном для извлечения виде (во вторичной памяти). Это состояние известно как 348 синдром Корсакова, или амнестический синдром; чаще всего диагностируется у алкоголиков.
Глия
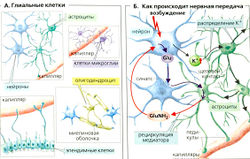
Центральная нервная система содержит около 1011 нейронов и в 10 раз больше глиальных клеток, таких как олигодендроциты, астроциты, эпендимные клетки и микроглия (А). Олигодендроциты (ОДЦ] формируют миелиновую оболочку, окружающую аксоны ЦНС (А].
Астроциты [АЦ] ответственны за внеклеточный гомеостаз К+ и Н+ в ЦНС. Нейроны высвобождают К+ в ответ на высокочастотную стимуляцию (Б). Астроциты предотвращают увеличение концентрации К+ в межклеточном пространстве и, следовательно, нежелательную деполяризацию нейронов в случае поглощения К+; то же самое происходит и с ионами Н+. Поскольку АЦ соединены щелевыми контактами, они могут передавать К+ или Н+ близлежащим астроцитам (Б). Кроме формирования барьера, предотвращающего абсорбцию медиаторов из одного синапса другим, АЦ также поглощают медиаторы, например глутамат (Glu). Внутриклеточный глутамат превращается в глутамин (GluNh2, который затем транспортируется из клетки и поглощается нервными клетками, где превращается обратно в Glu (рециркуляция медиатора; Б).
Некоторые АЦ имеют рецепторы для нейромедиаторов, например для Glu, которые запускают Са2+-волны от одного астроцита к другому. Астроциты также способны изменять концентрацию Са2+ в цитозоле нейронов, так что два типа клеток могут «общаться» друг с другом. АЦ также опосредуют транспорт веществ между капиллярами и нейронами и играют важную роль в энергетическом гомеостазе нейронов за счет опосредования синтеза и распада гликогена.
В период эмбрионального развития длинные отростки астроцитов служат направляющими структурами, которые помогают недифференцированным нервным клеткам мигрировать в нужные участки. Глиальные клетки также играют важную роль в развитии ЦНС, помогая контролировать экспрессию генов в кластерах нервных клеток при помощи ростовых факторов, таких как ФРН (ростовой фактор нервов), BDGF (ростовой фактор мозгового происхождения], GDNF (глиальный нейротропный фактор), или без них. GDNF служит также трофическим фактором для всех зрелых нейронов.
Деление глиальных клеток может вести к образованию рубцов (эпилептические очаги) и к образованию опухолей (глиом).
Иммунокомпетентная микроглия (А) вне ЦНС принимает на себя многие функции макрофагов при повреждениях или инфекции ЦНС. Эпендимные клетки выстилают внутренние полости ЦНС (А).