Синтез АТФ
Содержание
- 1 Анаэробный синтез АТФ: субстратное фосфорилирование, синтез АТФ из фосфокреатина, аденилаткиназная реакция
- 1.1 АТФ (аденозинтрифосфат): молекула, обеспечивающая энергией живые клетки
- 1.2 Синтез АТФ путем субстратного фосфорилирования
- 1.3 Получение АТФ из фосфокреатина
- 1.4 Креатин выводится в форме креатинина
- 1.5 Прием креатина повышает работоспособность
- 1.6 Образование АТФ из АДФ под действием аденилаткиназы
- 2 Аэробный синтез АТФ
- 3 Биосинтез АТФ путем окислительного фосфорилирования (часть I)
- 4 Биосинтез АТФ путем окислительного фосфорилирования (часть II)
- 5 Источники
Анаэробный синтез АТФ: субстратное фосфорилирование, синтез АТФ из фосфокреатина, аденилаткиназная реакция[править | править код]
АТФ (аденозинтрифосфат): молекула, обеспечивающая энергией живые клетки[править | править код]
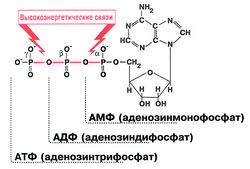
Молекулы АТФ жизненно необходимы. АТФ служит источником энергии, необходимой для сокращения мышц, проведения нервного импульса, протекания многих биохимических реакций и т.п. В покое расходуется 28 г (1 унция) АТФ в минуту, что эквивалентно 1,4 кг (3 фунта) в час, а при физической нагрузке расход АТФ достигает 0,5 кг в минуту! АТФ состоит из аденина, рибозы и трех фосфатных групп, которые называются а-, β- и у-фосфатными группами (рис. 10.1). Гидролиз высокоэнергетических фосфоангидридных связей между β- и у-атомами фосфора или между а- и β-атомами фосфора высвобождает энергию, необходимую для проведения биохимических реакций, т.е. для поддержания жизни организма.
Самый энергетически выгодный метод синтеза АТФ — это аэробное окислительное фосфорилирование. Однако АТФ может также образоваться в анаэробных условиях, хотя и с меньшей эффективностью. Существует три способа анаэробного синтеза АТФ: субстратное фосфорилирование, образование АТФ из фосфокреатина и в результате аденилаткиназной реакции. Хотя анаэробный синтез АТФ и не так энергетически выгоден, способность синтезировать АТФ в бескислородной среде может иметь жизненно важное значение.
Синтез АТФ путем субстратного фосфорилирования[править | править код]
На рис. 10.2 показано, что АТФ образуется в процессе гликолиза в ходе фосфоглицераткиназной и пируваткиназной реакций, а также в цикле Кребса в ходе реакции, катализируемой ферментом сукцинил-КоА-синтетазой с участием нуклеозидцифосфаткиназы (рис. 10.3). Примечание: для этих реакций кислород не требуется.
Получение АТФ из фосфокреатина[править | править код]
Фосфокреатин — это «аварийный запас» высокоэнергетического фосфата, который можно использовать для быстрого образования АТФ, необходимого для сокращения мышц в анаэробных условиях. Этот интенсивный механизм синтеза АТФ может в экстренных ситуациях спасти жизнь; однако запасы фосфокреатина расходуются очень быстро, всего за несколько секунд.
В периоды покоя, когда молекул АТФ много, креатинкиназа фосфорилирует креатин с образованием фосфокреатина. Особенно важна роль этой реакции в мышцах. Если вдруг требуется сделать резкий рывок, фосфокреатин фосфорилирует АДФ до АТФ, необходимого для сокращения мышц (рис. 10.4) По этой причине фосфокреатин еще называют «фосфаген».
Креатин выводится в форме креатинина[править | править код]
Креатин — это аминокислота, не входящая в состав белков. Креатин синтезируется из аргинина и выводится с мочой в форме креатинина. Уровень креатинина в крови и клиренс креатинина используются для оценки скорости клубочковой фильтрации при нарушении работы почек. Примечание: не путайте креатин, креатинин и карнитин.
Прием креатина повышает работоспособность[править | править код]
Эргогенные средства — это вещества, которые повышают скорость, силу или выносливость спортсмена. Многие из них опасны и запрещены к использованию. Мнения противоречивы, тем не менее многие ученые сходятся на том, что креатин — единственное эргогенное средство, для которого научно доказано его свойство повышать работоспособность как при спринтерских, так и при продолжительных нагрузках.
Образование АТФ из АДФ под действием аденилаткиназы[править | править код]
После того как АТФ гидролизуется для высвобождения энергии, необходимой для сокращения мышц, в клетках образуется и накапливается АДФ. Но АДФ тоже содержит энергоемкую а-фосфоангидридную связь (рис. 10.1). Природа изобретательна: эта энергия становится доступной после того, как в анаэробных условиях две молекулы АДФ под действием аденилаткиназы образуют АТФ (рис. 10.5) (раньше фермент аденилаткиназу называли миокиназой).
Аэробный синтез АТФ[править | править код]
Синтез АТФ в дыхательной цепи путем окислительного фосфорилирования[править | править код]
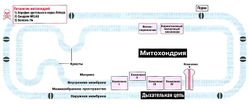
Митохондрия[править | править код]
Митохондрия — это органелла, по размеру сопоставимая с бактериальной клеткой. Примечательно, что у митохондрии есть две мембраны. Наружная мембрана пронизана молекулами порина. Порины образуют каналы, по которым через мембрану могут проходить молекулы с массой менее 10 кДа. Внутренняя мембрана ПРАКТИЧЕСКИ непроницаема; она образует впячивания — кристы. Через внутреннюю мембрану свободно проходят только небольшие молекулы — вроде Н20 и NH3. Лишь немногие другие молекулы с помощью белков-переносчиков и челночных систем способны преодолеть этот барьер.
Считается, что митохондрия — пример эндосимбиоза. Внутренняя мембрана митохондрии с заключенным в ней содержимым когда-то была древней анаэробной бактерией, которая проникла в примитивную клетку на ранних этапах эволюции. Сохранились и следы прошлого: так, митохондрия имеет свою собственную ДНК (мтДНК), кодирующую 37 генов. 24 из них участвуют в трансляции мтДНК, остальные кодируют белки дыхательной цепи. Примечательно, что только 13 из всех белков митохондриальной дыхательной цепи (а всего их более 85) закодированы в мтДНК. Остальные кодирует ядерная ДНК, и они транспортируются в митохондрию из цитоплазмы.
Дыхательная цепь[править | править код]
Дыхательная цепь — эффективный путь получения АТФ с использованием НАДН и ФАДН2, которые образуются в процессе окисления метаболического «топлива» [прежде всего углеводов и жирных кислот]. Дыхательная цепь состоит из пяти комплексов — I, II, III, IV и сложного комплекса грибовидной формы (комплекс V). Грибовидный «мультикомплекс» состоит из субъединиц F1 (субъединица «один») и F0 (субъединица «О», связывает олигомицин). Некоторые из комплексов дыхательной цепи содержат цитохромы, которые транспортируют электроны по цепи: комплекс III содержит цитохром b, а комплекс IV — цитохром а/аЗ. Кроме того, в транспорте электронов принимают участие убихинон (кофермент Q10) и цитохром С. Все комплексы дыхательной цепи расположены во внутренней мембране митохондрий. Комплексы I, III и IV не только переносят электроны, но также выполняют функцию молекулярных протонных насосов: они «выкачивают» протоны из матрикса в межмембранное пространство. Внутренняя мембрана непроницаема, в частности, она непроницаема для протонов, поэтому они возвращаются в матрикс только одним путем — через протонный канал комплекса F1/F0, который в этот момент синтезирует АТФ.
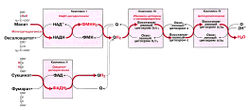
Поток электронов упрощенно показан на рис.
Патологии митохондрий[править | править код]
Существуют различные нарушения дыхательной цепи. Многие из них наследственно передаются по материнской линии, поскольку все митохондрии зиготы происходят из митохондрий яйцеклетки. При делении клетки тысячи молекул мтДНК случайным образом распределяются между дочерними клетками, поэтому разные ткани могут содержать как нормальные, так и мутантные молекулы мтДНК (это состояние называется гетероплазмией). Вследствие этого клиническая картина при таких патологиях очень изменчива. Мутации в ядерных генах, кодирующих белки дыхательной цепи, передаются по аутосомному типу и обычно вызывают более тяжелые нарушения.
Атрофия зрительного нерва Лебера[править | править код]
Атрофия зрительного нерва Лебера вызывается мутацией участка митохондриальной ДНК, который кодирует одну из субъединиц комплекса I. От этого нарушения дыхательной цепи митохондрий сильнее всего страдает, по-видимому, зрительный нерв. Болезнь проявляется во взрослом возрасте и приводит к потере зрения.
Митохондриальная энцефаломиопатия, лактацидоз и инсультоподобные эпизоды (синдром MELAS)[править | править код]
Причина синдрома MELAS — мутация гена мтДНК, кодирующего лейциновую транспортную РНК митохондрий. Эта мутация влияет на трансляцию мтДНК, и поэтому при синдроме MELAS нарушена структура всех комплексов дыхательной цепи, кроме комплекса II, который полностью кодируется ядерным геномом.
Болезнь Ли[править | править код]
Болезнь Ли — дегенеративное заболевание центральной нервной системы с характерными патологическими изменениями. Обычно развивается в раннем возрасте. Заболевание генетически гетерогенно: чаще всего причиной болезни являются мутации участков ядерных геномов, кодирующих компоненты дыхательной цепи, однако в некоторых случаях болезнь Ли развивается из-за мутаций митохондриальных генов. При болезни Ли может быть нарушена активность АТФ-синтетазы (комплекса V) или комплексов I, II, III, IV. При некоторых формах болезни Ли имеют место нарушения активности пируватдегидрогеназного комплекса.
Недостаточность пируватдегидрогеназного комплекса приводит к повышению в крови концентраций пирувата, лактата и аланина. У некоторых больных наблюдается улучшение состояния при приеме липоевой кислоты или тиамина (коферментов пируватдегидрогеназного комплекса). С ограниченным успехом применяется лечение кетогенной низкоуглеводной диетой. (Кетоновые тела легко проходят гематоэнцефалический барьер, и при их катаболизме образуется ацетил-КоА независимо от пируватдегирогеназного комплекса.)
Биосинтез АТФ путем окислительного фосфорилирования (часть I)[править | править код]
Биосинтез АТФ в дыхательной цепи, в котором принимает участие как поток электронов (е-), так и поток протонов (Н+), происходит путем окислительного фосфорилирования. Дыхательная цепь состоит из четырех комплексов (I, II, III, IV) и структуры грибовидной формы — АТФ-синтаза с субъединицами F0/F1 или комплекса V, который синтезирует АТФ из АДФ и неорганического фосфата (Фн). Ниже будет рассмотрено, как создается поток электронов и протонов в дыхательной цепи: первый начинается от комплекса I, второй — от комплекса II.
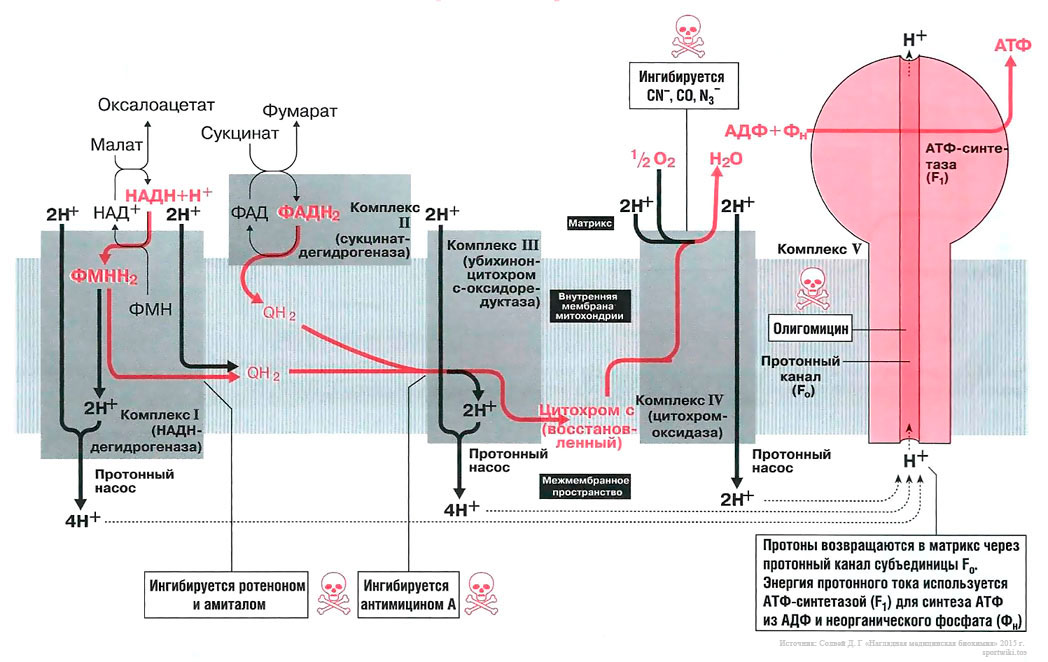
Комплекс I[править | править код]
Поток электронов начинается от НАДН. Энергия для синтеза АТФ возникает благодаря разделению зарядов в комплексе I, которое вызывает движение электронов (электрический ток) и протонов (протонный ток). Молекулярный насос комплекса I выкачивает четыре протона в межмембранное пространство. Другие комплексы (III и VI) тоже выкачивают протоны в межмембранное пространство, и образуется электрохимический градиент протонов; в конечном итоге все эти протоны возвращаются обратно через протонный канал АТФ-синтазы (см. ниже). В комплексе I электроны переносятся с НАДН на убихинон (кофермент Q). Два электрона и два протона восстанавливают убихинон до убихинола (QH2), и убихинол движется в толще мембраны к комплексу III.
Комплекс II[править | править код]
Поток протонов начинается от ФАДН2. Комплекс II содержит ФАД в виде простетических групп нескольких дегидрогеназ (например, сукцинатдегидрогеназы). Этот ФАД восстанавливается до ФАДН2. Далее комплекс II передает электроны убихинону (Q) для последующего переноса электронов к комплексу III. Примечание, комплекс II не выкачивает протоны.
Комплекс III[править | править код]
В роли донора электронов выступает убихинол QH2, который при этом окисляется до убихинона Q и в этом виде может возвращаться обратно и принимать следующую пару электронов и протонов. Убихинол передает электроны на цитохром, который транспортирует их в комплекс IV. Протонный насос комплекса III выбрасывает 4 протона в межмембранное пространство.
Комплекс IV[править | править код]
Электроны, поступившие от цитохрома с, передаются кислороду, и кислород полностью восстанавливается с образованием воды. Комплекс IV выбрасывает в межмембранное пространство только 2 протона.
АТФ-синтаза (комплекс V)[править | править код]
Этот комплекс состоит из «ножки гриба» — субъединицы F0, содержащей протонный канал, и из «выпуклой части» — АТФ-синтазы (или F1). Субъединица F0 получила свое название благодаря тому, что она ингибируется олигомицином, а субъединица F1 была первой открытой и выделенной «фракцией» среди всех элементов дыхательной цепи. Поток протонов проходит через протонный канал и запускает молекулярный двигатель, который заставляет АДФ и Фн реагировать друг с другом, образуя молекулы АТФ.
Чтобы синтезировать одну молекулу АТФ и транспортировать ее в цитозоль, требуется 4 протона. При окислении 1 молекулы НАДН+ высвобождается 10 протонов, энергия которых достаточно для образования 2,5 молекул АТФ. При окислении 1 молекулы ФАДН2 высвобождается 6 протонов, энергии которых достаточно для синтеза 1,5 молекул АТФ[1].
Утечка электронов приводит к образованию активных форм кислорода[править | править код]
Примерно 2% электронов высвобождаются из дыхательной цепи и связываются непосредственно с кислородом, образуя активные формы кислорода (АФК). Если работа дыхательной цепи нарушена, АФК образуются в большем количестве. Эти вещества повреждают митохондрии, вызывая все большие нарушения дыхательной цепи. Возникает порочный круг, и в результате из-за накопления различных повреждений под действием АФК происходит старение клетки.
Дыхательные яды[править | править код]
Вещества, которые ингибируют образование АТФ, потенциально токсичны для организма.
Амитал и ротенон блокируют транспорт электронов в комплексе I. Ротенон выделяют из корней растения деррис (Derris scandens) и нередко используют в качестве природного пестицида. Он малотоксичен для человека, поскольку плохо всасывается в желудочно-кишечном тракте. Однако ротенон ядовит для рыб, так как быстро всасывается через жабры. К тому же при долговременном воздействии ротенон опасен и для человека, так как вызывает развитие болезни Паркинсона.
Антимицин блокирует транспорт электронов в комплексе III.
Цианиды(CN-), угарный газ (СО) и азиды (N3-) ингибируют комплекс IV. Поэтому при отравлении цианидом блокируются аэробные метаболические процессы, несмотря на то что кровь достаточно насыщена кислородом. Из-за остановки аэробного метаболизма венозная кровь принимает цвет артериальной крови. Кроме того, наблюдается гипервентиляция, поскольку из-за накопления молочной кислоты стимулируется дыхательный центр.
Олигомицин блокирует протонный канал (F0 в комплексе V) и не дает протонам возвращаться в матрикс. Поэтому АТФ-синтаза (F1) теряет способность синтезировать АТФ.
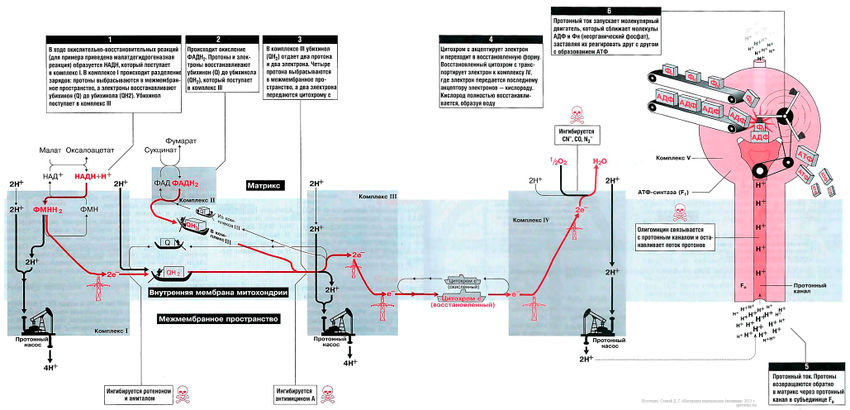
Биосинтез АТФ путем окислительного фосфорилирования (часть II)[править | править код]
На рис. 13.1 показан поток электронов и протонов в дыхательной цепи. Электроны и протоны от НАДН+ через комплекс I и от ФАДН2 через комплекс II передаются комплексу III. Затем электроны транспортируются в комплекс IV, где они присоединяются к кислороду. В это время протоны выкачиваются протонными насосами из матрикса в межмембранное пространство и возвращаются обратно в матрикс через протонный канал F0-субъединицы АТФ-синтазы (комплекс V). Поток протонов (протонный ток) включает молекулярным двигатель — F1-субъединицу АТФ-синтазного комплекса, и она располагает молекулы АДФ и Фн таким образом, что они объединяются в молекулы АТФ.
Источники[править | править код]
- ↑ В отечественных учебниках биохимии принято считать эти значения равными «3» и «2» соответственно, т.е. при окислении 1 молекулы НАДН образуется 3 молекулы АТФ, а при окислении ФАДН2 — 2 молекулы АТФ, что отражает теоретический максимум синтеза АТФ.