Скелетно-мышечные болевые синдромы
Источник: «Боль в спине»
Автор: Авторы: Подчуфарова Е.В., Яхно Н.Н. 2013.
Содержание
Скелетно-мышечные болевые синдромы[править | править код]
Миогенные болевые синдромы[править | править код]
Определенные трудности вызывает терминология, применяемая для описания состояния мышц - источников боли. В руководстве для специалистов по боли, изданном Международной ассоциацией по изучению боли, отмечено, что термин «миофасциальная боль» можно применять как в широком значении, включающем все виды мышечной боли, так и в узком, когда обязательно выявление ТЗ в мышцах [J. Charlton, ред., 2005]. При этом минимально необходимым для диагностики ТЗ считают локальную болезненность в пределах пальпируемого тяжа в мышце и воспроизводимость спонтанной боли при его пальпации. В отечественной литературе традиционно выделяют мышечнотонический и МФБС, истоки которого восходят к работам Я.Ю. Попелянского, который среди «заболеваний мышц от перенапряжения» выделял «нервно-мышечный спазм» (мышечно-тонический синдром), «миалгии», «миогелоз», «миофиброз», «невромиозиты» («мышечнодистрофические» синдромы) [Я.Ю. Попелянский, 1974]. «Мышечно-дистрофические» синдромы по основным клиническим характеристикам соответствуют описаниям МФБС в англоязычной литературе.
Очень часто невозможно отличить боль, исходящую из сустава, от боли, обусловленной повреждением мышц или их сухожилий, связанных с суставом. В частности, воспалительные изменения, затрагивающие сустав, часто распространяются и на прилежащие к нему мягкие ткани, включая мышцы. Распространенные болевые синдромы выявляют у 20-25% пациентов, страдающих ревматоидным артритом или системной красной волчанкой. Альгогенные вещества, такие, как брадикинин, серотонин, простагаландины, выделяющиеся при воспалении суставов, имеют большое значение в формировании мышечной боли. Патология сустава может вызывать перегрузку мышц, которая приводит к формированию локальной мышечной боли. Так, например, травма медиальных отделов коленного сустава, которую часто диагностируют у пациентов с остеоартрозом, вызывает боль в сухожилиях мышц, формирующих «гусиную лапку»: портняжной, тонкой и полусухожильной. Интенсивная и особенно необычная для мышцы нагрузка может стать причиной развития в ней боли. Известно, что определенный характер труда приводит к увеличению частоты возникновения болей в спине, связанных с перегрузкой тех или иных мышечных групп. Операторы швейных машин, например, обычно страдают от болей в шейном отделе позвоночника и плечевом поясе.
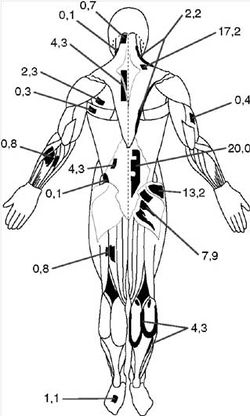
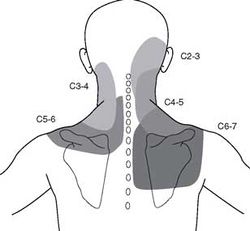
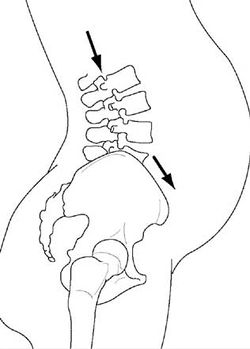
Мышечная боль может ощущаться локально в отдельных частях пораженной мышцы; распространяться на всю мышцу и ощущаться в областях, расположенных на расстоянии от пораженной мышцы (отраженная боль). Типично мышечную боль пациенты описывают как «ноющую», «сжимающую», «тянущую», «сверлящую», «разлитую». Паттерны боли, отраженной от мышц, детально описаны J.G. Travell и D.G. Simons (1989) и наиболее стабильно воспроизводятся при исследовании мышц плечевого пояса. Миогенная боль наиболее выражена при нагрузке на пораженную мышцу. Она также может возобновляться при нагрузке на мышцу после ее отдыха, например после сна. Часто это сопровождается ощущением скованности в мышце и необходимостью разогреть и разработать ее для уменьшения болезненности и скованности при движениях. В отличие от суставной боли мышечная, как правило, возобновляется или усиливается при возрастании нагрузки на мышцу. Другим вариантом развития мышечной боли считают боль в покое, которая значительно усиливается после физической нагрузки («непереносимость нагрузки») и отмечается у пациентов с фибромиалгией. При этом боль, обусловленная с «непереносимостью нагрузки», может сохраняться в течение нескольких дней, затрудняя физическую реабилитацию пациента. Доказано, что большая болезненность отмечается в так называемых статических (тонических) мышцах, находящихся в состоянии длительного напряжения для поддержания определенного положения тела (несущих позную нагрузку). Примером такой «статической» мышцы можно считать надостную. В отличие от «статических», «фазические» мышцы включаются только при необходимости выполнения движения. Пример «фазической» мышцы - четырехглавая мышца бедра, которая задействуется только при динамической нагрузке. Даже у здорового человека с высокой частотой можно выявить болезненность и уплотнения при пальпации «статических» мышц [S. Clemmesen, 1938; P. Croft и др., 1994] (Рис. 1), что следует учитывать при обследовании больных.
Боль в мышцах может быть локальной и распространенной. Состояние, для которого характерна локальная боль в мышце, сопровождающаяся формированием отраженной боли, - МФБС. К формированию распространенной боли в мышцах приводят системные заболевания соединительной ткани, полимиозит, фибромиалгия. Основной проблемой в идентификации мышцы в качестве источника боли в спине считают невозможность ни по локализации, ни по характеру боли точно определить, является ли мышца непосредственным источником локальной боли, или она включается рефлекторно вместе с развитием отраженной боли. Даже полное клиническое обследование не всегда позволяет решить этот вопрос. Примером можно считать боль в подвздошной и паховой области, связанную со спазмом подвздошно-поясничной мышцы, которая включается в патологический процесс при афферентации от пораженных органов брюшной полости или забрюшинного пространства (например, при формировании ретроперитонеального абсцесса). При этом напряженная мышца сама может становиться значимым источником болевой импульсации, маскируя соматическую патологию. Локальная болезненность мышц при пальпации может быть проявлением как периферической (при локальной боли), так и центральной сенситизации. Примерами первого состояния считают локальную боль при пальпации ТЗ при МФБС, второго - боль, возникающую при пальпации «чувствительных» зон при фибромиалгии.
Боль в мышцах отмечается и при соматических заболеваниях. В табл. 1 приведены лабораторные методы обследования, необходимые для исключения соматического заболевания в качестве причины боли в мышцах [H. Bliddal, M. Curatolo, 2008].
Таблица 1. Лабораторные методы обследования, необходимые для исключения соматического заболевания в качестве причины боли в мышцах
|
Изменение лабораторных показателей |
Возможное заболевание, симптомом которого стала боль в мышцах |
|
Снижение концентрации гемоглобина и увеличение количества лейкоцитов в крови |
Анемия, лейкоз |
|
Увеличение СОЭ, наличие С-реактивного белка |
Системные воспалительные заболевания (ревматическая полимиалгия, васкулит, полимиозит) |
|
Повышение активности креатинфосфокиназы |
Миозит |
|
Повышение активности амилазы |
Панкреатит |
|
Повышение активности печеночных трансаминаз |
Гепатит |
|
Повышение титра антител к вирусам гепатита В и С, гриппа, аденовирусам, коксакивирусам. вирусу Эпштейна-Барра, ВИЧ, T-клеточному лимфотропному вирусу I типа |
Миалгии при инфекционных гепатитах, гриппе, аденовирусной инфекции, инфицировании вирусами Коксаки, вирусом Эпштейн-Барра, полимиозит, связанный с ВИЧ-инфекцией, с инфицированием T-клеточным лимфотропным вирусом I типа |
|
Снижение или увеличение концентрации тиреотропного гормона в крови Повышение активности щелочной фосфатазы |
Гипо- и гипертиреоз Заболевания костного мозга, злокачественные новообразования |
|
Снижение концентрации кальция в крови |
Гипопаратиреоз |
Патофизиология миогенной ноцицепции
В отличие от боли, обусловленной раздражением кожи, миогенная боль менее четко локализуется. Возможное объяснение этого состоит в том, что ноцицептивные нейроны заднего рога спинного мозга, получающие афферентацию от мышц, имеют большее рецептивное поле по сравнению с ноцицептивными нейронами, связанными с кожными рецепторами. Кроме того, плотность болевых рецепторов в мышечной ткани меньше, чем в коже. В экспериментах на животных доказано, что если рецептивное поле полимодальных кожных ноцицепторов составляет менее 2 мм2, то в мышце оно может превышать 1 см2. Морфологически ноцицепторы относят к свободным нервным окончаниям. Диаметр свободного нервного окончания составляет 0,5-1 мкм. Кроме ноцицепторов, к свободным нервным окончаниям относят термо-рецепторы и низкопороговые механорецепторы. В мышце выделены высокопороговые механочувствительные рецепторы, для возбуждения которых необходимо воздействие, повреждающее ткани. Они связаны как с маломиелинизированными (A-δ), так и с немиелинизированными (С) нервными волокнами. Также обнаружены хемоноцицепторы, активирующиеся при ишемии, вызванной сдавлением мышцы. Клиническим примером активации этого типа ноцицепторов можно считать боль в икроножных мышцах при перемежающейся хромоте, обусловленной облитерирующим поражением сосудов ног. В мышцах также выделяют полимодальные ноцицепторы, которые активируются в ответ на интенсивную стимуляцию давлением и воздействие альгогенных веществ [S. Mense, U. Hoheisel, 2008]. Мало известно о рецепторах к различным молекулам на поверхности мышечных ноцицепторов. Предполагают, что они имеют рецепторы к воспалительным веществам (брадикинину, серотонину, простагландину Е2), протонам, аденозинтрифосфату (АТФ), факторам роста (фактору роста нервов), возбуждающим аминокислотам (глутамату). Для состояний, характеризующихся хронической болью в мышцах, большое значение имеют протон-чувствительные рецепторы, активирующиеся при снижении pH ткани, что наблюдают при длительной работе мышцы с повышением концентрации молочной кислоты, при ишемии и воспалении. Повторное введение в мышцу растворов с малым pH приводит к появлению длительно сохраняющейся гипералгезии. Кроме того, практически при всех патологических состояниях, сопровождающихся болью в мышцах (воспаление, длительное тоническое сокращение, формирование миофасциальных ТЗ) отмечается снижение pH в мышечной ткани. Другими рецепторами, потенциально значимыми для клинических расстройств, считают рецепторы к АТФ (пуринергический рецептор P2X3). АТФ в значительном количестве выделяется при повреждении миоцитов как при острой травме, так и при хронических состояниях (полимиозите, наследственных миопатиях), сопровождающихся некрозом мышечных волокон. Третий значимый рецептор - TrkA (tropomyosin-related kinase A - тропомиозинсвязанная киназа А), связывающийся с фактором роста нервных волокон. Этот фактор имеет значение при хронических болевых синдромах, поскольку участвует в формировании как периферической, так и центральной сенситизации. Фактор роста нервных волокон синтезируется в мышце. Под его воздействием происходит активация ноцицепторов С-волокон. При инъекции фактора роста нервных волокон в мышцу спонтанная боль не возникает, поскольку в этом случае афферентация по С-волокнам вызывает возбуждение небольшого количества нейронов заднего рога спинного мозга с относительно невысокой частотой или приводит к генерации в них подпороговых синаптических потенциалов. При этом выявлено, что, несмотря на отсутствие спонтанной боли, при введении фактора роста нервов в мышцу в дальнейшем возникают пролонгированная аллодиния и гипералгезия. Этим фактом пытаются объяснить спорное происхождение отдельных мышечных болевых синдромов, в частности боли в мышцах после нагрузки. При травматизации мышцы повторяющимися тоническими сокращениями (даже небольшой интенсивности), например, при длительной игре на музыкальном инструменте, выделение фактора роста нервных волокон и активация ноцицепторов вызывают генерирование низкочастотных разрядов или подпороговых потенциалов в нейронах заднего рога без субъективных неприятных ощущений, но с последующим развитием центральной сенситизации, на которой основано дальнейшее формирование хронического болевого синдрома. Среди альгогенных веществ, напрямую не связывающихся с определенным типом рецепторов, наибольшим активирующим воздействием на ноцицепторы мышц обладают гипертонические растворы солей натрия. Их эффект часто применяют для создания экспериментальных моделей мышечной боли [S. Mense, 2008].
Мышечно-тонические синдромы[править | править код]
Клинические характеристики мышечно-тонических синдромов описаны в работах Я.Ю. Попелянского (1997), В.П. Веселовского (1977), Г.А. Иваничева (2005), Ф.А. Хабирова (2006), А.А. Лиева (1995) и других авторов. По мнению В.П. Веселовского, мышечнотонические синдромы - это повышение тонуса скелетных мышц, которое может быть рефлекторным в ответ на афферентацию от внутренних органов, структур позвоночного столба («висцеромоторные», «остеомоторные» реакции) и миоадаптивным, возникающим при позных или «викарных» перегрузках определенных групп мышц. К позным перегрузкам относят повышение нагрузки на мышцы в зависимости от положения тела (деформации позвоночника, нарушения осанки). Например, при гиперлордотической деформации поясничного отдела позвоночника мышечно-тонические синдромы развиваются в задней группе мышц бедра и передней группе мышц голени. К «викарным» относят перегрузки мышц в ответ на ослабление функции их агонистов или антагонистов, например повышение тонуса в мышцах, отводящих стопу и приводящих бедро при слабости мышц передней поверхности голени при поражении корешка L5. Отечественные авторы выделяют понятие «миофиксация» [Я.Ю. Попелянский, В.П. Веселовский, 1976]. Миофиксация - ограничение движения в позвоночнике и крупных суставах, вызванное напряжением мышц. Миофиксацию разделяют на саногенетическую и патологическую. При саногенетической миофиксации мышечнотонический синдром направлен на иммобилизацию пораженного ПДС. При этом, чем больше напряжение мышц, тем менее выражена спонтанная боль и болезненность при пальпации в ПДС [С.С. Пшик, 1987]. При патологической миофиксации напряжение мышц коррелирует с выраженностью болевого синдрома. Обусловленная формированием мышечно-тонического синдрома миофиксация может быть локальной, когда имеется ограничение движения (блок) в одном ПДС, ограниченной (уменьшение амплитуды движений в шейном и верхнегрудном отделе позвоночника путем сокращения лестничных, трапециевидных, грудино-ключично-сосцевидных, малых грудных, передних зубчатых, ромбовидных мышц, мышцы, поднимающей лопатку, или в нижнегрудном и поясничном отделах позвоночника при напряжении многораздельных, подвздошно-реберных, квадратных мышц поясницы) и распространенной. Последняя характеризуется мышечно-тоническим синдромом не только мышц, обеспечивающих движения позвоночника, но и крупных суставов (мышечно-тонический синдром формируется также в надостной, подостной, дельтовидной, ягодичных, грушевидной и других мышцах) [В.П. Веселовский, 1991, Ф.А. Хабиров, 2002]. Больные с мышечно-тоническими синдромами жалуются на боли в позвоночнике или мышцах плечевого и тазового пояса, уменьшающиеся после отдыха, растирания, разминания и растяжения мышцы. Боль часто носит «стягивающий» характер. Визуально можно определить изменение контура, «выбухание» мышцы, которая при пальпации может иметь повышенную плотность. Произвольные движения с вовлечением спазмированной мышцы совершаются в неполном объеме. Компрессия сосудисто-нервных структур при мышечнотонических синдромах может вызывать иррадиацию боли в конечность, двигательные, чувствительные и вегетативные нарушения, локализующиеся в соответствующих зонах иннервации и васкуляризации. Хронические мышечно-тонические синдромы наиболее часто отмечают в тех мышцах, которые испытывают позные перегрузки, например при асимметрии конечностей, таза, выраженном сколиозе, патологии внутренних органов. Боль при этом, как правило, имеет слабую или умеренную интенсивность. Пациенты предъявляют жалобы на ощущение дискомфорта, тяжести после физической нагрузки, которые уменьшаются после разминания и согревания мышцы. Болезненность в спазмированной мышце возникает при ее активном сокращении и обычно отсутствует при растяжении. Считают, что не все мышцы одинаково подвергаются формированию мышечно-тонического синдрома. Среди мышц тазового пояса и спины наиболее подвержены формированию хронического напряжения трехглавая мышца голени, прямая мышца бедра, напрягатель широкой фасции, грушевидная мышца, квадратная мышца поясницы и все разгибатели позвоночника [Я.Ю. Попелянский, 1997]. В англоязычной литературе наиболее близкий к мышечнотоническому синдрому термин - «мышечный спазм». При перерастяжении и микротравматизации мышцы на фоне ее перегрузки или при длительном вынужденном положении может возникать локальная боль. При этом в ответ на травму происходит сокращение как пораженной мышцы, так и тех мышц, которые ее окружают. Это защитное напряжение мышц обозначают как рефлекторный мышечный спазм [Д.Г. Боренштейн и др., 2005].
Таким образом, важной клинической задачей считают выяснение механизма развития локального длительного мышечного напряжения - патологии внутренних органов, ПДС, движения или длительной неудобной позы, спровоцировавших спазм. Воздействие на основной патологический процесс в этом случае приведет к регрессу и мышечно-тонического синдрома. Примером можно считать рефлекторное развитие мышечно-тонического синдрома грушевидной мышцы при радикулопатии LV или SI, частота которого, по данным Я.Ю. Попелянского, в первом случае составляет 55,3%, во втором - 36,7%. Формирование мышечно-тонического синдрома в данном случае, возможно, обусловлено интенсивной афферентаций от пораженного диска и корешка в соответствующие сегменты спинного мозга и повышением активации мышцы, иннервирующейся соответствующими сегментами спинного мозга. Такое объяснение нельзя считать однозначным, так как, например, в отношении паравертебральных мышц Я.Ю. Попелянский и соавт. (1970) не выявили связи между латерализацией их напряжения и стороной корешкового поражения. Сходные данные получили и другие авторы [Г.К. Недзьведь и др., 1985]. Патологическое напряжение грушевидной мышцы может приводить к сдавлению между ней и крестцово-остистой связкой седалищного нерва и нижней ягодичной артерии. Пациенты обычно жалуются на боль в ягодичной области тянущего характера, которая усиливается при ходьбе, в положении стоя, при сидении на болезненной ягодице. Часто отмечаются парестезии в ноге, усиливающиеся при внутренней ротации бедра, запрокидывании ноги на ногу. Положительна проба Бонне - в положении пациента лежа на животе отмечается болезненность при абдукции согнутой в коленном суставе ноги и ограничение ее внутренней ротации, при которых происходит соответственно растяжение и сокращение грушевидной мышцы. Показано, что если мышечно-тонический синдром грушевидной мышцы сопровождает корешковую компрессию, после оперативного устранения грыжи диска он полностью регрессирует [Я.Ю. Попелянский, 1997]. Мышечно-тонический сидром грушевидной мышцы диагностируют у женщин в 6 раз чаще, чем у мужчин, что связано с большей частотой патологии органов малого таза у женщин, приводящей к формированию «висцеромоторной» реакции [Я.Ю. Попелянский, 1997]. В тех случаях, когда мышечный спазм сохраняется длительное время, изменения в самой мышце, в том числе развитие миофасциальных ТЗ независимо от наличия первичного источника болевой импульсации, могут становиться новыми источниками боли и требуют коррекции.
Часто мышечно-тонический синдром выявляют в мышце, выпрямляющей позвоночник. Он, как правило, обусловлен сопутствующей патологией позвоночных структур - наличием остро развившейся грыжи диска, компрессионной радикулопатии, спондилолистеза. Самостоятельное развитие напряжения мышцы, выпрямляющей позвоночник, без вертебральной патологии в качестве источника боли в спине сомнительно. Обычно остро развивающийся спазм этой мышцы при вертеброгенной патологии бывает безболезненным. В таких случаях он выполняет защитную функцию, иммобилизуя пораженный ПДС. Возможно, когда импульсация от пораженного ПДС сохраняется длительное время, изменения, происходящие в мышце на фоне ее перенапряжения, могут приводить к формированию болевого синдрома в связи с ишемией. Если повреждение мышцы, выпрямляющей позвоночник, возникло вследствие неловкого, резкого движения (сочетания наклона и вращения) в поясничном отделе позвоночника, боль сопровождает мышечный спазм уже на ранних стадиях заболевания. Тем не менее нельзя исключить наличия в этом и подобных случаях патологии ПДС (травмы дугоотростчатых суставов или диска) и «вторичного» рефлекторного вовлечения мышцы, выпрямляющей позвоночник. Боль обычно локализуется в паравертебральной области и значительно ограничивает движения в поясничном отделе позвоночника. Можно отметить, что прикрепление мышцы, выпрямляющей позвоночник, к поперечным отросткам позвонков создает относительно плохой рычаг для разгибания позвоночника. Ее пространственное расположение позволяет создавать при сокращении силу, направленную на сдвиг позвонка кзади, или противодействовать силе, направленной на сдвиг позвонка кпереди, обусловленной воздействием гравитации на поясничный отдел позвоночника. Соответственно, мышечно-тонические синдромы в мышце, выпрямляющей позвоночник, развиваются при дегенеративном спондилолистезе, когда соединительнотканные структуры позвоночника (волокна фиброзного кольца, фронтальная поверхность дугоотростчатых суставов и подвздошно-поясничная связка) утрачивают способность противодействовать силе гравитации. При этом мышце, выпрямляющей позвоночник, противодействует большая поясничная мышца, при сокращении которой к позвоночнику прикладывается сила, направленная на смещение позвонка кпереди. Вместе эти мышцы стабилизируют поясничный отдел позвоночника в сагиттальной плоскости.
Патофизиология мышечно-тонических синдромов[править | править код]
Точные механизмы формирования мышечно-тонических синдромов неизвестны. Мышечно-тонический синдром может выполнять саногенетическую функцию, ограничивая пораженную область от дальнейшего повреждения. Считают, что повышение активности паравертебральных мышц в ответ на боль направлено на повышение стабильности позвоночника и таза. В.П. Веселовским (1977) была предложена теория «миоадаптивных» синдромов, сопровождающих как компрессионные, так и рефлекторные болевые синдромы. При этом миоадаптивные реакции связывали с патологией позвоночника - остеохондрозом.
Определенное значение имеет повышение возбудимости сегментарных спинальных структур в ответ на афферентную импульсацию от раздражения рецепторов синувертебрального нерва в области пораженного диска. К другим рефлекторным механизмам, приводящим к формированию мышечно-тонического синдрома, относят так называемые висцеромоторные реакции в виде спазма мышцы в ответ на афферентацию из пораженного внутреннего органа (висцеросоматический рефлекс) [Я.Ю. Попелянский, 1997; Ф.А. Хабиров, 2002].
При нормальной работе мышц их сокращение чередуется с расслаблением. При этом на восстановление мышцы после сокращения тратится энергия основного обмена [Я.Ю. Попелянский, 1997]. В спазмированной мышце выявлено нарушение микроциркуляции и окислительного метаболизма [А.А. Лиев, 1995; D. Falla, 2008]. В экспериментальных исследованиях на животных на ранней стадии (1-20 сут) формирования миофасциальных ТЗ, которая характеризовалась пролонгированным мышечным сокращением, А.А. Лиевым (1995) при исследовании биоптатов мышц показано сужение артериол и расширение венул. При исследовании через 2 мес была выявлена значительная перестройка микроциркуляторного русла мышцы - сужение просвета артериол, появление извитых артериол, пре- и посткапилляров. При гистологическом исследовании на 1-20-е сутки наблюдения также отмечены функциональные (обратимые) изменения в мышцах и соединительной ткани фасций - активация фибробластов и повышение продукции коллагеновых волокон. При электронной микроскопии выявлено утолщение миофибрилл и увеличение размеров митохондрий. Начиная с 30-х суток наблюдения в мышечных волокнах развивались дистрофические и атрофические изменения, которые сопровождались уплотнением коллагеновых волокон фасций. На более поздних стадиях отмечался распад коллагеновых волокон, при электронной микроскопии обнаружена деструкция саркомеров миофибрилл и образование очагов фиброза. Эти исследования также свидетельствуют в пользу того, что большое значение в развитии миогенной боли имеют нарушения микроциркуляции и метаболизма мышцы [А.А. Лиев, 1995].
К сожалению, общепринятое упрощенное представление об изменении состояния мышечной системы в ответ на болевую стимуляцию - так называемый порочный круг «боль-мышечный спазм-боль» - не получило достаточного подтверждения ни в экспериментальных работах, ни при клинических наблюдениях. Хорошо известно, что изменение активации мышц неоднонаправлено. Если при острой боли в спине существует тенденция к повышению активации паравертебральных мышц [P. Hodges, 2008], то при хронической боли четких паттернов изменения ЭМГ-активации мышц не найдено [A. Alexiev, 1994; M. Cohen, 1986]. При остром повреждении ткани и связанной с ним боли, как правило, отмечают снижение активации глубоких и повышение активации поверхностных мышц спины [P. Hodges, 2008]. Длительно сохраняющиеся изменения состояния паравертебральных мышц приводят к негативным последствиям в виде повышения нагрузки на костные и связочные структуры позвоночника и таза, нарушению выполнения сложных движений в пораженном сегменте. Определенный интерес представляет то, что изменение состояния мышц часто сохраняется, даже если боль полностью регрессирует, и может способствовать ускорению дегенеративных изменений в структурах позвоночного столба и развитию повторных эпизодов боли в спине [H. Greene и др., 2001]. Хорошо известно, что наличие эпизода боли в поясничной области в анамнезе - фактор риска повторного возникновения боли в спине. Доказана связь изменения активации мышц брюшной стенки и снижения площади поперечного сечения многораздельных мышц с развитием повторного эпизода боли в спине [J. Cholewicki и др., 2005; J. Hides и др., 2001].
Предполагают, что изменения мышечного тонуса при хронической боли в спине очень индивидуальны и зависят от различных, часто не связанных собственно с состоянием позвоночного столба, факторов. В активации паравертебральных мышц имеют значение изменения возбудимости моторной и премоторной коры [M. Valeriani и др., 1999; J. Butler и др., 2003], мотонейронов спинного мозга [D. Le Pera и др., 2001; D. Farina, 2008] и изменение чувствительности мышечных веретен [J. Pedersen и др., 1997]. Также предполагают, что нарушение двигательной адаптации после эпизода острой боли в спине может быть связано с психологическими особенностями пациентов, в частности с их представлениями о боли и формирующимся на этой основе болевым поведением. Этот факт может объяснить тесную связь таких факторов риска хронической боли в спине, как наличие эпизодов боли в анамнезе и психологических особенностей (выраженность соматизации и использование неадаптивных стратегий преодоления боли) [P. Hodges, 2008]. Считают, что определенное значение в изменении активности паравертебральных мышц при хронической боли в спине могут иметь и нарушения сенсорного контроля. Пациенты с болью в спине по сравнению со здоровыми испытуемыми чаще ошибаются при выполнении движений в позвоночнике на заданный угол. Также у них отмечают уменьшение постуральных корректирующих реакций при воздействии вибрации на паравертебральные мышцы.
В работе, выполненной под руководством Я.Ю. Попелянского, показана связь активации мышц при поверхностной ЭМГ с нарушением вероятностного прогнозирования при скелетно-мышечных болевых синдромах [М.А. Подольская, 1983, 1986]. Таким образом, предполагают, что наибольший вклад в состояние паравертебральных мышц при боли в спине вносят не спинальные и стволовые механизмы, а более «высшие» центры, осуществляющие интеграцию сенсомоторной информации и организацию движений [Г.А. Иваничев, 2007; P. Hodges, 2008].
Лечение[править | править код]
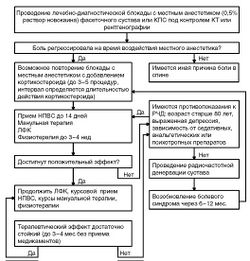
В большинстве случаев корректировать необходимо первичное состояние, вызвавшее формирование мышечно-тонического синдрома. При устранении первичного источника болевой импульсации рефлекторный мышечно-тонический синдром может регрессировать. В тех случаях, когда мышечно-тонические нарушения становятся основным или самостоятельным источником боли, применяют как местное, так и системное лечение. Проводят растяжение, массаж заинтересованной мышцы, воздействие согревающими физиопроцедурами, мануальную терапию, направленную на мобилизацию пораженного ПДС [Ф.А. Хабиров, 2006; Л.Г. Агасаров, 2008]. Целесообразна коррекция двигательного стереотипа, избегание провоцирующих нагрузок и поз. При отсутствии саногенетической роли мышечно-тонического синдрома возможно назначение миорелаксантов, обладающих анальгетическими свойствами, - тизанидина (сирдалуда) в дозе 6-12 мг/ сут (оптимальная доза подбирается путем титрования с 2 мг/сут), толперизона в дозе 300-450 мг/сут, нестероидных противовоспалительных средств (НПВС) [диклофенак (вольтарена) в дозе 100-150 мг/сут, кетопрофен по 100-320 мг/сут, кеторолака (кеторола), лорноксикама (ксефокама) в дозе 8-16 мг/сут и др.]. Несмотря на большой спектр препаратов группы НПВС, достоверных различий в их влиянии на течение боли в спине не выявлено. Соответственно, выбор НПВС в каждом конкретном случае будет определяться индивидуальной переносимостью и спектром побочных явлений. Необходимо отметить, что по данным показаниям НПВС не рекомендуют применять более 10-14 сут. Совместное применение с НПВП тизанидина (сирдалуда) позволяет повысить анальгетическую эффективность последних и снизить риск побочных явлений со стороны желудочно-кишечного тракта. Клинический пример
Пациентка Л., 30 лет, домохозяйка, при уборке квартиры и попытке достать упавший под диван предмет почувствовала острую боль («прострел») в поясничной области, усиливавшуюся при попытках выпрямления туловища. Была вынуждена лечь. Боль в положении лежа не беспокоила, но при попытке перейти в положение сидя или стоя резко усиливалась. На следующий день обратилась за медицинской помощью. Предшествующие эпизоды боли в спине и соматические заболевания в анамнезе отрицает. Соматическое и неврологическое обследование патологии не выявили. При невроортопедическом осмотре при пальпации выявлено болезненное напряжение мышцы, выпрямляющей позвоночник, на поясничном уровне. Флексия в поясничном отделе позвоночника ограничена до 30°, симптомы натяжения не выявлены. Поскольку у пациентки отсутствовали симптомы потенциально опасных заболеваний (не было лихорадки, локальной болезненности и повышения местной температуры в паравертебральной области, беспричинного снижения массы тела; боль в спине уменьшалась в покое; не было анамнестических указаний на травму позвоночника, злокачественное новообразование, внутривенные инфузии, наличие ВИЧ-инфекции и наркомании), дополнительные лабораторные и инструментальные обследования не проводили.
Поставлен диагноз: люмбалгия, мышечно-тонический синдром мышцы, выпрямляющей позвоночник. Пациентке объяснены биомеханические причины развития состояния и его доброкачественность, назначен диклофенак в дозе 100 мг/сут, тизанидин по 6 мг/сут, местно на поясничную область - мазь, содержащая диклофенак, сохранение повседневной активности. При осмотре через 5 сут болевой и мышечно-тонический синдром регрессировали. Рекомендовано ограничение резких движений, плавание.
Клинический пример
Пациент В., 70 лет, пенсионер, обратился с жалобами на выраженную боль в поясничной области ноющего характера, которая возникла без видимой причины примерно 2 нед назад. Ее интенсивность постепенно нарастала, и в последние 2 сут боль в пояснице отмечается ночью и нарушает сон. Она практически не зависит от положения, пациент отмечает лишь кратковременное облегчение при приеме НПВС. Перенесенные заболевания: с 60 лет - ишемическая болезнь сердца (ИБС), стенокардия напряжения I ф.к., гипертоническая болезнь II стадии, в 65 лет диагностирована аденома предстательной железы. При осмотре пациент нормостенического телосложения, в неврологическом статусе, кроме симптомов орального автоматизма и симметричного оживления глубоких рефлексов с конечностей, патологии не выявлено. Отмечалось напряжение мышцы, выпрямляющей позвоночник, на поясничном уровне с обеих сторон, ограничение разгибания и сгибания в поясничном отделе позвоночника (до 10 и 60° соответственно). Выявлена локальная болезненность при пальпации и перкуссии в проекции остистого отростка LIII
Поскольку особенности анамнеза пожилого пациента (сохранение боли в покое в ночное время и отсутствие зависимости ее интенсивности от движения) указывали на возможность наличия у него потенциально опасной патологии, а именно злокачественного новообразования, уже при первом обращении было проведено рентгенографическое исследование пояснично-крестцового отдела позвоночника и общий анализ крови. В последнем выявлено увеличение СОЭ до 42 мм/ч, остальные показатели без патологии. По данным рентгенографии определена нечеткость контуров тела LIII снижение его высоты, субхондральный остеосклероз, снижение высоты межпозвоночных промежутков LIII-LIV LIV-Lp LV-SI, задние остеофиты у нижнего края тел LII и LIII позвонков. Для уточнения данных рентгенографического исследования пациенту была проведена сцинтиграфия скелета, выявившая накопление радиофармпрепарата в теле LIII и в правом крыле подвздошной кости. При исследовании концентрации простатспецифического антигена выявлено его увеличение до 5,2 нг/мл (норма - до 4 нг/мл). Таким образом, люмбалгия с мышечно-тоническим синдромом обусловлена метастатическим поражением позвоночника на фоне злокачественного новообразования предстательной железы. В данном случае мышечно-тонический синдром выполняет защитную функцию, иммобилизуя пораженный ПДС.
Миофасциальный болевой синдром[править | править код]
МФБС - хронический болевой синдром, при котором в различных частях тела возникает локальная или сегментарная боль. Патогномоничным признаком МФБС считают ТЗ. Это участок локального продольного уплотнения, расположенный по направлению мышечных волокон, при раздражении которого (пальпаторном, уколом, перкуссией) появляется местная болезненность и иррадиация боли. Размер ТЗ составляет от 2 до 5 мм. Хотя при МФБС, как правило, неврологической симптоматики, свидетельствующей о поражении нервной системы, не выявляют, пациенты могут жаловаться на ощущение онемения, «ползание мурашек», покалывание в зоне иррадиации боли. Для каждой ТЗ характерна своя строго определенная область отраженной боли и парестезий. Еще в 1938 г. J. Kellgren были картированы зоны отраженной боли от большинства мышц путем введения в них здоровым добровольцам гипертонического солевого раствора. Детальное описание ТЗ в различных группах мышц дано в работах J.G. Travell и D.G. Simons (1989, 1992).
Наиболее часто ТЗ определяется в мышцах головы, шеи, надплечий и нижней части спины. Выделяют активные и латентные ТЗ. При наличии активных ТЗ определяется как спонтанная боль, возникающая обычно при нагрузке на заинтересованную мышцу, так и боль при пальпации мышцы в месте расположения ТЗ. Латентные ТЗ не сопровождаются спонтанной болью, но вызывается боль при их пальпации. Наиболее часто боль в области ТЗ пациенты описывают как интенсивную и острую, а отраженную - как ноющую. Активным ТЗ обычно сопутствует повышенная утомляемость мышцы и ограничение объема движений. В случаях, когда между двумя ТЗ или между ТЗ и костной структурой расположен сосудисто-нервный пучок или нерв, создаются условия для невроваскулярной компрессии. Пациенты при этом часто описывают сопутствующие ноющей боли онемение, парестезии, реже - гиперестезию или аллодинию в зоне иннервации соответствующего нерва. Может отмечаться отечность и ощущение скованности в дистальных отделах конечности. Обычно симптомы невроваскулярной компрессии регрессируют в течение нескольких минут после инактивации ТЗ путем введения в нее местного анестетика. Факторами, способствующими формированию МФБС, считаются:
- структурные особенности строения тела, вызывающие нефизиологическое длительное или постоянное напряжение мышц: асимметрия длины ног, тазового кольца, деформация стоп, удлинение второй плюсневой кости;
- позное напряжение: использование неудобной мебели, неправильная рабочая поза, приводящая к перегрузке отдельных групп мышц, длительная иммобилизация;
- перерастяжение мышцы, наблюдаемое при выполнении «неподготовленного» движения;
- механическое сдавление мышц (рюкзаком, ремнем, тесной одеждой);
- нарушения обмена веществ или питания;
- воздействие низкой температуры;
- сопутствующие психогенные расстройства.
В отсутствие провоцирующих факторов боль, отраженная от активной ТЗ, как правило, регрессирует в течение нескольких дней - недель, а сама активная ТЗ превращается в латентную. При продолжающемся воздействии провоцирующих факторов ТЗ сохраняются, а МФБС становится хроническим. Диагноз МФБС устанавливают на основании клинического обследования.
Критерии МФБС [по I. Russell, 2008, с изменениями]
Основные (необходимые) критерии
- Пальпируемый тяж в мышце (если она поддается пальпации).
- Участок локальной болезненности в пределах тяжа.
- При давлении на участок локальной болезненности воспроизводится типичный («узнаваемый») для пациента паттерн боли.
- Болезненность при пассивном движении, сопровождающемся растяжением пораженной мышцы, и возможное ограничение объема пассивных движений.
- Дополнительные симптомы:
- определяемое визуально или пальпаторно локальное сокращение мышцы при пальпации или перкуссии ТЗ заинтересованной мышцы;
- определяемое визуально или пальпаторно локальное сокращение мышцы при уколе ТЗ иглой;
- появление отраженной боли или иных сенсорных феноменов (парестезий) при сдавлении участка локальной болезненности в зоне, типичной для данной ТЗ.
Проблема диагностики МФБС состоит и в том, что относительно большое количество мышц потенциально может принимать участие в развитии МФБС, соответственно, врач должен владеть методикой мануального исследования различных мышц. Затруднения связаны с различной конституцией пациентов, толщиной подкожной жировой клетчатки, глубиной залегания мышц. Особенно труднодоступны при пальпации мышцы ног и ягодичной области (глубоко залегающая грушевидная мышца). Воспроизводимость диагноза МФБС при сравнении результатов обследования пациентов двумя независимыми обученными для диагностики МФБС специалистами остается низкой (табл. 2). Это отчасти можно объяснить тем, что области мышечного уплотнения с участками локальной болезненности и даже типичными паттернами отраженной боли и локальным сокращением мышцы часто выявляют и в здоровой части популяции. Доказано, что пациенты с МФБС от здоровых людей отличаются ограничением движений в пораженной мышце, уменьшением в ней силы (при активном сопротивлении) из-за возникающей при движении боли и снижением болевого порога, выявляемого при альгометрии [I. Russell, 2008].
Таблица 2. Валидность клинического обследования при выявлении МФБС (I.J. Russell, 2008)
|
Воспроизводимость симптома’ |
Симптом |
|
Высокая |
Выявление ТЗ в мышце |
|
Определение паттерна отраженной боли | |
|
Воспроизводимость «знакомой» боли | |
|
Низкая |
Выявление локальной болезненности |
|
Пальпация тугого тяжа в мышце | |
|
Выявление локального сокращения |
Примечание. *«Слепое» обследование проводили исследователи, специально обученные стандартизированным приемам клинического выявления симптомов МФБС.
Кроме скелетно-мышечных нарушений, у пациентов с МФБС часто отмечают расстройства сна и сопутствующие эмоциональные нарушения (тревожность и депрессия). Несмотря на продолжающуюся дискуссию о МФБС как самостоятельной нозологической единице с прямо противоположными точками зрения [M. Cohen, 2008; D. Simons, 2008], большинство исследователей и специалистов в области болевых синдромов (88%) считают диагноз МФБС правомочным [I.J. Russell, 2008]. Задача врача - диагностика МФБС в качестве причины боли в спине и конечностях для последующего ее устранения. Ниже приведены субъективные и объективные признаки МФБС в разных мышцах. В табл. 3 и 4-4 описаны анатомические и отдельные биомеханические особенности мышц спины.
Таблица 3. Мышцы спины
|
Мышцы |
Начало |
Прикрепление |
Основная функция |
|
Ременные |
Выйная связка, остистые отростки С7-Тh4 |
Ременная мышца головы: сосцевидный отросток и латеральная треть верхней выйной линии затылочной кости Ременная мышца шеи: задние бугорки поперечных отростков трех верхних шейных позвонков |
При одностороннем сокращении: боковой наклон и вращение головы в сторону сокращения мышцы При двустороннем сокращении: разгибание головы и шеи |
|
Промежуточный слой | |||
|
Мышца, выпрямляющая позвоночник |
Начинается широким сухожилием от задней поверхности крестца, задних отделов подвздошной ости, остистых отростков поясничных позвонков и надостистой связки |
Подвздошно-реберная мышца поясницы, груди и шеи: углы нижних ребер и поперечные отростки шейных позвонков Длиннейшая мышца груди, шеи и головы: поперечные отростки грудных и шейных позвонков, сосцевидный отросток Остистая мышца груди, шеи и головы: остистые отростки шейных, верхних грудных позвонков, нижняя выйная линия или затылочная кость |
При одностороннем сокращении: боковой наклон позвоночника При двустороннем сокращении: разгибание головы и позвоночника, при флексии - стабилизация позвоночника за счет постепенного удлинения мышцы |
|
Глубокий слой | |||
|
Поперечноостистые мышцы |
Полуостистая: от поперечных отростков шейных и грудных позвонков |
Затылочная кость, остистые отростки грудного и шейного отдела на 4-6 позвонков выше места начала |
При одностороннем сокращении: вращение головы, шейного и грудного отдела позвоночника в противоположную сторону При двустороннем сокращении: разгибание головы, шейного и грудного отдела позвоночника |
|
Многораздельные: от крестца, подвздошной кости, поперечных отростков Тh1-ТhЗ, суставных отростков С4-С7 |
Остистые отростки на 2-4 позвонка выше места Стабилизация позвоночника при его начала движениях | ||
|
Мышцы-вращатели: поперечные отростки, лучше развиты в грудном отделе |
Место соединения пластину дуги позвонка и Стабилизация позвоночника и поперечного отростка или остистый отросток на содействие при разгибании и 1-2 позвонка выше места начала ротации в отдельных ПДС | ||
|
Глубокие мелкие мышцы | |||
|
Межостистые |
Верхние поверхности остистых отростков в шейном и поясничном отделе |
Нижние поверхности остистых отростков на один позвонок выше места начала |
Дополнительные вращатели и разгибатели позвоночника |
|
Межпоперечные |
Поперечные отростки в шейном и поясничном отделе |
Поперечный отросток на один позвонок выше места начала |
Дополняют боковые наклоны, стабилизируют позвоночник |
|
Мышцы, поднимающие ребра. |
Верхушки поперечных отростков С7-Тh11 |
Ребро между его бугорком и углом |
Поднимают ребро, участвуют в акте дыхания, дополняют боковые наклоны позвоночного столба |
- Большинство мышц спины иннервируются задними ветвями спинномозговых нервов, однако отдельные мышцы иннервируются передними ветвями. Передние межпоперечные мышцы в шейном отделе позвоночника получаю иннервацию из передних ветвей спинномозговых нервов.
Таблица 4. Основные мышцы, обеспечивающие движения в суставах позвоночника
|
Сгибание (двустороннее сокращение мышц) |
Разгибание (двустороннее сокращение мышц) |
Боковой наклон (одностороннее сокращение мышц) |
Вращение (одностороннее сокращение мышц) | |
|
Атлантозатылочные суставы’ | ||||
|
Длинная мышца головы Передняя прямая мышца головы Передние волокна грудиноключичнососцевидной мышцы |
Задние прямые мышцы головы, большая и малая Верхняя косая мышца головы Полуостистая мышца головы Ременная мышца головы Длиннейшая мышца головы Трапециевидная |
Грудино-ключичнососцевидная Верхняя и нижняя косые мышцы головы Латеральная прямая мышца головы Длиннейшая мышца головы Ременная мышца головы |
Ипсилатерально Нижняя косая мышца головы Задние прямые мышцы головы, большая и малая Длиннейшая мышца головы Ременная мышца головы |
Контрлатерально Грудино ключичнососцевидная Полуостистая мышца головы |
|
Межпозвоночные суставы шейного отдела | ||||
|
Длинная мышца шеи Лестничные Грудино ключичнососцевидная |
Ременная мышца головы Полуостистая мышца головы и шеи |
Подвздошно-реберная мышца шеи Длиннейшая мышца головы и шеи Ременная мышца головы и шеи |
Мышцы-вращатели Полуостистая мышца головы и шеи Многораздельные мышцы Ременная мышца шеи | |
|
Межпозвоночные суставы грудного и поясничного отделов | ||||
|
Прямая мышца живота Большая поясничная мышца |
Мышца, выпрямляющая позвоночник Многораздельные мышцы Полуостистая мышца груди |
Подвздошно-реберная мышца груди и поясницы Длиннейшая мышца груди Многораздельные мышцы Наружная и внутренняя косая мышца живота Квадратная мышца поясницы |
Мышцы-вращатели Многораздельные мышцы Наружная косая мышцы живота во время синхронного сокращения с контрлатеральной внутренней косой мышцей живота Полуостистая мышца груди | |
* Ротация - основная функция этих суставов.
Наличие ТЗ в нижней части ременной мышцы шеи приводит к возникновению болевого ощущения с ипсилатеральной стороны у основания шеи. ТЗ пальпируется непосредственно над углом, образованным основанием шеи и надплечьем. Активация ТЗ в этой мышце происходит при позном напряжении, связанном с разгибанием шеи и поворотом головы (наблюдение за высоко расположенными объектами в бинокль, работа за столом с повернутой в сторону головой, неудобное положение во время сна, когда голова лежит на подлокотнике дивана). Напряжение и формирование ТЗ в задней группе мышц шеи - многораздельной и полуостистой мышцах - возникает при чтении и работе за столом с постоянно согнутой шеей. При этом особенно ограничиваются наклоны головы вперед, а положение во время сна на спине для многих пациентов становится невыносимым. При поражении мышцы, поднимающей лопатку, пациенты обычно жалуются на выраженную боль, скованность и ограничение поворотов головы. Чтобы посмотреть назад, пациенты часто разворачиваются всем телом. Сгибание шеи блокируется только в конце движения, разгибание не нарушено. Средние пучки трапециевидной мышцы могут активироваться путем перегрузки при управлении автомобилем, если водитель держит руки на верхней части рулевого колеса.
Наиболее частыми причинами боли в шейном отделе позвоночника, распространяющимися в руку, считают МФБС мышц плечевого пояса, а также синдром плечелопаточной периартропатии. Реже отмечают отраженные боли при заболеваниях внутренних органов (сердца, легких и плевры, органов средостения).
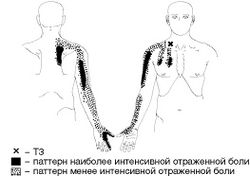
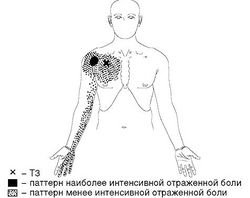
Скаленус-синдром. Одним из частых источников цервикобрахиалгии считают МФБС лестничных мышц. Боль локализуется в области плеча и над медиальным краем лопатки и распространяется по передней и задней поверхности плеча на лучевую часть предплечья, в большой и указательный пальцы (Рис. 2). Напряжение лестничных мышц происходит при удержании тяжелого предмета на уровне талии, при частых приступах кашля, участии мышц в парадоксальном дыхании, нахождении головы во время сна ниже уровня туловища, наклоне оси плечевого пояса, связанного с конституционально разной длиной ног, косым тазом, сколиозом.
Передняя лестничная мышца вверху прикрепляется к передним бугоркам поперечных отростков III и IV шейных позвонков, внизу - к I ребру. Подключичная артерия и нижние стволы плечевого сплетения огибают сверху I ребро и проходят между прикрепленными к нему передней и средней лестничными мышцами. В промежутке между передней лестничной мышцей, I ребром и ключицей проходит подключичная вена и подключичный лимфатический ствол. Напряженная и укороченная передняя лестничная мышца сдавливает нижний ствол плечевого сплетения. Это приводит к появлению онемения, покалывания и нарушению чувствительности в IV-V пальцах кисти, по внутренней поверхности кисти и предплечья, ощущению скованности движений в пальцах, особенно по утрам.
При обследовании выявляют ограничение латерофлексии в шейном отделе позвоночника в противоположную сторону. Движения в плечевом суставе, как правило, не ограничены. При клиническом обследовании диагностически важными считают пробу Адсона и тест на спазм лестничных мышц (максимальный поворот головы в сторону локализации боли и опускание подбородка в надключичную ямку, что приводит к сокращению лестничных мышц на той же стороне, активации в них ТЗ и вызывает характерный паттерн отраженной боли).
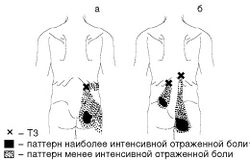
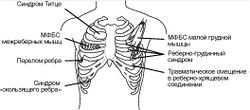
Синдром малой грудной мышцы. Частой причиной цервикобрахиалгического синдрома с распространением отраженной боли на переднюю поверхность надплечья, а также вдоль медиальной поверхности плеча, предплечья и ладони считают МФБС малой грудной мышцы (Рис. 3). ТЗ формируются и активируются при сдавлении мышцы ремнем рюкзака, при сильном кашле, опускании плеча, травмах грудной клетки, ИБС. Напряженная мышца может сдавливать проходящие вблизи ее прикрепления к клювовидному отростку лопатки подмышечную артерию и нижние стволы плечевого сплетения. Сосудистая компрессия подтверждается положительным результатом пробы Райта.
МФБС широчайшей мышцы спины (Рис. 4). ТЗ в широчайшей мышце спины активируются при неоднократном переносе тяжелых предметов на вытянутых вперед и вверх руках. J. Travel называет боль, связанную с МФБС широчайшей мышцы, «злокачественной болью в спине», поскольку она не устраняется при растяжении мышцы или изменении позы.
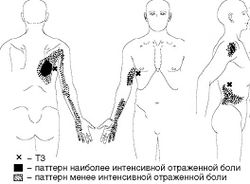
МФБС верхней задней зубчатой мышцы проявляется ощущением тупой, глубокой боли в верхней части спины, в области верхнего и медиального края лопатки (Рис. 5). Обычно ТЗ формируются и активируются при пневмонии, астме, хронической эмфиземе, увеличивая страдания пациента при заболеваниях легких. Наличие ТЗ в нижней задней зубчатой мышце приводит к возникновению болезненных ощущений в нижней части грудного отдела позвоночника и в области нижних ребер. При этом МФБС часто формируется при работе стоя на лестнице с поднятыми руками.
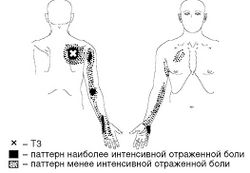
МФБС ромбовидных мышц. Боль, связанная с наличием ТЗ в ромбовидных мышцах, локализуется между медиальным краем лопатки и позвоночником, ощущается в отличие от МФБС зубчатых мышц как поверхностная, из-за чего многие пациенты пытаются растирать болезненную область (Рис. 6). ТЗ развиваются и активируются при частом позном напряжении с наклоном вперед, при наличии сутулости, сколиоза, вынужденном положении с удерживанием отведенного до 90° плеча.
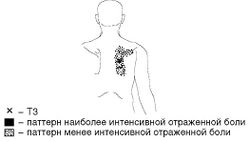
МФБС большой грудной мышцы. Активация ТЗ в грудинной части большой грудной мышцы приводит к иррадиации боли по передней поверхности грудной стенки, медиальной поверхности плеча и предплечья, в латеральном крае мышцы - к иррадиации боли в область молочной железы, с гиперчувствительностью в области соска и непереносимостью прикосновения к нему одежды (аллодиния). ТЗ в парастернальной порции мышцы слева дают зону иррадиации, характерную для локализации боли при ИБС (Рис. 7). Активация ТЗ происходит при подъеме тяжестей (особенно перед собой), работе тугими кусачками, нагрузке руки в положении отведения, длительном нахождении с опущенными надплечьями, что приводит к укорочению мышцы.
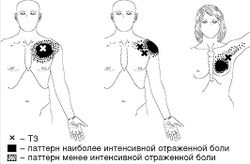
МФБС передней зубчатой мышцы характеризуется наличием ТЗ по переднебоковой поверхности грудной клетки и кнутри от нижнего угла лопатки. У некоторых больных отмечается гиперчувствительность молочной железы, сходная с таковой при МФБС большой грудной мышцы. Иногда больные испытывают затруднение при глубоком вдохе. Активация ТЗ происходит при быстром и продолжительном беге, толкании, подъеме тяжестей над головой, сильном кашле.
Межреберные мышцы вовлекаются в патологический процесс при интенсивном кашле, а также в результате травм и хирургических вмешательств на грудной клетке. При пальпации в межреберных промежутках выявляют локальную болезненность с воспроизведением характерного болевого паттерна.
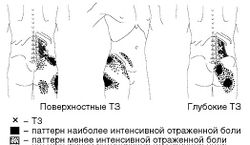
МФБС подвздошно-реберной мышцы проявляется болью в области грудного или поясничного отделов позвоночника (Рис. 8). Боль может иррадиировать в нижележащие отделы спины и ягодичную область. Активация ТЗ связана с боковым наклоном туловища при неудобной позе, например при неправильной осанке за рабочим столом, а также с форсированными движениями, подъемом груза, сопровождающимися разгибанием и поворотом туловища. Считают, что асимметрия длины ног и таза также способствует активации ТЗ в паравертебральных мышцах.
Боль, связанная с активацией ТЗ при МФБС многораздельных мышц, локализуется в области остистых отростков поясничных позвонков, пациенты описывают ее как боль «в позвоночнике» (Рис. 9). Иногда она может отражаться в переднюю брюшную стенку, имитируя патологию внутренних органов, или в область копчика (при локализации ТЗ на уровне SI). Активация ТЗ в многораздельных мышцах происходит при резком «неподготовленном» движении с наклоном и ротацией в поясничном отделе или при длительном пребывании в положении с наклоном вперед. Также они могут активироваться в условиях, сходных с причинами активации ТЗ в подвздошно-реберной мышце. При пальпации ТЗ полезно учитывать, что многораздельные мышцы составляют значительную часть мышечной массы, расположенной между поперечными и остистыми отростками в пояснично-крестцовой области, и покрывают заднюю поверхность крестца. При пальпации области, расположенной непосредственно медиальнее задней верхней подвздошной ости, определяется подкожная клетчатка, поверхностный слой поясничногрудной фасции, апоневроз мышцы, выпрямляющей позвоночник, и массивное брюшко многораздельной мышцы. Из-за особенностей своего прикрепления многораздельные мышцы создают оптимальный рычаг для разгибания позвоночника, больший, чем у глубоких пучков мышцы, выпрямляющей позвоночник. В вертикальном положении эти мышцы противодействуют сгибанию и смещению позвонка кпереди.
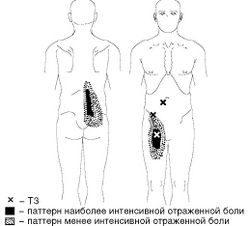
МФБС квадратной мышцы поясницы часто становится причиной глубокой ноющей боли в поясничной области, которая при наличии поверхностно расположенных ТЗ иррадиирует в зону КПС и в ягодичную область, а при ТЗ в глубине мышцы - в бедро, область гребня подвздошной кости и паховую область (Рис. 10). Эта мышца своим сокращением может компенсировать перекос таза при разнице в длине ног на стороне длинной ноги при ходьбе. Она также стабилизирует таз и поясничный отдел позвоночника во фронтальной и горизонтальной плоскости. В частности, при боковом наклоне на выпуклой стороне дуги квадратная мышца поясницы сокращается эксцентрически, регулируя угол наклона. Для возвращения в вертикальное положение необходимо ее концентрическое сокращение. Аналогично тому, как сокращение мышцы, выпрямляющей позвоночник, многораздельных мышц и большой поясничной мышцы стабилизирует позвоночник в сагиттальной плоскости, его стабилизация во фронтальной плоскости может достигаться участием квадратной мышцы поясницы, аддукторами и абдукторами бедра. Определенное значение квадратная мышца поясницы имеет при движении позвоночника в горизонтальной плоскости.
В квадратной мышце поясницы наиболее часто активные ТЗ формируются при форсированных движениях, сопровождающихся наклоном и поворотом туловища, подъемом груза, а также при позном напряжении, связанном с садовыми работами, уборкой помещений или вождением автомобиля. Боль обычно локализуется в области, ограниченной вверху реберной дугой, снизу - гребнем подвздошной кости, медиально - остистыми отростками поясничных позвонков, латерально - задней подмышечной линией. Болевые ощущения возникают или усиливаются при ходьбе, наклонах, поворотах в постели, вставании со стула, кашле и чихании. Обычно отмечается интенсивная боль в покое, нарушающая сон. Поскольку квадратная мышца лежит под мышцей, выпрямляющей позвоночник, для выявления в ней ТЗ необходима глубокая пальпация в положении пациента лежа на здоровом боку. Как правило, отмечается ограничение латерофлексии в поясничном отделе позвоночника в сторону, противоположную локализации спазмированной мышцы.
МФБС подвздошно-поясничной мышцы. Подвздошно-поясничная мышца образована двумя мышцами - большой поясничной и подвздошной. Боль, связанная с активацией ТЗ в этой мышце, может распространяться вдоль позвоночника от грудного отдела до паховой области и иногда иррадиирует по передней поверхности бедра (Рис. 11). Она обычно усиливается в вертикальном положении и в положении сидя. Часто ее паттерны трудно отличимы от активации ТЗ в квадратной мышце поясницы. Если отмечается укорочение или напряжение большой поясничной мышцы, формируется наклон таза или его ротация кпереди. Это в свою очередь приводит к усилению компрессии и воздействию силы, направленной на сдвиг позвонков кпереди, в пояснично-крестцовых и дугоотростчатых суставах поясничного отдела, поскольку они находятся в состоянии избыточного разгибания. Биомеханика большой поясничной мышцы при фиксированной ноге отличается от таковой подвздошной мышцы. Ее сокращение увеличивает поясничный лордоз и сгибание позвоночника в пояснично-крестцовой области относительно оси бедра. При увеличении поясничного лордоза к поясничному отделу позвоночника прикладывается большая сила, направленная на сдвиг позвонков кпереди. Этот феномен усиливается при смещении центра тяжести туловища относительно пояснично-крестцового отдела позвоночника, что, например, отмечается у женщин во II-III триместре беременности. В этом случае масса плода оказывает большее воздействие, направленное на сдвиг позвонков кпереди, и увеличивает разгибание в поясничной области. Один их механизмов компенсации этого воздействия - необходимое расслабление поясничной мышцы. Оно может быть достигнуто наружной ротацией бедра (при внутренней ротации мышца натягивается и воздействие на позвоночник возрастает), что и проявляется в изменении походки у беременных, которые обычно ставят ноги носками врозь. Похожие изменения походки отмечаются при слабости брюшной стенки и наличии «отвислого живота». Для дальнейшего противостояния смещению центра тяжести в этих случаях возникает необходимость в разгибании туловища, что увеличивает нагрузку на задние структуры позвоночного столба, например на дугоотростчатые суставы, вызывая их болезненную дисфункцию.
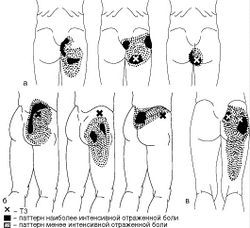
МФБС большой ягодичной мышцы проявляется болью, возникающей в положении сидя, при ходьбе с подъемом в гору, особенно при наклоне туловища кпереди. Боль, связанная с активацией ТЗ в этой мышце, редко иррадиирует в дистальные отделы ноги и локализуется преимущественно в ягодичной области (Рис. 12, а). Болезненные тугие тяжи в мышцах ягодичной области, пальпирующиеся непосредственно под кожной жировой клетчаткой, относятся к большой ягодичной мышце.
При сокращении большой ягодичной мышцы отмечают ротацию таза кзади, что приводит к сгибанию в поясничном отделе позвоночника и уменьшению нагрузки на задние отделы позвоночного столба, в частности компрессионного воздействия на дугоотростчатые суставы. Такая поза, как правило, отмечается у пациентов с латеральным стенозом позвоночного канала и дегенеративным поражением дугоотростчатых суставов.
Мышцы латеральной поверхности бедра (средняя и малая ягодичная мышцы, напрягатель широкой фасции). Боль, связанная с активацией ТЗ в средней ягодичной мышце, обычно ощущается вдоль гребной подвздошной кости, в крестце и ягодичной области (Рис. 12, б). Она может иррадиировать до середины бедра. Как правило, боль возникает или усиливается при ходьбе и может провоцироваться пребыванием в положении сидя в глубоком кресле. Если при ходьбе отмечается опускание одной половины таза, это свидетельствует о неспособности отводящих мышц бедра стабилизировать его. При этом возрастает нагрузка на дугоотростчатые суставы с противоположной стороны. При слабости этой группы мышц нога остается в положении большего приведения по сравнению с интактной стороной, что увеличивает компрессионную нагрузку на головку бедренной кости и латеральные отделы большого вертела на стороне поражения. Бурсит в области большого вертела может быть следствием нарушения биомеханики таза во фронтальной плоскости, коррекция которой значительно уменьшает его клинические проявления.
МФБС грушевидной мышцы характеризуется болью в ягодице, крестце, проекции тазобедренного сустава и по задней поверхности бедра по ходу седалищного нерва (Рис. 12, в). При напряжении грушевидной мышцы возможно сдавление седалищного нерва и нижней ягодичной артерии. Объем движений в поясничном отделе позвоночника не изменен. Поднимание прямой ноги часто ограничено. ТЗ в грушевидной мышце наиболее часто активируются при движениях, связанных с форсированной ротацией на одной ноге, падениях, при длительном отведении ног в тазобедренных и сгибании в коленных суставах во время акушерских и урологических манипуляций.
Патофизиология миофасциального болевого синдрома[править | править код]
Точная причина развития МФБС остается неизвестной. Существует несколько теорий патофизиологии миофасциальной боли. Так, согласно теории ишемического спазма исходным стимулом часто бывает физическая травма мышцы либо ее хроническое напряжение (мышечно-тонический синдром), что приводит к высвобождению внутриклеточного кальция и удлиненному ненормальному мышечному сокращению - спазму части мышцы. Этот спазм может вызывать боль и повреждение путем высвобождения простагландинов и других медиаторов воспаления, которые в свою очередь, возможно, дополнительно усиливают мышечный спазм. Такое продолженное сокращение может приводить к ишемии как на клеточном уровне путем усиления анаэробного гликолиза и избыточного образования молочной кислоты, так и к снижению локального кровотока. Эта «модель энергетического кризиса» (D. Simons) частично объясняет напряжение, имеющееся в плотных мышечных тяжах и сохраняющееся в покое. Однако маловероятно, что возникающая при МФБС хроническая боль носит ишемический характер, поскольку она не имеет характерных признаков острой ишемической боли. Также остается неясным, почему мышечное повреждение при МФБС должно приводить к образованию ТЗ, в то время как другие заболевания мышц не вызывают формирования ТЗ. Продолжается дискуссия о том, можно ли считать ТЗ зонами патологического мышечного сокращения или же участками контрактуры, не генерирующими биоэлектрическую активность. Тем не менее, несмотря на эти вопросы, распространено убеждение, что МФБС каким-то образом связан с локальным мышечным спазмом.
Локализация ноцицепторов внутри скелетной мышцы тесно связана с фасциями между мышечными волокнами. Наибольшая концентрация ноцицепторов отмечена в области концевой пластинки (высоко возбудимая часть мембраны мышечного волокна, ответственная за формирование потенциала действия, распространяющегося по всему волокну, приводя к сокращению), где, как правило, и обнаруживают ТЗ. Были предположения, что в ТЗ есть множественные локусы периферической сенситизации, а каждый такой локус состоит из одного или нескольких сенситизированных нервных окончаний [S. Inbody, 1998].
Острое или хроническое повреждение мышечной ткани приводит к развитию неврогенных изменений чувствительности (гипералгезия), двигательных (мышечный спазм), вегетативных (вазоконстрикция, повышенное потоотделение) и психических (тревожность, депрессия) проявлений. Это обусловлено тем, что длительная ноцицептивная афферентация вызывает нейропластические изменения, приводящие к центральной сенситизации в задних рогах спинного мозга и других отделах ноцицептивной системы, обеспечивающих восприятие боли. Это может приводить к функциональным и структурным изменениям в ЦНС, которые затем участвуют в формировании хронической боли, вегетативной дисфункции и психических расстройств. Именно вовлечением в патофизиологию МФБС структур ЦНС (задних рогов спинного мозга, зрительного бугра, соматосенсорной коры) объясняется распространение боли за пределы ТЗ (отраженные боли), вторичной гипералгезии и аллодинии [Р.Г. Есин и др., 2003]. Г.А. Иваничев (2007) рассматривает развитие МФБС в виде процесса, состоящего из нескольких этапов. На первом этапе формируется остаточная локальная деформация мышцы после выполнения статической работы минимальной интенсивности и большой продолжительности - «мышечно-фасциальный гипертонус», на втором - дисбаланс проприоцепции от участка «мышечно-фасциального гипертонуса», на третьем - дисфункция сегментарного аппарата спинного мозга, на четвертом - дисбаланс восходящей проприоцептивной импульсации в церебральные структуры. Пятый этап включает изменение нисходящего супрасегментарного контроля организации движений и шестой - формирование болезненности «мышечно-фасциального гипертонуса» путем ослабления механизмов торможения афферентации из участка деформации мышцы.
Повышенная возбудимость нейронов заднего рога спинного мозга - проявление центральной сенситизации - лишь первая ступень в формировании хронической боли, за которой следуют другие функциональные, а затем и структурные изменения как нейронов заднего рога, так и клеток глии. Показано, что афферентация от ноцицепторов мышц - более мощный индуктор возбудимости ЦНС, чем афферентация от ноцицепторов кожи [S. Mense, 2008].
Лечение[править | править код]
При лечении МФБС применяют комплексный подход. С точки зрения доказательной медицины проблеме МФБС уделено значительно меньше внимания, чем «неспецифической» боли в спине. Обычно пациентов с МФБС относят именно к этой диагностической категории. Таким образом, общие подходы к лечению «неспецифической» боли в спине (см. ниже) справедливы и в отношении МФБС.
Большая роль при лечении МФБС принадлежит местному лечению - растяжению, массажу заинтересованной мышцы и ТЗ, воздействию теплом или холодом, ультразвуком, чрескожной нейростимуляцией, инъекциям местных анестетиков в ТЗ. Считают, что при МФБС наиболее эффективны инъекции местных анестетиков в ТЗ. Обычно вводят 0,5-1 мл 0,5% раствора прокаина. Прокаин считается наименее миотоксичным местным анестетиком. Ряд авторов рекомендуют применение лидокаина в разведении 0,2-0,25%. Иногда к местному анестетику добавляют глюкокортикоид (дексаметазон в дозе 2-4 мг), но эффективность такого сочетания имеет слабую доказательность. Для усиления эффекта блокад дополнительно применяют пассивное растяжение мышцы или использование релаксирующих приемов мануальной терапии [Г.А. Иваничев, 2007; E.D. Lavelle и др., 2007].
Для уточнения эффективности введения ботулотоксина в ТЗ проведено несколько рандомизированных контролируемых исследований (РКИ), систематизированных в обзоре K. Ho и К. Tan [K. Ho и К. Tan, 2007]. Четыре из пяти проанализированных РКИ не подтвердили эффективность инъекций ботулотоксина при МФБС.
Д.Г. Тревел и Д.Г. Симонс рекомендуют распыление хладагента (этилхлорид) над мышцей и зоной отраженной боли. Орошение производят со скоростью 10 см/с, направление струи - 30° к поверхности кожи [Д.Г. Тревел, Д.Г. Симонс, 1989].
К другим местным методам лечения относят массаж, применение ультразвука (в непрерывном или импульсном режиме интенсивностью 0,2-0,5 Вт/см2 вокруг ТЗ). При МФБС возможно применение чрескожной электронейростимуляции, но ее эффективность, как большинства методов физиотерапии, при МФБС не доказана. По данным нескольких РКИ, при МФБС потенциальной эффективностью обладает акупунктура. Курс лечения составляет от 10 до 15 сеансов.
Важное место в лечении занимают аппликации на болевые участки кожи гелей, мазей, как противовоспалительных, так и раздражающих. Оправданно применение и аппликаций 40-50% раствора диметилсульфоксида в сочетании с глюкокортикоидами (гидрокортизоном) и местными анестетиками (1% раствором лидокаина или прокаина). Продолжительность воздействия - до 1,5 ч в сутки. На курс рекомендуется 8-10 аппликаций. Показана целесообразность применения трансдермальной терапевтический системы с 5% раствором лидокаина для лечения миогенной боли [C.E. Argoff, 2004]. По-видимому, наибольшая эффективность от этого вида местного воздействия должна отмечаться при наложении пластин на зону гипералгезии или аллодинии. Продолжительность лечения может составлять от нескольких дней до нескольких месяцев в зависимости от стойкости болевого синдрома и индивидуальной чувствительности.
Расслабление спазмированной мускулатуры, кроме того, можно достичь при помощи постизометрической релаксации (ПИР). ПИР представляет собой расслабление мышц после их волевого напряжения без изменения расстояния между точками прикрепления мышцы (после изометрического напряжения) [Г.А. Иваничев, 2007]. Пациент должен занять удобную позу в положении сидя или стоя, а врач после предварительного растяжения релаксируемой мышцы небольшим усилием просит пациента произвести активное ее сокращение в течение 6-10 с. Произвольное усилие, которое прикладывает пациент, должно быть относительно небольшим - 5-10% от максимально возможного. Задача врача - препятствовать движению, удерживая мышцу в исходном положении. При этом врач ощущает «включение» мышцы, не прилагая значительных усилий для противодействия движению. Затем врач просит пациента расслабиться, после чего производит дополнительно растяжение мышцы небольшим усилием. Пассивное растяжение также длится 6-10 с. Количество циклов может варьировать от 2-3 до 6-7. Врач ориентируется на реакцию пациента и свои ощущения в виде изменения напряжения мышцы и амплитуды движений. Общее количество сеансов может достигать 10-15.
Иногда для устранения ТЗ применяют методику прессуры или ишемической компрессии ТЗ. При этом производят энергичное пальцевое давление на ТЗ в течение 1-2 мин. Считают, что это воздействие вызывает фазные изменения кровотока (ишемия и реактивное полнокровие), которые, возможно, лежат в основе лечебного эффекта. При проведении процедуры мышцу растягивают до появления чувства дискомфорта, затем сдавливают ТЗ пальцем до появления переносимой боли. По мере адаптации к боли давление постепенно усиливают, помогая пальцем другой руки. Воздействие продолжается до 1 мин с силой 9-13 кг. При стойких ТЗ возможно сочетание ПИР и прессуры. Врач при этом оказывает давление на ТЗ в течение всего цикла ПИР. Различные методы релаксации мышц подробно описали Г.А. Иваничев (2005), Р.Г. Есин и соавт. (2003), Д.Г. Тревел и Д.Г. Симонс (1989), Л. Фергюсон и Р. Гервин (2008). В ряде случаев целесообразно добавление акупунктуры и рефлексотерапии. Этим методам лечения посвящено большое количество публикаций [Д.М. Табеева, 2004; Л.Г. Агасаров, 2008]. В основе лечебного воздействия, возможно, лежит активация антиноцицептивных (опиоидергических, серотониергических, катехоламинергических) механизмов.
Из лекарственных препаратов в дополнение к местным воздействиям рекомендуют прием НПВС (например, лорноксикам (ксефокам) по 4-8 мг 2 раза в сутки в течение 7-10 сут). Целесообразно применение миорелаксантов: тизанидина (сирдалуд) (по 2 мг 3 раза в сутки, при необходимости дозу постепенно повышают до 6-12 мг/сут в 3 приема), толперизона (по 300-450 мг/сут в 3 приема), баклофена (по 5 мг 2 раза в сутки с постепенным повышением дозы каждые 5 сут до 30 мг/сут). При хроническом течении МФБС целесообразно добавление к лечению антидепрессантов, обладающих собственной анальгетической активностью: амитриптилина (50-75 мг/сут), венлафаксина (75-150 мг/сут), дулоксетина (60-120 мг/сут), милнаципрана (50-100 мг/сут). При подострой и хронической боли возможно применение флупиртина в дозе 300-600 мг/сут - непрямого антагониста NMDA-рецепторов, обладающего анальгетическим и миорелаксирующим действием.
Целесообразна коррекция асимметрии тела, неоптимального двигательного стереотипа, избегание провоцирующих нагрузок и поз [Г.А. Иваничев, 2005; А.А. Лиев, 1995; Я.Ю. Попелянский, 1997; Ф.А. Хабиров, 2006; I. Russell, 2008]. Таким образом, целесообразно сочетание местных методов лечения с общими воздействиями. Схема лечения МФБС в зависимости от его длительности приведена в табл. 5.
Таблица 5. Лечение миофасциального болевого синдрома
|
Острая и подострая боль |
Хроническая боль | |
|
Медикаментозные методы | ||
|
Общие воздействия |
Местные методы воздействия* |
Общие воздействия |
|
НПВС и анальгетики: диклофенак (вольтарен) по 75-150 мг/сут, кетопрофен по 100-150 мг/сут, декскетопрофен по 75 мг/сут, лорноксикам (ксефокам) по 8-16 мг/ сут, кеторолак (кеторол) по 90 мг/сут при внутримышечном введении и 40 мг/ сут при приеме внутрь мелоксикам по 7,5-15 мг/сут, нимесулид (наиз) по 200 мг/сут, целекоксиб по 200 мг/сут, 7-14 сут флупиртин (катадолон) |
Инъекции местных анестетиков в ТЗ (0,5% раствор прокаина) Применение мазей с НПВС (диклофенак, кетопрофен, ибупрофен) 2-3 раза в сутки |
НПВС: диклофенак по 75-150 мг/сут, кетопрофен по 100-150 мг/сут, декскетопрофен по 75 мг/сут, порноксикам по 8-16 мг/сут, мелоксикам по 7,5-15 мг/сут, нимесулид по 200 мг/сут, целекоксиб по 200 мг/сут, кеторолак по 90 мг/сут при внутримышечном введении и 40 мг/сут при приеме внутрь 7-14 сут |
|
Миорелаксанты: тизанидин (сирдалуд) по 6-12 мг/сут, толперизон 300-450 мг/сут, баклофен до 30 мг/сут 10-14 сут |
Трансдермальная терапевтическая система с лидокаином в течение 12 ч |
Антидепрессанты: амитриптилин по 50-75 мг/сут, венлафаксин по 75-150 мг/сут, дулоксетин по 60-120 мг/сут, милнаципран по 50-100 мг/сут в течение 4-6 мес |
|
флупиртин по 300-600 мг/сут в течение 2-3 мес при подострой боли |
Аппликации 40-50% раствора диметилсульфоксида в сочетании с глюкокортикоидами (гидрокортизон) и местными анестетиками (1% раствор лидокаина или прокаина) |
флупиртин по 300-600 мг/сут 1-2 мес |
|
Орошение мышцы хладагентом (этиленхлорид) | ||
|
Немедикаментозные методы | ||
|
Коррекция асимметрии тела, неоптимального двигательного стереотипа, избегание провоцирующих нагрузок и поз |
Массаж: 10-15 сеансов |
Коррекция асимметрии тела, неоптимального двигательного стереотипа, избегание провоцирующих нагрузок и поз |
|
ПИР: 10-15 сеансов Ультразвуковое воздействие: 10 сеансов Прессура ТЗ Чрескожная электронейростимуляция Акупунктура: 10-15 сеансов |
ЛФК | |
*Оптимальная комбинация инъекций местных анестетиков в ТЗ с другими видами местного медикаментозного и немедикаментозного лечения.
**Целесообразно включать сочетание ПИР, массажа с 1-2 другими немедикаментозными местными методами лечения.
ЛФК - лечебная физкультура.
Клинический пример
Пациентка Б., 50 лет, швея, обратилась в клинику с жалобами на интенсивные боли ломящего, ноющего характера, иррадиирующие по наружной поверхности правого плеча и предплечья, преходящее ощущение онемения в IV-V пальцах правой кисти, ee отечность, больше выраженную в утреннее время. Указанные расстройства беспокоят в течение 2 мес, аналогичный эпизод длительностью примерно 3 нед отмечался год назад на фоне увеличения объема работы и самостоятельно регрессировал во время отпускного периода. Настоящее обострение пациентка также связывает с повышенной нагрузкой на рабочем месте и с эмоциональным стрессом, связанным с неблагополучной семейной ситуацией. Соматическое и неврологическое обследования, так же как и рутинные параклинические исследования, патологии не выявили. При невроортопедическом осмотре при пальпации выявлено болезненное уплотнение (тяж) в передней лестничной мышце справа с участком локальной болезненности в нем с воспроизведением характерной для пациентки боли, иррадиирующей в правое плечо - ТЗ. При обследовании выявлено ограничение латерофлексии в шейном отделе позвоночника влево. Проба Адсона и тест на «спазм» лестничных мышц (поворот головы вправо и опускание подбородка в надключичную ямку вызывает характерный паттерн боли) положительные. При рентгенографии шейного отдела позвоночника выявлены признаки остеохондроза (склероз замыкательных пластинок, снижение высоты межпозвоночных промежутков на уровне СV-СVI СVI-СVII формирование передних остеофитов на этом уровне), гипертрофия поперечных отростков СVII . Состояние было расценено как МФБС правой передней лестничной мышцы с признаками невроваскулярной компрессии подключичной вены и нижнего ствола плечевого сплетения справа. Пациентке проведены инъекции местного анестетика (0,5% раствор прокаина) в ТЗ, ПИР, назначен тизанидин в дозе 6 мг/сут и лорноксикам в дозе 16 мг/сут. Через 2 нед самочувствие пациентки значительно улучшилось, ТЗ практически исчезла, пальпация в ее проекции больше не приводила к формированию характерного болевого паттерна, регрессировали симптомы невроваскулярной компрессии. Были даны рекомендации по формированию адекватного двигательного стереотипа во время работы. Рекомендован правильный режим труда и отдыха, ограничение длительного пребывания за швейной машиной, обустройство рабочего места таким образом, чтобы спина опиралась на спинку стула, а локти - на подлокотники, которые должны находиться примерно на уровне рабочего стола.
Фибромиалгия[править | править код]
Фибромиалгия - хронический генерализованный болевой синдром, обычно сопровождающийся постоянным чувством усталости, депрессией, нарушениями сна, ощущением скованности в мышцах и суставах. Фибромиалгия более 100 лет назад была описана английским неврологом W. Govers, впервые употребившим термин «фиброзит» и обнаружившим участки в мышцах, пальпация которых вызывала боль. Этот симптом - болезненность при пальпации специфических «чувствительных» зон (англ. tender point) - считают решающим в диагностике фибромиалгии. Среди всех форм хронических болевых синдромов фибромиалгию считают ведущей по выраженности депрессии, степени дезадаптации и снижению качества жизни пациентов. Распространенность фибромиалгии в популяции составляет примерно 2-4%. Женщины трудоспособного возраста (от 20 до 40 лет) составляют 80% пациентов.
Общеприняты критерии диагностики фибромиалгии, предложенные Американским колледжем ревматологов.
- Распространенная хроническая боль в левой и правой половинах тела, выше и ниже талии или аксиальная боль (в шее, передней грудной стенке, спине), а также выше и ниже талии.
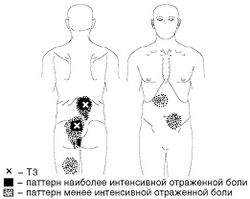
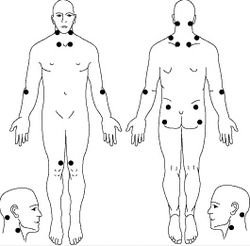
- Боль в не менее чем 11 из 18 парных двусторонних «чувствительных» зон, определенных в качестве диагностически значимых Американским колледжем ревматологов, при пальпации с давлением примерно в 4 кг (или до побледнения ногтевых пластинок) (Рис. 13):
- на затылке в месте прикрепления подзатылочных мышц;
- в области между поперечными отростками СV-СVII;
- посередине верхнего края трапециевидной мышцы;
- над лопаточной остью у медиального края лопатки;
- у второго грудинно-реберного сочленения;
- на 2 см дистальнее латерального надмыщелка плеча;
- вверху верхнелатерального квадранта ягодиц;
- позади большого вертела;
- на медиальной поверхности коленного сустава проксимальнее суставной щели.
Фибромиалгия обычно развивается постепенно, часто начинаясь с одной области тела. Определенной причины больные, как правило, назвать не могут, реже указывают на травму, эмоциональный стресс, инфекцию. Для заболевания характерны обострения и ремиссии, как правило, без влияния внешних факторов. Многие пациенты отмечают ощущение припухлости и скованности суставов (объективно отечность суставов обычно не выявляется), метеочувствительность (усиление болей в холодное время года).
Уже на ранних этапах изучения проблемы фибромиалгии отмечали значение психических нарушений. У 71% пациентов с фибромиалгией в анамнезе были указания на имевшиеся ранее депрессивные нарушения. При обследовании примерно у половины больных фибромиалгией присутствуют характерные жалобы на подавленное настроение, утрату интересов и чувства удовольствия, часты и дополнительные жалобы на снижение аппетита, нарушения сна.
Также при фибромиалгии обычно отмечается нарушение когнитивных функций. Пациенты испытывают трудности концентрации внимания, нарушения кратковременной памяти. Они хуже выполняют нейропсихологические тесты, связанные с переключением внимания [I. Russell, C. Bieber, 2006].
У пациентов с фибромиалгией часто (90% случаев) отмечают нарушения сна. Они проявляются жалобами на прерывистый поверхностный сон, трудности засыпания, повышенную двигательную активность во сне и частые пробуждения. Типична жалоба на отсутствие ощущения отдыха («восстановления») после ночного сна [I. Russell, C. Bieber, 2006; Г.Р. Табеева, 2000].
Выделяют первичную фибромиалгию, протекающую без видимой взаимосвязи с другими заболеваниями, и вторичную фибромиалгию, выступающую в качестве сопутствующего состояния при различной, чаще костно-мышечной патологии [F. Wolfe, J. Rasker, 2008], хотя клинически принципиальных различий между этими состояниями нет [В.В. Алексеев и др., 1999]. Фибромиалгия отмечается примерно у 1/3 пациентов, страдающих ревматоидным артритом, она встречается в 40% случаев системной красной волчанки, в 50% случаев синдрома Шегрена и часто сочетается с другими системными заболеваниями соединительной ткани. Фибромиалгия описана при боррелиозе, туберкулезе и сифилисе. При фибромиалгии в несколько раз чаще, чем в популяции, имеются головные боли напряжения, мигрени, «панические атаки», обмороки, гипервентиляционный синдром, кардиалгии, синдром раздраженного кишечника, туннельные невропатии, миофасциальные боли, абдоминалгии, синдром Рейно и артралгии. Поэтому дифференциальная диагностика фибромиалгии часто вызывает затруднения. Для целенаправленного поиска состояний, сопровождающихся развитием вторичной фибромиалгии важен подробный наследственный анамнез - наличие у ближайших родственников пациента ревматоидного артрита, системной красной волчанки, остеоартроза, болезни или синдрома Рейно.
Г.А. Иваничев (2007) рассматривает фибромиалгию как результат патологических явлений, начальным звеном которых становится формирование «мышечно-фасциального гипертонуса», который обладает свойствами генератора патологически усиленного возбуждения [по Г.Н. Крыжановскому]. В этом прослеживается сходство фибромиалгии и МФБС. Постепенно «генерализуясь», МФБС приобретает признаки фибромиалгии. Участием в патологическом процессе ретикуло-гипоталамо-лимбической системы объясняется наличие вегетативных нарушений. Соответственно, рассматривая формирование фибромиалгического синдрома, Г.А. Иваничев (2007), отмечает, что клинические проявления фибромиалгии легкой степени характеризуются местной болезненностью, локальным уплотнением и судорожным ответом при пальпации «мышечнофасциального гипертонуса» и местными вегетативными реакциями. Фибромиалгический синдром средней тяжести характеризуется наличием вышеуказанных симптомов, изменением двигательного стереотипа и наличием синдрома вегетативной дистонии, при выраженной фибромиалгии к имеющимся симптомам присоединяются диссомнические и эмоциональные нарушения (депрессия, астенический синдром).
В качестве дополнительных методов обследования с целью исключения вторичного генеза фибромиалгии пациенту рекомендуется лабораторное обследование, включающее общий анализ крови с исследованием концентрации гемоглобина, гематокрита, количества эритроцитов, тромбоцитов, лейкоцитов, состава лейкоцитарной формулы, СОЭ; развернутый биохимический анализ с определением концентрации глюкозы, кальция, общего белка, альбуминов, электролитов в крови (натрий, калий, карбонаты, хлориды), азота мочевины, креатинина, билирубина, общего белка, гормонов щитовидной и паращитовидной железы, активности ферментов печени (щелочной фосфатазы, аланинаминотрансферазы, аспартатаминотрансферазы, лактатдегидрогеназы, гамма-глутамилтрансферазы), креатинфосфокиназы; серологическое исследование, включающее маркеры вирусных гепатитов, ВИЧ, борелиоза; психологическое обследование и, при необходимости, сомнологическое обследование [I. Russell, C. Bieber, 2006; S. Carville и др., 2008].
Важно дифференцировать фибромиалгию от МФБС. Первая характеризуется хроническим течением с вовлечением множественных мышечных групп, распространением на большую часть тела и наличием болезненных («чувствительных») при пальпаторном воздействии зон, вызывающих только локальную боль. При МФБС существует тенденция к большей остроте процесса, вовлечению меньшего числа мышц и наличию ТЗ со всеми характерными для них признаками. Основные отличия двух указанных состояний приведены в табл. 6.
Таблица 6. Дифференциальная диагностика фибромиалгии и миофасциального болевого синдрома
|
Заболевание/ Признак |
Фибромиалгия |
Миофасциальный болевой синдром |
|
Возраст |
40-60 |
Взрослые всех возрастов |
|
Пол |
Ж>М |
ж=м |
|
Распространенность боли |
Диффузная |
Локальная |
|
Длительность |
Хроническое течение |
Хроническое с обострениями |
|
Болевые зоны |
Множественные (более 11) в мышцах, точках прикрепления сухожилий к костям, плотные мышечные тяжи обычно отсутствуют |
Единичные или множественные мышечные уплотнения (ТЗ), расположенные в вовлеченной мышце. Давление вызывает интенсивную отраженную боль в пределах определенной области |
|
Эффективность местных анестетиков |
Как правило, неэффективны |
Инъекция в триггерную точку, как правило, временно устраняет боль |
|
Локальное сокращение мышцы в ответ на надавливание |
Отсутствует |
Есть |
|
Симметричность |
Всегда двусторонность и часто симметричность |
Асимметричность и, как правило, односторонность |
|
Психические расстройства |
Частые, значительные: напряженность, тревога, депрессия, утомляемость, сниженный болевой порог, не зависят от мышечной болезненности |
Незначительные и вторичные по отношению к боли |
|
Нарушения сна |
Как правило, имеются; часто не связаны с болевым синдромом, отсутствует чувство отдыха после сна |
Могут быть в связи с болевым синдромом |
Этиология и патогенез[править | править код]
Этиология фибромиалгии остается неизвестной, а имеющиеся у больных морфологические, биохимические и психические изменения послужили основой для множества гипотез, как о генезе состояния, так и о нозологической его принадлежности. Так, в 40-е годы XX в. заболевание рассматривали в рамках «психогенного ревматизма», в 50-60-е годы - как психосоматическое расстройство. В 1980-е годы термин «фибромиалгия», обозначающий самостоятельное заболевание, прочно закрепился в литературе. Необходимо обращать внимание на значение психических травм в детстве и генетических факторов. Считают, что генетические факторы и факторы окружающей среды в одинаковой степени повышают риск развития фибромиалгии.
При однофотонной эмиссионной КТ (ОФЭКТ) при фибромиалгии выявляют снижение мозгового кровотока в ядрах таламуса и некоторых других структурах мозга, принимающих участие в обработке сенсорной информации, которое коррелирует с содержанием субстанции Р в цереброспинальной жидкости [J. Mountz и др., 1995]. Возможно, имеют значение изменения серотонинергической и норадренергической систем мозга, приводящие к недостаточности антиноцицептивных влияний. Количество чувствительных зон при фибромиалгии коррелирует со снижением концентрации серотонина в сыворотке крови, что соотносится с высокой терапевтической эффективностью антидепрессантов. При фибромиалгии отмечают усиление феномена «взвинчивания» нейронов задних рогов спинного мозга. Несколько нейрохимических медиаторов, возможно, участвуют в патогенезе фибромиалгии (субстанция Р, фактор роста нервных волокон, динорфин А, глутамат, оксид азота, серотонин, норадреналин). Первые пять из перечисленных веществ принимают участие в передаче афферентных ноцицептивных сигналов. Их концентрация увеличивается в биологических жидкостях пациентов с фибромиалгией. При первичной фибромиалгии фактор роста нервных волокон, по-видимому, опосредует повышение концентрации субстанции Р в цереброспинальной жидкости [I. Russell, 2006].
В патогенезе фибромиалгии, возможно, имеют значение цитокины. Отмечено повышение концентрации интерлейкина 8 (ИЛ-8) в сыворотке и ИЛ-6 в культуре лимфоцитов. Наибольшее увеличение концентрации ИЛ-8 отмечали при наличии сопутствующей депрессии, но оно также связано с длительностью заболевания и выраженностью боли [A. Gur и др., 2002].
Однозначной трактовки сочетания фибромиалгии и психических расстройств нет. Существует гипотеза, согласно которой фибромиалгия, возможно, одна из форм соматизированной депрессии. Отмечено, что пациенты с фибромиалгией преморбидно имеют личностные особенности, которые в ходе развития заболевания под воздействием различных причин трансформируются в депрессию, тревожные расстройства и ипохондрию. Согласно другой теории депрессия при фибромиалгии - следствие длительно существующей боли, и, наконец, возможно, существует общая патологическая основа для депрессии и фибромиалгии в виде нарушения деятельности нейрохимических систем мозга, участвующих в регуляции антиноцицептивной системы и эмоционального состояния. Возможно, что цитокины (ИЛ-8) принимают участие в развитии депрессии при фибромиалгии.
Генетические факторы, значение которых показано при фибромиалгии, в основном включают антигены системы гистосовместимости и локусы, кодирующие синтез серотониновых рецепторов типа 2А [I. Russell, 2006]. В стадии изучения находятся гены, принимающие участие в стрессовом ответе. Среди факторов окружающей среды, которые способны вызывать или ухудшать течение фибромиалгии, выделяют ранние жизненные стрессы и целый ряд биологических стрессоров, включая инфекции, физическую травму и некоторые типы эмоционального стресса.
Причина формирования чувствительных зон остается неизвестной. Чувствительные зоны при фибромиалгии, в отличие от ТЗ при МФБС, считают проявлениями центральной сенситизации и сами по себе они не вызывают ноцицептивной боли. В области ТЗ при МФБС выявляют биохимические изменения, которые не отмечаются в чувствительных зонах при фибромиалгии [H. Bliddal, 2008].
При фибромиалгии определяется избыточная α-активность на ЭЭГ (электроэнцефалография) во время IV стадии медленноволнового сна (так называемый α-Δ сон), что отражает недостаточность торможения активности нейрофизиологических систем бодрствования во время сна. Можно отметить, что у здоровых испытуемых, подвергшихся депривации сна, отмечались симптомы (ноющие боли в мышцах, чувство недостаточного отдыха после сна), аналогичные таковым у больных фибромиалгией, причем эти симптомы наблюдали лишь у тех пациентов, в повседневной жизни которых отсутствовали регулярные физические нагрузки.
Из гормональных нарушений при фибромиалгии важным считают снижение концентрации в крови гормона роста, максимум секреции которого приходится на первый эпизод глубокого медленноволнового сна (Δ-сна). Введение гормона роста пациентам с фибромиалгией показало эффективность в отношении уменьшения выраженности ее симптомов в плацебо-контролируемом исследовании [R. Bennett и др., 1998]. Также у пациентов с фибромиалгией обычно обнаруживают гиперкортицизм, у них в 2,5 раза чаще встречается нарушение функций щитовидной железы.
Вероятно, фибромиалгия представляет собой состояние, при котором нарушается взаимодействие ноцицептивной и антиноцицептивной систем. При этом ключевое значение имеет дефицит нисходящих ингибирующих боль влияний, который опосредован генетическими, эндокринными и средовыми факторами, что способствует формированию центральной сенситизации, усилению ноцицептивной импульсации на различных уровнях ЦНС.
Лечение[править | править код]
Специфического лечения фибромиалгии нет, рекомендуется сочетание как немедикаментозных, так и медикаментозных методов (табл. 7) [S. Carville и др., 2008]. Пациенту до назначения препаратов необходимо разъяснить суть заболевания. Важно добиться понимания пациентом взаимоотношений между болью, настроением, стрессом и факторами, касающимися семейных отношений. Следует настоятельно рекомендовать как взрослым пациентам, так и детям сохранять оптимальную профессиональную и учебную активность. Полезны регулярные занятия ЛФК (не реже 2 раз в неделю) с использованием аэробных упражнений, но важно предупреждать пациентов о необходимости выполнять упражнения до появления легкого ощущения дискомфорта, а не до боли. Для немедикаментозного лечения фибромиалгии также рекомендованы следующие методики: бальнеотерапия, массаж, методика биологической обратной связи (по поверхностной ЭМГ). Особое внимание рекомендуют уделять гигиене сна как важной составляющей части терапевтического плана, психотерапевтической и лекарственной коррекции тревожных и депрессивных расстройств.
Таблица 7. Лечение фибромиалгии
|
Лекарственные методы | |||
|
Препарат |
Доза начальная/ терапевтическая |
Комментарии | |
|
Амитриптилин |
10 мг на ночь/ 25-50 мг на ночь |
В нескольких РКИ показано уменьшение интенсивности боли и нарушений сна | |
|
Флуоксетин |
20 мг в сутки/ 20-80 мг в сутки |
В двух РКИ показано улучшение сна и уменьшение интенсивности боли (последнее - при дозе более 20 мг/сут) | |
|
Дулоксетин |
30-60 мг/60-120 мгв сутки |
В пяти РКИ - уменьшение интенсивности боли | |
|
Милнаципран |
25 мг в сутки/100 мг 2 раза в сутки |
В одном РКИ - уменьшение интенсивности боли | |
|
Трамадол |
50 мг/50-100 мг 3 раза в сутки |
В одном из двух РКИ показано умеренное уменьшение интенсивности боли | |
|
Прегабалин |
50 мг 3 раза в сутки/ 100-150 мг 3 раза в сутки |
РКИ показало уменьшение интенсивности боли при применении препарата в дозе 450 мг/сут, уменьшение выраженности утомляемости и нарушений сна отмечалось при дозе 300 мг/сут и более | |
|
Нелекарственные методы | |||
|
Сохранение оптимальной профессиональной и учебной активности | |||
|
Гигиена сна | |||
|
Биологическая обратная связь | |||
|
Массаж |
Приносит временное облегчение. Эффект редко сохраняется более 1-2 сут | ||
|
Психотерапия |
Необходимо разъяснить доброкачественную природу заболевания, взаимоотношение между болью, настроением,стрессом | ||
|
Нелекарственные методы | |||
|
ЛФК |
Упражнения могут увеличивать интенсивность боли, поэтому должны быть относительно легкими. Увеличение уровня физической активности должно происходить постепенно и начинаться с ходьбы, занятий на велотренажере, плавания в течение 5-10 мин 3 раза в неделю с постепенным повышением нагрузки до 30 мин через день или до 4 раз в неделю. При этом может отмечаться небольшое увеличение интенсивности боли. Улучшение достигается в течение 1-2 мес. По отдельным данным, водные процедуры (акватерапию) пациенты переносят лучше, чем аэробные упражнения | ||
Медикаментозное лечение (с позиций доказательной медицины приведенные ниже данные относятся к рекомендациям уровня A) включает в себя коррекцию нарушений сна, лечение депрессии и усталости. Нарушения сна у пациентов с фибромиалгией обусловлены различными причинами, но определено, что большинство из них связаны с низким содержанием серотонина в мозге, снижением секреции гормона роста и наличием генерализованной боли. Препараты из группы трициклических антидепрессантов (ТЦА), помимо антидепрессивного эффекта, помогают улучшить сон. Низкая концентрация серотонина и норадреналина коррелирует с возникновением депрессии, мышечной боли и усталостью. Применение ТЦА, в частности амитриптилина, помогает уменьшить эти симптомы. Рекомендовано назначение амитриптилина в дозе 25-50 мг/сут за 2-3 ч до сна, что дает возможность получить максимальный седативный эффект с минимальным эффектом последействия. При необходимости можно увеличивать дозу до 50-75 мг/сут в течение следующих недель. Для лечения фибромиалгии эффективен прегабалин в дозе 600 мг/сут и длительное применение (12 мес) милнаципрана в дозе 100-200 мг/сут [L. Arnold, 2007; Г.Р. Табеева, Ю.Э. Азимова, 2007].
Препарат выбора у детей и подростков - флуоксетин; перед началом лечения рекомендована консультация психиатра. Для дополнительного устранения боли на короткое время можно назначать трамадол (по 50-100 мг 2-4 раза в сутки). Использование других опиоидных анальгетиков не рекомендуют, так как в контролируемых исследованиях на фоне выраженных побочных эффектов положительного влияния в виде уменьшения боли зарегистрировано не было, что подтверждает значение центральной неврогенной дисфункции в развитии хронической боли при фибромиалгии. НПВС также не рекомендованы к использованию, так как нет доказательств их эффективности. В небольшом количестве исследований была продемонстрирована эффективность инъекционного введения препаратов в чувствительные зоны. Не рекомендуют использовать глюкокортикоиды для лечения фибромиалгии, если при обследовании не выявлено сопутствующих воспалительных скелетно-мышечных заболеваний.
Для лечения фибромиалгии рекомендовано применение и комбинированных методов (табл. 8). В исследовании, завершенном в 2002 г., был выявлен синергизм флуоксетина и амитриптилина при лечении пациентов с фибромиалгией, в том числе в отношении уменьшения выраженности депрессии. Таким образом, при отсутствии достаточного эффекта от лечения адекватными дозами амитриптилина можно добавить к лечению препарат из группы селективных ингибиторов обратного захвата серотонина (флуоксетин) в дозе 20 мг утром. Для пациента, у которого наиболее выражены боль и депрессия, дулоксетин может быть препаратом первого выбора. Дулоксетин также применяют при интенсивной боли, когда симптомы депрессии отсутствуют или выражены минимально, так как препарат обладает эффективностью в отношении купирования боли, независимо от наличия у пациента депрессии. В случаях, когда основными расстройствами становятся боль и нарушения сна, оправдано применение прегабалина в виде монотерапии, а также в сочетании с дулоксетином или милнаципраном. У пациентов с выраженным болевым синдромом в отсутствие депрессии и жалоб на нарушение сна возможно применение трамадола. Если отмечаются редкие нарушения сна, возможно добавление легких седативных средств. В этом же случае можно назначить прегабалин и дулоксетин в виде монотерапии. При умеренной выраженности боли и депрессии оптимальной считают монотерапию дулоксетином или милнаципраном [I. Russell, 2006]. Следует избегать сочетания селективных ингибиторов обратного захвата серотонина и трамадола из-за повышения риска развития серотонинового синдрома.
Таблица 8. Схемы медикаментозного лечения фибромиалгии, в зависимости от преобладания в клинической картине болевого синдрома, депрессии и нарушений сна (по Russell I. J., 2006, с изменениями).
|
Ведущие клинические синдромы |
Препарат / комбинация препаратов | ||
|
Боль |
Депрессия |
Диссомния | |
|
++ |
++ |
+ |
дулоксетин или милнаципрам; амитриптилин + флуоксетин |
|
+++ |
+ |
+++ |
прегабалин; грегабалин + дулоксетин |
|
+++ |
+++ |
+++ |
прегабалин + дулоксетин или милнаципрам |
|
+++ |
+ |
+ |
трамадол;трамадол+парацетамол; грегабалин; дулоксетин |
Другие подходы к лечению фибромиалгии включают в себя коррекцию коморбидных расстройств. При неэффективности приведенных выше сочетаний препаратов для коррекции нарушений сна, а также для уменьшения выраженности тревожных расстройств возможно добавление к лечению бензодиазепинов (альпразолам в начальной дозе 0,125 мг 3 раза в сутки с увеличением до 1-1,5 мг/сут в течение 5-7 сут или достижения эффекта на меньшей дозе, клоназепам в начальной дозе 0,5 мг на ночь с увеличением до 1-2 мг). Показана эффективность зопиклона и золпидема для коррекции бессонницы, при этом последний целесообразно назначить через день для уменьшения вероятности развития синдрома отмены. Учитывая, что снотворные препараты не влияют на другие проявления фибромиалгии, нарушения сна следует начинать лечить с прегабалина, который уменьшает и интенсивность боли.
Лечение повышенной усталости включает устранение нарушений сна и депрессии, а также возможных сопутствующих расстройств (гипотиреоза, анемии, хронических инфекционных заболеваний). Легкая физическая нагрузка обычно уменьшает выраженность усталости. Пациентам, ощущающим себя «изношенными» к концу дня, рекомендуют сочетать дневную активность с короткими периодами отдыха. Если ощущение утраты сил или дневной сонливости отчасти связано с принимаемыми пациентом снотворными препаратами или амитриптилином, добавление флуоксетина в небольших дозах в утреннее время может уменьшить эти проявления [I. Russell, 2006].
Прием кофеина для уменьшения выраженности и усталости не оправдан, так как его стимулирующее действие не постоянно и кратковременно.
Для лечения сопутствующего синдрома раздраженной толстой кишки необходимо применять коррекцию пищевых пристрастий - исключить кофеинсодержащие вещества, алкоголь, жирную пищу, продукты, содержащие углекислоту. Боль, связанная с этим состоянием, хорошо купируется приемом антиспастических препаратов и ТЦА. В случаях преобладания в клинической картине диареи рекомендуют назначение симптоматических средств, например лоперамида (2-8 мг/сут). При преобладании запоров целесообразно соблюдение диеты с использованием грубой волокнистой пищи, отрубей, которые нормализуют скорость пассажа пищи.
В отдельных случаях при наличии выраженной симптоматики, коморбидных психических расстройств, отсутствии комплаентности пациента или неэффективности лечения в амбулаторных условиях рекомендуют лечение в специализированных учреждениях: психиатрических, психотерапевтических, альгологических отделениях или реабилитационных центрах [S. Carville и др., 2008; D. Goldenberg и др., 2004].
Клинический пример
Пациентка К., 45 лет, домохозяйка. Обратилась в клинику с жалобами на постоянные ноющие боли в мышцах шеи, плечевого пояса, пояснице, усиливающиеся даже при относительно небольшой физической нагрузке (приготовление пищи, поход в магазин без подъема тяжестей), уменьшающиеся после отдыха. Также пациентку беспокоила повышенная утомляемость, ощущение скованности в мышцах и суставах, особенно по утрам. Отмечались нарушения сна (часто просыпалась по ночам, в основном под утро), отсутствие чувства отдыха после сна. Отмечает боли в правом верхнем квадранте живота, которые длятся от нескольких минут до нескольких часов, реже - в течение всего дня, метеоризм, эпизоды диареи, которые чередовались с запорами. Пациентка высказывала опасение относительно возможной злокачественной причины болей в брюшной полости, несмотря на опровергающие это данные многочисленных методов обследования. Боли в мышцах спины появились 10 лет назад без видимых причин, боли в животе - 7 лет назад. С этого же времени периодически (до 1-3 раз в неделю) стали беспокоить головные боли в виде ощущения «стягивания головы обручем» умеренной интенсивности, не сопровождавшиеся тошнотой или рвотой, фоно- и фотофобией. Два года назад присоединилось ощущение утренней скованности в суставах рук, больше кистей. Пациентка начала уставать от обычной домашней нагрузки, выполняла ее только в минимальном объеме. Ночной сон был поверхностным и не приносил ощущения полного отдыха. Из-за постоянных ноющих болей в спине не могла долго ходить или стоять. При обращении к врачам поставлены диагнозы «остеохондроз», «хронический гастрит», «хронический холецистит». Назначена мануальная терапия и НПВС (мелоксикам, диклофенак) - без положительного эффекта. Пациентка пробовала посещать фитнес-центр, но отмечала выраженное усиление боли в спине при выполнении даже относительно легких упражнений в течение 20-30 мин и прекратила занятия. Больная принимала клоназепам в дозе 1 мг на ночь, который несколько улучшал сон и уменьшал выраженность боли в животе, но не влиял на боль в мышцах. При беседе с больной обращал на себя внимание сниженный фон настроения, канцерофобия. Изменений в неврологическом статусе не выявлено. При пальпации мышц туловища и конечностей выявлены чувствительные зоны, расположенные в характерных местах: билатерально в области затылка у субокципитальной мышцы, билатерально посередине верхнего края трапециевидной мышцы, билатерально у второго костнореберного сочленения, билатерально в верхних квадрантах ягодиц и позади большого вертела, на латеральной поверхности локтевого и медиальной поверхности коленного суставов. Всего было обнаружено 14 чувствительных зон. Клинические анализы крови и мочи, биохимические анализы крови, ревмопробы - без отклонений от нормы.
Имеющееся у больной расстройства можно рассматривать как фибромиалгию с сопутствующими депрессивными расстройствами и инсомнией, сопровождающуюся головными болями напряжения и синдромом раздраженной толстой кишки. На фоне лечения прегабалином в дозе 300 мг/сут в сочетании с дулоксетином (60 мг/сут), постепенного увеличения уровня физической активности, ЛФК в теплом бассейне через 1,5 мес самочувствие пациентки улучшилось:существенно уменьшилась интенсивность боли в спине и конечностях, меньше стало беспокоить чувство утомляемости, улучшилось настроение и качество ночного сна, головные боли регрессировали до 1-2 эпизодов в месяц. Практически перестали беспокоить боли в животе, но сохранялась склонность к запорам, которые уменьшились при соблюдении диеты с использованием грубой волокнистой пищи. Через 4 мес после начала лечения пациентка смогла вернуться к удовлетворяющему ее уровню повседневной активности, эпизодически испытывая легкую боль в мышцах при длительном стоянии или пребывании на холоде.
Спондилоартропатические болевые синдромы[править | править код]
Межпозвоночные (дугоотростчатые, фасеточные) суставы - потенциальные источники боли в шее, грудном отделе и поясничнокрестцовой области (обычно - в шейной и поясничной областях), надплечьях и в ногах. Кроме этого, отраженная от дугоотростчатых суставов шейного отдела позвоночника боль может ощущаться в голове (цервикогенная головная боль). Вмешательства на дугоотростчатых суставах - вторая по частоте манипуляция в специализированных центрах по лечению боли в США. Существует много причин, приводящих к поражению суставов позвоночника. Боль в межпозвоночных суставах может быть связана с их острым или хроническим инфекционным поражением (например, туберкулезным спондилитом), системными воспалительными заболеваниями (ревматоидным артритом, спондилоартритами), метаболическими расстройствами (подагрой и псевдоподагрой). Потенциальными причинами боли в спине могут быть подвывихи, разрывы капсулы и хряща суставов, их микропереломы, но роль указанных изменений остается неизвестной. Наиболее частой причиной боли в спине, связанной с поражением дугоотростчатых (фасеточных) суставов, принято считать их дистрофические изменения (спондилоартроз, или фасеточный синдром).
Фасеточный синдром[править | править код]
Несмотря на множество исследований, посвященных проблеме фасеточного синдрома, эта диагностическая категория до сих пор не бесспорна. В первую очередь это связано с отсутствием четких клинических симптомов, характерных для дегенеративного поражения дугоотростчатых суставов. Характеристики боли, отраженной от дугоотростчатых суставов, изучены в основном при участии здоровых добровольцев, которым вводили внутрисуставно рентгенконтрастные вещества, растягивающие капсулу сустава. На Рис. 14 обозначена локализация боли, отраженной от суставов шейного отдела позвоночника. Можно отметить, что зоны отраженной боли от соседних суставов значительно перекрываются, а также напоминают паттерны боли, отраженной от мышц [H. Bliddal, M. Curatolo, 2008].
Биомеханика и патофизиология[править | править код]
Боль, связанная с поражением дугоотростчатых суставов, может отмечаться изолированно или сочетаться с другими биомеханическими нарушениями. К последним относят дегенеративный спондилолистез, связанный с сагиттальной ориентацией дугоотростчатых суставов в поясничном отделе позвоночника (Рис. 15). При этом состоянии вращательные нагрузки приводят к грубым изменениям как в дугоотростчатых суставах, так и в межпозвоночном диске. Поскольку межпозвоночный диск и дугоотростчатые суставы соответствующего ему уровня совместно обеспечивают движения в ПДС, их обычно обозначают в литературе как «трехсуставной комплекс». Дегенеративные изменения в межпозвоночном диске приводят к возрастанию нагрузки на дугоотростчатые суставы, и наоборот, поражение дугоотростчатых суставов может ускорять дегенерацию диска.
Дугоотростчатые суставы имеют типичное строение и состоят из суставного хряща, синовиальной оболочки, синовиальной жидкости и капсулы. Дугоотростчатые суставы формируются при соединении нижнего суставного отростка вышележащего позвонка с верхним суставным отростком нижележащего позвонка (Рис. 16). В поясничном отделе позвоночника нижний суставной отросток расположен медиальнее верхнего. В шейном отделе позвоночника суставные поверхности, как правило, ориентированы во фронтальной плоскости, при этом суставная поверхность верхнего суставного отростка направлена кверху и кзади, а нижнего суставного отростка - кпереди и книзу под углом 45°.
Каждый суставной отросток покрыт слоем гиалинового хряща толщиной 2-4 мм. Такая толщина необходима для противостояния большим нагрузкам. При компрессии суставных поверхностей из хряща выходит вода, при устранении давления она «всасывается» обратно. Осуществлению движений в нескольких плоскостях помогает способность суставного хряща деформироваться и возвращать выпукло-вогнутую форму суставной поверхности. Суставная поверхность нижнего суставного отростка вышележащего позвонка имеет выпуклую форму, суставная поверхность верхнего суставного отростка - вогнутую. Сзади капсула сустава утолщена и укреплена волокнами многораздельной мышцы. Волокна капсулы дугоотростчатого сустава ориентированы перпендикулярно его плоскости. Это вместе с особенностями строения суставных поверхностей благоприятствует движениям преимущественно в сагиттальной плоскости (сгибанию и разгибанию). Также возможны ограниченные по амплитуде движения во фронтальной и горизонтальной плоскости.
Исследование анатомии дугоотростчатых суставов, опубликованное в 1940 г. T. Horwitz и R. Smith, свидетельствует о том, что в поясничном отделе позвоночника дугоотростчатые суставы на уровне LIV-LV имеют более фронтальную ориентацию (70° по отношению к сагиттальной плоскости) по сравнению с суставами на уровне LII-LIII и LIII-LIV, которые ориентированы более параллельно по отношению к сагиттальной плоскости (под углом 40°) [цит. по L. Giles, 1997]. При увеличении возраста дугоотростчатые суставы становятся ориентированы более сагиттально. Часто (у 20-40% популяции) отмечается врожденная асимметрия ориентации суставных поверхностей фасеточных суставов на одном уровне (аномалия тропизма), клиническое значение которой остается предметом дискуссии.
Показано, что дугоотростчатые суставы содержат большое число инкапсулированных и неинкапсулированных нервных окончаний. Наличие низкопороговых механоцепторов в капсуле сустава свидетельствует в пользу того, что она выполняет и проприоцептивную функцию. Кроме субстанции Р и кальцитонин-ген родственного пептида, значительное количество нервных окончаний содержит нейропептид Y - вещество характерное для симпатических эфферентных волокон. При дегенеративном поражении дугоотростчатых суставов в хряще и синовиальной капсуле определяются медиаторы воспаления: простагландины, ИЛ-1 и ИЛ-6, ФНО-α [S. Cohen, 2007].
Основная функция дугоотростчатых суставов - поддержка и стабилизация позвоночника при всех возможных в нем видах движений. Сближение суставных отростков происходит когда нижний суставной отросток вышележащего позвонка смещается вперед относительно нижележащего позвонка при воздействии сил, направленных на смещение позвонка кпереди (Рис. 17). Такие же силы воздействуют на область поясничного отдела из-за выраженного лордоза. При этом наибольшей перегрузке подвержены ПДС на уровне LIV-LV и LV-SI. Сила, направленная на смещение позвонка кпереди, оказывает большее влияние на позвоночник в положении стоя по сравнению с положением сидя из-за уменьшения степени лордоза в последнем случае. Этой силе может противостоять только часть суставной поверхности суставных отростков, которая ориентирована во фронтальной плоскости.
Сближение суставных отростков происходит в случаях, когда суставной отросток вышележащего позвонка смещается вперед относительно нижележащего позвонка при воздействии сил, направленых на смещение вышележащего позвонка кпереди (воздействие гравитации, усиление лордоза)
Наиболее хорошо изучены особенности биомеханики в поясничном отделе позвоночника в ПДС LIV-LV, так как он наиболее подвержен дегенеративным изменениям. Амплитуда движений в сагиттальной плоскости в этом сегменте составляет 20-25°, такая же амплитуда характерна и для сегмента LV-SI. При этом ротация в каждом из суставов на нижнем поясничном уровне возможна лишь в пределах 3-5°. При ротации дугоотростчатый сустав на одной стороне испытывает компрессионное воздействие, в то время как на другой - растяжение. Если достигнут максимально возможный объем движения в суставе при ротации, ось вращения смещается кзади от дугоотростчатых суставов и основная нагрузка при этом ложится на межпозвоночный диск. Соответственно, резкие скручивающие движения в поясничном отделе позвоночника при фиксированном тазе могут приводить к травме межпозвоночных суставов и диска. Основные мышцы, противостоящие нагрузке на позвоночник при ротационных движениях, - внутренние и наружные косые мышцы живота. Кроме них, имеют значение многораздельные, подвздошно-поясничные мышцы, квадратные мышцы поясницы, мышца, выпрямляющая позвоночник [J. Porterfield, 1998].
Дугоотростчатые суставы принимают на себя 10-20% компрессионной нагрузки и 50% нагрузки, связанной с противодействием смещению позвонка кпереди, при нахождении человека в положении стоя. При наклоне вперед на небольшой угол основная нагрузка ложится на межпозвоночный диск, но по мере увеличения амплитуды движения возрастает воздействие нагрузки и на фронтальную часть поверхности дугоотростчатых суставов. При разгибании нагрузка на межпозвоночные суставы также возрастает (Рис. 18).
При движениях позвоночника межпозвоночный диск и дугоотростчатые суставы выступают как единое целое. Для примера можно рассмотреть биомеханику поясничного отдела позвоночника при наклоне вперед, так как это движение наиболее часто встречается в повседневной жизни. Вначале сгибание возникает на уровне сегмента L4. При этом центр тяжести смещается кпереди и увеличивается внутридисковое давление на уровне LIV-LV. Относительно несжимаемое пульпозное ядро в этом случае выполняет функцию «центра вращения». По мере продолжения движения на позвоночник начинает действовать сила, направленная на смещение вышележащего позвонка кпереди. Ей противостоят косые волокна фиброзного кольца, расположенные в латеральных отделах диска, и фронтальная плоскость суставной поверхности дугоотростчатых суставов. Если волокна фиброзного кольца остаются высокоэластичными и хорошо «натянутыми», то суставной хрящ нижнего суставного отростка LIV начинает соприкасаться с суставным хрящом верхнего суставного отростка LV позвонка и скользить вдоль него вверх. Его избыточному движению в этом направлении препятствует капсула сустава и связочная система задних отделов позвоночного столба. По мере увеличения угла наклона для стабилизации ПДС подключаются волокна переднего и заднего отделов фиброзного кольца, межостистая связка и глубокие отделы мышцы, выпрямляющей позвоночник, прикрепляющейся к поперечным отросткам и гребню подвздошной кости, которая при синхронном сокращении уменьшает компрессионное воздействие на фронтальную плоскость дугоотростчатых суставов. При наклоне вперед более чем на 40° отмечается релаксация мышцы, выпрямляющей позвоночник (феномен «флексии-релаксации»). По мере продолжения движения в него включается сегмент LV-SI. В этом сегменте силе, направленной на смещение вышележащего позвонка кпереди, противостоит еще одна структура - подвздошно-поясничная связка. Как только тело LV оказывает компрессионное воздействие на передние отделы межпозвоночного диска LV-SI, костные структуры, расположенные кзади, включая поперечные отростки, смещаются кверху и кпереди по отношению к гребню подвздошной кости. Это приводит к натяжению подвздошно-поясничной связки, прикрепляющейся к гребню подвздошной кости и поперечным отросткам пятого поясничного позвонка. Подвздошно-поясничная связка стабилизирует сегмент LV-SI не только при флексии, но и при ротации. Отсутствие такого пассивного «стабилизатора» на уровне Liv-Lv, возможно, предрасполагает к его более частой перегрузке и повреждению [L. Giles, 1997].
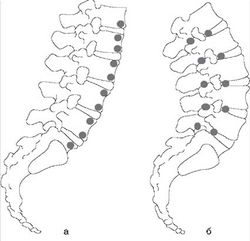
Показано, что наиболее оптимально поясничный отдел позвоночника противостоит компрессионным силам в положении флексии на 60-80°. Этот угол наклона обеспечивается при подъеме тяжести с «прямой» спиной. Поскольку при попытке поднимать груз с «прямой» спиной на самом деле отмечается вращение таза кзади и поясничный отдел позвоночника принимает оптимальный угол наклона вперед [J. Porterfield, 1998], сохранение лордоза в этом случае практически невозможно.
Дегенерация гиалинового хряща дугоотростчатого сустава - следствие дистрофических изменений межпозвоночного диска, поскольку снижение высоты последнего приводит к увеличению нагрузки на межпозвоночные суставы. Дальнейшее снижение высоты диска приводит к возникновению подвывихов в дугоотростчатых суставах, когда нижняя часть нижнего суставного отростка начинает соприкасаться с пластинкой дуги нижележащего позвонка или ее межсуставной частью (участок рядом с местом соединения ножки и дуги). Считают, что перегрузке дугоотростчатых суставов способствует слабость брюшной стенки. Она сопровождается наклоном таза кпереди и увеличением поясничного лордоза, формирующееся при этом разгибание в поясничном отделе увеличивает компрессионное воздействие на дугоотростчатые суставы (Рис. 19). Разница длины ног приводит к относительной перегрузке межпозвоночного сустава на стороне длинной ноги. Напряжение мышц передней поверхности бедра также вызывает увеличение компрессионного воздействия на сустав, так как ограничивает разгибание бедра при ходьбе, приводя к компенсаторному вращению таза [J. Porterfield, 1998].
В ранних исследованиях, основанных на анализе клинических особенностей болевого синдрома и результатах внутрисуставных блокад с местными анестетиками, были подробно описаны особенности боли, связанной с поражением дугоотростчатых суставов. Фасеточный синдром на поясничном уровне был описан Т. Helbig и С. Lee (1988). Эти авторы считали, что при фасеточном синдроме боль локализуется паравертебрально в поясничной области, она может иррадиировать в паховую область или бедро и провоцироваться разгибательно-вращательными движениями. Более поздние и методологически более точные исследования не подтвердили наличия типичных клинических характеристик боли, связанной с поражением дугоотростчатых суставов [C. Brummett, C. Cohen, 2008]. При обследовании пациентов с болью в поясничной области с применением диагностических блокад дугоотростчатых суставов было показано, что практически не существует специфических клинических характеристик, отличающих пациентов с положительным эффектом блокады от тех, у кого она оказалась неэффективной. Так, исследование M. Revel и др. (1992) выявило несколько факторов, связанных с эффективностью блокад дугоотростчатых суставов: возраст пациентов старше 65 лет, отсутствие усиления боли при кашле, при максимальном разгибании позвоночника, наклоне и максимальном наклоне вперед, выпрямлении после наклона вперед, при разгибательно-вращательных движениях и ее уменьшение в положении лежа. Методы мануальной диагностики, выявляющие патологию дугоотростчатых суставов в шейном отделе при сравнении с результатами блокад под рентгенологическим контролем, демонстрируют чувствительность 88% и относительно низкую специфичность - 39% [W. King и др., 2007].
В подавляющем большинстве случаев поражение дугоотростчатых суставов - результат многолетней повторяющейся травматизации, связанной с неоптимальным объемом движений в них и повышением нагрузки на эти суставы из-за дегенерации межпозвоночных дисков. В отдельных случаях поражение дугоотростчатых суставов может развиваться остро, например при хлыстовой травме шеи, спортивных травмах, когда отмечается повреждение сустава из-за гиперфлексии, избыточной ротации или тракционного механизма воздействия. По-видимому, гиперэкстензионный механизм редко становится причиной травматического поражения дугоотростчатых суставов. Частота поражения дугоотростчатых суставов у пациентов с хронической посттравматической болью в шейном отделе позвоночника составляет 60%. Однако травма, предшествующая возникновению боли в шейном отделе позвоночника, отмечается менее чем в 13% случаев [H. Bliddal, 2008].
Для диагностики фасеточного синдрома применяют блокаду медиальной ветви (БМВ) задней первичной ветви спинномозгового нерва или внутрисуставные инъекции местного анестетика под контролем КТ [S. Dreyer, P. Dreyfuss и др., 1996; P. Dreyfuss, S. Dreyer, 2003; G. Sowa, 2005]. Исчезновение боли в течение нескольких минут после проведения диагностической блокады считают стандартом для подтверждения связи боли в спине с патологией дугоотростчатых суставов. Показано, что диагностические блокады без соответствующего рентгенологического контроля приводят к ложноположительным результатам в 25-41% случаев [L. Manchikanti и др., 1999, 2000; A. Schwarzer и др., 1994, 1995]. Это связано с высокой частотой плацебочувствительности и с тем, что введение местного анестетика в проекцию сустава без рентгенологического контроля также может устранять и другие источники боли, например ТЗ в паравертебральных мышцах. При проведении блокад для исключения ложно-положительных результатов желателен плацебо-контроль (введение изотонического раствора или имитация введения анестетика). Распространенность боли, связанной с поражением дугоотростчатых суставов, значительно варьирует в зависимости от критериев, выбранных для ее диагностики. Считают, что наиболее часто поражаются суставы поясничного отдела позвоночника. С меньшей частотой фасеточный синдром возникает на шейном уровне, еще реже - на грудном. Большинство авторов сходятся во мнении, что частота фасеточного синдрома у пациентов с хронической болью в поясничной области составляет от 30 до 60%. Наиболее часто поражаются суставы на уровне LV-SI, LIV-LV, и LIII-LIV. Более высоко расположенные суставы поясничного отдела позвоночника редко становятся источником боли в спине. О распространенности фасеточного синдрома у пациентов с болями в шейном и грудном отделах позвоночника известно меньше. При хронической боли в шее частота патологии дугоотростчатых суставов, установленная с применением диагностических блокад, составляет 49-60%. Наиболее часто поражаются суставы на уровне СII-СIII и СV-СVI. Распространенность фасеточного синдрома среди пациентов с болью в грудном отделе позвоночника составляет 42-48% [С. Brummett, S. Cohen, 2008].
Частота дистрофических изменений в дугоотростчатых суставах по данным КТ исследований варьирует от 40 до 85% и увеличивается с возрастом. В асимптомной популяции дистрофические изменения суставов поясничного отдела позвоночника выявляют с частотой 8-14% [D. Weishaupt и др., 1998; M. Jensen и др., 1994; S. Wiesel и др., 1994]. При МРТ поясничного отдела позвоночника у 60 здоровых людей в возрасте от 20 до 50 лет отмечались частые изменения межпозвоночных дисков (выбухание - 62%, протрузии - 67% случаев) при отсутствии патологии со стороны дугоотростчатых суставов. В ряде случаев в дугоотростчатых суставах могут формироваться синовиальные «псевдокисты», которые приводят к кальцификации и асимметричной гипертрофии суставов. «Псевдокисты» могут оказывать компрессионное воздействие на невральные структуры позвоночного канала (Рис. 20). Они определяются при МРТ от 2 до 9,5% случаев боли с болью в поясничной области. Однако не получено убедительных данных о связи изменений, выявляемых при нейровизуализации, с клиническими проявлениями дисфункции дугоотростчатых суставов [C. Brummett, S. Cohen, 2008].
Имеются противоречивые данные о связи нейровизуализационных изменений в дугоотростчатых суставах с прогнозом эффективности диагностических блокад. В частности, G. Carrera и A. Williams (1984) свидетельствуют о зависимости эффекта диагностических блокад с относительно большим количеством местного анестетика (2-4 мл) от выраженности дистрофических изменений дугоотростчатых суставов по данным КТ. Более крупное исследование с участием 390 пациентов не обнаружило взаимосвязи между рентгенологическими изменениями и эффективностью блокад [R. Jackson и др., 1988]. Мультицентровое исследование с участием пациентов, которым проводили радиочастотную денервацию (РЧД) дугоотростчатых суставов на основании положительного эффекта БМВ, не выявило связи дистрофических изменений в дугоотростчатых суставах, по данным МРТ, с эффективностью данного метода лечения при ее оценке через 6 мес [S. Cohen и др., 2007]. В целом можно отметить, что рутинное использование методов нейровизуализации для диагностики клинически значимой патологии дугоотростчатых суставов нецелесообразно.
Отсутствие взаимосвязи клинических особенностей и данных нейровизуализации с эффективностью диагностических блокад суставов и БМВ у пациентов с болью в спине привело практически к формированию общепринятой точки зрения, что подтверждение как источника боли патологии дугоотростчатого сустава, возможно только при положительном эффекте диагностических блокад, проведенных под визуализационным контролем. Диагностические блокады
Внутрисуставную блокаду и БМВ считают одинаково ценными диагностическими процедурами. Доказательство этого основано на данных двух сравнительных исследований [R. Marks и др., 1992; T. Nash, 1990]. В то же время есть несколько факторов, потенциально снижающих диагностическую ценность БМВ. Еще в 30-е годы XX в. J. Kellgren показал, что при инъекции в мягкие ткани 0,5 мл жидкости распространяются на область, размером примерно 6 см2 [по C.M. Brummett, 2008]. Таким образом, введение 0,5 мл местного анестетика потенциально может анестезировать не только медиальную ветвь задней первичной ветви спинномозгового нерва, но и латеральную и промежуточную ветви. Поскольку последние иннервируют несколько структур позвоночника, которые сами по себе могут быть источниками боли (паравертебральные мышцы, связки, КПС), БМВ может уменьшать боль, непосредственно не связанную с дугоотростчатыми суставами и, следовательно, приводить к ложноположительной диагностике фасеточного синдрома. Считают, что частота ложноположительных результатов БМВ достигает 63% на шейном, 53% - на грудном и 27% - на поясничном уровне [L. Manchikanti и др., 2004].
Несмотря на то, что внутрисуставные инъекции предположительно более точно помогают выявить источник боли, они также имеют определенные недостатки. При введении даже 1-2 мл препарата возможен надрыв суставной капсулы и проникновение местного анестетика в эпидуральное пространство, межпозвоночное отверстие, желтую связку и паравертебральные мышцы, т.е. может оказываться воздействие на другие потенциальные источники боли [M. Dory, 1981; R. Moran и др., 1988; J. Raymond, J. Dumas, 1984; R. Marks и др., 1992]. Выполнение внутрисуставных инъекций признают технически более сложным, особенно при фронтальной ориентации суставов. Достоинством БМВ считают удобство проведения анестезии перед выполнением процедуры РЧД.
Для уменьшения частоты ложноположительных результатов блокад дугоотростчатых суставов S. Cohen и др. (2007) рекомендуют следующее:
- проводить плацебоконтролируемые инъекции;
- в качестве ориентира нижней точки для проведения блокады использовать поперечный отросток позвонка;
- ограничивать объем вводимого местного анестетика 0,5 мл;
- использовать для одной инъекции одну иглу;
- применять рентгеновскую КТ при выполнении внутрисуставных инъекций;
- избегать назначения седативных препаратов и опиоидных анальгетиков непосредственно перед и во время процедуры.
Частота ложноотрицательных результатов диагностических блокад дугоотростчатых суставов достигает 11%. Их точная причина остается неизвестной. Подразумевают возможность попадания местного анестетика в венозное русло и аберрантную иннервацию сустава другими нервами, а не ветвью задней первичной ветви спинномозгового нерва. При положительной аспирационной пробе (попадании в шприц венозной крови) рекомендуют прекратить процедуру и повторить ее позже.
Таким образом, дугоотростчатые суставы могут быть возможным источником боли в спине. Анатомические исследования свидетельствуют, что в результате дистрофических изменений ориентация дугоотростчатых суставов изменяется от более коронарной к сагиттальной, предрасполагая их к повреждению при вращательных движениях. Наиболее часто страдают суставы на уровне LIII-LIV, LIV-LV и Lv-SI а в шейном отделе позвоночника - CII-CIII и CV-CVI. Точная распространенность боли в спине, обусловленной поражением дугоотростчатых суставов, остается неизвестной, считают, что она встречается у 30-60% пациентов с болью в поясничной области, в 49-60% случаев боли в шейном отделе позвоночника и в 42-48% - в грудном отделе позвоночника.
Не описаны типичные клинические характеристики боли, связанной с поражением дугоотростчатых суставов. Как правило, отмечается наличие ноющей боли в поясничной области. Боль может быть локальной и отражаться в ягодицы, бедро, в область коленного сустава, а иногда - в голень. При патологии дугоотростчатых суставов в шейном отделе позвоночника она может появляться в шее, надплечьях, затылочной области, грудном отделе позвоночника. Боль может усиливаться при разгибании в шейном и поясничном отделе позвоночника. Может отмечаться умеренное ограничение объема движений в пораженных ПДС и болезненность при пальпации в паравертебральной области в проекции дугоотростчатых суставов (на 2-3 см латеральнее межостистого промежутка в поясничном отделе позвоночника). Основными методами диагностики фасеточного синдрома считают БМВ или внутрисуставное введение местного анестетика под контролем нейровизуализации. Непродолжительное уменьшение боли на время действия местного анестетика более чем на 80% от исходного уровня считают достаточно надежным критерием диагностики фасеточного синдрома. Эффект диагностических блокад свидетельствует о потенциальной эффективности РЧД суставов. Лечение
Для лечения боли, связанной с патологией дугоотростчатых суставов, используют мультимодальный подход. Применяют как методы, показавшие эффективность при хронической боли в спине (см. «Лечение неспецифической боли в спине»), так и специфические малоинвазивные вмешательства на суставах.
В программу лечения целесообразно включать лечебно-диагностические блокады с местными анестетиками [Е.Л. Соков, 1995; Л.П. Соков и др., 2004]. Обычно при положительном эффекте от блокады с местным анестетиком и отсутствии противопоказаний для назначения глюкокортикоидов их добавляют к местному анестетику, что пролонгирует лечебный эффект. Обычно используют дексаметазон (4 мг), бетаметазон (2-4 мг), метилпреднизолон (40 мг). При применении бетаметазона продолжительность действия блокады может составлять до 3-4 нед. В целом данные об эффективности внутрисуставного введения глюкокортикоидов для диагностики и лечения боли в спине, связанной с дисфункцией дугоотростчатых суставов, весьма противоречивы. По данным различных исследований, длительное уменьшение боли при внутрисуставном введении глюкокортикоидов отмечают в 18-63% случаев. При этом в большинстве исследований пациентам не проводили предшествующих диагностических блокад с местными анестетиками [J. Destouet и др., 1982; D. Long и др., 1996; G. Lewinnek, С. Warfield, 1986, F. Murtagh, 1988]. Результаты контролируемых исследований также не выглядят достаточно убедительными. В крупном исследовании G. Lilius и соавт. (1989) не обнаружили статистически значимых различий между внутрисуставным введением смеси местного анестетика и глюкокортикоида, введением этой же смеси периартикулярно и применением 0,9% раствора натрия хлорида. В другом сравнительном исследовании внутрисуставное введение глюкокортикоидов показало большую их эффективность при наблюдении в течение 6 мес по сравнению с внутрисуставным введением 0,9% раствора натрия хлорида [S. Carette и др., 1991]. Предполагают, что введение глюкокортикоидов наиболее эффективно у пациентов с большей активностью асептического воспаления на фоне дегенеративного поражения дугоотростчатых суставов. Это подтверждает ряд исследований с применением ОФЭКТ. Показано, что при положительных результатах ОФЭКТ в виде накопления радиоиндикатора в дугоотростчатых суставах, что отражает наличие в них изменений воспалительного характера, эффективность внутрисуставного введения глюкокортикоидов значительно возрастает (75% случаев положительного эффекта) по сравнению с группой пациентов без накопления радиоиндикатора (менее 40% случаев эффективности). Положительный эффект при этом регрессировал через 3 мес после проведения инъекций [A. Dolan и др., 1996; S. Pneumaticos и др., 2006]. Кроме нейровизуализационных особенностей, эффективность внутрисуставного введения глюкокортикоидов коррелировала с положительным эффектом от предшествующих блокад с местным анестетиком [C. Brummett, S. Cohen, 2008].
В настоящее время имеются многочисленные данные неконтролируемых исследований об эффективности РЧД дугоотростчатых суставов. Положительный эффект при боли в поясничном отделе позвоночника отмечают у 50-80% пациентов [S. Cohen и др., 2007; L. Niemisto и др., 2003; R. Rashbaum, 1983], а при послеоперационной люмбоишиалгии - в 30-50% случаев [S. Cohen и др., 2007; J. McCulloch, L. Organ, 1977; R. North и др., 1994; J. Schaerer, 1978]. Не получено достоверных различий в эффективности РЧД у пациентов с болевыми синдромами в шейном отделе позвоночника, которым не проводили оперативные вмешательства на шейном отделе позвоночника, и у оперированных пациентов [C. Brummett, S. Cohen, 2008].
Имеется всего несколько плацебоконтролирумых исследований эффективности РЧД у пациентов с люмбалгией, связанной с дисфункцией дугоотростчатых суставов. J. King и R. Lagger (1976) сравнили эффективность РЧД дугоотростчатых суставов, радиочастотного воздействия на паравертебральные мышцы (радиочастотная миотомия) и имитацию такого воздействия у 60 пациентов с болью в поясничнокрестцовой области. Наблюдение на протяжении 6 мес показало, что значительное уменьшение интенсивности боли отмечено у 27% пациентов, которым сделана РЧД, у 53% пациентов, которым была выполнена радиочастотная миотомия и ни у одного пациента в группе, получавшей имитацию радиочастотного воздействия. Недостатком данного исследования стало отсутствие отбора пациентов в исследование с применением диагностических блокад дугоотростчатых суставов или БМВ. Через 15 лет было проведено еще одно РКИ с участием 41 пациента с хронической болью в спине. Пациентам производили внутрисуставные диагностические блокады дугоотростчатых суставов с местным анестетиком, а затем - РЧД дугоотростчатых суставов или ее имитацию. Статистически значимые различия в эффективности РЧД и плацебо при наблюдении через месяц отмечали только у пациентов с четким положительным эффектом от диагностических блокад. В этой группе положительный эффект РЧД сохранялся и в течение 6 мес [J. Gallagher и др., 1974]. По данным наиболее крупного контролируемого исследования, при оценке состояния пациентов через 3 мес основным отличием группы, получавшей РЧД, и контрольной группы была большая частота снижения интенсивности боли (более чем на 50%) у пациентов основной группы (62% в основной и 39% в контрольной). При этом не было выявлено достоверных различий между пациентами, которым сделана РЧД или ее имитация, в снижении интенсивности боли по ВАШ, количестве употребляемых анальгетиков и ограничении активности [R. van Wijk и др., 2005].
В целом различия в эффективности РЧД при хронических болевых синдромах в шейном и поясничном отделах позвоночника зависят от критериев отбора пациентов в исследование. В систематическом обзоре об эффективности РЧД отмечено, что чем более точно удается выявить источник боли перед проведением РЧД на шейном и поясничном уровне, тем выше эффективность этого метода лечения [K. van Boxem и др., 2008].
Возобновление болевого синдрома после РЧД дугоотростчатых суставов связывают с их реиннервацией. Обычно это отмечается через 6-12 мес после проведенного вмешательства. В таком случае может быть выполнена повторная РЧД, и ее эффективность бывает не меньше, чем первичной. Имеется ряд неконтролируемых исследований, показывающих эффективность пульсовой РЧД [G. Mikeladze и др., 2003] и криоденервации [C. Birkenmaier и др., 2007; C. Barlocher и др., 2003; M. Staender и др., 2005] у пациентов со скелетно-мышечными болями в спине. Пульсовая РЧД - относительно новая методика, принцип которой основан на воздействии энергии радиоволн в пульсовом режиме 2?2 мс/с. При этом температура воздействия на превышает 42 °С, что минимизирует возможность повреждения окружающих нерв тканей. Механизм терапевтического действия до конца не изучен. Возможно, он связан с блокадой проведения возбуждения преимущественно по маломиелинизированным волокнам. Криоденервация заключается в деструкции медиальной ветви при воздействии на нее низкой температуры (50 °С) с помощью специального криозонда. Охлаждение производят с помощью углекислоты.
В настоящее время недостаточно данных об эффективности РЧД при цервикогенной головной боли. Исследования по сравнению стандартной и пульсовой РЧД при болях в шейном отделе позвоночника демонстрируют их сходную эффективность. Таким образом, учитывая меньший деструктивный эффект пульсовой РЧД и меньшее количество побочных эффектов, она предпочтительна у пациентов с болью в шейном отделе позвоночника.
Серьезные осложнения при малоинвазивных вмешательствах на дугоотростчатых суставах крайне редки. Метаболические и эндокринные расстройства, связанные с введением глюкокортикоидов, изучены мало, однако в этих случаях можно учитывать результаты исследований частоты осложнений при эпидуральном введении глюкокортикоидов. Возможно торможение гипоталамо-гипофизарнонадпочечниковой оси, сохраняющееся до 4 нед, и транзиторное повышение концентрации глюкозы, отмечающееся не более 1 нед [J. Kay и др., 1994; A. Ward и др., 2002]. Редко встречаются инфекционные осложнения: септический артрит, эпидуральный абсцесс, менингит [E. Alcock и др., 2003; С. Gaul и др., 2005; N. Orpen, N. Birch, 2003]. Описаны случаи спинальной анестезии и постпункционной головной боли [S. Cohen, 1994; J. Goldstone, J. Pennant, 1987]. Примерно в 1% случаев могут появляться невропатические боли, онемение и парестезии в крестцовой области или бедре, вероятно, связанные с термическим повреждением кожной ветви задней первичной ветви спинномозгового нерва или его вентральных ветвей. Эти явления, как правило, преходящи. Крайне редки ожоги, в основном, связанные с нарушением эксплуатации прибора для проведения денервации [C. Kornick и др., 2004]. На Рис. 21 приведена тактика лечения спондилоартропатических болевых синдромов.
Дисфункция крестцово-подвздошных сочленений[править | править код]
Считают, что дисфункция КПС в 10-25% случаев - основной источник боли в пояснично-крестцовой области [J. Maigne и др., 1996; A. Schwarzer и др., 1995]. Термин «дисфункция КПС» пришел из мануальной терапии, где обозначал нарушение биомеханики, проявляющееся болью и гипомобильностью КПС без других признаков определенного патологического процесса (сакроилеита). Иногда в этих случаях используют термин «блокада КПС». Особенно часто дисфункция КПС возникает у женщин во время беременности, что, возможно, связано с расслаблением связочного аппарата, стабилизирующего КПС [H. Ostgaard и др., 1991]. Есть много факторов, предрасполагающих к поражению КПС. Многие из них связаны с изменениями биомеханики на фоне конституциональной асимметрии длины ног, формирования косого и скрученного таза, изменения конфигурации поясничного отдела позвоночника. КПС страдают при воспалительных (анкилозирующий спондилит), метаболических (подагра и псевдоподагра) и дегенеративных (остеоартроз) заболеваниях суставов, что необходимо учитывать при дифференциальной диагностике их болезненной дисфункции.
Боль, связанная с дисфункцией КПС, может появляться в крестцовой области, иррадиировать в пах, в зону дерматома S1. Ее интенсивность, как правило, уменьшается после ходьбы. Боль обычно более выражена в первой половине дня и уменьшается к вечеру. Рентгенография и лабораторные исследования в этом случае не выявляют отклонений от нормы [R. DonTigny, 1990]. Для диагностики дисфункции КПС обычно применяют приемы невроортопедического обследования: феномен «опережения», феномен Патрика, дистракционные тесты (см. гл. «Обследование пациентов с болью в спине»). Их воспроизводимость при обследовании пациента разными специалистами невысока и зависит от уровня подготовки врача, проводящего обследование, навыкам мануальной диагностики. Диагностическая чувствительность и специфичность повышается при использовании нескольких невроортопедических тестов, выявляющих дисфункцию КПС. Считают, что диагностическую специфичность повышает введение в КПС местного анестетика под рентгенологическим контролем. Уменьшение интенсивности боли по ВАШ во время действия анестетика на 75 -90% считают достаточным для диагностики дисфункции КПС в качестве причины боли в спине [A. Schwarzer и др., 1995; P. Dreyfuss и др., 1996].
Биомеханика и патофизиология[править | править код]
КПС в своем роде уникальные по особенностям строения суставы. Их можно считать типичными синовиальными суставами из-за наличия в их полости синовиальной жидкости. Однако хрящи суставных поверхностей отличаются определенными особенностями. На крестцовой поверхности имеется толстый гиалиновый хрящ, на стороне подвздошной кости - более тонкий и фиброзированный. Суставные поверхности взрослого человека отличаются выраженной бугристостью, что обусловливает их значительное трение при движении. Такие особенности суставных поверхностей делают КПС не похожим ни на один другой сустав в организме. Суставные поверхности КПС можно разделить на краниальный и каудальный сегменты, последний по площади больше. Крестцовая суставная поверхность сустава более вогнута, открыта латерально, кзади и книзу, подвздошная - выпуклая и ориентирована зеркально первой. Ребристые выпуклости на суставной поверхности подвздошной кости и соответствующие им вдавления на крестцовой поверхности формируются в 20-30 лет. Такое строение значительно ограничивает амплитуду движений в суставе до колебания крестца в направлении вперед-назад относительно подвздошной кости, получившего название «нутация» (от лат. nutatio - качение, колебание). Плотные связки укрепляют сустав с двух сторон. Спереди находится передняя крестцово-подвздошная связка, волокна которой обычно переплетаются с нижней частью подвздошнопоясничной связки, сзади - задняя крестцово-подвздошная связка. Кпереди от последней расположена одна из самых мощных связок - межкостная связка. Дополнительные, стабилизирующие КПС связки - крестцово-остистая, крестцово-бугорная и длинная задняя крестцово-подвздошная связка. Связочный аппарат помогает сохранять стабильное положение крестца между подвздошными костями и ограничивает объем нутации при воздействии гравитации и подъеме тяжестей. Биомеханически крестец выполняет функцию опорного основания позвоночного столба, и КПС перераспределяет нагрузку туловища на ноги. Подвздошная кость, наоборот, передает нагрузку, возникающую при движении ног, на позвоночник. Основные движения, возможные в КПС, - нутация и поступательное движение между крестцовой и подвздошной суставными поверхностями. В целом амплитуда движений в КПС не превышает 4° при нутации, а поступательное движение в виде смещения суставных поверхностей - менее 2 мм. В основном движение в суставе обеспечивается возможностями деформации суставного хряща.
В стабилизации КПС принимают участие как структурные, так и динамические факторы. Крестец и суставные поверхности КПС в целом напоминают перевернутую треугольную призму, благодаря чему крестец под действием тяжести туловища «вклинивается» между подвздошными костями. Другой стабилизирующий фактор - бугристость суставных поверхностей. Нутация в КПС увеличивает натяжение крестцово-бугорных, крестцово-остистых и межкостных связок. Особенное значение имеет последняя, поскольку нутация приводит к натяжению этой связки, а она в свою очередь усиливает сближение и трение суставных поверхностей. Динамическую стабилизацию КПС обеспечивают мышцы. Наиболее значимыми при этом считают широчайшую мышцу спины, большую ягодичную мышцу, мышцу, выпрямляющую позвоночник, двуглавую мышцу бедра и косые мышцы живота. Одновременное сокращение контралатеральной широчайшей мышцы спины и ипсилатеральной большой ягодичной мышцы приводит к натяжению пояснично-грудной фасции и увеличению компрессии суставных поверхностей в КПС. Сокращение мышцы, выпрямляющей позвоночник, приводит к наклону крестца вперед относительно подвздошной кости (нутации), что в свою очередь стабилизирует сустав через натяжение крестцово-бугорных, крестцово-остистых и межкостных связок. Кроме этого, сокращение мышцы, выпрямляющей позвоночник, и многораздельных мышц приводит к натяжению пояснично-грудной фасции и стабилизирует КПС по механизму, описанному выше для широчайшей мышцы спины и большой ягодичной мышцы. Поскольку внутренняя и наружная косая мышцы живота прикрепляются к подвздошной кости, они также стабилизируют КПС. Мышечно-тонические синдромы, возникающие в перечисленных группах мышц, могут приводить к блокаде КПС. Анатомические и биомеханические особенности КПС предрасполагают к развитию их дисфункции при воздействии и других факторов: перегрузке одного из суставов на фоне разницы длины ног, деформации позвоночника, предшествующих оперативных вмешательствах на позвоночнике и суставах ног, поражении дугоотростчатых суставов. При асимметрии длины ног формируется наклон таза в сторону короткой ноги («косой таз»). При этом на стороне короткой ноги КПС занимает более горизонтальное положение, а на стороне длинной - более вертикальное. Наибольшее компрессионное воздействие на КПС, связанное с массой тела, приходится на сторону короткой ноги, а сила смещения крестца книзу - на сторону длинной конечности. Наклон крестца приводит к изменению биомеханики пояснично-крестцовых суставов, которые на вогнутой стороне формирующегося сколиоза испытывают воздействие компрессионной силы, а на выпуклой - силы натяжения. На стороне длинной ноги перегрузке подвергается и головка бедренной кости. Если действие указанных сил превышает прочность тканей, возникает их повреждение.
Лечение[править | править код]
Для лечения дисфункции КПС используют методы мануальной терапии (мобилизацию и манипуляции на КПС), физиотерапию (ультразвуковые методы воздействия), ЛФК, коррекцию разницы длины ног, если она составляет более 1,5 см, с помощью ортопедических стелек, внутрисуставное введение глюкокортикоидов, РЧД. Методы мануальной терапии и физиотерапию широко применяют при дисфункции КПС, но их эффективность в настоящее время считают не достаточно доказанной. Техника внутрисуставного введения местных анестетиков и глюкокортикоидов сходна с таковой при фасеточном синдроме. Некоторые специалисты предпочитают проводить две инъекции: одну иглу вводят в каудальные отделы сустава, другую - в верхнюю его часть для дополнительного распределения препаратов, в том числе и на крестцово-подвздошную связку. Эффективность внутрисуставного введения глюкокортикоидов доказана, но его положительный результат сохраняется относительно недолго [C. Slipman и др., 2001].
По мнению ряда исследователей, РЧД - эффективный метод лечения при дисфункции КПС. Ее цель - деструкция чувствительных нервов, иннервирующих КПС. Однако в отличие от дугоотростчатых суставов, иннервация КПС более сложна, что затрудняет применение РЧД в этом случае. Более ранние литературные данные свидетельствуют о том, что иннервация КПС осуществляется как передними, так и задними ветвями поясничных и крестцовых спинномозговых нервов, а более поздние исследования доказали преимущественную иннервацию КПС задними первичными ветвями спинномозгового нерва на уровне LV, а также латеральными ветвями задней первичной ветви спинномозговых нервов на уровне SI-SIV [K. Grob и др., 1995; J. Fortin и др., 1999]. РЧД указанных нервов проводят в месте их входа через задние крестцовые отверстия или выхода из КПС вдоль его задней границы. Вдоль задней границы КПС РЧД проводят с помощью двух электродов, расположенных вдоль границы сустава на расстоянии 4-6 мм друг от друга. Нижний электрод после радиочастотного воздействия скачкообразно перемещается на 4-6 мм краниальнее верхнего, затем воздействие повторяют, пока не будет создана линейная область деструкции вдоль всего сустава. Длительность денервации одного участка составляет 120-150 с, температура - 90 °С [C. Pino и др., 2005]. Другой метод денервации КПС - РЧД задних ветвей спинномозговых нервов на уровне LIV и LV (или изолированно на уровне LV) в сочетании с РЧД латеральных ветвей задних первичных ветвей спинномозговых нервов на уровне SI-SIII. Деструкцию задней ветви спинномозгового нерва на уровне LIV проводят в месте соединения верхнего суставного отростка и поперечного отростка LV. Задняя ветвь спинномозгового нерва на уровне LV локализуется в месте соединения верхнего суставного отростка SI и крыла крестца. Латеральные ветви задних первичных ветвей спинномозговых нервов на уровне SI-SIII подвергаются деструкции на уровне соответствующих крестцовых отверстий в позиции от 2 до 6 ч справа и от 6 до 10 ч слева. Денервацию проводят при температуре 80-90 °С в течение 6090 с [К. Malik, Н. Benson, 2008]. Иногда используют сочетание воздействий на двух уровнях [A. Gavargez и др., 2002]. Практически все исследования эффективности РЧД КПС проводили ретроспективно или обсервационно (когортные, случай-контроль). Эффективность РЧД КПС составляет 50-70% [K. Malik, Н. Benson, 2008]. С позиции доказательной медицины в настоящее время недостаточно данных в пользу эффективности РЧД при болевых синдромах, связанных с дисфункцией КПС [K. van Boxem и др., 2008].
Клинический пример
Пациент В., 50 лет, авиамеханик, обратился в клинику с жалобами на ноющую боль в поясничном отделе позвоночника, усиливающуюся при длительном пребывании в вертикальном положении, перемене положения: вставании со стула, попытке прогнуться назад. Также беспокоили тянущие боли по задней поверхности левого бедра, которые усиливались при начале ходьбы после длительного пребывания в положении сидя и постепенно уменьшались при «расхаживании». Практически ежедневные боли в поясничной области пациент отмечает на протяжении 7 лет, в течение года отметил присоединение боли в левом бедре. В предшествующие 5 лет пациент по поводу боли в поясничной области несколько раз в год проходил курсы лечения в неврологическом отделении медсанчасти по месту работы. Лечение включало в себя прием НПВС (кетопрофен, диклофенак), антидепрессантов (амитриптилин в дозе 50 мг/сут, максимально - курсом 2 мес), физиотерапию, ЛФК и массаж. Положительный эффект от консервативного лечения сохранялся, как правило, 2-3 мес после выписки из стационара. По роду деятельности пациент часто вынужден работать в неудобной позе, иногда - переносить тяжести. Это, с его слов, способствовало обострению боли в спине. Ухудшение состояния пациент отмечает на протяжении последних 4 мес, когда боль в спине и ноге усилилась, проведенное лечение с приемом НПВС внутрь (кетопрофен в дозе 150 мг/сут) и в виде мазей, мануальная терапия, физиотерапия и массаж не принесли значительного облегчения. Амбулаторно, в связи с подозрением на наличие радикулопатии, пациенту была проведена МРТ поясничного отдела позвоночника, выявившая центральную протрузию диска LIV-LV до 5 мм, после чего он был направлен на консультацию к нейрохирургу в клинику нервных болезней им. А.Я. Кожевникова. При осмотре в неврологическом статусе очаговой патологической симптоматики выявлено не было. Отмечалась сглаженность поясничного лордоза, умеренно выраженное напряжение мышцы, выпрямляющей позвоночник, сгибание в поясничном отделе не было ограничено (тест Шобера - 5,6 см), при разгибании определялась болезненность в поясничной области. При пальпации в паравертебральной области в положении лежа на животе отмечалась боль в проекции дугоотростчатых суставов на уровне LIII-LIV и LIV-LV При обследовании КПС выявлен «феномен опережения» и положительная проба Патрика слева. На рентгенограммах поясничного отдела позвоночника обнаружена деформация замыкательных пластин, остеофиты, снижение высоты межпозвоночных промежутков LIII-LIV, LIV-LV L-SI, антелистез LIV до 3 мм, не увеличивающийся при функциональных пробах (сгибании и разгибании в поясничном отделе позвоночника). Пациенту с диагностической целью последовательно были проведены блокады дугоотростчатых суставов на уровне LIII-LIV и LIV-LV 0,5% раствором прокаина, которые привели к полному регрессу болевого синдрома только при блокировании двух уровней. Введение в КПС местного анестетика также привело к значительному (с 6 до 1 балла по ВАШ) регрессу боли в ноге. Пациенту была выполнена РЧД дугоотростчатых суставов Liii-LiV и LiV-LV, которая устранила локальную боль в поясничной области. После проведения курса мануальной терапии, направленной на мобилизацию левого КПС, введение в него с прокаина и бетаметазона и ультразвукового воздействия на КПС с гидрокортизоном пациент отметил значительную положительную динамику: уменьшение болевого синдрома в левой ноге. Эффект терапии сохранялся при повторных обследованиях через 1, 3 и 6 мес.
Таким образом, комплексное лечение, направленное на устранение дисфункции КПС, принесло стойкий положительный эффект и от РЧД КПС целесообразно было воздержаться. Хронический люмбалгический синдром был обусловлен дегенеративным поражением дугоотростчатых суставов позвоночника, сопровождавшимся развитием спондилолистеза, проведение РЧД принесло значительное облегчение. Пациенту были даны рекомендации избегать нагрузки на поясничный отдел позвоночника и укреплять мышцы передней брюшной стенки.
Плечелопаточная периартропатия[править | править код]
Для плечелопаточной периартропатии характерна боль в области периартикулярных тканей плечевого сустава с ограничением объема движений в нем. Из-за прогрессирующей контрактуры отведение плеча ограничено. Плечо как бы приковано к лопатке и может быть отведено лишь в небольшом объеме («замороженное плечо»). Его маятникообразные движения в саггитальной плоскости относительно свободны. Основные нозологические варианты, включенные в собирательное понятие «плечелопаточная периартропатия», - патология вращающей манжеты плеча, адгезивный капсулит, МФБС мышц плечевого пояса [ О.А. Солоха, 2006].
Патология вращающей манжеты плеча - это самая распространенная причина боли и двигательных нарушений в плечевом суставе. Различают три формы поражения вращающей манжеты плеча:
- дегенеративный и компрессионный тендинит сухожилия надостной мышцы;
- кальцифицирующий субакромиальный тендинит (бурсит);
- полный или частичный разрыв сухожилия надостной мышцы.
Для патологии вращающей манжеты плеча характерна локализованность боли (в области дельтовидной мышцы, под акромионом, около большого бугорка плечевой кости) с незначительной зоной иррадиации, ее преобладание при движении; избирательное ограничение активного отведения плеча и наружной ротации при сохранности объема пассивных движений. При пальпации большого бугорка плечевой кости обнаруживают болезненность, крепитацию и локальную припухлость. Диагностическое значение имеет проба Ниэра: при введении раствора местного анестетика в субакромиальное пространство исчезает боль и восстанавливается объем движений. Патология вращающей манжеты плеча более характерна для мужчин старше 40-50 лет, обычно страдает доминирующая рука [Ю.В. Мозолевский, О.А. Солоха, 2000].
Адгезивный капсулит - хроническое фиброзное воспаление капсулы плечевого сустава. Заболевание встречается наиболее часто (в 70% случаев) у женщин после 45 лет, без связи с профессиональной деятельностью, занятиями спортом и физической активностью. Распространенность этого состояния в популяции достигает 2%. Локализация процесса односторонняя, редко - двусторонняя. Боль ноющая, постоянная, обычно локализована только в области плечевого сустава, усиливается в покое и ночью, а при движении немного уменьшается. Характерна утренняя скованность в плечевом суставе. Плечо на пораженной стороне приподнято. Наблюдается диффузная припухлость вокруг сустава, укорочение всех мышц плечевого пояса, их легкая атрофия и повышенная утомляемость. Объем активных и пассивных движений ограничен равномерно. При наклоне вперед объем движений в плечевом суставе не увеличивается. При отведении плеча более чем на 60° начинается ротация лопатки. При проведении пробы Ниэра боль уменьшается, но тугоподвижность в суставе сохраняется. Генез заболевания неясен. Течение адгезивного капсулита имеет определенную стадийность. На I стадии, длящейся до 3 мес, отмечается боль в области плечевого сустава и уменьшение амплитуды активных и пасивных движений (особенно сгибания, отведения, внутренней и наружной ротации). Боль выражена в покое и в ночное время. Ведение в сустав местного анестетика способствует значительному регрессу боли и восстановлению амплитуды движений. Морфологически на этой стадии определяется диффузный гиперваскулярный синовит. На II стадии («замораживания») - 3-9 мес - определяется резкое ограничение движений в суставе. Может сохраняться боль в покое. При артроскопии и биопсии капсулы определяется гипертрофический синовит с формированием субсиновиальных рубцовых изменений и фиброплазии капсулы. На III стадии ограничение движений значительно преобладает над болевым синдромом, который отмечается в основном при движении в суставе. Введение в сустав местного анестетика не улучшает амплитуду движений в нем. При артроскопии обнаруживают преобладание фиброзных изменений синовиальной оболочки, при биопсии капсулы выявляют плотную коллагеновую ткань с тонким слоем синовиальной оболочки без ее гиперваскуляризации и гипертрофии. III стадия длится с 9-го по 15-й месяц с момента начала заболевания. На IV стадии отмечают регресс боли и ограничения движений, артроскопию в этот период не проводят из-за улучшения состояния пациентов [M. Sheridan, 2006]. Примерно в 20-30% случаев адгезивный капсулит рецидивирует на другой стороне.
Лечение всех вариантов плечелопаточной периартропатии включает в себя назначение НПВС, ограничение двигательной активности в остром периоде (на I-II стадии адгезивного капсулита) и активную функциональную реабилитацию (до возможно полного восстановления объема движений) на всех последующих этапах. Также необходимо устранить мышечное напряжение с помощью лечебных блокад с местными анестетиками, назначения миорелаксантов и ПИР. В отдельных случаях, при выраженном мышечном напряжении, возможно применение ботулинического токсина с последующим подключением активной ЛФК [О.А. Солоха, Н.Н. Яхно, 2006]. При обнаружении патологии вращающей манжеты плеча (дегенеративного и компрессионного тендинитов), а также дегенеративного поражения акромиально-ключичного сустава и тендинита длинной головки бицепса лечение включает в себя местное введение глюкокортикоидов в соответствующие периартикулярные структуры (как правило, субакромиально). При адгезивном капсулите методом выбора считают внутрисуставное введение глюкокортикоидов (изолированно или с местным анестетиком) в сочетании с активной ЛФК.
Отдельные болевые синдромы как причина боли в грудной клетке[править | править код]
Синдром Титце впервые описан А. Tietze в 1921 г. Это относительно редкое состояние, характеризующееся наличием неспецифического доброкачественного обратимого болезненного отека в области II (в 60% случаев) или III реберных хрящей. В 80% случаев поражение одностороннее и ограничено одним реберным хрящом. Боль обычно хорошо локализована, но может иррадиировать по всей передней поверхности грудной стенки, а также в надплечье и шею. Покраснение, повышение температуры и другие изменения кожи над областью поражения отсутствуют. Боль обычно регрессирует спонтанно через 2-3 нед, но часто продолжает беспокоить на протяжении нескольких месяцев, а резидуальный отек может сохраняться до нескольких лет. Обычно заболевание развивается в молодом или детском возрасте. Причины его не известны, но у большинства пациентов в анамнезе выявляют предшествующие эпизоды респираторных инфекций, сильного кашля, тяжелой физической нагрузки, а также недостаточное питание.
Патогенетического лечения не существует, заболевание имеет доброкачественное самоограничивающееся течение, о чем необходимо проинформировать пациента. При выраженной боли возможно назначение НПВС внутрь или местно в виде мазей, физиопроцедуры с фонофорезом глюкокортикоидов на пораженную область, ее согреванием или охлаждением [M. Imamura, S. Imamura, 2008].
Реберно-грудинный синдром. Синдром Титце часто путают со значительно более распространенным реберно-грудинным синдромом («синдром передней грудной стенки», «костохондрит», «реберногрудинная хондродиния») - одной из наиболее частых причин болей в грудной клетке. В отличие от синдрома Титце при реберно-грудинном синдроме пальпаторно в 90% случаев можно выявить множественные зоны болезненности: в парастернальной области, ниже молочной железы, в проекции грудных мышц и грудины. Локальный отек отсутствует. Наиболее часто поражаются хрящи II и V ребра. При поражении верхних реберных хрящей боль обычно иррадиирует в область сердца. Она обычно усиливается при движениях грудной клетки.
Заболевание наиболее часто диагностируют у женщин после 40 лет, его патогенез остается неизвестным. Реберно-грудинный синдром дифференцируют с ИБС, при этом кроме особенностей болей, которые обычно носят не типичный для ИБС характер, также применяют блокады межреберных нервов с введением местных анестетиков по задней подмышечной линии, приносящие пациентам выраженное облегчение.
Лечение симптоматическое. Показано назначение НПВС, парацетамола, при недостаточной их эффективности - в сочетании со слабыми опиоидными анальгетиками. Можно использовать физиотерапевтическое воздействие - согревание болезненной области, чрескожную электронейростимуляцию. Применяют блокады межреберных нервов с местными анестетиками по задней подмышечной линии. Эта манипуляция имеет и психотерапевтическое значение, поскольку регресс болевого синдрома после ее проведения позволяет убедить пациента в доброкачественности заболевания и его «некардиогенной» причине. В табл. 9 приведены диагностические различия синдрома Титце и реберно-грудинного синдрома [J. Bonica, A. Sola, 1990].
Таблица 9. Диагностические различия синдрома Титце и реберногрудинного синдрома
|
Клиническая особенность |
Синдром Титце |
Реберно-грудинный синдром |
|
Распространенность |
Редко |
Более часто |
|
Возраст начала заболевания |
<40 лет |
>40 лет |
|
Количество пораженных областей |
в 80% случаев - одна |
>90% случаев - более одной |
|
Наиболее часто поражающиеся реберно-грудинные сочленения |
II (иногда Ill) |
II и V |
|
Локальный отек |
Есть |
Нет |
|
Сопутствующие расстройства |
Инфекции дыхательных путей |
Боль в шейном отделе позвоночника, ИБС, МФБС |
Синдром «скользящего ребра» характеризуется интенсивной болью в проекции нижнего края реберной дуги и увеличением подвижности переднего конца реберного хряща, как правило X, и реже VIII и IX ребра. Данное состояние было впервые описано в 1922 г. R. Davies-Colley, и его до настоящего времени под разными названиями («передний реберный синдром», синдром «щелкающего ребра», синдром «конца ребра», синдром «скользящего реберного хряща», синдром «смещения ребра») указывают в качестве частой причины болей в грудной клетке. Считают, что данное состояние имеет травматическое происхождение и связано с рецидивирующим подвывихом реберного хряща при ротации туловища. В отличие от вышерасположенных ребер, хрящевые части которых формируют грудино-реберные суставы, хрящевые части VIII-X ребер образуют сочленения с хрящевыми частями вышерасположенных ребер с помощью наружной межреберной мембраны. Эта зона - анатомически наиболее слабая область грудной клетки, предрасположенная к травматизации. После повреждения хрящевого сочленения свободная хрящевая часть ребра отклоняется вверх, смещаясь при дыхании в вертикальном или переднезаднем направлении относительно вышележащего хряща, что сопровождается болью и характерным ощущением «щелчка». Боль, как правило, носит острый или стреляющий характер, локализуется в верхнем квадранте брюшной стенки и провоцируется гиперэкстензией грудной клетки при подъеме рук вверх. В острой стадии заболевания пациент часто принимает вынужденное положение с наклоном туловища вперед и в больную сторону для уменьшения напряжения мышц брюшной стенки, прикрепляющихся к реберным углам. Иногда смещающийся реберный хрящ может травмировать надхрящницу вышерасположенного ребра и межреберный нерв. Обычно данное состояние принимают за проявление острой патологии органов брюшной полости, проводят диагностическую лапароскопию. В то же время осведомленность о данной нозологии позволяет избежать необоснованной инвазивной процедуры. Рентгенография при синдроме «скользящего ребра» не выявляет специфических изменений. Патогномоничный для данного состояния тест заключается в «подтягивании» согнутым пальцем края ребра кпереди. При этом воспроизводится типичный болевой паттерн, сопровождающийся характерным «щелчком». Поскольку данное состояние почти всегда одностороннее, проведение подобной манипуляции на здоровой стороне не сопровождается описанными феноменами. Диагноз также может быть подтвержден инфильтрацией пространства между отделенным хрящом и костной частью ребра 5 мл 0,5% раствора лидокаина, приводящей к полному регрессу болевых ощущений через 10 мин после процедуры.
Консервативное лечение синдрома «скользящего ребра» включает в себя разъяснение пациенту доброкачественной природы состояния, назначение НПВС, блокады с местными анестетиками и глюкокортикоидами. При неэффективности перечисленных мероприятий иногда выполняют резекцию края ребра.
Поражение грудино-ключичных суставов развивается при деформирующем остеоартрозе, ревматоидном артрите, анкилозирующем спондилите, псориатическом и инфекционных артритах. Боль при этих состояниях, как правило, локальная, но в ряде случаев может иррадиировать на переднюю поверхность грудной клетки, и тогда это состояние необходимо дифференцировать от заболеваний легких и сердца. Боль усиливается при подъеме надплечий и пальпации грудино-ключичного сустава. Иногда отмечают отек и крепитацию в проекции пораженного сустава.
Грудино-ключичный гиперостоз - относительно недавно описанное заболевание, проявляющееся двусторонним хроническим болезненным отеком ключиц, грудины и I ребра. Причина развития данного состояния не известна, возможна связь с псориатическим артритом. Диагностика этого состояния основана на выявлении характерных рентгенологических изменений - гиперостоза, утолщения и увеличения костной плотности ключиц и грудины, оссификации хрящевой части I ребра и формирования грудино-ключичного синостоза. Реже отмечают увеличение СОЭ и гипергаммаглобулинемию. Заболевание имеет рецидивирующее течение. Увеличение костных структур и распространение воспалительного процесса иногда приводит к окклюзии подключичной вены или развитию синдрома верхней апертуры. При грудино-ключичном гиперостозе и поражении грудино-ключичных суставов другой этиологии облегчение приносит прием НПВС, в отдельных случаях - глюкокортикоидов, а также лечение основного заболевания, вызвавшего артрит.
Ксифоидалгия - редкий синдром, характеризующийся болями на передней поверхности грудной клетки, в эпигастрии, которые воспроизводятся при пальпации мечевидного отростка грудины. Интенсивность боли может варьировать от слабой до высокой, требующей исключения коронарной патологии или острых заболеваний органов брюшной полости. Боль может возникать или усиливаться при наклоне вперед и поворотах туловища, в особенности после приема пищи, приводящего к увеличению давления в брюшной полости. В отличие от других костных и суставных источников боли в грудной клетке при ксифоидалгии прекращение движения, спровоцировавшего боль, как правило, не приводит к быстрому регрессу болевых ощущений. При глубокой пальпации мечевидного отростка боль может иррадиировать за грудину, а также в надплечья и спину. Причина заболевания неизвестна. При ксифоидалгии не выявлено каких-либо специфичных рентгенологических изменений. Заболевание обычно длится несколько недель или месяцев и регрессирует спонтанно. При легкой и умеренной интенсивности боли эффективны простые анальгетики и НПВС, при выраженном болевом синдроме можно инфильтрировать болезненную область местными анестетиками. Оперативное лечение (резекция мечевидного отростка) проводят пациентам с выраженным некупирующимся болевым синдромом, но этот метод применяют крайне редко.
Диффузный идиопатический скелетный гиперостоз (болезнь Форестье) - заболевание, относительно часто встречающееся у лиц среднего и пожилого возраста, в основном у мужчин. Основные симптомы - боли легкой и умеренной интенсивности и ощущение скованности в грудном и поясничном отделах позвоночника. При осмотре иногда определяют усиление грудного кифоза, минимальное ограничение объема движений в грудном отделе позвоночника и экскурсии грудной клетки. Часто выявляют локальную болезненность при пальпации грудного и поясничного отделов позвоночника. Для диагностики диффузного идиопатического скелетного гиперостоза, кроме клинических особенностей, необходимо проведение рентгенографии позвоночника, которая выявляет гиперостоз, наиболее выраженный в грудном отделе и проявляющийся линейной оссификацией по передней поверхности четырех и более смежных позвонков с сохранением рентгенологического просветления между костными отложениями и телами позвонков и относительной сохранностью высоты межпозвоночного промежутка. Также характерно формирование остеофитов между телами соседних позвонков, смыкающихся между собой в виде мостиков. При болевом синдроме, связанном с диффузным идиопатическим скелетным гиперостозом, симптоматическое лечение включает в себя курсовой прием НПВС, согревающие физиопроцедуры и упражнения, направленные на укрепление мышц спины.
При артропатическом синдроме с поражением реберно-поперечных суставов (обычно на фоне деформирующего остеоартроза) отмечают локализованную болезненность при пальпации в их проекции на 3 см кнаружи от остистых отростков. При этом пациенты описывают боль как тупую, иногда глубокую с ощущением жжения. Рентгенографическое исследование выявляет в этих случаях сужение суставной щели, субхондральный остеосклероз и краевые остеофиты, а также признаки дистрофического поражения других суставов. Эффективны методы мануальной терапии, направленные на мобилизацию пораженных ПДС, местные физиотерапевтические воздействия, блокады реберно-поперечных суставов с местными анестетиками и глюкокортикоидами. Возможно назначение НПВС в виде коротких курсов.
Отдельные скелетно-мышечные источники боли на передней поверхности грудной клетки приведены на Рис. 22.
Лечение неспецифической боли в спине[править | править код]
Большинство клинических рекомендаций по ведению пациентов с неспецифической болью в спине ориентировано в первую очередь на врачей общей практики.
Оптимальная тактика ведения пациента с острой болью в пояснично-крестцовой области, основанная на принципах доказательной медицины, сводится к нескольким положениям:
- информирование пациента;
- исключение постельного режима;
- назначение доказаного эффективного лечения;
- коррекция тактики ведения при ее неэффективности в период 4-12 нед.
Эффективность различных методов лечения острой боли в спине [M. Rossignol и др., 2007; M. van Tulder и др., 2006; Ш.Ф. Эрдес и др., 2008] приведена в табл. 10.
Таблица 10. Методы лечения острой неспецифической боли в поясничнокрестцовой области
|
Метод |
Рекомендации |
Уровень доказательности’ |
|
НПВС* |
Рекомендуются |
Высокий (А) |
|
Миорелаксанты* |
Рекомендуются |
Высокий (А) |
|
Комбинация миорелаксанта и НПВС или анальгетик** |
Рекомендуется |
Высокий (А) |
|
Совет сохранять активность*** |
Рекомендуется |
Высокий (А) |
|
Мануальная терапия |
Рекомендуется |
Умеренный(В) |
|
Анальгетики**** |
Рекомендуются |
Низкий (С) |
|
Информирование пациента о природе и прогнозе заболевания |
Рекомендуется |
Низкий (С) |
|
Акупунктура |
Рекомендуется |
Низкий (С) |
|
Постельный режим |
Не рекомендуется |
Высокий (А) |
|
Упражнения, укрепляющие мышцы |
Не рекомендуются |
Высокий (А) |
|
Специфическая программа ЛФК |
Не рекомендуется |
Высокий (А) |
|
Тракционная терапия |
Не рекомендуется |
Высокий (А) |
|
Чрескожная электронейростимуляция |
Не рекомендуется |
Низкий (С) |
|
Эпидуральное введение кортикостероидов |
Не рекомендуется |
Низкий (С) |
|
Физиотерапия***** |
Нет информации в пользу или против применения |
Отсутствует (D) |
|
Массаж |
Нет информации в пользу или против применения |
Отсутствует (D) |
|
Антидепрессанты |
Нет информации в пользу или против применения |
Отсутствует (D) |
|
«Школа боли в спине» |
Нет информации в пользу или против применения |
Отсутствует (D) |
|
Ношение пояса |
Нет информации в пользу или против применения |
Отсутствует (D) |
* Степень доказательности эффективности метода лечения представляет собой 4-х уровневую систему, где высокому уровню доказательности (А) соответствуют воспроизводимые данные качественно проведенных многочисленных рандомизированных контролируемых исследований, умеренному (В) - воспроизводимые данные менее качественных многочисленных рандомизированных контролируемых исследований (в основном, из-за небольших выборок пациентов), низкому (С) - данные одного рандомизированного контролируемого исследования или противоречивые данные многочисленных исследований с применением контрольных групп, очень низкому (отсутствию) (D) - исследования, проведенные без групп сравнения, теоретические предположения, мнения экспертов.
* - Эффективно уменьшают интенсивность боли, нет анальгетических преимуществ друг перед другом;
** - эффект больше, чем комбинация с плацебо;
*** - уменьшение инвалидизации, связанной с развитием хронической боли, длительности нетрудоспособности по сравнению с постельным режимом и традиционным лечением (прием анальгетиков), уменьшение интенсивности боли больше по сравнению с постельным режимом;
**** - эффективность неопиодных анальгетиков = эффективности НПВП, опиодные анальгетики несколько более эффективны, чем неопиодные;
***** - согревание, охлаждение, электротерапия, ультразвуковое воздействие
Правильная информация о природе заболевания, его прогнозе и методах лечения позволяет скорректировать представления пациента о боли в спине и усилить его активное участие в реабилитационных программах. Этому аспекту стали уделять больше внимания только несколько последних лет. Показано, что «образовательный буклет» снижает количество повторных обращений к врачу общей практики по поводу боли в спине, а разъяснение обученным средним медицинским персоналом, сопровождаемое буклетом о боли и последующим телефонным звонком, приводит к большей удовлетворенности пациента лечением. В то же время диагноз «грыжа диска», «радикулопатия» в отсутствие клинических симптомов компрессии спинномозговых корешков или признаков серьезной патологии, противоречивые мнения и советы врачей усиливают стресс и формируют неправильное представление о прогнозе заболевания, приводя к усилению болевого поведения, степени инвалидизации и ухудшению прогноза для выздоровления. Информирование пациента о заболевании может быть ограничено 3-5 ключевыми позициями (хороший прогноз, отсутствие необходимости проведения рентгенографии в отсутствие серьезной патологии, связь боли с мышцами, связками, диском и суставами, необходимость сохранять активность). Пациента желательно снабдить краткой памяткой, содержащей указанные положения.
Поддерживать уровень повседневной активности - важная позиция клинических рекомендаций по ведению пациентов с острой болью в спине. При острых скелетно-мышечных болях нет необходимости в соблюдении постельного режима (даже в первые дни заболевания), ношении фиксационных поясов, а также использовании опоры при передвижении (трость или костыли). Однако, учитывая, что в ряде случаев высокая интенсивность боли может значительно ограничивать объем повседневной активности, пациент может соблюдать постельный режим, но его необходимо проинформировать, что ограничение активности при этом можно считать только его способом уменьшить боль, а не методом лечения.
Если есть необходимость в обезболивании, необходимо назначить лекарственные препараты через равные интервалы времени (не по потребности), при этом «препаратами выбора» считают парацетамол и НПВС. Опубликованные систематические обзоры, включающие 50 РКИ (4863 пациента), свидетельствуют об эффективности НПВС при острой боли в пояснично-крестцовой области. Все НПВС условно можно разделить на группы исходя из преимущественного воздействия на изоформы циклооксигеназы (ЦОГ): ЦОГ-1 и ЦОГ-2. Большинство «стандартных» НПВС (диклофенак (вольтарен), кетопрофен, индометацин) относят к неселективным ингибиторам ЦОГ. К преимущественно селективным ингибиторам ЦОГ-2 относятся нимесулид и мелоксикам, к высокоселективным - коксибы. Селективность препаратов в отношении ЦОГ-2 обеспечивает более высокую степень безопасности в отношении ЖКТ. Частота побочных действий на ЖКТ при применении неселективных ингибиторов ЦОГ составляет 10%, а риск серьезных нежелательных явлений значительно возрастает в пожилом возрасте. Наименее часто побочные явления со стороны
ЖКТ при лечении неселективными НПВС отмечены при применении диклофенака (вольтарена) и ибупрофена, что, возможно, связано с более частым назначением низких доз этих препаратов. «Золотым стандартом» лечения острых скелетно-мышечных болевых синдромов считается диклофенак натрия (вольтарен), поэтому большинство сравнительных исследований по изучению эффективности терапии при острых болях в спине проводится с применением диклофенака. Его назначают в дозе 100-150 мг/сут. Продемонстрирован хороший эффект лорноксикама (ксефокама), препарата класса оксикамов, который назначают в суточной дозе 16 мг, в 2-3 приема. Благодаря сбалансированному ингибированию ЦОГ-1 и ЦОГ-2 и короткому периоду полувыведения препарат имеет выраженное анальгетическое и противовоспалительное действие в сочетании с невысоким риском возникновения нежелательных явлений. Эффективна последовательная схема применения кеторолака (кеторола) и нимесулида (найза). Кеторол при выраженном болевом синдроме может назначаться в первые дни заболевания (но не более 5 дней) в виде внутримышечных инъекций (90 мг/сут) с дальнейшим переходом на применение найза в дозе 200 мг/сут. В целом преимущество какого-либо одного НПВС перед другими при лечении острой боли вспине недоказано. Соответственно, при выборе НПВС необходимо принимать во внимание наличие и характер факторов риска побочных действий, наличие сопутствующих заболеваний, характер взаимодействия с другими лекарственными препаратами и стоимость. Максимальный рекомендуемый курс назначения НПВС внутрь - 10-14 сут.
Парацетамол не обладает преимуществами перед НПВС в отношении анальгетического эффекта. В то же время данные многочисленных исследований показывают эффективность парацетамола для купирования острых болевых синдромов другого происхождения. Спектр побочных действий этого препарата хорошо изучен и риск их развития относительно невысок. Это позволило большинству современных клинических рекомендаций назвать парацетамол препаратом первого ряда при лечении острой боли в спине, несмотря на меньшую, по сравнению с НПВС, доказательную базу [S. Kinkade, 2007; M.I. Harwood, 2005; С.С. Павленко, 2007].
Три систематических обзора, включившие 24 РКИ с участием 1662 пациентов, продемонстрировали эффективность миорелаксантов при острой боли в спине и достоверное отсутствие преимуществ какого-либо отдельного препарата. Анализировали как бензодиазепиновые (диазепам, тетразепамΨ), так и небензодиазепиновые (тизанидин, сирдалуд, толперизон, баклофен, циклобензапринΨ, флупиртинΘ) производные. Согласно современным клиническим рекомендациям миорелаксанты целесообразно назначать коротким курсом в виде монотерапии или в сочетании с парацетамолом и НПВС при недостаточной эффективности последних. Основными побочными эффектами, ограничивающими применение миорелаксантов, считают сонливость и головокружение, которые отмечают 70% пациентов [M. van Tulder и др., 2006].
Относительно немедикаментозных методов лечения острой боли в спине можно отметить, что мануальная терапия рекомендована пациентам, не вернувшимся к нормальному уровню повседневной активности. При этом большинство клинических рекомендаций, в том числе и последние европейские [ M. van Tulder, 2006], не указывают оптимальные сроки проведения мануальной терапии. Отмечено, что этот метод лечения эффективнее плацебо, но он не имеет преимуществ перед другими видами лечения (ЛФК, «школа боли в спине», приема анальгетиков). В целом манипуляции на позвоночнике у пациентов со скелетно-мышечной болью в спине, проводимые квалифицированными специалистами, можно считать безопасным методом лечения (риск развития синдрома компрессии конского хвоста составляет менее 1 на 1 млн).
ЛФК при острой боли в пояснично-крестцовой области посвящено 12 РКИ с участием 1900 пациентов. В 8 из них ее эффективность сравнивали с другими методами лечения [прием НПВС, стандартное лечение врачом общей практики, поддержание обычной активности, мануальная терапия, «школа боли в спине», физиотерапия (коротковолновая диатермия)]. Не выявлено преимуществ ЛФК перед перечисленными методами лечения. В 4 РКИ сравнивали эффективность ЛФК и «неактивных» методов лечения (образовательный буклет, имитация ультразвукового воздействия, постельный режим). Результаты этих наблюдений были также не в пользу ЛФК. Современные клинические рекомендации отмечают нецелесообразность назначения специальных упражнений при острой боли в пояснично-крестцовой области [M. van Tulder, 2006].
Мультидисциплинарные программы лечения целесообразно использовать у работающих пациентов с подострой болью в спине и ограничением активности более 4-8 нед. Обычно они включают в себя образовательную программу («школа боли в спине»), ЛФК, изучение и изменение условий труда, поведенческую психотерапию. При этом значение каждого из указанных методов воздействия изучить невозможно.
При острой боли в спине не эффективны тракции позвоночника и чрескожная электрическая нейростимуляция. Из-за недостаточности доказательной базы в программу лечения пациента с острой болью в поясничной области нецелесообразно включать физиотерапию, ношение согревающего пояса, применение психотерапии, посещение «школы боли в спине», назначение массажа. Существует слабая доказательность эффективности акупунктуры при острой боли в пояснично-крестцовой области.
Таким образом, в подавляющем большинстве случаев острая боль в спине - доброкачественное самоограничивающееся состояние, и большинство пациентов не нуждается в проведении дополнительных инструментальных обследований. Оптимальным считают активный подход к лечению. При необходимости медикаментозного лечения препаратами выбора считают НПВС и парацетамол. Пациентам, состояние которых не улучшается после 4 нед лечения, необходимо повторное обследование на маркеры «потенциально опасных» заболеваний позвоночника, а также определение признаков психосоциального неблагополучия и коррекция лечения с учетом выявленных нарушений.
На основании изучения эффективности лечения у пациентов, страдающих хроническими, преимущественно скелетно-мышечными болевыми синдромами, при которых выявление точного источника боли часто затруднительно, разработаны клинические рекомендации по ведению пациентов с хронической болью в спине. Тем не менее во всех случаях хронических болевых синдромов необходимо попытаться максимально тщательно выявить источник болевой импульсации, используя данные как неврологического, так и невроортопедического обследования с применением инвазивных (диагностических блокад) методов обследования. Исходя из различного удельного веса психологических факторов и объективных нарушений в каждом отдельном случае хронического болевого синдрома лечение пациентов должно быть направлено на коррекцию как периферических источников боли, так и сопутствующих психологических расстройств. Методы лечения хронической боли в спине и целесообразность их применения с позиций современных клинических рекомендаций приведены в табл. 11.
Таблица 11. Методы лечения хронической неспецифической боли в пояснично-крестцовой области
|
Метод |
Рекомендации |
Уровень доказательности1 |
|
НПВС |
Рекомендуются |
Высокий (А) |
|
Миорелаксанты (бензодиазепиновые производные) |
Рекомендуются |
Высокий (А) |
|
Миорелаксанты (небензодиазепиновые производные) |
Рекомендуются |
Низкий (С) |
|
Антидепрессанты* |
Рекомендуются |
Высокий (А) |
|
Слабые опиоиды, трансдермальные терапевтические системы с сильными опиодными анальгетиками** |
Рекомендуются |
Высокий (А) |
|
Капсаицин местно |
Рекомендуется |
Высокий (А) |
|
ЛФК |
Рекомендуется |
Высокий (А) |
|
Когнитивно-поведенческая психотерапия |
Рекомендуется |
Высокий (А) |
|
Мультидисциплинарный подход |
Рекомендуется |
Высокий (А) |
|
Мануальная терапия |
Рекомендуется |
Умеренный (В) |
|
Массаж |
Рекомендуется |
Низкий (С) |
|
«Школа боли в спине» |
Рекомендуется |
Умеренный (В) |
|
Акупунктура |
Рекомендуется |
Низкий (С) |
|
Постельный режим |
Не рекомендуется |
Высокий (А) |
|
Тракционная терапия |
Не рекомендуется |
Высокий (А) |
|
Чрескожная электронейростимуляция |
Не рекомендуется |
Умеренный (В) |
|
Эпидуральное введение кортикостероидов |
Не рекомендуется |
Отсутствует (D) |
|
Физиотерапия*** |
Нет информации в пользу или против применения |
Отсутствует (D) |
|
Ношение пояса |
Нет информации в пользу или против применения |
Отсутствует (D) |
|
РЧД и другие малоинвазивные вмешательства |
Нет информации в пользу или против применения |
Отсутствует (D) |
1 Уровни доказательности см. в табл. 10
* Норадренергические и норадреэргические и серотонинергические антидепрессанты.
** При неэффективности других методов лечения.
*** Согревание, охлаждение, электротерапия, ультразвуковое воздействие
При хронической боли в спине большое внимание при лечении необходимо уделять немедикаментозным методам лечения. Доказано, что при хронической боли в пояснично-крестцовой области эффективна ЛФК. Она способствует уменьшению интенсивности болевого синдрома и улучшению функциональных возможностей. Ее эффективность выше, чем традиционное лечение у врача общей практики с применением НПВС и других анальгетиков. Разные методы физических упражнений (аэробная нагрузка, растяжение мышц) имеют сходную клиническую эффективность. Нет преимуществ индивидуальных занятий перед занятиями ЛФК в группе. В целом эффективность ЛФК заключается в уменьшении частоты обострений и выраженности боли при них. ЛФК включена как эффективный метод практически во все клинические рекомендации по лечению хронической боли в спине [Ш.Ф. Эрдес и др., 2009; S. Haldeman, 2008; M. van Tulder и др., 2006].
Отношение к массажу при хронической боли в спине в различных клинических рекомендациях не однозначно. В Европейских клинических рекомендациях он не рекомендован при хронической боли в спине [M. van Tulder и др., 2006]. Исследователи из Канады считают его применение хорошо или умеренно доказанным. Эффективность обычного и традиционного тайского массажа одинакова. Польза от массажа повышается при его сочетании с ЛФК, образовательной программой и при его выполнении квалифицированным специалистом. Эффект сохраняется длительное время (до года) [M. Imamura и др., 2008].
Пациентам с хронической болью в спине с высоким уровнем доказательности не рекомендуют назначать постельный режим и тракционную терапию. Также не рекомендовано ношение бандажей и корсетов [M. van Tulder и др., 2006].
Эффективность мануальной терапии зависит от квалификации проводящего ее специалиста. Ее оценка затруднена, так как существует множество разновидностей мануальной терапии, а также из-за того, что выбор этого метода лечения часто определяется предпочтениями пациента. Показано, что применение мануальной терапии эффективнее, чем ее имитация. Она обладает эффективностью, сходной с применением анальгетиков, ЛФК и «школой боли в спине».
В современных клинических рекомендациях физиотерапевтические воздействия (лазеротерапия, диатермия, лечение ультразвуком, термотерапия, чрескожная электрическая стимуляция) не рекомендованы в качестве методов лечения боли в спине. Тем не менее, все эти методы широко используют при лечении хронической боли в спине в повседневной практике, вероятно, из-за выраженного дополнительного эффекта плацебо. При этом оценка их истинной эффективности крайне затруднена, так как качественные РКИ отсутствуют.
Мультидисциплинарный подход к лечению пациентов с хронической болью в поясничной области подразумевает программы медикаментозного лечения, информирования пациента, ЛФК и психотерапевтические воздействия, проводящиеся на регулярной основе (несколько часов в неделю) с участием нескольких специалистов (психотерапевта, инструктора по ЛФК, терапевта). Мультидисциплинарный подход эффективен в отношении снижения интенсивности боли и степени инвалидизации [M. van Tulder и др., 2006].
При хронической боли образовательные программы («школа боли в спине») эффективнее простого совета поддерживать активность и мануальной терапии в отношении снижения интенсивности боли и инвалидизации при оценке в ближайший период лечения. При оценке отдаленных результатов образовательные программы не имеют преимуществ перед указанными выше методами [M. van Tulder и др., 2006; S. Haldeman, 2008].
Когнитивно-поведенческая психотерапия уменьшает интенсивность боли и улучшает функциональный статус по сравнению с плацебо или ожиданием лечения. Программы, сочетающие поведенческую психотерапию с постепенным увеличением физической активности, эффективнее традиционного лечения в отношении возвращения к труду [M. van Tulder, 2006].
Для уменьшения интенсивности боли применяются НПВС, опиоидные анальгетики, миорелаксанты, антидепрессанты.
Существуют многочисленные качественные доказательства, что неселективные и селективные ингибиторы ЦОГ-2 достоверно снижают интенсивность хронической боли в спине. Доказательств преимущества анальгетической активности одного НПВС перед другим нет. При длительном приеме НПВС возрастает риск побочных явлений, в первую очередь со стороны ЖКТ и кардиоваскулярных осложнений. Соответственно, необходимо назначать их короткими курсами и с учетом индивидуальных особенностей пациента. Длительность приема НПВС при хронической боли в спине в клинических рекомендациях четко не оговаривается.
При отсутствии эффекта от других анальгетиков и НПВС или при наличии противопоказаний к их использованию для уменьшения выраженной боли в спине рекомендуют назначать слабые опиоидные анальгетики (трамадол, кодеин). Применение сильных опиоидных анальгетиков необходимо ограничить трансдермальными терапевтическими системами с постепенным пролонгированным высвобождением препарата.
Существуют доказательства, что слабые опиоидные анальгетики эффективно уменьшают хроническую боль в спине. Есть данные, что сильные опиоиды уменьшают боль в спине, а их использование в виде трансдермальных терапевтических систем позволяет резко снизить развитие побочных явлений и практически предотвращает возможность их использования в немедицинских целях. Показано, что аналгетическая эффективность опиоидных анальгетиков выше, чем у плацебо или НПВС.
Миорелаксанты (например, тизанидин (сиралуд)) при слабо выраженной хронической боли в спине можно применять в качестве альтернативы НПВС, при более выраженной боли - как дополнение к анальгетикам. Общепринято мнение, что миорелаксанты назначают для уменьшения боли, связанной с «мышечным спазмом». Однако проведенные исследования доказывают, что эта группа препаратов хоть и уменьшает интенсивность боли, но не влияет на мышечное напряжение [M. van Tulder и др., 2006].
При лечении хронических болевых синдромов традиционно предпочтение отдают антидепрессантам. Анальгетическая активность отмечена у амитриптилина, имипрамина, доксепина, кломипрамина, мапротилина, венлафаксина, дулоксетина, пароксетина и флуоксетина. Существуют доказательства, что норадренергические и норадренергическиесеротонинергические антидепрессанты эффективно помогают пациентам с хронической болью в спине и их эффективность выше, чем у ингибиторов обратного захвата серотонина. Анальгетический эффект антидепрессантов не зависит от наличия или отсутствия сопутствующей депрессии. Повседневная активность пациентов и трудоспособность при применении антидепрессантов достоверно не улучшаются.
Убедительные доказательства эффективности противосудорожных препаратов для лечения хронической боли в спине отсутствуют. Для кратковременного уменьшения болевого синдрома возможно назначение аппликаций перцового пластыря.
Акупунктура (прокалывание кожи иглой в акупунктурных точках) не эффективнее других методов лечения. Ее добавление к сочетанию ЛФК и НПВС или к «школе боли в спине», сочетающейся с ЛФК и приемом НПВС, несколько повышает эффективность лечения. Оценить эффективность метода довольно сложно из-за множества разных техник проведения процедуры.
Пролотерапия (инъекции склерозантов) не эффективнее плацебо и не рекомендована при хронической боли в спине.
В отсутствие точно установленного источника боли в спине нецелесообразно применение инвазивных методов лечения: рефлексотерапии, РЧД, электротермальной денервации и радиочастотной термокоагуляции. Показано, что эффективность малоинвазивных вмешательств на позвоночнике повышается при выявлении «специфического» (суставного, дискогенного) источника боли в спине.
Список рекомендуемой литературы[править | править код]
- Агасаров Л.Г. Восстановительное лечение при дорсопатиях. - М., 2008. - 174 с.
- Алексеев В.В., Мозолевский Ю.В., Маневич Т.М. Фибромиалгия //
Неврологический журнал. - 1999. - № 1. - С. 34-40. Боль. Руководство для врачей и студентов / Под ред. Н.Н. Яхно. - М., Медпресс, 2009. - 300 с.
- Боренштейн Д.Г., Визель С.В., Боден С.Д. Боли в шейном отделе позвоночника. Диагностика и комплексное лечение /Пер. с англ. - М.: Медицина, 2005.- 790 с.
- Веселовский В.П. Практическая вертеброневрология и мануальная терапия. - Рига, 1991. - 341 с.
- Веселовский В.П.Формылюмбоишиальгии(клинико-экпериментальное, электрофизиологическое, биохимическое и биофизическое обоснование); Дис. ... д-ра мед. наук. - Казань, 1977. - 427 с.
- Есин Р.Г., Файзуллин Р.И., Рогожин А.А. и др. Клиническая миология. - Казань: Фэн, 2003. - 272 с.
- Иваничев Г.А. Мануальная медицина. - М.: Медпресс, 2005. - 486 с. Иваничев Г.А. Миофасциальная боль. - Казань, 2007. - 392 с. Крыжановский Г.И. Детерминантные структуры в патологии нервной системы. - М., 1980. С. 61-144.
- Лиев А.А. Варианты и формы вертеброгенных миофасциальных люмбоишиалгических синдромов: Автореф. дис. ... д-ра мед. наук. -
Казань, 1995.
- Мозолевский Ю.В., Солоха С.А. Боль в области плечевого сустава // Неврологический журнал. - 2000. - № 4. - С. 4-9.
- Недзьведь Г.К., Гаврилина Т.В., Лихачев С.А. К патогенезу мышечно-тонического синдрома при поясничном остеохондрозе // Периферическая нервная система/ Под ред. Н.П. Антонова // Наука и техника. - 1985. - № 8. - С. 95-101.
- Павленко С.С. Боли в нижней части спины. - Новосибирск, 2007. - 172 с.
- Певзнер К.Б., Алексеев В.В. Пункционная чрескожная радиочастотная деструкция суставных нервов в лечении хронических поясничных болей, устойчивых к традиционной терапии // Боль. - 2005. - № 3. - С. 45-50.
- Подольская М.А. Мышечная преднастройка при поясничном остеохондрозе: Дис. ... канд. мед. наук. - Казань, 1983. - 159 с.
- Подольская М.А. Подвижность вероятностного прогнозирования в области моторики больных с неврологическими проявлениями поясничного остеохондроза // Материалы III съезда невропатологов и психиатров Белоруссии. - Минск, 1986. - C. 93-95.
- Попелянский Я.Ю. Вертеброгенные заболевания нервной системы. - Йошкар-Ола: Марийское книжное издательство, 1983. - Т. 2. - 372 с.
- Попелянский Я.Ю. Вертеброгенные заболевания нервной системы. - Казань: Издательство казанского университета, 1974. - Т. 1. -
285 с.
- Попелянский Я.Ю., Веселовский В.П. Участие позных и викарных мышечных перегрузок в формировании люмбоишиальгических синдромов // Невропатология и психиатрия. - 1976. - № 9. - С. 1281-1286.
- Попелянский Я.Ю. Вертеброгенные заболевания нервной системы. - Казань: Издательство казанского университета, 1981. - Т. 3. -
362 с.
- Попелянский Я.Ю. Ортопедическая неврология. - Казань, 1997. - Т. 1, 2.
- Попелянский Я.Ю., Марченко И.З., Бобровникова Т.И. О функциональном состоянии сегментарных и крупных позвоночных мышц при поясничном остеохондрозе // Невропатология и психиатрия. - 1970. - № 11. - С. 1626-1631.
- Пшик С.С. Миофиксационный симптомокомплекс у больных с синдромами поясничного остеохондроза: Дис. ... д-ра мед. наук. -
Казань, 1987. - 246 с.
- Соков Е.Л. Лечебные блокады в нейроортопедии. - М.: РУДН, 1995. - 192 с.
- Соков Л.П., Соков Е.Л., Соков С.Л. Клиническая нейротравматология и нейроортопедия: Руководство. - М.: Камерон, 2004. - 528 с.
- Солоха О.А., Яхно Н.Н. Диагностика и лечение синдрома плечелопаточной периартропатии// Неврологический журнал. - 2006. - № 1. - С. 26-31.
- Табеева Г.Р. Фибромиалгия // Consilium medicum. - 2000. - Т. 2. - № 12. - С. 506-508.
- Табеева Г.Р., Азимова Ю.Э. Фибромиалгия: современное понимание патогенеза и новые подходы к лечению // Боль. - 2007. - № 4. - С. 9-14.
- Табеева Д.М. Практическое руководство по иглорефлексотерапии. - М.: МЕДпресс, 2004. - 440 с.
- Тревел Д.Г., Симонс Д.Г. Миофасциальные боли /Пер. с англ. - М.: Медицина, 1989. - Т. 1-2.
- Фергюсон Л., Гервин Р. Лечение миофасциальной боли. Клиническое руководство /Пер. с англ. - М.: МЕДпресс-информ, 2008. - 539 с. Хабиров Ф.А. Клиническая неврология позвоночника. - Казань: Медицина, 2002. - 272 с.
- Хабиров Ф.А. Руководство по клинической неврологии позвоночника. - Казань: Медицина, 2006. - 518 с.
- Эрдес Ш.Ф. и др. Неспецифическая боль в нижней части спины. Клинические рекомендации для участковых терапевтов и врачей общей практики. - М.: КомплектСервис, 2008. - 70 с.
- Alcock E., Regaard A., Browne J. Facet joint injection: A rare form cause of epidural abscess formation // Pain. - 2003. - № 103. - P. 209-210.
- Alexiev A.R. Some differences in the electromyographic erector spinae activity between normal subjects and low back pain patients during the generation of isometric trunk torque // Electromyogr Clin Neurophysiolog. - 1994. - Vol. 34. - P. 495-499.
- Argoff C.E., Galer B.S., Jensen M.P. et al. Effectiveness of the lidocaine patch 5% on pain qualities in three chronic pain states: assessment with the Neuropathic Pain Scale // Curr Med Res. Opin. - 2004. - № 20. - Suppl. 2. - P. 21-28.
- Arnold L.M. Duloxetine and other antidepressants in the treatment of patients with fibromyalgia // Pain Med. - 2007. - Vol. 8. - Suppl. 2. - P. 63-74.
- Barlocher C.B., Krauss J.K., Seiler R.W. Kryorhizotomy: An alternative technique for lumbar medial branch rhizotomy in lumbar facet syndrome // J. Neurosurg. - 2003. - № 98. - P. 14-20.
- Bennett R.M., Clark S.C., Walczyk J.A. Randomized, double-blind, placebo-controlled study of growth hormone in the treatment of fibromyalgia // American Journal of Medicine. - 1998. - Vol. 104. - P. 227-231.
- Birkenmaier C., Veihelmann A., Trouillier H. et al. Medial branch blocks versus pericapsular blocks in selecting patients for percutaneous cryodenervation of lumbar facet joints // Regional Anesthesia and Pain Medicine. - 2007. - Vol. 32. - P. 27-33.
- Bliddal H., Curatolo M. Clinical manifestations of muscle and joint pain // Fundamentals of musculosceletal pain /Ed. by Graven-Nielsen T., Arendt-Nielsen L., Mense S. - Seattle: IASP Press, 2008. - P. 327-345.
- Bonica J.J., Sola A.F. Chest pain caused by other disorders. The management of pain. Ed. Bonica J.J. - London: Lea and Febiger, 1990. - P. 1114-1145.
- Brummett C.M., Cohen S.P. Facet Joint Pain in Benzon: Raj's Practical Management of Pain, 4th ed. - Mosby, 2008. Butler J.E., Taylor J.L., Gandevia S.C. Responses of human motoneurons to corticospinal stimulation during maximal voluntary contraction and ischemia // J. Neurosci. - 2003. - Vol. 23. - P. 10224-10230.
- Carette S., Marcoux S., Truchon R. et al. A controlled trial of corticosteroid injections into facet joints for chronic low back pain // N Engl J Med. - 1991. - Vol. 325. - P. 1002-1007.
- Carrera G.F., Williams A.L. Current concepts in evaluation of the lumbar facet joints // Crit Rev Diagn Imaging. - 1984. - Vol. 21. - P. 85-104.
- Carville S.F., Arendt-Nielsen S., Bliddal H. et al. EULAR evidence based recommendations for the management of fibromyalgia syndrome // Annals of the Rheumatic Diseases. - 2008. -Vol. 67 - P. 536-541.
- Charlton J.E., ed. Core Curriculum for Professional Education in Pain, 3rd edition. Seattle. - WA: IASP Press, 2005.
- Cholewicki J., Silfies S.P., Shah R.A. et al. Delayed trunk muscle reflex responses increase the risk of low back injuries // Spine. - 2005. - Vol. 30. - P. 2614-2620.
- Cohen M., Quintner J. The horse is dead: let myofascial pain syndrome rest in peace // Pain Medicine. - 2008. - Vol. 9(4). - P. 464-465.
- Cohen M.J., Swanson G.A., Naliboff B.D. Comparison of electromyographic response patterns during posture and stress tasks in chronic low back pain patients and control // J Psychosom Res. - 1986. - Vol. 30. - P. 135-141.
- Cohen S., Raja S. Pathogenesis, Diagnosis, and Treatment of Lumbar Zygapophysial (Facet Joint Pain) // Anesthesiology. - 2007. - Vol. 106. - P. 591-614.
- Cohen S.P. Postdural puncture headache and treatment following successful lumbar facet block // Pain Digest. - 1994. - Vol. 4. - P. 283-284.
- Cohen S.P., Hurley R.W., Christo P.J. et al. Clinical predictors of success and failure for lumbar facet radiofrequency denervation // Clin J Pain. - 2007. - Vol. 23. - P. 45-52.
- Croft P., Schollum J., Silman A. Population study of tender point counts and pain as evidence of fibromyalgia // BMJ. - 1994. - Vol. 309. - P. 696-699.
- Destouet J.M., Gilula L.A., Murphy W.A., Monsees B. Lumbar facet joint injection: Indication, technique, clinical correlation, and preliminary results // Radiology. - 1982. - Vol. 145. - P. 321-325.
- Dolan A.L., Ryan P.J., Arden N.K. et al. The value of SPECT scans in identifying back pain likely to benefit from facet joint injection // Br J Rheumatol. - 1996. - Vol. 35. - P. 1269-1273.
- DonTigny R. Anterior dysfunction of the sacroiliac joint as a major factor in the etiology of idiopathic low back pain syndrome // Phys Ther. - 1990. - Vol. 70. - P. 250-262.
- Dory M.A. Arthrography of the lumbar facet joints // Radiology. - 1981. - Vol. 140. - P. 23-27.
- Dreyer S.J., Dreyfuss P.H. Low back pain and the zygapophysial (facet) joints // Arch Phys Med Rehabil. - 1996. - Vol. 77. - P. 290-300.
- Dreyfuss P., Halbrook B., Pauza K. et al. Efficacy and validity of radiofrequency neurotomy for chronic lumbar zygapophysial joint pain // Spine. - 2000. - Vol. 25. - P. 1270-1277.
- Dreyfuss P.H., Dreyer S.J. Lumbar zygapophysial (facet) joint injections // Spine J. - 2003. - Vol. 3. - P. 50S-59S.
- Dreyfuss P.H., Michaelsen M., Pauza K. et al. The value of history and physical examination in diagnosing sacroiliac joint pain // Spine. - 1996. - Vol. 21. - P. 2594-2602.
- Falla D. Neuromuscular control of the cervical spine in neck pain disorders // Fundamentals of musculosceletal pain /Ed. by Graven-Nielsen T., Arendt-Nielsen L., Mense S. - Seattle: IASP Press, 2008. - P. 417- 430.
- Farina D. Effect of experimental muscle pain on motor unit properties // Fundamentals of musculosceletal pain /Ed. by Graven-Nielsen T., Arendt-Nielsen L., Mense S. - Seattle: IASP Press, 2008. - P. 461-475.
- Fortin J., Kissling R., O'Connor B. et al. Sacroiliac joint innervation and pain // Am J Orthop. - 1999. - Vol. 28. - P. 687-690.
- Gallagher J., Petriccione di Vadi P.L., Wedley J.R. et al. Radiofrequency facet joint denervation in the treatment of low back pain: A prospective controlled double-blind study to assess its efficiency // Pain Clin. - 1994. - Vol. 7. - P. 193-198.
- Gaul C., Neundorfer B., Winterholler M. Iatrogenic (para-) spinal abscesses and meningitis following injection therapy for low back pain // Pain. - 2005. - Vol. 116. - P. 407-410.
- Gavargez A., Groenemeyer D., Schirp S. et al. CT-guided percutaneous radiofrequency denervation of the sacroiliac joint // Eur Radiol. - 2002. - Vol. 12. - P. 1360-1365.
- Geisser M.E., Ranavaya M., Haig A.J. et al. A meta-analytic review of surface electromyography among persons with low back pain and normal, healthy controls // J Pain. - 2005. - Vol. 6. - Vol. 11. - P. 711-726.
- Gerwin R.D., Shannon S., Hong C.Z. et al. Interrater reliability in myofascial trigger point examination // Pain. - 1997. -Vol. 69. - P. 65-73.
- Giles L. Zygapophysial (facet) joints // Clinical anatomy and management of low back pain / Ed. by Giles L., Singer K. - Butterworth/Heinemann, 1997. - P. 72-96.
- Goldenberg D., Burckhardt C., Crofford L. Management of fibromyalgia syndrome // JAMA. - 2004. - Vol. 292. - P. 2388-2395.
- Goldstone J.C., Pennant J.H. Spinal anaesthesia following facet joint injection. A report of two cases. // Anaesthesia. - 1987. - Vol. 42. - P. 754-756.
- Greene H., Cholewicki J., Galloway M.T. et al. A history of low back injury is a risk factor for recurrent back injuries in varsity athletes// Am J Sport Med. - 2001. - Vol. 29. - P. 795-800.
- Grob K., Neuhuber W., Kissling R. Innervation of the sacroiliac joint of the human // Z Rheumatol. - 1995. - Vol. 54. - P. 117-122. Gur A., Karakoc M., Nas K. et al. Cytokines and depression in cases with fibromyalgia // Journal of Rheumatology. - 2002. - Vol. 29 (2). - P. 358-361.
- Haldeman S., Dagenais S. What have we learned about the evidence-informed management of chronic low back pain? // The Spine Journal. - 2008. - Vol. 8. - P. 266-277.
- Harwood M.I., Smith B.J. Low Back Pain: A Primary Care Approach // Clinics in Family Practice. - 2005. - Vol. 7. - № 2. - P. 279-303.
- Helbig T., Lee C.K. The lumbar facet syndrome // Spine. - 1988. - Vol. 13. - P. 61-64.
- Hides J.A., Jill G.A., Richardson C.A. Long term effects of specific stabilizing exercises for first episode low back pain // Spine. - 2001. - Vol. 26. - P. 243-248.
- Ho K., Tan К. Botulinum toxin A for myofascial trigger point injection: A qualitative systematic review // European Journal of Pain. - 2007. - Vol. 11. - P. 519-527.
- Hodges P. Changes in sensorimotor control in low back pain // Fundamentals of musculosceletal pain /Ed. by Graven-Nielsen T., Arendt-Nielsen L., Mense S. - Seattle: IASP Press, 2008. - P. 445-453.
- Imamura M., Furlan A.D., Dryden T. et al. Evidence-informed management of chronic low back pain with massage // The Spine Journal. - 2008. - Vol. 8. - P. 123-133.
- Imamura M., Imamura S. Tietze Syndrome in Frontera: Essentials of Physical Medicine and Rehabilitation, 2nd ed. - Saunders, An Imprint of Elsevier, 2008.
- Inbody S.B. Myofascial pain syndrome // Neurobase, fourth ed. - 1998.
- Jackson R.P., Jacobs R.R., Montesano P.X. 1988 Volvo award in clinical sciences. Facet joint injection in low-back pain: A prospective statistical study // Spine. - 1988. - Vol. 13. - P. 966-971.
- Jensen M.C., Brant-Zawadzki M.N., Obuchowski N. et al. Magnetic resonance imaging of the lumbar spine in people without back pain // N Engl J Med. - 1994. - Vol. 331. - P. 69-73.
- Kay J., Findling J.W., Raff H. Epidural triamcinolone suppresses the pituitary-adrenal axis in human subjects // Anesth Analg. - 1994. - Vol. 79. - P. 501-505.
- Kellegren J.H. On the distribution of pain arising from deep somatic structures with charts of segmental pain areas // Clin Sci. - 1939. - Vol. 4. - P. 35-46.
- King J.S., Lagger R. Sciatica viewed as a referred pain syndrome // Surg Neurol. - 1976. - Vol. 5. - P. 46-50.
- King W., Lau P., Lees R., Bogduk N. The validity of manual examination in assessing patients with neck pain // Spine J. - 2007. - Vol. 7. - P. 22-26.
- Kinkade S. Evaluation and Treatment of Acute Low Back Pain // American Family Physician. - 2007. - Vol. 75. - № 8. - P. 1181-1188.
- Kornick C., Kramarich S.S., Lamer T.J., Todd Sitzman B. Complications of lumbar facet radiofrequency denervation // Spine. - 2004. - Vol. 29. - P. 1352-1354.
- Lavelle E.D., Lavelle W., Smith Н. Myofascial trigger points // Med Clin North Am. - 2007. - Vol. 91 (2). - P. 229-239.
- Le Pera D., Graven-Nielsen T., Valeriani M. et al. Inhibition motor system excitability at cortical and spinal level by tonic muscle pain // Clin Neurophysiology. - 2001. - Vol. 112. - P. 1633-1641.
- Lewinnek G.E., Warfield C.A. Facet joint degeneration as a cause of low back pain // Clin Orthop Relat Res. - 1986. - P. 216-222.
- Lilius G., Laasonen E.M., Myllynen P. et al. Lumbar facet joint syndrome. A randomised clinical trial // J Bone Joint Surg Br. - 1989. - Vol. 71. - P. 681-684.
- Lilius G., Laasonen E.M., Myllynen P. et al. Lumbar facet joint syndrome. Significance of non-organic signs. A randomized placebo-controlled clinical study // Rev Chir Orthop Reparatrice Appar Mot. - 1989. - Vol. 75. - P. 493-500.
- Lippitt A.B. The facet joint and its role in spine pain. Management with facet joint injections // Spine. - 1984. - Vol. 9. - P. 746-750.
- Long D.M., BenDebba M., Torgerson W.S. et al. Persistent back pain and sciatica in the United States: Patient characteristics // J Spinal Disord. - 1996. - Vol. 9. - P. 40-58.
- Maigne J.Y., Aivaliklis A., Pfefer F. Results of sacroiliac joint double block and value of sacroiliac pain provocation tests in 54 patients with low back pain // Spine. - 1996. - Vol. 21. - P. 1889-1892.
- MalikK., Benzon H. Low back pain in Benzon: Raj's Practical Management of Pain, 4th ed. - Mosby, 2008.
- Manchikanti L., Boswell M.V., Singh V. et al. Prevalence of facet joint pain in chronic spinal pain of cervical, thoracic, and lumbar regions // BMC Musculoskel Disord. - 2004. - Vol. 5. - P. 15.
- Manchikanti L., Manchikanti K.N., Damron K.S., Pampati V. Effectiveness of cervical medial branch blocks in chronic neck pain: A prospective outcome study //Pain Physician. - 2004. - Vol. 7. - P. 195-201.
- Manchikanti L., Manchikanti K.N., Manchukonda R. et al. Evaluation of therapeutic thoracic medial branch block effectiveness in chronic thoracic pain: A prospective outcome study with minimum 1-year follow up // Pain Physician. - 2006. - Vol. 9. - P. 97-105.
- Manchikanti L., Pampati V., Bakhit C.E. et al. Effectiveness of lumbar facet joint nerve blocks in chronic low back pain: A randomized clinical trial // Pain Physician. - 2001. - Vol. 4. - P. 101-117.
- Manchikanti L., Pampati V., Fellows B., Bakhit C.E. Prevalence of lumbar facet joint pain in chronic low back pain // Pain Physician. - 1999. - Vol. 2. - P. 59-64.
- Manchikanti L., Pampati V., Fellows B., Bakhit C.E. The diagnostic validity and therapeutic value of lumbar facet joint nerve blocks with or without adjuvant agents // Curr Rev Pain. - 2000. - Vol. 4. - P. 337-344.
- Marks R.C., Houston T., Thulbourne T. Facet joint injection and facet nerve block: A randomised comparison in 86 patients with chronic low back pain // Pain. - 1992. - Vol. 49. - P. 325-328.
- McCulloch J.A., Organ L.W. Percutaneous radiofrequency lumbar rhizolysis (rhizotomy) // Can. Med. Assoc. J. - 1977. - Vol. 116. - P. 28-30.
- Mense S., Hoheisel U. Mechanisms of central nervous hyperexcitability due to activation of muscle nociceptors / Fundamentals of musculosceletal pain /Ed. by Graven-Nielsen T., Arendt-Nielsen L., Mense S. - Seattle: IASP Press, 2008. - P. 61-73.
- Mense S., Hoheisel U. Morphology and functional types of muscle nociceptors / Fundamentals of musculosceletal pain /Ed. by Graven-Nielsen T., Arendt-Nielsen L., Mense S. - Seattle: IASP Press, 2008. - P. 3-17.
- Mikeladze G., Espinal R., Finnegan R. et al. Pulsed radiofrequency application in treatment of chronic zygapophyseal joint pain // Spine. - 2003. - Vol. 3. - P. 360-362.
- Moran R., OConnell D., Walsh M.G. The diagnostic value of joint facet injections // Spine. - 1988. - Vol. 13. - P. 1407-1410.
- Mountz J.M., Bradley L.A., Modell J.G. et al. Fibromyalgia in women. Abnormalities of regional cerebral blood flow in the thalamus and the caudate nucleus are associated with low pain threshold levels // Arthritis and Rheumatism. - 1995. - Vol. 38. - P. 926-938.
- Murtagh F.R. Computed tomography and fluoroscopy guided anesthesia and steroid injection in facet syndrome // Spine. - 1988. - Vol. 13. - P. 686-689.
- Nash T.P. Facet joints - Intraarticular steroids or nerve block? // Pain Clin. - 1990. - Vol. 3. - P. 77-82.
- Niemisto L., Kalso E., Malmivaara A. et al. Radiofrequency denervation for neck and back pain: A systematic review within the framework of the Cochrane Collaboration Back Review Group // Spine. - 2003. - Vol. 28. - P. 1877-1888.
- North R.B., Han M., Zahurak M. et al. Radiofrequency lumbar facet denervation: Analysis of prognostic factors // Pain. - 1994. - Vol. 57. - P. 77-83.
- Ojala T., Arokoski J. P., Partanen J. The Effect of Small Doses of Botulinum Toxin A on Neck-Shoulder Myofascial Pain Syndrome: A DoubleBlind,Randomized, and Controlled Crossover Trial // Clin Journ Pain. - 2006. - Vol. 22. - P. 90-96.
- Orpen N.M., Birch N.C. Delayed presentation of septic arthritis of a lumbar facet joint after diagnostic facet joint injection // J Spinal Disord Tech. - 2003. - Vol. 16. - P. 285-287.
- OstgaardH.C., Andersson G.J., Karlsson K. Prevalence ofback pain in pregnancy // Spine. - 1991. - Vol. 16. - P. 549-552.
- Pedersen J., Sjolander P., Wenngren B.I. et al. Increased intramuscular concentration of bradykinin increases the static fusimotor drive to muscle spindles in neck muscles of the cat // Pain. - 1997. - Vol. 70. - P. 83-91.
- Pino C.A., Hoeft M.A., Hofsess C. et al. Morphologic analysis of bipolar radiofrequency lesions: Implications for treatment of the sacroiliac joint // Reg Anesth Pain Med. - 2005. - Vol. 30. -P. 335-338.
- Pneumaticos S.G., Chatziioannou S.N., Hipp J.A. et al. Low back pain: Prediction of short-term outcome of facet joint injection with bone scintigraphy // Radiology. - 2006. - Vol. 238. - P. 693-698.
- Porterfield J., DeRosa C. Mechanical low back pain. 2nd ed. - Philadelphia: W.B.Saunders Company, 1998. - P. 278. Rashbaum R.F. Radiofrequency facet denervation: A treatment alternative in refractory low back pain with or without leg pain // Orthop Clin North Am. - 1983. - Vol. 14. - P. 569-575.
- Raymond J., Dumas J.M. Intraarticular facet block: Diagnostic test or therapeutic procedure? // Radiology. - 1984. - Vol. 151. - P. 333-336.
- Revel M.E., Listrat V.M., Chevalier X.J. et al. Facet joint block for low back pain: Identifying predictors of a good response // Arch Phys Med Rehabil. - 1992. - Vol. 73. - P. 824-828.
- Rossignol M., Arsenault B., Dione C. et al. Clinic in low back pain in interdisciplinary practice (CLIP) guidelines. - Direction de sante publique. - Montreal: Agence de la sante et des services sociaux de Montreal. - 2007. - P. 41.
- Russell I.J. Myofascial pain syndrome and fibromyalgia syndrome in Raj's Practical Management of Pain, 4th ed. /Ed. H. Benzon. - Philadelphia: Mosby Elsivier. - 2008. - P. 1319.
- Russell I.J., Bieber C.S. Myofascial pain and fibromialgia syndrome // McMahon S, Wall and Melzack's Textbook of Pain. 5th ed. - Churchill Livingstone, 2006. - Р. 1280.
- Schaerer J.P. Radiofrequency facet rhizotomy in the treatment of chronic neck and low back pain // Int Surg. - 1978. - Vol. 63. - P. 53-59.
- Schwarzer A.C., Aprill C.N., Bogduk N. The sacroiliac joint in chronic low back pain // Spine. - 1995. - Vol. 20. - P. 31-37.
- Schwarzer A.C., Aprill C.N., Derby R. et al. The false-positive rate of uncontrolled diagnostic blocks of the lumbar zygapophysial joints // Pain. - 1994. - Vol. 58. - P. 195-200.
- Schwarzer A.C., Wang S.C., Bogduk N. et al. Prevalence and clinical features of lumbar zygapophysial joint pain: a study in an Australian population with chronic low back pain // Ann Rheum Dis. - 1995. - Vol. 54. - P. 100-106.
- Shekelle P., Woolf S.H., Eccles M. Clinical guidelines: Developing guidelines // BMJ. - 1999. - Vol. 318. - P. 593-596.
- Sheridan M.A. Upper extremity: emphasis on frozen shoulder // Orthop Clin North Am. - 2006. - Vol. 37 (4). - P. 531-539.
- Silvers H.R. Lumbar percutaneous facet rhizotomy // Spine. - 1990. - Vol. 15. - P. 36-40.
- Simons D.G. The Dead Horse, Like the Phoenix, Is Arising- // Pain Medicine. - 2008. - Vol. 9 (4). - P. 469-470.
- Slipman C.W., Lipetz J.S., Plastaras C.T. et al. Fluoroscopically guided therapeutic sacroiliac joint injections for sacroiliac joint syndrome // Am J Phys Med Rehabil. - 2001. - Vol. 80. - P. 425-432.
- Sowa G. Facet-mediated pain // Dis Mon. - 2005. - Vol. 51. - P. 18-33.
- Staender M., Maerz U., Tonn J.C. et al. Computerized tomography-guided kryorhizotomy in 76 patients with lumbar facet joint syndrome // J. Neurosurg Spine. - 2005. - Vol. 3. - Р. 444-449.
- Travell J.G., Simons D.G. Myofascial Pain and Dysfunction: The Trigger Point Manual. Vol.2 The lower extremities. - Lippincott Williams & Wilkins, 1992. - P. 628.
- Valeriani M., Restuccia D., Lazzaro V. et al. Inhibition of human of the human primary motor area by painful heat stimulation of the skin // Clinical Neurophysiology. - 1999. - Vol. 110. - P. 1475-1480.
- van Boxem K., van Eerd M., Brinkhuize T. Radiofrequency and pulsed radiofrequency treatment of chronic pain syndromes: the available evidence // Pain Practice. - 2008. - Vol. 8 (5). - P. 385-93.
- van Kleef M., Barendse G.A., Kessels A. et al. Randomized trial of radiofrequency lumbar facet denervation for chronic low back pain // Spine. - 1999. - Vol. 24. - P. 1937-1942.
- van Tulder M., Becker А., Bekkering T. et al. European guidelines for the management of acute nonspecific low back pain in primary care // European Spine Journal. - 2006. - Vol. 15. - Suppl. 2. - P. 169-191.
- van Wijk R.M., Geurts J WW., Wynne H.J. et al. Radiofrequency denervation of lumbar facet joints in the treatment of chronic low back pain: A randomized, double-blind, sham lesion-controlled trial // Clin J Pain. - 2005. - Vol. 21. - P. 335-344.
- Ward A., Watson J., Wood P. et al. Glucocorticoid epidural for sciatica: Metabolic and endocrine sequelae // Rheumatology (Oxford). - 2002. - Vol. 41. - P. 68-71.
- Weishaupt D., Zanetti M., Hodler J. et al. MR imaging of the lumbar spine: Prevalence of intervertebral disk extrusion and sequestration, nerve root compression, end plate abnormalities, and osteoarthritis of the facet joints in asymptomatic volunteers // Radiology. - 1998. - Vol. 209. - P. 661-666.
- Wiesel S.W., Tsourmas N., Feffer H.L. et al. A study of computer-assisted tomography. I. The incidence ofpositive CAT scans in an asymptomatic group of patient// Spine. - 1984. - Vol. 9. - P. 549-551.
- Wolfe F., Rasker J. Fibromyalgia // Kelly's Textbook of rheumatology / Ed. by Ferestein G. - W.B. Saunders Company, 2008 - www.mdconcult.com