Миорелаксанты - классификация, препараты, применение
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Миорелаксанты[править | править код]
Историческая справка. Источники. Химические свойства. Кураре — это обобщающее название ядов, используемых для смазывания стрел южноамериканскими индейцами. История открытия и применения кураре долгая и увлекательная. В течение многих веков индейцы, обитающие по берегам Амазонки и Ориноко, применяли его для охоты — раненые животные погибали от паралича. Изготовление кураре было покрыто тайной, которой владели лишь колдуны. Вскоре после открытия Америки сэр Уолтер Рали и другие первопроходцы и ученые заинтересовались этим ядом, и в конце XVI века он впервые был доставлен в Европу. После работ путешественника и естествоиспытателя фон Гумбольдта, проведенных в 1805 г., начались поиски растений — источников кураре. Оказалось, что кураре из восточных областей Амазонки содержится в растениях рода стрихнос (Strychnos). В дальнейшем стало известно, что южноамериканские растения этого рода содержат преимущественно четвертичные алкалоиды, обладающие способностью блокировать нервно-мышечное проведение, тогда как азиатские, африканские и австралийские — четвертичные алкалоиды, по свойствам близкие к стрихнину.
Именно с помощью кураре Клод Бернар впервые показал, что точкой приложения фармакологических веществ может быть область соединения нерва с мышцей (Bernard, 1856). В клинике же кураре, видимо, впервые применил Уэст в 1932 г.: он использовал высокоочищенные препараты этого вещества у больных со столбняком и спастическими состояниями.
Резкий толчок исследованиям кураре был дан Джиллом (Gill, 1940). После долгого и подробного изучения индейских способов изготовления кураре он привез в США достаточное количество этого яда, чтобы можно было начать изучение его химических и фармакологических свойств. Для миорелаксации кураре впервые применили Гриффит и Джонсон в 1942 г. (Griffith and Johnson, 1942). Подробнее с захватывающей историей исследования этого вещества, его номенклатурой, получением и расшифровкой строения отдельных его алкалоидов и многими другими деталями можно ознакомиться в обзорах Mcl ntyre (1947) и Bovet (1972), а также в предыдущих изданиях настоящей книги.
Структура тубокурарина (рис. 9.2) была установлена Кингом в 1935 г. Синтетическое производное тубокурарина — диметил-тубокурарин — содержит 3 дополнительные метильные группы, одна из которых присоединена ко второму атому азота (превращая его тем самым в четвертичный), а две другие образуют эфирные связи с бензольными кольцами. Активность этого соединения у человека в 2—3 раза выше, чем тубокурарина.
Самые мощные из алкалоидов кураре — токсиферины — получают из стрихноса ядовитого (Strychnos toxifera). В клиниках европейских и других стран широко использовалось полусинтетическое производное токсиферинов — алкуроний (N.N'-ди-аллилнортоксиферина дихлорид). Семена деревьев и кустарников рода эритрина (Erythrina), широко распространенных в тропических и субтропических районах, содержат эритроидины, обладающие курареподобным действием.
В 1949 г. Бове и сотр. опубликовали данные о нескольких синтетических курареподобных веществах, в том числе — галламине (Bovet, 1972). Ранние исследования зависимости активности таких веществ от их структуры привели к разработке полиметилен-ди-триметиламмониевых соединений — так называемых метониевых производных(Barlow and Ing, 1948; Patonand Zaimis, 1952). Самым мощным из них как миорелаксант оказался декаметоний, содержащий в полиметиленовой цепи 10 атомов углерода (рис. 9.2). Гексаметоний, содержащий 6 таких атомов, на нервно-мышечное проведение не действовал, но зато оказался мощным ганглиоблокатором (см. ниже).
В 1949 г. было описано курареподобное действие суксаметония хлорида, и вскоре его стали применять для кратковременной миорелаксации (Dorkins, 1982).
Классификация и химические свойства[править | править код]
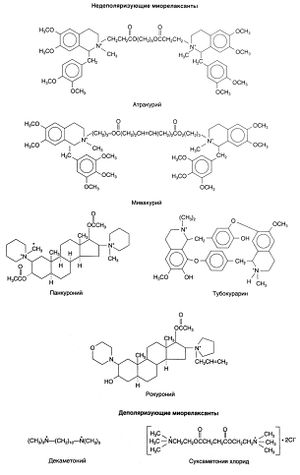
В настоящее время широко используется только один деполяризующий миорелаксант — суксаметония хлорид и множество недеполяризующих миорелаксантов (рис. 9.2). При выборе препарата исходят из того, чтобы его фармакокинетические свойства (табл. 9.1) соответствовали предполагаемому сроку операции, а побочные эффекты (сердечно-сосудистые и другие) были минимальными. В соответствии с этими требованиями имеются две классификации миорелаксантов. В первой из них все они подразделяются на препараты короткого, среднего и длительного действия. Блокада нервно-мышечного проведения, вызываемая миорелаксантами длительного действия (тубокурарином, диметилтубокурарином, панкуронием и доксакурием), слишком продолжительная и стойкая, и поэтому были разработаны средства средней продолжительности действия — векуроний и атракурий. Вскоре последовало появление миорелаксанта короткого действия — мивакурия. Препараты длительного действия обычно обладают наиболее высокой активностью, в связи с чем дозы их должны быть низкими — а это приводит к более позднему началу действия. Рокуроний и рапакуроний — миорелаксанты средней продолжительности действия, но с низкой активностью и быстрым началом. Последнее свойство позволило использовать их вместо суксаметония хлорида для расслабления мышц гортани и челюстей при интубации трахеи (Bevan, 1994; Savarese et al., 2000).
Вторая классификация основана на химическом строении миорелаксантов. В этой классификации они подразделяются на природные алкалоиды и их производные, аммониевые стероиды и бензилизохинолины (табл. 9.1). Природный алкалоид тубокурарин и полусинтетический алкалоид алкуроний имеют большое историческое значение, но сейчас используются редко. Новые препараты обладают не только более коротким действием, но и существенно меньшими побочными эффектами, главными из которых являются ганглиоблокирующее и ваголитическое действие и высвобождение гистамина. Диметилтубокурарин также оказывает ганглиоблокирующий эффекта вызывает высвобождение гистамина, хотя и в меньшей степени, чем тубокурарин. Типичный аммониевый стероид панкуроний почти не вызывает высвобождение гистамина, однако он блокирует М-холинорецепторы, что приводит к тахикардии. Последняя не возникает при использовании новейших аммониевых стероидов — векурония,рокурония, рапакурония и пипекурония.
Бензилизохинолины, видимо, не оказывают ганглиоблокирующее и ваголитическое действие, но вызывают незначительное высвобождение гистамина. Атракурий и его новое производное мивакурий обладают своеобразным метаболизмом, и поэтому показания к их назначению особые. Так, элиминация атракурия происходит двумя путями — гидролизом эфирной связи эстеразами плазмы и спонтанной деградацией (отщеплением N-ал-киловой группы). Оба эти пути не зависят от почечной экскреции. Мивакурий чрезвычайно чувствителен к холинэстеразам, что и предопределяет кратковременность его действия.
Структурно-функциональная зависимость. Между деполяризующими и недеполяризующими миорелаксантами имеются несколько структурных отличий. Молекулы недеполяризующих миорелаксантов (тубокурарина, токсиферинов, аммониевых стероидов и бензил изохинолинов) относительно большие и жесткие, а деполяризующих (декаметония и суксаметония хлорида) — более гибкие и способные к свободному вращению фрагментов вокруг одинарных химических связей (рис. 9.2; Bovet, 1972). В связи с этим у деполяризующих миорелаксантов расстояние между четвертичными аммониевыми группами может меняться, достигая максимально возможного значения (для декаметония — 1,45 нм), а у недеполяризующих оно постоянно (обычно 1 ± 0,1 нм); l-тубокурарин значительно менее активен, чем d-тубокурарин. Расстояние между атомами азота у них одинаковое, однако у d-тубокурарина все гидрофильные группы располагаются с одной стороны.
Фармакологические свойства[править | править код]
Действие на скелетные мышцы. Местный паралич, вызываемый кураре, был впервые описан Клодом Бернаром в 1850-х гг. Современными методами (флюоресцентная и электронная микроскопия, микроионофоретическая аппликация фармакологических средств, исследование одиночных каналов методом локальной фиксации, микроэлектродная регистрация) было установлено, что точкой приложения тубокурарина и других миорелаксантов служит постсинаптическая мембрана нервно-мышечного синапса. В общих чертах механизм их действия сводится к тому, что они соединяются с постсинаптическими N-холинорецепторами и препятствуют действию на них ацетилхолина. Если нанести такой препарат непосредственно на постсинаптическую мембрану изолированного мышечного волокна, то это волокно перестает отвечать как на раздражение двигательного нерва, так и на аппликацию ацетилхолина. При этом и сама постсинаптическая мембрана, и волокно в целом сохраняют способность деполяризоваться при повышении внеклеточной концентрации калия и отвечать на прямое электрическое раздражение.
Для более подробного ознакомления с действием миорелаксантов необходимо вспомнить некоторые детали активации N-холинорецептора ацетилхолином. Высвобождение ацетилхолина нервным окончанием, возникновение миниатюрных потенциалов концевой пластинки, их суммация, развитие постсинаптического потенциала действия и сокращение мышечного волокна рассмотрены в гл. 6. В электрофизиологических исследованиях показано, что ацетилхолин и другие стимуляторы вызывают временное открывание отдельных каналов, подчиняющееся закону «все или ничего». В результате возникает П-образный импульс тока, значения длительности которого экспоненциально распределяются относительно средней величины в 1 мс. Средняя проводимость открытого канала составляет 10—20 пСим. Длительность пребывания канала в открытом состоянии гораздо больше зависит от природы стимулятора, чем проводимость (Sakmann, 1992).
Таблица 9.1. Миорелаксанты
|
Препарат |
Группа (химическое строение) |
Фармакологические свойства |
Начало действия, мин |
Продолжительность действия, мин |
Элиминация |
|
Суксаметония хлорид |
Диацетилхолин |
Деполяризующий, сверхкороткого действия |
1-1,5 |
5-8 |
Гидролиз псевдохолинэстеразой |
|
Тубокурарин |
Природный алкалоид (циклический бензилизо-хинолин) |
Недеполяризующий, длительного действия |
4-6 |
80-120 |
Почечная экскреция и печеночный метаболизм |
|
Атракурий |
Бензилизохинолин |
Недеполяризующий, промежуточного действия |
2-4 |
30-60 |
Спонтанная деградация, гидролиз псевдохолинэстеразой, почечная экскреция |
|
Доксакурий |
Бензилизохинолин |
Недеполяризующий, длительного действия |
4-6 |
90-120 |
Почечная экскреция |
|
Мивакурий |
Бензилизохинолин |
Недеполяризующий, короткого действия |
2-4 |
12-18 |
Гидролиз псевдохолинэстеразой |
|
Панкуроний |
Аммониевый стероид |
Недеполяризующий, длительного действия |
4-6 |
120-180 |
Почечная экскреция |
|
Пипекуроний |
Аммониевый стероид |
Недеполяризующий, длительного действия |
2-4 |
80-100 |
Почечная экскреция и печеночный метаболизм |
|
Рапакуроний |
Аммониевый стероид |
Недеполяризующий, промежуточного действия |
1-2 |
15—30 |
Печеночный метаболизм |
|
Рокуроний |
Аммониевый стероид |
Недеполяризующий, промежуточного действия |
1-2 |
30-60 |
Печеночный метаболизм |
|
Векуроний |
Аммониевый стероид |
Недеполяризующий, промежуточного действия |
2-4 |
60-90 |
Почечная экскреция и печеночный метаболизм |
При нанесении недеполяризующего миорелаксанта тубокурарина в возрастающих концентрациях амплитуда потенциала концевой пластинки постепенно снижается, однако потенциал действия может возникать вплоть до тех пор, пока эта амплитуда не уменьшится на 70% и более. Это говорит о высокой надежности нервно-мышечной передачи. Как и другие конкурентные блокаторы рецепторов, тубокурарин снижает частоту открываний каналов, а не проводимость одиночного канала или длительность его пребывания в открытом состоянии (Katz and Miledi, 1978). При использовании высоких концентраций производных кураре и других недеполяризующих миорелаксантов блокада канала носит неконкурентный и потенциалзависимый характер (Colquhoun et al., 1979).
Время спада миниатюрного потенциала концевой пластинки примерно такое же, как средняя длительность пребывания канала в открытом состоянии (1 —2 мс). Поскольку эти потенциалы обусловлены спонтанным выделением одиночных квантов ацетилхолина (около 10 молекул), количество ацетилхолина в синаптической щели при развитии этих потенциалов невелико, он быстро разрушается АХЭ, и его отдельные молекулы не успевают повторно связаться с рецепторами и снова вызвать открывание каналов. Время уменьшения концентрации выделившегося ацетилхолина в синаптической щели меньше, чем время спада потенциала (или тока) концевой пластинки.
В присутствии ингибиторов АХЭ потенциал и ток концевой пластинки удлиняются до 25—30 мс. Значит, перед тем как ацетилхолин диффундирует из синаптической щели, он успевает многократно связаться с рецепторами. Не удивительно, что ингибиторы АХЭ являются антагонистами недеполяризующих миорелаксантов: увеличение пребывания ацетилхолина в синаптической щели приводит к тому, что он успевает вытеснить миорелаксант из связи с рецептором.
Для активации N-холинорецептора необходимо, чтобы с этим рецептором соединились две молекулы стимулятора (по одной на каждый участок связывания — на стыках субъединиц ау и аб,см. выше). Для этой активации характерна положительная императивность, и поэтому она происходит в узком диапазоне концентраций стимулятора (Sine and Claudio, 1991; Changeux and Edelstein, 1998). Хотя с каждым рецептором могут связаться 2 молекулы недеполяризующего миорелаксанта или, например, а-нейротоксина, присоединения одной из них достаточно для его блокирования.
Механизм действия деполяризующих миорелаксантов (суксаметония хлорида, декаметония) иной. Сначала они, как и ацетилхолин, открывают постсинаптические каналы и вызывают деполяризацию постсинаптической мембраны. Однако они остаются в синаптической щели гораздо дольше, прежде всего из-за устойчивости к действию АХЭ. Поэтому и вызываемая ими деполяризация более продолжительная, что приводит к временным фасцикуляциям мышц. После этой начальной фазы наступает блокада нервно-мышечного проведения и вялый паралич мышц. Причина этого в следующем: высвобождающийся из нервных окончаний ацетилхолин действует на уже деполяризованную постсинаптическую мембрану и не может деполяризовать ее еще больше; в тоже время потенциал действия вызывается изменением мембранного потенциала в сторону деполяризации. Если постсинаптическая мембрана деполяризована до —55 мВ (в норме ее потенциал составляет —80 мВ), то она полностью нечувствительна к действию ацетилхолина. Такая последовательность (сначала повторные возбуждения мышц, проявляющиеся фасцикуляциями, затем блокада проведения с вялым параличом) наблюдается поддействием деполяризующих миорелаксантов и у человека; впрочем, она зависит от природы средства для общей анестезии, типа мышцы и скорости введения миорелаксанта. Сравнительная характеристика действия деполяризующих и недеполяризующих миорелаксантов приведена в табл. 9.2.
У некоторых животных и иногда — у человека декаметонийи суксаметония хлорид оказывают своеобразный эффект, действуя сначала как деполяризующие, а затем как недеполяризующие миорелаксанты (двухфазное действие; Zaimis, 1976). В таких случаях сначала быстро возникает типичная для деполяризующих миорелаксантов блокада; ей предшествуют фасцикуляции, а сама блокада усугубляется ингибиторами АХЭ. Однако вскоре появляются черты, характерные для действия недеполяризующих миорелаксантов, — быстрое утомление при тетанизирующем раздражении двигательного нерва, усугубление блокады тубокурарином и ее уменьшение под действием ингибиторов АХЭ.
Двухфазное действие заметно и при микроэлектродной регистрации — при продолжающемся воздействии препарата первоначальная деполяризация сменяется постепенной реполяризацией. Эта вторая фаза сходна с десенситизацией рецепторов (Katz and Thesleff, 1957).
Таблица 9.2. Сравнительная характеристика недеполяризующих (тубокурарин) и деполяризующих (декаметоний) миорелаксантов
|
Тубокурарин |
Декаметоний | |
|
Предварительное введение тубокурарина |
Суммация эффектов |
Антагонистическое действие |
|
Предварительное введение декаметония |
Эффекта нет либо антагонистическое действие |
Умеренное привыкание, но возможна суммация эффектов |
|
Введение ингибиторов АХЭ на фоне миорелаксантов |
Уменьшение степени блокады |
Степень блокады не уменьшается |
|
Изменения в постсинаптической мембране |
Снижение чувствительности к ацетилхолину, деполяризации нет |
Стойкая деполяризация |
|
Фаза возбуждения скелетных мышц |
Нет |
Преходящие фасцикуляции |
|
Тетанизирующее раздражение двигательного нерва при частичной блокаде |
Быстрое утомление |
Стойкий тетанус |
У человека при продолжающемся введении суксаметония хлорида или при повышении его концентрации нервно-мышечная блокада может медленно перейти от депопяризацион-ного к недеполяризационному (конкурентному) типу, или от первой ко второй фазе (Durand and Katz, 1982). Характер блокады в известной степени зависит от применяемого средства для обшей анестезии: при длительном введении суксаметония хлорида и декаметония переход ко второй фазе чаще наблюдается на фоне фторзамещенных углеводородов (Zaimis, 1976; Fogdall and Miller, 1975). Характеристики первой и второй фаз нервно-мышечной блокады, вызванной деполяризующими миорелаксантами, приведены в табл. 9.3.
В начале своего действия деполяризующие миорелаксанты вызывают открывание постсинаптических каналов (это можно зарегистрировать методом анализа флюктуаций потенциала концевой пластинки). Вероятность открывания канала при присоединении декаметония ниже, чем при присоединении ацетилхолина (Katz and Miledi, 1978); следовательно, декаметоний можно отнести к частичным агонистам N-холинорецепторов. В высоких концентрациях декаметоний блокирует канал (Adams and Sakmann, 1978).
Хотя фасцикуляции можно объяснить раздражением пресинаптического нервного окончанием с последующим антидромным возбуждением аксона и двигательной единицы, основной точкой приложения деполяризующих и недеполяризующих миорелаксантов все же служит постсинаптическая мембрана. Пресинаптическое действие недеполяризующих миорелаксантов может иметь значение при продолжительном высокочастотном раздражении нерва, так как активация пресинаптических N-холинорецепторов усиливает выделение медиатора из окончаний мотонейронов (Bowman et al., 1990; Van der Kloot and Molgo, 1994).
Многие лекарственные средства и токсины влияют на другие этапы нервно-мышечной передачи, например на синтез и высвобождение ацетилхолина (Van der Kloot and Molgo, 1994; см. также гл. 6). В клинике с этой целью подобные препараты не используются. Одно из исключений составляет ботулотоксин А; его вводят в глазные мышцы при косоглазии и блефароспазме, а также в другие мышцы при их спазме (например, в мышцы лица) (гл. 6 и 66). Иногда ботулотоксин А вводят также в нижний пищеводный сфинктер при ахапазии кардии (гл. 38). Второе исключение — это дантролен. Этот препарат, блокирующий высвобождение Са2+ из саркоплазматического ретикулума, применяют при злокачественной гипертермии (см. ниже). Точки приложения ряда лекарственных средств и веществ, применяемых в фармакологическом анализе, приведены на рис. 9.3. Клинические характеристики миорелаксации. При в/в введении достаточной дозы недеполяризующего миорелаксанта развивается мышечная слабость, сменяющаяся полным вялым параличом. Первыми реагируют мелкие быстрые мышцы (глаз, челюстей, гортани), а затем уже мышцы туловища и конечностей. В последнюю очередь наступает паралич межреберных мышц и диафрагмы, и тогда возникает остановка дыхания. Восстановление обычно происходит в обратном порядке, и первой начинает работать диафрагма (Feldman and Fauvel, 1994; Sava-rese et al., 2000).
После однократного в/в введения 10—30 мг суксаметония хлорида развиваются фасцикуляции, особенно мышц грудной клетки и живота; миорелаксация наступает через 1 мин, достигает максимума на 2-й минуте и обычно проходит через 5 мин. Во время миорелаксации обычно наблюдается временная остановка дыхания. Для более длительной миорелаксации применяют постоянную в/в инфузию. После ее остановки действие препарата вскоре прекращается, так как он быстро гидролизуется псевдохолинэстеразой плазмы и печени. После применения суксаметония хлорида возможна боль в мышцах. Для ее уменьшения и устранения фасцикуляций пытались предварительно вводить недеполяризующие миорелаксанты в малых дозах, однако подход этот сомнителен, так как требует увеличения дозы суксаметония хлорида.
Длительная деполяризация приводит к существенному выходу из мышц К+ и входу Na+, СГ и Са2+. У больных с обширными повреждениями тканей при этом возможна опасная для жизни гиперкалиемия. Подробнее мы рассмотрим ее ниже; здесь же необходимо подчеркнуть, что при целом ряде состояний суксаметония хлорид противопоказан или должен применяться с большой осторожностью. Вторая фаза нервно-мышечной блокады, возникающая при длительной инфузии суксаметония хлорида, еще более осложняет его применение.
Действие на ЦНС. Тубокурарин и другие четвертичные соединения при в/в введении в обычныхдозах почти не влияют на ЦНС, так как не проникают через гематоэнцефалический барьер.
Решающий опыт, позволяющий ответить на вопрос о центральных влияниях кураре в терапевтических дозах, поставил сам на себе с помощью своих коллег врач-анестезиолог Смит (Smith et al., 1947). После интубации трахеи ему в/в ввели тубокурарин в дозе, в 2,5 раз превышающей необходимую для полного паралича всех мышц; дыхание поддерживалось с помощью ИВЛ. За все время эксперимента не было никаких признаков угнетения или спутанности сознания, анестезии или нарушения каких-либо видов чувствительности; Несмотря на адекватную ИВЛ, было чувство нехватки воздуха; кроме того, из-за накапливающейся в носоглотке слизи (глотание было невозможно) возникало ощущение удушья. В целом можно сказать, что впечатление было не из приятных. Авторы пришли к выводу,что тубокурарин, будучи введенным в/в даже в высоких дозах, не оказывает на ЦНС возбуждающего, угнетающего или анестезирующего действия и что единственным его эффектом служит паралич скелетных мышц.
Таблица 9.3. Характеристики первой и второй фаз действия суксаметония хлорида
|
Первая фаза |
Вторая фаза | |
|
Потенциал постсинаптической мембраны |
Деполяризация до —55 мВ |
Реполяризация до —80 мВ |
|
Начало |
Быстрое развитие сразу после введения |
Постепенное развитие |
|
Зависимость от дозы |
Не выражена |
Обычно развивается на фоне высоких доз или длительного действия |
|
Восстановление |
Быстрое |
Замедленное |
|
Разряд из 4 импульсов или тетанизирующее раздражение двигательного нерва |
Утомления нет |
Утомление” |
|
Механическая активность мышц |
Фасцикуляции, затем вялый паралич |
Вялый паралич |
Действие на вегетативные ганглии и М-холинорецепторы[править | править код]
Многие недеполяризующие миорелаксанты в той или иной степени оказывают ганглиоблокирующее действие. Как и в случае нервно-мышечной передачи, это действие предупреждается или устраняется ингибиторами АХЭ.
Тубокурарин в обычных дозах вызывает, очевидно, частичную блокаду передачи возбуждения на постганглио-нарные вегетативные нейроны и клетки мозгового вещества надпочечников. Это приводит к падению АД и тахикардии. Панкуроний и диметилтубокурарин в обычных дозах в меньшей степени оказывают этот эффект, а у ат-ракурия, векурония, доксакурия, пипекурония, мивакурия и рокурония он выражен совсем незначительно (Pollard, 1994; Savarese et al., 2000). Во время общей анестезии важна сохранность гемодинамических рефлексов. Панкуроний же оказывает ваголитическое действие (видимо, вследствие блокады М-холинорецепторов), проявляющееся тахикардией.
Деполяризующий миорелаксант суксаметония хлорид в обычных дозах редко вызывает эффекты, обусловленные ганглиоблокирующим действием. В то же время при его применении иногда наблюдаются гемодинамичес реакции, связанные, по-видимому, с возбуждением сначала парасимпатических (брадикардия), а затем симпатических (повышение АД и тахикардия) постганглионарных нейронов.
Высвобождение гистамина[править | править код]
У человека при внутрикожном или внутриартериальном введении тубокурарин вызывает типичные для действия гистамина волдыри. Некоторые другие побочные эффекты тубокурарина (бронхоспазм, снижение АД, повышение секреции трахее бронхиальных и слюнных желез) также объясняются высвобождением гистамина. Диметилтубокурарин, суксаметония хлорид, мивакурий, доксакурий и атракурий и. же вызывают высвобождение гистамина, хотя и менее выраженное и проявляющееся в основном при быстром введении этих препаратов. У аммониевых стероидов панкурония, векурония, пипекурония и рокурония этот эффект еще менее выражен (Basta, 1992; Watkins, 1994).Высвобождение гистамина обусловлено прямым влияний миорелаксантов на тучные клетки, а не анафилактической реакцией, опосредованной IgE (Watkins, 1994).
Гиперкалиемия[править | править код]
Как уже говорилось, деполяризующие миорелаксанты могут вызывать быстрый выход К+ из мышц. Возможно, именно этим объясняется длительная остановка дыхания, наблюдающаяся у больных с электролитными нарушениями после применения данных препаратов (Dripps, 1976). Вызванная суксаметония хлоридом гиперкалиемия — это угрожающее жизни состояние. Особенно опасна она для больных с сердечной недостаточностью, принимающих диуретики или сердечные гликозиды, при обширных повреждениях тканей или ожогах и т. п. В таких случаях часто приходится добавлять недеполяризующие миорелаксанты в достаточно высоких дозах. Суксаметония хлорид противопоказан или требует особо осторожного применения и при нетравматическом рабдомиолизе, травмах глаз, повреждениях спинного мозга с пара- или тетраплегией, миопатиях. Детям до 9 лет его теперь также не назначают (если только нет необходимости в срочной интубации трахеи), так как описаны случаи гиперкалиемии, рабдомиолиза и остановки кровообращения. Часто эти осложнения возникают на фоне скрытой дистрофии (Savarese et al., 2000). Возможно, у новорожденных повышена чувствительность и к недеполяризующим миорелаксантам.
Лекарственные взаимодействия[править | править код]
Выше мы рассмотрели взаимодействия между недеполяризующими и деполяризующими миорелаксантами. С клинической точки зрения наиболее важны также взаимодействия между этими препаратами и средствами для общей анестезии, некоторыми антибиотиками, антагонистами кальция и ингибиторами АХЭ.
Поскольку ингибиторы АХЭ препятствуют разрушению ацетилхолина, а те из них, которые относятся к четвертичным аммониевым основаниям (неостигмин, пиридостигмин и эдрофоний), оказывают также прямое N-холиностимулирующее действие (гл. 8), их применяют при передозировке недеполяризующих миорелаксантов. Иногда неостигмин и эдрофоний используют для декураризации — быстрого прекращения действия недеполяризующих миорелаксантов по окончании общей анестезии. После декураризации нельзя назначать суксаметония хлорид — это может привести к выраженной и длительной блокаде нервно-мышечного проведения. Иногда одновременно с ингибиторами АХЭ применяют М-холиноблокаторы (атропин или гликопиррония бромид); при этом стремятся избежать чрезмерной стимуляции М-холинорецепторов и прежде всего — брадикардии. Напротив, в отношении деполяризующих миорелаксантов ингибиторы АХЭ действуют как синергисты, усугубляя блокаду нервно-мышечного проведения (особенно в начальной фазе миорелаксации). Это пример того, насколько важны отличия между обоими типами миорелаксантов.
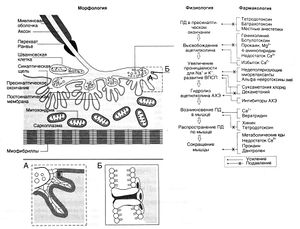
Описание к рис. 9.3. Точки приложения веществ, действующих на нервы, мышцы и нервно-мышечные синапсы. Слева — схема строения нервно-мышечного синапса, в центре — этапы синаптической передачи (подробнее см. гл. 6), справа — точки приложения различных веществ. На врезках приведены отдельные участки нервно-мышечного синапса в увеличенном виде; при самом большом увеличении (врезка Б) виден погруженный в мембрану N-холинорецептор. Его подробное строение приведено на рис. 9.1. ПД-по-тенциал действия. Многие ингаляционные анестетики (галотан, изофлуран, энфлуран) оказывают стабилизирующий эффект на постсинаптическую мембрану, действуя тем самым как синергисты недеполяризующих миорелаксантов. Следовательно, при совместном использовании таких анестетиков и недеполяризующих миорелаксантов доза последних должна быть снижена (Fogdall and Miller, 1975).
Аминогликозиды вызывают блокаду нервно-мышечного проведения за счет подавления высвобождения ацетилхолина из пресинаптических окончаний (вследствие подавления входа кальция) и в меньшей степени — за счет неконкурентного связывания с N-холинорецепторами. Эта блокада устраняется солями кальция; ингибиторы АХЭ при ней менее эффективны. Тетрациклины также могут вызвать блокаду нервно-мышечного проведения, предположительно — за счет образования комплексных соединений с Са2+. К ухудшению нервно-мышечного проведения приводят и некоторые другие антибиотики, например полимиксин В, колистин, клиндамицин и линкомицин (Pollard, 1994); они могут действовать и на пресинаптическом, и на постсинаптическом уровне. Антагонисты кальция усугубляют блокаду, вызванную как недеполяризующими, так и деполяризующими миорелаксантами. Пока не ясно, обусловлен ли этот эффект снижением кальцийзависимого высвобождения ацетилхолина из пресинаптического окончания или влияниями на постсинаптические процессы. У больных, получающих эти препараты, необходима коррекция дозы миорелаксантов. Если же самопроизвольное дыхание вовремя не восстанавливается, могут быть эффективными соли кальция.
Выраженные взаимодействия с деполяризующими и недеполяризующими миорелаксантами характерны также для триметафана камсилата, наркотических анальгетиков, прокаина, лидокаина, хинидина, фенелзина, фенитоина, пропранолола, солей магния, глюкокортикоидов, сердечных гликозидов, хлорохина, катехоламинов и диуретиков (Zaimis, 1976; Pollard, 1994; Savarese et al., 2000).
Побочные эффекты[править | править код]
Основные побочные эффекты миорелаксантов — это продленное апноэ (необычно длительное угнетение дыхания), сердечно-сосудистая недостаточность и реакции, связанные с высвобождением ацетилхолина.
Продленное апноэ. Нарушения в восстановлении нормального дыхания в послеоперационном периоде не всегда связаны с миорелаксантами. Их причиной может быть обструкция дыхательных путей, снижение РаС02 вследствие гипервентиляции при ИВЛ, передозировка неостигмина при декураризации. К факторам риска продленного апноэ относятся: 1) нарушения температуры тела, 2) электролитные нарушения (особенно К+, см. выше), 3) низкая активность псевдохолинэстеразы (при этом снижается скорость элиминации суксаметония хлорида), 4) невыявленная миастения либо злокачественное новообразование (например, мелкоклеточный рак легкого, сопровождающийся паранеопластическим синдромом Итона—Ламберта), 5) снижение мышечного кровотока (миорелаксанты медленнее вымываются из мышц), 6) почечная недостаточность (замедление экскреции миорелаксантов). Обезвоженным или тяжелым больным миорелаксанты назначают крайне осторожно.
Злокачественная гипертермия. Это опасное для жизни состояние, вызываемое некоторыми средствами для общей анестезии и миорелаксантами. Для него характерна резко выраженная мышечная ригидность, а следовательно, и увеличенный метаболизм в мышцах. В результате, с одной стороны, повышается теплопродукция в мышцах и возникает гипертермия, с другой — развивается метаболический ацидоз. Причиной является нерегулируемый выброс Са2+ из саркоплазматического ретикулума. Есть данные, что злокачественную гипертермию могут вызывать суксаметония хлорид и фторзамещенные углеводороды (галотан, изофлуран, севофлуран), применяемые по отдельности, но все же чаще всего это осложнение возникает при сочетании средств для общей анестезии и деполяризующих миорелаксантов. Существует аутосомно-доминантная предрасположенность к злокачественной гипертермии. Она может сочетаться с врожденными миопатиями (болезнью центрального стержня), однако в большинстве случаев она протекает бессимптомно вплоть до первой операции под общей анестезией.
Предрасположенность к злокачественной гипертермии выявляют с помощью контрактурной пробы in vivo. Для этого свежий биоптат скелетной мышцы подвергают действию различных концентраций галотана и кофеина и измеряют силу развивающейся контрактуры. Более чем в 50% семей с положительной контрактурной пробой обнаруживают мутации гена Ryr-1, кодирующего кальциевый канал саркоплазматического ретикулума («рианодиновый рецептор» Ryr-1). Описано более 20 мутаций в той части этого гена, которая отвечает за внутриклеточный домен канала. Обнаружены также мутации гена медленного кальциевого канала L-типа и других связанных с кальциевыми каналами белков. К сожалению, из-за больших размеров гена Ryr-1 и генетической гетерогенности предрасположенности к злокачественной гипертермии диагностировать это состояние путем генотипирования нельзя (Hopkins, 2000; Jurkat-Rott et al., 2000).
Основой лечения злокачественной гипертермии служит в/в введение дантролена. Этот препарат блокирует выход Са2+ из саркоплазматического ретикулума, препятствуя активации кальциевых каналов саркоплазматического ретикулума под действием Са2+ и кальмодулина (Fruen et al., 1997). Эти каналы тесно связаны с потенциалзависимыми кальциевыми каналами L-типа в области так называемых триад — структур, образованных Т-трубочками и цистернами саркоплазматического ретикулума. Каналы L-типа, расположенные в Т-трубочках, играют роль датчиков потенциала. Кальциевые каналы саркоплазматического ретикулума, каналы L-типа и еще несколько белков, расположенных в Т-трубочках, сарко-плазматическом ретикулуме и окружающей саркоплазме, регулируют высвобождение и действие Са2+ (Lehmann-Horn and Jurkat-Rott, 1999).
Кроме того, при злокачественной гипертермии проводят меры по охлаждению тела и борьбе с ацидозом, назначают ингаляции 100% кислорода. Благодаря настороженности анестезиологов и применению дантролена смертность от этого осложнения снижается.
При болезни центрального стержня (ее название обусловлено тем, что при биопсии мышц в центре красных мышечных волокон выявляются очаги в виде стержней) уже у новорожденных выявляется мышечная слабость и задержка двигательного развития. У таких больных высока вероятность развития злокачественной гипертермии при общей анестезии с использованием деполяризующих миорелаксантов. Заболевание вызывается мутациями гена Ryr-1, причем пять из этих мутаций связаны с предрасположенностью к злокачественной гипертермии. Некоторые другие миопатии и дистонии также сочетаются с повышенным риском мышечных контрактур и гипертермии при общей анестезии. Кроме того, у предрасположенных лиц суксаметония хлорид вызывает ригидность жевательных мышц, затрудняющую интубацию трахеи и другие меры по поддержанию проходимости дыхательных путей. Эго состояние связывают с мутацией гена, кодирующего а-субъединицу быстрого натриевого канала (Vita et al., 1995). Ригидность жевательных мышц может быть первым признаком того, что при продолжении данного режима анестезии и миорелаксации может наступить злокачественная гипертермия (Hopkins, 2000).
Паралич дыхательных мышц. При параличе дыхательных мышц, вызванном передозировкой миорелаксантов или усиленной реакцией на них, проводят ИВЛ с повышенной F102 и принимают меры, направленные на поддержание проходимости дыхательных путей, вплоть до восстановления нормального дыхания. Если применялись недеполяризующие миорелаксанты, то это восстановление можно ускорить введением неостигмина метилсульфата, 0,5—2 мг в/в, или эдрофония, 10 мг в/в (Watkins1994).
Борьба с другими побочными эффектами. Неостигмин устраняет только блокаду нервно-мышечного проведения, вызванную недеполяризующими миорелаксантами При этом он может усилить такие их побочные эффекты как артериальная гипотония, и вызвать бронхоспазм В таких случаях назначают симпатомиметики. Для устранения мускариноподобного действия миорелаксантов вводят атропин или гликопиррония бромид. Реакции, обусловленные высвобождением гистамина, эффективно устраняются Н1-блокаторами, особенно если их вводить перед миорелаксантами.
Фармакокинетика[править | править код]
Миорелаксанты — четвертичные аммониевые основания, они очень плохо всасываются из ЖКТ. Это было известно уже южноамериканским индейцам — они безбоязненно поедали мясо животных убитых отравленными кураре стрелами. Биодоступность таких миорелаксантов при в/м введении высокая. При в/в введении действие их наступает быстро. При этом надо помнить, что, поскольку препараты с высокой активностью используют в низких концентрациях, они начинают действовать позднее, так как больше времени занимают процессы диффузии.
Блокада, вызванная недеполяризующими миорелаксантами длительного действия (тубокурарином, панкуронием), примерно через 30 мин после введения может уменьшаться из-за распределения этих препаратов в организме. После этого уровень их в плазме и степень блокады в течение длительного времени остаются постоянными. При введении последующих доз распределение не столь выражено и препараты могут накапливаться.
Аммониевые стероиды содержат эфирные группы, которые подвергаются гидролизу в печени. Обычно продукты гидролиза обладают некоторой остаточной активностью (примерно вдвое меньшей, чем исходное вещество) и поэтому вносят вклад в общую динамику действия миорелаксанта. Аммониевые стероиды средней продолжительности действия (векуроний, рокуроний, рапакуроний; табл. 9.1) быстрее метаболизируются печенью, чем панкуроний и пипекуроний. Миорелаксация при использовании таких препаратов наступает быстрее, и поэтому лучше несколько раз ввести средства средней продолжительности действия, чем один раз — миорелаксант длительного действия (Savarese et al., 2000).
Атракурий превращается в менее активные метаболиты как под действием эстераз плазмы, так и в результате спонтанной деградации. Благодаря этому его Т,^ не изменяется при почечной недостаточности, и именно его лучше использовать у таких больных (Hunter, 1994). Мивакурий еще быстрее расщепляется псевдохолинэстеразой, и поэтому среди всех недеполяризующих миорелаксантов он обладает самым коротким действием.
Чрезвычайно короткое действие суксаметония хлорида также в значительной степени обусловлено его гидролизом псевдохолинэстеразой. Продленное апноэ при использовании суксаметония хлорида и мивакурия в большинстве случаев обусловлено дефектом или дефицитом этого фермента — наследственным (Pantuck, 1993; Primo-Parmo et al., 1996) или возникшим на фоне заболеваний печени или почек либо нарушений питания. Впрочем, в некоторых случаях активность псевдохолинэстеразы в плазме у таких больных нормальная (Whittaker, 1986).
Применение[править | править код]
Миорелаксация при хирургических вмешательствах. Миорелаксанты применяются в основном во время больших операций для того, чтобы добиться расслабления мышц (прежде всего живота) и тем самым облегчить хирургические манипуляции. Поскольку при этом степень расслабления мышц уже не зависит от глубины общей анестезии, последняя может быть значительно более поверхностной. Тем самым снижается риск угнетения дыхания и гемодинамических рефлексов и укорачивается восстановительный период. В то же время нельзя, ориентируясь на миорелаксацию, давать больному чрезмерно поверхностную анестезию — иначе возможны болевые рефлексы и вообще сохранность сознательного восприятия боли. Миорелаксанты используют также в травматологии и ортопедии, например при вправлении вывихов и переломов. Препараты короткого действия в сочетании со средствами для общей анестезии часто облегчают интубацию трахеи, ларингоскопию, бронхоскопию и эзофагоскопию.
Миорелаксанты вводят парентерально, почти всегда в/в. В связи с риском тяжелых осложнений их должны применять только анестезиологи или врачи, имеющие соответствующий опыт; под рукой должно быть все необходимое для реанимационных мероприятий. Подробнее о дозировке миорелаксантов и контроле за миоре-лаксацией можно прочитать в пособиях по анестезиологии (Pollard, 1994; Savarese et al., 2000).
Оценка типа и степени нервно-мышечной блокады. Это исследование проводят путем раздражения локтевого нерва и регистрации электромиограммы либо напряжения мышцы, приводящей большой палец. Наиболее важны реакции на повторные либо тетанизирующие стимулы, так как для оценки силы одиночных сокращений необходимо сравнивать ее с контрольными (до введения миорелаксантов) значениями. Чаще всего используют такие режимы стимуляции, как разряд из 4 импульсов, два последовательных разряда и тетанизирующее раздражение (Waud and Waud, 1972; Drenck et al., 1989). Необходимо учитывать, что чувствительность к миорелаксантам и скорость развития и окончания блокады у исследуемой мышцы и других мышц—особенно гортани, живота и диафрагмы — различны. В мышцах челюстей и гортани блокада возникает и заканчивается раньше, чем в мышце, приводящей большой палец, поэтому интубацию трахеи можно проводить до развития полной блокады при раздражении локтевого нерва. Первыми же восстанавливаются сокращения диафрагмы, и поэтому в тот момент, когда начинает проходить блокада при раздражении локтевого нерва, функция дыхательных мышц должна быть вполне достаточной, и можно проводить экстубацию (Savarese et al., 2000).
Электросудорожная терапия. Этот метод лечения, применяемый в психиатрии, несет риск травм — во время судорог возможны даже вывихи и переломы. Поскольку сами по себе судороги не необходимы для терапевтического эффекта, при электросудорожной терапии применяют миорелаксанты в комбинации с тиопенталом. Это сочетание, особенно на фоне постиктального торможения, обычно вызывает временное угнетение дыхания или даже апноэ, поэтому всегда должно быть под рукой все необходимое для интубации трахеи, ИВЛ и ингаляции кислорода. Сразу после припадка и расслабления мышц челюсти вводят ротовой воздуховод и принимают меры по предотвращению аспирации слизи и слюны. В качестве миорелаксантов чаше всего используют суксаметония хлорид и мивакурий в связи с их коротким действием. На одну из конечностей больного накладывают манжету с тем, чтобы миорелаксант в нее с кровью не попадал; по сокращениям мышц этой конечности судят об эффективности разряда.
Некоторые другие препараты, применяемые при спастических состояниях. Для повышения функциональных возможностей и устранения неприятных ощущений при спастичности, связанной с центральным параличом, пытались с переменным успехом применять ряд препаратов. Те из них, которые действуют на уровне ЦНС (баклофен, бензодиазепины, тизанидин). К средствам периферического действия относятся ботулотоксин А и дантролен.
Анаэробная бактерия Clostridium botulinum вырабатывает целый ряд токсинов (ботулотоксинов), связывающихся с белками пресинаптических окончаний и блокирующих высвобождение ацетилхолина. Один из этих токсинов — ботулотоксин А — применяется в качестве лекарственного средства. Он вызывает вялый паралич скелетных мышц и снижение выделения ацетилхолина парасимпатическими и симпатическими холинергическими окончаниями. Его действие длится 3—4 мес, а восстановление обусловлено прорастанием новых нервных окончаний. При повторных введениях ботулотоксина А возможно развитие устойчивости, обусловленной выработкой антител (Davies and Bames, 2000).
Сначала ботулотоксин А применялся только при косоглазии, блефароспазме и лицевом гемиспазме, но затем его стали использовать и при многих других спастических состояниях и дистониях — спастической дисфонии, оромандибулярной дистонии, спастической кривошее, спазмах нижнего пищеводного сфинктера и трещинах заднего прохода. Его применяют также в дерматологии для устранения чрезмерной потливости ладоней и подмышечных впадин, не поддающейся лечению местными средствами и электрофорезом, а также в косметологии для сглаживания морщин на лице. В таких случаях ботулотоксин А вводят местно в мышцы или кожу (Boni et al., 2000).
Дантролен пытаются применять не только при злокачественной гипертермии (см. выше), но и при спастичности и гиперрефлексии. Этот препарат вызывает общую мышечную слабость, и поэтому он показан только больным с резко выраженной спастичностью, не способным к самостоятельному передвижению. Дантролен может оказывать гепатотоксическое действие; при постоянном его приеме необходимо периодически проверять биохимические показатели функции печени (Kita and Goodkin, 2000).