Агонисты опиатных рецепторов
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Агонисты-антагонисты и частичные агонисты опиатных рецепторов[править | править код]
Препараты этой группы отличаются от других наркотических анальгетиков. Нальбуфин и буторфанол блокируют μ-рецепторы, а их обезболивающее действие обусловлено стимуляцией к-рецепторов. Пентазоцин близок к ним, однако его блокирующее действие на μ-рецепторы гораздо слабее, и он может быть даже их частичным агонистом. Бупренорфин является только частичным агонистом μ-рецепторов. Эти препараты созданы в надежде получить обезболивающие средства, в меньшей степени угнетающие дыхание и вызывающие зависимость, чем классические наркотические анальгетики. В настоящее время их применение ограничено из-за побочных действий и небольшой обезболивающей активности.
Пентазоцин[править | править код]
Этот препарат является стимулятором к-рецепторов и слабым блокатором μ-рецепторов. Он синтезирован в поиске мощных анальгетиков, не вызывающих зависимости.
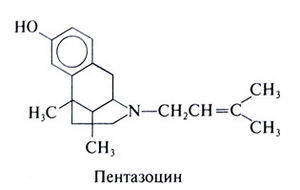
Химические свойства. Пентазоцин — производное бензоморфа-на. Его структурная формула следующая:
Пентазоцин содержит крупный боковой радикал у атома азота, гомологичного N-17 морфина. Этот фрагмент имеют многие блокаторы и агонисты-антагонисты опиатных рецепторов. Обезболивающее действие и угнетение дыхания оказывает в основном /-изомер пентазоцина.
Фармакодинамика. По действию на ЦНС пентазоцин напоминает морфин и другие стимуляторы μ-рецепторов, вызывая обезболивание, заторможенность и угнетение дыхания. Обезболивающее действие связано со стимуляцией к-рецепторов. Высокие дозы пентазоцина (60—90 мг) вызывают дисфорию и психотомиметический эффект. Их механизм не ясен, очевидно, имеет значение активация к-рецепторов головного мозга, поскольку эти симптомы могут устраняться налоксоном.
По действию на сердечно-сосудистую систему пентазоцин отличается от стимуляторов μ-рецепторов, в высоких дозах повышая АД и ЧСС. При ИБС в/в введение пентазоцина увеличивает среднее давление в аорте, конечно-диастолическое давление в левом желудочке, среднее давление в легочной артерии и работу сердца (Alderman etal., 1972; Lee etal., 1976). Эти явления могут быть связаны с повышением сывороточной концентрации катехоламинов.
На μ-рецепторы пентазоцин действует как слабый блокатор или частичный агонист. В низких дозах (20 мг парентерально) он угнетает дыхание так же, как 10 мг морфина, но повышение дозы не ведет к пропорциональному усилению этого эффекта. Пентазоцин не уменьшает угнетение дыхания, вызванное морфином. В то же время при физической зависимости от морфина и других стимуляторов μ-рецепторов пентазоцин может вызвать абстинентный синдром; даже в отсутствие его явных проявлений обезболивающий эффект этих препаратов ослабляется. Увеличение дозы выше 50—100 мг не сопровождается усилением обезболивающего действия и угнетения дыхания (Bailey and Stanley, 1994).
Фармакокинетика. Пентазоцин хорошо всасывается из ЖКТ и при п/к или в/м введении. Обезболивающий эффект достигает пика через 15—60 мин после в/м введения и через 1—3 ч после приема внутрь. Т1/2 пентазоцина составляет 4—5 ч. Значительная часть препарата метаболизируется при первом прохождении через печень, поэтому его биодоступность при приеме внутрь не превышает 20%. Пентазоцин инактивируется в печени и выводится почками.
Побочные эффекты. Самые частые из них — заторможенность, потливость и дурнота; бывает также тошнота, но рвота возникает реже, чем на фоне морфина. Дозы выше 60 мг (при парентеральном введении) оказывают психотомиметическое действие, включая навязчивые причудливые мысли, тревожность, кошмары и галлюцинации. Передозировка одного пентазоцина редко бывает смертельной. Высокие дозы вызывают сильное угнетение дыхания (этот эффект устраняется налоксоном) в сочетании с артериальной гипертонией и тахикардией. П/к и в/м введение пентазоцина болезненно, многократные инъекции в течение длительного времени могут вызвать выраженный фиброз подкожной клетчатки и мышц. У больных, регулярно получавших наркотические анальгетики, введение пентазоцина может спровоцировать абстинентный синдром. Избежать этого обычно позволяет переход на пентазоцин через 1—2 дня после отмены этих препаратов.
Толерантность и физическая зависимость. Регулярное лечение пентазоцином вызывает толерантность к его обезболивающему действию и субъективным эффектам. Однако пентазоцин не предотвращает и не ослабляет абстинентный синдром при отмене морфина — более того, при назначении в высоких дозах больным с зависимостью от морфина он сам вызывает абстинентный синдром за счет блокады μ-рецепторов.
У бывших наркоманов длительное лечение пентазоцином (60 мг каждые 4 ч) вызывает физическую зависимость и внезапная отмена препарата или введение налоксона вызывает абстинентный синдром. После суточных доз более 500 мг этот синдром включает спастическую боль в животе, тревожность, озноб, подъем температуры, рвоту, слезотечение и потливость, хотя симптомы выражены слабее, чем после отмены морфина. Избежать этих явлений помогает постепенная отмена пентазоцина или его замена на стимуляторы μ-рецепторов (морфин или метадон). Абстинентный синдром после отмены пентазоцина описан и у новорожденных.
Применение. Пентазоцин используют как анальгетик; хотя он также способен вызвать зависимость, ее риск ниже, чем при лечении морфином и другими стимуляторами μ-рецепторов. По-видимому, при приеме внутрь вероятность злоупотребления препаратом ниже, поэтому пентазоцин стараются назначать внутрь.
Пентазоцина лактат выпускается в виде раствора для инъекций. Таблетки пентазоцина содержат 50 мг пентазоцина и 0,5 мг налоксона (в виде гидрохлоридов), чтобы предотвратить использование этих таблеток инъекционными наркоманами: при приеме внутрь налоксон быстро разрушается в печени, однако при инъекции растворенных таблеток налоксон вызывает абстинентный синдром. Применяются также таблетки пентазоцина с аспирином или парацетамолом. По обезболивающему действию при парентеральном введении 30—60 мг пентазоцина соответствуют 10 мг морфина, при приеме внутрь 50 мг пентазоцина эквивалентны 60 мг кодеина.
Нальбуфин[править | править код]
Нальбуфин по строению близок к налоксону и оксиморфону (табл. 23.5). Это агонист-антагонист опиатных рецепторов, по действию напоминающий пентазоцин; однако нальбуфин в большей степени блокирует μ-рецепторы и реже вызывает дисфорию.
Фармакодинамика и побочные эффекты. 10 мг нальбуфина в/м соответствуют 10 мг морфина по скорости развития, силе и длительности обезболивающего действия и субъективным ощущениям. В эквивалентных дозах нальбуфин угнетает дыхание так же, как и морфин, но его эффект достигает максимума при дозе 30 мг, и дальнейшее ее увеличение не усиливает ни угнетение дыхания, ни обезболивание. В отличие от пентазоцина и буторфанола, нальбуфин в дозе 10 мг существенно не влияет на АД, давление в легочной артерии, сердечный индекс и работу сердца у больных ИБС, в том числе при инфаркте миокарда (Roth et al., 1988). По действию на ЖКТ нальбуфин, видимо, соответствует пентазоцину. В дозе 10 мг и ниже он достаточно хорошо переносится, чаще всего наблюдаются заторможенность, потливость и головная боль. Высокие дозы (70 мг) могут оказывать психотомиметическое действие, включая дисфорию, скачку мыслей и искаженное восприятие своего тела. Нальбуфин метаболизируется в печени, его Т1/2 составляет 2—3 ч. При приеме внутрь активность препарата снижается в 4—5 раз по сравнению с в/м введением.
Толерантность и физическая зависимость. У больных, регулярно получающих низкие дозы морфина (60 мг/сут внутрь), нальбуфин вызывает абстинентный синдром. Длительное лечение нальбуфином приводит к физической зависимости с риском абстинентного синдрома, по тяжести соответствующего таковому при отмене пентазоцина. Вероятность злоупотребления нальбуфином в отсутствие опиатной зависимости примерно такая же, как в случае пентазоцина.
Применение. Нальбуфин (в виде гидрохлорида) используют в качестве анальгетика. Поскольку он является агонистом-антагонистом опиатных рецепторов, его можно назначать лишь через некоторое время после морфина и других стимуляторов μ-рецепторов, чтобы не вызвать абстинентный синдром. Обычная доза у взрослых — 10 мг парентерально каждые 3—6 ч, в отсутствие толерантности ее можно повысить до 20 мг.
Буторфанол[править | править код]
Буторфанол (табл. 23.5) — это производное морфинана, по характеру действия напоминающее пентазоцин.
Фармакодинамика и побочные эффекты. В послеоперационном периоде буторфанол в дозе 2—3 мг парентерально вызывает обезболивание и угнетает дыхание примерно в той же степени, что и 10 мг морфина или 80—100 мг петидина; по скорости развития, силе и длительности этих эффектов буторфанол соответствует морфину. Т1/2 буторфанола составляет около 3 ч. Подобно пентазоцину, он увеличивает давление в легочной артерии и работу сердца, но несколько снижает АД (Popio et al., 1978).
Основные побочные эффекты включают сонливость, слабость, потливость, головокружение и тошноту. Риск психотомиметического действия ниже, чем на фоне эквивалентных доз пентазоцина, но проявляется оно так же. Возможна физическая зависимость от буторфанола.
Применение. Буторфанол (в виде тартрата) лучше использовать при острой, а не хронической боли. Из-за побочного действия на миокард препарат хуже подходит при сердечной недостаточности и инфаркте миокарда, чем морфин и петидин. Обычная доза составляет 1—4 мг в/м или 0,5—2 мгв/в каждые 4 ч. Применяется также аэрозоль для ингаляций в нос, особенно полезен он бывает при сильной головной боли, устойчивой к другим методам лечения.
Бупренорфин[править | править код]
Бупренорфин (табл. 23.5) — высоко липофильное полусинтетическое производное тебаина, по активности превосходящее морфин в 25—50 раз.
Фармакодинамика и побочные эффекты. По обезболивающему действию и другим центральным эффектам бупренорфин близок к морфину. Примерно 0,4 мг бупренорфина соответствуют 10 мг морфина при в/м введении (Wallenstein et al., 1986). Длительность действия выше, чем у морфина, хотя этот показатель непостоянен. Некоторые эффекты бупренорфина развиваются значительно медленнее и длятся дольше, чем соответствующие эффекты морфина: так, миоз достигает максимума через 6 ч после в/м введения, максимальное угнетение дыхания — примерно через 3 ч.
Бупренорфин — частичный агонист μ-рецепторов. В высоких дозах он вызывает абстинентный синдром после длительного лечения стимуляторами μ-рецепторов. Он восстанавливает дыхание после анестезии фентанилом примерно так же, как налоксон, но при этом частично сохраняется обезболивание (Boysen et al., 1988). В клинических испытаниях бупренорфин мало влиял на дыхание, но не ясно, прекращает ли угнетение дыхания нарастать после определенной дозы (как в случае пентазоцина и нальбуфина). Налоксон предупреждает угнетение дыхания и другие эффекты бупренорфина, но если они уже развились, даже высокие дозы налоксона устраняют их не сразу, что говорит о прочном связывании бупренорфина с опиатными рецепторами. Действительно, Т1/2 комплекса μ-рецепторов с бупренорфином составляет 166 мин, а с фентанилом — 7 мин (Boas and Villiger, 1985). Поэтому сывороточная концентрация бупренорфина не отражает его эффект. По влиянию на сердечно-сосудистую систему и другим побочным эффектам (заторможенность, тошнота, рвота, дурнота, потливость, головная боль) бупренорфин напоминает морфин и другие стимуляторы μ-рецепторов.
Фармакокинетика. Бупренорфин хорошо всасывается при любом способе применения, в том числе при приеме под язык. Сывороточная концентрация достигает пика через 5 мин после в/м введения и через 1—2 ч после приема внутрь или под язык. Т1/2 составляет около 3 ч, но он слабо отражает длительность действия (см. выше). Около 96% препарата связывается с белками плазмы. С мочой выделяются продукты N-деалкилирования и конъюгации бупренорфина, но основная его часть выводится с калом в неизмененном виде.
Физическая зависимость. Через 2—14 сут после отмены бупренорфина развивается отсроченный абстинентный синдром, напоминающий таковой при отмене морфина (но обычно менее выраженный) и длящийся 1—2 нед (Bickel et al., 1988; Fudala et al., 1989).
Применение. Бупренорфин применяется для обезболивания и для поддерживающего лечения у опиоидных наркоманов (Johnson et al., 2000). Он получил предварительное одобрение для лечения героиновой зависимости после прохождения закона о лечении наркомании через Конгресс США и его подписания президентом в октябре 2000 г.; ожидается одобрение ФДА.
В качестве анальгетика бупренорфин вводят в/м или в/в по 0,3 мг каждые 6 ч; хороший эффект обеспечивает прием 0,4— 0,8 мг под язык (например, для обезболивания в послеоперационном периоде). При поддерживающем лечении опиоидной зависимости 6—8 мг бупренорфина эквивалентны 60 мг метадона.
Другие препараты[править | править код]
Мептазинол — агонист-антагонист опиатных рецепторов. По обезболивающей активности морфин превосходит его примерно в 10 раз и действует несколько дольше. Мептазинол выступает и как М-холиностимулятор, что может вносить вклад в его обезболивающий эффект (Holmes and Ward, 1985). Впрочем, последний устраняется налоксоном. Мептазинол ведет к абстинентному синдрому у животных, получающих стимуляторы μ-рецепторов. Вероятность злоупотребления меньше, чем в случае морфина, так как в высоких дозах мептазинол часто вызывает дисфорию. Дезоцин, производное аминотетралина, — это также агонист-антагонист опиатных рецепторов. По силе и длительности обезболивающего действия он соответствует морфину. После 30 мг увеличение дозы дезоцина не приводит к дальнейшему угнетению дыхания. У бывших наркоманов он вызывает примерно такой же субъективный эффект, как и стимуляторы μ-рецепторов (Jasinski and Preston, 1985).