Бензодиазепины
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Бензодиазепины[править | править код]
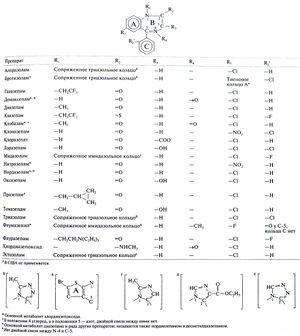
Основные эффекты всех бензодиазепинов одинаковы. В то же время выраженность тех или иных эффектов и фармакокинетические свойства у разных бензодиазепинов различны, и это часто определяет выбор препарата. Есть основания полагать, что в седативный, снотворный, миорелаксирующий, анксиолитический и противосудорожный эффекты вносят различный вклад разные механизмы действия бензодиазепинов. По последним данным, отдельные эффекты этих препаратов связаны с действием на определенные субъединицы ГАМКА-рецепторов. Мы подробно остановимся лишь на бензодиазепинах, применяемых главным образом как снотворные, но опишем также общие свойства этой группы и важные различия между отдельными препаратами. Химические свойства. Формулы бензодиазепинов и ряда сходных веществ приведены в табл. 17.1. Термин бензодиазепин относится к бензольному кольцу (кольцо А), соединенному с семичленным диазепиновым кольцом (кольцо В). Поскольку все применяемые препараты этой группы содержат 1,4-диазепиновое кольцо В и ароматический заместитель (кольцо С) у С-5, бензодиазепинами в узком смысле слова называют 5-арил-1,4-бензодиазепины. Модификация бензодиазепинового ядра позволила получить вещества со сходной активностью: 1,5-бензодиазепины (клобазам) и продукты замены бензольного кольца А на гетероциклы, в частности натиофен (бротизолам). Заместители у N-1 и С-3 могут быть самыми разными; получены также бензодиазепины с триазольным или имидазольным кольцом, присоединенным к N-1 и С-2. Кетогруппа при С-5 вместо кольца С и метильная группа у N-4 — важные структурные особенности флумазенила, блокатора бензодиазепиновых рецепторов (Нае-fely, 1983).
Кроме указанных препаратов синтезировано большое количество веществ другой структуры, конкурирующих с бензодиазепинами и флумазенилом за участки связывания в ЦНС (Gardner et al., 1993). В молекулах этих соединений могут находиться конденсированные кольца индола и пиридина (β-карболины), а также имидазопиридиновые (золпидем), имидазопиримиди-новые, имидазохинолоновые и циклопирролоновые (зопиклон) структуры.
Фармакологические свойства[править | править код]
Почти все эффекты бензодиазепинов связаны с влиянием на ЦНС: в первую очередь это седативное, снотворное, противосудорожное, анксиолитическое, миорелаксирующее действие и антероградная амнезия. Лишь два эффекта, по-видимому, обусловлены действием на периферические ткани: расширение коронарных артерий (при в/в введении обычных доз некоторых бензодиазепинов) и блокада нервно-мышечного проведения (на фоне очень высоких доз).
По активности in vivo и in vitro выделяют полные агонисты (стимуляторы) бензодиазепиновых рецепторов (они оказывают выраженный эффект, занимая небольшое число рецепторов), например диазепам, и частичные агонисты (их максимальный эффект менее выражен или требует активации большего числа рецепторов). Некоторые вещества — обратные агонисты — в отсутствие стимуляторов оказывают действие, обратное таковому диазепама; описаны также частичные обратные агонисты Большинство эффектов агонистов и обратных агонистов устраняет или предотвращает флумазенил — блокатор бензодиазепиновых рецепторов, конкурирующий за них с бензодиазепинами. Сходным образом действуют и некоторые другие препараты.
ЦНС. Бензодиазепины влияют на активность всех отделов ЦНС, но одни затрагиваются в большей степени,чем другие. Эти препараты не способны вызвать такое глубокое угнетение ЦНС, как барбитураты и ингаляционные анестетики. Бензодиазепины очень близки по фармакологическим свойствам, но различаются по избирательности действия, что существенно влияет на показания к отдельным препаратам.
С увеличением дозы бензодиазепинов на смену седативному действию приходят сон и далее сопор. Нередко пишут об анестезирующем эффекте некоторых бензодиазепинов, но истинной общей анестезии не наступает, поскольку сознание обычно сохраняется и не достигается достаточного для операции расслабления мышц. Однако высокие дозы вызывают антероградную амнезию, что может создать иллюзию анестезии.
Новые данные о молекулярных основах разнообразия бензодиазепиновых рецепторов (см. ниже) привели к попыткам отделить анксиолитический эффект от седативного и снотворного. Однако эта задача оказалась непростой, так как количественно оценить тревожность и седативный эффект у человека сложно, а надежность экспериментальных моделей на животных не известна. Существование множества бензодиазепиновых рецепторов отчасти объясняет видовые различия в эффектах бензодиазепинов.
Модели тревожности у животных. В экспериментах на животных основное внимание уделяли способности бензодиазепинов повышать активность (подвижность, пищевое и питьевое поведение), подавляемую новыми или неприятными раздражителями. Для этого поведение животных, ранее вознаграждавшееся пищей или водой, периодически наказывалось ударом тока. Удар предварялся зрительным или звуковым сигналом, и животные, не получавшие бензодиазепинов, в ответ на этот сигнал почти полностью прекращали активность. Бензодиазепины устраняли различие в активности животных на фоне ударов тока и в их отсутствие, причем применяемые дозы, как правило, не влияли на активность в отсутствие ударов тока и не вызывали двигательных нарушений. В других моделях незнакомая обстановка резко снижала поисковую активность у крыс, и бензодиазепины устраняли этот эффект. Наркотические анальгетики и нейролептики не вызывают подобного растормаживания, а фенобарбитал и мепробамат делают это лишь вдозах, угнетающих спонтанную активность или ведущих к атаксии.
Различия между дозами бензодиазепинов, вызывающими двигательные нарушения и растормаживание, сильно зависят от препарата, вида животного и схемы опыта. Хотя эти различия могли способствовать продвижению на рынок некоторых бензодиазепинов в качестве избирательных транквилизаторов и снотворных средств, они не позволили предсказать седативную активность бензодиазепинов, нашедших применение в качестве анксиолитических препаратов.
Толерантность. Говоря о различии между растормаживанием и седативным и атаксическим действием бензодиазепинов, часто ссылаются на данные о толерантности у животных. Так, толерантность к угнетающему влиянию на спонтанную и вознаграждаемую активность наступает через несколько дней; растормаживающее же действие вначале нарастает, а ослабевает через 3-4 нед (File, 1985). У большинства людей, длительно принимающих бензодиазепины, сонливость исчезает в течение нескольких дней, но толерантность к ряду проявлений психомоторной заторможенности (например, при тесте реакции на движущийся объект) обычно не наблюдается. Толерантность к анксиолитическому действию остается спорной (Lader and File, 1987). Многие больные способны обходиться без существенного изменения дозы, и ее снижения и повышения, очевидно, отражают колебания эмоциональной нагрузки. Однако некоторые больные не снижают дозу по окончании стресса или постоянно наращивают ее, что, по-видимому, говорит о зависимости (Woods et al., 1987; DuPont, 1988).
Некоторые бензодиазепины снижают мышечный тонус, не влияя на двигательную активность, и могут ослаблять ригидность при центральных параличах. Однако у человека (в отличие от животных) их избирательность ограничена. Клоназепам оказывает миорелаксирующее действие в дозах, недостаточных для седативного эффекта, — в отличие от диазепама и большинства его аналогов. К миорелаксирующему и атаксическому действию бензодиазепинов развивается толерантность.
Бензодиазепины подавляют эпилептические припадки, вызванные пентетразолом и пикротоксином, но судороги, вызванные стрихнином и током высокого напряжения, предотвращаются лишь в дозах, резко нарушающих двигательную активность. У клоназепама, нитразепама и нордазепама противосудорожная активность более избирательна, чем у других препаратов. Бензодиазепины подавляют также фотогенные припадки у павианов и припадки при алкогольном абстинентном синдроме у людей. К сожалению, толерантность к противосудорожному действию ограничивает применение бензодиазепинов при эпилепсии (гл. 21).
Бензодиазепины оказывают обезболивающее действие у животных, но у человека отмечен лишь преходящий обезболивающий эффект при в/в введении этих препаратов, который в действительности может быть обусловлен амнезией. Несомненно, однако, что бензодиазепины, в отличие от барбитуратов, не вызывают гипералгезию.
Влияние на ЭЭГ и структуру сна. По действию на ЭЭГ в состоянии бодрствования бензодиазепины напоминают другие транквилизаторы и снотворные: снижается доля a-ритма, а доля быстрого низкоамплитудного ритма возрастает. К этим эффектам развивается толерантность.
Большинство бензодиазепинов ускоряют засыпание (особенно при первом использовании), уменьшают число и длительность пробуждений. Обычно сокращается I стадия (поверхностный сон), резко укорачиваются III и IV стадии (глубокий мед ленный сон). Большинство препаратов сокращают время от появления сонных веретен до начала быстрого сна (V стадии). Уменьшается и общая продолжительность быстрого сна, но возрастает число его периодов, главным образом под конец сна. Золпидем подавляет быстрый сон в меньшей мере, благодаря чему может иметь преимущество перед бензодиазепинами в качестве снотворного (Dujardin et al., 1998).
Несмотря на укорочение быстрого сна и IV стадии медленного сна, обычно бензодиазепины увеличивают общее время сна, главным образом за счет удлинения II стадии (основной составляющей медленного сна). Этот эффект тем выраженнее, чем короче был сон до назначения бензодиазепинов. Кроме того, несмотря на учащение периодов быстрого сна, снижаются частота переходов к I стадии, частота пробуждений и число движений во сне. Ночные пики концентрации СТГ, пролактина и ЛГ не меняются. При регулярном приеме бензодиазепинов на ночь их влияние на структуру сна обычно сглаживается через несколько дней. После отмены препарата возможен рикошетный эффект, особенно выраженным бывает увеличение доли и общей продолжительности быстрого сна. Впрочем, если доза была не слишком велика, больной отмечает лишь укорочение сна, но не усугубление бессонницы.
Хотя отмечены некоторые различия в действии бензодиазепинов на структуру сна, все они обычно приносят ощущение глубокого освежающего сна. Не ясно, влиянием на какой показатель структуры сна оно обусловлено. В результате преимущества отдельных препаратов в качестве снотворных определяются главным образом их фармакокинетикой, а не возможными различиями в фармакодинамике.
Механизм действия. Большинство эффектов бензодиазепинов связывают с действием на рецепторы тормозного медиатора ГАМК. Эти мембранные рецепторы подразделяют на два основных типа: ГАМКа и ГАМКв. ГАМКд-рецепторы — это хемочувствительные хлорные каналы, образованные пятью субъединицами, пронизывающими клеточную мембрану. Эти рецепторы опосредуют большую часть тормозных сигналов в ЦНС. ГАМ Кв-рецепторы сопряжены с G-белками; они состоят из единственного белка с семью трансмембранными доменами. Бензодиазепины действуют только на ГАМКд-рецепторы соединяясь с особым участком рецептора, отличным oт участка связывания ГАМК. В отличие от барбитуратов сами они не активируют рецептор и требуют присутствия ГАМК, то есть лишь модулируют ее действие. Бензодиазепины и аналоги ГАМК связываются с рецепторами в наномолярных концентрациях и действуют как аллостерические регуляторы связывания друг друга. Лиганды бензодиазепиновых рецепторов могут действовать как стимуляторы, обратные агонисты и блокаторы: первые увеличивают, а вторые уменьшают хлорный ток, возникающий в ответ на активацию ГАМКА-рецепторов. В первом случае кривая зависимости эффекта от концентрации ГАМК сдвигается влево, а во втором — вправо. Блокаторы бензодиазепиновых рецепторов устраняют оба этих эффекта, но в отсутствие стимулятора и обратного агониста не оказывают никакого эффекта. Одно из таких веществ, флумазенил, используется как антидот при передозировке бензодиазепинов. Кроме того, поведенческие и электрофизиологические эффекты бензодиазепинов могут быть ослаблены или устранены предварительным введением блокаторов ГАМКд-рецепторов (например, бикукуллина).
Данные, полученные при клонировании кДН К субъединиц ГАМКд-рецепторов, подтверждают прямое влияние бензодиазепинов на эти рецепторы (Schofield et al., 1987; Pritchett et al., 1989). При экспрессии in vitro ГАМКд-рецепторов, образованных из соответствующих субъединиц (см. ниже), выявляются участки связывания с высоким сродством к бензодиазепинами регистрируется хлорный ток, активируемый ГАМ К и усиливаемый бензодиазепинами. Такие рецепторы по свойствам близки к своим естественным аналогам в нейронах ЦНС. ГАМКд-рецептор включает 5 гомологичных субъединиц. На сегодня описано 16 вариантов субъединиц, объединенных в 7 семейств: 6 а-субъединиц, по 3 β- и у-субъединицы и по одной 5-, е-, и- и 0-субъединице. Кроме того, возможен альтернативный сплайсинг РНК некоторых из них (у2 и а6). Точный состав ГАМКд-рецепторов пока не известен, считается, что большинство из них включает а-, Щ и у-субъединицы, которые могут находиться в разных соотношениях. Разнообразие субъединиц ведет к неоднородности ГАМКд-рецепторов, что, по крайней мере отчасти, объясняет различия в фармакологических свойствах бензодиазепиновых рецепторов, выявляемые в поведенческих, биохимических и функциональных исследованиях. Изучение клонированных ГАМКд-рецепторов показало, что присоединение у-субъединицы к а- и β-субъединицам придает рецептору чувствительность к бензодиазепинам (Pritchett et al., 1989). Рецепторы из одних а- и р-субъединиц функционируют и реагируют на барбитураты, но не связывают бензодиазепины и не реагируют на них. Предполагается, что бензодиазепиновый рецептор лежит на стыке а- и р-субъединиц и обе они влияют на его свойства (McKeman et al., 1995). Так, рецепторы с а1-субъединицей отличаются по свойствам от рецепторов с а2-, а3- и аз-субъединицами (Pritchett and Seeburg, 1990), что согласуется с данными о неоднородности ГАМКд-рецепторов, полученными при изучении связывания меченых лигандов с мембранами нейронов. Рецепторы с а6-субъединицей обладают низким сродством к диазепаму, но избирательны в отношении обратного агониста RO-15-4513, который испытывался как антидот этанола (Liiddens et al., 1990). Тип у-субъединицы также влияет на свойства бензодиазепиновых рецепторов: у1-субъединица снижает сродство к бензодиазепинам (McKeman et al., 1995). Теоретически разные субъединицы могут образовывать сотни тысяч ГАМКА-рецепторов, но ввиду особенностей сборки число рецепторов ограничено (Sieghart et al., 1999).
Новые работы проливают свет на значение отдельных субъединиц ГАМКд-рецепторов для тех или иных эффектов бензодиазепинов in vivo. После замены в а1-субъединице Гис101 на аргинин диазепам утрачивает способность усиливать действие ГАМК на рецептор (Kleingoor et al., 1993). У мышей с такими субъединицами теряется седативное, амнестическое и отчасти противосудорожное действие диазепама, но сохраняются его анксиолитические, миорелаксирующие свойства и способность усиливать эффект этанола (Rudolph et al., 1999; McKeman et al.,2000). Аналогичная замена в а2-субъединице нарушает у мышей анксиолитическое действие диазепама (Low et al., 2000). Выявление связи поведенческих эффектов бензодиазепинов с теми или иными субъединицами поможет разработать препараты с меньшим числом побочных действий. Так, соединение L-838 417 усиливает действие ГАМК на рецепторы, состоящие из а2-, а3-или а5-субъединиц, но не влияет на рецепторы с а1-субъединицей; в результате оно оказывает анксиолитический эффект в отсутствие седативного (McKeman et al., 2000).
Субъединицы ГАМКд-рецепторов могут отвечать и за нормальную локализацию собранных рецепторов в синапсах. У мышей без у2-субъединицы эта локализация нарушалась, хотя происходила сборка рецепторов и их перенос на клеточную мембрану (Essrich etal., 1998). Распределение рецепторов регулирует также белок гефирин.
ГАМКрецепторы и эффекты бензодиазепинов. Высокая безопасность бензодиазепинов объясняется, по-видимому, зависимостью их эффектов от наличия ГАМК в синаптической щели: в ее отсутствие бензодиазепины не влияют на ГАМКд-рецепторы. Барбитураты в низких дозах также усиливают действие ГАМК, но в высоких напрямую активируют эти рецепторы, вызывая глубокое угнетение ЦНС (см. ниже). Растормаживающее и седативное действие бензодиазепинов может быть сопряжено с потенцирующим влиянием на ГАМКергические пути, регулирующие активность моноаминергических нейронов. Эй нейроны отвечают за общую активацию и служат важными посредниками тормозного действия страха и наказания на поведение. Миорелаксирующий и противосудорожный эффекты связывают с усилением тормозного влияния ГАМКергических нейронных контуров в различных отделах ЦНС. В большинстве исследований in vivo и in situ местное и системное введение бензодиазепинов снижало спонтанную и индуцированную электрическую активность главных (крупных) нейронов всех отделов головного и спинного мозга. Эту активность регулируют, в частности, мелкие тормозные вставочные нейроны, в основном ГАМКергические, путем прямого и возвратного торможения. Выраженность эффектов бензодиазепинов может колебаться в широких пределах в зависимости от типа тормозных нейронных контуров, источника и силы возбуждающего сигнала, а также условий эксперимента и методов оценки. Так, контуры возвратного торможения часто включают мощные тормозные синапсы на теле нейрона рядом с аксонным холмиком. Действуя на рецепторы в области этих синапсов, ГAM К (будь то выделившаяся из пресинаптических окончаний или искусственно апплицированная) повышает хлорную проницаемость; это вызывает шунтирование деполяризующих токов и затрудняет генерацию потенциала действия. Бензодиазепины существенно увеличивают период после короткой активации возвратных ГАМКергических волокон, в течение которого ни естественные, ни искусственные возбуждающие стимулы не могут вызвать потенциал действия; этот эффект устраняет блокатор ГАМКд-рецепторов бикукуллин.
В исследованиях in vitro показано, что бензодиазепины усиливают хлорный ток за счет повышения частоты вспышек открывания одиночных каналов под действием субмаксимальной концентрации ГАМК (Twyman et al., 1989). В терапевтических концентрациях они потенцируют постсинаптическое торможение, снижая тем самым реакцию на раздражение афферентных волокон. Наблюдается также удлинение спонтанных миниатюрных ТПСП. Барбитураты также усиливают хлорный ток, но за счет повышения времени пребывания одиночных каналов в открытом состоянии. Бензодиазепины смещают влево кривую зависимости эффекта (то есть хлорного тока) от концентрации
ГАМК, но не увеличивают максимальный ток. Вместе с данными работ in vivo это укладывается в гипотезу, согласно которой действие бензодиазепинов обусловлено потенцированием действия ГАМК на ГАМКд-рецепторы. Как говорилось выше, ряд экспериментальных бензодиазепинов и сходных веществ действуют как обратные агонисты бензодиазепиновых рецепторов: они уменьшают вызываемый ГАМК хлорный ток, приводя к эпилептическим припадкам и другим эффектам, обратным таковым типичных бензодиазепинов (Gardner, 1988; Gardner et al., 1993). Отдельные вещества, в первую очередь флумазенил, блокируют эффекты тех и других in vitro и in vivo, но сами не оказывают какого-либо действия. Новые данные, полученные в молекулярных исследованиях, подтвердили гипотезу о ГАМКд-рецепторах как основной мишени бензодиазепинов. Более того, разнообразие этих рецепторов позволяет объяснить многие наблюдения, казалось, противоречившие ей (De Lorey and Olsen, 1992; Doble and Martin, 1992; Sieghart, 1992; Ragan et al., 1993; Symposium, 1992). Все же некоторые эффекты бензодиазепинов сложно связать с действием на ГАМКд-рецепторы. Так, низкие концентрации бензодиазепинов вызывают торможение нейронов гиппокампа, не устраняемое бикукуллином и пикротоксином (Pole, 1988). Кроме того, эти вещества не влияют на снотворное действие бензодиазепинов у крыс, хотя его предотвращает флумазенил (Mendelson, 1992). При высоких концентрациях, используемых д ля премедикации перед общей анестезией (гл. 14) и для купирования эпилептического статуса (гл. 21), действие бензодиазепинов может иметь дополнительные механизмы. К ним относятся нарушение обратного захвата аденозина с усилением эффектов этого тормозного медиатора (Phillis and O’Regan, 1988), а также не связанные с ГАМК торможение тока Са2+, нарушение зависимого от Са2+ выброса медиаторов и блокада быстрых натриевых каналов (Macdonald and McLean, 1986).
ГАМКд-рецепторы могут быть также точкой приложения общих анестетиков, этанола, ингаляционных наркотиков и некоторых метаболитов эндогенных стероидов (Mehta and Ticku, 1999; Beckstead et al., 2000). Особый интерес среди последних представляет метаболит прогестерона прегнанолон (За-гидрокси-5а-дигидропрогестерон). Он образуется в головном мозге из стероидов, поступающих с кровью или выделяемых глией, и действует подобно барбитуратам, в том числе усиливает вызываемый ГАМК хлорный ток и способствует связыванию бензодиазепинов и стимуляторов ГАМК-рецепторов. Как и барбитураты, в высоких концентрациях прегнанолон вызывает хлорный ток и в отсутствие ГАМК. Опыты с трансфекцией клеток показали, что его действие не требует у-субъединиц ГАМКА-рецептора. Впрочем, в отличие от барбитуратов, он не ослабляет возбуждающее действие глутамата (см. ниже). Эти эффекты возникают очень быстро и, по-видимому, обусловлены действием на уровне мембранных рецепторов. Аналог прегнанолона альфаксалон ранее использовался за пределами США в качестве анестетика.
Дыхательная система. Снотворные дозы бензодиазепинов в норме не влияют на дыхание, но все же следует соблюдать особую осторожность, назначая эти препараты детям (Kriel et al., 2000) и при нарушении функции печени, например на фоне алкоголизма (Guglielminotti et al.,1999). В более высоких дозах, вводимых для премедикации перед обшей анестезией или эндоскопией, бензодиазепины несколько снижают альвеолярную вентиляцию и вызывают дыхательный ацидоз, что связано, видимо, с подавлением вентиляторной реакции на гипоксию, а не на гиперкапнию. На фоне X03JI этот эффект усиливается и могут развиться альвеолярная гипоксия и наркотическое действие С02. Бензодиазепины способны вызвать апноэ лишь в сочетании с общими анестетиками или наркотическими анальгетиками, поэтому при тяжелом отравлении показанием к ИВЛ обычно служит лишь одновременный прием других веществ, угнетающих ЦНС (чаще всего этанола).
В то же время снотворные дозы бензодиазепинов могут усугублять нарушения дыхания во сне за счет падения тонуса мышц глотки и гортани и ослабления реакции дыхательного центра на гиперкапнию (Guilleminault в Symposium, 1990b). Последнего эффекта бывает достаточно, чтобы вызвать гиповентиляцию и гипоксию при тяжелых ХОЗЛ, хотя иногда у таких больных бензодиазепины улучшают сон и его структуру. Снижая тонус мышц глотки и гортани, снотворные дозы бензодиазепинов могут усугубить влияние обструктивных апноэ во сне на альвеолярную гипоксию, легочную гипертензию и нагрузку на сердце. Многие врачи считают обструктивные апноэ во сне противопоказанием к алкоголю и любым транквилизаторам и снотворным, включая бензодиазепины; их надо назначать с осторожностью и при храпе из-за риска перевести частичную обструкцию дыхательных путей в обструктивные апноэ во сне. Кроме того, в восстановительном периоде после инфаркта миокарда эти препараты могут способствовать появлению эпизодов апноэ во время быстрого сна, сопровождаемых снижением оксигенации крови (Guilleminault в Symposium, 1990b); впрочем, влияние бензодиазепинов на выживаемость при болезнях сердца не изучалось.
Сердечно-сосудистая система. В обычных дозах и у здоровых людей бензодиазепины мало влияют на сердечнососудистую систему; их побочные эффекты при апноэ во сне и болезнях сердца описаны выше. В высоких дозах все бензодиазепины снижают АД и повышают ЧСС. В случае мидазолама это обусловлено снижением ОПСС, а в случае диазепама — уменьшением сократимости левого желудочка и работы сердца. Диазепам увеличивает коронарный кровоток, возможно, за счет накопления аденозина в интерстициальной ткани; поскольку аденозин угнетает сократимость, этот эффект может объяснять отрицательное инотропное действие диазепама. В высоких дозах мидазолам существенно снижает мозговой кровоток и экстракцию кислорода головным мозгом (Nugent et al., 1982). ЖКТ. Некоторые гастроэнтерологи считают, что бензодиазепины помогают при ряде болезней ЖКТ с психосоматическим компонентом, однако доказательств этого недостаточно. Бензодиазепины снижают риск стрессовых язв у крыс, а диазепам существенно снижает ночную желудочную секрецию у людей.
Фармакокинетика. Физико-химические свойства и фармакокинетика бензодиазепинов существенно влияют на их клиническое применение. В неионизированной форме все они достаточно липофильны, но степень их липофильности различается более чем в 50 раз в зависимости от полярности и электроотрицательности заместителей.
Все бензодиазепины почти полностью всасываются после приема внутрь (клоразепат — в виде нордазепама, или десметилдиазепама, в который он быстро превращается путем декарбоксилирования в кислой среде желудка). Некоторые препараты (празепам и флуразепам) попадают в системный кровоток лишь в виде активных метаболитов.
По длительности действия выделяют препараты: 1) сверхкороткого действия, 2) короткого действия (Т1/2 < 6 ч), к которым относятся триазолам и небензоди-азепиновые препараты золпидем (Т1/2 около 2 ч) и зопиклон (Т1/2 5—6 ч), 3) средней продолжительности действия (Т1/2 6—24 ч), к которым относятся эстазолам и темазепам, 4) длительного действия (Т1/2 > 24 ч), к которым относятся флуразепам, диазепам и квазепам.
Бензодиазепины и их активные метаболиты связываются с белками плазмы. Степень связывания существенно зависит от липофильности и колеблется от 70% для алпразолама почти до 99% для диазепама. Концентрация свободных бензодиазепинов в СМЖ примерно такая же, как в плазме. Бензодиазепины могут конкурировать за белки плазмы с другими препаратами, но клинически значимых взаимодействий не описано.
Изменение сывороточной концентрации большинства бензодиазепинов описывают двухкамерные фармакокинетические модели (гл. 1); для наиболее липофильных препаратов лучше подходят трехкамерные модели. После в/в введения (или приема внутрь для препаратов с быстрым всасыванием) бензодиазепины быстро накапливаются в головном мозге и других хорошо кровоснабжаемых органах, затем происходит перераспределение в ткани с меньшим кровоснабжением, особенно в мышечную и жировую. Чем выше липофильность препарата, тем быстрее идет этот процесс. Если препараты принимаются на ночь для нормализации сна, то скорость перераспределения может иметь большее значение для длительности действия, чем скорость метаболизма (Dettli в Symposium, 1986а). Кинетику перераспределения диазепама и других высоко липофильных препаратов усложняет кишечнопеченочный кругооборот. Бензодиазепины имеют большой объем распределения, у пожилых он часто бывает увеличен (Swift and Stevenson в Symposium, 1983). Бензодиазепины проникают через плаценту и в молоко.
Метаболизм бензодиазепинов включает 3 основных этапа. Эти этапы, а также взаимоотношения между разными бензодиазепинами и их метаболитами представлены в табл. 17.2. В метаболизме многих бензодиазепинов участвует цитохром Р450, в частности изоферменты IIIA4 и IIC9. Эритромицин, кларитромицин, ритонавир, итра-коназол, кетоконазол, нефазодон и грейпфрутовый сок ингибируют изофермент 1IIA4 и могут нарушать метаболизм таких бензодиазепинов (Dresser et al., 2000). Другие бензодиазепины, например оксазепам, сразу подвергаются конъюгации (Tanaka, 1999). Поскольку активные метаболиты некоторых бензодиазепинов разрушаются медленнее, чем исходные вещества, длительность действия таких препаратов мало связана с Т|/2 исходного соединения. Например, Т1/2 флуразепама составляет 2—3 ч, а его основного активного метаболита (N-дезалкилфлуразепама) — более 50 ч. В то же время у препаратов, которые инактивируются в первой же реакции метаболизма, не образуя активных производных (оксазепама, лоразепама, темазепама, триазолама и мидазолама), длительность действия определяется Т1/2.
У бензодиазепинов с заместителем у N-1 (или С-2) первый и самый быстрый этап метаболизма состоит в модификации или отщеплении этого заместителя. За исключением триазолама, алпразолама, эстазолама и мидазолама, содержащих дополнительное триазольное или имидазольное кольцо, на первом этапе образуются биологически активные продукты N-деалкилирования. Один из них, нордазепам — основной метаболит диазепама, клоразепата, празепама и галазепама; кроме того, он образуется из демоксепама, важного метаболита хлордиазепоксида.
На втором этапе происходит гидроксилирование по С-3, обычно при этом также получается активный метаболит (например, оксазепам из нордазепама). Модификация или отщепление заместителей при N-1 происходит гораздо быстрее, чем гидроксилирование (Т, «40—50 ч и более), поэтому гидро-ксидированных метаболитов с неизмененными заместителями почти нет. Однако существуют два важных исключения:
1) при длительном приеме диазепама накапливается небольшое количество темазепама (в табл. 17.2 не показано), 2) в случае квазепама сера у С-2 замещается кислородом с образованием 2-оксоквазепама, большая часть которого медленно гид-роксилируется по С-3 без отщепления заместителя у N-1. Впрочем, при длительном приеме квазепама его 3-гидроксилиро-ванное производное накапливается лишь в небольшом количестве из-за очень быстрой конъюгации. В то же время накапливается N-дезалкилфлуразепам, продукт дополнительного пути метаболизма квазепама, и вносит существенный вклад в действие препарата.
Третий этап метаболизма бензодиазепинов — конъюгация -гидроксилированных производных (в основном с глюкуроновой кислотой). Т1/2 этой реакции обычно составляет 6—12 ч; ее продукты неактивны. Это единственный существенный путь метаболизма оксазепама и лоразепама и основной путь темазепама, так как его превращение в оксазепам идет медленнее. Метаболизм триазолама и алпразолама начинается с гидроксилирования метильной группы у триазольного кольца (в случае алпразолама реакцию резко замедляет отсутствие хлора у кольца С). Образующиеся вещества (а-гидроксилированные производные) сохраняют активность, но почти не накапливаются из-за быстрых дальнейших превращений, прежде всего конъюгации. Триазольное кольцо эстазолама не имеет метильной группы и гидро-ксилируется лишь в небольшой степени, основной путь его метаболизма — С-30-окисление. 3-гидроксилированные производные алпразолама и триазолама также образуются в значительных количествах (в табл. 17.2 не указано). Триазольное кольцо резко ускоряет гидроксилирование этих трех препаратов по сравнению с другими бензодиазепинами. Их 3-гидроксилированные производные перед выведением быстро конъюгируются или окисляются дальше, до бензофенонов (в табл. 17.2 не указано).
Мидазолам также быстро подвергается метаболизму, в основном путем гидроксилирования метильной группы у имидазольного кольца; 3-гидроксимидазолам образуется лишь в небольшом количестве. Альфа-гидроксимидазолам достаточно активен.
Его Т1/2 составляет около 1 ч, и он выводится после конъюгации. Длительное в/в введение мидазолама ведет к накоплению этого метаболита, иногда значительному (Oldenhofet al., 1988).
Ароматические кольца бензодиазепинов (А и С) гидроксилируются лишь в небольшой степени. Существенное значение имеет восстановление NOj-группы в 7-м положении клоназепама, нитразепама и флунитразепама (Т1/2 этой реакции составляет 20—40 ч). Образующиеся амины неактивны, перед выведением они в различной степени ацетилируются.
Очевидно, бензодиазепины не вызывают существенной индукции цитохрома Р450 и при длительном лечении не ускоряют свой собственный метаболизм и метаболизм других веществ. Циметидин и пероральные контрацептивы ингибируют С-3-гидроксилирование и N- 1-деалкилирование бензодиазепинов; действие этанола, изониазида и фенитоина на эти реакции менее выражено. У пожилых и при болезнях печени они обычно нарушаются в большей степени, чем конъюгация бензодиазепинов и их метаболитов.
В идеале действие снотворного препарата должно быстро начинаться при приеме на ночь, длиться на протяжении всей ночи и прекращаться к утру. Теоретически этим требованиям в наибольшей степени соответствует триазолам, а флуразепам и квазепам, казалось бы, не годятся из-за медленной элиминации N-дезалкилфлуразепама. Однако на практике бензодиазепины короткого действия имеют ряд недостатков, включая ранние пробуждения (у некоторых больных) и больший риск рикошетного эффекта после отмены препарата (Gillin et al., 1989; Roehrs et al. в Symposium, 1990b; Roth and Roehrs, 1992). В то же время тщательный подбор дозы позволяет с успехом использовать флуразепам и другие бензодиазепины более длительного действия, чем триазолам (Vogel, 1992). Подробнее о метаболизме и фармакокинетике бензодиазепинов см. обзоры Greenblatt et al., 1983а, b, 1991, 1993; Greenblatt, 1991; Hilbert and Battista, 1991.
Побочные эффекты. В момент достижения максимальной сывороточной концентрации снотворные дозы бензодиазепинов в той или иной степени вызывают дурноту, чувство усталости, нарушение координации движений, замедление реакции, оглушенность, антероградную амнезию. Когнитивные функции страдают в меньшей степени, чем двигательные. Если препарат принимается на ночь, сохранение этих явлений после пробуждения рассматривается как побочное действие. Они могут сильно мешать вождению и другой деятельности, крайне опасно одновременное употребление алкоголя. Выраженность указанных нарушений четко зависит от дозы, но человек может их не замечать: большинство больных недооценивают, насколько их состояние далеко от нормы. Побочным действием бывает и дневная сонливость, хотя лечение и уменьшает сонливость, вызванную хронической бессонницей (Dement, 1991). Риск и выраженность побочных эффектов растут с возрастом; здесь играют роль возрастные изменения и фармакокинетики, и фармакодинамики (Meyer, 1982; Swift et al. в Symposium, 1983; Monane, 1992).
Нередко бензодиазепины вызывают слабость, головную боль, нечеткость зрения, головокружение, тошноту, рвоту, боль в эпигастрии, понос; изредка бывают артрал-гия, боль в груди, недержание мочи. Противосудорожные бензодиазепины иногда даже увеличивают частоту припадков у больных эпилепсией.
Изменения психики. Иногда бензодиазепины оказывают парадоксальное действие: например, флуразепам может вызывать кошмары, особенно в первую неделю лечения, бывают также говорливость, тревожность, раздражительность, тахикардия, потливость. На фоне различных бензодиазепинов описаны случаи амнезии, эйфории, гипомании, беспокойства и галлюцинаций. Проявлениями растормаживающего эффекта порою оказываются причудливое развязное поведение, гнев, агрессия. Описаны также случаи паранойи, депрессии, суицидальных мыслей. Риск подобных парадоксальных реакций невелик и, по-видимому, зависит от дозы. Сообщения о повышенном риске нарушений сознания и поведения привели к запрету триазолама в Великобритании, но ФДА признало его низкие дозы (0,125— 0,25 мг) безопасными и эффективными. Опрос английских семейных врачей показал, что после запрещения триазолама его замена другими снотворными не снизила число побочных эффектов (Hindmarch et al., 1993). Эти данные согласуются с результатами контролируемых испытаний, говорящих об одинаковой частоте указанных побочных эффектов на фоне разных бензодиазепинов (Jonas et al., 1992; Rothschild, 1992).
Длительный прием бензодиазепинов может вести к зависимости и злоупотреблению, но их риск ниже, чем в случае барбитуратов и наркотических анальгетиков (Ulemhuth et al., 1999). Особой формой злоупотребления можно считать и использование флунитразепама при так называемом изнасиловании на свидании (Woods and Winger, 1997). Легкая зависимость возникает у многих больных, регулярно принимающих стандартные дозы бензодиазепинов. Отмена препарата вызывает временное усиление симптомов, послуживших показанием к его назначению, таких, как бессонница и тревожность. Возможны дисфория, раздражительность, потливость, кошмары, тремор, снижение аппетита, слабость и дурнота, особенно при резкой отмене (Ре-tursson, 1994). Соответственно, отменять бензодиазепины следует постепенно. При обычной схеме лечения больные крайне редко увеличивают дозу без указаний врача, и лишь изредка наблюдается непреодолимая тяга к бензодиазепинам после их отмены. Риск злоупотребления наиболее высок при алкоголизме или наркомании в анамнезе, причем такие больные обычно используют несколько веществ. Они редко предпочитают бензодиазепины барбитуратам и даже алкоголю, но часто добавляют их для усиления действия других веществ (алкоголя и наркотических анальгетиков) или уменьшения их токсичности (например, кокаина). Длительный прием высоких доз бензодиазепинов вызывает более тяжелый абстинентный синдром, включая возбуждение, депрессию, панику, паранойю, миалгию, подергивание мышц и даже эпилептические припадки и делирий. Подробнее о бензодиазепиновой зависимости см. в обзорах Woods et al. (1992), DuPont (1988).
Несмотря на перечисленные побочные эффекты, бензодиазепины сравнительно безопасны. В отсутствие других препаратов даже очень высокие дозы редко ведут к смерти или коме. Смерть от бензодиазепинов часто бывает вызвана одновременным употреблением алкоголя. Передозировка бензодиазепинов редко вызывает тяжелые нарушения дыхания и кровообращения, но даже обычные дозы могут усугублять дыхательную недостаточность при ХОЗЛ и обструктивных апноэ во сне (см. выше).
Бывают также аллергические реакции, поражение печени и угнетение кроветворения, но риск этих явлений невелик. Они описаны для флуразепама и триазолама, но не для темазепама. Высокие дозы бензодиазепинов, введенные перед родами или во время них, могут вызвать у новорожденного гипотермию, артериальную гипотонию и легкое угнетение дыхания; если мать злоупотребляла бензодиазепинами, возможен также абстинентный синдром.
Кроме усиления эффекта других транквилизаторов и снотворных описаны лишь отдельные случаи клинически значимых фармакодинамических взаимодействий бензодиазепинов. Так, этанол не только ускоряет их всасывание, но и усиливает угнетение ЦНС. Сочетание бензодиазепинов с вальпроевой кислотой может вызывать психотические реакции. Фармакокинетические взаимодействия описаны выше.
Применение[править | править код]
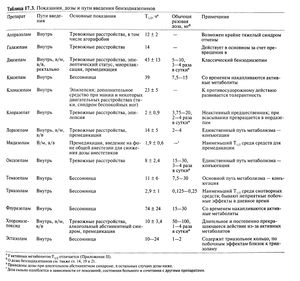
Показания, дозы и пути введения применяемых в США бензодиазепинов приведены в табл. 17.3. В этой таблице содержатся основные показания к разным бензодиазепинам, но важно отметить, что большинство препаратов взаимозаменяемы: например, диазепам можно использовать при алкогольном абстинентном синдроме, а как снотворные могут действовать большинство бензодиазепинов. В целом показания к данному препарату отражают его Т1/2 и могут не соответствовать инструкции изготовителя. В качестве противосудорожных средств применяют бензодиазепины с длинным Т1/2, для купирования эпилептического статуса нужны препараты, быстро проникающие в головной мозг. Для снотворных средств желателен короткий Т1/2, хотя это повышает риск злоупотребления и усугубляет синдром отмены после длительного использования. Для лечения тревожности требуются препараты с длинным Т 1/2, несмотря на больший риск неврологических и когнитивных нарушений из-за их накопления.
Применение бензодиазепинов при бессоннице описано ниже (см. также Symposium, 1990b; Teboul and Choui-nard, 1991; Vogel, 1992; Dement, 1992; Walsh and Engel-hardt, 1992; Maczaj, 1993). Кроме того, их используют в анестезиологии (гл. 13 и 14), при тревожности (гл. 19), эпилепсии (гл. 21) и спастичности (гл. 22).