Лечение стронгилоидоза (препараты)
Категория:
«Фармакология».
Содержание
Лекарства и гельминтозы[править | править код]
Гельминты делят на три основные группы — нематоды (круглые черви), трематоды (плоские черви) и цестоды (ленточные черви). Все они относятся к многоклеточным организмам, обладающим специфическими органами. Большинство гельминтов не размножается в организме человека. Весьма характерной для гельминтозов является эозинофилия. Классификация и биология гельминтов в обобщенном виде представлены в табл. 6.28.
Яйца нематод, (круглые черви, анкилостомы, хлыстовики) для созревания нуждаются в пребывании в почве с переходом в инфекционную фазу, поэтому при достаточно высоком уровне гигиены передача яиц нематод затруднительна. Яйца круглых червей (виды Ascaris) после проглатывания мигрируют через легкие в кишечник. Паразиты семейства AncylostomaticLae (Ancylostoma duodenale, Necator americanus) проникают в организм человека через кожу; их жизненный цикл включает этап пребывания в легких и миграцию в кишечник. Хлыстовик (виды Trichurus) распространен в тропиках.
Лекарства и круглые черви[править | править код]
Аскаридоз[править | править код]
Аскаридоз обусловлен кишечными нематодами, заражение которыми происходит через загрязненные овощи, фрукты и питьевую воду
Возбудителем аскаридоза служит Ascaris lumbricoides. Это самый распространенный в мире гельминтоз, который возникает после проглатывания зрелых яиц аскарид, содержащихся в загрязненной растительной пище и питьевой воде.
Взрослые нематоды обычно живут в тонкой кишке. Они могут мигрировать в главный желчный проток, желчный пузырь и панкреатический проток или пенетрировать стенку тонкой кишки, что приводит к спорадической инфекции. Клиническими проявлениями аскаридоза служат тупые боли в верхней части живота, потеря аппетита, тошнота, рвота и вздутие живота.
Для лечения аскаридоза применяют пирантела памоат или пиперазин
Пирантела памоат, антигельминтное средство широкого спектра действия, впервые был использован в ветеринарной медицине, однако в настоящее время он является препаратом выбора для лечения аскаридоза. По химической структуре он представляет собой 6-членное азотсодержащее кольцо, соединенное этиленовыми связями с фурановым кольцом. Он действует как деполяризующий нервно-мышечный блокатор, открывающий неселективные катионные каналы типа никотининовых рецепторов, таким образом он вызывает спастический паралич и медленную контрактуру червей. Антагонистом пирантела является пиперазин (см. далее).
Пирантел и его производные используют также для лечения инвазий, вызываемых Enterobius vermicularis и анкилостомами, но эти препараты неактивны против Т. trichiura. Однако родственный агент оксипантел активен в отношении последнего вида.
Поскольку пирантела памоат плохо абсорбируется из ЖКТ, его концентрация в кишечнике может достигать сравнительно высокого уровня. Большая часть вещества экскретируется с фекалиями.
Побочные эффекты пирантела памоата (головная боль, головокружение, сыпь, лихорадка и расстройства ЖКТ) при использовании препарата в обычных дозах возникают сравнительно редко и относительно слабы. Препарат обычно принимают внутрь однократно в дозе 5-10 мг/кг. Очень высокие дозы могут вызвать у животных нервно-мышечную блокаду.
Пиперазин является высокоэффективным средством при инвазии Ascaris lumbricoides и Е. vermicularis. Он блокирует нервно-мышечное соединение у нематод и вызывает вялый паралич у A. lumbricoides.
Таблица 6.28 Гельминты, вызывающие паразитарные заболевания
По химической структуре Пиперазин представляет собой простой циклический вторичный амин, вызывающий вялый паралич у червей, действуя как агонист ГАМК и повышая проводимость хлоридов (см. также ивермектин). Пирантела памоат и пиперазин по своим эффектам антагонистичны по отношению друг к другу, поэтому их нельзя применять совместно.
Пиперазин быстро абсорбируется после приема внутрь. Его побочные эффекты: иногда возникающие головокружение и реакция типа уртикарии. Пиперазин противопоказан лицам с установленной гиперчувствительностью, эпилепсией, нарушениями функций почек или печени.
Анкилостомоз[править | править код]
Анкилостомоз также одна из самых распространенных инвазий. Заболевание вызывают Ancylostoma duodenale (Старый Свет) или Necator americanus (Новый Свет). A. duodenale встречается преимущественно в районах с температурным режимом, характерным для Средиземноморского бассейна, Среднего Востока, Северной Индии, Китая и Японии, в то время как N. americanus распространен в тропических и субтропических районах Африки, Азии и Америки. Взрослые нематоды живут в кишечнике человека как кровососущие паразиты. Жизненный цикл паразитов обоих видов сходен, однако место проникновения в организм инвазионных (филярийных) форм паразитов различается: для анкилостом Старого Света — слизистая оболочка рта, Нового Света — кожа. Главные симптомы инвазии — развитие железодефицитной анемии и потеря белков плазмы.
Средство лечения анкилостомоза — пирантела памоат
Пирантела памоат эффективнее против A. duodenale, чем против N. americanus. Антигельминтное действие этого препарата обсуждалось ранее. Однократное введение препарата снижает число нематод в организме, однако для полного излечения может потребоваться несколько курсов терапии.
Энтеробиоз[править | править код]
Энтеробиоз (оксиуроз) — заболевание, вызываемое острицами. Это распространенная во всех странах глистная инвазия, возбудителем которой является Е. vermicularis. Заболевание относится к наиболее часто встречающимся гельминтозам в развитых странах северного полушария, особенно среди школьников. Основным клиническим симптомом является зуд в области ануса.
Для лечения энтеробиоза обычно применяют пирантела памоат.
Стронгилоидоз[править | править код]
Стронгилоидоз (инвазия Strongyloides stercoralis) встречается во всех странах, особенно в тропиках и субтропиках. Инвазионная форма (филярийная личинка) способна пенетрировать интактную кожу, вызывая зудящую эритему в месте проникновения. Личинки вместе с кровотоком переносятся в легкие. Содержащиеся в мокроте личинки попадают в тонкую кишку вместе с мокротой, пенетрируют слизистую оболочку и созревают до взрослых нематод. Оплодотворенные самки выбрасывают частично созревшие яйца, которые затем попадают в фекалии. Экскретируемые со стулом личинки могут проникать через слизистую оболочку нижних отделов толстой кишки и кожу ануса (аутоинфекция). Иммунная система организма человека и репродуктивная система паразита сбалансированы так, что серьезно не страдает ни тот, ни другой. Когда этот баланс нарушается, большое число личинок может проникнуть во все части тела, вызывая гиперинвазию.
Стронгилоидоз у пациентов (кроме беременных) лечат, используя альбендазол или тиабендазол
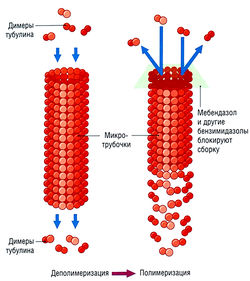
Альбендазол — производное бензимидазола, высокоэффективное в лечении стронгилоидоза. Бензимидазолы, как показывает название, являются производными бициклического соединения (бен-зол/имидазол). С 1970-х гг. в клиническую практику введены три аналога — тиабендазол, мебендазол и альбендазол. Из них препаратом выбора стал альбендазол. Все они являются многоцелевыми анти-гельминтными средствами, особенно при кишечных инвазиях. Бензимидазолы вызывают многочисленные изменения биохимии паразитов, включая блокирование захвата глюкозы, истощение запасов гликогена и снижение образования АТФ у чувствительных нематод. Предполагается, что они интерферируют с бета-тубулином, и возникающая резистентность паразитов связана с изменениями генов тубулина (рис. 6.28). Было показано, что эти вещества убивают червей, их яйца и личинки. При пероральном приеме абсорбируется менее 5% вещества. Обычно назначают трехдневный курс терапии в дозе 400 мг 1 раз в день.
Взрослые и дети старше 2 лет альбендазол переносят хорошо, хотя описаны случаи расстройств ЖКТ и головной боли. Однако экспериментально было показано, что препарат обладает тератогенными свойствами и потенциально эмбриотоксичен, поэтому альбендазол не следует назначать беременным.
Тиабендазол является производным бензимидазола, специфически ингибирующим митохондриальную систему фумаратредуктазы различных гельминтов. Препарат быстро абсорбируется из ЖКТ и при пероральном приеме в дозе 50 мг/кг в сутки, разделенных на 2 части, чрезвычайно эффективен против стронгилоидоза. При лечении гиперинвазии длительность его применения должна составлять не менее 5 сут.
Применение тиабендазола связано с частым возникновением побочных эффектов: головокружение и дискомфорт ЖКТ (тошнота, рвота и потеря аппетита). В экспериментах препарат проявлял тератогенный и эмбриотоксический потенциал, поэтому его не следует назначать беременным; в качестве альтернативного средства можно использовать ивермектин.
Лекарства и личинки нематод[править | править код]
Висцеральный токсокароз (синдром «блуждающей личинки»), ангиостронгилез и трихиноз служат примерами инвазий личинками нематод.
Токсокароз возникает в результате миграции личинок нематоды Toxocara canis во внутренние органы. У большинства пациентов число инвазирующих личинок невелико, и симптомы обычно не возникают. Инвазия часто ассоциируется с эозинофилией.
Трихиноз более распространен в Европе и Америке, чем в Африке и Азии; его возбудитель — нематода Trichinella spiralis. Инициальная фаза инвазии может вызвать преходящие расстройства со стороны ЖКТ: тошноту, диарею, рвоту и боли в животе. Фаза мышечной инвазии личинок обычно вызывает появление триады: миалгия, отек век глаз и эозинофилия.
Ангиостронгилез вызывает нематода Angiostrongy-lus cantonensis в тихоокеанской зоне Азии. Основными клиническими проявлениями церебрального ангиостронгилеза являются эозинофильный менингит с периферической эозинофилией.
Все перечисленные инвазии лечат с помощью перорального приема тиабендазола в течение по крайней мере 1-2 нед.
Филяриоз Банкрофта, бругиоз, лоаоз[править | править код]
Филяриоз Банкрофта и бругиоз вызывают нематоды Wuchereria bancrofti и Brugia malayi соответственно. Эти виды филяриоза имеют различное географическое распространение:
- филяриоз Банкрофта встречается в Центральной Африке, Южной Америке, Индии и Южном Китае;
- распространение бругиоза ограничено Индонезией, Малайским полуостровом, Вьетнамом, Южным Китаем, Центральной Индией и Шри Ланкой.
И филяриоз Банкрофта, и бругиоз относят к лимфатическому филяриозу, т.к. нематоды локализуются в лимфатической системе. Инвазию диагностируют в основном с помощью определения микрофилярий в периферической крови.
Лоаоз вызывает африканский глазной червь (Loa loa). Заболевание эндемично только для дождевых лесов Центральной и Западной Африки. Основной клинический признак — нестойкая опухоль, или калабарская опухоль, которая возникает в результате постоянной миграции взрослых нематод в подкожной ткани.
Диэтилкарбамазин используют для подавления и лечения инвазий, вызываемых нематодами W. bancrofti, В. malayi и Loa loa
Диэтилкарбамазин представляет собой диэтилкарбамидное производное пиперазина. Механизм его действия остается неясным. Препарат быстро убивает микрофилярий, но менее активен в отношении взрослых червей. Лекарство активно только in vivo. Диэтилкарбамазин способен уничтожать микрофилярий и взрослых нематод при филяриозе Банкрофта, бругиозе и лоаозе. Для устранения инвазии W. bancrofti необходима общая кумулятивная пероральная доза, равная 72 мг/кг, однако для уничтожения В. malayi рекомендуются менее высокие дозы. В зависимости от конкретных обстоятельств дозы могут варьировать. Особенно эффективно применение данного лекарства вместе с альбендазолом. Диэтилкарбамазин существенно менее эффективен в случае осложненного лимфатического филяриоза. Диэтилкарбамазин хорошо абсорбируется при пероральном приеме, Т1/2 в плазме составляет 2-10 час в зависимости от pH мочи; 50% пероральной дозы выделяются с мочой, особенно если моча имеет кислый pH.
Побочные эффекты диэтилкарбамазина при низких дозах незначительны и исчезают при продолжении лечения. Побочные эффекты включают анорексию, тошноту, головную боль и рвоту. Важным является факт, что гибель микрофилярий сопровождается ранними аллергическими реакциями замедленного типа. Прием диэтилкарбамазина во время беременности безопасен.
Онхоцеркоз (речная слепота)[править | править код]
Заболевание вызывает Onchocerca volvulus — нематода, распространенная во всех частях Западной и Центральной Африки, особенно по берегам рек саванны южнее Сахары.
Ивермектин используют для лечения онхоцеркоза как препарат выбора вместо диэтилкарбамазина
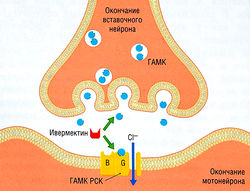
Ивермектин представляет собой полусинтетическое производное авермектина, выделенного из почвенного гриба в 1970-х гг. β-Авермектин широко использовали для обработки сельскохозяйственных культур и уничтожения нематод и артроподов у крупного рогатого скота, прежде чем применить его для нужд человека. В 1990-х гг. было обнаружено, что это вещество крайне эффективно против онхоцеркоза (речной слепоты) и, как оказалось позднее, против других паразитов. Это чрезвычайно сложная мультикольцевая структура, в которой отсутствует азот. Лекарство действует, обездвиживая Onchocerca volvulus в результате тонического паралича периферической мышечной системы. Предполагаемый механизм действия показан на рис. 6.29.
Ивермектин является препаратом выбора для лечения инвазии, вызываемой Onchocerca volvulus. Однократной пероральной дозы 0,15-0,20 мг/кг, принимаемой каждые 6-12 мес, достаточно для подавления заболевания, но не излечения, поскольку взрослая форма паразита не погибает. Таким образом, ивермектин используют для популяционного контроля онхоцеркоза. Препарат эффективен также при лимфатическом филяриозе, вызываемом W. bancrofti или В. malayi (однократный ежегодный прием). Полезным дополнением к терапии ивермектином служит альбендазол. Ивермектин используют, кроме того, для лечения кишечных расстройств, вызываемых нематодами, и даже заболеваний, вызываемых членистоногими (головная вошь, чесоточный клещ).
Пик концентрации ивермектина в крови отмечается через 4-5 час. Препарат имеет длительный Т1/2 (60 час) и очень высокий объем распределения. Метаболизм вещества осуществляет CYP3A4, ивермектин в неизмененном виде в моче не обнаруживается. Его концентрация в ЦНС низкая.
Побочных эффектов у ивермектина в основном нет, хотя были сообщения о слабом раздражении глаз, преходящих неспецифических изменениях ЭКГ и сонливости у пациентов. Очень большие дозы оказались токсичными для животных. В ходе лечения возникает воспалительная реакция немедленного типа как результат гибели микрофилярий. Обычно эта реакция слабая, однако может быть и тяжелой (реакция Мазотти).
Трихиуриаз и капилляриоз[править | править код]
Трихиуриаз (болезнь, вызванная хлыстовиком) распространен во всем мире, однако чаще всего встречается в тропических и субтропических районах. Заболевание вызывают нематоды Trichuris trichiura. Яйца паразита обычно окрашены желчью, имеют бочкообразную форму, а в фекалиях выглядят как биполярные слизистые пробки. Яйца имеют характерный вид, что служит диагностическим признаком. В случае умеренно выраженной инвазии симптомы не проявляются, однако могут быть расстройства со стороны ЖКТ (боли в животе, диарея, тошнота, анорексия), а также анемия, выпадение прямой кишки и кахексия.
Возбудителем кишечного капилляриоза является нематода Capillaria philippinensis. Болезнь зарегистрирована на Филиппинах, в Таиланде, Японии и Иране. Симптомы: водянистый стул, недомогание, анорексия, тошнота и рвота.
Лечение трихиуриаза и капилляриоза проводят с помощью альбендазола (см. ранее) или мебендазола.
Мебендазол является другим производным бензимидазола, ингибирующим у нематод транспорт глюкозы. Мишень для его действия — цитоплазматические микротрубочки и кишечные клетки нематод, где он связывается с рецепторами колхицина на димерах тубулина (см. рис. 6.29). После перорального приема абсорбируется небольшое количество препарата, которое интенсивно метаболизируется в печени, превращаясь в неактивные метаболиты; таким образом мебендазол обладает избирательным действием на паразитов.
Лекарства и трематоды (плоские черви)[править | править код]
Шистосомоз (бильгарциоз)[править | править код]
Шистосомоз вызывают трематоды Schistosoma japoniсит, S. mansoni и S. haematobium в зависимости от географического распространения:
- S. japonicum — Китай, Филиппины, Таиланд, Лаос и индонезийский остров Целебес;
- S. mansoni — Средний Восток, Африка и Южная Америка;
- S. haematobium — Африка и Средний Восток.
Рис. 6.29 Взаимодействие между синапсом нематоды и ивермектином. Потенцирование гамма-аминомасляной кислоты (ГАМК) вызывает приток С1 и гиперполяризацию мотонейронов. Ивермектин также потенцирует высвобождение ГАМК, что объясняет механизм его антигельминтного действия (паралич червя). ГАМК— гамма-аминомасляная кислота; РСК — рецептор-связанный канал [Brody, Larner, Minneman and Neu. Human Pharmacology Molecular to Clinical, Mosby-Year Book Inc.; 1994].
Промежуточным организмом-хозяином, передающим паразитов, служат брюхоногие (пресноводные улитки).
S. japonicum и S. mansoni первично инвазируют печень, селезенку и ЖКТ, a S. haematobium поражает мочеполовой тракт.
Шистосомоз лечат празиквантелом
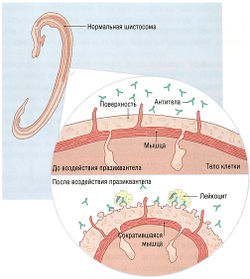
Празиквантел представляет собой производное пиразинизохинолина с комплексным ядром, содержащим пиперазин. Это лекарство после его введения в практику в 1970-х гг. произвело настоящую революцию в лечении шистомоза. На взрослых шистосом оно оказывает двоякий эффект. В минимальных терапевтических концентрациях празиквантел повышает мышечную активность трематод, после чего следует сокращение и спастический паралич. В более высоких, но все еще терапевтических концентрациях, препарат вызывает вакуолизацию и везикулез оболочки чувствительных трематод (рис. 6.30), хотя точный молекулярный механизм его действия остается неизвестным.
Празиквантел высокоэффективен против широкого спектра трематод, включая все виды шистосом, патогенных для человека, хотя в США его применение ограничено шистосомозом. Препарат вводят различными путями, в том числе в дозе 50 мг/кг, разделенных на 3 части, принимаемых после еды. Прием в течение 2 сут дает высокий эффект. Лекарство биодоступно при пероральном приеме с пиком концентрации в плазме через 1-2 час, хотя возможен заметный пресистемный метаболизм. Т1/2 в плазме варьирует от 1 до 3 час. Лекарство взаимодействует с CYP-индуцирующими препаратами.
Празиквантел хорошо переносим и безопасен, если его суточную дозу дают однократно или в 3 приема в течение одного дня при лечении моноинвазии или смешанной инвазии всеми видами Schistosoma. Побочные эффекты (дискомфорт в ЖКТ, тошнота, головная боль и головокружение) могут появиться вскоре после приема лекарства. Гибель паразитов может сопровождаться реакциями гиперчувствительности. Это может быть опасным, если паразиты инфицировали глаз.
Празиквантел безопасен для детей, однако к лечению беременных лучше всего приступить после родов, хотя сообщения о мутагенном, тератогенном или эмбриотоксическом действии празиквантела в литературе отсутствуют.
Клонорхоз и описторхоз[править | править код]
Клонорхоз вызывает трематода Clonorchis sinensis. Он эндемичен для Китая, Тайваня, Гонконга, Японии и Кореи. Возбудителем описторхоза в Таиланде, Лаосе и Камбодже служит Opisthorchis viverrini, тогда как О. felineus встречается в России, Центральной и Восточной Европе. В большинстве случаев инвазии в начальной стадии бессимптомны, однако если симптомы появляются, то носят острый характер: озноб, лихорадка, эпигастральный дискомфорт, гепатоспленомегалия и эозинофилия. В хронической стадии часто возможны симптомы со стороны ЖКТ: тошнота, рвота, потеря аппетита и боли в животе. Наиболее частым осложнением является рецидивирующий холангит. Эти заболевания часто служат также причиной панкреатита.
Рис. 6.30 Механизм действия празиквантела. До воздействия лекарства многочисленные антитела к антигенам поверхности шистосомы не повреждают паразита. Под действием празиквантела повышается проницаемость мембраны к некоторым моно- и дивалентным катионам, в частности Са2+, и это индуцирует приток Са2+ в оболочку паразита в течение 1-2 сек. Возникшие изменения проницаемости поверхности шистосом к внешним ионам вызывают образование небольших впадин и пузырьковидных структур, делая шистосому чувствительной клейкоцитам организма-хозяина, которые в результате адгезии, опосредованной антителами, убивают шистосому [Brody, Larner, Minneman and Neu. Human Pharmacology Molecular to Clinical, Mosby-Year Book Inc.; 1994].
Клонорхоз и описторхоз лечат пероральным приемом празиквантела в дозе 50-75 мг/кг, разделенных на 3 части, после еды, в течение 2 сут.
Парагонимоз[править | править код]
Парагонимоз вызывает легочная трематода различных видов Paragonimus, чаще всего P. westermani. Однако были описаны многие другие патогенные виды:
- в Азии — P. skrjabini, P. hueitungenesis, P. heterotrema, P. philippinensis и P. miyazakii
- в Латинской Америке — P. kellicotti, P. mexicanus, P. ecuadoriensis и P. calilensis
- в Африке — P. africanus и P. uterobilateralis. Парагонимоз передается человеку через употребляемые в пищу инфицированные и непроваренные ракообразные, которые служат вторичным промежуточным организмом-хозяином для Paragonimus. В Японии источником заражения является мясо кабана (промежуточный организм-хозяин P. westermani).
Основные клинические проявления парагонимоза относятся к легким (плевральные боли, диспноэ, кровянистая мокрота, кашель). Осложнениями могут быть плевральный выпот, пневмоторакс, абсцесс и эмпиема легких. Обычно наблюдается эозинофилия. Сообщалось, что эктопическая миграция трематод происходит практически во все внутренние органы. Наиболее серьезным осложнением является церебральный парагонимоз, чаще всего встречающийся у детей в Японии и Корее.
Парагонимоз лечат перорально празиквантелом в дозе 50-75 мг/кг, разделенных на 3 части, после еды, в течение 3 сут или битионолом.
Механизм действия битионола связан с подавлением дыхания митохондрий паразита. Препарат используют в дозе 50 мг/кг, разделенных на 2 или 3 части, после еды, через день; всего 10-15 доз.
Побочные эффекты битионола нередки и в целом носят умеренный и преходящий характер. Однако иногда возникают тяжелые симптомы: анорексия, диарея, тошнота, рвота, головокружение, головная боль и абдоминальные колики.
Фасциолез[править | править код]
Фасциолез вызывают трематоды Fasciola hepatica, F. gigantica и другие виды Fasciola (японский большой печеночный сосальщик). Инвазия встречается повсеместно и представляет собой обычное явление у коров, коз и лошадей, будучи эндемичной в Европе, Южной и Центральной Америке, Африке и Азии. После проглатывания трематоды инвазируют систему желчных путей человека. По данным литературы, источником заражения служат такие пресноводные растения, как кресс водяной, салат-латук и люцерна, а также говяжья печень. Трематоды поселяются во внутрипеченочных желчных протоках. У пациентов с фасциолезом обычно наблюдают гепатомегалию, лихорадку и эозинофилию.
Раньше фасциолез лечили битионолом, назначаемым через день в дозе 50 мг/кг, разделенных на 3 части, которые принимали после еды; курс лечения состоял из 10-15 доз. Применяли также празиквантел в дозе 75 мг/кг, разделенных на 3 части, в течение 7 сут. Недавно было обнаружено, что более эффективным в лечении фасциолеза, чем битионол или празиквантел, является другое производное бензимидазола — триклабендазол. Его назначают в дозе 10 мг/кг однократно.
Фасциолопсиоз[править | править код]
Фасциолопсиоз вызывает трематода Fasciolopsis buski в эндемичных районах (Восточный Китай, Тайвань, Таиланд, Вьетнам, Лаос, Индия, Индонезия). Инвазия происходит в результате употребления в пищу контаминированных водных растений. Трематода поселяется в двенадцатиперстной кишке и тощей кишке. Большей частью инвазия протекает бессимптомно, однако в тяжелых случаях могут быть такие клинические признаки и симптомы, как лихорадка, эозинофилия, генерализованный отек, непроходимость кишечника, а также истощение.
Лечение фасциолопсиоза проводят празиквантелом в дозе 50-75 мг/кг, разделенных на 3 части, в течение 3 сут.
Гетерофиоз[править | править код]
Гетерофиоз вызывают члены семейства трематод Fleterophyidae (например, Heterophyes heterophyes и Меtagonimus yokogawai). Н. heterophyes обнаруживается главным образом в Египте, странах Средиземно-морского бассейна и Японии. М. yokogawai наиболее часто встречается на Дальнем Востоке, и заражение происходит в результате потребления сырой рыбы. Обычно инвазия протекает бессимптомно, хотя в тяжелых случаях наблюдаются признаки и симптомы со стороны ЖКТ (колики, абдоминальная болезненность и диарея).
Для лечения гетерофиоза применяют перорально празиквантел в дозе 50 мг/кг, разделенных на 3 части, в течение 1-2 сут.
Лекарства и цестоды[править | править код]
Крупные кишечные ленточные черви (кроме Taenia solium)[править | править код]
При тениозе, вызываемом взрослыми цестодами Taenia saginata (невооруженный цепень, или бычий солитер), человек является окончательным организмом-хозяином. Взрослые цестоды локализуются в тонкой кишке. Отдельные черви достигают 5-8 м в длину и состоят из 1000-2000 сегментов, или проглоттид, которые содержат репродуктивные органы и отделяются от червя, когда заполняются оплодотворенными яйцами, выделяясь с фекалиями. Т. saginata распространена повсеместно, инвазия часто встречается в Эфиопии и Мексике и относительно часто — в Южной Америке и Западной и Восточной Африке. Инвазия редко вызывает тяжелые клинические явления, однако ее следует отличать от тениоза, обусловленного Taenia solium.
Дифиллоботриоз вызывает взрослая цестода Diphyllobothrium latum, или широкий лентец. Инвазия встречается во многих районах мира (Европе, Ближнем Востоке, Сибири, Японии и Северной Америке). Люди заражаются, употребляя в пищу плохо проваренное филе из лосося, форели и щуковых рыб, представляющих собой промежуточный организм-хозяин. Взрослый червь у человека является самым длинным (4-10 м длиной). В большинстве случаев симптомы заражения отсутствуют, однако в Финляндии у некоторых пациентов с этим заболеванием была выявлена анемия вследствие дефицита витамина В12.
Для лечения описанных инвазий крупными цестодами используют празиквантел, никлосамид или гастрографин.
ПРАЗИКВАНТЕЛ. Пациенту дают послабляющий раствор электролитов (например, GoLytely, промывной раствор полиэтиленгликоля) для уменьшения объема фекалий. Затем назначают перорально празиквантел в дозе 10 мг/кг однократно. Через 2-3 час следует прием сульфата магния как быстро действующего слабительного для изгнания цестоды.
НИКЛОСАЛЛИД. Никлосамид представляет собой галогенированный салициламид, введенный в практику в 1960-е гг. и более не применяемый в США. Его антигельминтное действие связано со стимуляцией захвата кислорода цестодой при низких концентрациях вещества и блокированием поглощения глюкозы при высоких концентрациях. Когда червь погибает, сколекс (головка ленточного червя) высвобождается из кишечной стенки, и червь переваривается. В случае инвазии Taenia solium высвобождающиеся оплодотворенные яйца могут вызвать опасный цистицеркоз.
Никлосамид является дешевым, эффективным и практически везде доступным средством. Препарат абсорбируется из ЖКТ в небольшом количестве. В день лечения пациент не должен принимать пищу. Доза для взрослых составляет 2 г, для детей — меньше. Таблетки перед проглатыванием должны быть основательно разжеваны, их следует запить небольшим количеством воды. Принимать после этого слабительное, чтобы изгнать червя, не обязательно, т.к. сколекс и проглоттиды перевариваются в результате действия лекарства.
Побочные эффекты никлосамида тяжестью не отличаются, хотя могут возникать умеренные расстройства ЖКТ.
ГАСТРОГРАФИН. Гастрографин представляет собой водорастворимое контрастное вещество, используемое при рентгенографии ЖКТ. Обнаружено, что оно оказывает антигельминтный эффект на кишечных цестод (Taenia saginata, D. latum, Diplogo-noporus grandis), хотя о механизме его антигельминтного действия сведений нет. Гастрографин (300 мл) дают после приема послабляющего раствора. Его вводят через дуоденальный зонд через рот, продвигая до дуоденального изгиба. При рентгеноскопии червь виден как рентгенопрозрачное затенение. Когда паразит достигает прямой кишки, у пациента стимулируют дефекацию.
Taenia solium и Cysticercus cellulosae[править | править код]
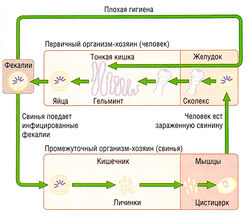
Taenia solium — цепень, или свиной солитер — распространен во всем мире. Взрослая цестода живет в тонкой кишке человека подобно Taenia saginata и D. latum, имеет 800-900 проглоттид и достигает в длину 2-3 м. Жизненный цикл Taenia solium показан на рис. 6.31.
Цистицеркоз вызывают личинки Taenia solium (Cysticercus cellulosae), которые живут подкожно в мышцах, глазной впадине, головном мозге. Большинство случаев инвазии обусловлено потреблением пищи и воды, зараженных яйцами Taenia solium. Тениоз и цистицеркоз встречаются в Латинской
Америке, Восточной Европе, Индии, Пакистане, Индонезии, Китае и Корее. Клинические проявления церебрального цистицеркоза зависят от локализации цист.
Для лечения тениоза, вызванного Taenia solium, и цистицеркоза используют гастрографин, празиквантел и альбендазол
Гастрографин является препаратом выбора для лечения тениоза, поскольку не повреждает цестоды. При их повреждении в просвет кишечника высвобождаются опасные живые яйца Taenia solium. Об антигельминтном действии и терапевтических дозах гастрографина см. ранее.
Цистицеркоз лечат празиквантелом и альбендазолом лишь после удаления червей с помощью гастрографина. Празиквантел применяют перорально ежедневно в дозе 75 мг/кг, разделенных на 3 части, в течение 7 сут. Через неделю курс лечения повторяют. На протяжении всего периода терапии назначают преднизолон, чтобы предотвратить или снизить аллергические реакции, которые могут возникнуть в результате разрушения цистицерков.
Альбендазол применяют для лечения цистицеркоза (а также эхинококкоза; см. далее). Препарат абсорбируется из ЖКТ, быстро и интенсивно метаболизируется в печени. При использовании препарата против кишечных цестод рекомендуется принимать его на пустой желудок, но если мишенью должны быть тканевые цестоды — вместе с жирной пищей. Проводят два 7-дневных курса терапии с интервалом 1 нед в дозе 10-15 мг/кг в сутки, разделенных на 3 части. Также назначают преднизолон для уменьшения аллергических реакций.
Побочные эффекты альбендазола: преходящий дискомфорт со стороны ЖКТ и головная боль.
Эхинококкоз[править | править код]
Эхинококкоз вызывают личиночные формы цестод Echinococcus granulosus и Е. multilocularis, заражение происходит пероральным путем
Echinococcus granulosus распространен по всему миру. Эхинококкоз (кистозное гидатидное заболевание) встречается в Восточной Африке, на Средиземно-морском побережье, в Южной Америке, на Среднем Востоке, в Австралии, Индии и России.
Е. multilocularis — второй по распространенности вид. Вызываемый им эхинококкоз (альвеолярное гидатидное заболевание) регистрируется в Канаде, Центральной Европе, Сибири, на Аляске и в Северной Японии.
Взрослые цестоды Echinococcus granulosus и Е. multilocularis имеют длину 2-7 мм и 1,2-4,5 мм соответственно. Взрослые цестоды живут в тонкой кишке окончательных организмов-хозяинов (собака, лиса, волк). Человек является промежуточным организмом-хозяином и заражается, проглатывая яйца, экскретируемые зараженным окончательным организмом-хозяином. Клинические проявления зависят от размера кисты (Echinococcus granulosus) и степени инвазии (.Е. multilocularis) печени, легких и других органов. Эхинококкоз, вызываемый Е. multilocularis, напоминает карциному по способности к метастазированию и часто имеет летальный исход.
Хирургическое вмешательство все еще остается средством выбора в операбельных случаях эхино-коккоза. Эффективной может быть химиотерапия с применением альбендазола (четыре 30-дневных курса в дозе 10-15 мг/кг в сутки, разделенных на 3 части, интервалы между курсами — 15 сут).
Гименолепидоз[править | править код]
Гименолепидоз вызывает Hymenolepis папа (карликовый цепень) и Н. diminuta. Последний является самой мелкой цестодой человека, ее размер составляет 1-4 см. Обычно она инвазирует детей в тропиках и субтропиках. Заражение происходит в результате потребления пищи и воды, загрязненных яйцами червей. Аутозаражение и быстрое размножение цестод повышает обсемененность паразитами организма истощенных или иммунодефицитных детей, что вызывает расстройства ЖКТ, включая тошноту, рвоту, диарею и боли в животе.
Н. diminuta является обычным паразитом крыс и мышей, иногда инвазирующим человека. Взрослые цестоды могут достигать 20-60 см в длину. Жизненный цикл цестоды требует присутствия промежуточного организма-хозяина (блохи) и окончательного организма-хозяина (крысы и мыши). Иногда заражаются люди (случайно проглоченные инфицированные блохи).
Для терапии применяют празиквантел в дозе 10-25 мг/кг однократно. При инвазии Н. папа можно использовать никлосамид.
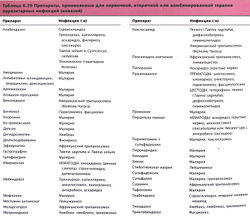
Некоторые из антипаразитарных препаратов и заболевания, для которых они предназначены, перечислены в табл. 6.29.
Читайте также[править | править код]
- Антипаразитарные средства (препараты)
- Лекарства и паразиты
- Лечение малярии (препараты)
- Лечение амебиаза (препараты)
- Лечение токсоплазмоза (препараты)
Литература[править | править код]
- Baird JK. Effectiveness of antimalarial drugs. N Engl J Med 2005; 352: 1565-1577.
- Barrett MP, Burchmore RJ, Stich A et al. The trypanosomiases. Lancet 2003; 362: 1469-1480.
- Docampo R, Moreno SN. Current chemotherapy of human African trypanosomiasis 2003; 90(Suppl): 10-13.
- Greenwood BM, Bojang K, Whitty CJ, Targett GA. Malaria. Lancet 2005; 365: 1487-1498.
- Horton J. Global anthelmintic chemotherapy programs: learning from history. Trends Parasitol 2003; 19: 405-409.
- Murray J, Berman C, Davies N, Saravia. Advances in leishmaniasis. Lancet 3656: 1561-1577H.
- Olliaro PL, Taylor WR. Antimalarial compounds: from bench to bedside. J Exp Biol 2003; 206: 3753-3759 [A review of antimalarial drugs].
- Petersen E. Malaria chemoprophylaxis: when should we use it and what are the options? Expert Rev Anti Infect Ther 2004; 2: 119-132 [Antimalarial coverage for those not normally exposed to malaria].
- Stanley SL. Amoebiasis. Lancet 2003; 361: 1025-1034 [A comprehensive overview of the use of drugs and for amoebic infections].
- Strickland GT (ed.) Hunter’s Tropical Medicine and Emerging Infectious Diseases, 8th edn. Philadelphia: W.B. Saunders; 2000 [This textbook describes general aspects of tropical and parasitic diseases and their treatment].
- Upcroft P, Upcroft JA. Drug targets and mechanisms of resistance in the anaerobic protozoa. Clin Microbiol Rev 2001; 1: 150-164.
- Wilairatana P, Krudsood S, Treeprasertsuk S, Chalermrut K, Looareesuwan S. The future outlook of antimalarial drugs and recent work on the treatment of malaria. Arch Med Res 2002; 33: 416-421 [Malarial resistance and how to combat it in the future].