Лечение малярии (препараты) — различия между версиями
Dormiz (обсуждение | вклад) |
Ars (обсуждение | вклад) (→Читайте также) |
||
| (не показаны 2 промежуточные версии 2 участников) | |||
| Строка 103: | Строка 103: | ||
=== 4-Аминохинолины (хлорохин, амодиахин) === | === 4-Аминохинолины (хлорохин, амодиахин) === | ||
| − | + | [[Image:PeidgT6,27.jpg|250px|thumb|right|Таблица 6.27 Противомалярийные препараты и механизм их действия]] | |
'''ХЛОРОХИН'''. Хлорохин представляет собой 4-аминохинолин, впервые синтезированный в 1934 г., однако затем открытый независимо в результате противомалярийных исследований в 1943 г. Химически он близок другим хинолонам, также обладающим антипаразитарными свойствами. Близкородственным аналогом является амодиахин. | '''ХЛОРОХИН'''. Хлорохин представляет собой 4-аминохинолин, впервые синтезированный в 1934 г., однако затем открытый независимо в результате противомалярийных исследований в 1943 г. Химически он близок другим хинолонам, также обладающим антипаразитарными свойствами. Близкородственным аналогом является амодиахин. | ||
| − | |||
| − | |||
| − | |||
Хлорохин и амодиахин действуют как гематошизотропные (шизонтоцидные) препараты. Предполагается, что они накапливаются в лизосомах паразита (пищеварительных вакуолях), где переваривается гемоглобин. Здесь они ингибируют полимеризацию гемина, токсичного для паразита, в нерастворимый и нетоксичный гемозоин (малярийный пигмент). Накапливающийся гемин убивает паразита. | Хлорохин и амодиахин действуют как гематошизотропные (шизонтоцидные) препараты. Предполагается, что они накапливаются в лизосомах паразита (пищеварительных вакуолях), где переваривается гемоглобин. Здесь они ингибируют полимеризацию гемина, токсичного для паразита, в нерастворимый и нетоксичный гемозоин (малярийный пигмент). Накапливающийся гемин убивает паразита. | ||
| Строка 268: | Строка 265: | ||
== Читайте также == | == Читайте также == | ||
| − | + | *[[Тропические болезни]] | |
*[[Антипаразитарные средства (препараты)]] | *[[Антипаразитарные средства (препараты)]] | ||
**[[Противомалярийные средства (препараты)]] | **[[Противомалярийные средства (препараты)]] | ||
| Строка 276: | Строка 273: | ||
*[[Лечение амебиаза (препараты)]] | *[[Лечение амебиаза (препараты)]] | ||
*[[Лечение токсоплазмоза (препараты)]] | *[[Лечение токсоплазмоза (препараты)]] | ||
| − | *[[Лечение | + | *[[Лечение стронгилоидоза (препараты)]] |
Текущая версия на 21:24, 9 апреля 2015
Категория:
«Фармакология».
Содержание
Малярия[править | править код]
Читайте также: Противомалярийные средства (препараты)
Малярия — протозойное заболевание, которое обычно переносят некоторые виды комаров. Возбудитель имеет два отдельных организма-хозяина, каждый из которых играет особую роль в жизненном цикле паразита
В тропических странах малярия является основным паразитарным заболеванием. Каждый год во всем мире регистрируют 200 млн случаев заболеваний малярией и 2 млн случаев летальных исходов от нее. Болезнь эндемична более чем для 100 стран в Африке, Азии, Океании, Центральной и Южной Америке и некоторых островов Карибского бассейна, где живут приблизительно 60% населения Земли.
Существует четыре вида малярийных паразитов (плазмодиев)
Малярию обычно передают комары рода Anopheles. В редких случаях заражение происходит в результате врожденной передачи, трансфузии инфицированной крови или использования загрязненных шприцев. Заболевание вызывают плазмодии малярии четырех видов:
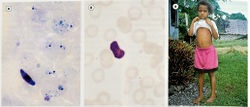
- Plasmodium falciparum — широко распространенный вид, вызывающий наиболее тяжелые инфекции; почти все случаи летальных исходов от малярии обусловлены плазмодием этого вида (рис. 6.23а);
- Plasmodium vivax — часто встречающийся вид; малярия, вызываемая этим плазмодием, носит более доброкачественный характер, чем после заражения P. malariae и P. ovale (рис. 6.236);
- Plasmodium malariae также имеет широкое распространение;
- Plasmodium ovale распространен в основном в Африке.
Четыре вида малярии
- P. falciparum вызывает наиболее тяжелую инфекцию; основной проблемой является резистентность плазмодия этого вида к противомалярийным препаратам
- P. vivax обусловливает более доброкачественный характер заболевания, чем P. malariae и P. ovale
- P. vivax и P. ovale ответственны за повторные приступы заболевания; возбудитель локализуется в печени
- P. ovale распространен главным образом в Африке
Клиническая картина малярийной инфекции зависит от вида паразита и иммунного статуса организма-хозяина
Острая малярия, вызываемая P. falciparum, представляет собой потенциально фатальное заболевание, и неиммунные лица, оказавшиеся в эндемичных районах, подвергаются риску получения тяжелой инфекции. Острая малярия встречается там, где экспозиция ограничена или носит сезонный характер и где иммунитет в популяции данного района относительно низкий. В этих условиях может возникнуть эпидемия малярии, поражающая все возрастные группы. Осложнения: поражения ЦНС (церебральная малярия), гипогликемия, отек легких, острая почечная недостаточность и массированный внутрисосудистый гемолиз.
Повторная хроническая инфекция часто приводит к спленомегалии и прогрессирующей анемии (рис. 6.23в). Наиболее высокому риску летального исхода от инфекции, вызванной P. falciparum, подвержены беременные, не получающие лечения, особенно там, где передача носит интермиттирующий характер. Плод у таких женщин неизбежно испытывает влияние плацентарной недостаточности.
Дети, рожденные иммунными матерями в голоэндемических районах, обычно не заражаются малярией в течение нескольких месяцев после рождения, главным образом за счет пассивного переноса материнских антител через плаценту. Затем эти дети в раннем возрасте становятся подверженными тяжелым повторным острым приступам, потенциально опасным для жизни, а после 5 лет тяжесть и частота этих приступов снижаются по мере развития иммунитета.
Клинически тяжелая малярия — нечастое явление среди взрослого населения (за исключением беременных и лиц с нарушениями иммунной системы), постоянно проживающего в районах с высокой вероятностью передачи инфекции.
Противомалярийные лекарства действуют на различные фазы жизненного цикла малярийного паразита
Жизненный цикл малярийного паразита (рис. 6.24) проходит несколько фаз:
- спорозоиты образуются в комаре-переносчике из половых форм паразита и мигрируют в слюнные железы комара (спорогония);
- попадая после укуса комара в кровоток человека, спорозоиты быстро проникают в паренхиматозные клетки печени, где вырастают в крупные тканевые шизонты, содержащие большое число мерозоитов (процесс, известный как внеэритроцитарная шизогония);
- через 5-20 дней (в зависимости от вида) крупные тканевые шизонты разрываются и высвобождают мерозоиты, которые инвазируют циркулирующие эритроциты, где быстро размножаются;
- эритроциты организма-хозяина обычно разрушаются, высвобождая мерозоиты, которые снова проникают в интактные эритроциты и разрушают их, создавая тем самым порочный круг;
- некоторые мерозоиты, развиваясь, превращаются в мужские и женские гаметоциты, в результате инфицированный человек становится резервуаром инфекции для комаров; таким образом завершается цикл передачи.
Разрушение эритроцитов с последующим высвобождением продуктов распада паразитов вызывает эпизодические (с интервалами, длительность которых зависит от вида паразита) приступы озноба и лихорадки, столь характерные для малярии. Некоторые тканевые формы P. vivax и P. ovale персистируют в печени в течение нескольких месяцев и даже лет в виде гипнозоитов, ответственных за рецидивы, свойственные этим формам малярии. P. falciparum или P. malariae гипнозоиты не образуют. Рецидив инфекции вызывают персистирующие кровяные формы паразита у пациентов после неадекватной терапии или при ее отсутствии.
Выбор препарата для лечения малярии зависит от вида паразита, биодоступности, метаболизма и побочных эффектов лекарства и состояния иммунитета организма-хозяина
Поскольку эффективность лекарства против малярийной инфекции является функцией взаимодействия между паразитом, лекарством и организмом человека, выбор лекарственного вещества зависит от:
- вида паразита и стадии его развития. Лекарственная резистентность среди различных видов Plasmodia становится глобальной проблемой. Существуют также различия эффективности препаратов по отношению к разным штаммам одних и тех же видов плазмодия в различных географических районах;
- метаболизма лекарственного препарата, который может быть неодинаков у различных географических популяций (например, ферменты CYP);
- баланса между терапевтическим и побочными эффектами;
- иммунитета организма-хозяина: лица, имеющие иммунитет определенного уровня в результате длительного воздействия инфекции, излечиваются легче (отвечают даже на более низкие дозы препарата) или обладают более высокой степенью защиты, чем неиммунные лица.
Противомалярийные лекарственные средства классифицируют соответственно фазе жизненного цикла плазмодия, на которую они действуют
Противомалярийные лекарственные средства избирательно действуют на различные фазы жизненного цикла плазмодия (см. рис. 6.24), поэтому различают:
- гистошизотропные (шизонтоцидные) средства, вызывающие гибель тканевых шизонтов (внеэритроцитарных форм) в печени;
- гематошизотропные (шизонтоцидные) средства, уничтожающие плазмодии в эритроцитах, предотвращая или обрывая клинический приступ;
- гаметоцидные средства, уничтожающие половые формы плазмодия (гаметоциты), предотвращая их передачу;
- гипнозоитоцидные средства, действующие на покоящиеся гипнозоиты P. vivax и P. ovale, присутствующие в печени; эти лекарства предотвращают рецидивы;
- споронтоцидные средства, которые прерывают фазу спорогонии у комаров, питавшихся кровью носителей гаметоцитов. В результате комары уже не могут передавать инфекцию.
До настоящего времени не разработаны препараты, активные против спорозоитов, присутствующих в крови.
Применение соответствующих противомалярийных средств позволяет создать защиту, предотвратить передачу малярии и излечить заболевание
Для предотвращения клинического приступа противомалярийные препараты применяют до возникновения инфекции или прежде, чем она станет очевидной. Цель состоит в том, чтобы предотвратить появление любого из симптомов приступа болезни с помощью:
- супрессивной профилактики с применением гематошизотропных средств, чтобы предупредить острый приступ болезни;
- каузальной профилактики с помощью гистошизотропных средств, чтобы предотвратить колонизацию печени паразитами.
При куративном (терапевтическом) вмешательстве используют лекарства, направленные против уже развившейся инфекции. Лечение состоит в супрессивной обработке с целью устранения острого приступа, обычно с помощью гематошизотропных лекарств. Для предотвращения рецидивов малярии необходимо использовать гипнозоитоцидные средства против покоящихся форм паразита в печени.
Для предотвращения передачи инфекции требуется ее устранение у комаров с помощью гаметоцитоцидных или споронтоцидных средств. Это очень важно для избавления от малярии в тех районах, где она эндемична.
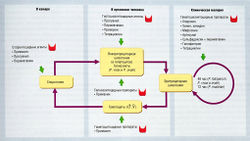
Общеупотребительными являются противомалярийные препараты, относящиеся к нескольким группам химических веществ
Обобщенные данные о действии различных противомалярийных препаратов представлены в табл. 6.27.
Противомалярийные препараты[править | править код]
4-Аминохинолины (хлорохин, амодиахин)[править | править код]
ХЛОРОХИН. Хлорохин представляет собой 4-аминохинолин, впервые синтезированный в 1934 г., однако затем открытый независимо в результате противомалярийных исследований в 1943 г. Химически он близок другим хинолонам, также обладающим антипаразитарными свойствами. Близкородственным аналогом является амодиахин.
Хлорохин и амодиахин действуют как гематошизотропные (шизонтоцидные) препараты. Предполагается, что они накапливаются в лизосомах паразита (пищеварительных вакуолях), где переваривается гемоглобин. Здесь они ингибируют полимеризацию гемина, токсичного для паразита, в нерастворимый и нетоксичный гемозоин (малярийный пигмент). Накапливающийся гемин убивает паразита.
Хлорохин действует на эритроцитарные формы P. vivax, P. ovale и P. malariae, а также на P. falciparum, чувствительный к хлорохину. Он обладает также гаметоцидным действием на первые три формы. Хлорохин не активен против латентных тканевых форм P. vivax или P. ovale.
Кроме того, хлорохин применяют против печеночных амеб, а также при воспалительных заболеваниях с аутоиммунным компонентом.
Резистентный штамм P. falciparum транспортирует хлорохин из своей пищеварительной вакуоли быстрее, чем чувствительные штаммы. Блокаторы кальциевых каналов (например, верапамил и нифедипин) супрессируют отток хлорохина и при совместном применении с хлорохином теоретически должны делать эффективной терапию, направленную против резистентных к хлорохину штаммов. Недавние попытки установить генетическую основу резистентности оказались не совсем успешными, свидетельствуя о том, что резистентность может быть обусловлена множественными механизмами.
Хлорохин — наиболее широко применяемое противомалярийное средство в тропиках. Концентрация его в крови достигает терапевтической в течение 2-3 час, из организма он выводится медленно, главным образом почками. Хлорохин экскретируется в неизмененном виде (около 50%) или метаболизированным в печени, в основном путем окисления ферментами CYP.
Побочные эффекты хлорохина: тошнота, рвота, беспокойное состояние, нарушения зрения (расплывчатость, смазанность), гипотензия и зуд. Считается, что во время беременности хлорохин относительно безопасен.
АМОДИАХИН. Амодиахин сходен с хлорохином, однако сохраняет определенную активность против резистентных к хлорохину штаммов P. falciparum, хотя это преимущество обычно недолговременно. При продолжающемся введении амодиахина один из его метаболитов, хинонеимин, вызывает токсический гепатит и потенциально фатальный агранулоцитоз. В настоящее время применение амодиахина прекращено.
Ариламиноалкоголи[править | править код]
Хинолинметанолы (хинин, хинидин и мефлохин) и фенантренметанол (галофантрин) относятся к гематошизотропным средствам, т.к. действуют только на эритроцитарные стадии малярийного плазмодия, когда плазмодий занят перевариванием гемоглобина. Эти препараты применяют для лечения острой формы заболевания благодаря их быстрому действию.
Хинин имеет длительную (350-летнюю) историю применения. Это алкалоид, экстрагированный из коры хинного дерева (цинхоны), произрастающего в Южной Америке. В неочищенной форме в виде настоя коры хинин завезли в Европу много столетий назад и использовали для лечения лихорадки.
И лишь значительно позднее было обнаружено, что это специфическое средство для лечения малярии. Несмотря на долгую историю, хинин остается препаратом выбора для лечения тяжелой осложненной малярии.
Механизм действия хинина состоит в том, что он как слабое основание ингибирует детоксицирующую полимеризацию гема. Хинин обладает шизонтоцидными свойствами и оказывает слабый эффект на другие формы, за исключением гаметоцитоцидного действия на P. malariae и P. vivax, поэтому его не используют для профилактики. Кроме того, хинин блокирует ионные каналы подобно хинидину (D-энантиомер хинина), который используют как антиаритмическое средство. Он действует также на скелетные мышцы, снижая их возбудимость, поэтому в низких дозах его применяют для устранения судорожных сокращений мышц ног.
Основное назначение хинина при малярии состоит в его в/в введении как супрессивного и терапевтического средства при резистентной к хлорохину инфекции. Вслед за начальным в/в введением его принимают перорально. Его всегда используют как настой контролируемого приготовления. Хинин считают относительно безопасным во время беременности.
Умеренные побочные реакции на хинин — обычное явление при его в/в введении. В случае применения высоких доз наблюдают характерную триаду побочных эффектов: цинхонизм, гипогликемию и гипотензию. Симптомы цинхонизма включают шум в ушах, потерю слуха, тошноту, рвоту, беспокойное состояние и нарушения зрения (расплывчатость, смазанность). Наиболее частый серьезный побочный эффект — гипогликемия. Хинин и его изомер хинидин относятся к веществам, блокирующим ионные каналы. В результате этого действия на калиевые ионные каналы сердца, ответственные за ток IКг, вещества могут вызвать сердечную аритмию.
Мефлохин, сходный по химической структуре с хинином, представляет собой длительно действующий гематошизотропный препарат, эффективный при лечении всех видов малярии, включая лекарственно полирезистентный P. falciparum. Мефлохин можно также использовать для супрессивной профилактики.
Мефлохин доступен только в форме таблеток. Побочные эффекты мефлохина: тошнота, рвота, абдоминальные колики, синусовая брадикардия, __ синусовая аритмия и постуральная гипотензия. Тяжелыми, но относительно редкими побочными эффектами являются острый психоз и преходящая энцефалопатия с судорогами. Предполагается, что мефлохин может привести к появлению дефектов у плода в случае приема препарата в I триместре беременности.
Галофантрин — другое синтетическое противомалярийное средство, активное против полирезистентного P. falciparum. Оральная биодоступность препарата изменчивая и слабая, однако повышается в случае приема лекарства вместе с жирной пищей. Препараты для парентерального введения отсутствуют. Галофантрин пациенты обычно переносят хорошо, побочные эффекты слабые и обратимые, например тошнота, боли в животе и диарея. Однако было показано, что при использовании препарата в стандартных дозах он удлиняет интервал QT на электрокардиограмме, и есть единичные сообщения о тяжелых, иногда летальных аритмиях (например, torsades de pointes).
Антифолаты[править | править код]
см. также Антибиотики
Сульфонамиды (сульфадоксин, сульфален и ко-тримоксазол), сульфон (дапсон), бигуаниды (прогуанил и хлорпрогуанил) и диаминопиридин (пириметамин) обладают свойством ингибировать метаболизм фолатов у паразита. Эти лекарства можно разделить на два типа:
- тип 1 — сульфоанамиды и дапсон, конкурирующие за фермент DHPS, обнаруженный только у плазмодиев;
- тип 2 — бигуаниды и диаминопиримидины, специфически ингибирующие форму DHFR, найденную только у малярийного плазмодия (рис. 6.25).
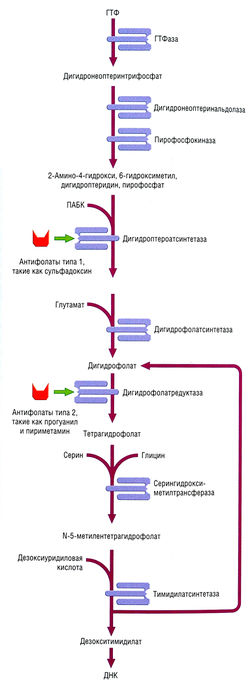
Поскольку антифолаты обоих типов ингибируют все стадии роста плазмодиев, их используют и для профилактики, и для лечения. Антифолаты действуют как споронтоциды, т.к. предотвращают процесс образования спорозоитов в организме комара. Смесь антифолатов типов 1 и 2 применяют против резистентного к хлорохину P. falciparum.
Сульфадоксин имеет длительный Т1/2, равный 120-200 час. Препарат менее эффективен против P. vivax по сравнению с P. falciparum. Комбинация сульфадоксина с пириметамином в соотношении 20 : 1 дает синергичный эффект, хотя это сочетание действует лишь на поздние стадии развития паразита в эритроцитах. По-видимому, его противомалярийное действие запаздывает по сравнению с хлорохином. Эта комбинация может вызвать системный васкулит, синдром Стивенса-Джонсона или токсический эпидермальный некролиз у пациентов, гиперчувствительных к сульфонамидам. В целях предосторожности его лучше не применять на поздних стадиях беременности, во время лактации и у новорожденных детей, чтобы избежать теоретически возможного развития ядерной желтухи.
Т1/2 сульфалена составляет 65 час; препарат часто используют в комбинации с пириметамином.
Т1/2 дапсона равен 25 час; препарат применяют главным образом в комбинации с пириметамином и в сочетании с профилактическим препаратом малопримом.
Ко-тримоксазол (триметоприм плюс сульфаметоксазол) представляет собой антибактериальную комбинацию, обладающую противомалярийной активностью.
Прогуанил (и его аналог хлорпрогуанил со значительно более длительным Т1/2) метаболизируется в печени с образованием активных метаболитов. Родительские соединения являются бигуанидами, которые перестраиваются в активные метаболиты циклогуанил и хлорциклогуанил соответственно. Эти метаболиты действуют как ингибиторы DHFR. Обнаружены две группы ферментов, метаболизирующих эти лекарства.
Так, метаболизм, осуществляемый ферментом печени CYP2C19, может быть либо интенсивным, либо слабым. Лица со слабым метаболизмом составляют 3-6% населения в Европе и Африке и 13-23% — в Азии.
Беспрецедентно высокое преобладание (71%) лиц с генотипом слабых метаболизаторов CYP2C19, характеризующегося плохим метаболизмом прогуанила, обнаружено на островах Вануату Восточной Меланезии. Исследования, проведенные на Вануату, показали также, что родительское соединение прогуанил обладает значительной активностью против малярии, вызываемой P. falciparum и P. vivax, независимо от метаболита циклогуанила.
Т1/2 прогуанила составляет 11-20 час. Он оказывает замедленное шизонтоцидное действие на эритроцитарные формы плазмодиев, однако высокоэффективен против внеэритроцитарных форм в печени и обладает споронтоцидным действием на P. falciparum. Благодаря его безопасности прогуанил (200 мг/сут) широко применяют в комбинации с хлорохином (300 мг/нед) в качестве каузального профилактического лекарства. Эту комбинацию можно использовать во время беременности.
Прогуанил как монотерапию уже не рекомендуют для лечения малярии, однако недавно вновь появился интерес к его применению в комбинации с сульфонами, сульфонамидами или атоваконом. В США препарат недоступен.
Т1/2 пириметамина равен 95 час. Его используют только в комбинации с сульфонамидами или сульфонами для профилактики и терапии ввиду широкого распространения резистентности к этому лекарству.
К сожалению, ген dhfr у P. falciparum спонтанно мутирует, обычно в результате воздействия лекарственных веществ. Этот ген сообщает паразиту резистентность к пириметамину и/или циклогуанилу. Резистентность к сульфадоксину возникает вследствие точковых мутаций в этом гене. Как пириметамин, так и сульфадоксин элиминируются из организма медленно, и после введения стандартной комбинации инициальная концентрация лекарственных веществ в плазме достигает уровня, до статочного для уничтожения большинства штаммов P. falciparum. Вслед за этим медленно снижается концентрация лекарств, и погибают лишь чувствительные штаммы, тем самым создавая условия для возникновения резистентных штаммов.
8-Аминохинолины[править | править код]
Более 100 лет лет назад было выявлено, что примахин, 8-аминохинолин, химически родственный красителю метиленовому синему, обладает активностью против малярийных паразитов.
Разнообразные противомалярийные 8-аминохи-нолины были синтезированы в основном в 1940-х гг., хотя все еще продолжают появляться новые вещества этой группы (например, тафенохин).
Плазмохин особенно активен против неразмно-жающихся стадий плазмодия (т.е. гаметоцитов и гипнозоитов). В настоящее время он является единственным доступным гаметоцидным препаратом в отношении P. falciparum и гипнозоитоцидным (антирецидивным) — для P. vivax и P. ovale.
Примахин принимают внутрь, т.к. при парентеральном введении он вызывает тяжелую гипотензию. Он обладает высокой биодоступностью. Вещество переходит через плаценту и экскретируется в грудное молоко, поэтому его нельзя использовать во время беременности и лактации. Примахин быстро распадается с образованием различных метаболитов, некоторые из них могут быть противомалярийными.
Однократной дозы примахина 30-45 мг достаточно для элиминации гаметоцитов P. falciparum, а 15 мг/сут в течение 14 сут убивают гипнозоитов и обеспечивают радикальное излечение от малярии, вызванной P. vivax и P. ovale. Примахин при пероральном применении пациенты переносят в целом хорошо, особенно представители европеоидной расы. Примахин может вызвать желудочный дискомфорт ограниченной степени.
Более серьезным расстройством является метгемоглобинемия. Самый тяжелый побочный эффект — острый внутрисосудистый гемолиз у пациентов с недостаточностью глюкозо-6-фосфатдегидрогеназы. Это сцепленный с Х-хромосомой наследственный дефект данного фермента эритроцитов у некоторых лиц, чаще встречающийся в определенных географических группах. Однако тяжелый гемолиз регистрируется редко.
Тафенохин, родственный примахину, имеет более высокий терапевтический индекс, чем примахин, и элиминируется гораздо медленнее (Т1/2 составляет около 14 сут). Первое из названных свойств делает тафенохин более безопасным лекарством, однако его терапевтическая эффективность до сих пор не установлена.
Антипаразитарное действие противомалярийных лекарств
- 4-Аминохинолины (например, хлорохин) концентрируются в лизосомах паразита, где переваривается гемоглобин
- Ариламиноалкоголи (например, хинин и мефлохин) действуют на паразитов, переваривающих гемоглобин
- Антифолаты (например, сульфадоксин, пириметамин и прогуанил) действуют на метаболизм фолатов паразита
- Антибиотики, в частности тетрациклин, ингибируют синтез рибосомных белков паразита
- Примахин особенно активен против гаметоцитов и гипнозоитов
- Артемизинин и его производные имеют конфигурацию пероксидов (триоксан), обусловливающую их действие
Наиболее тяжелые побочные эффекты противомалярийных лекарств
- Хлорохин и прогуанил в основном имеют умеренные побочные эффекты; могут быть относительно безопасными во время беременности
- Амодиахин: летальный агранулоцитоз
- Хинин: гипогликемия; применяют во время беременности при тяжелой малярии
- Мефлохин: острый психоз и преходящая энцефалопатия с судорогами
- Галофантрин: удлинение интервала QT на ЭКГ
- Сульфадоксин и пириметамин: синдром Стивенса-Джонсона
- Примахин: острый внутрисосудистый гемолиз у пациентов с недостаточностью глюкозо-6-фосфатдегидрогеназы
- Тетрациклин: нарушение развития костей и зубов у детей младше 8 лет
Антибиотики[править | править код]
Антибиотики (например, тетрациклин, доксициклин, клиндамицин; см. «Лекарства и бактерии» ) действуют не сразу, однако оказывают выраженный эффект на эритроцитарные стадии малярии. Все антибиотики относятся к ингибиторам синтеза рибосомных белков плазмодия:
- тетрациклин оказался полезным, дополняющим хинин средством против полирезистентного к лекарствам P. falciparum,
- доксициклин используют как супрессивное профилактическое средство, особенно в районах, где распространена резистентность плазмодиев к мефлохину (например, в Таиланде и Камбодже). Однако у некоторых пациентов доксициклин оказывает фотосенсибилизирующее действие. Тетрациклины противопоказаны во время беременности и лактации, а также для детей младше 8 лет, поскольку эти антибиотики могут вызвать расстройства оссификации костей и зубов.
Клиндамицин является синтетическим производным линкомицина; он оказался эффективным в лечении малярии, вызванной P. falciparum. Его можно использовать также в комбинации с хинином.
АРТЕМИЗИНИН И ЕГО ПРОИЗВОДНЫЕ. Артемизинин (хингхаосу) — сесквитерпеновый лактон, экстрагированный из травянистого растения Artemisia annua (полынь однолетняя). Его применяли в Китае как жаропонижающее средство более 2000 лет. Активный компонент выделен и описан в 1971 г. Ответственной за противомалярийную активность является его пероксидная структура (триоксан). Препарат применяют перорально и в виде суппозиториев, получено несколько полусинтетических производных. Общеупотребительные производные артемизинина — артеметер, артесунат и дигидроартемизинин (последний представляет собой основной метаболит артеметера и артесуната).
Клинические испытания артемизинина и его производных (артеметера, применяемого в/м, и артесуната, используемого перорально и в виде препаратов для в/в введения) показывают, что они представляют собой гематошизотропные (шизонтоцидные) вещества, быстро действующие на плазмодии, включая полирезистентные штаммы P. falciparum. Однако рецидивы являются обычным явлением.
Эти препараты имеют большое значение в лечении тяжелых и осложненных форм малярии, в том числе церебральной малярии. В Таиланде было установлено, что таблетки артесуната в комбинации с мефлохином были более эффективными против полирезистентного P. falciparum, чем артесунат или мефлохин в отдельности. Артемизинин и его производные оказывают выраженный эффект на гаметоцитогенез. Исследования, проведенные в Таиланде и на границе с Мьянмой, показывают, что препараты группы артемизинина могут уменьшать передачу инфекции и, соответственно, распространение резистентных штаммов.
Производные артемизинина в настоящее время занимают определенное место среди наиболее перспективных лекарственных средств в химиотерапии малярии вследствие их различной молекулярной структуры, быстро наступающего эффекта и относительной безопасности.
Новые противомалярийные лекарства[править | править код]
АРТЕМЕТЕР-ЛУМЕФАНТРИН. В ходе лечения малярии двумя различными препаратами вероятность появления мутантного штамма, резистентного к обоим веществам, можно рассчитать путем перемножения частот мутаций для каждого лекарства в отдельности. Артемизинин уменьшает биомассу плазмодиев примерно на 4 log (т.е. в 10 000 раз) в расчете на каждый бесполый цикл. Такое быстрое снижение имеет большое теоретическое значение, когда производные артемизинина используют в комбинации с другими противомалярийными препаратами, т.к. численность популяции, в которой могут возникать мутации по отношению ко второму лекарству, заметно уменьшается.
Лумефантрин представляет собой медленно выводимое из организма противомалярийное средство, применяемое перорально в виде раствора в линолевой кислоте. Однако его биодоступность заметно варьируется. Комбинацию лумефантрина с артеметером при их фиксированном количественном соотношении используют для лечения неосложненных инфекций, вызванных P. falciparum.
АТОВАКОН-ПРОГУАНИЛ. Противомалярийные свойства нафтохинонов были выявлены в середине 1940-х гг. Наиболее интересным соединением этой группы является гидроксинафтохинон (атовакон), убивающий резистентных паразитов P. falciparum. Один атовакон не применяют из-за высокой частоты рецидивов, однако его стандартная комбинация с прогуанилом позволяет предотвратить рецидивы.
ХЛОРПРОГУАНИЛ-ДАПСОН. Эта комбинация представляет собой новый способ применения двух уже известных лекарств и является возможной альтернативой комбинации сульфадоксин плюс пириметамин. Первая комбинация элиминируется быстрее, чем вторая, тем самым снижая риск развития резистентных штаммов. Кроме того, комбинация хлорпрогуанил плюс дапсон сохраняет активность против плазмодиев с мутациями гена dhfr в позициях 108, 51 и 59 и эффективна при лечении неосложненной малярии в Африке.
ПИРОНАРИДИН. Пиронаридин представляет собой основание, структурно родственное амодиахину, однако имеет иной механизм действия и другие побочные эффекты. Препарат, применяемый в настоящее время перорально, эффективен против полирезистентного P. falciparum и хорошо переносится пациентами, однако оральная биодоступность низкая.
Основные побочные эффекты пиронаридина: головная боль, головокружение, расстройства ЖКТ и преходящие изменения на ЭКГ.
Резистентность паразитов к противомалярийным лекарствам[править | править код]
Появление резистентных к хлорохину штаммов P. falciparum было впервые отмечено в Таиланде в 1959 г. и в Колумбии в 1960 г. Последующее быстрое распространение резистентных к хлорохину штаммов P. falciparum по всему миру стало серьезной проблемой, которая еще более осложнилась широким распространением плазмодия, резистентного к комбинации сульфадоксин плюс пириметамин и хинину.
В Юго-Восточной Азии и некоторых африканских странах существуют также штаммы P. falciparum, резистентные к мефлохину. Однако, несмотря на широкое распространение резистентных к хлорохину штаммов P. falciparum, а также недавнее появление резистентных к этому лекарству P. vivax в Папуа Новой Гвинее, хлорохин все еще остается широко применяемым во всем мире противомалярийным препаратом, что свидетельствует о серьезной необходимости поисков альтернативных противомалярийных средств.
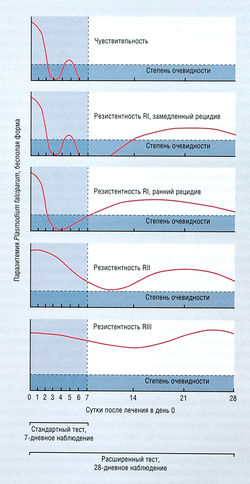
Резистентность паразитов к противомалярийным препаратам имеет разную степень выраженности, начиная от минимальной утраты эффективности лечения, что определяется только по удлинению рецидивов, и заканчивая высоким уровнем резистентности, когда препарат не дает супрессивного эффекта. В 1967 г. ВОЗ предложила классификацию степеней резистентности, основанную на реакции паразитов P. falciparum в ответ на обычно рекомендуемые дозы хлорохина (рис. 6.26). Эту систему классификации используют также для других гематошизотропных средств и других видов малярии у человека.