Стимуляторы серотониновых рецепторов
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Стимуляторы серотониновых рецепторов
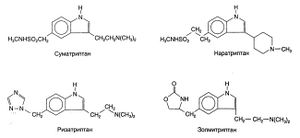
Как химическое строение, так и фармакологические свойства препаратов этой группы могут быть совершенно различными (табл. 11.4). Это и не удивительно при таком разнообразии серотониновых рецепторов. Применение избирательных стимуляторов 5-НТ1А-рецепторов помогло выяснить функцию этих рецепторов в головном мозге и привело к созданию нового класса транквилизаторов, в том числе буспирона, гепирона и ипсапирона (гл. 19). Избирательные 5-НТ1D-стимуляторы (например, суматриптан) обладают уникальной способностью вызывать сужение мозговых сосудов. Суматриптан стал первым из новейших стимуляторов серотониновых рецепторов, применяемых при мигрени (см. ниже). К другим препаратам данной группы, одобренных ФДА, относятся золмитриптан, наратриптан и ризатриптан. Все они избирательно стимулируют 5-НТ1D- и 5-НТ1В-рецепторы. Уже получены и продолжают разрабатываться большое количество избирательных стимуляторов 5-НТ4-рецепторов для лечения желудочно-кишечных нарушений (гл. 38). Все эти препараты подробно разбираются в главах, посвященных медикаментозному лечению тех или иных болезней.
Применение стимуляторов серотониновых рецепторов при мигрени
Мигренью страдают 10—20% населения. Нетрудоспособность от нее в США составляет около 64 млн дней в год. Несмотря на то что мигрень — это отдельный неврологический синдром, ее проявления многообразны. Наиболее частые ее формы — это: 1) мигрень без ауры или простая мигрень, 2) мигрень с аурой, или классическая мигрень (эта форма подразделяется, в свою очередь, на мигрень с типичной аурой, мигрень с длительной аурой, мигрень без головной боли и мигрень с внезапной аурой), 3) другие, более редкие формы. Аура может предшествовать головной боли на срок до 24 ч и часто сопровождается светобоязнью, гиперакузией, полиурией, поносом, нарушениями настроения и аппетита. Иногда возникает аура без последующей головной боли. Приступы мигрени могут длиться несколько часов или суток, чередуясь порой с довольно длительными межприступными интервалами. Частота приступов бывает самой разной, но обычно составляет от 4 в месяц до 1 в год.
Лечить мигрень сложно. Во-первых, реакции на лекарственные средства различаются не только у разных больных, но даже у одного и того же больного в разное время. Во-вторых, явно недостаточно изучен патогенез мигрени. Эффективность противомигренозных препаратов зависит от наличия или отсутствия ауры, длительности и тяжести приступа, а также неизвестных пока генетических и средовых факторов (Deleu et al., 1998). Особенностью мигрени, хотя и достаточно неопределенной и непостоянной, служит так называемая распространяющаяся депрессия — волна торможения, иррадиирующая по коре головного мозга от первичного очага. Этой волне сопутствует сужение сосудов, сменяющееся их расширением (Olesen et al., 1981). Сомнительно, однако, чтобы только этой сосудистой реакцией можно было объяснить местные отек и болезненность при пальпации, порой наблюдающиеся у больных.
В соответствии с представлениями о ведущей роли серотонина в патогенезе мигрени, при лечении ее приступов используют прежде всего стимуляторы серотониновых рецепторов. Представления эти основаны на следующих данных, полученных как на животных, так и на человеке: 1) концентрация серотонина в тромбоцитах и плазме меняется в зависимости от стадии приступа мигрени, 2) в большинстве случаев во время приступа концентрация серотонина и его метаболитов в моче повышена, 3) приступ можно спровоцировать резерпином, фенфлурамином и другими препаратами, вызывающими высвобождение биогенных аминов (в том числе серотонина) из внутриклеточных депо.
5-НТ1-стимуляторы (триптаны)
Появление препаратов этой группы — суматриптана, золмитриптана, наратриптана и ризатриптана — стало важным этапом как в исследовании, так и в лечении мигрени. Все они являются избирательными 5-НТ1-стимуляторами, и их применение в эксперименте позволило выяснить новые механизмы патогенеза мигрени. С клинической же точки зрения они не только эффективно уменьшают головную боль, но, в отличие от алкалоидов спорыньи, подавляют, а не усиливают тошноту и рвоту.
Историческая справка. Суматриптан стал первым противомигренозным средством, разработка которого была основана на экспериментальных данных о патогенезе мигрени. Эта разработка была начата в 1972 г. Хемпфри и сотр. (Humphrey et al., 1990). Целью их исследований было получить вещества, вызывающие избирательное сужение внечерепных сосудов головы (в то время была распространена сосудистая теория мигрени, согласно которой головная боль при мигрени возникает вследствие расширения артериовенозных анастомозов внечерепных артерий). Особое внимание авторы обратили на серотониновые рецепторы в сонных артериях — считалось, что эффект классических противомигренозных средств (например, алкалоидов спорыньи) обусловлен сужением артериовенозных анастомозов в системе этих артерий, а это сужение, в свою очередь, опосредовано активацией серотониновых рецепторов (Saxena, 1978). Хемпфри и сотр. получили множество производных серотонина и опробовали их действие на препаратах изолированных сосудов и в условиях In vivo. Наконец, в 1984 г. был синтезирован суматриптан, оказывающий мощный сосудосуживающий эффект на препарате подкожной вены собаки (Humphrey et al., 1990) — в этой вене, как считалось, имеются те же самые серотониновые рецепторы, что и в сонных артериях. В 1992 г. суматриптан в США был внедрен в клиническую практику, а в конце 1990-х гг. ФДА одобрило и применение трех других триптанов (Limmoth and Diener, 1998).
Химические свойства. Все триптаны представляют собой производные индола, замещенные в 3-й и 5-й позициях. Их структурные формулы приведены на рис. 11.5.
Фармакологические свойства. В отличие от алкалоидов спорыньи, триптаны действуют преимущественно на 5-НТ,-рецепторы (что указывает на роль этих рецепторов в патогенезе мигрени). Более того, эти средства избирательно активируют 5-НТ1в- и 5-НТ1D-рецепторы, а их сродство к другим серотониновым рецепторам либо низкое, либо отсутствует вовсе. На а1-, а2- и β-адренорецепторы, М-холинорецепторы, а также дофаминовые и бен-зодиазепиновые рецепторы триптаны не действуют. Эффективность триптанов и алкалоидов спорыньи в терапевтических дозах зависит от их сродства к 5-НТ,в- и 5-НТ1D-рецепторам, но не к 5-НТ1А- и 5-НТ1Е-рецепторам. Таким образом, можно полагать, что главной точкой приложения противомигренозных средств должны быть 5-НТ1в- и 5-НТ1D-рецепторы.
Механизмы действия. Существуют две гипотезы относительно эффективности стимуляторов 5-НТ1в- и 5-НТ1D-рецепторов при мигрени. Согласно одной из них, активация этих рецепторов приводит к сужению сосудов, в том числе — артериовенозных анастомозов. В соответствии же с распространенными представлениями о патогенезе мигрени, ее приступы обусловлены возникающим по неясной причине расширением артериовенозных анастомозов в системе сонных артерий. При этом до 80% крови сбрасывается по этим анастомозам (расположенным преимущественно в коже головы и в ушах), минуя капиллярное русло; это приводит к ишемии и, следовательно, гипоксии мозга. Значит, эффективный противомигренозный препарат должен вызывать сужение анастомозов, тем самым восстанавливая нормальный мозговой кровоток. Действительно, эрготамин, дигидроэрготамин и суматриптан оказывают именно такие влияния на сосуды, причем выраженность этих влияний коррелирует с активацией 5-НТ1в- и 5-НТ1D-рецепторов (den Boer etal., 1991).
Другая гипотеза основана на том, что указанные рецепторы располагаются преимущественно на пресинаптических окончаниях, регулируя высвобождение из этих окончаний медиаторов (рис. 11.3). Полагают, что 5-НТ1-стимуляторы могут подавлять выделение провоспалительных пептидов из нервных окончаний в околососудистое пространство. Так, введение капсаицина или одностороннее электрическое раздражение тройничного нерва приводят к деполяризации проходящих рядом с сосудами твердой мозговой оболочки аксонов, что сопровождается выходом из этих сосудов плазмы; на фоне же эрготамина, дигидроэрготамина и суматриптана пропотевание плазмы уменьшается (Moskowitz, 1992). Именно этим действием и объясняют эффективность противомигренозных средств.
Фармакокинетика. Максимальная сывороточная концентрация суматриптана достигается примерно через 12 мин после п/к введения и через 1—2 ч после приема внутрь. Его биодоступность при п/к введении составляет 97%, но при приеме внутрь или интраназально — лишь 14—17%. Т1/2 суматриптана — 1—2 ч. Его элиминация осуществляется преимущественно за счет ферментативного расщепления под действием МАО с последующим выведением метаболитов с мочой.
Максимальная сывороточная концентрация золмитриптана достигается через 1,5—2 ч после приема внутрь; биодоступность при этом составляет 40%. Золмитриптан превращается в активный N-деметилированный метаболит, сродство которого к 5-НТ1В- и 5-НТ1D-рецепторам в несколько раз выше, чем исходного препарата. Т1/2 и того, и другого — 2—3 ч.
Максимальная сывороточная концентрация наратриптана достигается через 2—3 ч после приема внутрь; биодоступность при приеме внутрь составляет 70%. Его действие среди всех триптанов самое длительное (Т1/2 около 6 ч). На 50% он выводится в неизмененном виде с мочой; еще около 30% выводится в виде продуктов окисления цитохромом Р450.
Максимальная сывороточная концентрация ризатриптана достигается через 1—1,5 ч после приема внутрь обычных таблеток (после приема рассасывающихся во рту таблеток —лишь через 1,6—2,5 ч); биодоступность при приеме внутрь составляет 45%. Главный путь элиминации — ферментативное расщепление под действием МАО.
Степень связывания с белками плазмы колеблется от 14% (суматриптан, ризатриптан) до 30% (наратриптан).
Побочные эффекты и противопоказания. 5-НТ1-стимуляторы оказывают редкие, но тяжелые побочные эффекты на сердце — спазм коронарных артерий, преходящую ишемию и даже инфаркт миокарда, предсердные и желудочковые аритмии. В большинстве случаев такие осложнения возникают у больных с факторами риска ИБС. Чаще же триптаны вызывают незначительные побочные эффекты. При п/к введении суматриптана хотя бы один из таких эффектов возникает у 83% больных; в большинстве случаев — боль, покалывание или жжение в области инъекции. Самый частый побочный эффект при интраназальном введении суматриптана — горький вкус во рту. При приеме внутрь триптаны могут вызвать парестезию, астению и утомляемость, приливы, чувство стеснения или боль в груди, боль в шее и нижней челюсти, сонливость, дурноту, тошноту, потливость.
Триптаны противопоказаны при ИБС, заболеваниях сосудов мозга или конечностей, других сердечно-сосудистых болезнях (в частности, артериальной гипертонии). Наратриптан противопоказан также при выраженной печеночной и почечной недостаточности. Ризатриптан при болезнях печени и почек не противопоказан, но должен назначаться с осторожностью. Наконец, суматриптан, ризатриптан и золмитриптан нельзя сочетать с ингибиторами МАО.
Применение при мигрени. Триптаны эффективны как средства для купирования приступов мигрени (независим от наличия ауры), но не для их профилактики. Лечение надо начинать как можно раньше после развития при ступа. Чаще всего триптаны назначают внутрь, но у больных с тошнотой и рвотой иногда лучше использовать иные пути введения. Примерно у 70% больных после п/к введения 6 мг суматриптана головная боль сильно облегчается. Если этого не происходит, то через 24 ч введение можно повторить. Суматриптан выпускается также в виде таблеток и аэрозоля для интраназального введения-последнем случае эффект развивается уже через 15 мин Внутрь суматриптан назначают в дозе 25—100 мг; спустя 2 ч прием можно повторить, но общая доза за 24 ч не должна превышать 300 мг. Интраназально вводят 5-20 мг; спустя 2 ч введение можно повторить, но общая доза за 24 ч не должна превышать 40 мг. Все остальные препараты назначают внутрь. Доза золмитриптана составляет 1,25—2,5 мг; спустя 2 ч прием можно повторить (но не более 10 мгза 24 ч). Доза наратриптана —1—2,5 мг прием можно повторить не ранее чем спустя 4 ч, а общая доза за 24 ч не должна превышать 5 мг. Наконец, ризатриптан принимают в дозе 5—10 мг; спустя 2 ч прием можно повторить, но общая доза за 24 ч не должна превышать 30 мг. Не известно, насколько безопасно применять триптаны при частых приступах (3—4 раза в месяц). Поскольку они вызывают быстрое (хотя и не очень выраженное) повышение АД, их не следует назначать при артериальной гипертонии с нестабилизированным АД. Время между приемом разных триптанов или приемом триптанов и алкалоидов спорыньи не должно быть меньше 24 ч.
Алкалоиды спорыньи
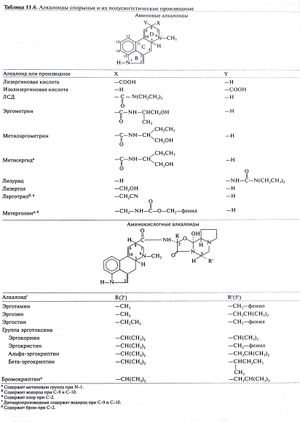
Способность спорыньи вызывать прерывание беременности была известна более 2 тысяч лет назад, но лишь в начале XX века были выделены ее алкалоиды, раскрыто их строение и началось изучение механизмов их действия. Эти работы стали важной вехой в развитии современной фармакологии. Эффекты этих веществ сложны и разнообразны (табл. 11.5), что ограничивает их клиническое применение. В целом можно сказать, что эффекты эти сводятся к стимуляции либо блокаде адренорецепторов, дофаминовых и серотониновых рецепторов. Конечные реакции на алкалоиды спорыньи зависят от природы препарата, его дозы, физиологического состояния и эндокринного статуса, конкретного органа или ткани, а в условиях эксперимента — еще и от методики и вида животного.
Историческая справка. Спорынья (маточные рожки) — это покоящаяся стадия гриба Claviceps purpurea, паразитирующего на завязи ржи и других злаков. В течение многих столетий были известны отравления, в том числе смертельные, вызванные зараженным этим грибом хлебом. В ассирийских письменах IX века до нашей эры можно найти упоминание о «тлетворных нарывах на колосьях». Первые описания отравления спорыньей появились в средние века: в этих описаниях говорилось об эпидемиях странных болезней, при которых возникала гангрена рук и ног. В тяжелых случаях ткани становились черными и сухими, затем конечности мумифицировались и наступала их самоампутация. Считалось, что человека пожирает «божий огонь» — кожа как будто обугливалась, а больной испытывал нестерпимое жжение. Болезнь получила также название «антонова огня» по имени святого Антония: считалось, что в его обители может наступить исцеление. Возможно, так оно и было, например паломники в этой обители могли получать продукты, не зараженные спорыньей. Известны были и другие симптомы отравления, например прерывание беременности. Во всяком случае, как маточное средство спорынья стала применяться гораздо раньше, чем была установлена ее связь с «антоновым огнем».
Таблица 11.5. Фармакологические эффекты некоторых алкалоидов спорыньи
|
Препарат |
Эффекты | ||
|
Серотониновые рецепторы |
Дофаминовые рецепторы |
Альфа-адренорецепторы | |
|
Эрготамин |
В некоторых сосудах — частичный агонист; в различных гладкомышечных органах — неизбирательный блокатор; в ЦНС — слабый стимулятор или блокатор |
Существенных влияний на ЦНС или периферические органы не выявлено, но при в/в введении оказывает сильное рвотное действие |
Частичный агонист или блокатор в кровеносных сосудах и других гладкомышечных органах; в периферической и центральной нервной системе — преимущественно блокатор |
|
Дигидроэрготамин |
Частичный агонист или блокатор в некоторых гладкомышечных органах; в латеральном коленчатом теле, возможно, стимулятор |
Неизбирательный блокатор в симпатических ганглиях; слабое рвотное действие |
Частичный агонист в венах; блокатор в других кровеносных сосудах и гладкомышечных органах, периферической и центральной нервной системе |
|
Бромокриптин |
Известно лишь о слабом блокирующем действии |
Частичный агонист или блокатор в различных отделах ЦНС; возможно, стимулятор в дофаминер-гических нейронах, подавляющие секрецию пролактина; рвотное действие слабее, чем у эрготамин; |
Стимулирующего действия не оказывает; в различных тканях несколько менее активный блокатор, ; чем дигидроэрготамина |
|
Эргометрин и метилэргометрин |
Частичные агонисты в сосудах пуповины и плаценты человека; избирательные и довольно активные блокаторы в различных гладкомышечных органах; частичные агонисты или блокатор в некоторых отделах ЦНС |
Слабые блокаторы в некоторых сосудах; частичные агонисты ил] блокаторы в некоторых отделах ЦНС; рвотное действие и торможение секреции пролактина слабее, чем у бромокриптина |
Частичные агонисты в кровеносных сосудах (менее активные, чем эрготамин); блокирующее действие слабое |
|
Метисергид |
Частичный агонист или блокатор в некоторых кровеносных сосудах и отделах ЦНС; избирательный и очень мощный блокатор некоторых периферических тканях и отделах ЦНС |
Данных о блокирующем или стимулирующем действии мало; - рвотным действием не обладает в |
Блокирующее и стимулирующее действие слабое или отсутствует |
Химические свойства. Алкалоиды спорыньи — это производные тетрациклического соединения 6-метилэрголина(табл. 11.6), у которых имеется двойная связь в кольце D и заместитель в β-конфигурации в положении 8. В качестве лекарственных средств из природных алкалоидов применяются амиды лизергиновой кислоты. Первым из алкалоидов спорыньи в чистом виде был выделен эрготамин (в 1920 г.). В 1932 г. был выделен эргометрин. Посредством ферментативной гидрогенизации природных алкалоидов спорыньи были получены многочисленные полусинтетические препараты, например дигидроэрготамин. Синтетическое производное бромокриптин (2-бром-а-эргокриптин) применяют для подавления секреции пролактина (гл. 56); это его действие обусловлено стимуляцией дофаминовых рецепторов. К другим веществам этого ряда относятся, в частности, мощный галлюциноген ЛСД и блокатор серотониновых рецепторов метисергид. Оба обсуждаются ниже.
Фармакокинетика. Подробно фармакокинетические свойства алкалоидов спорыньи рассмотрены в обзоре Perrin (1985). Эрготамин после приема внутрь в крови почти не обнаруживается из-за элиминации при первом прохождении через печень. При приеме под язык его биодоступность также часто недостаточна да оказания эффекта. Считается, что кофеин повышает степень и скорость всасывания эрготамина, однако даже при этом биодоступность последнего, видимо, не превышает 1%. При использовании эрготамина в свечах его биодоступность выше.
Пути печеночного метаболизма эрготамина изучены плохо. На 90% его метаболиты выделяются с желчью. В неизмененном виде эрготамин содержится в кале и моче в следовых концентрациях. Т1/2 эрготамина составляет около 2 ч, но его сосудосуживающий эффект длится 24 ч и больше. Дигидроэрготамин всасывается хуже, а элиминируется быстрее — видимо, из-за еще более интенсивного печеночного метаболизма.
Эргометрин и метилэргометрин быстро всасываются из ЖКТ; их максимальная сывороточная концентрация достигается через 1—1,5 ч и превышает максимальную сывороточную концентрацию при приеме эквивалентных доз эрготамина более чем в 10 раз. Через 10 мин после приема внутрь в дозе 0,2 мг эргометрин вызывает сокращение матки у родильниц. Если судить по продолжительности действия, то эргометрин должен элиминироваться быстрее, чем эрготамин. Т1/2 метилэргометрина составляет 0,5—2 ч.
Применение при мигрени. Эффективность алкалоидов спорыньи при мигрени была обнаружена в 1920-х гг. С тех пор и по наши дни они применяются для купирования приступов этого заболевания. Их недостатком является неизбирательность — они действуют на 5-НТ,- и 5-НТ2-рецепторы, а также на адренорецепторы и дофаминовые рецепторы. Так, дигидроэрготамин конкурирует с мечеными лигандами за все подтипы 5-НТ1-рецепторов, а также за 5-НТ2А- и 5-НТ2в-рецепторы, D2-peцeпторы, а1- и а2-адренорецепторы. Все эти многочисленные эффекты затрудняют понимание механизмов действия алкалоидов спорыньи при мигрени. С учетом эффектов триптанов — стимуляторов 5-НТ1В- и 5-HT1D-рецепторов (см. выше) — можно предположить, что именно действием на эти рецепторы объясняется эффективность алкалоидов спорыньи как средств для купирования приступов мигрени. С другой стороны, производное спорыньи метисергид является преимущественно блокато-ром серотониновых рецепторов и используется для профилактики этих приступов (см. ниже).
Алкалоиды спорыньи следует назначать либо при частых, но умеренных, либо при редких, но тяжелых приступах. Как и другие средства для купирования приступа мигрени, их надо принимать как можно быстрее после начала головной боли. Их всасывание в ЖКТ непостоянно, и может быть, именно этим объясняется непостоянство их эффектов. Поэтому в США применяются препараты для приема под язык (эрготамин) либо для интраназапьного введения и инъекций (дигидроэрготамин). Эрготамин назначают в дозе 2 мг под язык; прием можно повторять с интервалами в 30 мин, но общая доза за 24 ч не должна превышать 6 мг, а за неделю — 10 мг. Дигидроэрготамин вводят в/в, n/к или в/м по 1 мг; введение можно повторять с интервалами в 1 ч, но не более 2 мг в/в (3 мг п/к или в/м) за 24 ч и 6 мг — за неделю. Интраназально вводят 0,5 мг (1 впрыскивание) в каждую ноздрю; при необходимости введение повторяют через 15 мин (при этом общая доза становится 2 мг, то есть 4 впрыскивания). Не установлено, насколько безопасно превышать общую дозу 3 мг за 24 ч или 4 мг за неделю.
Побочные эффекты и противопоказания. Примерно у 10% больных эрготамин вызывает тошноту и рвоту, обусловленные прямым действием на рвотный центр. Впрочем, оценить истинную распространенность этого побочного эффекта сложно, так как тошнота и рвота — частые спутники приступов мигрени. Нередко наблюдается слабость в ногах, порой в руках и ногах возникают боли, в отдельных случаях тяжелые. Другие проявления так называемого эрготизма (синдрома, возникающего при отравлении спорыньей) — онемение и покалывание в пальцах рук и ног. Описаны ангинальные боли и преходящие тахикардия либо брадикардия — видимо, обусловленные вызванным эрготамином спазмом коронарных артерий. Возможны местный отек и зуд, не требующие отмены эрготамина. При развитии же явного эрготизма препарат отменяют и назначают симптоматическое лечение, направленное на нормализацию гемодинамики — антикоагулянты, низкомолекулярные декстраны и мощные вазодилататоры (например, нитропрусс ид натрия). Дигидроэрготамин оказывает меньший эффект на сосуды и матку и реже вызывает рвоту.
При беременности или возможной беременности алкалоиды спорыньи не назначают — они могут оказать отрицательное действие на плод и вызвать прерывание беременности. Кроме того, они противопоказаны при ИБС, заболеваниях периферических сосудов, артериальной гипертонии, почечной и печеночной недостаточности, сепсисе. Алкалоиды спорыньи нельзя применять вместе с другими сосудосуживающими средствами. Промежуток времени между приемом алкалоидов спорыньи и триптанов должен быть не меньше 24 ч.
Применение при послеродовом кровотечении. Все природные алкалоиды спорыньи усиливают сокращения матки. При применении малых доз нарастают частота и сила сокращений, но расслабление бывает полным. Большие дозы вызывают еще более сильные и длительные сокращения, сопровождающиеся неполным расслаблением — вплоть до постоянной контрактуры. Из-за этих особенностей алкалоиды спорыньи не могут применяться для стимуляции родовой деятельности, но вполне пригодны для остановки маточных кровотечений и повышения тонуса матки после родов или аборта. Беременная матка чрезвычайно чувствительна к этим препаратам, и поэтому даже малые их дозы сразу после родов вызывают выраженную реакцию со стороны ее мускулатуры, не оказывая при этом каких-либо существенных побочных эффектов. В современной акушерской практике алкалоиды спорыньи используют прежде всего для остановки послеродовых кровотечений. Действие препаратов этой группы на матку отличается в основном количественно. Эргометрин в этом отношении более активен, чем эрготамин, а также менее токсичен. Поэтому в качестве маточных средств сегодня применяют эргометрин и его полусинтетическое производное метилэргометрин.
ЛСД
Из всех неизбирательных стимуляторов серотониновых рецепторов ЛСД привлекает наибольшее внимание. В дозах всего 1 мкг/кг он резко меняет поведение человека, вызывает расстройства восприятия (особенно зрительного и слухового) и галлюцинации. Этим объясняется как его употребление наркоманами (гл. 24), так и огромный интерес со стороны исследователей. Химическая структура ЛСД приведена в табл. 11.6.
ЛСД был впервые получен Альбертом Гоффманом, случайно употребившим этот препарат и обнаружившим в результате его необычные свойства. Предшественник ЛСД — алкалоид спорыньи лизергиновая кислота — галлюциногенными свойствами не обладает. В состав молекулы ЛСД входит индолалкил-аминовый остаток, и поэтому уже в ранних работах было высказано предположение о том, что ЛСД может действовать на серотониновые рецепторы. Вскоре было показано, что ЛСД действительно является стимулятором или частичным агонистом серотониновых рецепторов головного мозга. ЛСД стимулирует 5-НТ1А-ауторецепторы на телах серотонинергических нейронов шва ствола мозга, существенно снижая частоту импульсации этих нейронов. Влияние ЛСД и серотонина на эти нейроны примерно одинаково, но в тех мозговых структурах, где заканчиваются серотонинергические волокна (например, подкорковых зрительных центрах), серотонин гораздо активнее (Aghajanian et al., 1987). Именно таким неодинаковым действием на тела серотонинергических нейронов и на иннервируемые этими нейронами структуры может объясняться необычное влияние ЛСД на зрительное восприятие. Данные опытов с применением метода выбора препарата (этот метод, как полагают, дает возможность судить о субъективном компоненте реакций животных на психотропные средства) позволяют предположить, что стремление к ЛСД и другим галлюциногенам обусловлено активацией 5-НТ2А-рецепторов (Glennon, 1990). Это согласуется и с результатами исследований сопряженной с рецепторами фосфоинози-тидной системы, в которых было показано, что ЛСД и другие галлюциногены являются стимуляторами или частичными агонистами 5-НТ2А- и 5-НТ2с-рецепггоров. Пока нет ответа на важный вопрос о том, в какой степени влияние галлюциногенов на поведение также обусловлено стимуляцией 5-НТ2С-рецепторов. ЛСД взаимодействует и со многими другими серотониновыми рецепторами, включая недавно клонированные рецепторы с невыясненной функцией. С другой стороны, галлюциногенные производные фенилэтиламина, например 1-(4-бром-2,5-диме-токсифенил)-2-аминопропан, — это избирательные стимуляторы 5-НТм- и 5-НТ2С-рецепторов. Данные исследований на добровольцах позволяют утверждать, что наше понимание механизмов действия галлюциногенов существенно продвинулось. В таких исследованиях можно проверять на человеке гипотезы, высказанные на основании опытов на животных. Так, методом по-зитронно-эмиссионной томографии (Vollenweider et al., 1997) было показано, что характер активации мозга после приема галлюциногена псилоцибина во многом такой же, как у галлюцинирующих больных шизофренией. Как и в опытах на животных, этот эффект псилоцибина блокировался предварительным введением блокаторов 5-HT2a- и 5-НТ2С-рецепторов (Vollenweider etal., 1998).
8-гидрокси-(2-N,N-дипропиламин)-тетралин и другие препараты с избирательным действием на 5-НТ1А-рецепторы. 8-гидрокси-(2-N,N-дипропиламин)-тетрапин — это избирательный 5-НТ 1А-стимулятор, служащий ценным средством для научных исследований. Его структурная формула следующая:
Он не действует ни на другие 5-НТ1-рецепторы, ни на 5-НТ2-, 5-HT3- и 5-НТ4-рецепторы. 8-гидрокси-(2-N,N-дипропиламин)-тетралин стимулирует 5-НТ1А-ауторецепторы серотонинергических нейронов шва ствола мозга, снижая частоту импульсации этих нейронов. Кроме того, он стимулирует постсинаптические 5-НТ)А-реиепторы в иннервируемых этими нейронами структурах (например, в гиппокампе), также оказывая при этом тормозное действие.
Некоторые длинноцепочечные арилпиперазины (буспирон, гепирон, ипсапирон) являются избирательными частичными агонистами 5-НТ1А-рецепторов; другие близкие к ним арилпиперазины — их блокаторами. Первый из препаратов этой серии — буспирон — оказался довольно эффективным транквилизатором (гл. 19). Однако больные часто предпочитают применять при тревожности бензодиазепиновые транквилизаторы — видимо, потому, что они, в отличие от буспирона, обладают не только анксиолитическим, но и седативным действием. Гепирон и ипсапирон разработаны для лечения не только тревожных расстройств, но и депрессии.
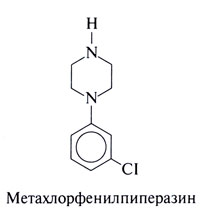
Метахлорфенилпиперазин
Эффекты метахлорфенилпиперазина (структурная формула приведена ниже) in vivo обусловлены в основном активацией 5-НТ1В-рецепторов, а возможно, также и 5-НТ2A- и 5-НТ2С-рецепторов (хотя в опытах со связыванием меченых лигандов in vitro такой избирательности не выявлено). Это вещество является активным метаболитом антидепрессанта тразодона.
Метахлорфенилпиперазин широко использовался для изучения роли серотониновых рецепторов головного мозга у человека. Он влияет на многие нейроэндокринные процессы и оказывает выраженные эффекты на психику, главный из которых — тревожность (Murphy, 1990). Метахлорфенилпиперазин усиливает секрецию кортизола и пролактина — возможно, путем активации 5-НТ1-, 5-НТ2A- и 5-НТ2с-рецепторов. Кроме того, он повышает выработку СТГ, но это влияние, видимо, не связано с се-ротониновыми рецепторами. Вызываемая метахлорфе-нилпиперазином тревожность, возможно, частично обусловлена активацией 5-HT2a- и 5-НТ2С-рецепторов, так как их блокаторы эту тревожность уменьшают. Данные опытов на животных позволяют предположить, что в развитии вызываемой метахлорфенилпиперазином тревожности в большей степени играют роль 5-НТ2С-рецепторы.