Пероральные сахаропонижающие средства
Содержание
Пероральные сахаропонижающие средства
Историческая справка
Если к открытию инсулина привели целенаправленные поиски, то производные сульфанилмочевины были обнаружены случайно. В 1942 г. М. Жанбон с коллегами заметили, что некоторые сульфаниламиды вызывают у экспериментальных животных гипогликемию. Они продолжили эксперименты с этими соединениями, и в скором времени появилось первое производное сульфанилмочевины для лечения сахарного диабета — карбутамид (1 -бутил-3-сульфанилмочевина). Этот препарат был позже изъят из продажи из-за побочного действия на костный мозг, однако он стал родоначальником новой группы лекарственных средств. Клинические испытания толбутамида — первого препарата этой группы, нашедшего широкое применение, — на больных инсулинонезависимым сахарным диабетом были начаты в начале 1950-х гг. С тех пор появилось около 20 производных сульфанилмочевины, которые широко используются во всем мире.
В 1997 г. для клинического применения был разрешен первый представитель еще одной группы пероральных сахаропонижающих средств — мегпитинидов (производных бензойной кислоты). Этот препарат, репаглинид, действует быстро и уменьшает постпрандиальную гипергликемию, если его принимают перед едой. Подобно производным сульфанилмочевины, меглитиниды стимулируют секрецию инсулина.
В начале XIX века в растении Galega officinalis (козлятник лекарственный), которым в средние века лечили сахарный диабет, был обнаружен алкалоид галегин (изоамиленгуанидин). Он снижал уровень глюкозы в крови, но оказался слишком токсичным для клинического применения. В 1920-х гт. сахарный диабет пробовали лечить бигуанидами, но из-за открытия инсулина эти попытки отошли на второй план. Позднее выяснилось, что слабым сахаропонижающим действием обладает противомалярийный препарат прогуанил. Бигуаниды были внедрены в клиническую практику вскоре после производных сульфанилмочевины. Первый бигуанид — фенформин — часто вызывал лакта-цидоз, вследствие чего был изъят из продажи в США и в Европе. Другой препарат этой группы — метформин — не оказывал тяжелых побочных эффектов и широко использовался в Европе, но в США был разрешен к применению только в 1995 г.
Производные тиазолидиндиона появились в 1997 г. Подобно бигуанидам, эта группа препаратов повышает чувствительность тканей к инсулину. Они связываются с внутриклеточными рецепторами, активируемыми индукторами пероксисом (так называемыми PPAR-рецепторами, особенно с PPARy-рецептора-ми), что стимулирует захват глюкозы мышцами и снижает продукцию глюкозы. Первый из препаратов этой группы, трогли-тазон, оказался гепатотоксичным и в 2000 г. в США был запрещен. Два других — розигпитазон и пиоглитазон — токсическим действием на печень не обладают и применяются во всем мире.
Производные сульфанилмочевины
Строение
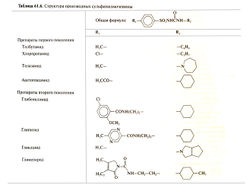
Производные сульфанилмочевины принято делить на два поколения. Ихструктурапоказана в табл.61.6.
Все препараты представляют собой замещенные производные арилсульфанилмочевины, различаясь радикалами в пара-положении бензольного кольца и у атома азота в остатке мочевины. К первому поколению относятся толбутамид, ацетогексамид, толазамид и хлорпропамид. Представители второго поколения производных сульфанилмочевины — глибенкламид, Гликлазид (Диабетон МВ) (часто применяется в бодибилдинге), гликлазид и глимепирид — обладают намного более сильным действием, чем препараты первого поколения.
Механизм действия
Производные сульфанилмочевины снижают уровень глюкозы в крови, стимулируя секрецию инсулина р-клетками. Однако при сахарном диабете действие этих препаратов данным эффектом не ограничивается. У больных инсулинонезависимым сахарным диабетом производные сульфанилмочевины поначалу усиливают секрецию инсулина поджелудочной железой и, кроме того, снижают печеночный клиренс инсулина, еще более увеличивая уровень этого гормона в крови. В первые месяцы лечения концентрация инсулина в плазме натощак и секреция инсулина в ответ на прием глюкозы внутрь возрастают. В дальнейшем концентрация инсулина падает до исходной, которая была перед началом лечения, но, несмотря на это, уровень глюкозы в плазме остается пониженным. Почему так происходит, не ясно. Возможно, пониженный уровень глюкозы способствует более сильному действию инсулина на ткани-мишени. Не исключено также, что хроническая гипергликемия сама по себе нарушает секрецию инсулина, оказывая токсическое действие на β-клетки.
При длительном лечении производными сульфанилмочевины их первоначальный стимулирующий эффект на секрецию инсулина пропадает. Полагают, что это обусловлено уменьшением числа рецепторов сульфанилмочевины на β-клетках. Если лечение приостановить, реакция β-клеток на введение препарата восстанавливается. Производные сульфанилмочевины, кроме того, стимулируют секрецию соматостатина и, по-видимому, слегка подавляют секрецию глюкагона (Krall, 1985).
Ген рецептора сульфанилмочевины клонирован. Сам рецептор представляет собой субъединицу АТФ-зависи-мого калиевого канала. Связывание производных сульфанилмочевины с рецепторами приводит к уменьшению проводимости этих каналов (Aguilar-Bryan et al., 1995; Philipson and Steiner, 1995). Действие препаратов напоминает действие физиологических стимуляторов секреции инсулина (в частности, глюкозы и лейцина), которые тоже снижают проводимость АТФ-зависимых калиевых каналов (Ribalet and Ciani, 1987; Boyd, 1988). Уменьшение выходящего калиевого тока приводит к деполяризации мембраны и входу кальция в клетки через потенциалзависимые кальциевые каналы.
По вопросу о том, обладают ли производные сульфанилмочевины внепанкреатическим действием, существуют разногласия (Beck-Nielsen, 1988). У больных инсулинонезависимым сахарным диабетом, получающих эти препараты, увеличивается плотность рецепторов инсулина на моноцитах, липоцитах и эритроцитах (Olefeky and Reaven, 1976). Производные сульфанилмочевины усиливают эффект инсулина в культуре клеток и стимулируют синтез белков — переносчиков глюкозы (Jacobs et al., 1989). Кроме того, данные препараты подавляют глюконеогенез в печени (Blumenthal, 1977); не понятно, правда, то ли это непосредственный эффект производных сульфанилмочевины, то ли результат повышения чувствительности к инсулину. Попытки объяснить долговременное действие производных сульфанилмочевины повышением чувствительности тканей-мишеней к инсулину остаются малоубедительными, поскольку этот эффект теряется на фоне прямого сахаропонижающего эффекта, обусловленного стимуляцией секреции инсулина. Внепан-креатические эффекты производных сульфанилмочевины действительно имеют место, но в лечении инсулинонезависимого сахарного диабета они играют незначительную роль. Фармакокинетика. Производные сульфанилмочевины обладают сходным спектром действия, но существенно различаются по фармакокинетике (Приложение II). Все препараты хорошо всасываются из ЖКТ, хотя скорость всасывания у них неодинакова. Прием пищи и гипергликемия замедляют всасывание (гипергликемия подавляет моторику желудка и кишечника, тормозя всасывание многих веществ). Принимая во внимание время достижения терапевтической концентрации в крови, препараты с коротким Т1/2 следует назначать за 30 мин до еды. В плазме производные сульфанилмочевины на 90—99% связаны с белками, главным образом с альбумином. Связывание с белками плазмы наименее выражено у хлорпропамида, наиболее — у глибенкламида. Объем распределения большинства препаратов составляет около 0,2 л/кг.
Производные сульфанилмочевины первого поколения значительно различаются по Т1/2 и метаболизму. Т1/2 аце-тогексамида короток, но препарат восстанавливается до активного метаболита с Т1/2, составляющим 4—7 ч, как у толбутамида и толазамида. Суточные дозы этих препаратов нередко приходится делить на несколько приемов.
Хлорпропамид имеет длинный Т1/2 (24—48 ч). Производные сульфанилмочевины второго поколения примерно в 100 раз активнее, чем препараты первого поколения (Le-bovitz and Feinglos, 1983). Обладая короткими Т1/2 (3—5 ч), они тем не менее оказывают сахаропонижающее действие на протяжении 12—24 ч. Поэтому многие из них достаточно принимать один раз в сутки. Причина несоответствия между Т1/2 и длительностью эффекта не ясна.
Все производные сульфанилмочевины метаболизиру-ются в печени, и их метаболиты выводятся почками. Хлорпропамид метаболизируется не полностью, примерно 20% его выводится в неизмененном виде. При почечной и печеночной недостаточности производные сульфанилмочевины назначают с осторожностью.
Побочные эффекты
Побочные эффекты производных сульфанилмочевины редки. Они наблюдаются примерно у 4% больных, принимающих препараты первого поколения, и немного реже — у принимающих препараты второго поколения (Paice et al., 1985). Как и следовало ожидать, производные сульфанилмочевины иногда вызывают гипогликемию, в том числе гипогликемическую кому (Femerand Neil, 1988; Seltzer, 1989). Особенно часто от этого страдают пожилые больные с почечной или печеночной недостаточностью, принимающие препараты с большим Т1/2 Чем длиннее Т)/2 препарата, тем выше риск гипогликемии. У пожилых тяжелая гипогликемия иногда проявляется неврологическими нарушениями, напоминающими инсульт, и требует неотложного вмешательства. Многие из этих больных нуждаются во в/в инфузии глюкозы на протяжении 24—48 ч (в связи с длинным Т|/2 принимаемого производного сульфанилмочевины). У каждого пожилого больного с признаками нарушения мозгового кровообращения нужно проверять уровень глюкозы плазмы.
Действие производных сульфанилмочевины, особенно первого поколения, усиливают очень многие лекарственные средства, тормозящие их метаболизм или экскрецию. Некоторые препараты вытесняют производные сульфанилмочевины из соединения с белками плазмы и таким образом увеличивают концентрацию свободных активных веществ в крови (Seltzer, 1989). К ним относятся сульфаниламиды, клофибрат, дикумарол, салицилаты и фенилбутазон. Другие препараты, а также этанол усиливают действие производных сульфанилмочевины, так как сами по себе снижают уровень глюкозы в крови.
Побочные эффекты производных сульфанилмочевины помимо гипогликемии включают тошноту и рвоту, холе-статическую желтуху, агранулоцитоз, апластическую и гемолитическую анемию, сыпь и системные аллергические реакции. У 10—15% принимающих эти препараты, особенно хлорпропамид, при употреблении спиртных напитков отмечается антабусная реакция (гл. 18). Производные сульфанилмочевины иногда вызывают гипонатриемию, усиливая действие АДГ на собирательные трубочки (Paice et al., 1985). Этот побочный эффект наблюдается почти у 5% больных; при лечении хлорпропамидом — чаше, чем при использовании других препаратов, при лечении гли-бенкламидом и глипизидом — реже. Данное свойство производных сульфанилмочевины позволяет применять их для лечения легких форм несахарного диабета (гл. 29).
Долгие споры идут о том, увеличивают ли производные сульфанилмочевины смертность от сердечно-сосудистых заболеваний. Увеличение смертности впервые было продемонстрировано в крупном кооперированном испытании «Университетская программа изучения сахарного диабета» (University Group Diabetes Program — UGDP), где сравнивали влияние диетотерапии, пероральных сахаропонижающих средств (толбутамида и фенформина) и инсулинотерапии на риск сердечно-сосудистых осложнений инсулинонезависимого сахарного диабета. За восьмилетний период наблюдения смертность от сердечно-сосудистых заболеваний среди принимающихтолбутамид оказалась в 2 раза выше, чем у получающих плацебо или инсулинотерапию (Meinert et al., 1970). В течение 10 лет шли споры, принимать ли этот результат во внимание, поскольку он был получен неожиданно, исследование не планировалось специально для проверки данного вопроса, а увеличение смертности отмечалось не во всех клиниках — участницах исследования, а только в трех из них. Более позднее проспективное исследование «Сахарный диабет в Великобритании* (UK Prospective Diabetes Study Group, 1998a) продемонстрировало, что на протяжении 14лет лечения производными сульфанилмочевины как первого, так и второго поколения смертность от сердечно-сосудистых заболеваний не повышается.
Применение
Производные сульфанилмочевины используют для нормализации уровня глюкозы в крови у больных инсулинонезависимым сахарным диабетом, которым не помогает диетотерапия. Однако отменять диетотерапию при назначении этих препаратов нельзя, поскольку она увеличивает эффективность медикаментозного лечения. Некоторые врачи по-прежнему предпочитают инсулинотерапию пероральным сахаропонижающим средствам. Производные сульфанилмочевины лучше всего помогают тем больным инсулинонезависимым сахарным диабетом, которым для устранения гипергликемии требуются низкие дозы инсулина (менее 40 ед/сут), а также больным с ожирением и больным старше 40 лет. Противопоказаниями для назначения этих препаратов служат инсулинозависимый сахарный диабет, беременность, лактация, выраженная почечная и печеночная недостаточность.
При правильном отборе больных производные сульфанилмочевины оказывают первоначальный эффект в 50—80% случаев (Krall, 1985). Все препараты равноэффективны. Уровень глюкозы в плазме у многих больных не возвращается к норме, но снижается настолько, что симптомы гипергликемии пропадают. С учетом того что хронические осложнения сахарного диабета обусловлены главным образом гипергликемией, целью лечения должна быть нормализация уровня глюкозы в плазме как натощак, так и после приема пищи. Примерно у 5—10% больных через год лечение перестает быть эффективным, о чем свидетельствует неприемлемо высокий уровень глюкозы в плазме. Это происходит в результате изменения метаболизма препарата, прогрессирующей дисфункции р-клеток или нарушения диеты. Еще одна причина — пропущенный диагноз латентного аутоиммунного диабета взрослых (медленнопрогрессирующего инсулинозависимого сахарного диабета). Назначение дополнительного перорального сахаропонижающего средства может исправить ситуацию, но подавляющему большинству таких больных рано или поздно все равно требуется инсулин.
Начальная суточная доза толбутамида составляет 500 мг, максимальная суточная доза — 3000 мг. Для ацетогексамида эти дозы составляют соответственно 250 и 1500 мг. Толазамид и хлорпропамид обычно назначают в суточной дозе 100—250 мг; максимальная суточная доза толазамида — 1000 мг, хлорпропами-да — 750 мг. Толбутамид, ацетогексамид и толазамид часто назначают в 2 приема, за 30 мин перед завтраком и ужином. Начальная суточная доза глибенкламида составляет 2,5—5 мг, максимальная суточная доза — 20 мг. Лечение глипизидом обычно начинают с приема 5 мг 1 раз в сутки. Максимальная суточная доза этого препарата составляет 40 мг; суточные дозы свыше 15 мг назначают в 2 приема. Начальная суточная доза гликлази-да — 40—80 мг, максимальная — 320 мг*. Лечение глимепиридом начинают с приема 0,5 мг 1 раз в сутки; максимальная суточная доза этого препарата — 8 мг. Лечение производными сульфанилмочевины корректируют по лабораторным показателям, что нужно делать довольно часто.
При обоих типах сахарного диабета испытывалось комбинированное лечение инсулином и производными сульфанилмочевины. При инсулинозависимом сахарном диабете добавление производных сульфанилмочевины к инсулинотерапии не помогало поддерживать уровень глюкозы в плазме в нормальных пределах. При инсулинонезависимом сахарном диабете получены более интересные, но одновременно более противоречивые результаты. В одних исследованиях комбинированное лечение не обладало никакими преимуществами, в других оно значительно облегчало компенсацию сахарного диабета. Залогом успеха комбинированного лечения служат остаточная секреция инсулина β-клетками и малая длительность заболевания.
Репаглинид
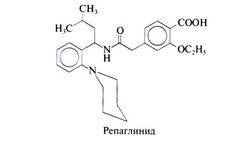
Представитель меглитинидов репаглинид — пероральное сахаропонижающее средство, стимулятор секреции инсулина. Репаглинид — производное бензойной кислоты, по структуре (см. ниже) совсем не похожее на производные сульфанилмочевины.
Тем не менее репаглинид, подобно производным сульфанилмочевины, стимулирует секрецию инсулина за счет закрывания АТФ-зависимых калиевых каналов в мембране β-клеток. Препарат быстро всасывается в ЖКТ, максимальная сывороточная концентрация достигается в течение часа. Т1/2 репаглинида составляет примерно 1 ч. Фармакокинетика препарата позволяет принимать его перед каждым приемом пиши, в отличие от производных сульфанилмочевины, которые принимают 1—2 раза в су-тки. Метаболизируется репаглинид главным образом в печени; метаболиты сахаропонижающим действием не I обладают. Бальным с печеночной недостаточностью препарат назначают с осторожностью. Кроме того, осторожности требует наращивание доз при почечной недостаточности, так как около 10% препарата метаболизируется в почках. Как и у производных сульфанилмочевины, основной побочный эффект репаглинида — гипогликемия.
Натеглинид
Еще одно пероральное сахаропонижающее средство, стимулятор секреции инсулина, — натеглинид — является производным D-фенилаланина. Подобно репаглиниду и производным сульфанилмочевины, он блокирует АТФ-зависимые калиевые каналы в мембране β-клеток. Натеглинид оказывает более быстрый, но менее стойкий эффект на секрецию инсулина, чем другие пероральные сахаропонижающие средства (Kalbag et al., 2001). Препарат применяют в основном для того, чтобы подавить постпрандиальную гипергликемию у больных инсулинонезависимым сахарным диабетом. Недавно его применение с этой целью было одобрено ФДА. Для достижения максимального эффекта натеглинид нужно принимать за 1—10 мин до еды в дозе 120 мг. Препарат метаболизируется преимущественно в печени, поэтому при печеночной недостаточности его назначают с осторожностью. Примерно 16% натеглинида в неизмененном виде выводится почками, и при почечной недостаточности его доза должна быть уменьшена. Первые клинические испытания показали, что натеглинид вызывает гипогликемию реже, чем другие пероральные сахаропонижающие средства (Horton et al., 2001).
Бигуаниды
Метформин и фенформин появились в 1957 г., буформин — в 1958 г. Последний использовался мало, но два первых получили широкое распространение. В 1970-х гг. фенформин во многих странах был изъят из продажи, поскольку часто вызывал лактацидоз. При лечении метформином это осложнение наблюдалось редко, и его продолжали широко применять в Европе и в Канаде. В 1995 г. препарат был разрешен к использованию в США. В качестве монотерапии и в комбинации с производными сульфанилмочевины метформин облегчает поддержание нормогликемии и улучшает липидный профиль у тех больных, у которых неэффективны диетотерапия или монотерапия производными сульфанилмочевины (DeFronzo etal., 1995).
Основная часть метформина всасывается в тонкой кишке. Препарат стабилен, не связывается с белками плазмы и выводится в неизмененном виде с мочой. Его Т1/2 составляет около 2 ч. Максимальная суточная доза метформина в США — 2,5 г; его принимают 3 раза в сутки во время еды.
Метформин устраняет гипергликемию, но не вызывает гипогликемию (Bailey, 1992). Даже в больших дозах он не стимулирует секрецию инсулина поджелудочной железой, поэтому гипогликемия и не возникает. Препарат не обладает сколько-нибудь значительным действием на секрецию глюкагона. кортизола, СТГ и соматостатина.
Он уменьшает уровень глюкозы в крови, снижая продукцию глюкозы печенью и усиливая действие инсулина на мышечную и жировую ткани. Относительно механизма, посредством которого метформин снижает продукцию глюкозы печенью, идут споры, однако большинство данных указывает на то, что препарат тормозит глюконеогенез (Stumvoll etal., 1995). Крометого. метформин снижает уровень глюкозы в плазме за счет подавления ее всасывания в ЖКТ, но этот его эффект, по-видимому, не имеет особого клинического значения.
Больным с почечной недостаточностью метформин противопоказан. Кроме того, его нельзя применять при болезнях печени, наличии в анамнезе лактацилоза любой этиологии, требующей медикаментозного лечения сердечной недостаточности и легочных заболеваниях, сопровождающихся хронической гипоксией. После исследований с в/в введением рентгеноконтрастных средств метформин следует отменить на 48 ч. Лечение возобновляют, только убедившись, что функция почек вернулась к норме. Все перечисленные выше состояния предрасполагают к избыточной продукции молочной кислоты и, следовательно, к развитию лактацилоза, который может угрожать жизни. Распространенность лактацидоза при лечении метформином составляет менее 0,1 на 1000 больных в год; риск смертельных исходов сшс ниже.
Остальные побочные эффекты метформина наблюдаются почти у 20% бальных и включают понос, неприятные ощущения в животе, тошноту, металлический привкус во рту, потерю аппетита. Их обычно удается свести к минимуму, наращивая дозу препарата постепенно и принимая его во время еды. При длительном лечении метформином часто нарушается всасывание в ЖКТ витамина В,2 и фолиевой кислоты. Всасывание витамина В,: нормализуют пищевые добавки, содержащие кальций (Bauman et al., 2000).
Важно помнить, что лечение метформином должно быть прекращено, если уровень лактата в плазме превышает 3 ммоль/л. Препарат отменяют также при снижении функции почек или печени. Больным, которые лечатся длительным голоданием или придерживаются сверхнизкокалорийных диет, тоже лучше воздержаться от приема метформина. Инфаркт миокарда и сепсис требуют немедленной отмены препарата. Максимальная суточная доза метформина составляет 2,5 г; его принимают 2—3 раза в сутки. При лечении метформином уровень гликозилированного гемоглобина А)с уменьшается примерно на 2%, то есть на столько же, на сколько его снижают производные сульфанилмочевины. Препарат не вызывает прибавку в весе и способен уменьшить содержание триглицеридов в плазме на 15—20%. Общепризнано, что снижение уровня гликозилированного гемоглобина А|с, каким бы путем оно ни было достигнуто (инсулинотерапией или пероральными сахаропонижающими средствами), сопряжено с уменьшением риска микроан-гиопатических осложнений сахарного диабета. В то же время метформин — единственный препарат, который снижает риск макроангиопатических осложнений при инсулинонезависимом сахарном диабете (UK Prospective Diabetes Study Group, 1998b). Метформин можно комбинировать с производными сульфанилмочевины, производными тиазолидиндиона и инсулинотерапией. В продаже имеется комбинированный препарат глибенкла-мид/метформин.
Производные тиазолидиндиона
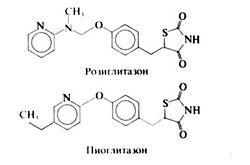
В клинической практике применялись три препарата этой группы — троглитазон, розиглитазон и пиоглитазон. Троглитаэон появился первым из трех, но в настоящее время изъят из продажи в связи с сильной гепатотоксичностью. Структурные формулы розиглитазона и пиоглитазона следующие:
Производные тиазолидиндиона избирательно связываются с внутриклеточными PPARy-рецеггторами (рецепторами, активируемыми индукторами пероксисом). В результате происходит активация чувствительных к инсулину генов, участвующих в регуляции углеводного и липидного обмена. Для того чтобы производные тиазолидиндиона оказали свой эффект, необходимо присутствие инсулина. Основное фармакологическое действие этих препаратов — уменьшение инсулинорезистентности периферических тканей, однако сообщалось и о снижении продукции глюкозы в печени. Производные тиа-золидиндиона усиливают транспорт глюкозы в мышечные волокна и липоциты, стимулируя синтез некоторых белков — переносчиков глюкозы и их перемещение к клеточной мембране. Кроме того, эти препараты активируют гены, участвующие в регуляции метаболизма свободных жирных кислот в периферических тканях. Не исключено, что именно за счет этого эффекта производные тиазолидиндионов и снижают инсулинорезистентность.
На данный вопрос должны ответить ведущиеся сейчас исследования.
Розиглитазон и пиоглитазон принимают один раз в сутки. Оба препарата всасываются в течение 2 ч, однако максимальный терапевтический эффект достигается только спустя 6—12 нед после начала лечения. Производные тиазолидиндионов метаболизируются в печени, и их можно принимать при почечной недостаточности. Однако они противопоказаны при тяжелом поражении печени или значительном подъеме активности аминотрансфераз.
При лечении производными тиазолидиндиона внимательно наблюдают за функцией печени. Остальные побочные эффекты этих препаратов включают анемию, прибавку в весе, отеки и гиперволемию. Производные тиазолидиндиона обычно не назначают при сердечной недостаточности HI—IV функционального класса (по классификации Нью-Йоркской кардиологической ассоциации).
При инсулинонезависимом сахарном диабете лечение розиглитазоном и пиоглитазоном способно снизить уровень гликозилированного гемоглобина А1с на 1—1,5%. Эти препараты можно комбинировать с инсулином и другими пероральными сахаропонижающими средствами. Производные тиазолидиндиона уменьшают уровень триглицеридов (на 10—20%), но увеличивают уровень холестерина ЛПВП (на 19%) и холестерина ЛПНП (на 12%). Сообщалось, что эти препараты уменьшают долю мелких плотных ЛПНП и увеличивают долю крупных, менее атерогенных.
Оба препарата метаболизируются в печени с участием изоферментов цитохрома Р450: в случае розиглитазона это изофермент IIC8, в случае пиоглитазона — изоферменты IIIA4 и IIC8. Поэтому на сывороточную концентрацию этих препаратов могут повлиять другие лекарственные средства, которые метаболизируются теми же изоферментами. На сегодняшний день клинически значимых лекарственных взаимодействий для производных тиазолидиндиона не описано, но такие взаимодействия могут быть выявлены в идущих сейчас клинических испытаниях.
Ингибиторы а-глюкозидаз
Эти препараты подавляют переваривание крахмала, декстринов и дисахаридов в ЖКТ, ингибируя а-глкжозида-зы щеточной каемки. Вследствие замедленного всасывания углеводов исчезает резкий подъем уровня глюкозы в крови после еды — как у здоровых людей,так и у больных сахарным диабетом.
Акарбоза (олигосахарид бактериального происхождения) и миглитол (производное дезоксинойиримицина) являются конкурентными ингибиторами a-D-глюкози-дазы и сахаразы-изомальтазы и слегка понижают активность панкреатической амилазы. Оба препарата подавляют постпрандиальную гипергликемию у бальных всеми формами сахарного диабета. При декомпенсирован-ном инсулинонезависимом сахарном диабете ингибиторы a-глюкозидаз значительно снижают уровень гликозилированного гемоглобина А1с, однако у больных с легкой или умеренной гипергликемией их эффективность (оцениваемая по уровню гликозилированного гемоглобина A1c) составляет всего 30—50% эффективности других пероральных сахаропонижающих средств. Ингибиторы а-глюкозидаз не стимулируют секрецию инсулина и, следовательно, не вызывают гипогликемию. В качестве монотерапии эти препараты применяют у пожилых больных, а также у больных, страдающих преимущественно постпрандиальной гипергликемией. В остальных случаях ингибиторы а-глюкозидаз назначают в комбинации с другими пероральными сахаропонижающими средствами или с инсулинотерапией. Препараты принимают непосредственно перед едой. Всасываются они плохо.
Лечение ингибиторами а-глюкозидаз приводит к нарушениям всасывания. Этот эффект, а также другие побочные эффекты — метеоризм, понос, вздутие живота — зависят от дозы препарата. Их можно свести к минимуму, наращивая дозу постепенно (начинают с разовой дозы 25 мг перед едой в течение 4—8 нед, затем с интервалами в 4—8 нед эту дозу постепенно увеличивают до 75 мг). Препараты принимают перед каждым основным приемом пищи; легкие закуски предваряют приемом меньших доз ингибитора а-глюкозидаз. Акарбоза наиболее эффективна, если больной соблюдает диету с высоким содержанием крахмала и клетчатки и низким содержанием глюкозы и сахарозы (Bressler and Johnson, 1992). Когда у больного, получающего комбинированное лечение ингибитором а-глюкозидаз и инсулином или стимулятором секреции инсулина, развивается гипогликемия, ее лучше всего купировать глюкозой, а не крахмалом, са-карозой или мальтозой.