Мочеполовая система
Категория:
«Фармакология».
Содержание
- 1 Лекарственные средства и мочеполовая система
- 2 ФИЗИОЛОГИЯ НИЖНИХ ОТДЕЛОВ МОЧЕВЫВОДЯЩИХ ПУТЕЙ
- 3 ПАТОФИЗИОЛОГИЯ И НАРУШЕНИЯ МОЧЕИСПУСКАНИЯ
- 4 Недержание мочи
- 5 Доброкачественная гиперплазия предстательной железы
- 6 Лечение недержания мочи и доброкачественной гиперплазии предстательной железы
- 7 Перспективы лечения доброкачественной гиперплазии предстательной железы
- 8 РАК ПРЕДСТАТЕЛЬНОЙ железы
- 9 ЭРЕКТИЛЬНАЯ ДИСФУНКЦИЯ
- 10 Средства, используемые для лечения эректильной дисфункции
- 11 ИНФЕКЦИИ МОЧЕВЫВОДЯЩИХ ПУТЕЙ
- 12 Литература
Лекарственные средства и мочеполовая система[править | править код]
К мочеполовой системе относятся органы, участвующие в накоплении мочи и мочеиспускании (мочевой пузырь и уретра), и органы, составляющие мужскую и женскую репродуктивную систему (яичники, матка, яички, семявыносящий канал). Предстательная железа (простата) является частью репродуктивной системы, нарушения функции простаты клинически проявляются затруднением оттока мочи.
ФИЗИОЛОГИЯ НИЖНИХ ОТДЕЛОВ МОЧЕВЫВОДЯЩИХ ПУТЕЙ[править | править код]
Нормальное мочеиспускание характеризуется управляемым изгнанием мочи
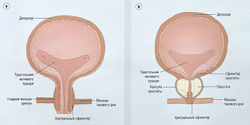
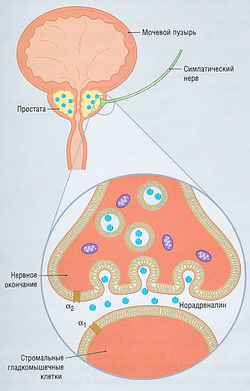
К нижним отделам мочевыводящих путей относятся детрузор (изгоняющая мышца мочевого пузыря), мышцы треугольника мочевого пузыря и уретра (рис. 17.1). Рефлекс мочеиспускания находится под контролем периферической нервной системы и центральной нервной системы.
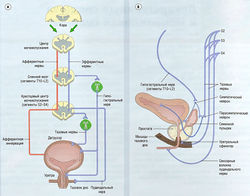
Нижние отделы мочевыводящих путей иннервируются парасимпатическими, симпатическими и соматическими нервами (рис. 17.2, табл. 17.1). Иннервация детрузора — преимущественно холинергическая, т.е. ацетилхолином, активирующим постсинаптические рецепторы, что приводит к сокращению мышц мочевого пузыря и мочеиспусканию. В активации сокращения мышц мочевого пузыря принимают участие мускариновые М3-рецепторы. Адренергическая иннервация детрузора, осуществляемая за счет взаимодействия нейромедиатора норэпинефрина (норадреналина) с β2-адренорецепторами, расслабляет детрузор и приводит к увеличению вместимости мочевого пузыря, но пределы его физиологического объема у людей ограничены. Основная функция детрузора — изгнание мочи (см. рис. 17.2).
Рис. 17.2 Иннервация нижних отделов мочевыводящих путей и мочеиспускательный рефлекс: (а) у женщин; (б) у мужчин. Симпатическая, парасимпатическая и соматическая иннервация осуществляется посредством тазового, пудендального и гипогастрального нервов. Афферентные нервы проходят от задних рогов спинного мозга к находящемуся под сознательным контролем центру мочеиспускания. Эфферентные нервы из этого центра идут в крестцовый центр мочеиспускания и через тазовое сплетение иннервируют мочевой пузырь, вызывая его сокращение. При этом эфферентные нервы ингибируют гипогастральный и пудендальный нервы, расслабляя мышцы области оттока (треугольник мочевого пузыря) и тазового дна.
Удержание мочи в норме обеспечивается динамическим равновесием парасимпатической и симпатической систем. Зона треугольника мочевого пузыря и уретра имеют богатую адренергическую иннервацию. Во время наполнения мочевого пузыря норадреналин, вырабатываемый симпатической нервной системой, активирует а1-адренорецепторы, отвечающие за закрытие сфинктеров. Наружный сфинктер уретры, являясь поперечнополосатой мышцей, вместе с мышцами тазового дна играет важную роль в удержании мочи.
Таблица 17.1 Функции рецепторов нижних отделов мочевыводящих путей
- Детрузор
- М3-холинорецепторы — сокращение
- β2-адренорецепторы — расслабление. Эти рецепторы функционально доминируют над констриктивным действием а1-адренорецепторов
- Уретра
- а1-адренорецепторы — релаксация, β2-адренорецепторы — констрикция
- М-холинорецепторы — функция неясна
- Предстательная железа
- а1-адренорецепторы, преобладающие в строме, — сокращение. Активация этих рецепторов приводит к повышению сопротивления току мочи при гиперплазии предстательной железы (динамический компонент)
- М-холинорецепторы эпителия — участие в секреторной функции
У мужчин уретра проходит через простату. Сопротивление току мочи усиливается при увеличении размера простаты и/или тонуса периуретральных гладких мышц. Сокращенное состояние гладких мышц обеспечивается действием норадреналина на а1-адренорецепторы.
ПАТОФИЗИОЛОГИЯ И НАРУШЕНИЯ МОЧЕИСПУСКАНИЯ[править | править код]
Недержание мочи возникает при невозможности удерживать мочу должным образом. У мужчин это обычно связано с увеличением размера предстательной железы
В целом нарушения мочеиспускания можно разделить на две основные группы: (1) нарушение удержания мочи (недержание); (2) нарушение оттока мочи (задержка).
Недержание мочи[править | править код]
Недержание мочи встречается более чем у 10% взрослого женского населения. Это состояние, определяемое как ненамеренное мочеиспускание (табл. 17.2), сильно влияет на качество жизни. В США продается больше памперсов для взрослых, чем для педиатрического использования. Недержание мочи у пожилых людей, прикованных к постели, является решающим фактором в необходимости нанимать сиделку.
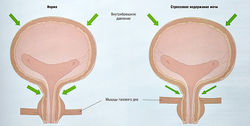
Стрессовое недержание мочи — непроизвольное мочеиспускание при отсутствии сокращения детрузора, когда внутрипузырное давление превышает давление в мочеиспускательном канале. У некоторых беременных непроизвольное мочеиспускание может произойти при кашле, чихании, смехе или во время физических упражнений. Первичная причина — изменение взаимоположения уретры и главным образом внутрибрюшных структур (рис. 17.3).
При раздражении мочевыводящих путей может возникнуть недержание мочи в сочетании с сильными позывами к опорожнению. Существуют моторный и сенсорный типы недержания мочи. Моторный тип связан с гиперактивностью детрузора и/или снижением его растяжимости. Сенсорный тип связан с раздражением, вызванным простатитом или циститом. Гиперактивность детрузора характеризуется его непроизвольными сокращениями во время фазы наполнения, которые могут быть спонтанными или спровоцированы и которые пациент не может подавить полностью.
Таблица 17.2 Типы недержания мочи у мужчин и женщин
- Недержание мочи
- Моторные нарушения со стороны детрузора
- Сенсорные нарушения
- Гиперрефлексия
- Инволюнторная — сокращения детрузора вследствие неврологических нарушений (например, травмы)
- Стрессовая — дефект запирательного механизма уретры
- Нарушения передачи внутрибрюшного давления на проксимальный отдел уретры
- Нарушение эстрогенного статуса
- Доброкачественная гиперплазия предстательной железы
- Симптомы со стороны нижних отделов мочевыводящих путей, характеризующиеся задержкой мочи, вторичным увеличением размера простаты, нестабильностью работы детрузора
Гиперактивность детрузора может развиваться вследствие препятствия оттоку мочи (например, при доброкачественной гиперплазии предстательной железы), воспаления предстательной железы и мочевого пузыря (например, при простатите и интерстициальном цистите), мочекаменной болезни с камнями, закупоривающими уретру, или неизвестных причин.
У некоторых пациентов недержание мочи вызвано сочетанием нескольких причин и требует расширенной диагностики. Гиперрефлексия — это состояние неконтролируемой активности детрузора, связанное с неврологическими причинами.
Информация по фармакотерапии нарушений мочеиспускания представлена в табл. 17.3.
Таблица 17.3 Фармакотерапия нарушений мочеиспускания у женщин и мужчин
- Острое недержание мочи и гиперрефлексия
- Холинолитики
- Комбинированные средства
- Антидепрессанты
- Антагонисты а1адренорецепторов
- Агонисты β2-адренорецепторов
- Десмопрессин
- Стрессовое недержание мочи
- Агонисты а-адренорецепторов
- Эстрогены (у женщин в постменопаузе)
- Доброкачественная гиперплазия предстательной железы
- Антагонисты а1адренорецепторов
- Ингибиторы 5а-редуктазы
- Комбинированные средства
Терапия недержания мочи и гиперрефлексии направлена на уменьшение активности детрузора и увеличение емкости мочевого пузыря.
Лечение недержания мочи и задержки мочи
- При недержании мочи лечение направлено на уменьшение активности детрузора, повышение емкости мочевого пузыря, увеличение давления на выходе из него
- При задержке мочи лечение направлено на увеличение активности детрузора и уменьшение сопротивления току мочи
Доброкачественная гиперплазия предстательной железы[править | править код]
Признаки доброкачественной гиперплазии предстательной железы часто ассоциируются с ее увеличением и затруднением оттока мочи
Доброкачественная гиперплазия предстательной железы (ДГПЖ) — наиболее часто диагностируемое заболевание у 85% мужчин старше 50 лет. К 80 годам 50% всех мужчин в США нуждаются в симптоматическом лечении. ДГПЖ характеризуется увеличением простаты и сопровождается признаками затруднения оттока мочи и недержанием мочи; может развиться длительная или полная задержка мочи.
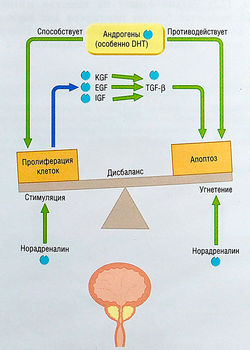
Хотя патогенез ДГПЖ не полностью раскрыт на молекулярном уровне, ясно, что присутствует связь с андрогенными факторами, особенно с 5а-редуцированным метаболитом тестостерона и дигидротестостерона (DHT) (рис. 17.4).
Рис. 17.4 Факторы, контролирующие тканевую пролиферацию и апоптоз в простате. DHT — дигидротестостерон; ECF — эпидермальный фактор роста; IGF — инсулиноподобный фактор роста; KCF — фактор роста кератиноцитов; TGF-p — трансформирующий фактор роста р.
Появление симптома затруднения оттока мочи всегда вторично по отношению к процессу увеличения простаты и является следствием развития статического и динамического компонентов механизма задержки мочи. Статический компонент — результат механической непроходимости, которая возникает из-за сжатия уретры увеличенной в размерах предстательной железой. Динамический компонент связан с изменениями тонуса гладких мышц в фибромышечной строме капсулы простаты и шейке мочевого пузыря. Тонус периуретральных гладких мышц зависит от активности симпатической нервной системы (СНС), которая посредством норадреналина стимулирует a1-адренорецепторы (рис. 17.5). Увеличение тонуса мышц повышает сопротивление току мочи и уменьшает отток мочи. Механизмы, вовлеченные в формирование этого симптома и никтурии у пациентов с ДГПЖ, сложны и могут включать компоненты, которые сохраняются даже при отсутствии механической преграды для оттока мочи.
Рис. 17.5 Симпатическая иннервация простаты. Показаны места действия ар и а2-рецепторов. Норадреналин из симпатического нерва действует на агрецепторы.
Лекарственные средства, обычно назначаемые при ДГПЖ, перечислены в табл. 17.3.
Лечение недержания мочи и доброкачественной гиперплазии предстательной железы[править | править код]
В большинстве случаев лечение сводится к оказанию экстренной симптоматической помощи, а не к воздействию на причину заболевания.
Лекарственная терапия недержания мочи вследствие раздражения и гиперрефлексии[править | править код]
Основа терапии — средства, снижающие мышечный тонус детрузора и повышающие емкость мочевого пузыря
Парасимпатическая нервная система (ПСНС) регулирует сократимость мочевого пузыря. Повышенная сократимость обусловливает применение для лечения недержания мочи лекарственных средств, снижающих мышечный тонус. Клиническая эффективность этих средств доказана, но, к сожалению, роль ПСНС в нормальном функционировании мочевого пузыря составляет одно из главных ограничений в их использовании. В дозах, незначительно превышающих терапевтические, эти средства могут вызвать полный паралич пузыря и/или задержку мочи.
Другим ограничением использования средств первого поколения, снижающих мышечный тонус, является возможность появления неблагоприятных побочных эффектов (например, сухости во рту, при которой пациенты не могут нормально говорить, жевать и глотать) вследствие антагонизма препаратов к мускариновым холинорецепторам в других органах. Возможны и другие классические побочные эффекты — нарушения зрения, запор и сонливость.
ОКСИБУТИНИН. Оксибутинин является наиболее часто назначаемым препаратом для лечения недержания мочи (табл. 17.4). Эффективность оксибутинина отмечена в нескольких плацебо-контролируемых исследованиях. Несмотря на некоторые его недостатки, это лекарственное средство стало препаратом выбора. Оксибутинин оказывает прямое расслабляющее действие на гладкие мышцы, однако этот эффект достигается при существенно более высоких концентрациях препарата (в 500 раз), чем необходимо для блокирования М-холинорецепторов; при терапевтических концентрациях в плазме оксибутинин действует только на М-холинорецепторы.
Молекулярным биологам удалось идентифицировать пять подтипов мускариновых рецепторов — М1-М5, но для подтипов М4 и М5 еще не определены конкретные физиологические функции. Относительно подтипов М1, М2, М3 оксибутинин имеет некоторую селективность: 10-кратную для подтипов M1 и М3, по сравнению с подтипом М2. Мочевой пузырь и слюнные железы имеют М3-рецепторы. Этим объясняется сухость во рту, наблюдаемая при приеме стандартной дозы оксибутинина. Для оценки отношения польза-вред были проведены контролируемые клинические испытания новой формы препарата — оксибутинина XL, показавшие положительные свойства препарата с измененной фармакокинетикой.
Оксибутинин — третичный амин, который хорошо всасывается, но подвергается метаболизму при первом прохождении. С этим связана очень низкая его биодоступность — всего 6%. Вероятно, этим объясняется изменчивость ответа на применение препарата у разных пациентов. Период полувыведения составляет всего 2 час, что существенно меньше оптимального, поэтому для достижения 24-часового эффекта необходимо принимать препарат 3 раза в день или даже более часто.
Активный метаболит оксибутинина, N-десетилоксибутинин, создает более высокие концентрации в плазме и может оказать значительное влияние на клинический профиль. Однако фармакология исходного препарата и его метаболита сходная.
Большая часть пациентов в период лечения оксибутинином испытывает классические антимускариновые побочные эффекты (сухость во рту, запор, нарушения зрения, сонливость), но прием препарата приводит к сокращению частоты и тяжести эпизодов недержания мочи. Для уменьшения неблагоприятных эффектов предпринимали попытки вводить препарат интравезикулярно (в мочевой пузырь).
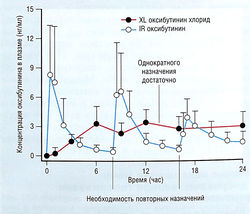
Оксибутинин XL (пролонгированная форма), несомненно, решает одну из проблем стандартной лекарственной формы IR (немедленного высвобождения) — необходимость частого повторного применения. Клинические данные указывают на лучший эффект оксибутинина XL по сравнению со стандартной лекарственной формой, что может быть следствием более стабильных 24-часовых концентраций препарата или различного метаболического профиля. Сравнение фармакокинетических профилей оксибутинина IR и оксибутинина XL показано на рис. 17.6. Улучшенный клинический профиль формы XL можно объяснить фармакокинетическими различиями, включающими более стабильный 24-часовой профиль.
ДРУГИЕ M-ХОЛИНОБЛОКАТОРЫ. Помимо новой формы оксибутинина появился другой препарат нового поколения — толтеродин, селективный блокатор М3-рецепторов. В США для лечения рефлекторного мочевого пузыря недавно был одобрен солифенацима сукцинат. Еще один антагонист М-рецепторов, троспия хлорид, имеет длительный период полувыведения (около 15 час), его полный фармакокинетический и клинический профиль представлен в табл. 17.4. Толтеродин весьма эффективен, но также вызывает классические антимуска-риновые побочные эффекты. В исследованиях было показано, что толтеродин имеет лучший клинический профиль по сравнению с оксибутинином, однако фармакологическое обоснование этого не вполне ясно. Возможно, толтеродин блокирует все три подтипа мускариновых рецепторов. Только тщательно контролируемые сравнительные исследования позволят определить, являются ли профили этих двух лекарственных средств действительно различными. Недавнее сравнительное исследование толтеродина и оксибутинина выявило лишь небольшое различие между ними.
Известны и другие средства с антимускариновым (эмероний, пропантелин) или смешанным антимускариновым и расслабляющим гладкие мышцы эффектом (например, дицикломин), а также смешанным, антимускариновым и блокирующим кальциевые каналы, эффектом — пропиверина гидрохлорид. Все они обладают антимускариновыми побочными эффектами и не подходят для приема 1 раз в день.
ДРУГИЕ СРЕДСТВА. Некоторые трициклические антидепрессанты эффективны у пациентов с гиперактивностью детрузора, но имипрамин — единственный препарат, который используют относительно широко. Имипрамин главным образом применяют при лечении ночного недержания мочи (энуреза) у детей. Он имеет более ограниченное использование для лечения гиперактивности мочевого пузыря у пожилых людей.
Имипрамин оказывает комплексное фармакологическое действие, включая блокаду М-рецепторов. Пока неизвестно, этот эффект или угнетение моноаминовой активности объясняет его действие на детрузор. Использование трициклических антидепрессантов, включая имипрамин, может вызывать серьезные побочные сердечно-сосудистые эффекты (например, ортостатическую гипертензию и аритмию), особенно у детей. Очевидно, что оценивать отношение польза-риск необходимо в каждом случае индивидуально.
Десмопрессин — синтетический аналог вазопрессина, действующий на V2-рецепторы и оказывающий антидиуретический эффект. Препарат фактически не имеет вазопрессорной активности, реализующейся через V1-рецепторы. Это приводит к существенному сокращению ночного образования мочи. Десмопрессин применяют для лечения энуреза у детей, а также для уменьшения частоты никтурии у пациентов с ДГПЖ и рассеянным склерозом. Препарат может быть эффективен у некоторых взрослых с гиперактивностью детрузора.
Стрессовое недержание мочи[править | править код]
Медикаментозное лечение направлено на увеличение сопротивления току мочи
Умеренное или выраженное стрессовое недержание мочи эффективно лечат хирургически. Традиционное медикаментозное лечение назначают пациентам с умеренно выраженными клиническими проявлениями для их уменьшения у пациентов, которым не помогают, например, упражнения для укрепления мышц тазового дна. Цель лечения — увеличить сопротивление току мочи. Теоретически это можно достичь увеличением интрауретрального давления или усилением функциональных возможностей слизистой оболочки мочеиспускательного канала.
а-АДРЕНОСТИMУЛЯТОРЫ. Эти средства увеличивают давление в уретре. Наиболее широко используемый препарат — эфедрин, однако он действует также на β-рецепторы как косвенный симпатомиметик, способствующий выбросу норэпинефрина из нервных окончаний, поэтому он может повышать артериальное давление, вызывать нарушения сна и тремор. Есть данные, что при длительном назначении эфедрина развивается тахифилаксия. В качестве альтернативы в США ранее применяли фенилпропаноламин.
ЭСТРОГЕНЫ. Терапевтический эффект эстрогенов заключается в индукции пролиферации слизистой оболочки мочеиспускательного канала с последующим увеличением сопротивления току мочи. Кроме того, эстрогены усиливают эффект агонистов возбуждения периуретральных гладких мышц. Терапия может включать комбинацию эстрогенов и адренергических агонистов. Традиционно эстрогены назначают в виде имплантируемого кольца.
Доброкачественная гиперплазия предстательной железы[править | править код]
Лечение ДГПЖ направлено на уменьшение размера простаты с помощью ингибиторов 5a-редуктазы или на уменьшение сокращения гладких мышц, окружающих уретру, с помощью селективных а1адреноблокаторов
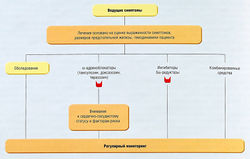
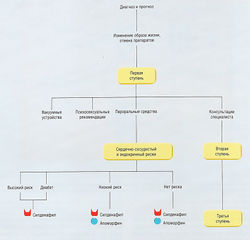
Медикаментозное лечение обычно используют при умеренных клинических проявлениях. У пациентов с выраженной симптоматикой или задержкой мочи предпочтительным методом является хирургический. Возможный алгоритм лечения представлен на рис. 17.7.
Рис. 17.7 Алгоритм лечения при симптомах дисфункции нижних отделов мочевыводящих путей, ассоциированных с доброкачественной гиперплазией предстательной железы.
Признаками ДГПЖ является нарушение оттока мочи, связанное с увеличением размеров простаты и рестрикцией мочеиспускательного канала. Существуют два компонента обструкции: (1) механический, являющийся результатом физической непроходимости, вызванной увеличением простаты; (2) динамический (непостоянный), связанный с изменениями тонуса гладких мышц простаты (см. рис. 17.5). Лечение направлено либо на уменьшение механической обструкции, либо на стимуляцию периуретральных гладких мышц простаты.
Препараты, используемые в лечении ДГПЖ, уменьшают размер простаты либо снижают тонус гладких мышц простаты
ПРЕПАРАТЫ, УМЕНЬШАЮЩИЕ РАЗМЕР ПРОСТАТЫ. В пролиферации предстательной железы участвуют различные факторы, но андрогены, в частности дигидротестостерон, играют первостепенную роль (см. рис. 17.4). Для лекарственной терапии доброкачественной гиперплазии предстательной железы основными препаратами являются ингибиторы 5а-редуктазы, т.к. они влияют на метаболизм андрогенов, особенно на дигидротестостерон. Повышение концентрации андрогенов поддерживает доброкачественный рост предстательной железы, а снижение уровня андрогенов приводит к существенной инволюции железисто-эпителиального компонента простаты.
Финастерид — препарат, блокирующий действие фермента 5а-редуктазы, катализирующего синтез DHT из тестостерона. Препарат снижает концентрацию DHT в плазме, а эффект на простату подобен таковому при кастрации. Во время длительных исследований при ежедневном применении финастерида в дозе 5 мг в течение года или более наблюдалось уменьшение размеров простаты. В этих исследованиях обнаружилось, что потребность в хирургическом лечении уменьшилась до 50%. Однако в большинстве исследований не было доказано влияние финастерида на симптомы ДГПЖ и отсутствовал эффект в течение первых 6 мес терапии. Главный неблагоприятный побочный эффект, связанный с использованием препарата — снижение либидо у 15% пациентов, что обусловлено четкой связью между андрогенами и мужской сексуальной активностью.
Финастерид в сниженной до 1 мг дозе был предложен для лечения мужского облысения, поскольку рост некоторых типов волос зависит от уровня DHT. Хотя в луковице волос присутствует только 5а-редуктаза 1-го типа, считается, что эффект обусловлен обобщенным действием финастерида на все системные андрогены.
Существует две изоформы 5а-редуктазы. Финастерид преимущественно ингибирует 2-й тип изоформы — основную изоформу в ткани простаты. Одно из ограничений применения финастерида — относительная стимуляция 5а-редуктазой 1-го типа эктопического синтеза DHT вне простаты (в коже, печени и фибробластах), что может поддерживать рост предстательной железы. С учетом этого созданы и проходят испытания препараты, ингибирующие оба типа 5ос-редуктазы. Для такого лечения ДГПЖ недавно был одобрен дутастерид. Однако в отсутствие долгосрочных клинических наблюдений неизвестно, имеет ли двойное ингибирование терапевтическое преимущество, т.к. побочные эффекты неселективного воздействия могут превышать клинический эффект.
СЕЛЕКТИВНЫЕ a1-АДРЕНОБЛОКАТОРЫ. В отличие от финастерида, препараты этой группы приводят к быстрому улучшению симптоматики.
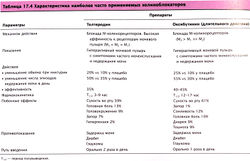
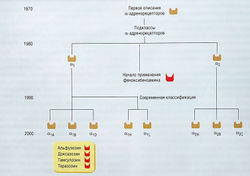
Использование феноксибензамина показало эффективность различных блокаторов адренорецепторов при ДГПЖ. Рекомендуется сначала назначать празозин, а затем другие селективные а-адреноблокаторы (альфузозин, доксазозин, индорамин, тамсулозин и теразозин). В настоящее время эти средства — основа терапии ДГПЖ. Фармакологические и клинические характеристики этого класса препаратов представлены в табл. 17.5.
|
Таблица 17.5 Обзор основных блокаторов а-адренорецепторов | |
|
Препарат |
Свойства |
|
Альфузозин |
Имеет равную аффинность к подтипам а1А, а1В и a1D а1рецепторов. Выпускают в различных лекарственных формах. Т1/2 составляет 3 и 11 час. Можно применять 2-3 раза в день |
|
Доксазозин |
Самый длительно действующий блокатор а-адренорецепторов (16-22 час). Имеет равную аффинность к подтипам a1A, а1B и а1D а1рецепторов. Применяют при лечении артериальной гипертензии |
|
Празозин |
Несмотря на сложность дозировки и побочные эффекты препарат широко применяют из-за невысокой цены |
|
Тамсулозин |
Считается уроселективным и имеет высокую аффинность к а1А-рецепторам простаты, бoльшую, чем к подтипам а1В и a1D. Выпускают только в форме таблеток по 0,4 мг, что затрудняет подбор дозы. Т1/2 составляет 16 час |
|
Теразозин |
Фармакологический и клинический профиль идентичен доксазозину. Применяют также как компонент антигипертензивной терапии в некоторых странах |
Полученные данные были рассмотрены в Международном консультативном комитете ВОЗ по антагонистам а-рецепторов и проблеме ДГПЖ (a-Receptor Antagonist Committee of the WHO International Consultation on BPH). Эксперты пришли к выводу, что различия между препаратами этой группы в значительной степени определены их фармакологическими свойствами, т.е. в соответствующих дозах все они имеют почти равную эффективность и сходные побочные эффекты. На этом основании теразозин можно рассматривать как типичный представитель этого класса препаратов. Однако тамсулозин фармакокинетически может несколько отличаться от других блокаторов а-рецепторов.
Начиная с открытия а1 и а2-рецепторов понимание фармакологии адренорецепторов существенно расширилось (рис. 17.8). В простате посредством молекулярного клонирования были обнаружены три подтипа а1адренорецепторов.
Подтипы а1адренорецепторов — а1А, а1В и а1D — имеют высокую аффинность к празозину. Есть также данные о существовании а1-рецепторов, имеющих низкую аффинность к этому препарату. Большинство исследователей считают, что главным фактором повышения тонуса простаты являются рецепторы подтипа а1А в периуретральной строме.
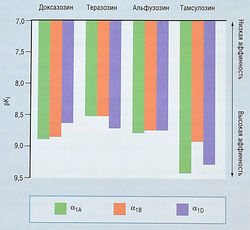
Как лекарственные средства a1-адреноблокаторы доказали свою безопасность и эффективность при лечении симптомов, связанных с ДГПЖ. Пациенты отмечают терапевтический эффект уже с первых недель лечения. Наблюдаемые изменения в мочеиспускании и остаточном объеме мочи связаны с влиянием препаратов на давление мочи в уретре. Механизм улучшения оттока мочи хорошо изучен, но механизмы положительного влияния а-адреноблокаторов на такие симптомы, как частота позывов и никтурия, выяснены не полностью. Празозин можно использовать в течение нескольких лет, но следует помнить о вызываемой им ортостатической гипотензии, возникающей после приема первой дозы. Теразозин — первый селективный a-адреноблокатор без подобного побочного эффекта. Препарат имеет аффинность к подтипам а1А, а1В и a1D a1-адренорецепторов (рис. 17.9). Кроме того, теразозин отличается от празозина фармакокинетически, его эффект развивается постепенно с меньшим количеством ортостатических нарушений после приема первой дозы и более длинным периодом полувыведения.
Рис. 17.9 Аффинность (pKj) доксазозина, теразозина, альфу-зозина и тамсулозина к подтипам а1А1 а,в и а-адренорецепторов.
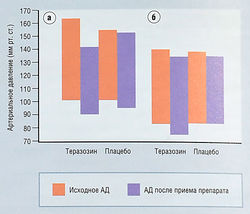
а-Адреноблокаторы первоначально разрабатывали как антигипертензивные средства, однако теразозин практически не влияет на давление крови у нормотоников (рис. 17.10). Тем не менее лекарственные средства данной группы могут вызывать постуральную гипотензию, головокружение, усталость, сонливость и головную боль. У большинства пациентов с головокружением постуральная гипотензия не наблюдается. Неблагоприятные эффекты, как правило, имеют умеренную степень, могут быть преходящими, поэтому необходимость в отмене препарата отсутствует. Клинические данные о тера-зозине основаны на более чем 3 млрд пациентодней и доказывают, что препарат пациенты переносят хорошо. Несколько долгосрочных исследований установили, что эффективность теразозина сохраняется до 7 лет без развития тахифилаксии.
Лечение доброкачественной гиперплазии предстательной железы
- а1-Адреноблокаторы широко применяют в первые 2 нед при острых симптомах. Для этих препаратов характерны побочные эффекты со стороны сердечно-сосудистой системы (головокружение, головная боль, усталость)
- Ингибиторы 5а-редуктазы применяют у пациентов с увеличенной простатой. Клинический эффект от их применения (уменьшение размеров простаты) может проявиться только через 1 год терапии
Перспективы лечения доброкачественной гиперплазии предстательной железы[править | править код]
До недавнего времени считалось, что a-адреноблокаторы являются наиболее важной группой лекарственных средств для облегчения симптомов ДГПЖ. В течение многих лет разрабатывали препараты, избирательно действующие на этот тип адренорецепторов, исходя из предположения, что неблагоприятные сердечно-сосудистые эффекты, связанные с а1А- и а1С-рецепторами, будут уменьшены. Однако клинические испытания неутешительны и относительно эффективности, и относительно нивелирования побочных эффектов. Тамсулозин в малых дозах не вызывает постуральной гипотензии, но его эффективность может быть ниже, чем у других препаратов этой группы в тех же дозах. Стало ясно, что для повышения эффективности нужна блокада не только а1A-рецепторов, но и других подтипов а1рецепторов, локализованных вне простаты (например, в мочевом пузыре или в спинном мозге), которые могут быть причиной некоторых симптомов ДГПЖ.
Таблица 17.6 Растительные лекарственные средства, применяемые при доброкачественной гиперплазии предстательной железы
- Hypoxis rooperi (южноамериканская звездная трава)
- Urtica spp. (жгучая крапива)
- Sabal serrulatum (карликовая пальма)
- Serenoa repens В (американская карликовая пальма)
- Cucurbita реро (семена тыквы)
- Pigeum Africanum (африканская пальма)
- Populus tremula (осина)
- Echinacea purpurea (цветы эхинацеи)
- Secale cereale (рожь)
Эффективность и безопасность этих растительных лекарственных средств неясны.
Таблица 17.7 Ежегодная заболеваемость и смертность от различных форм рака в США
|
Локализация |
Заболеваемость |
Смертность |
|
Мочевыводящие пути | ||
|
Простата |
200 000 |
38 000 |
|
Яички |
6800 |
325 |
|
Мочевой пузырь |
51 200 |
10 500 |
|
Почки |
27 600 |
11 300 |
|
Прочие | ||
|
Желудочно-кишечный тракт |
220 000 |
120 000 |
|
Легкие |
1 72 000 |
153 000 |
Логично было бы использование комбинации финастерида и антагониста a1-рецептора, что привело бы к быстрому улучшению клинической картины и воздействию на причину заболевания. Однако клинические исследования по-прежнему доказывают, что вероятная терапевтическая польза минимальна. Назначение одного антагониста а1 рецептора достаточно в большинстве случаев.
Интересно, что увеличивается использование пациентами с ДГПЖ растительных лекарственных средств (табл. 17.6). Безопасность и эффективность — главная проблема для пациентов, применяющих такие средства, т.к. контроль качества таких средств намного ниже, чем при производстве лекарственных средств.
РАК ПРЕДСТАТЕЛЬНОЙ железы[править | править код]
Рак предстательной железы на ранней и метастазирующей стадиях можно лечить гормон-модулирующей терапией, но чтобы лечение было успешным, необходимо хирургическое вмешательство в комбинации с медикаментозной и лучевой терапией
Рак предстательной железы — третья из наиболее частых причин смерти от рака в развитых странах (табл. 17.7), при этом имеются значительные разногласия относительно методов его лечения, особенно ограниченных повреждений. Основная причина разногласий — трудности с прогнозом, т.к. сложно определить, какие повреждения будут прогрессировать, а какие останутся ограниченными и бессимптомными. Другими словами, многие пациенты с раком предстательной железы умирает не от него, а от других причин. Основное направление лечения — борьба с жизнеугрожающими процессами. К сожалению, в большинстве стран лишь около 30% злокачественных новообразований простаты диагностируют, когда процесс еще не вышел за пределы железы.
На ранней стадии рак предстательной железы зависит от уровня андрогенов. На этом основании гормональную терапию используют в сочетании с хирургическим лечением и лучевой терапией.
Действие андрогенов на клетки простаты можно модулировать различными способами. Клинически медикаментозная кастрация аналогом GnRH столь же эффективна, как орхэктомия
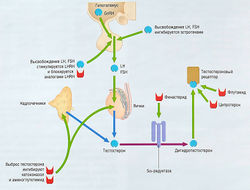
Секреция тестостерона зависит от LH и FSH (рис. 17.11). Ингибирование секреции было достигнуто при использовании аналога гонадотропин-рилизинг гормона LHRH, который действует как частичный агонист в стимулировании секреции LH и FSH. Сначала аналоги GnRH вызывают временное увеличение концентраций LH и FSH, но затем концентрация тестостерона существенно уменьшается. Это происходит из-за десенсибилизации GnRH-рецепторов в гипофизе. Долгосрочный эффект — снижение уровня тестостерона в плазме до уровня у кастрированных людей. Временное увеличение уровня тестостерона, получившее название «феномен вспышки», свидетельствует о теоретическом риске стимуляции метастатического роста опухоли. По этой причине в течение первых 4 нед лечения аналогами GnRH рекомендуется дополнительная терапия антиандрогенами (см. далее). Новое поколение суперселективных агонистов типа абареликса, которое, возможно, не провоцирует начальное повышение уровня тестостерона, пока находится в разработке.
Рис. 17.11 Уменьшая различными методами влияние тестостерона на простату, можно контролировать рак предстательной железы. Выброс гонадотропин-рилизинг гормона (GnRH) из гипоталамуса можно блокировать эстрогенами, а эффекты лютеинизиру-ющего гормона рилизинг гормона (LHRH) для высвобождения FSH и LH — аналогами LHRH. Синтез тестостерона можно блокировать кетоконазолом или аминоглутетимидом. Превращение тестостерона в дигидротестостерон, участвующий в формировании гиперплазии предстательной железы, блокируется ингибитором 5а-редуктазы (например, финастеридом). Также возможно заблокировать рецепторы тестостерона флутамидом или ципротероном. FSH — фолликулостимулирующий гормон; LH — лютеинизирующий гормон.
В большинстве стран GnRH-терапия — метод выбора в лечении рака предстательной железы (табл. 17.8). Имеются аналоги препарата — лейпролид, бусерелин, лейпрорелин и гозерелин. Для начальной терапии все эти средства используют в форме инъекций в течение 3 мес. Все аналоги GnRH угнетают сексуальную функцию. Фармакодинамика и фармакокинетика различных лекарственных средств и их форм описаны в табл. 17.9.
Антиандрогены действуют локально в пределах простаты, блокируя ее рост дигидротестостероном
Антиандрогены весьма эффективны, но, к сожалению, их первичный механизм действия может самоограничиваться при блокировании действия андрогенов. Как класс лекарственных средств антиандрогены влияют на рецепторы андрогенов не только на уровне простаты, но и на уровне гипоталамо-гипофизарной системы. На этом уровне андрогены обычно испытывают саморегулирующее влияние отрицательной обратной связи. В результате центральной блокады рецепторов андрогенов секреция LH растет, а биосинтез тестостерона увеличивается.
Другие методы блокады андрогенов
Эстрогены, особенно диэтилстильбэстрол, блокируют выработку GnRH гипоталамусом, сокращая LH и FSH и уменьшая производство тестостерона. DES оказывает значительное токсическое воздействие на сердечно-сосудистую систему, вызывает эректильную дисфункцию и гинекомастию. В настоящее время DES больше не является препаратом первой линии при лечении рака предстательной железы.
|
Таблица 17.8 Лечение локализованного и метастатического рака предстательной железы | |
|
Метод |
Вид рака предстательной железы |
|
Наблюдение |
Локализованный |
|
Радикальная радиотерапия |
Локализованный |
|
Радикальная простатэктомия |
Локализованный |
|
Антиандрогенная терапия |
Метастатический |
|
Двусторонняя орхэктомия | |
|
Аналоги LHRH | |
|
Двусторонняя адренэктомия | |
Финастерид — конкурентный ингибитор 5а-редуктазы, фермента, катализирующего синтез DHT из тестостерона в простате (см. ранее). Препарат используют в лечении ДГПЖ, но его эффективность при раке предстательной железы остается спорной. Финастерид блокирует только 5а-редуктазу 2-го типа, но чтобы достичь максимальной клинической эффективности при раке предстательной железы и при ДГПЖ, необходимо блокировать обе изоформы. Дутастерид (препарат, способный ингибировать обе изоформы 5ос-редуктазы) сейчас находится на стадии разработки.
Таблица 17.9 Фармакотерапия рака предстательной железы
|
Препарат |
Дозировка |
Побочный эффект | |
|
Аналоги LHRH |
Лейпролид |
3-месячная |
Приливы крови |
|
Гозерелин |
Импотенция | ||
|
Бусерелин |
Снижение либидо | ||
|
Лейпрорелин | |||
|
Нестероидные антиандрогены |
Флутамид |
250 мг 3 раза в день |
Гинекомастия |
|
Нилутамид |
300 мг/сут |
Диарея | |
|
Бикалутамид |
1 50 г/сут | ||
|
Гестагенные антиандрогены |
Ципротерона ацетат |
100 мг 3 раза в день |
Задержка жидкости Импотенция |
|
Эстрогены |
Диэтилстильбэстрол |
2-5 мг/сут |
Импотенция Гинекомастия Сердечно-сосудистая токсичность |
ЭРЕКТИЛЬНАЯ ДИСФУНКЦИЯ[править | править код]
В течение последнего десятилетия в лечении эректильной дисфункции был достигнут значительный прогресс в связи с появлением эффективных лекарственных средств
Эректильная дисфункция (половое бессилие) — не способность достигать и/или поддерживать эрекцию, достаточную для удовлетворительного полового акта. Причинами эректильной дисфункции могут быть физиологические, неврогенные, эндокринные, сосудистые и травматические факторы. Эректильную дисфункцию подразделяют на психогенную, органическую или смешанную.
Таблица 17.10 Лекарственные средства, вызывающие эректильную дисфункцию
|
Группа |
Препараты |
|
Гипотензивные |
Клонидин, метилдопа, гидрохлоротиазид, β-адреноблокаторы |
|
Психотропные |
Ингибиторы МАО, трициклические антидепрессанты, фенотиазины, бензодиазепины |
|
Депрессанты ЦНС |
Седативные средства, наркотики, этанол, анксиолитики, |
|
Прочие |
Атропин, эстрогены, циметидин, противоопухолевые средства |
Потенциальные факторы риска развития этого нарушения: пожилой возраст, курение, гипертензия, ожирение, диабет, болезни сосудов, депрессия и применение некоторых лекарственных средств (табл. 17.10). Эректильная дисфункция может оказывать существенное влияние на качество жизни многих людей. Вероятность наличия той или иной формы эректильной дисфункции для людей старше 40 лет составляет около 55%.
При эрекции происходит расслабление гладких мышц кавернозных тел и наполнение их кровью, уровень эрекции определяется степенью кровенаполнения
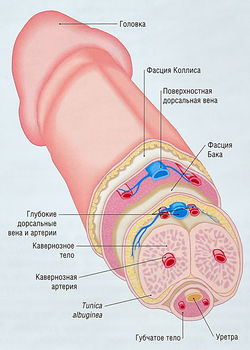
Процесс эрекции — это сложный цикл взаимосвязанных сосудистых процессов, достигающих высшей точки при накоплении крови в половом члене под давлением, обеспечивающем его упругость. Эрекция может происходить только при расслаблении гладких мышц артерий и кавернозных тел (рис. 17.12) и заполнении тканей кровью. Увеличение давления расширяет эластичные трабекулярные стенки. Артерии посредством вено-окклюзирующего механизма снижают венозный отток, что увеличивает давление и делает половой член твердым. Расслабление происходит после сокращения гладких мышц сосудов полового члена.
Рис. 17.12 Анатомия полового члена. Эрекция возникает при увеличении двух кавернозных тел и губчатого тела во время их заполнения артериальной кровью. Различные фасции (особенно tunica albuginea) предотвращают чрезмерное увеличение полового члена и ограничивают венозный дренаж, что приводит к эрекции.
Эрекция зависит от местных сосудистых процессов, но регуляция реализуется через интеграцию нейрональных и гормональных механизмов на различных уровнях
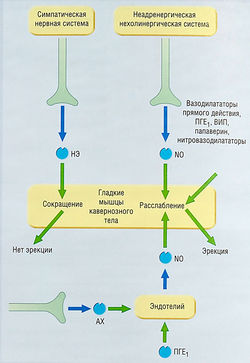
Тонус гладких мышц кавернозных тел зависит от работы многих систем и проводящих путей (рис. 17.13), которые делятся на внешние (спинальные или супраспинальные проводящие пути классической нейротрансмиссии) и внутренние, определяемые пара- и аутокринными контролирующими системами с различными нейромодуляторными субстанциями.
Рис. 17.13 Автономный контроль эрекции. Применение средств, влияющих на релаксацию гладких мышц кавернозного тела, приводит к изменению эрекции. N0 — оксид азота; АХ — ацетилхолин; ВИП — вазоактивный интестинальный пептид; НЭ — норэпинефрин; ПГЕ, — простагландин Е).
Нормальная эрекция происходит, когда эти механизмы работают скоординированно. Эрекцию также обеспечивают симпатическая нервная система и NO-содержащие нервные волокна (система НАНХ), осуществляющие местную регуляцию. Нейротрансмиттеры и нейромодуляторы перечислены в табл. 17.11. Однако для нормальной функции необходима регуляция и со стороны ЦНС.
Особенно интересна система НАНХ. При сексуальном возбуждении высвобождается NO, активизирующий внутриклеточный ферментный каскад (рис. 17.14). NO синтезируется из предшественника L-аргинина, который конвертируется ферментом NO-синтазой. В пределах кавернозного тела NO вызывает увеличение синтеза цГМФ, он, в свою очередь, уменьшает внутриклеточную концентрацию ионов кальция, что ведет к расслаблению гладких мышц сосудов и развитию эрекции. цГМФ разрушается ФДЭ-5, которая частично участвует в процессе расслабления (в этом процессе более значима роль СНС). Норадреналин вызывает сокращение гладких мышц кавернозного тела, что приводит к расслаблению.
Таблица 17.11 Лекарственные средства, влияющие на тонус гладких мышц
|
Расслабляющие |
Стимулирующие |
|
Ацетилхолин |
Норэпинефрин |
|
Оксид азота |
Эндотелин-1 |
|
Вазоактивный интестинальный пептид |
Нейропептид Y |
|
Простагландин Е, | |
|
Кальцитонин-высвобождающий пептид |
Аденозинтрифосфат |
Средства, используемые для лечения эректильной дисфункции[править | править код]
Перед лечением необходимо полное диагностическое обследование
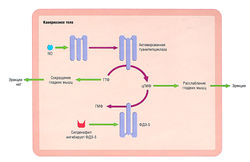
Алгоритм лечения пациентов с эректильной дисфункцией приведен на рис. 17.15. После обследования и постановки диагноза выбор метода лечения зависит от конкретного случая. Отправная точка этого выбора — модификация потенциально обратимых причин. Это может быть коррекция образа жизни, например уменьшение стрессов, изменения питания, отказ от курения, более эффективный контроль уровня глюкозы крови у больных диабетом. В случаях ятрогенной эректильной дисфункции (см. табл. 17.10) прекращение или модификация лекарственной терапии может иметь значительный успех. Иногда необходима интервентная терапия, которая может включать лекарства, психотерапию, минимально «агрессивные» процедуры (например, вакуумные устройства) либо хирургическое лечение.
Рис. 17.14 Контроль сокращения и расслабления гладких мышц кавернозного тела и эрекция. Представлены эффекты силденафила. N0 — оксид азота; ГМФ — гуанозинмонофосфат; ГТФ — гуанозинтрифосфат; ФДЭ-5 — фосфодиэстераза 5; цГМФ — циклический гуанозинмонофосфат.
Средства, влияющие на центральные или периферические механизмы эрекции
Пионером создания лекарственных средств для лечения эректильной дисфункции был Brindley в 1970-е гг. В то время сосудорасширяющие средства типа папаверина и феноксибензамина вводили интракавернозно. Такая монотерапия имела осложнения в виде фиброза и формирования фиброзных узлов, в результате была ограничена в применении. В некоторых странах широко использовали методику Trimix — комбинацию фентоламина, папаверина и простагландина Ej (табл. 17.12). Комбинация этих препаратов позволяет уменьшить дозы каждого препарата в отдельности и снижает частоту побочных эффектов. Для монотерапии до последнего времени наиболее часто применяли простагландин E1.
|
Таблица 17.12 Влияние лекарственных средств на гладкие мышцы кавернозного тела | |
|
Препарат |
Свойства |
|
Папаверин |
Прямой релаксирующий эффект посредством влияния на уровень внутриклеточного кальция. Возможно, блокирует фосфодиэстеразу |
|
Фентоламин |
Влияние вторично. Блокирует постсинаптические а1-адренорецепторы (см. рис. 1 7.1 3) |
|
Простагландин Е1 |
Увеличение цАМФ, мобилизация кальция, также возможно пресинаптическое влияние на выброс нейротрансмиттеров |
|
цАМФ — циклический аденозинмонофосфат. | |
ПГЕ1 алпростадил после приема внутрь быстро разрушается в крови, не создавая высоких системных концентраций, поэтому препарат обычно вводят интракавернозно. Алпростадил в дозе 5-20 мкг эффективен в лечении эректильной дисфункции, вызванной широким спектром причин. Почти у 70% пациентов отмечается полное восстановление эрекции. Обычный неблагоприятный побочный эффект — боль в месте введения препарата — является причиной прекращения терапии у остальных 30% пациентов. В долгосрочных исследованиях выяснилось, что частота развития фиброзов относительно низкая (< 1%). До появления силденафила лечение у большинства пациентов проводили именно интракавернозным введением алпростадила.
|
Таблица 17.13 Изоформы фосфодиэстеразы и ее ингибирование силденафилом | |||||
|
Изоформа |
Субстрат |
Эффект цГМФ на гидролиз цАМФ |
Локализация |
Мишени силденафила |
Значение IС50 <нМ)* |
|
ФДЭ-1 |
цГМФ > цАМФ |
Нет эффекта |
Головной мозг, сердце, почки, печень, скелетные мышцы, сосудистые и висцеральные гладкие мышцы |
Желудочки сердца |
280 |
|
ФДЭ-2 |
цАМФ, цГМФ |
Стимуляция |
Кора надпочечников, головной мозг, кавернозное тело, сердце, почки, печень, скелетные мышцы, висцеральные гладкие мышцы |
Кавернозное тело |
68 000 |
|
ФДЭ-3 |
цАМФ |
Ингибирование |
Кавернозное тело, сердце, тромбоциты, почки, печень, сосудистые и висцеральные гладкие мышцы |
Кавернозное тело |
16 200 |
|
ФДЭ-4 |
цАМФ |
Нет эффекта |
Почки, легкое, молочная железа, сердце, скелетные мышцы, сосудистые и висцеральные гладкие мышцы |
Скелетные мышцы |
7200 |
|
ФДЭ-5 |
цГМФ |
Нет точных данных |
Кавернозное тело, тромбоциты, скелетные мышцы, сосудистые и висцеральные гладкие мышцы |
Кавернозное тело |
4 |
|
ФДЭ-6 |
цГМФ |
Нет точных данных |
Сетчатка глаза |
Колбочки Палочки |
34 38 |
- IC50 — концентрация силденафила, необходимая для ингибирования активности фермента на 50%. ФДЭ — фосфодиэстераза; цАМФ — циклический аденозинмонофосфат; цГМФ — циклический гуанозинмонофосфат.
В попытке уменьшить боль на участке инъекции была разработана интрауретральная система введения. Однако при сравнении с интракавернозным способом введения эффективность оказалась ниже. Также отмечается относительно высокая частота ощущений жжения и зуда в мочеиспускательном канале, провоцируемых установкой интрауретральной системы.
Ингибиторы ФДЭ-5
Появление первого ингибитора ФДЭ-5 изменило фармакотерапию эректильной дисфункции. Возможность перорального применения, эффективность и безопасность привели к увеличению числа пациентов, которые начали обращаться за помощью по поводу эректильной дисфункции. До разработки силденафила лишь около 2% пациентов, страдающих эректильной дисфункцией, были готовы говорить о своей проблеме. После появления силденафила число таких пациентов увеличилось до 18%.
Силденафил — мощный ингибитор фосфодиэстеразы 5 (табл. 17.13) и при определенных условиях увеличивает эффекты цГМФ путем ингибирования распада этого нуклеотида (рис. 17.16). Препарат действует только в условиях сексуальной стимуляции и восстанавливает естественный ответ на сексуальное возбуждение.
Рис. 17.16 Механизм ингибирующего влияния силденафила на фосфодиэстеразу 5 (ФДЭ-5). ФДЭ-5 и ее ингибитор силденафил 56В в процессе эрекции. N0 — оксид азота; ГТФ — гуанозинтрифосфат; цГМФ — циклический гуанозинмонофосфат.
Силденафил быстро всасывается и начинает действовать в пределах 1 час, период полувыведения составляет 4-6 час. Однако вследствие относительно высокой концентрации в плазме, достигнутой в терапевтическом диапазоне дозы (25, 50 и 100 мг), функциональный и фармакодинамический период намного длиннее. У некоторых пациентов эрекция сохранялась в течение 36 час после приема единственной дозы.
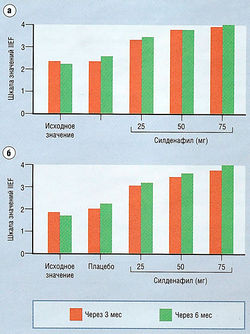
Силденафил эффективен при лечении эректильной дисфункции, вызванной широким спектром причин (рис. 17.17). Эрекция возникает у 65-70% пациентов (у больных диабетом процент немного ниже). Степень эрекции при интракавернозном введении выше, но удобство пероральной формы обусловливает большую ее распространенность.
Рис. 17.17 Эректогениый эффект силденафила. Улучшение возможности попыток (а) и стабильной эрекции (б) после 3 мес и б мес приема препарата, оцениваемой пациентами по международному индексу эректильной функции (IIEF).
Основные неблагоприятные побочные эффекты силденафила — сердечно-сосудистые. Возможны также головная боль, нарушения носового дыхания, отеки. Все они, вероятно, следствие ингибирования ФДЭ-5, т.е. основного механизма действия препарата. Дисфагия и диспепсия, наблюдаемые при высоких дозах препарата, также могут быть связаны с ингибированием ФДЭ-5, в данном случае нижнего пищеводного сфинктера. В некоторых случаях пациенты пытаются самостоятельно устранить головную боль и диспепсию НПВС и антагонистами Н2-рецепторов соответственно.
Силденафил также вызывает у 5% пациентов обратимые нарушения зрения в форме изменений восприятия цвета (синяя аура). Это происходит из-за невысокой селективности, которую силденафил проявляет к ФДЭ-5 по сравнению с ФДЭ-6, участвующей в ретинальной передаче цветовосприятия (см. табл. 17.13).
Увеличивая концентрацию NO, силденафил также усиливает действие нитроглицерина, изосорбита и других средств на основе органических нитратов. Вследствие выраженной вазодилатации, опосредованной NO, это может привести к развитию значительной гипотензии. По этой причине использование силденафила абсолютно противопоказано пациентам, принимающим такие препараты.
Силденафил в основном элиминируется в печени посредством CYP3A4. Дозу препарата следует уменьшать у пожилых пациентов и при почечной и печеночной недостаточности. При приеме ингибиторов CYP3A4, например циметидина, кетоконазола и эритромицина, необходимо снижение дозы силденафила. Есть данные, что силденафил влияет на эффект вазоактивных агентов, например амлодипина и ингибиторов АПФ. Проблема сердечнососудистого риска беспокоит пациентов, принимающих силденафил, что также может оказывать отрицательное воздействие при использовании этого препарата.
Недавно для лечения эректильной дисфункции в клиническую практику был введен ингибитор ФДЭ-5 варденафил, который, предположительно, имеет более быстрое начало действия, чем силденафил. Тадалафил — препарат длительного действия с периодом полувыведения 17,5 час, что удобнее для пациента.
Таблица 17.14 Классификация лекарственных средств для лечения эректильной дисфункции
|
Действие |
Дисфункция | |
|
Начальная |
Длительная | |
|
Центральное |
Апоморфин |
Тестостерон |
|
Периферическое |
Простагландин Е, Методика Trimix |
Силденафил |
Лекарственные средства центрального действия, стимулирующие эрекцию
Многие пациенты с эректильной дисфункцией, как правило, имеют сопутствующую сердечно-сосудистую патологию, которая не диагностирована. Хотя силденафил радикально изменил лечение эректильной дисфункции, однако очевидно, что многие мужчины еще не обратились за медицинской помощью, поэтому следует подумать о безопасности будущей терапии. Существующие методы лечения влияют главным образом на периферические сосуды, перенаправляя кровь в расширенные сосуды полового члена. Однако есть и другие варианты (табл. 17.14).
Силденафил и интракавернозные средства действуют путем увеличения активности NO-системы или уменьшения активности СНС. СНС, осуществляя передачу нервных импульсов к половому члену, играет главную роль в формировании нормального сексуального ответа. В целях использования механизмов контроля СНС была выпущена сублингвальная форма дофаминового агониста апоморфина.
В целом, клинические данные показывают, что апоморфин в дозе 2 и 3 мг эффективен в терапии эректильной дисфункции, вызванной широким диапазоном причин. При использовании этого средства на восстановление нормальной сексуальной функции требуется менее 20 мин. Отмечается хорошая переносимость препарата, что делает апоморфин целесообразным дополнением в лекарственной терапии эректильной дисфункции.
Лечение эректильной дисфункции
- Революционный препарат в лечении эректильной дисфункции — пероральный ингибитор фосфодиэстеразы 5 силденафил. Силденафил действует местно, в отличие от средств, вводимых интракавернозно.
- Эффективным также может быть апоморфин центральный агонист дофамина
Преждевременное семяизвержение
При преждевременном семяизвержении иногда помогает применение местных обезболивающих средств (местных анестетиков).
ИНФЕКЦИИ МОЧЕВЫВОДЯЩИХ ПУТЕЙ[править | править код]
Инфекции мочевыводящих путей — частые инфекционные заболевания
Многие антимикробные средства экскретируются в мочу в неизменном виде и в высоких концентрациях. По этой причине низкие и относительно нетоксичные дозы многих классов антибиотиков эффективны при инфекциях мочевыводящих путей.
Большинство циститов вызывают бактериальные возбудители. Среди них Е. coli встречается наиболее часто — до 85% случаев. Эти бактерии чувствительны к широкому диапазону антибиотиков. Однако при нозокомиальных (госпитальных) инфекциях часто необходимо парентеральное введение антибиотиков. Исторически число микробных колоний, превышающее 105 в 1 мл, рассматривали как критерий для диагноза «инфекция мочевыводящих путей». В настоящее время считается, что 50% женщин с симптомами инфекции мочевыводящих путей имеют намного более низкий уровень обсеменения мочи. Кроме того, присутствие лейкоцитов в мочевом осадке слабо коррелирует с диагнозом «инфекция мочевыводящих путей».
Часто инфекция восходит вверх по уретре. Особенно это актуально для женщин, поскольку уретра у них более короткая, чем у мужчин, а влагалище колонизировано бактериями. Сексуальные контакты — главный фактор, вынуждающий молодых женщин использовать контрацептивные диафрагмы и спермициды, которые изменяют нормальную вагинальную флору, что существенно увеличивает риск циститов. Пиелонефрит наиболее часто возникает при проникновении инфекции из уретры, за исключением туберкулеза и корковых абсцессов почек. Гематогенный и лимфогенный пути распространения инфекции редки, но иногда может происходить контактное заражение от соседних органов.
Пиелонефриты и простатиты требуют интенсивной и длительной терапии (типичный срок лечения составляет 2-4 нед или даже более), в то время как при катаральных инфекционных заболеваниях (например, циститах) нужно всего нескольких дней терапии (в зависимости от выбранного антибиотика).
Возбудители инфекций мочевыводящих путей
- Escherichia coli
- Staphylococcus saprophyticus
- Klebsiella/Enterobacter
- Proteus
- Pseudomonas
- Enterococci
- Staphylococcus epidermidis
Можно проводить профилактическую терапию антибиотиками для предотвращения рецидивов. Женщин, имевших более трех эпизодов цистита, относят к этой группе пациентов. Оптимально профилактические препараты должны устранять патогенный агент и не вызывать бактериальной резистентности. Наиболее часто используются ко-тримоксазол — комбинацию триметоприма с сульфаметоксазолом.
Инфекции мочевыводящих путей классифицируют следующим образом:
- острый цистит;
- острый пиелонефрит;
- острый бактериальный простатит;
- хронический бактериальный простатит;
- небактериальный простатит;
- острый эпидидимит;
- простатодиния.
Схемы антибиотикотерапии представлены в табл. 17.15. В дополнение к антибиотикам при всех формах простатитов и простатодинии применяют доксазозин или теразозин в дозах, подобных тем, что используют при лечении ДГПЖ.
Таблица 17.15 Антибиотикотерапия инфекций мочевыводящих путей
|
Заболевание |
Антибиотик |
Форма |
Длительность |
|
Острый пиелонефрит |
Ампициллин 1 г каждые 6 час и гентамицин 1 мг/кг каждые 8 час |
в/в |
21 день |
|
Ко-тримоксазол 160/800 мг каждые 12 час |
орально |
21 день | |
|
Ципрофлоксацин 750 мг каждые 12 час |
орально |
21 день | |
|
Офлоксацин 200-300 мг каждые 12 час |
орально |
21 день | |
|
Хронический пиелонефрит |
Как при остром пиелонефрите, но продолжительность терапии З-6 мес | ||
|
Острый цистит |
Ко-тримоксазол 160/800 мг, 2 таблетки |
орально |
однократно |
|
Цефалексин 250-500 мг каждые 6 час |
орально |
1-3 дня | |
|
Ципрофлоксацин 250-500 мг каждые 12 час |
орально |
1-3 дня | |
|
Нитрофурантоин 100 мг каждые 12 час |
орально |
7 дней | |
|
Норфлоксацин 400 мг каждые 12 час |
орально |
1-3 дня | |
|
Офлоксацин 200 мг каждые 12 час |
орально |
1-3 дня | |
|
Острый бактериальный простатит |
Как при остром пиелонефрите |
21 день | |
|
Хронический бактериальный простатит |
Ко-тримоксазол 180/800 мг каждые 12 час |
орально |
1-3 мес |
|
Ципрофлоксацин 250-500 мг каждые 12 час |
орально |
1-З мес | |
|
Офлоксацин 200-400 мг каждые 12 час |
орально |
1-3 мec | |
|
Острый эпидидимит передающийся половым путем передающийся неполовым путем |
Цефтриаксон 250 мг однократно + доксициклин 100 мг каждые 12 час |
в/м орально |
10 дней |
|
Как при хроническом бактериальном простатите |
орально |
3 нед |
Интерстициальный цистит характеризуется общими признаками цистита (боли в области мочевого пузыря, частые мочеиспускания) при отсутствии какой-либо бактериальной инфекции. Точная причина заболевания пока не известна; вероятно, триггерным механизмом являются нарушения барьерной функции эпителия внутренней поверхности мочевого пузыря с повреждением гликозаминогликанов.
Типичные причины интерстициального цистита — частые инфекции мочевыводящих путей, радиация, цитотоксические лекарственные средства, а также неизвестные, обычно идиопатические причины. Клинические исследования показали, что терапия гиалуронатом натрия, заменяющим гликозаминогликан, эффективна в 80% случаев, хотя такое лечение стоит очень дорого. Кроме того, эффективно пероральное применение препарата полисульфата пеносана, восстанавливающего эпителий внутренней поверхности мочевого пузыря.
Литература[править | править код]
- Bill-Axelson A, Holmberg L, Ruutu М et al. The Scandinavian prostate cancer group study no. 4. Radical prostatectomy versus watchful waiting in early prostate cancer. N EnglJ Med 2005; 352: 1977-1984.
- David RD, De Blieux PMC, Press R. Rational antibiotic treatment of outpatient genitourinary infections in a changing environment. The American Journal of Medicine 2005; 118 (Suppl 1): 7-13.
- Franco AVM. Recurrent urinary tract infections. Best Practice & Research Clinical Obstetrics & Gynaecology 2005; 19: 861-873.
- Gemzell-Danielsson K, Mandl I, Marions L. Mechanisms of action of mifepristone when used for emergency contraception. Contraception 2003; 68: 471-476.
- McConnell JD, Roehrborn CC, Bautista OM et al. The Medical Therapy of Prostatic Symptoms (MTOPS) Research Group. The long-term effect of doxazosin, finasteride, and combination therapy on the clinical progression of benign prostatic hyperplasia. N Engl J Med 2003; 349: 2387-2398.
- Melman A, Bar-Chama N, McCullough A, Davies K, Christ G. The first human trial for gene transfer therapy for the treatment of erectile dysfunction: preliminary results. European Urology 2005; 48: 314-31 8.
- Mulhall JP, Montorsi F. Evaluating preference trials of oral phosphodiesterase 5 inhibitors for erectile dysfunction pean Urology 2006; 49: 30-37.
- OuslanderJG. Drug Therapy: Management of Overactive der. N EnglJ Med 2004; 350:786-799.
- Stief CG, Uckert S, Jonas U. Strategies in the oral pharmacotherapy of male erectile dysfunction viewed from bench and bedside (Part II). The Journal of Men’s Health & Gender 7 2: 325-332.