Экскреция (выведение) лекарственных средств
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Экскреция (выведение) лекарственных средств[править | править код]
Лекарственные средства выводятся из организма в неизмененном виде или в виде метаболитов. Полярные соединения экскретируются легче, чем неполярные, жирорастворимые (исключение составляет выведение через легкие), поэтому жирорастворимые препараты сначала превращаются в более полярные метаболиты.
Основной орган, отвечающий за выведение лекарственных средств и их метаболитов, — почки. С калом выводятся невсосавшиеся в кишечнике вещества, а также препараты (и их метаболиты), которые секретируются в желчь или непосредственно в ЖКТ и затем не подвергаются повторному всасыванию. Лекарственные средства, которые выводятся с грудным молоком, могут оказать неблагоприятное действие на ребенка. Легкими выводятся в основном газообразные и летучие соединения и, в очень незначительном количестве, некоторые другие лекарственные средства и их метаболиты.
Выведение с мочой[править | править код]
Лекарственные средства могут фильтроваться в почечных клубочках, секретироваться в просвет канальцев и реабсорбироваться из канальцев обратно в плазму. Возрастные изменения функции почек обычно затрагивают эти физиологические процессы в равной степени. У новорожденных функция почек снижена; в течение первых месяцев жизни происходит ее быстрое становление. У пожилых функция почек может быть существенно нарушена, так как в течение жизни она постепенно снижается со скоростью примерно 1% в год.
Количество профильтровавшегося в клубочках лекарственного средства зависит от СКФ и степени связывания препарата с белками плазмы (фильтруется только свободный препарат). В проксимальных почечных канальцах лекарственные средства могут дополнительно секретироваться путем активного транспорта. В роли переносчика амфифильных анионов выступает Р-гликопротеид, а конъюгированных метаболитов (продукты конъюгации с глюкуроновой кислотой, сульфатом и глутатионом) — белок MRP2 (белок полирезистентности-2). Эти переносчики локализуются в мембране щеточной каемки апикальной поверхности эпителиальных клеток.
Сходные системы транспорта органических катионов секретируют препараты, представляющие собой органические основания. Реабсорбируются лекарственные средства главным образом путем неионной диффузии, хотя существуют и системы активного транспорта из просвета канальцев в плазму (эти системы локализуются в основном в дистальных почечных канальцах).
В неионизированной форме слабые кислоты и основания пассивно реабсорбируются в проксимальных и дистальных канальцах по концентрационному градиенту, возникающему благодаря реабсорбции воды. Ионизированные формы слабых электролитов хуже проникают через мембрану эпителиальных клеток канальцев. Таким образом, пассивная реабсорбция слабых электролитов зависит от pH мочи. При ощелачивании мочи слабые кислоты присутствуют в ней преимущественно в ионизированной форме и потому хуже реабсорбируются и в большей степени экскретируются. При закислении мочи, напротив, экскреция слабых кислот снижается. Для слабых оснований ситуация обратная. Ощелачивание и закисление мочи используют при отравлениях некоторыми лекарственными средствами для усиления их почечной экскреции. Степень влияния pH мочи на экскрецию лекарственного средства зависит от выраженности и стойкости изменения pH, а также от того, какой вклад вносит пассивная реабсорбция путем неионной диффузии (см. выше) в элиминацию препарата. Наиболее ощутимо pH мочи влияет на экскрецию слабых кислот и оснований, наполовину диссоциированных при pH от 5 до 8 (то есть в диапазоне колебаний pH мочи). Вместе с тем экскреция и относительно сильных кислот, например салицилатов, возрастает в 4—6 раз при ощелачивании мочи с pH от 6,4 до 8. Доля неионизированных салицилатов при этом уменьшается с 1 до 0,04%.
Выведение с желчью и калом[править | править код]
Аналогичные транспортные системы в мембране гепатоцитов активно секретируют лекарственные средства и их метаболиты в желчь. Р-гликопротеид транспортирует амфифильные и жирорастворимые препараты, а белок MRP2 — в основном конъюгированные метаболиты (продукты конъюгации с глутатионом и глюкуроновой кислотой, некоторые сульфаты). Белок MRP2 участвует также в транспорте эндогенных соединений. Врожденное отсутствие этого белка приводит к синдрому Дубина—Джонсона. Органические катионы секретируются в желчь также путем активного транспорта. В кишечник лекарственные средства и их метаболиты попадают с желчью или непосредственно из крови, так как в апикальной мембране энтероцитов тоже присутствуют белки-переносчики, транспортирующие эти вещества в просвет кишечника (например, Р-гликопротеид). Из кишечника препараты и их метаболиты могут вновь всасываться в кровь (конъюгированные метаболиты, например глюкурониды, предварительно гидролизуются кишечной микрофлорой) и возвращаться в печень. При значительном кишечно-печеночном кругообороте время действия препарата существенно увеличивается.
Другие пути выведения[править | править код]
Довольно большое количество лекарственного средства может выводиться с потом, со слюной и слезами. Таким путем выводятся в основном неионизированные жирорастворимые препараты, которые проходят через эпителиальные клетки потовых, слюнных и слезных желез путем диффузии. Экскреция слабых электролитов зависит от градиента pH. Лекарственные средства, которые выводятся со слюной, попадают в полость рта и обычно проглатываются. Концентрации некоторых препаратов в слюне и в сыворотке изменяются параллельно друг другу, поэтому в тех случаях, когда получить пробу крови трудно, можно ориентироваться на концентрацию лекарственного средства в слюне. То же самое справедливо и в отношении молока. Поскольку pH молока ниже, чем крови, концентрация основных веществ в молоке может быть чуть выше, чем в крови, а концентрация кислых — наоборот. Неэлектролиты (этанол, мочевина) легко проникают в молоко независимо от pH и достигают в нем той же концентрации, что и в сыворотке. Накопление лекарственных средств в волосах и коже имеет значение для судебно-медицинских исследований.
Пресистемное выведение[править | править код]
Источник: «Наглядная фармакология».
Автор: X. Люльман. Пер. с нем. Изд.: М.: Мир, 2008 г.
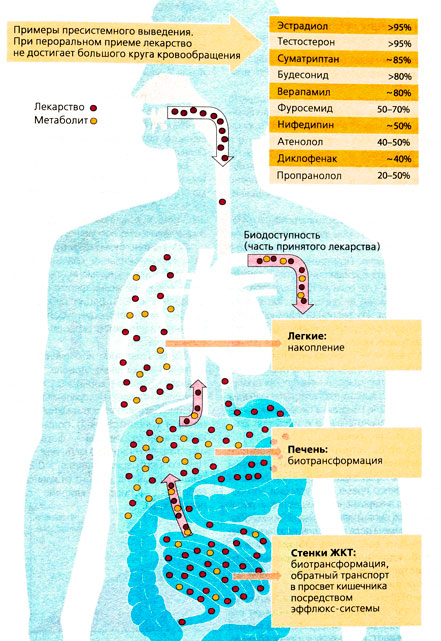
В зависимости от своих физико-химических свойств лекарства по-разному действуют на поверхности и внутри клеток, а также участвуют в бактериальном обмене веществ. Всегда, когда необходима системная терапия и нельзя использовать местные лекарственные средства, при обсуждении фармакокинетики надо учитывать влияние дополнительных факторов. Рассмотрим пероральный прием лекарства. Проследим «судьбу» лекарства до достижения им большого круга кровообращения.
1) Вещество проходит барьер кишечного эпителия и попадает в клетки слизистой оболочки (энтероциты), но Р-гликопротеины транспортируют его обратно. Тем самым в действительности происходит всасывание лишь небольшого количества лекарства. Прием одного и того же препарата может иметь неодинаковые последствия, так как у разных пациентов процесс всасывания протекает по-разному и зависит от приема других лекарств.
2) Действие вещества на пути от кишечника до большого круга кровообращения может быть ослаблено из-за взаимодействия с ферментами, например с цитохром оксид азой.
а) Лекарство способно разрушаться уже в кишечном эпителии. Активность цитохромоксидазы может усиливаться или блокироваться другими веществами. Например, грейпфрутовый сок тормозит действие СУРЗА4-оксидазы в кишечной стенке; в результате концентрация принимаемого препарата может возрасти и достичь токсического уровня.
б) Большую роль играет обмен веществ в печени, где происходит обезвреживание ядов. Ферменты печени так видоизменяют химически родственные и чужеродные организму вещества, что они затем могут выводиться. Количество вещества, достигшее венозной крови, зависит от того, сколько лекарства получено из печени и метаболизировано. Важно, что синтез ферментов (увеличение объема гладкого эндоплазматического ретикулума) может индуцироваться другими лекарствами.
Этот путь лекарства в организме называют «пресистемным выведением».
3) При парентеральном приеме лекарства пресистемное выведение исключается. Лекарство после инъекции в вену попадает через полую вену в правое предсердие, затем в легкие, левое предсердие, наконец, пройдя большой круг кровообращения, в коронарную систему. Легкие, богатые липидами и имеющие большую поверхность, принимают значительную часть амфифильных и липофильных лекарственных веществ, а при падении концентрации лекарства в крови легкие медленно возвращают его обратно. При быстром введении лекарства путем внутривенных инъекций легкие действуют как буфер, защищая сердце от высоких концентраций вещества.
В определенных ситуациях высокий уровень пресистемного выведения может быть желательным. Важный пример — применение глюкокортикоидов при астме, когда основное количество введенного путем ингаляции лекарства проглатывается, и благодаря пресистемному выведению нагрузка на организм весьма незначительна. Примером положительной роли пресистемного выведения являются превращения ацетилсалициловой кислоты, которую назначают в целях снижения тромбообразования.
ЭКСКРЕЦИЯ ЛЕКАРСТВ[править | править код]
Категория:
«Фармакология».
Лекарства экскретируются из организма различными путями: через почки (моча), кишечный тракт (желчь и фекалии), легкие (выдыхаемый воздух), материнское молоко и пот. Экскреция с мочой и фекалиями — наиболее важные пути элиминации лекарств.
Экскреция лекарств
- Почечная и фекальная экскреция — наиболее важные пути элиминации лекарств
- Некоторые лекарственные конъюгаты гидролизуются в нижнем отделе ЖКТ с образованием исходного лекарства, которое реабсорбируется (процесс энтерогепатической циркуляции), тем самым увеличивая продолжительность действия лекарства
- Часть введенной дозы некоторых лекарств, экскретируемая почками в неизмененном виде, зависит от pH мочи
- Клиренс креатинина может быть использован для определения поражения почек и как показатель необходимости снижения дозы, если экскреция почками играет существенную роль в элиминации лекарства больным раком и с недостаточностью экспрессии изоформы UGTIA1 глюкуронозилтрансферазы следует снизить дозу иринотекана, ингибитора топоизомеразы I, чтобы уменьшить вероятность возникновения миелосупрессии и диареи.
Экскреция через почки[править | править код]
Экскреция через почки осуществляется путем фильтрации и секреции. Фильтрация происходит в клубочках почек, секреция — по ходу нефрона. При заболеваниях почек процесс экскреции некоторых лекарств нарушается. Почечная экскреция многих лекарств коррелирует со способностью почек экскретировать креатинин. Если трудно или невозможно определить функцию почек непосредственно, измеряя 24-часовой клиренс креатинина, почечную функцию можно определить, используя общепринятый алгоритм Кокрофта и Голта. Эти исследователи установили соотношение между возрастом пациента, массой его тела и концентрацией креатинина в сыворотке (Cs cr), из которого можно вычислить клиренс креатинина (С1сг) почками у пациентов мужского пола:
Сlсr (мл/мин) = [(140 - возраст) X идеальная МТ (кг)] / [0,8145 X Cscr (мкмоль/л)]
Для женщин величину клиренса креатинина нужно умножить на 0,85.
Экскреция креатинина почками осуществляется за счет фильтрации и секреции, но по мере снижения функции почек возрастает величина секретируемой фракции. Возможно, что это соотношение применимо ко всем лекарствам, которые фильтруются и секретируются почками.
Различные способы повышения экскреции лекарств почками
На основании соотношения между рКа и pH мочи определяют долю ионизированного лекарства и, соответственно, его количество после фильтрации, не способное реабсорбироваться путем диффузии через люминальную поверхность нефрона. Так, салициловая кислота, относящаяся к слабым кислотам (рКа 3,0), в основном метаболизируется до экскреции с мочой. Однако по мере повышения pH мочи все большая часть дозы теряется с мочой. И действительно, для лечения интоксикации, вызванной салицилатами, может быть использовано подщелачивание мочи с помощью перорального или парентерального введения бикарбонатов с целью повышения элиминации салициловой кислоты почками. Этот способ также может быть полезен в случае передозировки фенобарбитала.
Повышение оттока мочи увеличивает элиминацию некоторых лекарств почками, поскольку при этом сокращается время контакта вещества с люминальной поверхностью и тем самым уменьшается время для реабсорбции неионизированных молекул.
Экскреция через желудочно-кишечный тракт[править | править код]
Удаление лекарств из ЖКТ можно ускорить применением лаважного электролитного раствора полиэтиленгликоля. Большие объемы этого раствора можно либо принять внутрь, либо ввести в ЖКТ через назогастральную трубку, чтобы усилить кишечную перистальтику и ускорить экскрецию неабсорбированного лекарства через прямую кишку. Уменьшение времени прохождения через ЖКТ связано с индукцией диареи и снижением абсорбции питательных веществ, однако в острой ситуации это не имеет клинического значения.
Энтерогепатическая циркуляция удлиняет фармакологический эффект некоторых лекарств
Некоторые конъюгаты лекарств, экскретируемые в желчь, гидролизуются в нижнем отделе тонкой кишки, высвобождая исходное лекарство, которое реабсорбируется в кровоток, благодаря чему действие лекарства удлиняется. Этот процесс рециклирования называют энтерогепатической циркуляцией. Например, клиническое значение имеют следующие процессы:
- энтерогепатическая циркуляция седативного снотворного лекарства лоразепама включает гидролиз его глюкуронидного конъюгата в нижнем отделе тонкой кишки;
- предполагается, что отсутствие эффекта оральной контрацепции может быть обусловлено ингибированием энтерогепатической циркуляции после антибиотикотерапии, в результате которой удаляются кишечные бактерии, гидролизующие стероидный конъюгат, поэтому клиренс стероидов усиливается, и становится более вероятным исчезновение контрацептивного эффекта.
Экскреция через легкие[править | править код]
Летучие лекарства экскретируются через легкие. Такой путь имеет основное значение для анестетиков общего действия газо- или парообразной форме. Эти анестетики вводятся и выводятся через легкие, давая возможность легко контролировать анестезию с помощью коррекции концентрации анестетика во вдыхаемой газовой смеси. Экскреция через легкие позволяет осуществлять мониторинг концентрации выдыхаемого анестетика в конце спокойного выдоха, что может служить суррогатным показателем уровня анестезии. Этанол экскретируется через легкие в небольших количествах. Этот путь элиминации для этанола количественно незначим, однако он стал основой неинвазивного метода определения концентрации этанола в крови для юридических целей.
Читайте также[править | править код]
- Пути введения лекарственных средств
- Абсорбция
- Распределение лекарственных средств
- Метаболизм препаратов и лекарств
- Клиренс лекарственных средств
- Период полувыведения (полужизни)
- Фармакокинетика
- Влияние пола, возраста, наследственности на действие лекарственных средств
- Взаимодействие лекарственных средств
- Влияние заболеваний на действие лекарства