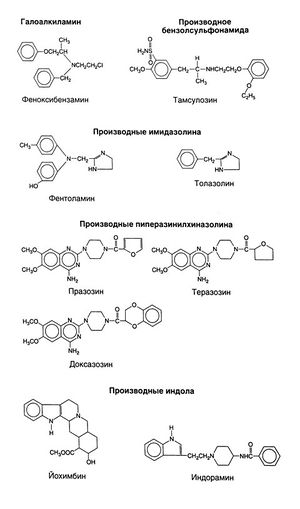
Альфа-адреноблокаторы
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Адреноблокаторы[править | править код]
Многие препараты препятствуют влияниям симпатической нервной системы, тем самым существенно изменяя деятельность органов с симпатической иннервацией. Некоторые из них имеют важное клиническое значение, особенно для лечения сердечно-сосудистых заболеваний. Мы остановимся на адреноблокаторах — препаратах, препятствующих действию норадреналина, адреналина и ряда других адренергических средств на адренорецепторы.
Почти все средства этой группы являются обратимыми конкурентными блокаторами α- или β-адренорецепторов. Исключение составляет феноксибензамин — необратимый α-адреноблокатор, образующий с рецепторами ковалентную связь. Разные типы и подтипы адренорецепторов существенно отличаются по структуре. Разработка средств с разным сродством к разным адренорецепторам позволила избирательно устранять симпатические влияния на те или иные органы. Так, β1-адреноблокаторы подавляют эффекты адреналина и норадреналина на сердце, но мало влияют на активацию β2-адренорецепторов бронхов и совсем не влияют на реакции, опосредованные α, - и α2-адренорецепторами. Для понимания фармакологических свойств и клинических эффектов адреноблокаторов важно знать физиологию вегетативной нервной системы и точки приложения адренергических средств.
Альфа-адреноблокаторы[править | править код]
Многие физиологические эффекты катехоламинов опосредованы α-адренорецепторами. К важнейшим таким эффектам относится сужение артерий и вен, обусловленное активацией α1 -адренорецепторов. Стимуляция α2-адренорецепторов приводит к снижению симпатического тонуса, повышению парасимпатического тонуса, облегчению агрегации тромбоцитов, подавлению высвобождения ацетилхолина и норадреналина из нервных окончаний, снижению секреции инсулина и угнетению липолиза. Активация этих рецепторов сопровождается также сужением артерий и вен в некоторых сосудистых бассейнах.
Фармакологические свойства и химическое строение α-адреноблокаторов разнообразны. Некоторые из этих средств обладают выраженной избирательностью по отношению к α1- или α2-адренорецепторам. Так, празозин гораздо активнее в отношении α1-адренорецепторов, а йохимбин — α2-адренорецепторов; сродство же фентоламина к обоим подтипам α-адренорецепторов примерноодинаково. Недавно появились препараты, действующие на отдельные подгруппы в пределах одного подтипа адренорецепторов. Так, тамсулозин активнее в отношении α1А-адренорецепторов, чем α1В-адренорецепторов. Химические свойства. Формулы некоторых а-адреноблокаторов приведены на рис. 10.4. Эти разнородные по строению вещества можно разделить на несколько групп, в том числе — галоалкиламины, производные имидазолина, производные пипера-зинилхиназолина и производные индола.
Фармакологические свойства[править | править код]
Сердечно-сосудистая система. Важнейшие с клинической точки зрения эффекты α-адреноблокаторов связаны с их влиянием на сердечно-сосудистую систему. Оно обусловлено как центральным, так и периферическим действием, а конечный результат зависит от состояния сердечно-сосудистой системы в момент введения препаратов и от соотношения их сродства к α1- и α2-адренорецепторам.
Альфа1-адреноблокаторы. Блокада α1-адренорецепторов препятствует сосудосуживающему действию эндогенных катехоламинов. Это может сопровождаться расширением артериол и вен и снижением АД. Выраженность этого эффекта зависит от симпатического тонуса; поэтому она больше в положении стоя, и особенно — при гиповолемии. В большинстве случаев гипотензивное действие α-адреноблокаторов компенсируется барорефлекторными реакциями — повышением ЧСС и сердечного выброса и задержкой жидкости. Эти реакции еще больше усиливаются, если препарат блокирует α2-адренорецепторы симпатических окончаний, что приводит к усиленному высвобождению норадреналина и стимуляции постсинаптических β1-адренорецепторов сердца и юкстагломерулярных клеток (Langer, 1981; Starke et al., 1989; см. также гл. 6). Активация а-адренорецепторов сердца может сопровождаться повышением сократимости, однако не известно, какое значение может иметь блокада этих рецепторов у человека.
Блокада α1-адренорецепторов препятствует также сосудосуживающему и прессорному действию экзогенных адренергических средств. Конечная реакция при этом зависит от того, какое именно адренергическое средство вводится: реакция на фенилэфрин подавляется полностью, на норадреналин — лишь частично (не устраняется его стимулирующее действие на β1-адренорецепторы сердца), а реакция на адреналин может измениться на депрессорную (парадоксальную) из-за его стимулирующего действия на сосудистые β2-адренорецепторы.
Альфа2-адреноблокаторы. Альфа2-адренорецепторы играют важную роль в регуляции влияний симпатической нервной системы — как на центральном, так и на периферическом уровне. Как уже говорилось, стимуляция пресинаптических α2-адренорецепторов подавляет высвобождение норадреналина из симпатических окончаний. Активация же α2-адренорецепторов ствола мозга приводит к снижению симпатического тонуса и АД; именно так действует клонидин. Напротив, блокада α2-адренорецепторов (например, йохимбином) сопровождается повышением симпатического тонуса и высвобождения норадреналина из симпатических окончаний; это приводит к стимуляции α1-адренорецепторов сосудов и β1-адренорецепторов сердца и, следовательно, к повышению АД (Goldberg and Robertson, 1983). Препараты, блокирующие и α1-, и α2-адренорецепторы, также вызывают повышение симпатического тонуса и высвобождения норадреналина, но не подъем АД — блокада α1-адренорецепторов препятствует сужению сосудов.
В некоторых сосудах имеются α2-адренорецепторы, активация которых приводит к сокращению гладких мышц, однако считается, что на эти рецепторы действуют преимущественно катехоламины крови, а на α1-адренорецепторы — выделяемый симпатическими окончаниями норадреналин (Davey, 1987; van Zwieten, 1988). В ряде других сосудов стимуляция α2-адренорецепторов вызывает расслабление гладких мышц, опосредованное выделением N0. Роль этих рецепторов в регуляции органного кровотока не ясна (Cubeddu, 1988). В подкожной вене ноги человека стимуляция α2-адренорецепторов приводит к сокращению гладких мышц, а в тыльных венах кисти преобладают α-адренорецепторы (Haefeli et al., 1993; Gavin et al., 1997). Как бы то ни было, центральные эффекты α2-адреноблокаторов и их действие на симпатические окончания явно преобладают над их прямыми влияниями на сосуды.
Прочие органы. Альфа-адреноблокаторы влияют и на другие гладкомышечные органы. Так, они тормозят сокращения пузырного треугольника, сфинктера мочевого пузыря и гладких мышц предстательной железы; в результате облегчается отток мочи. Недавно было показано, что в вызванных катехоламинами сокращениях гладких мышц предстательной железы важную роль играют α1А-адренорецепторы (Ruffolo and Hieble, 1999). Стимуляция α-адренорецепторов может сопровождаться сокращением гладких мышц бронхов, но эффект этот выражен слабо. Катехоламины вызывают мобилизацию глюкозы из печени; у человека это действие опосредовано преимущественно β-адренорецепторами, хотя определенный вклад вносят и α-адренорецепторы (Rosen et al., 1983). Стимуляция α2А-адренорецепторов облегчает агрегацию тромбоцитов, но последствия блокады тромбоцитарных α-адренорецепторов in vivo пока не ясны. Стимуляция α2-адренорецепторов островков поджелудочной железы при. водит к выраженному торможению секреции инсулина соответственно, блокада этих рецепторов может приводить к облегчению высвобождения данного гормона (Kas-hiwagietal., 1986).
Феноксибензамин[править | править код]
Феноксибензамин — это необратимый блокатор α1- и α2-адренорецепторов. Его активность в отношении α1-адренорецепторов несколько выше, однако не известно играет ли это какую-либо роль у человека.
Химические свойства. Адреноблокаторы из группы галоалкиламинов по своей структуре близки к азотистым ипритам. И для тех, и для других характерно замыкание одной из хлорэтильных групп в положительно заряженное этилениминовое кольцо с высвобождением аниона хлора и образованием карбкатиона (гл. 52). Последний, видимо, играет важнейшую роль в блокад адренорецепторов. Предполагается, что за сродство к адренорецепторам отвечает арил алкильная группа, так как сам по себе образующийся каркатион, очевидно, способен реагировать с сульфгидрильными. карбоксильными и аминогруппами многих белков. Вследствие описанных реакций феноксибензамин образует ковалентные связи с α-адренорецепторами и тем самым вызывает их необратимую блокаду. Восстановление чувствительности тканей к α-адреностимуляторам обусловлено, по-видимому, синтезом новых рецепторов.
Фармакологические свойства. Основные эффекты феноксибензамина обусловлены блокадой α-адренорецепторов гладких мышц. Он вызывает снижение ОПСС и повышение сердечного выброса, частично обусловленное рефлекторным повышением симпатического тонуса. Возникающая при этом тахикардия усиливается в результате повышенного высвобождения норадреналина (из-за блокады пресинаптических α2-адренорецепторов) и сниженной его инактивации (из-за подавления нейронального и экстранейронального захвата; см. ниже и гл. 6). Прессорный эффект экзогенных катехоламинов уменьшается; более того, адреналин на фоне феноксибензамина вызывает снижение АД вследствие активации сосудистых бета-адренорецепторов. У лиц с нормальным АД феноксибензамин в положении лежа почти не вызывает артериальной гипотонии, однако при переходе в положение стоя у них на фоне приема феноксибензамина наблюдается выраженная ортостатическая гипотонии (отсутствует рефлекторное сужение сосудов). Кроме того, нарушаются компенсаторные реакции на гиповолемию и на вызванную средствами для обшей анестезии вазодилатацию.
Феноксибензамин подавляет как нейрональный, так и экстранейрональный захват катехоламинов. Галоалкиламины не только блокируют а-адренорецепторы, но и вызывают необратимое снижение реакций на серотонин, гистамин и ацетилхолин. Для достижения этого последнего эффекта требуются несколько большие дозы феноксибензамина, чем для блокады α--адренорецепторов. Подробнее с фармакологическими свойствами галоалкиламинов можно ознакомиться в обзорах Nickerson and Hollenberg (1967) и Furchgott (1972), а также в предыдущих изданиях настоящей книги.
Фармакокинетика феноксибензамина изучена недостаточно. Его Т1/2, видимо, меньше 24 ч. Однако, поскольку он вызывает необратимую блокаду α-адренорецепторов, длительность его действия зависит не только от времени его присутствия! крови, но и от скорости синтеза этих рецепторов. Для восстановления нормальной плотности полноценных α-адренорецепторов на поверхности клеток требуется, возможно, не-сколькосуток (Hamilton et al., 1982). Реакция на катехоламины может восстановиться раньше, так как на гладких мышцах сосудов имеются так называемые резервные α1-адренорецепторы (Hamilton et al., 1983).
Применение. Основное показание к феноксибензамину — феохромоцитома. Это опухоль из мозгового вещества надпочечников или из симпатических ганглиев, вырабатывающая огромные количества катехоламинов. В результате развивается артериальная гипертония с резкими подъемами ДЦ (катехоламиновыми кризами). Лечение в большинстве случаев хирургическое, однако в ожидании операции часто назначают феноксибензамин. Это позволяет предупредить катехоламиновые кризы и уменьшить другие осложнения, связанные с избытком катехоламинов, например гиповолемию и повреждение миокарда. Обычно феноксибензамин назначают за 1—3 нед до операции, сначала 10 мг 2 раза в сутки, затем дозу с интервалами в сутки увеличивают до тех пор, пока АД не стабилизируется на удовлетворительном уровне. Иногда дозу приходится ограничивать из-за развития ортостатической гипотонии. Еще один неприятный побочный эффект — заложенность носа. В целом же обычная суточная доза феноксибензамина при феохромоцитоме составляет— 120 мг в 2—3 приема. Впрочем, некоторые специалисты предпочитают проводить операцию без предварительного назначения феноксибензамина (Boutros et al., 1990). При неоперабельной или злокачественной феохромоцитоме может понадобиться длительный прием этого препарата. У некоторых больных, особенно со злокачественной феохромоцитомой, в дополнение к феноксибензамину назначают метирозин (Brogden et al., 1981; Perry et al., 1990). Этот препарат ингибирует тирозингидроксилазу — фермент, катализирующий лимитирующую реакцию синтеза катехоламинов (гл. 6). Применяют также p-адреноблокаторы, но только на фоне α-адреноблокаторов (см. ниже).
Феноксибензамин был первым α-адреноблокатором, который стали применять при аденоме предстательной железы. Блокада α-адренорецепторов гладких мышц этой железы и сфинктера мочевого пузыря позволяет улучшить отток мочи и уменьшить никтурию (Caine et al., 1981). Сегодня при этом заболевании применяют более эффективные и безопасные α-адреноблокаторы, например теразозин (см. ниже). Феноксибензамин применялся также для устранения вегетативной гиперрефлексии при перерыве спинного мозга (Braddom and Rocco, 1991).
Побочные эффекты. Главный побочный эффект феноксибензамина — ортостатическая гипотония, которая часто сочетается с рефлекторной тахикардией и нарушениями ритма сердца. Она бывает особенно тяжелой при гиповолемии и при состояниях, сопровождающихся расширением сосудов (прием вазодилататоров, физическая нагрузка, употребление алкоголя или большого количества пиши). Нарушение сокращения гладких мышц семявыносящих и семявыбрасывающих протоков приводит к обратимым аспермии и расстройствам эякуляции. При проведении мутационного теста Эймса феноксибензамин оказывает мутагенный эффект, а у животных при повторном введении вызывает развитие сарком брюшины и опухолей легких (1 ARC, 1980). Клиническое значение этих фактов не установлено.
Фентоламин и толазолин[править | править код]
Производное имидазолина фентоламин — это конкурентный α-адреноблокатор, обладающий примерно одинаковым сродством к α1- и α2-адренорецепторам. Его влияния на сердечно-сосудистую систему почти такие же, как у феноксибензамина. Кроме того, фентоламин блокирует серотониновые рецепторы и вызывает высвобождение гистамина из тучных клеток. Обнаружено также, что он блокирует калиевые каналы (McPherson, 1993). Толазолин близок к фентоламину, но обладает несколько меньшей активностью. Толазолин и фентоламин оказывают стимулирующее действие на гладкие мышцы ЖКТ, устраняемое атропином. Они повышают также секрецию соляной кислоты в желудке, а толазолин, кроме того, стимулирует секрецию слюнных, слезных и потовых желез.
Фармакокинетика фентоламина почти не изучена; известно только, что он в значительной степени метаболизируется. Толазолин хорошо всасывается из ЖКТ и выделяется с мочой.
Применение. Фентоламин используют при катехоламиновых кризах у больных феохромоцитомой. Его следует применять осторожно — быстрое в/в введение может привести к резкому падению АД Еще одно показание к фентоламину при феохромоцитоме — паралитическая кишечная непроходимость, обусловленная тормозящим действием катехоламинов на гладкие мышцы ЖКТ. Фентоламин вводят местно для предупреждения некроза кожи, развивающегося при случайном попадании в ткани α-адреностимулятора при в/в введении. Его используют также при гипертонических кризах, обусловленных отменой клонидина или употреблением тираминсодержащих продуктов одновременно с ингибиторами МАО. Однако, хотя в развитии этих кризов важную роль играет чрезмерная активация α-адренорецепторов, данных об эффективности и о безопасности фентоламина в сравнении с другими препаратами при этих состояниях мало. Предлагалось вводить фентоламин с папаверином в пещеристые тела полового члена при импотенции (Sidi, 1988; Zentgraf et al., 1988), однако долговременная эффективность такого лечения не определена. Введение в пещеристые тела фентоламина может привести к приапизму (его можно устранить α-адреностимуляторами, например фенилэфрином) и ортостатической гипотонии. При повторных введениях фентоламина может развиться фиброз полового члена (Sidi, 1988). Есть данные о том, что при импотенции иногда бывает эффективным прием фентоламина внутрь (Zorgniotti, 1994; Becker et al., 1998).
Толазолин применяют при стойкой легочной гипертензии новорожденных (вместо него можно использовать ингаляции NO и введение препаратов простагландинов; Gouyon and Francoise, 1992) и для улучшения видимости дистальных сосудов при артериографии (Gouyon and Francoise, 1992; Wilms et al., 1993).
Побочные эффекты. Главный побочный эффект фентоламина — артериальная гипотония. Кроме того, из-за рефлекторных реакций могут развиться выраженная тахикардия, нарушения ритма сердца и ишемия миокарда вплоть до инфаркта. Действие фентоламина на ЖКТ может приводить к боли в животе, тошноте, обострению язвенной болезни. Таким образом, фентоламин следует применять с особой осторожностью при ИБС и язвенной болезни.
Празозин и сходные препараты[править | править код]
Празозин — главный представитель производных пипе-разинилхиназолина. Это очень активный и высокоизбирательный препарат: его сродство к α1-адренорецепторам примерно в 1000 раз выше, чем к α2-адренорецепторам. На α1А-, α1В- и α1D-адренорецепторы он действует примерно одинаково. Кроме того, празозин является сравнительно мощным ингибитором фосфодиэстеразы — более того, именно с этой целью он и был первоначально разработан (Hess, 1975). Празозин — один из самых распространенных гипотензивных препаратов, и его фармакологические свойства подробно изучены.
Фармакологические свойства. Празозин. Основные эффекты празозина обусловлены блокадой α1-адренорецепторов артериол и вен. Это приводит к снижению ОПСС и венозного возврата. Празозин, в отличие от многих других вазодилататоров, обычно не вызывает повышение ЧСС. Это обусловлено несколькими причинами. Во-первых, в терапевтических дозах празозин практически не действует на α2-адренорецепторы и поэтому, видимо, не усиливает высвобождение норадреналина из симпатических окончаний в сердце. Во-вторых, празозин снижает преднагрузку сердца (в отличие, например, от гидралазина, почти не вызывающего расширение вен) и поэтому почти не увеличивает ни сердечного выброса, ни ЧСС. Наконец, есть данные о том, что празозин снижает симпатический тонус благодаря центральному действию (Cubeddu, 1988). У больных артериальной гипертонией празозин, по-видимому, тормозит барорефлекс (Sasso and O’Conner, 1982). Празозин и сходные с ним средства оказывают благоприятное, хотя и не очень выраженное, действие на липидный состав крови у человека — они снижают уровень ЛПНП и триглицеридов и повышают уровень ЛПВП. Клиническое значение этого феномена пока не ясно. Наконец, празозин и другие производные пи-перазинилхиназолина могут влиять на клеточный рост, причем это влияние не связано с их α1-адреноблокирующим действием (Yang et al., 1997; Ни etal., 1998).
Празозин хорошо всасывается из ЖКТ. При приеме внутрь его биодоступность составляет 50—70%, а максимальная сывороточная концентрация обычно достигается через 1—3 ч. Празозин в значительной степени связывается с белками плазмы (лишь 5% пребывает в крови в свободном виде), преимущественно с кислым а,-глико-протеидом. Поэтому при изменениях концентрации этого белка в крови (например, при воспалении) может изменяться и величина свободной фракции празозина (Rubin and Blashke, 1980). Элиминация празозина осуществляется в основном путем печеночного метаболизма — в неизмененном виде с мочой выделяется лишь незначительная его часть. Т1/2 составляет 2—3 ч, но при сердечной недостаточности он может возрастать до 6—8 ч. Длительность гипотензивного действия — обычно 7—10 ч.
При лечении празозином обычно начинают с 1 мг на ночь (желательно, чтобы после первой дозы больной оставался в положении лежа в течение нескольких часов во избежание ортостатической гипотонии). Затем назначают 1 мг 2—3 раза в сутки и далее дозу увеличивают в зависимости от АД. Максимальный гипотензивный эффект обычно достигается при дозе в 20 мг/сут. Если празозин используют для облегчения оттока мочи при аденоме предстательной железы, то его доза обычно составляет 1—5 мг 2 раза в сутки. Необходимость принимать празозин 2 раза в сутки причиняет некоторые неудобства, и современные а,-адреноблокаторы этого недостатка лишены.
Теразозин. Этот препарат по структуре очень близок к празозину (Kyncl, 1993; Wilde etal., 1993). Активность его несколько ниже, чем у празозина, но избирательность столь же высока. Как и празозин, он действует примерно одинаково на α1А-, α1B- и α1D-адренорецепторы. Основные же отличия этих двух препаратов касаются их фармакокинетики. Теразозин более водорастворим и обладает большей биодоступностью (> 90%) при приеме внутрь (Cubeddu, 1988; Frishmanetal., 1988). Это позволяет легче подбирать дозу. Т1/2 составляет около 12 ч, а продолжительность действия — больше 18 ч. Поэтому в большинстве случаев как при артериальной гипертонии, так и при аденоме предстательной железы теразозин можно принимать 1 раз в сутки. При аденоме предстательной железы теразозин оказался эффективнее финастерида (Lepor et al., 1996). Элиминация теразозина осуществляется в основном путем метаболизма — в неизмененном виде с мочой выделяется лишь 10%. Лечение обычно начинают c 1 мг, затем дозу постепенно увеличивают, ориентируясь на клинический эффект. Для достижения максимального эффекта при аденоме предстательной железы иногда требуются дозы до 10 мг/сут.
Доксазозин. Это также структурный аналог празозина обладающий высокой избирательностью по отношении к a1-адренорецепторам, но не по отношению к их под. группам (a1А-, α1B- и α1D-адренорецепторам). Как и теразозин, он отличается от празозина в основном по фармакокинетическим свойствам (Babamoto and Hirokawa 1992). Его Т1/2 составляет около 20 ч, а продолжительность действия может достигать 36 ч (Cubeddu, 1988) Биодоступность и характер элиминации (преимуществ венно путем метаболизма) доксазозина и празозина сходны. Большая часть метаболитов доксазозина выводитсяс калом. Влияние на сердечно-сосудистую систему у досазозина примерно такое же, как у празозина. При аргериальной гипертонии и аденоме предстательной железы лечение начинают с 1 мг. В недавнем клиническом испытании возможность монотерапии доксазозином при артериальной гипертонии была поставлена под сомнение. Проходит испытания препарат доксазозина длительного действия; предварительные данные свидетельствуюто том, что при использовании этого препарата легче подбирать дозу (Os and Stokke, 1999).
Альфузозин. Это пиперазинилхиназолиновый α1-адреноблокатор, обладающий одинаковым сродством ко всем подгруппах α1 -адренорецепторов (Foglaret al., 1995; Kenny etal., 1996). Его достаточно широко применяют при аденоме предстательной железы. Биодоступность при приеме внутрь составляет около 64%, а Т1/2 — 3—5 ч. В США альфузозин не выпускается.
Тамсулозин. Это производное бензолсульфамида. Тамсулозин обладает некоторой избирательностью по отношению к α1A и α1D-адренорецепторам по сравнению с α1B-адренорецёпторами (Kenny et al., 1996). Благодаря этому он может в большей степени действовать на α-адренорецепторы предстательной железы (относящиеся в большей степени к подгруппе a,A), чем на сосудистые a-адренорецепторы (относящиеся преимущественно к подгруппе α1в). Тамсулозин достаточно эффективен при аденоме предстательной железы и при этом мало влияет на АД (Wilde and McTavish, 1996; Bedushi et al., 1998). Тамсулозин хорошо всасывается из ЖКТ; его Т1/2 составляет 5—10 ч. Элиминация осуществляется преимущественно путем метаболизма с участием микросомальных ферментов печени. Лечение можно начинать с 0,4 мг, хотя обычно оказывается эффективней доза в 0,8 мг. Побочный эффект — нарушения эякуляции.
Побочные эффекты. Важнейший побочный эффект празозина и его аналогов — это так называемый эффект первой дозы: выраженная ортостатическая гипотония (вплоть до обморока) в течение 30—90 мин после приема первой дозы препарата. Иногда обмороки наблюдаются и при быстром увеличении дозы либо при добавлении второго гипотензивного средства больным, уже принимающим большую дозу празозина. Механизмы этого побочного эффекта, равно как и его постепенного уменьшения со временем, не известны. Возможно, определенную роль играет центральное действие празозина и его аналогов, сопровождающееся снижением симпатического тонуса (см. выше). Риск эффекта первой дозы снижается, если начинать лечение с 1 мг на ночь, повышать дозу медленно, а дополнительные гипотензивные средства назначать с осторожностью. Поскольку ортостатическая гипотония может развиться и при длительном лечении празозином и его аналогами, важно периодически измерятьАД как в положении лежа, так и при переходе в положение стоя. В редких случаях празозин оказывает и другие побочные эффекты, иногда требующие отмены препарата.
К ним относятся головная боль, астения и дурнота. Жалобы на дурноту носят неспецифический характер и обычно не связаны с ортостатической гипотонией. Данных о побочных эффектах аналогов празозина мало, но, видимо, эти побочные эффекты такие же, как у самого празозина. Как уже говорилось, тамсулозин в дозе 0,4 мг/сут мало влияет на АД, но может вызвать нарушения эякуляции.
Применение. Артериальная гипертония. Празозин и его аналоги широко используются при артериальной гипертонии (гл. 33). Основные различия между препаратами этой группы, как уже говорилось, касаются длительности их действия, а следовательно, частоты приема. В последние годы интерес к ним сильно возрос, так как они благотворно влияют на липидный состав крови и на инсулинозависимую регуляцию обмена глюкозы; для больных с артериальной гипертонией и повышенным риском атеросклероза это особенно важно (Grimm, 1991). Возможен и еще один механизм положительного эффекта празозина и его аналогов: известно, что катехоламины — это мощные стимуляторы гипертрофии гладких мышц сосудов, и это их действие опосредовано арадренорецепторами (Majesky et al., 1990; Okazaki et al., 1994). Препараты же группы празозина именно эти рецепторы и блокируют. Впрочем, пока не известно, насколько эти препараты снижают риск атеросклероза.
Сердечная недостаточность. Как и другие вазодилататоры, арадреноблокаторы используются при сердечной недостаточности. Празозин оказывает при этом состоянии кратковременный эффект, обусловленный расширением артериол и вен; это приводит к снижению пред- и посленагрузки сердца, повышению сердечного выброса и уменьшению застоя в легких (Colucci, 1982). Однако при сердечной недостаточности празозин, в отличие от ингибиторов АПФ и сочетания гидралазина с нитратами, не увеличивает продолжительности жизни (Cohn et al., 1986).
Аденома предстательной железы. Сокращение гладких мышц пузырного треугольника, сфинктера мочевого пузыря и предстательной железы, вызванное активацией α1-адренорецепторов, препятствует оттоку мочи. Вызывая расслабление этих мышц, празозин может оказывать благоприятный эффект у больных с нарушением мочеиспускания (например, при увеличении предстательной железы или при устранении супраспинальных влияний на парасимпатические крестцовые центры вследствие травмы спинного мозга) (Kirby et al., 1987; Anders-son, 1988). Эффективность и важная роль арадреноблокаторов при аденоме предстательной железы была показана во множестве клинических испытаний. Самым распространенным хирургическим методом лечения этого заболевания служит трансуретральная резекция предстательной железы, однако эта операция сопряжена с серьезными осложнениями, а улучшение порой бывает временным. В связи с этим разработаны и консервативные методы лечения, в частности α1-адреноблокаторами. Применяется также финастерид — препарат, подавляющий превращение тестостерона в дигидротестостерон и тем самым способствующий уменьшению размеров предстательной железы (гл. 59). Однако в целом его эффективность, видимо, ниже, чем у α-адреноблокаторов (Lepor et al., 1996). Как уже говорилось, действие последних при аденоме предстательной железы обусловлено расслаблением гладких мышц пузырного треугольника, сфинктера мочевого пузыря и предстательной железы. Альфа|-адреноблокаторы вызывают быстрое улучшение оттока мочи, тогда как эффект финастерида обычно проявляется только через несколько месяцев. Первым адреноблокатором, нашедшим широкое распространение при аденоме предстательной железы, был феноксибензамин. Однако безопасность этого необратимого α-адреноблокатора не была убедительно доказана, и поэтому вместо него сегодня применяют конкурентные блокаторы. Широко применяются и достаточно всесторонне исследованы при аденоме предстательной железы празозин, теразозин, доксазозин, тамсулозин и альфузозин (Cooper et al., 1999). Их эффективность и побочные эффекты, за исключением тамсулозина, сходны, хотя прямых сравнительных испытаний мало. Тамсулозин в обычной дозе (0,4 мг/сут) обычно не вызывает ортостатическую гипотонию, но сравнительных испытаний его эффективности при аденоме предстательной железы также недостаточно. Опыты на животных позволяют сравнивать активность арадреноблокаторов, однако это еще не дает возможности судить об их влияниях на предстательную железу человека или строить предположения об их клинической эффективности (Breslin et al., 1993). Пока не известно, α1-адренорецепторы какой подгруппы отвечают за сокращение гладких мышц предстательной железы человека, однако все больше данных свидетельствуют о том, что в ней преобладают α1д-адре-норецепторы (Price et al., 1993; Faure et al., 1994; Forray et al., 1994). Исследования сокращений гладких мышц предстательной железы в ответ на связывание лигандов также говорят о важности α1А-адренорецепторов(Forrayetal., 1994). Возможно, дальнейшие исследования в этой области послужат основой для разработки и применения избирательных α1А-адреноблокаторов. Однако не исключено, что в патогенезе обструктивных нарушений при аденоме предстательной железы играют также роль арадренорецепторы других органов, например мочевого пузыря, спинного и головного мозга.
Прочие заболевания. Есть отдельные сообщения об эффективности празозина при вазоспастической стенокардии, однако несколько небольших контролируемых испытаний этого не подтвердили (Robertson et al., 1983b; Winniford et al., 1983). В некоторых исследованиях показано, что празозин может снижать частоту спазмов сосудов пальцев при болезни Рейно, однако сравнительные испытания эффективности празозина и других вазодилататоров (например, антагонистов кальция) не проводились (Surwit et al., 1984; Wollersheim et al., 1986). Возможно, празозин оказывает благоприятное действие и при других состояниях, сопровождающихся спазмами сосудов (Spittell and Spittell, 1992). У животных празозин подавляет желудочковые аритмии, возникающие при перевязке коронарной артерии и реперфузии, однако клиническое значение этого факта пока не установлено (Davey, 1986). Наконец, празозин может быть полезен при митральной и аортальной недостаточности, так как снижает после-нагрузку сердца — однако здесь также необходимы дальнейшие исследования (Jebavy et al., 1983; Stanaszek et al., 1983).
Алкалоиды спорыньи[править | править код]
Это первые из обнаруженных α-адреноблокаторов. Их основные фармакологические свойства были описаны в классических работах Дейла (Dale, 1906). Свойства эти чрезвычайно разнообразны: алкалоиды спорыньи в разной степени могут выступать в роли блокаторов или частичных агонистов α-адренорецепторов, серотониновых и дофаминовых рецепторов.
Химические свойства. Подробно химическое строение алкалоидов спорыньи рассматривается в гл. 11. Препараты типа эргометрина, не обладающие пептидной боковой цепью, не оказывают адреноблокирующее действие. Из природных алкалоидов наибольшей α-адреноблокирующей активностью обладает эрготоксин (смесь из трех алкалоидов — эргокорнина, эргокристина и эргокриптина). Гидрирование ароматического ядра лизергиновой кислоты повышает α-адреноблокирующую активность и снижает (хотя и не устраняет полностью) способность препаратов стимулировать сокращения гладких мышц, опосредованную серотониновыми рецепторами.
Фармакологические свойства. Как природные, так и дигидрогенизированные пептидные алкалоиды спорыньи оказывают α-адреноблокирующее действие. Это действие довольно длительное (учитывая, что алкалоиды спорыньи — конкурентные блокаторы), но все же гораздо короче, чем у феноксибензамина. Кроме того, эти препараты являются довольно активными блокаторами серотониновых рецепторов. Гидрогенизированные алкалоиды спорыньи — это одни из самых мощных из известных α-адреноблокаторов, однако в клинике из-за множества побочных эффектов их можно применять лишь в дозах, вызывающих минимальную блокаду α-адренорецепторов.
Основные эффекты алкалоидов спорыньи обусловлены их центральным действием и прямым стимулирующим влиянием на гладкие мышцы. Последнее наблюдается во многих гладкомышечных органах (гл. 11) — например, дигидроэрготаксин может вызвать спастические сокращения кишечника.
На фоне пептидных алкалоидов спорыньи прессорная реакция на адреналин может изменяться на депрессорную (парадоксальную). В то же время все природные алкалоиды спорыньи вызывают существенное повышение АД, обусловленное сужением преимущественно посткапиллярных сосудов. Гидрогенизация уменьшает этот эффект, но все же дигидроэрготамин обладает достаточно сильным сосудосуживающим действием, и в какой-то степени оно сохраняется и у дигидроэрготаксина. Эрготамин, эргометрин и другие алкалоиды спорыньи могут вызвать спазм коронарных артерий, у больных ИБС часто сопровождающийся ишемией миокарда и стенокардией. Алкалоиды спорыньи обычно вызывают брадикардию, даже если АД не повышается. Этот эффект обусловлен преимущественно повышением парасимпатического тонуса, хотя не исключено и снижение симпатического тонуса (вследствие центрального действия) и прямое угнетающее влияние на миокард.
Побочные эффекты. Основной побочный эффект, из-за которого приходится ограничивать дозы алкалоидов спорыньи, — это тошнота и рвота. Длительное применение или передозировка алкалоидов спорыньи может приводить к ишемии разных органов (стенокардии, гангрене конечностей) вследствие спазма сосудов (Galeret al., 1991) — особенно на фоне уже имеющихся сосудистых заболеваний. В тяжелых случаях необходимо срочно вводить вазодилататоры. Сравнительных испытаний различных препаратов приданном состоянии нет, но, видимо, наиболее эффективны прямые вазодилататоры типа нитропруссида натрия (Caerlineretal., 1994). Подробнее побочные эффекты алкалоидов спорыньи и отравление ими описаны в гл. 11. Применение. Основные показания к алкалоидам спорыньи — послеродовая гипотония или атония матки и мигрень (Mitchell and Elboume, 1993; Saxena and De Deyenl, 1992; см. также гл. 11).
В настоящее время, однако, при мигрени применяют более эффективные и безопасные препараты, например суматриптан и другие 5-НТ1-стимуляторы (Dechant and Clissold, 1992; см. также гл. 11). Эргометрин и метилэргометрин — эффективные средства при послеродовом кровотечении вследствие атонии матки. По-видимому, их эффект обусловлен сдавлением сосудов матки при ее сокращении. Для усиления сокращений матки применяют также синтетические производные гормона нейрогипофиза окситоцина (гл. 56). Они не только способствуют остановке послеродовых кровотечений, но и вызывают или усиливают родовую деятельность. Динопростон (аналог простагландина Е2) тоже эффективен при послеродовых кровотечениях и может применяться при недостаточной реакции на алкалоиды спорыньи и препараты окситоцина (Winkler and Rath,1999). Алкалоиды спорыньи использовались также в диагностике ИБС как средства, вызывающие спазм коронарных артерий; в качестве ноотропных средств (Wadworth and Chrisp, 1992); для лечения ортостатической гипотонии (Stumf and Mitrzyk, 1994). Влияние бромокриптина на выработку пролактина — см. гл. 56.
Прочие α-адреноблокаторы[править | править код]
Индорамин. Это конкурентный α1-адреноблокатор, применяемый при артериальной гипертонии. Он является также конкурентным блокатором Н1 -рецепторов и серотониновых рецепторов (Cubeddu, 1988). В связи с избирательным действием на α-адренорецепторы индорамин снижает АД, почти не вызывая тахикардии. Кроме того, он уменьшает частоту приступов синдрома Рейно (Holmes and Sorkin, 1986).
Биодоступность индорамина обычно ниже 30%, хотя может заметно различаться. Он в значительной степени метаболизируется при первом прохождении через печень (Holmes and Sorkin, 1986; Pierce, 1990), причем некоторые его метаболиты сохраняют активность. Небольшая часть препарата выделяется в неизмененном виде с мочой. Т1/2 индорамина составляет около 5 ч. К побочным эффектам относятся седативное действие, сухость во рту, нарушения эякуляции. Индорамин достаточно эффективен как гипотензивное средство, однако фармакокинетика его сложна, и его роль в лечении артериальной гипертонии пока не ясна. В США он не выпускается.
Лабеталол. Это мощный β-адреноблокатор, обладающий также конкурентным α1-адреноблокирующим действием. Подробнее см. ниже.
Кетансерин. Этот препарат был разработан как блокатор серотониновых рецепторов, но он обладает также α1-адреноблокирующим действием. Подробнее см. гл. 11.
Урапидил. Это новый избирательный агадреноблокатор, по химическому строению отличающийся от препаратов группы празозина. Он вызывает снижение АД, обусловленное, очевидно, преимущественно блокадой периферических α1-адренорецепторов, хотя есть данные и о его центральном действии (Cubeddu, 1988; van Zwieten, 1988). Урапидил быстро метаболизируется (Т1/2 около 3 ч). Значение урапидила для лечения артериальной гипертонии пока не установлено. В США он не используется.
Буназозин. Это агадреноблокатор из группы пиперазинилхиназолинов. У больных артериальной гипертонией он снижает АД (Harder and Thurmann, 1994). В США буназозин не выпускается.
Йохимбин. Это избирательный конкурентный а2-адреноблокатор. Он представляет собой индолалкиламиновый алкалоид, выделяемый из коры йохимбе Pausinystalia yohimbe и корней раувольфии Rauwolfia. По структуре он близок к резерпину. Йохимбин легко проникает через гематоэнцефалический барьер и благодаря центральному действию вызывает повышение АД и ЧСС. Кроме того, он повышает двигательную активность и вызывает тремор. Таким образом, его центральные эффекты противоположны действию а2-адреностимулятора клонидина (Goldberg and Robertson, 1983; Grossman et al., 1993). Кроме того, йохимбин блокирует серотониновые рецепторы. Когда-то его применяли при нарушениях половой функции у мужчин; эффективность его в этом отношении доказана не была, но интерес к йохимбину при таких расстройствах в настоящее время вновь оживает. Он повышает половую активность у крыс (Clark et al., 1984) и может быть полезен в некоторых случаях психогенной импотенции (Reid et al., 1987). С другой стороны, гораздо больше убедительных данных об эффективности при импотенции силденафила и апоморфина. В нескольких небольших исследованиях получены данные о том, что йохимбин может быть полезен при диабетической нейропатии и ортостатической гипотонии.
Нейролептики. Некоторые природные и синтетические препараты разных химических групп, разработанные как D2-блокаторы, обладают и α-адреноблокирующим действием. У животных и человека достаточно сильное такое действие оказывают хлорпромазин, галоперидол и другие нейролептики — производные фенотиазина и бутирофенона.