Алкилирующие средства
Источник:
Клиническая фармакология по Гудману и Гилману том 3.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Алкилирующие средства[править | править код]
Историческая справка[править | править код]
Сернистый иприт β,β'-дихлордиэтилсульфид) был синтезирован в 1854 г., но его кожно-нарывное действие описано лишь в 1887 г. В Первую мировую войну врачи уделяли основное внимание действию сернистого иприта на кожу, глаза и дыхательные пути. Позже выяснилось, что он вызывает и тяжелое системное поражение. В 1919 г. Крумбхаар и Крумбхаар опубликовали данные, согласно которым для отравления сернистым ипритом характерна лейкопения, а на аутопсии обнаруживаются аплазия костного мозга, атрофия лимфоидной ткани и изъязвление слизистой ЖКТ.
Между двумя мировыми войнами активно исследовали химические и биологические свойства азотистых ипритов (хлорэтиламинов). Выраженная токсичность этих веществ по отношению к лимфоидной ткани навела Гилмана, Гудмана и Догерти на мысль изучить их действие на перевиваемую лимфосаркому мышей. В 1942 г. прошли первые клинические испытания, положившие начало современной химиотерапии (Gilman, 1963).
Поскольку азотистые иприты рассматривались как боевые отравляющие вещества, в то время все исследования были засекречены. Результаты были опубликованы лишь по окончании Второй мировой войны (см. Gilman and Philips, 1946, а также более поздний обзор Ludlum and Tong, 1985).
Синтезированы тысячи производных хлорэтиламинов, но из них лишь единицы в определенных клинических ситуациях оказались лучше первого препарата этой группы — хлорметина. В настоящее время используются 5 основных подклассов алкилирующих средств: 1) хлорэтиламины, 2) этиленимины, 3) алкилсульфонаты, 4) производные нитрозомочевины и 5) триазены.
Химические свойства[править | править код]
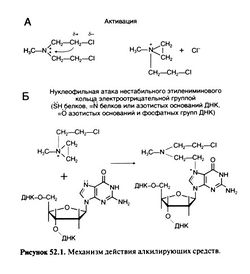
Все алкилирующие средства имеют сильные электрофильные группы, которые путем образования карбкатионов или переходных комплексов взаимодействуют с нуклеофильными группами (фосфатными, сульфгидрильными, ими-дазольными, гидрокси-, карбокси- и аминогруппами) других молекул с образованием ковалентной связи. Цитотоксическое действие этих препаратов напрямую связано с алкилированием ДНК. Бифункциональные алкилирующие средства (например, хлорэтиламины) наиболее активно соединяются с атомом N-7 гуанина — возможно, их биологическое действие связано главным образом с этой реакцией. Однако алкилированию подвергаются и другие атомы азотистых оснований (особенно атомы N-1 и N-3 аденина, N-3 цитозина и 0-6 гуанина), а также фосфатные группы ДНК, аминогруппы и сульфгидрильные группы белков.
Рассмотрим взаимодействие алкилирующих средств с атомом N-7 гуанина на примере хлорметина (рис. 52.1). На первом этапе протекает реакция мономолекулярного нуклеофильного замещения (SN1) с высвобождением аниона хлора, образованием карбкатиона и замыканием одной из хлорэтильных групп в положительно заряженное этилениминовое кольцо — образуется высокоактивное промежуточное соединение (рис. 52.1, А). Третичный азот хлорметина становится нестабильным четвертичным, и промежуточное соединение быстро реагирует с нуклеофильными (электроотрицательными) участками различных молекул. Эти реакции идут по механизму бимолекулярного нуклеофильного замещения (SN2). Алкилирование азота гуанина (рис. 52.1, Б) имеет ряд важных последствий. Во-первых, гуанин находится в ДНК преимущественно в лактамной форме, что позволяет ему образовывать водородные связи с цитозином
комплементарной цепи. Однако при алкилировании гуанина атом N-7 становится четвертичным, получая положительный заряд, из-за чего гуанин приобретает свойства кислоты и переходит в лактимную форму. При репликации ДНК измененный гуанин образует пару уже не с цитозином, а с тимином, что ведет к замене пары гуанин—цитозин на пару аденин—тимин. Во-вторых, алкилирование дестабилизирует имидазольное кольцо гуанина, что приводит к раскрытию кольца и отщеплению гуанина. Все эти повреждения ДНК требуют репарации. В-третьих, хлорэтиламины (например, хлорметин) способны к циклизации второй хлорэтильной группы и алкилированию второго гуанина или другой нуклеофильной группы с образованием сшивки цепей ДНК или ДНК с белком, что резко нарушает функцию ДНК. Как цитотоксичность, так и мутагенность алкилирующих средств можно объяснить любым из перечисленных процессов, однако активность бифункциональных алкилирующих средств коррелирует именно с числом сшивок между цепями ДНК (Garcia et al., 1988). Механизм гибели поврежденных клеток до конца не ясен (см. ниже, «Механизм действия»).
Все хлорэтиламины неустойчивы, хотя и в различной степени, поэтому при использовании каждого из этих препаратов надо учитывать его химические свойства. Так, хлорметин крайне нестабилен и почти полностью вступает в химические реакции уже через несколько минут после введения. Другие препараты, например хлорамбуцил, достаточно устойчивы для приема внутрь. Действие циклофосфамида проявляется только после его активации микросомальными ферментами печени.
Этиленимины (например, ТиоТЭФ) реагируют по механизму бимолекулярного нуклеофильного замещения (SN2); поскольку раскрытие этилениминового кольца катализируется ионами Н+, они более активны при низком pH.
Структурно-функциональная зависимость[править | править код]
Алкилирующие средства — неоднородная группа соединений, которые способны in vivo вызывать присоединение алкильных групп к ДНК и другим макромолекулам. Активность препарата зависит от его физических и химических свойств — липофильности, способности проникать через биологические мембраны, Kd, устойчивости в водном растворе и сродства к различным участкам макромолекул. Некоторые наиболее эффективные препараты, например циклофосфамид и производные нитрозомочевины, приобретают способность к алкилированию лишь in vivo в результате сложных химических превращений.
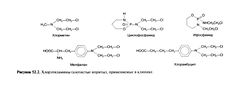
Хлорэтиламины, или азотистые иприты, можно рассматривать как аналоги сернистого иприта, в котором сера замещена азотом: их активность обеспечивают также две хлорэтильные группы. В прошлом широко применялся хлорметин, но затем были получены его модификации с большей устойчивостью и избирательностью действия, а потому и менее токсичные. Чтобы создать устойчивые препараты для приема внутрь, активный фрагмент хлорметина соединяли с аминокислотами (например, с фенилаланином — так был получен мелфалан), замешенным бензольным кольцом (например, с фенилбутиратом — так был получен хлорамбуцил), пиримидинами (например, с урацилом) и другими веществами (рис. 52.2). Хотя высокой избирательности достичь не удалось, некоторые из полученных препаратов обладали важными преимуществами перед хлорметином.
Относительно устойчивые хлорэтиламины удалось получить путем соединения с замещенным бензольным кольцом. За счет смещения к нему электронной плотности от азота у этих веществ сильно снижена способность к образованию этилениминового кольца и карбкатионов, что позволяет им не сразу реагировать с макромолекулами крови и других тканей, а распределяться по всему организму. Среди ароматических хлорэтилами-нов основное значение имеют хлорамбуцил и мелфалан, эти препараты можно назначать внутрь.
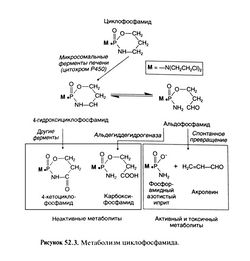
Роль метаболической активации в действии алкилируюших средств хорошо видна на примере циклофосфамида, наиболее широко применяемого препарата из этой группы. При его разработке исходили из двух предположений. Во-первых, что замещение метильной группы хлорметина оксазафосфориновым кольцом снизит реактивность, так как хлорэтильные группы не смогут ионизироваться, пока не будет расщеплена фосфоамид-ная связь в этом кольце. Во-вторых, что в опухолях повышена активность фосфатаз и фосфамидаз, способных расщеплять оксазафосфориновое кольцо, обеспечивая таким образом избирательную активацию препарата в опухолевых клетках. Как и предполагалось, циклофосфамид обладает достаточной устойчивостью в водном растворе, а его алкилируюшая, цитотоксическая и мутагенная активность in vitro оказались слабыми. В то лее время при введении онкологическим больным и экспериментальным животным препарат проявлял выраженную противоопухолевую активность, а кроме того, обладал мутагенным и канцерогенным действием. Однако гипотеза об активации циклофосфамида фосфатазами и фосфамидазами оказалась неверной. В действительности он гидроксилируется микросомальными ферментами печени (рис. 52.3), и затем его активные метаболиты попадают в опухолевые клетки (см. ниже). Избирательное действие циклофосфамида на некоторые опухоли частично объясняется способностью нормальных тканей, например ткани печени, разрушать эти метаболиты с помощью альдегиддегидрогеназы и других ферментов.
Ифосфамид, как и циклофосфамид, содержит оксазафосфо-риновое кольцо. Оба препарата содержат по две хлорэтильные группы, но у и фосфа мида одна из них связана с азотом оксаза-фосфоринового кольца, тогда как у циклофосфамида обе группы связаны с внециклическим азотом. Ифосфамид также активируется в печени путем гид роке ил ирован ия, однако его активация происходит медленнее. При этом значительная часть хлорэтильных групп окисляется до хлораиетальдегида. Очевидно, с этим связаны необходимость применения более высоких доз и фосфамида и некоторые различия в спектре противоопухолевой активности.
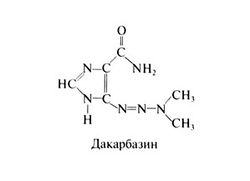
Производное триазена дакарбазин (5-(3,3-диметил-1-триазе-но)-имидазол-4-карбоксамид] вначале считался антиметаболитом, однако он действует как алкилирующее средство. Его структурная формула следующая:
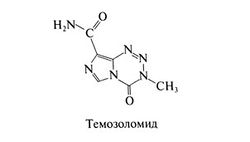
Дакарбазин активируется микросомальными ферментами печени путем отщепления от атома азота одной из метильных групп. В опухолевых клетках от образовавшегося вещества спонтанно отделяется алкилирующий фрагмент — катион метилдиазония. Близкий по строению триазен темозоломид активируется спонтанно; этот препарат применяется при глиомах и меланоме (Agarwala and Kirkwood, 2000). Его структурная формула следующая:
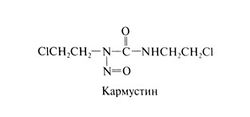
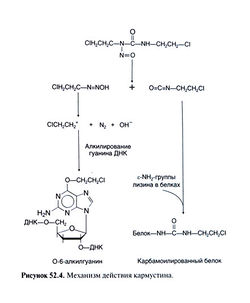
К производным нитрозомочевины относятся кармустин 11,3-бис-(2-хлорэтил)-1 -нитрозомочевина], ломустин [ 1 -(2-хло-рэтил)-3-циклогексил-1-нитрозомочевина], его метильное производное семустин, а также противоопухолевый антибиотик стрептозоцин. Эти препараты спонтанно распадаются на алкилирующий и карбамоилирующий фрагменты (рис. 52.4). Структурная формула кармустина следующая:
Все производные нитрозомочевины, обладающие противоопухолевой активностью, спонтанно распадаются, выделяя алкилирующий фрагмент — хлорэтильный карбкатион. Это сильный электрофил, быстро связывающийся с различными молекулами, включая гуанин, цитозин и аденин (Ludlum, 1990). После присоединения к ДНК он может отщеплять хлор и образовывать сшивки внутри одной цепи или между двумя цепями ДНК. Эта реакция протекает относительно медленно, и ДНК может быть восстановлена метилгуанин-ДНК-метилтрансферазой (Dolan et al., 1990). Усиленный синтез данного фермента в глиомах сопровождается устойчивостью к производным нитрозомочевины и препаратам, метилирующим ДНК (дакарбазину, темозоломиду и прокарбазину). Как и в случае хлорэтиламинов, цитотоксичность производных нитрозомочевины связывают со сшивкой цепей ДНК (Hemminki and Ludlum, 1984). Кроме карбкатиона при распаде кармустина, ломустина и семустина образуется замещенный изоцианат, карбамоилирующий остатки лизина в белках. В результате последней реакции, по-видимому, инактивируются ряд ферментов, участвующих в репарации ДНК.
Поскольку действие хлорэтиламинов начинается с образования положительно заряженного этилениминового кольца, не удивительно, что стабильные этиленимины также обладают противоопухолевой активностью. Ряд соединений из этой группы, включая триэтиленмеламин и ТиоТЭФ, применяется в клинике. В стандартных дозах практически единственным побочным действием ТиоТЭФ является угнетение кроветворения, поэтому он широко используется при высокодозной химиотерапии. Альтре-тамин (гексаметилмеламин) рассматривается в этом разделе из-за его структурного сходства с триэтиленмеламином. Альтре-тамин активируется микросомальными ферментами печени (Friedman, 2001), которые деметилируют его с выделением формальдегида. Выявлена связь между степенью деметилирования и противоопухолевой активностью препарата у мышей.
Представляет интерес ряд соединений из обширной группы эфиров алкансульфоновых кислот. Одно из них, бусульфан, используется при хроническом миелолейкозе и при высокодозной химиотерапии. Его структурная формула следующая:
Бусульфан относится к симметричным эфирам метансуль-фоновой кислоты и двухатомных спиртов. Получены эфиры спиртов с длиной цепи от 2 до 10 атомов углерода, наибольшая активность и терапевтический диапазон достигаются при промежуточном числе атомов (4 или 5). При инкубации с ДНК in vitro бусульфан образует сшивки между гуанинами (Tong and Ludlum, 1980).
Механизм действия[править | править код]
Мы рассмотрим механизмы действия всех алкилирующих средств в одном разделе. Хотя в их действии много общего, следует указать на ряд важных различий.
Цитотоксическое действие[править | править код]
Основной фармакологический эффект алкилируюших средств — нарушение репликации ДНК и деления клеток. Способность этих препаратов повреждать ДНК в быстро делящихся клетках объясняет как их противоопухолевое действие, так и многие побочные эффекты. В первую очередь страдают ткани с высоким пролиферативным индексом, но некоторые препараты повреждают и те ткани, где этот индекс невелик (печень, почки), а также зрелые лимфоциты. Хотя алкилированию подвергаются и покоящиеся клетки, цитотоксичность резко усиливается, если ДНК повреждается во время подготовки клетки к делению. Если системы репарации успевают устранить повреждение ДНК до начала деления, то гибели клетки не происходит.
В отличие от многих других противоопухолевых препаратов алкилирующие средства действуют на клетки во всех периодах клеточного цикла. Тем не менее это действие обычно проявляется при вступлении клетки в период S — клеточный цикл останавливается. На синхронизированной культуре клеток можно выявить, что клетки несколько более чувствительны к хлорэтиламинам в конце периода G1 и в периоде S, чем в митозе, в периоде G2 и в начале периода G1. Дело в том, что неспаренные нуклеотиды сильнее подвержены алкилированию, чем нуклеотиды в спирализованной ДНК, а во время репликации цепи ДНК на отдельных участках расплетаются.
Механизм гибели клетки при алкилировании ДНК детально не изучен. Показано, что в нормальных клетках костного мозга и слизистой ЖКТ повреждение ДНК вызывает остановку клеточного цикла на границе периодов G1 и S, после чего происходит репарация ДНК или, если ДНК повреждена слишком сильно, развивается апоптоз. Эти процессы регулирует белок р53, и при мутации или делеции гена ТР53 опухолевые клетки избегают апоптоза и продолжают пролиферировать (Fisher, 1994; Kastan, 1999).
Хотя основной мишенью всех алкилирующих средств служит ДНК (рис. 52.1), следует указать на важные различия между бифункциональными и монофункциональными препаратами. Первые образуют сшивки цепей ДНК и оказывают главным образом цитотоксическое действие, тогда как вторые (прокарбазин, темозоломид) метилируют ДНК и наряду с цитотоксичностью обладают резко выраженной мутагенностью и канцерогенностью. Очевидно, сшивки цепей ДНК более губительны для клетки, чем метилирование отдельных пуриновых оснований с их последующим отщеплением и разрывом цепи ДНК. Метилирование совместимо с жизнью клетки, но оно чревато мутациями, которые, передаваясь дочерним клеткам, могут вызвать злокачественное перерождение.
Большинство клеток способно к репарации ДНК; по-видимому, репарация играет большую роль в низкой чувствительности покоящихся клеток к алкилирующим средствам, в избирательности действия этих средств на различные типы клеток и в развитии устойчивости. Алкилирование одной цепи ДНК обычно устраняется достаточно легко, но сшивка цепей, возникающая, например, при действии хлорэтиламинов, требует более сложных систем репарации. На фоне низких доз этих препаратов клетка может устранить часть сшивок, но при повышении дозы их число резко возрастает, вызывая распад ДНК. Найдены ферменты репарации (Matijasevic et al., 1993), отщепляющие алкильные группы от атома 0-6 гуанина (метилгуанин-ДНК-метилтрансфераза), от атомов N-3 аденина и N-7 гуанина (3-ме-тиладенин-ДНК-гликозилаза). Высокая активность метилгуанин-ДНК-метилтрансферазы обеспечивает клетке устойчивость к производным нитрозомочевины и триазенам (Pegg, 1990).
Механизм проникновения алкилирующих средств в клетки-мишени изучен недостаточно. Хлорметин, по-видимому, попадает в клетки опухолей мышей путем активного транспорта, как аналог холина. Мелфалан, будучи аналогом фенилаланина, переносится по меньшей мере двумя системами активного транспорта, в норме переносящими лейцин и другие нейтральные аминокислоты. Липофильные препараты (производные нитрозомочевины, кармустин и ломустин) проникают в клетки путем диффузии.
Механизмы устойчивости[править | править код]
К алкилирующим средствам часто развивается устойчивость; нередко она оказывается перекрестной, но так бывает не всегда, поэтому сочетание различных алкилирующих средств при высокодозной химиотерапии теоретически обосновано. Механизмы устойчивости до конца не ясны, однако ее связывают с развитием в опухолевых клетках специфических биохимических изменений (Tew et al., 2001), включая: 1) снижение активного транспорта препарата (например, хлорметина и мелфалана), 2) увеличение синтеза нуклеофильных вешеств, прежде всего тиолов (например, глутатиона), которые связывают и инактивируют электрофилъные метаболиты алкилируюших средств, 3) повышение активности ферментов парации ДНК (например, метилгуанин-ДНК-метилтрансферазы, отшепляющей от ДНК алкильные группы после действия производных нитрозомочевины) и 4) ускоренное окисление альдегиддегидрогеназой активных метаболитов циклофосфамида в неактивные кето- и карбоксипроизводные (рис. 52.3).
Для преодоления лекарственной устойчивости предложен ряд веществ, включая соединения, истощающие запасы глутатиона (L-бутионинсульфоксимин); тиолы, которые избирательно связывают активные метаболиты алкилирующих средств в здоровых тканях, снижая токсичность (амифостин); ингибиторы метилгуанин-ДНК-метилтрансферазы (О-6-бензипгуанин) и ингибиторы глутатионтрансфераз — ферментов, ускоряющих конъюгацию тиолов с алкилирующими средствами (этакриновая кислота). Хотя все эти вещества активны при некоторых экспериментальных опухолях, их клиническая эффективность пока не доказана. Только О-6-бензилгуанин (в сочетании с карму-стином или прокарбазином) проходит испытания 2-й фазы при злокачественных глиомах (Schilsky et al., 2000).
Побочные эффекты[править | править код]
Алкилирующие средства различаются не только по противоопухолевой активности, но и по характеру и тяжести побочных эффектов. Большинство препаратов сильно угнетают кроветворение, в меньшей степени страдают слизистые. Хлорметин, мелфалан, хлорамбуцил, циклофосфамид и ифосфамид вызывают раннюю нейтропению: число нейтрофилов снижается до минимума на 6—10-е сутки и восстанавливается на 14—21-е сутки. Циклофосфамид реже других препаратов вызывает тромбоцитопению. Бусульфан угнетает все ростки кроветворения, прежде всего стволовые клетки, поэтому его назначают перед аллотрансплантацией костного мозга. При лечении бусульфаном возможна стойкая кумулятивная панцитопения, длящаяся месяцами. Кармустин и ломустин вызывают отсроченную тромбоцитопению и нейтропению, которые достигают максимума через 4—6 нед и затем постепенно проходят.
Алкилирующие средства угнетают клеточный и гуморальный иммунитет, поэтому их применяют при аутоиммунных болезнях. На фоне стандартных доз угнетение иммунитета обратимо.
Кроме системы кроветворения алкилирующие средства поражают быстро делящиеся клетки слизистых, вызывая стоматит и слущивание слизистой кишечника. Особенно важную роль поражение слизистой ЖКТ играет при высокодозной химиотерапии с трансплантацией костного мозга, поскольку это осложнение чревато развитием сепсиса. Мелфалан и ТиоТЭФ в меньшей степени действуют на слизистые, чем другие средства. При высокодозной химиотерапии на первый план выходят другие побочные эффекты, чем при назначении стандартных доз (табл. 52.1).
Другие органы поражаются реже, чем костный мозг и слизистые, но возникающие в них изменения могут быть необратимыми и даже вести к смерти. Все алкилирующие средства вызывают пневмосклероз, при высокодозной химиотерапии встречается поражение эндотелия с развитием вено-окклюзивной болезни печени, длительное лечение производными нитрозомочевины чревато почечной недостаточностью, ифосфамид в высоких дозах часто поражает ЦНС, вызывая эпилептические припадки, кому и иногда смерть. Все эти препараты могут стать причиной вторичных лейкозов, особенно прокарбазин (метилирующее средство) и производные нитрозомочевины. При метаболизме циклофосфамида и ифосфамида образуется акролеин, вызывающий поражение почек и тяжелый геморрагический цистит. Предотвратить последний помогает месна (2-меркапто-этансульфонат) — она содержит сульфгидрильную группу и связывает акролеин в моче.
Нестабильные алкилирующие средства — хлорметин и производные нитрозомочевины — обладают сильным кожно-нарывным действием (благодаря чему хлорметин с успехом применяется местно при опухолях кожи, например грибовидном микозе), при длительном использовании вызывают флебит, а при попадании в ткани — изъязвление. Большинство алкилирующих средств вызывают алопецию.
Поражение ЦНС проявляется тошнотой и рвотой, особенно после в/в введения хлорметина или кармустина. Наиболее нейротоксичен ифосфамид: он вызывает угнетение сознания вплоть до комы, эпилептические припадки и паралич. Это объясняют образованием хлорацетальдегида из хлорэтильной группы, связанной с оксазафосфориновым кольцом. Высокие дозы бусульфана также иногда вызывают эпилептические припадки; кроме того, он ускоряет элиминацию противосудорожного препарата фенитоина (гл. 21).
Алкилирующие средства значительно повышают риск вторичных лейкозов. Почти у 5% больных возникает острый мие-лолейкоз, нередко связанный с делециями 5q или 7q или моно-сомией по 5-й или 7-й хромосоме; заболеваемость достигает максимума через 4 года после химиотерапии (Levine and Bloomfield, 1992). Вторичные лейкозы чаще вызывают мелфалан, производные нитрозомочевины и прокарбазин; для циклофосфамида они менее характерны.
Наконец, алкилирующие средства нарушают репродуктивную функцию у мужчин и у женщин, вызывая необратимую азооспермию и аменорею (особенно у женщин в пременопаузе).
Хлорэтиламины[править | править код]
Общие свойства алкилирующих средств, в том числе хлорэтиламинов, рассмотрены выше, и теперь мы остановимся на отличительных особенностях отдельных препаратов.
Хлорметин[править | править код]
Хлорметин (мехлорэтамина гидрохлорид, мустарген, эм-бихин) — первый хлорэтиламин, нашедший клиническое применение, и самый активный препарат из этой группы.
Фармакокинетика. При соприкосновении с мягкими тканями хлорметин вызывает тяжелые местные реакции, поэтому в большинстве случаев его вводят в/в. В воде и биологических жидкостях он быстро разрушается, взаимодействуя с водой и другими нуклеофильными молекулами (скорость реакции сильно зависит от pH), поэтому его Т1/2 очень мал.
Таблица 52.1. Основные побочные эффекты высоких доз цитостатиков
|
Препарат |
Максимальная переносимая доза (суммарная), мг/м2 |
Отношение к стандартной дозе |
Органы, поражаемые в первую очередь" |
|
Циклофосфамид |
7000 |
7 |
Сердце,печень” |
|
Ифосфамид |
16 000 |
2,7 |
Почки, ЦНС, печень6 |
|
ТиоТЭФ |
1000 |
18 |
ЖКТ, ЦНС, печень6 |
|
Мелфалан |
180 |
5,6 |
ЖКТ, печень6 |
|
Бусульфан |
640 |
9 |
ЖКТ, печень6 |
|
Кармустин |
1050 |
5,3 |
Легкие,печень6 |
|
Цисплатин |
200 |
2 |
Почки;нейропатия |
|
Карбоплатин |
2000 |
5 |
Почки,печень6; нейропатия |
Применение. Хлорметин применяют главным образом в составе схемы МОРР (хлорметин, винкристин, прокарбазин и преднизон) при лимфогранулематозе (DeVita et al., 1972). Препарат вводят в/в струйно по 6 мг/м2 в 1-й и 8-й дни каждого курса, курсы повторяют через 28 сут. В других схемах хлорметин вытеснили циклофосфамид, мелфалан и другие, более стабильные алкилирующие средства.
Побочные эффекты. Основные ранние побочные эффекты хлорметина — тошнота, рвота, слезотечение и угнетение кроветворения. Лейкопения и тромбоцитопения препятствуют применению высоких разовых доз.
Как и все алкилирующие средства, хлорметин влияет на репродуктивную функцию, у мужчин вызывая олигозооспермию, а у женщин — нарушения менструального цикла вплоть до аменореи. Из-за риска тератогенного действия хлорметин и другие алкилирующие средства не назначают в I триместре беременности и лишь в крайних случаях применяют во II и в III триместрах. Кормление грудью следует прекратить до начала лечения.
Попадание хлорметина в подкожную клетчатку вызывает болезненное уплотнение, которое сохраняется длительное время. В тяжелых случаях развиваются некроз и отторжение тканей. При попадании препарата под кожу надо быстро ввести в это место 2-5% раствор тиосульфата натрия и в течение 6— 12 ч периодически прикладывать лед. Тиосульфат активно реагирует с хлорметином, предотвращая его взаимодействие с тканями.
Циклофосфамид[править | править код]
Механизм действия. По цитотоксическому действию циклофосфамид в целом сходен с другими алкилирующими средствами, однако имеет и некоторые особенности. Препарат редко приводит к тромбоцитопении, но вызывает выраженную алопецию. Ни в стандартных, ни в высоких дозах циклофосфамид не обладает тяжелой ранней или отсроченной нейротоксичностью, хотя может вызвать тошноту и рвоту. Он не оказывает кожно-нарывного действия и при попадании на кожу не вызывает раздражения.
Фармакокинетика. Циклофосфамид хорошо всасывается при приеме внутрь. Как говорилось выше, циклофосфамид активируется микросомальными ферментами печени. Вначале происходит гидроксилирование с образованием 4-гидроксицикло-фосфамида, который находится в равновесии со своим ациклическим таутомером, альдофосфамилом (рис. 52.3). По данным исследований, проведенных in vitro на микросомальных ферментах печени человека и на трансфицированных клетках, синтезирующих различные изоферменты цитохрома Р450, циклофосфамид активируется изоферментами подсемейства II В, а близкий построению ифосфамид — изоферментами подсемейства IIIA (Chang et al., 1993). Вероятно, с этим связаны некоторые различия в спектре противоопухолевой активности и побочном действии, а также более медленная активация ифосфамида in vivo. В печени и в опухолевых клетках часть 4-гидрокси-циклофосфамида окисляется до неактивных метаболитов (карбоксифосфамида и 4-кетоциклофосфамида) под действием аль-дегиддегидрогеназы и, возможно, других ферментов. По-види-мому, эти реакции уменьшают повреждение печени. Основная часть 4-гидроксициклофосфамида и альдофосфамида попадает в кровь и достигает клеток-мишеней. В опухолевых клетках аль-дофосфамид спонтанно расщепляется на фосфорамидный азотистый иприт и акролеин. Первый обеспечивает противоопухолевую активность, со вторым же связывают развитие геморрагического цистита. Предотвратить последний или снизить его тяжесть позволяет в/в введение месны — тиола, быстро связывающего акролеин в кислой среде мочевых путей (Tew et al2001).
Индукторы микросомальных ферментов печени, например фенобарбитал, ускоряют активацию препарата, но не влияют на его эффективность и побочное действие.
При в/в введении лишь небольшая часть циклофосфамида выводится с калом и мочой в неизмененном виде. Максимальная сывороточная концентрация достигается через 1 ч после приема внутрь, Т 1/2 составляет около 7 ч.
Применение. Циклофосфамид назначают внутрь и в/в. Рекомендуемые дозы сильно разнятся, поэтому при выборе доз, способа и последовательности введения циклофосфамида и других противоопухолевых препаратов следует опираться на результаты клинических испытаний. При злокачественных новообразованиях с высокой чувствительностью к химиотерапии — лимфомах и хронических лейкозах — возможна монотерапия циклофосфа-мидом (100 мг/м2/сут внутрь в течение 14 сут). При лимфомах и раке молочной железы его назначают совместно с другими препаратами по 500 мг/м2 в/в каждые 3—4 нед; если лечение длится долго, дозу корректируют в зависимости от числа нейтрофилов: оно не должно опускаться ниже 500—1000 мкл-1. Для высокодозной химиотерапии с трансплантацией костного мозга или стволовых клеток крови общая доза составляет 5—7 г/м2 за 3 сут. В этом случае возможны стоматит, геморрагический колит и цистит (для профилактики и лечения последнего назначают месну и диуретики); реже наблюдается поражение легких, почек, печени и сердца.
Спектр активности циклофосфамида очень широк. Это неотъемлемый компонент многих схем лечения лимфом; монотерапия циклофосфамидом позволяет достичь полной ремиссии и, по-видимому, излечения при лимфоме Беркитта. В сочетании с метотрексатом и фторурацилом (или доксорубицином) его часто назначают в качестве адъювантной химиотерапии при раке молочной железы. Кроме того, препарат активен при миеломной болезни, хроническом лимфолейкозе, раке легкого, яичников, шейки матки, а также при солидных опухолях у детей, включая нейробластому и ретинобластому.
Важное преимущество циклофосфамида — возможность приема внутрь и, соответственно, длительного применения небольших доз. Среди других алкилирующих средств по активности он занимает промежуточное положение: менее активен, чем вводимый в/в хлорметин, но более активен, чем принимаемый внутрь хлорамбуцил.
Ввиду мощного иммуносупрессивного действия представляет значительный интерес использование циклофосфамида для профилактики отторжения трансплантата, при аутоиммунных заболеваниях (включая гранулематоз Вегенера и ревматоидный артрит), а также при нефротическом синдроме у детей. Однако применять препарат следует с осторожностью: не только из-за ранних побочных действий, но и из-за риска бесплодия, вторичных лейкозов и тератогенного действия.
Побочные эффекты. Циклофосфамид в составе любой схемы химиотерапии часто вызывает тошноту и рвоту, угнетение кроветворения (меньше всего он снижает число тромбоцитов), стоматит и алопецию; изредка развивается пневмосклероз. Введение циклофосфамида в/в не осложняется тромбофлебитом; не опасно и попадание препарата в подкожную клетчатку. У 5— 10% больных возникает асептический геморрагический цистит, по-видимому, связанный с раздражающим действием акролеина (см. выше). Одновременное назначение месны значительно снижает риск цистита (Brock and Pohl, 1986); рекомендуется также обильное питье. При появлении гематурии или болезленного мочеиспускания препарат следует сразу же отменить, Еще одно осложнение — синдром гиперсекреции АДГ, обычно возникающий при дозах более 50 мг/кг (DeFronzo et al., 1973). Поскольку такие больные обычно получают интенсивную инфузионную терапию, важно помнить о риске водной интоксикации.
Ифосфамид[править | править код]
Ифосфамид, структурный изомер циклофосфамида, также активируется в печени путем гидроксилирования оксазафосфоринового кольца. Он появился в начале 1970-х тт., но из-за побочного действия (тяжелого геморрагического цистита) применялся редко. Теперь благодаря назначению месны и инфузионной терапии этот недостаток в значительной мере преодолен.
Применение. В сочетании с другими препаратами ифосфамид широко применяют при саркомах (у детей и у взрослых), а также при опухолях яичка. Кроме того, в клинических испытаниях была показана его эффективность при раке легкого, шейки матки и лимфомах. Препарат часто используют для высокодозной химиотерапии с трансплантацией костного мозга или стволовых клеток в общей дозе 12—14 г/м2, однако при этом иногда возникают тяжелые поражения ЦНС, вплоть до комы и смерти. Такое действие ифосфамида связывают с его метаболитом хлорацетальдегидом (Colvin, 1982). Кроме геморрагического цистита препарат вызывает тошноту, рвоту, потерю аппетита, лейкопению, поражение ЦНС (в стандартных дозах — сонливость и оглушенность) и почек (Brade et al., 1987).
Ифосфамид вводят в/в (за 30 мин или медленнее) по 1,2 г/м2/сут в течение 5 сут. Вместе с ифосфамидом, а также через 4 ч и через 8 ч после его введения в/в струйно вводят месну, ее разовая доза составляет 20% дозы ифосфамида, общая доза — 60%. Другой вариант — однократное введение месны вместе с ифосфамидом в той же дозе, что и ифосфамид. Показано также обильное питье или инфузионная терапия (не менее 2 л/сут). Курсы химиотерапии повторяют через 3—4 нед. Фармакокинетика. При дозах 3,8—5 г/м2 Щ2 ифосфамида составляет около 15 ч, для стандартных доз этот показатель несколько ниже.
Побочные эффекты. Ифосфамид обладает тем же побочным действием, что и циклофосфамид, но чаще вызывает тромбоцитопению, поражение ЦНС и мочевых путей (в отсутствие месны).
Мелфалан[править | править код]
Механизм действия. По механизму действия мелфалан (бис-хло-рэтиламинофенилаланин) мало отличается от других хлорэтиламинов. Он не оказывает кожно-нарывного действия.
Фармакокинетика. Всасывание мелфалана при приеме внутрь неполное и колеблется в пределах 50—80%. мелфалана составляет 45—90 мин. На 10—15% препарат выводится с мочой в неизмененном виде (Alberts et al., 1979b).
Применение. При миеломной болезни мелфалан назначают внутрь по 6 мг/сут в течение 2—3 нед; в это время необходимо внимательно следить за картиной крови. Далее делают перерыв продолжительностью до 4 нед. Когда число лейкоцитов и тромбоцитов начнет расти, переходят к поддерживающей терапии (2—4 мг/сут). Для достижения оптимального результата требуется достаточно сильное угнетение кроветворения (число лейкоцитов надо поддерживать в пределах 2500—3500 мкл'1). При в/в введении обычно используют дозу 16 мг/м (вводят за 15— 20 мин). Эту дозу вводят 4 раза с интервалами в 2 нед, а затем, в зависимости от эффекта и переносимости, — с интервалами в 4 нед; при лейкопении и нарушении функции почек дозу снижают.
Хотя по спектру активности мелфалан близок к другим алки-лирующим средствам, благодаря возможности приема внутрь он особенно удобен при миеломной болезни.
Побочные эффекты. Подобно другим алкилирующие средствам, мелфалан прежде всего угнетает кроветворение. Тошнота и рвота встречаются редко. Стандартные дозы мелфалана не вызывают алопецию. Поражение печени и почек также не отмечено.
Хлорамбуцил[править | править код]
Механизм действия. По действию на костный мозг, лимфоидную ткань и слизистые хлорамбуцил близок к другим хлорэти-ламинам. Возможно поражение ЦНС, но только на фоне высоких доз. При приеме внутрь в дозах 20 мг/сут и более хлорамбуцил может вызывать тошноту и рвоту.
Фармакокинетика. Хлорамбуцил хорошо всасывается при приеме внутрь, Т1/2 составляет около 1,5 ч. Препарат почти полностью метаболизируется (Alberts et al., 1979а).
Применение. Стандартная доза хлорамбуцила составляет 0,1— 0,2 мг/кг/сут (обычно 4—10 мг) внутрь в один прием в течение по меньшей мере 3—6 нед. При достижении ремиссии или развитии лейкопении дозу снижают. В зависимости от течения заболевания иногда назначают поддерживающую терапию по 2 мг/сут. Есть и другие схемы лечения.
В обычных дозах хлорамбуцил — наименее активный из хло-рэтиламинов. Его обычно применяют для лечения хронического лимфолейкоза и макроглобулинемии Вальденстрема. При миеломной болезни препарат обладает почти такой же эффективностью, как мелфалан и циклофосфамид. Сообщалось также об успешном лечении аутоиммунных заболеваний — васку-лита на фоне ревматоидного артрита, а также аутоиммунной гемолитической анемии с Холодовыми антителами.
Побочные эффекты. При хроническом лимфолейкозе лечение хлорамбуцилом нередко длится годами. Эффект достигается постепенно и часто не сопровождается существенным угнетением кроветворения.
Хотя длительное применение высоких доз хлорамбуцила может вызвать тяжелую гипоплазию костного мозга, обычно этот препарат вызывает лишь умеренную лейкопению, которая развивается постепенно и быстро проходит после его отмены. Изредка наблюдаются желудочно-кишечные нарушения, азооспермия, аменорея, пневмосклероз, эпилептические припадки, дерматит и поражение печени. По данным Национальной исследовательской группы по эритремии, проводившей крупное контролируемое испытание хлорамбуцила, препарат значительно увеличивает риск вторичных лейкозов и других злокачественных новообразований при лечении эритремии; тот же эффект отмечался и при длительной адъювантной химиотерапии рака молочной железы (Lemer, 1978).
Этиленимины и метилмеламины[править | править код]
ТиоТЭФ, триэтиленмеламин и альтретамин[править | править код]
Механизм действия. Сейчас при стандартной химиотерапии вместо этилениминов почти всегда назначают хлорэтиламины, а этиленимины применяются лишь по специальным показаниям. ТиоТЭФ (триэтилентиофосфорамид) используется для внутрипузырного введения при раке мочевого пузыря и в составе экспериментальных схем высокодозной химиотерапии (Kletzel et al., 1992). Альтретамин (гексаметилмеламин) применяется как препарат резерва при раке яичников.
Микросомальные ферменты печени быстро превращают ТиоТЭФ в триэтиленфосфорамид (Ng and Wax-man, 1991). Протонирование азота этилениминовых колец и их раскрытие приводит к активации обоих веществ с последующим образованием сшивок цепей ДНК.
Фармакокинетика. При стандартных дозах (до 80 мг/м2) фармакокинетика ТиоТЭФ у детей и у взрослых почти одинакова. Уже через 5 мин после в/в введения ТиоТЭФ сывороточная концентрация триэтиленфосфорамида выше, чем концентрация исходного препарата. Т,/2 составляет 1,2—2 ч для TиоТЭФ и 3—24 ч для триэтиленфосфорамида. Те же величины получены и при высокодозной терапии (300 мг/м2/сут в течение 3 сут) у детей (Kletzel et al., 1992). Менее 10% введеннойдозы выделяется с мочой в виде ТиоТЭФ или триэтиленфосфорамида. Остальная часть препарата метаболизируется, реагирует с макромолекулами или спонтанно разрушается.
Побочные эффекты. По побочным эффектам ТиоТЭФ близок к другим алкилирующим средствам. Он вызывает угнетение кроветворения и, в меньшей степени, стоматит. Цитопения развивается несколько позже, чем на фоне циклофосфамида: число лейкоцитов достигает минимума на 2-й неделе, число тромбоцитов — на 3-й.
Алкилсульфонаты[править | править код]
Бусульфан[править | править код]
Механизм действия. Угнетение кроветворения — практически единственное побочное действие стандартных доз бусульфана, что отличает его от других противоопухолевых препаратов. В низких дозах он избирательно поражает клетки гранулоцитарного ряда, поэтому основным показанием к бусульфану служит развернутая фаза хронического миелолейкоза. Однако при повышении дозы возможно развитие анемии и тромбоцитопении; иногда возникает тяжелая стойкая панцитопения. Низкие дозы бусульфана почти не повреждают лимфоидную ткань и слизистую ЖКТ. На фоне высоких доз возможны пневмосклероз и вено-окклюзивная болезнь печени.
Фармакокинетика. Бусульфан хорошо всасывается при приеме внутрь по 2—6 мг/сут; Т1/2 составляет 2—3 ч. Почти весь препарат выводится почками в виде метансульфоновой кислоты. У детей и подростков до 18 лет клиренс бусульфана выше, чем у взрослых, поэтому они переносят более интенсивную высокодозную терапию (Vassal et al., 1993).
Применение. Доза бусульфана, назначаемая при хроническом миелолейкозе, зависит от числа лейкоцитов и тяжести состояния, обычно начинают с 2—8 мг/сут внутрь. На 2—3-й неделе лечения снижается число лейкоцитов, затем уменьшается селезенка. Ориентируясь на клинические и гематологические показатели, дозу корректируют с целью снижения числа лейкоцитов ниже 10 000 мюг1. В дальнейшем возможна поддерживающая терапия по 1—3 мг/сут.
Несмотря на эффективность при хроническом миелолейкозе (первоначальный курс лечения вызывает ремиссию у 85—90% больных), бусульфан в значительной мере вытеснили препараты интерферона а и гидроксимоче-вина.
Бусульфан помогает и при других миелопролифера-тивных заболеваниях, включая эритремию и сублейке-мический миелоз. Высокодозная химиотерапия бусуль-фаном (640 мг/м2) и циклофосфамидом с успехом применяется для подготовки к трансплантации костного мозга при остром миелолейкозе (Santos et al., 1983). В этом случае препараты разделяют на несколько доз и дают на протяжении 3—4 сут, чтобы снизить риск острого поражения ЦНС, проявляющегося, в частности, эпилептическими припадками. Это осложнение может развиться через несколько часов после введения препарата. Как указывалось выше, бусульфан ускоряет метаболизм фенитоина.
Побочные эффекты. Основное побочное действие бусульфана — угнетение кроветворения, особую опасность представляет стойкая тромбоцитопения. Реже встречаются тошнота, рвота понос, бесплодие и аменорея, описаны случаи тератогенного действия. Бусульфан повышает риск вторичных лейкозов. Вначале лечения хронического миелолейкоза происходят массовая гибель опухолевых клеток и высвобождение пуринов, что ведет к гиперурикемии и может вызывать поражение почек из-за отложения уратов в канальцах (синдром распада опухоли); избежать этого позволяет одновременное назначение ап-лопуринола. Отмечен также ряд необычных осложнений, причина которых не ясна, — катаракта, гинекомастия, хейлит, глоссит, ангидроз, пневмосклероз и гиперпигментация кожи, напоминающая первичную надпочечниковую недостаточность (Tew et al., 2001).
Производные нитрозомочевины[править | править код]
Производные нитрозомочевины играют большую роль в лечении опухолей головного мозга и ЖКТ. Они действуют как бифункциональные алкилирующие средства, но по фармакологическим свойствам и побочным эффектам отличаются от хлорэтиламинов. Большое внимание привлекают кармустин и ломустин: будучи липофиль-ными, они способны проникать через гематоэнцефали-ческий барьер, что крайне важно при лечении опухолей головного мозга. К сожалению, все производные нитрозомочевины (кроме стрептозоцина) сильно угнетают кроветворение, что ограничивает их применение. Кроме того, длительное лечение этими препаратами, особенно семустином, может вести к почечной недостаточности. Как и другие алкилирующие средства, они — сильные канцерогены.
Особый интерес вызывает противоопухолевый антибиотик стрептозоцин, представляющий собой глюкозу, в которой атом С-2 связан с метилнитрозомочевиной. Он имеет высокое сродство к р-клеткам островков поджелудочной железы и вызывает сахарный диабет у экспериментальных животных. Стрептозоцин назначают при злокачественной инсулиноме и карциноиде. Сама метил-нитрозомочевина активна при некоторых опухолях и вызывает отсроченное угнетение кроветворения. Ее характерное свойство — карбамоилирование остатков лизина в белках (рис. 52.4). Однако стрептозоцин не угнетает кроветворение и обладает лишь слабой карбамоилируюшей активностью. Чтобы добиться тканевой специфичности и снизить токсичность, были синтезированы комплексы нитрозомочевины с различными молекулами-переносчиками. Например, хлорозотоцин (соединение глюкозы с хлорнитрозомочсвиной) не вызывает сахарный диабет и, в отличие от большинства производных нитрозомочевины, мало угнетает кроветворение и обладает слабой карбамоилируюшей активностью; впрочем, по эффективности он также не превосходит другие препараты этой группы.
Кармустин[править | править код]
Механизм действия. Основа действия кармустина — алкилирование атома 0-6 гуанина. Препарат активен во всех периодах клеточного цикла. Ему свойственно отсроченное угнетение кроветворения: лейкопения и тромбоцитопения достигают максимума на 4—6-й неделях. Осложнения высокодозной химиотерапии кармусгином — вено-окклюзивная болезнь печени, пневмосклероз, почечная недостаточность и вторичные лейкозы (Tewetal., 2001).
Фармакокинетика. Кармустин нестабилен в водном растворе и в биологических жидкостях. Т1/2 при в/в введении колеблется от 15 до 90 мин и более (Levin et al., 1978). В течение 24 ч с мочой уделяется 30—80% препарата в виде метаболитов. Алкилирущие фрагменты кармустина (хлорэтильные карбкатионы) быстро появляются в СМЖ, где их концентрация достигает 15-30% сывороточной концентрации (Oliverio, 1976).
Применение. Кармустин обычно вводят в/в за 1—2 ч в до-зе j50—200 мг/м2; курсы повторяют через 6 нед. При сочетании с другими противоопухолевыми препаратами дозу кармустина снижают на 25—50%.
По спектру активности кармустин напоминает другие алкилирующие средства. Он эффективен при лимфогранулематозе, в меньшей степени — при лимфомах и мие-ломной болезни. Благодаря способности проникать через гематоэнцефалический барьер препарат входит в состав комбинированного лечения злокачественных глиом и метастазов в головной мозг. Сообщалось об эффективности кармустина при меланоме и опухолях ЖКТ.
Стрептозоцин[править | править код]
Стрептозоцин — это антибиотик, продуцируемый Streptomy-ces achromogenes. Он активен во всех периодах клеточного цикла и применяется главным образом при злокачественных инсулиномах.
фармакокинетика. После в/в инфузии стрептозоцина в дозе 200—1600 мг/м2 его максимальная сывороточная концентрация достигает 30—40 мкг/мл. Тсоставляет около 15 мин. Лишь 10—20% препарата выводится с мочой (Schein et al., 1973).
Применение. Стрептозоцин вводят в/в. Возможны две схемы применения стрептозоцина: 1) по 500 мг/м21 раз в сутки в течение 5 сут, затем каждые 6 нед курс повторяют, 2) по 1000 мг/м2 1 раз в неделю в течение 2 нед с последующим повышением недельной дозы; максимальная доза составляет 1500 мг/м2/нед.
Стрептозоцин применяют в основном при злокачественных инсулиномах. Он значительно увеличивает годичную выживаемость, в случае ремиссии медиана выживаемости увеличивается вдвое.
Побочные эффекты. Стрептозоцин часто вызывает тошноту; примерно в 2/3 случаев наблюдаются поражения печени и почек, обычно обратимые. Нефротоксическое действие связано с повреждением проксимальных канальцев: оно зависит от дозы, носит кумулятивный характер и может быть смертельным. Для его раннего выявления следует регулярно определять белок в моче. Стрептозоцин нельзя сочетать с нефротоксичными препаратами. У 20% больных возможно угнетение кроветворения — анемия, лейкопения и тромбоцитопения.
Триазены[править | править код]
Дакарбазин и темозоломид[править | править код]
Дакарбазин после активации в печени способен метилировать ДНК. В печени он превращается в монометилтриазеноимида-золкарбоксамид. Темозоломид спонтанно превращается в то же соединение. Эти препараты активны во всех периодах клеточного цикла. Устойчивость к ним связывают с отщеплением метильных групп от гуанина с помощью метилгуанин-ДНК-метилтрансферазы.
Фармакокинетика. Дакарбазин вводят в/в, его начальный Т1/2 составляет около 20 мин, а конечный — около 5 ч (Loo et al., 1976). Т|/2 возрастает при печеночной и почечной недостаточности. Около половины препарата выводится почками в неизмененном виде путем канальцевой секреции. Повышение концентрации в моче 5-аминоимидазол-4-карбоксамида (промежуточного продукта при синтезе пуринов) связано с катаболизмом дакарбазина, а не с нарушением обменных процессов. Концентрация дакарбазина в СМЖ составляет около 14% сывороточной концентрации (Friedman, 2001).
Применение. При меланоме дакарбазин вводят по 3,5 мг/кг/сут в/в в течение 10 сут; курс повторяется каждые 4 нед. Другая схема — 250 мг/м2/сут в течение 5 сут каждые 3 нед. Попадание препарата в подкожную клетчатку вызывает некроз тканей и сильную боль.
Дакарбазин применяют в составе схем полихимиотерапии при меланоме, лимфогранулематозе и саркомах у взрослых. Темозоломид эффективен при злокачественных глиомах (Ne-wlands et al., 1992; Agarwala and Kirkwood, 2000).
Побочные эффекты. Дакарбазин и темозоломид вызывают тошноту и рвоту более чем у 90% больных, эти симптомы появляются через 1—2 ч после введения и могут сохраняться до 12 ч. Угнетение кроветворения (лейкопения и тромбоцитопения) обычно умеренное или слабое. На фоне дакарбазина возможен гриппоподобный синдром, включающий недомогание, озноб, лихорадку и миалгию. Иногда наблюдаются алопеция, приливы, поражение печени, ЦНС и кожи.