Антиметаболиты
Источник:
Клиническая фармакология по Гудману и Гилману том 3.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Антиметаболиты[править | править код]
Антагонисты фолиевой кислоты[править | править код]
Антагонисты фолиевой кислоты, главным из которых является метотрексат, занимают особое место среди противоопухолевых препаратов: с их помощью были получены первые полные, хотя и краткосрочные, ремиссии при лейкозах (Farber et al., 1948) и впервые удалось излечить солидную опухоль — хориокарциному (Hertz, 1963). Эти успехи послужили мощным стимулом к дальнейшему развитию химиотерапии. Интерес к антагонистам фолиевой кислоты еще больше повысили достижения высокодозной химиотерапии в сочетании с фолинатом кальция, снижавшим токсичность препаратов. Благодаря этому расширился спектр противоопухолевой активности метотрексата; теперь его назначают, например, при остеогенной саркоме, на которую препарат в стандартных дозах не действовал.
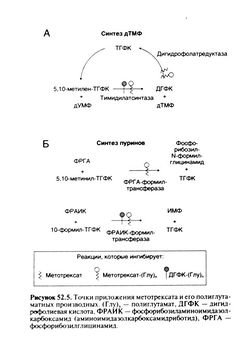
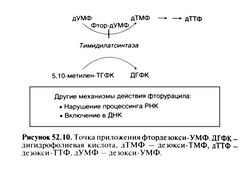
Когда выяснилось, что кроме дигидрофолатредуктазы метотрексат напрямую ингибирует ферменты синтеза пуринов и тимидилатсинтазу, коферментами которых служат восстановленные фолаты, был начат поиск антагонистов фолиевой кислоты, избирательно ингибирующих эти ферменты (рис. 52.5). Путем замены атомов N-5, N-8 и N-10 и модификации боковых цепей молекулы метотрексата удалось синтезировать препараты, сохранившие свойственную ему способность образовывать внутри клетки стойкие полиглутаматы, однако лучше проникающие в опухоль (Messmann and Allegra, 2001): ралтит-рексед, ингибитор тимидилатсинтазы; лометрексол, ингибитор синтеза пуринов, и пеметрексед, сочетающий оба механизма действия (Calvete et al., 1994; Beardsley et al., 1986; Chen etal., 1999).
Метотрексат не только оказывает цитотоксическое действие, но и угнетает клеточный иммунитет, благодаря чему с успехом применяется как иммунодепрессант при псориазе (McDonald, 1981; гл. 65), а также при аллотрансплантации костного мозга, трансплантации органов, дерматомиозите, ревматоидном артрите, гранулематозе Вегенера и болезни Крона (Messmann and Allegra, 2001; Feagan et al., 1995; гл. 53).
Структурно-функциональная зависимость. Фолиевая кислота — это витамин, из которого образуются восстановленные фолаты (производные ТГФК), служащие переносчиками одноуглеродных групп при синтезе предшественников нуклеиновых кислот — дТМФ и пуринов.
Антагонисты фолиевой кислоты в первую очередь ингибируют дигидрофолатредуктазу (рис. 52.5). Это уменьшает запасы восстановленных фолатов, необходимых для синтеза дТМФ и пуринов, и вызывает накопление полиглутаматов дигидрофолиевой кислоты, которые вместе с полиглутаматами метотрексата напрямую ингибируют зависимые от восстановленных фолатов ферменты синтеза пуринов и тимидилатсинтазу (рис. 52.5); в результате клетка погибает (Allegra et al., 1986, 1987b; Messmann and Allegra, 2001). Получены препараты с неодинаковым сродством к дигидрофолатредуктазе разных видов живых организмов; некоторые из препаратов почти не действуют на человеческий фермент, однако активны в отношении бактерий (триметоприм) или простейших (пириметамин; гл. 40). В то же время метотрексат токсичен для всех исследованных видов. С помощью кристаллографии взаимодействие метотрексата и его аналогов с дигидрофолатредуктазой разных видов изучено на уровне отдельных атомов (Matthews et al., 1985; Stone and Morrison, 1986; Kraut and Matthews, 1987; Schweitzer et al., 1989; Bystroffand Kraut, 1991; Blakley and Sorrentino, 1998).
Будучи полярными соединениями, фолиевая кислота и многие ее антагонисты гидрофильны и плохо проникают через гематоэнцефалический барьер, а в клетки попадают с помощью белков-переносчиков (Elwoodj 1989; Dixon et al., 1994). У млекопитающих описаны две системы транспорта фолатов; 1) фолатсвязываюший белок с высоким сродством к фолиевой кислоте. но низким сродством к метотрексату и его аналогам (El-wood. 1989) и 2) переносчик восстановленных фолатов — основной путь переноса метотрексата, ралтитрекседа и большинства других антагонистов фолиевой кислоты (Westerhof et al 1995). В клетке фолилполиглутаматсинтаза превращает эти вещества из моноглутаматов в пол иглутаматы (Cichowicz and Shane, 1987); к метотрексату может присоединяться до 6 остатков глутаминовой кислоты. Клеточная мембрана почти непроницаема для полиглутаматов, поэтому метотрексат накапливается и долгое время сохраняется в опухоли и нормальных тканях, например печени. По сравнению с моноглутаматами полиглутаматы фолиевой кислоты и ее антагонистов имеют намного большее сродство к ферментам синтеза пуринов и тимидилатсин-тазе, но не к дигид рофолатредуктазе.
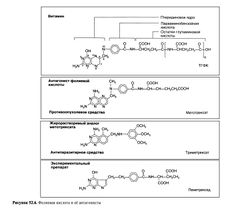
Получены новые антагонисты фолиевой кислоты с более избирательным сродством к системам транспорта фолатов. Например, мощный ингибитор дигидрофолатредуктазы эдатрек-сат (10-этил-10-деазааминоптерин) проникает в опухолевые клетки лучше, чем в здоровые; этот препарат сейчас проходит клинические испытания (Grant et al., 1993). Чтобы обойти системы транспорта фолатов и облегчить проникновение в ЦНС были синтезированы липофильные антагонисты фолиевой кислоты. Одним из первых препаратов этой группы стал тримет-рексат (рис. 52.6). Он обладает умеренной противоопухолевой активностью (в сочетании с фолинатом кальция для уменьшения токсичности), однако оказался эффективным при пневмоцистной пневмонии (Allegra et al., 1987а).
Пеметрексед—еще один новый антагонист фолиевой кислоты (рис. 52.6). Он быстро превращается в полиглутамат и ингибирует как дигидрофолатредуктазу, так и ферменты синтеза пуринов и тимидилатсинтазу. В предварительных испытаниях показана его активность при раке толстой кишки, мезотелиоме и немелкоклеточном раке легкого (Rusthoven et al., 1999).
Механизм действия. Фолиевая кислота вначале должна быть восстановлена дигид рофолатредуктазой до ТГФК, после чего может присоединять различные одноуглеродные группы и переносить их на другие молекулы. В реакции, катализируемой тимидилат-синтазой, дезокси-УМФ превращается в дезокси-ТМФ, получая метиленовую группу от 5,10-метилен-ТГФК; последняя окисляется до дигидрофолиевой кислоты и для участия в дальнейших реакциях должна быть снова восстановлена (рис. 52.5). Метотрексат и другие антагонисты фолиевой кислоты с высоким сродством к дигидрофолатредуктазе (К, 0,01—0,2 нмоль/л) нарушают образование ТГФК, вызывая дефицит восстановленных фолатов и накопление токсичных полиглутаматов ди гидрофолиевой кислоты. При этом тормозятся реакции переноса одноуглеродных групп, необходимые для синтеза пуринов и дТМФ; в итоге нарушаются синтез нуклеиновых кислот и другие обменные процессы. Токсическому действию метотрексата препятствует фолинат кальция (кальциевая саль 5-формил-ТГФК), который попадает в клетку с помощью переносчика восстановленных фолатов и превращается в другие производные ТГФК (Boarman etal., 1990).
Как большинство антиметаболитов, метотрексат лишь отчасти избирателен в отношении опухолевых клеток и поражает также быстро пролиферирующие нормальные клетки, в том числе костного мозга и слизистой ЖКТ. Антагонисты фолиевой кислоты действуют в периоде S и наиболее активны в отношении клеток, находящихся в логарифмической фазе роста.
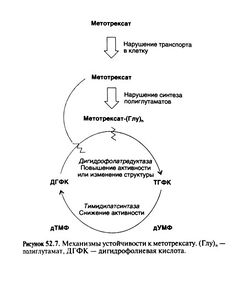
Механизмы устойчивости. На экспериментальных моделях были воспроизведены многочисленные механизмы приобретения устойчивости к метотрексату (рис. 52.7) на всех этапах его действия: 1) нарушение транспорта препарата в клетки (Assaraf and Schimke, 1987; Trippett et al., 1992), 2) мутации гена DHFR, кодирующего дигидрофолатредуктазу, которые снижают ее сродство к метотрексату (Srimatkandada et al., 1989), 3) повышение концентрации дигидрофолатредуктазы путем амплификации или усиления экспрессии гена pHFR (Pauletti et al., 1990; Mat-herley et al., 1997), 4) нарушение синтеза полиглутаматов метотрексата (Li et al., 1992), 5) снижение активности тимидилатсинтазы (Curt etal., 1985). Через 24 ч после лечения метотрексатом в лейкозных клетках повышается уровень дигидрофолатредуктазы, вероятно, за счет усиления ее синтеза. Показано, что этот процесс саморегулируется на уровне мРНК: свободный фермент связывается со своей мРНК, блокируя трансляцию, а при добавлении метотрексата трансляция возобновляется (Chu et al., 1993). Длительное лечение ведет к отбору опухолевых клеток с резко повышенной активностью дигидрофолатредукгазы. Они содержат множество копий гена DHFR в двойных микрохромосомах, в равномерно окрашиваемых участках обычных хромосом или во внехромосомных структурах (так называемых амплисомах). Амплификация гена как механизм устойчивости к противоопухолевым препаратам впервые описана применительно к метотрексату (Schimke et al., 1978), в дальнейшем аналогичный механизм был обнаружен для ряда других препаратов, включая фторурацил и пентостатин (Stark and Wahl, 1984). Показано, что амплификация гена DHFR имеет клиническое значение при раке легкого (Curt et al., 1983) и лейкозах (Goker et al., 1995).
В высоких дозах метотрексат может проникать в клетки с нарушенными системами транспорта фолатов и накапливаться там в концентрации, достаточной для ингибирования увеличенного количества дигидрофолатредукгазы.
Побочные эффекты. Основные побочные эффекты метотрексата и других антагонистов фолиевой кислоты связаны с поражением быстро пролиферирующих клеток костного мозга и слизистых. Стоматит и угнетение кроветворения (в частности, тромбоцитопения) достигают максимума на 5—10-е сутки после введения препарата. В тяжелых случаях возможны спонтанные кровотечения и угрожающие жизни инфекции, поэтому иногда таким больным проводят профилактическое переливание тромбоцитарной массы, а при лихорадке назначают антибиотики широкого спектра действия. Если выведение метотрексата не нарушено, побочные эффекты обычно проходят в течение 2 нед, но при почечной недостаточности выведение препарата нарушается и развивается стойкое угнетение кроветворения. В связи с этим дозу метотрексата при ХПН снижают пропорционально уменьшению СКФ.
Метотрексат может вызвать пневмонит: в легких возникают очаговые инфильтраты, быстро исчезающие при отмене препарата; повторное лечение иногда проходит без этого осложнения. Предположение, что пневмонит имеет аллергическую природу, пока не доказано.
Важнейший побочный эффект в случае длительного назначения метотрексата (при псориазе и ревматоидном артрите) — фиброз и цирроз печени. У больных псориазом, получавших метотрексат внутрь в течение 6 мес и более, риск портального фиброза был выше, чем на фоне другого лечения. Это осложнение требует отмены препарата. Высокие дозы метотрексата могут вызвать преходящее повышение активности печеночных ферментов, но риск стойких изменений невелик.
Интратекальное введение метотрексата часто вызывает симптомы раздражения мозговых оболочек и воспалительные изменения в СМЖ. Изредка возникают эпилептические припадки, кома, и наступает смерть. Фолинат кальция при поражении ЦНС не помогает.
Антагонисты фолиевой кислоты эмбриотоксичны, и в предварительных испытаниях метотрексат в сочетании с аналогом простагландинов мизопростолом показал высокую эффективность как средство для прерывания беременности в I триместре (Hausknecht, 1995).
Кроме того, метотрексат вызывает алопецию, дерматит, поражение почек, нарушение овуляции и сперматогенеза, а также обладает тератогенным действием.
Фармакокинетика. При приеме внутрь в дозе до 25 мг/м метотрексат хорошо всасывается; биодоступность высоких доз ниже, поэтому их обычно вводят в/в. Максимальная сывороточная концентрация составляет 1—10 мкмоль/л для доз 25— 100 мг/м2 и 0,1—1 ммоль/л для высоких доз (1,5 г/м2 и выше). Элиминация метотрексата протекает в три фазы (Sonneveld et al., 1986). Начальная фаза отражает быстрое распределение препарата в тканях, средняя — его выведение почками (Т1/2 2—3 ч). Конечный Тщ составляет 8— 10 ч, однако он резко удлиняется при почечной недостаточности, что может вести к тяжелому поражению костного мозга и слизистых. Метотрексат медленно проникает в плевральную полость и полость брюшины. Однако его накопление в плевральном выпоте и асцитической жидкости с последующим выделением может долго поддерживать высокую сывороточную концентрацию препарата и усиливать токсичность.
Примерно на 50% метотрексат связывается белками плазмы (прежде всего с альбумином), причем многие препараты (сульфаниламиды, салицилаты, тетрациклин, хлорамфеникол, фенитоин) вытесняют его из комплекса с белками. Вместе с метотрексатом такие препараты следует назначать с осторожностью. В течение 48 ч (главным образом в первые 8—12 ч) 90% метотрексата выводится почками в неизмененном виде, небольшая часть попадает в кал, вероятно, с желчью. Обычно лишь малая часть препарата метаболизируется, но при назначении высоких доз происходит накопление метаболитов, особенно нефротоксичного 7-гидроксиметотрексата (Messmann and Allegra, 2001). Метотрексат попадает в мочу путем клубочковой фильтрации и канальцевой секреции, поэтому одновременное назначение лекарственных средств, которые снижают почечный кровоток (НПВС), нефротоксичны (цисплатин) или относятся к слабым органическим кислотам (аспирин, пиперациллин), может замедлить выведение метотрексата и вызвать выраженное угнетение кроветворения (Stoller et al., 1977; Iven and Brasch, 1988; Thyss et al., 1986). Особые предосторожности следует соблюдать при почечной недостаточности: у таких больных дозу снижают пропорционально уменьшению СКФ.
Полиглутаматы метотрексата сохраняются в организме длительное время — несколько недель в почках и несколько месяцев в печени. Существует также кишечно-печеночный кругооборот метотрексата.
Важно подчеркнуть, что концентрация метотрексата в СМЖ составляет лишь 3% средней сывороточной концентрации, поэтому для уничтожения опухолевых клеток в ЦНС стандартных доз недостаточно. Высокие дозы (> 1,5 г/м2) позволяют создать терапевтическую концентрацию и в СМЖ.
Применение. При тяжелом псориазе метотрексат назначают по 2,5 мг/сут внутрь в течение 5 сут (после чего делают перерыв хотя бы на 2 сут) или по 10—25 мг в/в 1 раз в неделю. Рекомендуют начать с пробной дозы 5—10 мг парентерально для исключения идиосинкразии. Прерывистые курсы метотрексата в низких дозах используют при ревматоидном артрите, устойчивом к другим препаратам (Hoffmeister, 1983). Лечение метотрексатом неопухолевых заболеваний требует особого внимания к фармакокинетике и побочному действию препарата (Weinstein 1977).
Метотрексат эффективен при остром лимфолейкозе у детей и входит в схемы индукционной, консолидирующей, высокодозной и поддерживающей химиотерапии. В последнем случае его вводят в/м по 30 мг/м2/нед (за 2 введения) или по 175—525 мг/м2 2 дня каждого месяца. Показано, что у детей успех лечения обратно пропорционален клиренсу метотрексата; высокая средняя сывороточная концентрация препарата при в/в инфузии снижала риск рецидива (Borsi and Мое, 1987). Активность препарата при лейкозах у взрослых невелика, исключение составляет нейролейкоз. Интратекальное введение метотрексата применяется для профилактики и лечения диффузной опухолевой инфильтрации мозговых оболочек при лейкозе, лимфомах и солидных опухолях. При этом в СМЖ создается высокая концентрация препарата, и ремиссия может быть получена даже при неэффективности в/в введения, так как благодаря гематоэнцефа-лическому барьеру лейкозные клетки, попавшие в ЦНС, мало подвергались действию метотрексата, вводимого в/в, и могли сохранить чувствительность к нему. Доза для интратекального введения у всех больных старше 3 лет составляет 12 мг (Bleyer, 1978). Инъекции повторяют каждые 4 сут, пока опухолевые клетки не исчезнут из СМЖ. Изредка назначают фолинат кальция, чтобы устранить токсическое действие метотрексата, попадающего в системный кровоток. При люмбальной пункции метотрексат плохо проникает из места введения к верхнелатеральной поверхности полушарий, и лучшего распределения препарата помогает добиться резервуар Оммайя с постоянным катетером в боковом желудочке. Назначение препарата по 1 мг каждые 12—24 ч достаточно эффективно и позволяет снизить нейротоксичность.
Метотрексат с успехом применяется при трофобла-стической болезни, прежде всего при хориокарциноме: в развернутой стадии он обеспечивает излечение в 75% случаев (в сочетании с дактиномицином), на ранней стадии — более чем в 90% случаев. Метотрексат вводят по 1 мг/кг в/м в 1,3,5 и 7-й дни; во 2,4,6 и 8-й дни назначают фолинат кальция (0,1 мг/кг); в отсутствие тяжелых побочных эффектов курсы повторяют через 3 нед. Для результатов лечения определяют концентрацию бета-субъединицы ХГ в моче.
Метотрексат помогает также при остеогенной саркоме и грибовидном микозе, а в составе полихимиотерапии-при лимфоме Беркитта и других лимфомах, раке молочной железы, яичников и мочевого пузыря, опухолях головы и шеи. Высокие дозы метотрексата назначают при остеогенной саркоме, а также — в сочетании с другими противоопухолевыми препаратами — при лейкозах и лимфомах. Такие дозы создают терапевтическую концентрацию метотрексата в СМЖ, что важно для профилактики нейролейкоза. Высокие дозы метотрексата (0,25—7 5 r/м2) вводят путем в/в инфузии в течение 6—72 ч. Чтобы ограничить поражение нормальных клеток и ослабить побочное действие, одновременно назначают фо-линат кальция, например, после 6-часовой инфузии метотрексата его вводят по 15 мг/м2 каждые 6 ч (всего 7 раз). Оптимальная схема введения метотрексата и фолината кальция до сих пор не разработана (Ackland and Schilsky, 1987). Высокодозная химиотерапия чревата тяжелыми побочными эффектами, однако при соблюдении ряда предосторожностей достаточно безопасна. Лечение должно проводиться опытным химиотерапевтом под контролем сывороточной концентрации метотрексата. Если через 48 ч она составляет 1 мкмоль/л и выше, необходимо вводить фолинат кальция в высоких дозах (100 мг/м2), пока концентрация не упадет ниже токсического уровня — 0,02 мкмоль/л (Stoller et al., 1977). Важно поддерживать высокий диурез и щелочную реакцию мочи, так как при низком pH метотрексат откладывается в почечных канальцах. Асцит и плевральный выпот замедляют выведение препарата, усиливая токсичность. Согласно отдельным сообщениям, при развитии олигурической ОПН гемодиализ обеспечивает выведение метотрексата со скоростью, равной половине скорости выведения при нормальной функции почек (Wall et al., 1996).
Аналоги пиримидинов[править | править код]
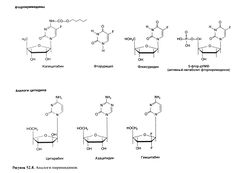
Это неоднородная группа противоопухолевых препаратов (рис. 52.8), которые благодаря сходству с естественными метаболитами ингибируют синтез пиримидиновых нуклеотидов или нарушают образование и функции нуклеиновых кислот. Так, аналоги дезоксицитидина блокируют синтез ДНК, а аналог урацила фторурацил нарушает синтез дТМФ, а также процессинг и функции РНК. Аналоги пиримидинов используются при различных болезнях, включая злокачественные новообразования, псориаз и инфекции, вызванные грибами и ДНК-содержащими вирусами. Знание путей активации и метаболизма этих препаратов помогает в разработке схем полихимиотерапии, в которых разные препараты усиливают действие друг друга.
Механизм действия. Наиболее полно изучены аналоги пиримидинов, содержащие галоген у атома С-5, — фторурацил, флоксуридин и противовирусное средство идоксуридин (5-йододезокси-уридин). Фтор по атомному радиусу близок к водороду, тогда как более крупные атомы брома и йода соответствуют метальной группе. В связи с этим идоксуридин выступает как аналог тимидина, и его действие связано с фосфорилированием и включением в ДНК вместо дезокси-ТТФ. Фторурацил же благодаря небольшому размеру атома фтора по биохимическим свойствам напоминает урацил, однако связь С—F намного прочнее связи С—H, что препятствует замещению фтора метильной группой под действием тимидилатсинтазы. Вместо этого метаболит фторурацила фтордезокси-УМФ прочно связывается с тимидилатсинтазой и ее коферментом 5,10-метилен-ТГФК, ингибируя этот фермент. Таким образом, замещение водорода атомом галогена подходящего размера позволяет получать соединения, которые за счет структурного сходства с естественными нуклеотидами вступают в свойственные пиримидинам реакции, но при этом нарушают ряд важных метаболических процессов.
Среди производных фторурацила наибольшее значение имеет капецитабин (М-4-пентоксикарбонил-5'-дезоксифторцитидин), активный при раке молочной железы и толстой кишки. Препарат принимают внутрь. В печени, других тканях и в опухоли он под действием карбоксилэстераз превращается в 5'-дез-оксифторцитидин. Далее цитидиндезаминаза переводит последний в 5'-дезоксифторуридин. На следующем этапе тимидин-фосфорилаза отщепляет 5'-дезоксирибозу, и в результате внутри клетки образуется фторурацил. К капецитабину особенно чувствительны опухоли с повышенной активностью тимидин-фосфорилазы (Ishikawa et al., 1998).
Нуклеотиды РНК и ДНК содержат соответственно рибозу и 2'-дезоксирибозу. Исследованы аналоги пиримидинов с различными модификациями этих моносахаридов. Например, путем замены в цитидине рибозы на арабинозу был получен цитарабин (l-b-D-арабщюзилщггозин). Как видно на рис. 52.8, у рибозы 2'-гидроксигруппа обращена вниз (a-конфигурация), а у арабинозы — вверх (бета-конфигурация), благодаря чему ферменты распознают цитарабин как дезоксицитидин и фосфорилируют его с образованием трифосфата, который конкурирует с дезокси-ЦТФ за встраивание в ДНК (Chabneret al., 2001). Встраивание цитарабинтрифосфата в ДНК прекращает репликацию и нарушает транскрипцию.
Большое внимание привлекают два других аналога цитидина (рис. 52.8). Азацитидин как аналог цитидина относится к антиметаболитам, он встраивается в основном в РНК и активен при лейкозах; в то же время препарат ингибирует метилирование цитидина в ДНК (необходимое для нормального функционирования хроматина) и вызывает дифференцировку опухолевых клеток in vitro. Гемцитабин (2’,2'-дифтордезоксицигидин) встраивается в ДНК и препятствует продолжению репликации. Он активен при различных солидных опухолях, включая рак поджелудочной железы, легкого и яичников.
Фторпиримидины[править | править код]
Механизм действия. Для проявления цитотоксического действия фторурацил нуждается в активации путем рибозилирования и фосфорил и рова ния (рис. S2.9). Существует несколько путей образования фтор-УМФ из фторурацила. Фторурацил превращается вофторуридин под действием уридинфосфорилазы и далее — во фтор-УМФ под действием уридинкиназы; в реакции фторурацила с фосфорибозилпирофосфатом, катализируемой оротатфосфорибозилтрансферазой, фтор-УМФ образуется в одну стадию. Далее последний может претерпевать другие изменения, в том числе встраиваться в РНК. Однако ключевую роль для цитотоксического действия играют превращение фтор-УМф во фтор-УДФ, восстановление фтор-УДФ рибонуклеозидци-фосфатредуктазой до фтордезокси-УДФ и последующее дефосфорилирование до фтордезокси-УМФ — мощного ингибитора тимидилатсинтазы. Последний может образовываться и в две стадии, когда тимидинфосфорилаза превращает фторурацил во фтордезоксиуридин, который с помощью тимидинкиназы превращается во фтордезокси-УМФ. Часть этих метаболических путей можно обойти путем использования флоксуридина (фтор-дезоксиуридина), из которого под действием тимидинкиназы сразу образуется фтордезокси-УМФ.
Фтордезокси-УМФ образует ковалентные связи с тимидилатсинтазой и 5,10-метилен-ТГФК (рис. 52.10). Этот тройной комплекс напоминает переходный комплекс, возникающий при превращении дезокси-УМФ в дезокси-ТМФ: в норме на следующем этапе метиленовая группа переносится с восстановленного фолата на дезокси-УМФ и комплекс распадается, однако в случае фтордезокси-УМФ связь между атомами С и F слишком прочная и переноса не происходит, что ведет к стойкому ингибированию фермента (Santi et al., 1974). Ингибирование тимидилатсинтазы истощает запасы дезокси-ТТФ, необходимого для синтеза ДНК.
Кроме того, фторурацил встраивается в РНК и ДНК. В присутствии фторурацила в клетках на фоне дефицита дезокси-ТТФ в Д Н К вместо последнего включаются фтордезокси-УТФ и дезокси-УТФ — субстрат тимидилатсинтазы, накапливающийся при ее ингибировании. Насколько такое нарушение структуры ДНК опасно для клетки — не ясно (Canman et al., 1993). Предполагается, что оно активирует эксцизионную репарацию, в результате чего могут возникать разрывы цепей ДНК, поскольку для репарации нужен дезокси-ТТФ, а его запасы истощены из-за ингибирования тимидилатсинтазы (Mauro et al., 1993). встраивание фторурацила в РНК также поражает клетку — за счет нарушения как процессинга РНК, так и трансляции (Armstrong, 1989; Danenberg et al., 1990).
Описаны различные механизмы устойчивости к фторурацилу и флоксуридину, включая прекращение синтеза или снижение активности ферментов, необходимых для активации фторурацила, снижение активности цитидилаткиназы (что препятствует его включению в РНК), амплификацию гена тимидилатсинтазы (Washtein, 1982) и изменение ее структуры со снижением сродства к фтордезокси-У МФ (Barbour et al., 1990). Согласно экспериментальным и клиническим исследованиям, активность фторурацила возрастает при низком уровне тимидинфосфорилазы и дигидропиримидиндегидрогеназы, участвующих в его катаболизме, а также тимидилатсинтазы, его фермента-мишени (van Т riest et al., 2000). Показано, что уровень тимидилатсинтазы подвержен тонкой саморегуляции по принципу обратной связи: фермент связывается со своей мРНК и препятствует трансляции. Благодаря этому активность тимидилатсинтазы быстро меняется в зависимости от потребностей клетки в разные периоды клеточного цикла. Описанный механизм может играть важную роль в быстрой выработке устойчивости к фторурацилу (Chu et al., 1991; Swain et al., 1989). В некоторых опухолевых клетках снижена концентрация 5,10-метилен-ТГФК, из-за чего не образуются тройные ингибирующие комплексы между ней, фтордезокси-У МФ и тимидилатсинтазой. Как показывают экспериментальные и клинические данные, добавление экзогенного восстановленного фолата в виде фолината кальция способствует возникновению этих комплексов и повышает эффективность фторурацила (Ullman et al., 1978; Grogan et al., 1993).
Следует заметить, что, за исключением сниженной концентрации восстановленных фолатов, клиническое значение других механизмов устойчивости к фторурацилу и его аналогам не установлено (Grem et al., 1987).
Для усиления активности фторурацил назначают вместе с рядом препаратов, обладающих различными механизмами действия (табл. 52.2). Кроме фолината кальция наибольший интерес вызывают сочетания фторурацила с метотрексатом, интер-феронами и цисплатином, все эти сочетания проходят клинические испытания. Вещества, блокирующие синтез пиримидинов на ранних стадиях (например, ингибитор аспартаткарбамо-илгрансферазы N -фосфоноацетил-L-аспартат), усиливают действие фторурацила в экспериментальных условиях, однако их клиническая эффективность не доказана (Grem et al., 1988). Метотрексат, блокируя синтез пуринов, повышает уровень фосфорибозилпирофосфата, что способствует активации фторурацила и усиливает его цитотокснческое действие; метотрексат должен назначаться перед фторурацилом, а не наоборот. Показано, что сочетание фторурацила с цисплатином высокоэффективно при опухолях головы и шеи, однако молекулярные основы взаимодействия этих препаратов изучены недостаточно (Grem, 2001).
Фармакокинетика. Фторурацил и флоксуридин вводят в/в, так как их биодоступность при приеме внутрь невелика и подвержена сильным колебаниям. Они разрушаются во многих тканях, особенно в печени. Тимидинфосфорилаза и дезоксиури-динфосфорилаза превращают флоксуридин во фторурацил, который инактивируется дигидропиримидиндегидрогеназой путем восстановления пиримидинового кольца. Дигидропирими-диндегидрогеназа содержится в печени, слизистой кишечника и других тканях, а также в опухолях; врожденная недостаточность этого фермента резко повышает чувствительность к фторурацилу (Lu et al., 1993; Milano et al., 1999). В тех редких случаях, когда фермент совсем отсутствует, даже обычные дозы фторурацила вызывают тяжелые побочные эффекты. Выявить таких больных позволяет определение дигидропиримидиндегидрогеназы в лейкоцитах или измерение отношения сывороточных концентраций фторурацила и его метаболита 5,6-дигид-рофторурацила (Heidelberger, 1975; Zhang et al., 1992). Последний в итоге превращается в а-фтор-бета-аланин (2-фтор-З-амино-пропионат).
При введении фторурацила в/в струйно его сывороточная концентрация достигает 0,1—1 ммоль/л; Т1/2 составляет 10— 20 мин. В течение 24 ч после однократного введения лишь 5—10% препарата выделяется с мочой. Несмотря на высокую активность дигидропиримидиндегидрогеназы в печени, печеночная недостаточность не требует снижения дозы, так как в печени этот фермент имеется в избытке и, кроме того, фторурацил может разрушаться и в других тканях. При д лительной в/в инфузии в течение 24—120 ч сывороточная концентрация фторурацила колеблется в пределах 0,5—8 мкмоль/л. Препарат легко проникает в СМЖ: после введения обычных доз его концентрация в СМЖ в течение 12 ч превышает 0,01 мкмоль/л (Grem,2001).
Капецитабин хорошо всасывается при приеме внутрь, создавая высокую сывороточную концентрацию 5'-дезоксифторуридина (Т1/2 около 1 ч) и в 10 раз меньшую концентрацию фторурацила. Печеночная недостаточность замедляет превращение капецитабина в 5’-дезоксифторуридин и во фторурацил, но не известно, возрастает ли при этом риск токсического действия (Twelves etal., 1999).
Применение. Фторурацил вызывает ремиссию у 10—20% больных с метастазирующими опухолями молочной железы и ЖКТ; кроме того, он помогает при раке яичников, шейки матки, мочевого пузыря, предстательной и поджелудочной желез и ротоглотки. Больным в удовлетворительном состоянии (без истощения и нарушения кроветворения) фторурацил назначают еженедельно по 750 мг/м2 (без фолината кальция) или по 500—600 мг/м2 (с фолинатом кальция), лечение длится 6—8 нед. Другая схема — по 500 мг/м2/сут в течение 5 сут с повторением курса каждый месяц, при сочетании с фолинатом кальция дозу снижают до 375—425 мг/м2 из-за риска стоматита и поноса. Кроме того, фторурацил вводят путем длительной в/в инфузии: продолжительностью до 21 сут (по 300 мг/м2/сут) или в течение 48 ч с повторением курса каждые 2 нед (de Gramont et al., 1998).
Флоксуридин (фтордезоксиуридин) назначают главным образом в виде длительной инфузии в печеночную артерию при метастазах рака толстой кишки или после резекции печени по поводу таких метастазов (Kemeny et al.,1999). Частота ремиссий при внутриартериальной инфузии составляет 40—50%, что вдвое выше, чем при в/в введении. Инфузия длится 14—21 сут и сопровождается небольшими общими побочными эффектами, однако после многократного повторения таких курсов лечения существенно возрастает риск стеноза желчных протоков (Kemeny et al., 1987; Hohn et al., 1986). Введение флоксуридина в артерии, питающие опухоль, может быть эффективным и в других случаях, например при опухолях головы и шеи. При первых проявлениях побочного действия (обычно стоматита или поноса) инфузию следует немедленно прекратить, так как эти осложнения развиваются постепенно, достигая максимальной выраженности к 7— 14-м суткам лечения.
Таблица 52.2. Препараты, усиливающие действие фторурацила
|
Препарат |
Предполагаемые механизмы взаимодействия |
|
Цисплатин |
Фторурацил нарушает репарацию вызванных цисплатином разрывов цепей ДНК. Цисплатин усиливает ингибирование тимидилатсинтазы, повышая запасы восстановленных фолатов |
|
Интерфероны |
Способствуют активации фторурацила. Препятствуют повышению синтеза тимидилатсинтазы |
|
Фолинат кальция |
Усиливает ингибирование тимидилатсинтазы, повышая запасы восстановленных фолатов |
Капецитабин разрешен ФДА для химиотерапии метаста-зирующего рака молочной железы при неэффективности паклитаксела с антрациклинами (см. ниже). Его назначают внутрь (2500 мг/м2/сут в 2 приема во время еды) в течение 2 нед, после чего делают перерыв на 1 нед. Этот цикл повторяют еще два раза.
Повысить частоту ремиссий позволяет сочетание фто-рурацила с другими препаратами (табл. 52.2): с циклофосфамидом и метотрексатом (при раке молочной железы), цисплатином (при опухолях головы и шеи), фолина-том кальция (при раке толстой кишки). Адъювантная химиотерапия, включающая фторурацил, повышает выживаемость при раке молочной железы (Early Breast Cancer Trialists Collaborative Group, 1988) и толстой кишки (схема с фолинатом кальция; Wolmark et al., 1993). Фторурацил обладает радиосенсибилизирующим действием и назначается на фоне облучения при местнораспространенных опухолях головы и шеи, раке пищевода, легкого и прямой кишки. Его также используют местно при предраковых заболеваниях кожи и многоочаговом базальноклеточном раке. Фторурацил помогает при тяжелом псориазе, устойчивом к другим препаратам (Alper et al., 1985).
Побочные эффекты. Фторурацил и флоксуридин имеют сходные побочные эффекты, которые обычно проявляются поздно, и в начале лечения сложно предсказать их риск и тяжесть. В первую очередь появляются снижение аппетита и тошнота, за ними следуют стоматит и понос, развитие которых указывает на то, что введена уже достаточная доза. Поражение слизистых на всем протяжении ЖКТ может вести к профузному поносу, шоку и смерти, особенно при длительной инфузии фторурацила или его сочетании с фолинатом кальция. При введении фторурацила в/в струйно на первый план выходит угнетение кроветворения. Число лейкоцитов достигает минимума через 9—14 сут после первого введения препарата, иногда наблюдаются также тромбоцитопения и анемия. Возможны выпадение волос вплоть до полной алопеции, поражение ногтей, дерматит, гиперпигментация и атрофия кожи. Описаны случаи поражения ЦНС, включая острые мозжечковые нарушения; при интратекальном введении иногда поражается спинной мозг. Наконец, изредка наблюдается кардиотоксическое действие, особенно острая боль в груди с признаками ишемии на ЭКГ. Ввиду узкого терапевтического диапазона фторпиримидинов лечение должно проводиться под контролем опытного химиотерапевта.
Побочное действие капецитабина в целом то же, что и фторурацила (понос, угнетение кроветворения); несколько чаше встречается прогрессирующая ладонно-подошвенная эритро-дизестезия — покраснение, шелушение, боль и парестезия кистей и стоп.
Цитарабин[править | править код]
Цитарабин (цитозин-арабинозид) — наиболее активный из антиметаболитов, применяемых при остром миелолейкозе, лучшее средство для индукционной монохимиотерапии этого заболевания (Garcia-Carbonero et al., 2001).
Механизм действия. Цитарабин — эпимер цитидина по 2'-гидроксигруппе (рис. 52.8). Поскольку она находится в транс-положении относительно З'-гидроксигруппы, цитарабин выступает как аналог 2'-дезоксицитидина. Эта 2'-гидроксигруппа препятствует вращению пиримидинового основания вокруг N—С-свя-зи, поэтому полиарабинонуклеотиды не способны создавать компактную пространственную структуру подобно полирибо-нуклеотидам.
Цитарабин попадает в клетку с помощью белков—переносчиков нуклеозидов. Как большинство аналогов нуклеотидов он требует активации. Дезоксицитндинкиназа фосфорилирует цитарабин с образованием цитарабинмонофосфата, который затем с помощью соответствующих ферментов превращается в цитарабиндифосфат и цитарабинтрифосфат. Последний конкурирует с дезокси- ЦТФ за включение в Д Н К, осуществляемое ДНК-полимеразами. Встроенный в ДНК цитарабинмонофос-фат действует как мощный ингибитор этих ферментов, препятствуя не только удлинению цепи во время репликации, но и репарации ДНК. Показана четкая зависимость между количеством молекул цитарабина в составе ДНК и степенью нарушения ее синтеза: так, включение 1 молекулы препарата на 2000 нуклеотидов приводит к гибели примерно половины клеток.
Цитарабин приводит к необычной дупликации участков ДНК, что повышает вероятность рекомбинации, транслокации и амплификации различных генов. Цитарабин превращается также в цитарабиндифосфатхолин (аналог естественного метаболита ЦДФ-холина), который нарушает синтез мембранных гликоп-ротеидов и гликолипидов. Кроме того, цитарабинмонофосфат препятствует присоединению галактозы, N-ацетилгалактозамина и сиаловых кислот к гликопротеидам мембран, а цитарабинтрифосфат тормозит синтез ЦМФ-N-ацетилнейраминовой кислоты. Таким образом, цитарабин нарушает строение, функции и антигенную структуру клеточных мембран.
Цитарабин вызывает окончательную дифференцировку лейкозных клеток in vitro, что сопровождается снижением экспрессии онкогена МУС(Bianchi Scarra et al., 1986). Однако эти изменения наблюдаются на фоне цитотоксической концентрации препарата и могут просто отражать необратимое повреждение клетки. Впрочем, исследование костного мозга у некоторых больных со стойкой ремиссией на фоне лечения цитарабином выявило сохранение маркеров лейкозных клеток, что указывает на дифференцировку последних.
Механизм гибели клеток при лечении цитарабином до конца не изучен. В нормальных и опухолевых клетках под действием цитарабина происходит фрагментация ДНК и появляются другие морфологические и биохимические признаки апоптоза (Smets, 1994). Судьбу клетки определяет сложное взаимодействие различных сигналов. Действуя на лейкозные клетки in vitro, цитарабин вызывает образование церамида, мощного индуктора апоптоза. С другой стороны, в них повышается активность протеинкиназы С, ингибитора апоптоза в кроветворных клетках. Соответственно, гибель или выживание клетки будет зависеть от того, какой из этих эффектов окажется более выраженным (Strum et al., 1994). Важную роль в регуляции роста и дифференцировки опухолевых клеток играют факторы транскрипции, контролирующие экспрессию генов. Апоптоз при действии цитарабина связывают с активацией факторов транскрипции семейств АР-1 (гетеродимеры белков Fos и Jun) и NFkB (Kharbanda et al., 1990). Сообщалось также, что цитарабин вызывает дефосфорилирование белка Rb, который получает возможность связываться с факторами транскрипции семейства E2F и инактивировать их, что препятствует экспрессии многочисленных генов, необходимых для продолжения клеточного цикла (Ikeda et al., 1996).
Чувствительность к цитарабину зависит также от периода клеточного цикла. По-видимому, действие цитарабина должно продолжаться на протяжении как минимум одного клеточного цикла, чтобы для всех клеток оно пришлось на период S, когда препарат наиболее активен. Это служит обоснованием длительной в/в инфузии цитарабина. Согласно ряду исследований, в/в струйное введение цитарабина лучше всего повторять через 8—12ч, что позволяет поддерживать терапевтическую концентрацию цитарабинтрифосфата в клетках на протяжении хотя бы одного клеточного цикла. Клеточный цикл миелобластов длится 1-2 сут, и схема лечения острого миелолейкоза обычно включает в/в струйное введение цитарабина каждые 12 ч в течение 5-7 сут или длительную инфузию в течение 7 сут.
Механизмы устойчивости. Чувствительность к цитарабину зависит от соотношения скоростей его активации и распада, определяющего долю препарата, которая превращается в цитара-бинтрифосфат. Скорость этого процесса зависит от способности дезоксицитидинкиназы переводить цитарабин в цитарабинмонофосфат. Важную роль в распаде препарата играет цитидиндезаминаза, под действием которой из цитарабина образуется неактивный уридинарабинозид; активность этого фермента повышена во многих тканях и в некоторых опухолях. Другой фермент, дезокси-ЦМФ-дезаминаза, превращает цитарабин-монофосфат в неактивный уридинарабинозидмонофосфат. При остром миелолейкозе выявлена связь между способностью лейкозных клеток образовывать и накапливать цитидинарабино-зидтрифосфат и длительностью полных ремиссий (Preisleret al., 1985). Большое значение имеет наличие у опухолевых клеток достаточного количества белков-переносчиков (Wiley et al., 1985).
Сывороточная концентрация цитарабина быстро падает ниже той, что необходима для насыщения систем его транспорта и активации, поэтому была испытана высокодозная химиотерапия. Введение препарата по 2—3 г/м 6 раз каждые 12 ч позволило увеличить сывороточную концентрацию в 20—50 раз и повысить эффективность индукционной и консолидирующей химиотерапии острого миелолейкоза (Bishop et al., 1996; Mayer et al., 1994).
В линиях опухолевых клеток мышей и человека, устойчивых к цитарабину, найдены различные биохимические изменения. Чаще всего встречается снижение активности дезоксицитидинкиназы (Flasshove et al., 1994). Описано также повышение активности ЦТФ-синтазы с накоплением дезокси-ЦТФ (Garcia-Carbonero et al., 2001). Вероятно, повышенный уровень дез-окси-ЦТФ не дает цитарабинтрифосфату нарушать синтез ДНК. Кроме того, возможно повышение активности цитидин-дезаминазы и снижение сродства ДНК-полимераз к цитарабинтрифосфату. Наконец, кроме скоростей активации и распада цитарабина цитотоксичность препарата зависит от реакции клетки на повреждение ДН К. Например, усиление синтеза белков Вс12 и Bcl-XL позволяет лейкозным клеткам избежать апоп-тоза при действии цитарабина in vitro (Ibrado et al., 1996). На реакцию может повлиять и степень фосфорилирования факторов транскрипции и белков, распознающих повреждение ДНК. Показано, что фосфорилирование белка Вс12 и факторов транскрипции семейства АР-1 в клеточных линиях миелобластов человека сопряжено с устойчивостью к цитарабину in vitro (Kolia and Studzinski, 1994). Клиническое значение перечисленных явлений изучено недостаточно.
Фармакокинетика. Из-за высокой активности цитидиндезами-назы в печени и слизистой ЖКТ биодоступность цитарабина при приеме внутрь не превышает 20%, поэтому его назначают в/в. При введении препарата в дозе 30—300 мг/м2 максимальная сывороточная концентрация составляет 2—50 мкмоль/л. После в/в введения препарат выводится быстро (начальный Т1/2 = 10 мин), а затем — медленнее (конечный Т1/2 около 2,5 ч). За 12—24 ч менее 10% препарата выводится почками в неизмененном виде, основную же часть в моче составляет продукт дезаминирования — неактивный уридинарабинозид. Длительная в/винфузия позволяет достичь более высокой концентрации в СМЖ, чем струйное введение. При интратекальном введении в дозе 50 мг/м даже через 7 ч дезаминируется лишь небольшая часть препарата, и максимальная концентрация в СМЖ достигает 1—2 ммоль/л; она снижается медленно, и конечный Т1/2 составляет около 3,4 ч. Терапевтическая концентрация (> 0,4 мкмоль/л) поддерживается в СМЖ в течение 24 ч. Разработан также липосомный цитарабин для интратекального введения: благодаря медленному высвобождению препарата терапевтическая концентрация сохраняется в среднем 12 сут, что позволяет избежать частых люмбальных пункций. По предварительным данным, липосомный цитарабин (50 мг каждые 2 нед) позволяет дольше задерживать прогрессирование нейролейкоза, чем обычный препарат (Glantz et all 1999).
Применение. Существуют две стандартные схемы введения цитарабина: 100 мг/м2 в/в струйно каждые 12 ч в течение 5—7 сут и 100—200 мг/м2/сут путем длительной инфузии в течение 5—7 сут. Дети лучше переносят высокие дозы цитарабина, чем взрослые. При нейролейкозе препарат вводят интратекально по 30 мг/м2 каждые 4 сут; по предварительным данным, в этих случаях не менее эффективен липосомный цитарабин (50 мг каждые 2 нед). При остром миелолейкозе как у детей, так и у взрослых более эффективна высокодозная химиотерапия (6 раз по 2—3 г/м2 в течение 2 ч каждые 12ч), однако она сопровождается большей нейротоксичностью, особенно у пожилых (Mayer et al., 1994).
Цитарабин применяют в качестве индукционной химиотерапии при острых лейкозах у детей и взрослых. Вероятность ремиссии при монохимиотерапии составляет 20—40%. Цитарабин наиболее активен при остром миелолейкозе у взрослых. Желательно сочетать цитарабин с другими препаратами, особенно антрациклинами и ми-токсантроном. Цитарабин используют также в составе полихимиотерапии при лимфомах высокой степени злокачественности у детей и взрослых и при рецидивах острого лимфолейкоза.
Побочные эффекты. Цитарабин сильно подавляет кроветворение и может вызвать тяжелую лейкопению, тромбоцитопению и анемию с мегалобластозом костного мозга. Другие побочные эффекты включают нарушения со стороны ЖКТ, стоматит, конъюнктивит, преходящее повышение активности печеночных ферментов, пневмонит, лихорадку и дерматит. При интратекальном введении и использовании высоких доз (особенно более 3 г/м в/в) у больных старше 40 лет на фоне почечной или печеночной недостаточности возможно поражение ЦНС, проявляющееся, в частности, эпилептическими припадками (Rubin etal., 1992).
Гемцитабин[править | править код]
Гемцитабин — наиболее активный из антиметаболитов, вошедших в клиническую практику за последние годы. Он применяется в составе схем химиотерапии первой линии при раке поджелудочной железы и немелкоклеточном раке легкого. Изначально внимание привлекла высокая активность гемцитабина при солидных опухолях у мышей и при трансплантатах опухолей человека у бестимусных мышей (Hertel et al., 1990).
Механизм действия. Гемцитабин имеет много общего с цитарабином. Он попадает в клетки путем активного транспорта (Mackey et al., 1998), далее дезоксицитидинкиназа фосфорилирует его с образованием дифтордезокси-ЦМФ (Heinemann et al., 1988), который превращается в дифтордезокси-ЦЦФ и дифтордезокси-ЦТФ. По характеру активации и воздействию на ДНК гемцитабин близок к цитарабину, однако имеет дополнительные точки приложения. Эти препараты по-разному включаются в ДНК и ингибируют ДНК-полимеразы и поэтому неодинаковы по спектру активности (Iwasaki et al., 1997). В отличие от цитарабина гемцитабин действует не только в периоде S, поэтому в равной степени влияет на быстро и медленно пролиферирующие клетки. Его цитотоксичность связана с нарушением синтеза ДНК: дифтордезокси-ЦЦФ как мощный ингибитор рибонуклеозиддифосфатредукгазы истощает запасы дезокси-рибонуклеотидов, а дифтордезокси-ЦТФ конкурирует с дезокси-ЦТФ, действуя как слабый ингибитор ДНК-полимераз, а также встраивается в ДНК. В последнем случае после присоединения еще одного нуклеотида синтез цепи обрывается (Hei-nemannet al., 1990; Huang etal., 1991). Очевидно, этот нуклеотид мешает ферментам репарации удалить дифтордезокси-ЦМФ из ДНК. Способность клеток включать дифтордезокси-ЦМФ в ДНК играет решающую роль в развитии апоптоза под действием гемцитабина (Huang et al., 1995).
Фармакокинетика. Гемцитабин вводят путем в/в инфузии. Скорость его выведения во многом определяется дезаминированием, и основным метаболитом гемцитабина является дифтордезоксиуридин. В зависимости от пола и возраста Т1/2 гемцитабина составляет 40—90 мин; начальный Т1/2 дифтордезоксиури-дина около 27 мин, конечный — около 14 ч (Abbruzzese et al.,1991). Клиренс гемцитабина зависит от дозы и может сильно различаться у разных людей.
Активация гемцитабина, как и цитарабина, зависит от способности дезоксицитидинкиназы превращать его в дифтордезокси-ЦМФ. В культуре клеток фермент насыщается при концентрации гемцитабина 15—20 мкмоль/л, такая сывороточная концентрация создается путем инфузии со скоростью около 10мг/м2/мин (Grunewald et al., 1991; 1992). Чтобы не превышать эту концентрацию и усилить образование дифтордезокси-ЦТФ, продолжительность инфузии увеличили до 90 мин. По сравнению с введением препарата за 30 мин такая инфузия повышает концентрацию дифтордезокси-ЦТФ в лимфоцитах, а также степень угнетения кроветворения и, возможно, эффективность (Тешрего et al., 1999).
Нарушение репарации ДНК под действием гемцитабина может усиливать цитотоксичность других противоопухолевых препаратов, особенно препаратов платины. Согласно исследованиям на клеточных линиях опухолей, гемцитабин увеличивает количество связей цисплатина с ДНК — вероятно, за счет подавления эксцизионной репарации (van Moorsel et al., 1999).
Применение. По стандартной схеме гемцитабин вводят по 1—1,2 г/м2 в/в в течение 30 мин 1 раз в неделю в течение 3 нед, затем делают перерыв на 1 нед. Кроме рака поджелудочной железы и немелкоклеточного рака легкого к гемцитабину чувствителен рак мочевого пузыря, шейки матки, яичников и молочной железы.
Побочные эффекты. Основное побочное действие гемцитабина — угнетение кроветворения, которое усиливается при увеличении продолжительности инфузии. Не менее чем в 40% случаев развиваются другие побочные эффекты, включая гриппоподобный синдром, слабость и небольшое повышение активности печеночных ферментов. Тяжелые осложнения редки, но иногда возникает пневмонит, поддающийся лечению глюко-кортикоидами. Описаны отдельные случаи гемолитико-уремического синдрома (Аарго et al., 1998).
Аналоги пуринов[править | править код]
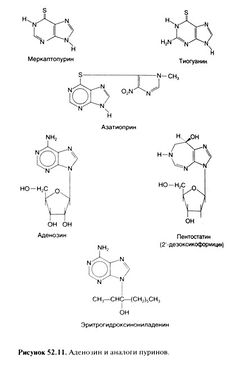
После первых работ Хитчингса и сотр., начатых в 1942 г., действие многочисленных аналогов пуриновых оснований, нуклеозидов и нуклеотидов было проверено на различных экспериментальных моделях. В результате многолетних испытаний были получены не только противоопухолевые препараты (меркаптопурин и тиогуанин), но и иммунодепрессанты (азатиоприн; Schwartz, 2000) и противовирусные средства (ацикловир, ганцикловир, видарабин, зидовудин). Структурные формулы некоторых из них приведены на рис. 52.11. Попутно был открыт аналог гипоксантина аллопуринол — мощный ингибитор ксанти-ноксидазы (гл. 27). Большие надежды возлагались на ингибиторы аденозиндезаминазы эритрогидроксинониладе-нин и пентостатин. Последние исследования подтвер. дили активность пентостатина при волосатоклеточном лейкозе, хроническом лимфолейкозе и лимфомах. В эксперименте ингибиторы аденозиндезаминазы усиливают действие аналогов аденозина, например видарабина; кроме того, они обладают свойствами иммунодепрессантов. Флударабин и кладрибин — препараты, устойчивые к действию аденозиндезаминазы, — высокоэффективны при различных лейкозах и лимфомах (Beutler, 1992; Cheson 1992; Piro, 1992; Calabresi and Schein 1993; Chabneretai2001).
Структурно-функциональная зависимость. Меркаптопурин и тиогуанин, с успехом применяемые при лейкозах, — это аналоги соответственно гипоксантина и гуанина, у которых кислород кетогруппы в положении 6 пуринового кольца заменен на серу При замене кислорода на хлор или селен также получаются вещества, обладающие противоопухолевым действием. Таким же действием обладают и соединения тиопуринов с рибозой или 2'-дезоксирибозой. Эти аналоги нуклеозидов легко гидролизуются пуриннуклеозидфосфорилазой, активность которой повышена во многих опухолях, высвобождая меркаптопурин и тиогуанин. Все аналоги пуриновых оснований и нуклеозидов (за некоторым важным исключением) нуждаются в активации путем превращения в нуклеотиды.
Значительные усилия были направлены на получение производных этих препаратов с более избирательным действием и широким терапевтическим диапазоном. Азатиоприн (рис. 52.11),S-имидазолильное производное меркаптопурина, менее подвержен инактивации путем S-метилирования, неферментатив-ного окисления или превращения в тиомочевую кислоту под действием ксантиноксндазы. В тканях он медленно, вероятно, без участия ферментов, реагирует с тиолами (в частности, глу-татионом), высвобождая меркаптопурин. Азатиоприн — более активный иммунодепрессант, чем меркаптопурин (Elion, 1967).
Большим шагом вперед стало открытие ингибиторов аденозиндезаминазы — пентостатина (К = 2,5 пмоль/л) и эритрогид-роксинониладенина К=2 нмоль/л). Пентостатин (2'-дезоксико-формицин) вырабатывается Streptomyces antibioticus (рис. 52.11).
По строению он напоминает переходный комплекс при гидролизе аденозина аденозиндезаминазой, и его сродство к ферменту в Ю7 раз выше, чем у естественного субстрата. Комплекс фермент-ингибитор очень стоек, лишь через 25—30 ч его количество снижается вдвое за счет диссоциации (Agarwal et al., 1977; Agarwal, 1982). Пентостатин нарушает дезаминирование не только нуклеотидов, но и их аналогов, используемых в химиотерапии.
Механизм действия. Клетки животных содержат нуклеозидки-назы, которые превращают аденозин, дезоксиаденозин, дезоксигуанозин, дезоксиинозин и многие их аналоги в 5'-монофосфаты. Ферментов, катализирующих фосфорилирование инозина, гуанозина и их аналогов, в организме нет, поэтому вначале пуриннуклеозидфосфорилаза, активность которой высока во многих тканях, отщепляет от них рибозу, а затем гипоксантин-фосфорибозилтрансфераза превращает образовавшиеся азотистые основания в рибонуклеозидмонофосфаты. Дезоксигуанозин, дезоксиинозин и их аналоги также могут гидролизоваться пуриннуклеозидфосфорилазой и далее превращаться в соответствующие рибонуклеозидмонофосфаты.
Гипоксантинфосфорибозилтрансфераза превращает тиогуанин и меркаптопурин соответственно в тио-ГМФ и тио-ИМФ. Тио-ИМФ имеет низкое сродство к гуанилаткиназе (ферменту, катализирующему превращение ГМФ в ГДФ), и поэтому тио-ИМФ накапливается в клетке. Впрочем, детальные исследования обнаружили меркаптопурин в составе ДНК в виде тиоде-зокси-ГМФ, что указывает на медленный метаболизм меркаптопурина под действием ферментов пуринового обмена. Тио-ИМФ ингибирует ряд важных реакций, таких, как превращение ИМФ в аденилосукцинат и затем в АМФ, а также окисление ИМФ до ксантозинмонофосфата под действием ИМФ-де-гидрогеназы. В присутствии тиогуанина в клетках вначале накапливается тио-ГМФ, который медленно превращается в тио-ГДФ (под действием гуанилаткиназы), а затем в тио-ГТФ, который встраивается в нуклеиновые кислоты. Кроме того, внутриклеточной концентрации тио-ГМФ достаточно для необратимого ингибирования ИМФ-дегидрогеназы. Вероятно, это связано с образованием дисульфидных связей между тио-ГМФ и ферментом. С другой стороны, тио-ГМФ, тио-ИМФ и другие монофосфаты аналогов пуриновых нуклеозидов имитируют нормальную регуляцию по принципу отрицательной обратной связи, вызывая аллостерическое ингибирование амидофосфори-бозилтрансферазы, катализирующей ключевую реакцию синтеза пуринов — образование фосфорибозиламина из глутамина и фосфорибозилпирофосфата. Этот фермент служит основным регулятором синтеза пуриновых нуклеотидов; в частности, при повышении внутриклеточной концентрации естественных мононуклеотидов и их аналогов его активность снижается. Кроме того, АДФ, АТФ и их аналоги препятствуют синтезу фосфорибозилпирофосфата. Меркаптопурин ингибирует также фосфоф-руктокиназу — один из ферментов гликолиза (Mojena et al., 1992). Наконец, тиопуринметилтрансфераза превращает меркаптопурин в S-метилмеркаптопурин, а нуклеотиды, содержащие S-метилмеркаптопурин, ингибируют ферменты синтеза пуринов. Показано также, что S-метилмеркаптопурин тормозит ангиогенез in vitro и in vivo (Presta et al., 1999).
Несмотря на многочисленные исследования, до сих пор не ясно, в какой мере эффективность и токсичность тиогуанина и меркаптопурина обусловлены встраиванием в ДНК (Во et al.,1999; Marathias et al., 1999). Например, обнаружено, что риск осложнений при беременности существенно возрастет, если отец ребенка получал меркаптопурин в течение 3 мес перед зачатием (Rajapakse et al., 2000). Тиопурины препятствуют синхронной активации различных ферментов, участвующих в репликации ДНК; важную роль может играть и нарушение полн-аденилирования РНК (Carrico and Sartorelli, 1977; Giverhauget al., 1999).
Показано, что даже непродолжительное действие тиогуанина нарушает синтез мембранных гликопротеидов, что также способно вызвать гибель клетки. Вероятно, этот эффект связан с нарушением синтеза нуклеотидсахаров, содержащих ГДФ.
Таким образом, тиопурины оказывают цитотоксическое действие за счет нарушения различных метаболических процессов, включая синтез пуринов, взаимопревращения нуклеотидов, синтез нуклеиновых кислот, гликопротеидов, и, по последним данным, за счет подавления ангиогенеза. Соответственно, невозможно выделить какой-либо один механизм действия этих препаратов (Hortelano and Bosca, 1997).
Аналог аденозина видарабин (арабинозиладенин) не обладает выраженным цитотоксическим действием из-за быстрого дезаминирования, однако применяется как противогерпетическое средство (гл. 50). Флударабин устойчив к дезаминированию и обладает значительной активностью при хроническом лимфолейкозе и лимфомах низкой степени злокачественности, устойчивых к другим противоопухолевым препаратам (Bloch, 1975;Chun et al., 1986; Calabresi and Shein, 1993; Keating et al., 1998; * Zinzani et al., 2000; Chabner et al., 2001).
Пентостатин — мощный ингибитор аденозиндезаминазы, однако связь между этим действием и цитотоксичностью не ясна. Очевидно, повышение концентраций производных аденозина по механизму отрицательной обратной связи ингибирует аденозилгомоцистеиназу, в результате чего нарушаются процессы метилирования. Кроме того, пентостатин нарушает синтез НАД. Наконец, пентостатинтрифосфат способен встраиваться в ДНК, вызывая разрыв ее цепей (Siaw and Coleman, 1984; Johnston et al., 1986; Begleiter et al., 1987; Calabresi et al., 1993; Chabner et al., 2001).
Наследственная недостаточность аденозиндезаминазы нарушает функцию Т- и В-лимфоцитов, но мало влияет на другие клетки (Giblett et al., 1972). Соответственно, у экспериментальных животных пентостатин вызывает выраженный иммунодефицит, а его применение в клинике может привести к тяжелым и даже смертельным оппортунистическим инфекциям. После обнаружения высокой активности аденозиндезаминазы в опухолевых Т-лимфоцитах монотерапия пентостатином была с успехом испытана при Т-клеточных лейкозах и лимфомах (в частности, грибовидном микозе). Однако препарат действует и при В-клеточных лейкозах, вызывая ремиссию у 25% больных хроническим лимфолейкозом, устойчивым к другим противоопухолевым препаратам, и у 90% больных волосатоклеточным лейкозом. Высокую активность при волосатоклеточном лейкозе показал и другой аналог пуринов — кладрибин (2-хлордезоксиаденозин). Этот препарат устойчив к действию аденозиндезаминазы; он фосфорилируется дезоксицитидинкиназой и встраивается в ДНК. Югадрибин помогает при различных лейкозах и лимфомах; ввиду высокой эффективности и меньшей токсичности его часто назначают вместо пентостатина при волосатоклеточном лейкозе (Symposium, 1984; Tritsch, 1985; Beutler, 1992; Kay et al., 1992; Estey et al., 1992; Saven and Piro, 1992; Hoffman et al., 1994; Tallman et al., 1995; Dearden et al., 1999; Chabner et al.,2001).
Механизмы устойчивости. Основным недостатком аналогов пуринов, как и других антиметаболитов, является быстрое развитие устойчивости к ним. В культуре клеток устойчивость обычно вызвана недостаточностью или полным отсутствием гипок-сантинфосфорибозилтрансферазы. Возможно также снижение сродства этого фермента к аналогам пуринов. Такие изменения обычно сопровождаются перекрестной устойчивостью к мер-каптопурину, тиогуанину и 8-азагуанину.
Другие механизмы устойчивости лейкозных клеток к аналогам пуринов включают: 1) повышение активности щелочной фосфатазы лейкоцитов, 2) нарушение транспорта препаратов в клетки, 3) ускоренное разрушение препаратов и их фосфорилированных производных, 4) нарушение аллостерического ингибирования амидофосфорибозилтрансферазы, 5) усиление репарации ДНК, 6) утрату или снижейие активности аденинфосфорибозилтрансферазы и аденозинкиназы, участвующих в активации аналогов аденина и аденозина, или дезоксицитидин-киназы, активирующей флударабин, 7) усиление синтеза белка—переносчика MRP5 (Wijnholds et al., 2000). Какой из этих механизмов устойчивости наиболее распространен в клинической практике, остается неизвестным (Brockman, 1974).
Меркаптопурин[править | править код]
Открытие меркаптопурина Элионом и сотр. стало важной вехой в истории создания противоопухолевых препаратов и иммунодепрессантов. Меркаптопурин и его производное азатиоприн остаются важнейшими препаратами этих групп (ReJlingetal., 1999а, b; Mahoney etal., 1998). Меркаптопурин применяют главным образом в качестве поддерживающей химиотерапии при остром лимфолейкозе. Структурно-функциональная зависимость, механизм действия, а также механизмы устойчивости меркаптопурина обсуждались выше. Структурная формула меркаптопурина приведена на рис. 52.11.
Фармакокинетика. Из-за неполного всасывания и разрушения при первом прохождении через печень биодоступность меркаптопурнна при приеме внутрь колеблется в широких пределах и составляет лишь 5—37%. Для подбора дозы может потребоваться измерение сывороточной концентрации. Биодоступность меркаптопурина повышается на фоне высоких доз метотрекса-Г та (Innocenti et al., 1996). Т1/2 меркаптопурина при в/в введении относительно мал (около 50 мин у взрослых), что связано с быстрым разрушением препарата, его захватом клетками и выведением с мочой. Из-за высокой активности белков-переносчи-ков, выводящих меркаптопурин через гематоэнцефалический барьер, его концентрация в ЦНС невелика (Deguchi et al., 2000). Кроме превращения в тио-ИМФ под действием гипоксантин-фосфорибозилтрансферазы существуют еще два важных пути метаболизма меркаптопурина. Во-первых, он может подвергаться S-метилированию под действием тиопурин-8-метилтрансферазы с последующим окислением метилированных производных. Ген тиопуринметилтрансферазы имеет несколько аллельных вариантов (Yates et al., 1997; Iyer, 1999; Relling et al.,1999b), причем у 15% англичан, например, активность этого фермента мала или совсем отсутствует (Weinshilboum, 1989). Низкая активность тиопуринметилтрансферазы в эритроцитах сопровождается усилением токсичности меркаптопурина. Показано, что при введении меркаптопурина или меркаптоинози-на образуются нуклеотиды, содержащие S-метилмеркаптопурин. В лимфоцитах и костном мозге больных, получавших меркаптопурин или азатиоприн, обнаружено существенное количество таких нуклеотидов (моно-, ди- и трифосфатов). S-метилированные производные тиопуринов могут подвергаться десульфированию, и часть содержащейся в них серы выводится с мочой в виде неорганического сульфата. Второй важный путь метаболизма меркаптопурина — его окисление до неактивной тиомочевой кислоты, катализируемое ксантиноксидазой. Активность этого фермента относительно высока в печени.
Попытка замедлить инактивацию меркаптопурина привела к синтезу аналога гипоксантина аллопуринола — мощного ингибитора ксантиноксидазы, который не только блокирует окисление меркаптопурина в тиомочевую кислоту, но и нарушает образование мочевой кислоты из гипоксантина и ксантина (гл. 57). Препятствуя окислению меркаптопурина и азатиопри-на, аллопуринол усиливал их действие на клетки. Аллопуринол значительно повышал противоопухолевую активность меркаптопурина у мышей, но возрастала и токсичность, поэтому расширить терапевтический диапазон меркаптопурина не удалось (Zinner and Klastersky, 1985).
Применение. Меркаптопурин назначают внутрь, начальная доза составляет 2,5 мг/кг/сут (100—200 мг/сут). При достижении гематологической ремиссии и улучшении состояния дозу снижают, в качестве поддерживающей терапии меркаптопурин обычно назначают по 1,5-2,5 мг/кг/сут. Если через 4 нед лечение не приноситуспеха, суточную дозу постепенно повышают до 5 мг/кг, пока не проявится побочное действие. При солидных опухолях общая доза меркаптопурина, вызывающая угнетение кроветворения, колеблется от 18 до 106 мг/кг (в среднем 45 мг/кг).
Меркаптопурин способен вызвать гиперурикемию и гиперурикозурию. Освобождение пуриновых нуклеотидов из погибших клеток, а также нарушение превращения ИМФ в ГМФ и АМФ ведут к накоплению пуриновых оснований и их ускоренному окислению до мочевой кислоты под действием ксантиноксидазы. В таких случаях показан аллопуринол, однако он усиливает токсичность меркаптопурина (а также азатиоприна). На фоне аллопуринола дозу этих препаратов следует снизить примерно в 4 раза.
В первых клинических испытаниях меркаптопурин вызывал ремиссию у 40% детей с острым лейкозом. У взрослых его эффективность намного ниже, но иногда также удается добиться ремиссии. В целом при остром лимфолейкозе препарат применяют прежде всего для поддерживающей, а не для индукционной химиотерапии. Перекрестная устойчивость к меркаптопурину и противоопухолевым препаратам других групп не отмечена.
Меркаптопурин можно использовать для поддерживающей химиотерапии при хроническом миелолейкозе, но существуют и более эффективные препараты. При хроническом лимфолейкозе, лимфомах и солидных опухолях меркаптопурин, даже в высоких дозах, не действует.
В качестве иммунодепрессанта предпочтительнее назначать азатиоприн.
Побочные эффекты. Основной побочный эффект — угнетение кроветворения, но обычно оно развивается медленнее, чем при применении антагонистов фолиевой кислоты. Тромбоцитопения, лейкопения и анемия возникают не раньше чем через несколько недель после начала лечения. Отмена препарата обычно быстро восстанавливает нормальное кроветворение. Примерно у 25% взрослых наблюдаются потеря аппетита, тошнота и рвота; риск стоматита и поноса невелик. У детей осложнения со стороны ЖКТ развиваются реже. Сообщалось, что примерно у 1/3 взрослых на фоне меркаптопурина возникает желтуха.
Ее патогенез не известен, могут играть роль некроз гепатоци-тов и холестаз; после прекращения лечения желтуха проходит. Кроме того, возможно поражение кожи. Применение меркаптопурина и азатиоприна в качестве иммунодепрессантов сопряжено с рядом поздних осложнений (Schein and Winokur,1975; Kirschner, 1998; Korelitz et al., 1999). При длительном приеме в I триместре беременности меркаптопурин оказывает тератогенное действие. Описан случай острого миелолейкоза на фоне длительного лечения меркаптопурином болезни Крона (Heizer and Peterson, 1998).
Азатиоприн[править | править код]
Азатиоприн (рис. 52.11) применяется в качестве иммунодепрессанта. История его создания, механизм действия и метаболизм описаны выше (см. также гл. 53).
Триогуанин[править | править код]
В 1955 г. Элион и Хитчингс сообщили о синтезе тиогуа-нина (рис. 52.11). Его механизм действия описан выше. Препарат наиболее эффективен в сочетании с цитараби-ном при остром миелолейкозе.
Фармакокинетика. При приеме внутрь всасывание тиогуанина неполное и непостоянное; сывороточная концентрация достигает максимума через 2—4 ч после приема и у разных людей может отличаться более чем в 10 раз. Тиогуанин выделяется с мочой, в основном в виде S-метилтиогуанина; важнейшими его метаболитами в моче служат также неорганический сульфат, а при длительной в/в инфузии — и 8-гидрокситиогуанин (Kitchen et al., 1999). Тиомочевая кислота образуется в меньшем количестве, так что дезаминирование под действием гуаниндеза-миназы не играет ведущей роли в метаболизме тиогуанина. Непосредственный продукт дезаминирования — тиоксантин — не активен, поэтому тиогуанин, в отличие от меркаптопурина и азатиоприна, можно назначать вместе с аллопуринолом в обычной дозе.
Применение. Тиогуанин выпускается в таблетках для приема внутрь. Средняя суточная доза составляет 2 мг/кг, если через 4 нед не наблюдается улучшения и нет побочных эффектов, ее постепенно увеличивают до 3 мг/кг.
Тиогуанин назначают при острых лейкозах; его сочетание с цитарабином — наиболее эффективная схема индукционной химиотерапии острого миелолейкоза. Активность тиогуанина в отношении солидных опухолей невелика. Препарат широко применяется в качестве иммунодепрессанта при гломерулонефритах и коллагено-зах.
Побочные эффекты. Основное значение имеют угнетение кроветворения и побочные эффекты на ЖКТ (менее выраженные, чем на фоне меркаптопурина). Кроме того, тиогуанин менее гепатотоксичен, чем меркаптопурин.
Флударабин[править | править код]
Флударабин (9-Р-В-арабинофуранозил-2-фтораденин,2-фторарабинозиладенин) — фторированный аналог противовирусного средства видарабина, устойчивый к дезаминированию. Обычно применяется фосфат флудараби-на. Флударабин активен при хроническом лимфолейкозе и лимфомах низкой степени злокачественности (Са-labresi et al., 1993; Chabner et al., 2001; Zinzani et al., 2000; Nagleret al., 2000; Petrus et al., 2000). В крови мембранная 5'-нуклеотидаза быстро дефосфорилирует препарат, а в клетках он снова фосфорилируется дезоксицитидинки-назой, превращаясь в активный метаболит — флудара-бинтрифосфат. Последний ингибирует ДНК-полимеразы, праймазу, лигазы и рибонуклеотидредуктазу, а также встраивается в ДНК и РНК (Brockman et al., 1980). В составе ДНК флударабин препятствует удлинению цепи (Kamiyaetal., 1996), а в составе РНК нарушает ее процессинг и функции, в том числе трансляцию мРНК (Plunkett and Gandhi, 1992). Важную роль может играть активация апоптоза (Huang et al., 1995), что объясняет эффективность флудараби на при медленно текущих лимфопроли-феративных заболеваниях, когда лишь небольшая часть опухолевых клеток находится в периоде S (Dighiero, 1996). Механизм цитотоксического действия флударабина подробно не изучен, основную роль, очевидно, играют прекращение репликации и активация апоптоза (Sandoval et al., 1996).
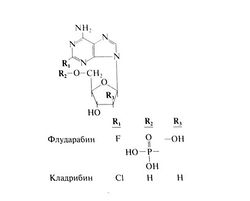
Структурные формулы флударабина и близкого по структуре кладрибина следующие:
Фармакокинетика. Флударабин вводят в/в, в крови он быстро дефосфорилируется. Его конечный Т(/2 составляет около 10 ч. Основная часть флударабина выводится почками, причем около 23% — в неизмененном виде, так как он достаточно устойчив к дезаминированию.
Применение. Флударабин вводят в/в по 20—30 мг/м2/сут в течение 5 сут, при почечной недостаточности дозу снижают. Инфузия длится от 30 мин до 2 ч. Курс повторяют каждые 4 нед; как правило, после 2—3 курсов постепенно наступает улучшение.
Флударабин обычно назначают при хроническом лим-фолейкозе; накапливаются также данные о его эффективности при В-клеточных лимфомах, устойчивых к стандартному лечению. Флударабин действует при лимфомах низкой степени злокачественности, остром про-миелоцитарном лейкозе, Т-клеточных лимфомах кожи и макроглобулинемии Вальденстрема (Chun et al., 1991). Он вызывает ремиссию у 32—48% больных хроническим лимфолейкозом, устойчивым к лечению алкилирующи-ми средствами. При нелеченных лимфомах низкой степени злокачественности вероятность полных ремиссий на фоне химиотерапии флударабином и циклофосфами-дом приближается к 90% (Hochster et al., 1994). Сочетание флударабина, митоксантрона и дексаметазона позволяет достичь ремиссии более чем в 90% случаев лим-фом низкой степени злокачественности (McLaughlin et al., 1996; Emmanouilidesetal., 1998).
Побочные эффекты. Возможны угнетение кроветворения, тошнота, рвота, лихорадка, озноб, слабость, недомогание и снижение аппетита. Наращиванию дозы препятствуют лимфопения и тромбоцитопения, иногда они имеют кумулятивный характер (Malspeis et al., 1990). Под действием флударабина гибнут лимфоциты CD4 (O’Brien et al., 1993). Встречаются оппортунистические инфекции (Cheson, 1995) и синдром распада опухоли. Стандартные дозы могут вызвать нейропатию (Cheson et al., 1999); другие неврологические нарушения — угнетение сознания, эпилептические припадки, неврит зрительного нерва и кома — чаще возникают на фоне высоких доз. Риск и тяжесть ней-ротоксического действия нарастают с возрастом. Описаны случаи тяжелого и даже смертельного пневмонита, вызванного сочетанием флударабина с пентостатином. Поскольку значительная часть препарата (около 1/4) выводится с мочой, то при ХПН его следует применять с осторожностью; начальную дозу снижают пропорционально падению СКФ.
Пентостатин[править | править код]
Пентостатин (2'-дезоксикоформицин) выделен из культуры Streptomyces antibioticus. Он напоминает переходный комплекс, возникающий при дезаминировании аденозина, и является мощным ингибитором аденозиндезаминазы. В присутствии пентостатина в клетке растет концентрация адениновых рибо- и дезоксирибонуклеотидов, которые ингибируют рибонуклеотидредуктазу и нарушают синтез ДНК. Дезоксиаденозин инактивирует аденозилгомоцистеиназу, из-за чего накапливается токсичный для лимфоцитов S-аденозилгомоцистеин. Кроме того, пентостатин нарушает синтез РНК, а его производное — пентостатинтрифосфат — встраивается в ДНК.
В сочетании с дезоксиаденозином пентостатин вызывает апоптоз опухолевых клеток при остром монобластном лейкозе (Niitsu et al., 1998). Механизм цитотоксичности пентостатина до конца не ясен, очевидно, при волосатоклеточном лейкозе и Т-клеточных лимфомах его действие связано с нарушением соотношения между пуриновыми нуклеотидами (Calabresi et al., 1993; Chabner et al., 2001; Rafel etal.,2000).
Структурная формула пентостатина представлена на рис. 52.11.
Фармакокинетика. Пентостатин вводят в/в; есть данные о том, что при дозе 4 мг/м начальный Т1/2 составляет 11 мин, конечный — около 5,7 ч. Препарат почти полностью выводится почками, и при ХПН дозу снижают пропорционально падению СКФ.
Применение. Пентостатин назначают по 4 мг/м2 в/в с интервалом в 2 нед. Сначала вводят 500— 1000 мл 5% глюкозы в 0,45% NaCl, затем струйно или путем инфузии продолжительностью до 30 мин вводят пентостатин, после к чего вводят еще 500 мл жидкости. При попадании в ткани препарат не вызывает некроза, отторжения тканей или воспаления.
Пентостатин крайне эффективен в качестве индукци-онной терапии волосатоклеточного лейкоза. По некоторым данным, даже при устойчивости к препаратам интерферона а частота полных ремиссий составляет 58%, а частичных — 28%. Пентостатин показан при хроническом лимфолейкозе и миелолейкозе, остром промиело-цитарном лейкозе, Т-клеточных лимфомах кожи и других лимфомах, а также гистиоцитозе X (Diliman, 1994; Cortes et al., 1997). Солидные опухоли и миеломная болезнь малочувствительны к пентостатину.
Побочные эффекты. На фоне обычных доз (4 мг/м ) отмечаются угнетение кроветворения, поражение ЖКТ, сыпь и повышение активности печеночных ферментов. Снижается число Т-лимфоцитов, возможны также нейтропения, лихорадка и оппортунистические инфекции (Steis et al., 1991). Нарушение иммунитета иногда сохраняется в течение нескольких лет после отмены пентостатина (Kraut etal., 1990). Высокие дозы (10 мг/м2) опасны тяжелым поражением почек и UHC. Сочетание пентостатина с флударабином может вызвать тяжелый и даже смертельный пневмонит.
Кладрибин[править | править код]
Кладрибин (2-хлордезоксиаденозин) — устойчивый к адснозиндезаминазе аналог пуринов, активный при волосатоклеточном лейкозе, хроническом лимфолейкозе и лимфомах низкой степени злокачественности (Estey et а!.. 1992; Kay etal., 1992; Beutler, 1992; Deardenetal., 1999; Tondini et al., 2000). Он безопасен и умеренно эффективен при прогрессирующем рассеянном склерозе (Rice et al.. 2000). В клетках кладрибин фосфорилируется дезоксииитндинкинаюй и затем превращается в кладрибинт-рифосфат Кладрибин включается в ДНК, вызывая разрывы цепей, и истощает запасы НАД и АТФ; в некоторых клеточных линиях он вызывает апоптоз (Piro, 1992-Beutler, 1992). Препарат активен в отношении как делящихся, так и покоящихся клеток.
Структурная формула кладрибина приведена выше вместе с формулой флударабина.
Фармакокинетика. При приеме внутрь кладрибин всасывается лишь на 55 ± 17%, и поэтому его вводят в/в (Liliemark et al.1992). Начальный и конечный Т)/2 составляют соответственно 35 мин и 6,7 ч; препарат выводится в основном почками (Liliemark and Juliusson, 1991). Кладрибин проникает через гематоэнцефалический барьер, и его концентрация в СМЖ достигает 25% сывороточной концентрации. При опухолевой инфильтрации мозговых оболочек его концентрация в СМЖ может быть выше, чем сывороточная.
Применение. Кладрибин вводят путем длительной в/в инфузии по 100 мкг/кг/сут в течение 7 сут; проводится лишь 1 курс.
Ввиду высокой эффективности и низкой токсичности кладрибин служит препаратом выбора при волосатоклеточном лейкозе. Единственный курс химиотерапии вызывает полную ремиссию в 80% случаев и частичную остальных 20% случаев (Saven and Piro, 1992; Deardenet al., 1999). Препарат активен при хроническом лимфолейкозе, остром миелолейкозе (особенно у детей), лимфомах низкой степени злокачественности, Т-клеточных лимфомах кожи, включая грибовидный микоз и синдром Сезари, макроглобулинемии Вальденстрема, а также при гистиоцитозе X (Piro etal., 1988; Piro, 1992; Santana et al., 1992; Kuzel et al., 1992; Kay et al., 1992; Saven et al., 1992; Dimopoulos et al., 1993; Robak et al., 1999; Saven and Buri-an, 1999; Tondini et al., 2000).
Побочные эффекты. Основное значение имеет угнетение кроветворения; после нескольких курсов иногда наблюдается кумулятивная тромбоцитопения. Часто возникают оппортунистические инфекции, их риск коррелирует со снижением числа лимфоцитов CD4. Другие осложнения включают тошноту, рвоту, высокую лихорадку, головную боль, слабость, сыпь и синдром распада опухоли. Нейротоксическое и иммуносупрессивное действие выражено слабее, чем у пентостатина, вероятно, потому, что кладрибин не ингибирует аденозиндезаминазу.