Вирусные векторы (генотерапия)
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Вирусные векторы[править | править код]
Благодаря особенностям жизненного цикла вирусов, первые векторы (носители трансгенов) для генотерапии стали разрабатывать именно на их основе. Вирусы переносят чужеродные гены, которые затем способны экспрессироваться в зараженных клетках. Упрощенно вирус можно представить как нуклеиновую кислоту, упакованную в оболочку. Вирус проникает в клетку-мишень, где происходит экспрессия вирусного генома. Для создания хорошего вектора необходимо изменить некоторые свойства вируса. В большинстве случаев вирус должен быть лишен возможности к репродукции, чтобы предотвратить неконтролируемое распространение трансгена. Кроме того, часть вирусного генома необходимо удалить, чтобы освободить место для чужеродного генетического материала. Другие необходимые изменения зависят от типа вируса. Вирусные векторы широко используют в доклинических исследованиях и в настоящее время именно с ними проводят большинство клинических испытаний.
При выборе вектора необходимо учитывать некоторые важные особенности жизненного цикла и биологии исходного вируса (Robbins and Ghivizzani, 1998). Для успешной трансдукции необходимо обеспечить избирательное заражение клеток-мишеней (тропность) и последующую экспрессию трансгена. Тропность частично определяется наличием специфических мембранных рецепторов, связывающих вирус на поверхности клетки и облегчающих его проникновение внутрь. Для экспрессии трансгена необходимо проникновение вирусного генома в ядро клетки с последующей успешной транскрипцией и трансляцией. Несколько дополнительных факторов определяют продолжительность экспрессии трансгена в зараженной клетке. Наконец, на пригодность вируса в качестве вектора влияют некоторые методические аспекты генной инженерии и получения вирусного вектора. Основные вирусные векторы, используемые сейчас в клинических испытаниях или признанные перспективными, созданы на основе ретровирусов (в частности, лентивирусов), аденовирусов, аденоасоциированных вирусов и вируса простого герпеса. Ниже приведены основные биологические свойства каждого типа вирусного вектора, важные для генотерапии. Конкретное применение отдельных векторов более подробно описано далее в этой главе.
Ретровирусы[править | править код]
Это небольшие РНК-содержащие вирусы, способные заражать только делящиеся клетки, в которых они репродуцируются. Вирусный геном (в виде провируса) встраивается в ДНК клетки-мишени. Поэтому ретровирусные векторы теоретически способны обеспечить длительную экспрессию трансгенов в некоторых типах клеток. Большинство ретровирусных векторов получено на основе вируса лейкоза мышей Молони. Геном вируса изменен так, чтобы избежать экспрессии вирусных белков в зараженных клетках, что предотвращает развитие иммунного ответа против этих клеток. Поскольку эти вирусы заражают только делящиеся клетки, ретровирусные векторы используют в основном для трансдукции клеток ex vivo (см. ниже) или для экспериментального лечения злокачественных новообразований.
Жизненный цикл. Геном ретровирусов состоит из плюс-цепи РНК. Оболочка ретровирусов образуется из мембраны зараженной клетки и содержит вирусные белки. Для репликации генома и сборки вирусов необходимы три вирусных гена — gag, pol и env. В зараженной клетке путем обратной транскрипции на матрице вирусной РНК происходит образование двухцепочечной ДНК (провируса), которая затем встраивается в клеточный геном. Это обеспечивают вирусные белки — обратная транскриптаза и интеграза. Для проникновения провируса в ядро необходимо разрушение ядерной оболочки клетки, происходящее в ходе митоза. Встроившийся в клеточный геном провирус использует аппарат клетки для транскрипции вирусныхмРНК, их процессинга и трансляции. Жизненный цикл вируса завершается с синтезом новых плюс-цепей РНК на матрице провируса. Специфическая последовательность в молекуле РНК (psi) дает сигнал сборки, после чего новые вирусы отпочковываются от поверхности клетки.
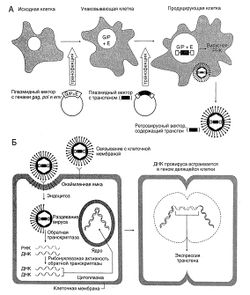
Конструкция и получение вектора. Ретровирусные векторы получают из соответствующего провируса. Гены gag, pol и env удаляют, чтобы освободить место для нового генетического материала и предотвратить репродукцию вируса (рис. 5.1). В ретровирусный вектор может быть включено до 8000 пар нуклеотидов чужеродной ДНК. Поскольку рекомбинантный вирус не может синтезировать вирусные мРНК, то в трансфицированных клетках отсутствует и синтез вирусных белков, которые могли бы вызвать иммунный ответ. Вместе с геном, предназначенным для лечения, в вектор можно ввести промотор и энхан-сер, обеспечивающие эффективную экспрессию трансгена и, в ряде случаев, ее тканеспецифичность. Можно использовать также вирусные промотор и энхансер, расположенные в области длинных концевых повторов (LTR).
После удаления генов, кодирующих вирусные белки и обеспечивающих репродукцию вируса, вирус способен репродуцироваться только в специально созданных линиях упаковывающих клеток, синтезирующих эти белки (рис. 5.1). В геном этих клеток встраивают вирусные гены (gag, pol и env) таким образом, чтобы они находились на разных хромосомах. Это снижает вероятность обратной рекомбинации этих генов в исходный вирусный геном и образования вирусов, способных к репродукции. После введения рекомбинантной ДН К провируса в упаковывающие клетки последние начинают производить ретровирусный вектор. ДНК провируса вводят в виде плазмиды, в которой между двумя длинными концевыми повторами заключены небольшой участок гена gag с сигналом сборки и чужеродные гены. Трансдукцию упаковывающих клеток осуществляют стандартным методом. Разработано несколько модификаций этого подхода, призванных снизить вероятность рекомбинации с образованием вируса, способного к репродукции (Jolly, 1994).
Описание к рисунок 5.1. Использование ретровирусного вектора. А. Схема получения ретровирусного вектора. Для получения не способных к репродукции ретровирусных векторов используют специальные линии клеток, способные синтезировать те вирусные белки, гены которых удалены при конструировании вектора. В клетки подходящей линии (например, эмбриональные клетки почки человека) с помощью бактериальных плазмид вводят гены gag (G), pol (Р) и env (Е). Клетки, синтезирующие соответствующие вирусные белки, называют упаковывающими. Затем плазмиду, содержащую рекомбинантную ДНК провируса, в которой вместо генов gag, pol и env находится нужный трансген, используют для трансдукции упаковывающих клеток. Теперь клетки содержат все, что нужно для сборки вирусов, и ретровирусные векторы начинают накапливаться в культуральной среде. Эти векторы содержат трансген, но лишены вирусных генов gag, pol и env, а потому при заражении следующей клетки они не могут репродуцироваться. Б. Экспрессия трансгена в клетке-мишени после внедрения РНК-содержащего ретровирусного вектора (см. «Жизненный цикл»).
Клетки-мишени. Способность вируса избирательно заражать определенные типы клеток в значительной степени определяется взаимодействием между белком внешней оболочки вируса (у ретровирусов кодируется геном env) и соответствующим мембранным рецептором клетки. Вирус лейкоза мышей Молони является экотропным, то есть заражает только клетки мышей. Для расширения круга клеток-мишеней используют ген env штамма 4070А вируса лейкоза мышей. Этот штамм является амфотропным и заражает клетки не только мышей, но и других млекопитающих, в том числе — человека. Псевдотипирование, то есть упаковка вирусного генома в оболочку, содержащую белки другого вируса, позволяет расширить круг клеток-мишеней. Например, гликопротеид вируса везикулярного стоматита, называемый G-белком (не путать с G-белками, участвующими во внутриклеточной передаче сигнала; гл. 2), легко включается в оболочку вируса лейкоза мышей Молони (Chen et al., 1996). Наличие этого белка расширяет круг клеток-мишеней и облегчает заражение. Кроме того, включение G-белка повышает стабильность ретровирусного вектора и позволяет при ультрацентрифугировании получить более высокий титр вирусов. Недостаток G-белка — его токсичность по отношению к упаковывающим клеткам. Этот недостаток можно частично преодолеть, используя упаковывающие клетки с индуцируемой экспрессией G-белка (lida et all 1996). Ретровирусные векторы, содержащие другие вирусные белки, например белки вируса лейкоза гиббонов (Gallardo et al., 1997) или вируса лимфоцитарного хориоменингита (Miletic et al., 1999), менее токсичны по отношению к клеткам млекопитающих.
Применение. С помощью ретровирусных векторов обычно осуществляют трансдукцию клеток больного ex vivo или векторы вводят непосредственно в ткани. Первый подход требует выделения клеток больного и поддержания их в культуре, заражения клеток ретровирусным вектором и последующего введения клеток больному. Так пытались модифицировать лимфоциты и стволовые кроветворные клетки при недостаточности аденозиндезаминазы (Parkman et al., 2000) и семейной гиперхолестеринемии (Grossman et al., 1994). Аналогичным образом поступали, чтобы вызвать экспрессию иммуномодуляторов в опухолевых клетках (Lode and Reisfeld, 2000). Прямую инъекцию ретровирусных векторов пробуют применять в основном для лечения солидных опухолей (Gomez-Navarro et al., 1999).
Безопасность. Поскольку вирус встраивается в клеточный геном (что важно для длительной экспрессии), причем случайным образом, существует риск возникновения мутации (инсер-ционный мутагенез). Например, встраивание вируса может изменить функцию гена, регулирующего деление клеток, что приведет к нежелательным последствиям. Способные к репродукции ретровирусы обладают некоторой канцерогенностью, однако этого не наблюдается у ретровирусных векторов, лишенных такой способности.
Лентивирусы[править | править код]
Вирусы, относящиеся к этому подсемейству ретровирусов, способны заражать как делящиеся, так и неделящиеся клетки (Buchschacher, Jr. and Wong-Staal,2000). Из лентивирусов лучше всего изучен ВИЧ-1, а векторы, полученные на его основе, теоретически обладают рядом преимуществ перед описанными ретровирусными векторами. Особенно многообещающей является их способность к высокоэффективной трансдукции стволовых кроветворных клеток (Miyoshi et al., 1999). Эти векторы также могут обеспечить длительную экспрессию трансгена. Однако в силу происхождения лентивирусных векторов перед проведением клинических испытаний необходимо убедиться в их безопасности (Amado and Chen, 1999).
Жизненный цикл. Лентивирусы сходны с другими ретровирусами (Tang et al., 1999). Основное отличие, объясняющее способность лентивирусов заражать неделящиеся клетки, состоит в том, что вирусный преинтеграционный комплекс взаимодействует с ядерной оболочкой, а затем транспортируется через нее. Этот преинтеграционный комплекс состоит из вирусного генома (в виде ДНК), интегразы и белка матрикса, кодируемого геном gag. Белок матрикса содержит последовательность, обеспечивающую связывание вируса с порой ядерной оболочки. Последующий перенос внутрь ядра делает возможным интеграцию вирусного генома в ДНК неделящейся клетки.
Конструкция и получение вектора. Лентивирусные векторы лишены способности к репродукции благодаря удалению из генома ВИЧ-1 некоторых дополнительных генов, поэтому для их получения используют упаковывающие клетки, в которых независимые гены кодируют необходимые для сборки вируса компоненты (Srinivasakumar and Schuening, 1999). Это существенно снижает риск рекомбинации при получении вектора, в результате которой теоретически возможно восстановление способности вируса к репродукции. Удаление гена tat и длинных концевых повторов (LTR) также снижает риск восстановления способности к репродукции при получении вектора или in vivo.
Клетки-мишени. Лентивирусные векторы способны заражать как делящиеся, так и неделящиеся клетки, например стволовые кроветворные клетки или специализированные клетки — мышечные, нейроны, гепатоциты, фоторецепторы сетчатки. Однако иногда для осуществления трансдукции необходимо заставить клетки перейти в период G( клеточного цикла (Park et al., 2000). С целью расширения круга клеток-мишеней лентивирусный белок, кодируемый геном env, можно заменить путем псевдотипирования на G-белок вируса везикулярного стоматита или на другой подходящий белок (Li et al., 1998). Длительную экспрессию трансгенов, доставленных с помощью лентивирусного вектора, наблюдали в ЦНС экспериментальных животных. Стабильная и эффективная доставка трансгенов осуществлена также в клетки сетчатки.
Применение лентивирусных векторов почти не вызывает воспаления или других признаков поражения тканей.
Безопасность. Поскольку лентивирусные векторы получают на основе генома ВИЧ-1, особенную озабоченность вызывает риск рекомбинации, восстанавливающей способность к репродукции (Amado and Chen, 1999). Репродуцирующийся лентивирусный вектор теоретически опасен тем, что он может вызвать инсерционный мутагенез или приобрести свойства исходного ВИЧ-1. Не ясно также, к чему приведет заражение ВИЧ человека, которого ранее лечили с помощью лентивирусного вектора. Теоретически ВИЧ-инфекция может вызвать мобилизацию встроенного вектора, поскольку ВИЧ способен выступить в роли вируса-помощника. Кстати, это может быть использовано для генотерапии ВИЧ-инфекции с помощью лентивирусных векторов. Сомнения в безопасности должны быть устранены в ходе усовершенствования конструкции векторов и методов их получения.
Аденовирусы[править | править код]
Аденовирусы содержат линейную двухцепочечную ДНК и способны к репродукции независимо отделения клетки-хозяина. Аденовирусные векторы имеют ряд преимуществ, что стимулирует разработку их клинического применения. Они позволяют доставлять гены в различные ткани человека, в том числе в эпителий дыхательных путей, эндотелий, миокард и скелетные мышцы, клетки периферической и центральной нервной системы, гепатоциты, экзокринные клетки поджелудочной железы и различные типы опухолей. Известно более 40 серотипов аденовирусов человека, а вызываемые ими заболевания подробно описаны (Horwitz, 1990). Почти все взрослые люди перенесли аденовирусную инфекцию, и в их крови имеются антитела против аденовирусов.
Аденовирусные векторы обеспечивают эффективную трансдукцию как делящихся, так и неделящихся клеток с последующей экспрессией трансгенов. Можно использовать разные пути введения, например в/в, внутрибрюшинный, внутрипузырный, внутричерепной, интратекальный, а также инъекцию в желчные пути или непосредственно в паренхиму органа. Многообразие путей введения позволяет выбрать наилучший для выбранной мишени. Аденовирусные векторы имеют два существенных недостатка. Во-первых, после заражения клетки вирусный геном не встраивается в ДНК клетки, поэтому длительной экспрессии трансгена не происходит. Во-вторых, аденовирусная инфекция активирует как клеточное, так и гуморальное звенья иммунитета, что ведет к уничтожению трансфицированных клеток и снижает эффективность повторного введения вектора. Побочные эффекты аденовирусных векторов также объясняются иммунным ответом.
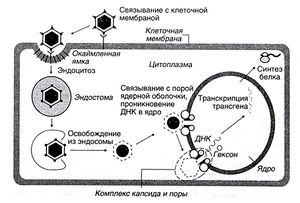
Жизненный цикл. Аденовирусная инфекция начинается со связывания нитей, выступающих на вершинах икосаэдрического капсида, с рецептором вирусов Коксаки и аденовирусов, расположенным на мембране клетки (рис. 5.2). Затем происходит взаимодействие последовательности из трех аминокислотных остатков (Apr— Гли—Асн), расположенной в основании вирусного пентона, с клеточными интегринами (avβ3- или аvβ5-интегрином), что приводит к эндоцитозу и интернализации вируса. Вирус покидает эндосому до ее слияния с лизосомой и таким образом избегает переваривания. Вирусная ДНК проникает в ядро клетки, где начинается синтез вирусных мРНК, причем деления клетки для этого не требуется. В делящихся клетках при высоком уровне заражения иногда происходит встраивание вирусного генома в ДНК клетки, однако это достаточно редкое событие, существенно не влияющее на применимость аденовирусных векторов. Экспрессия и репликация вирусного генома проходят в определенной последовательности, которую во многом определяют гены Е1А и E1B, расположенные в 5'-области аденовирусного генома. Эти гены обеспечивают трансактивацию нескольких вирусных генов, расположенных дальше в З'-направлении (Horwitz, 1990).
Поскольку гены Е1 участвуют в репродукции аденовирусов, их удаление блокирует или, по крайней мере, существенно затрудняет репродукцию. Из-за более сложного строения вируса удалить из вектора все аденовирусные гены труднее, чем ретровирусные. Синтез аденовирусных белков после заражения клеток существующими аденовирусными векторами активирует клеточное и гуморальное звенья иммунитета. В некоторых случаях это может ограничивать использование вектора вследствие гибели трансфицированных клеток и низкой эффективности повторного введения вектора.
Описание к рисунок 5.2. Использование аденовирусного вектора. Рекомбинантный аденовирус связывается со специфическими рецепторами на поверхности клетки-мишени и проникает в нее путем эндоцитоза. Вирусные белки обеспечивают выход вируса из эндосомы до ее слияния с лизосомой; благодаря этому вирус избегает разрушения. Аденовирусная ДНК освобождается от белков и проникает в ядро, где начинается синтез новых мРНК. При этом аденовирусная ДНК, содержащая трансген, не встраивается в геном клетки-хозяина.
Конструкция и получение вектора. Из множества известных серотипов аденовирусов для получения векторов используют в основном серотипы 2 и 5. Аденовирусные векторы первого поколения были получены путем удаления Е1- и E3-районов из вирусного генома. После этих делеций вирус не способен к репродукции, а в геном можно включить до 7500 пар нуклеотидов чужеродной ДНК. В аденовирусных векторах второго поколения удалены также Е2- и E4-районы, что способствует снижению иммуногенности, но снижает экспрессию трансгенов в зараженных клетках. В результате удаления еще большего числа вирусных генов получены аденовирусные векторы, зависящие от вирусов-помощников (Kochanek, 1999). В их состав можно включить больше чужеродной ДНК, и при их применении снижен риск иммунного ответа, однако такие векторы трудно сконцентрировать, и они менее стабильны in vivo.
Аденовирусные векторы в большом количестве получают путем заражения упаковывающих клеток (обычно эмбриональных клеток почки человека, линии 293), экспрессирующих вирусный белок Е1, что компенсирует отсутствие соответствующего гена в рекомбинантном вирусе. Затем зараженные клетки лизируют, а лизат подвергают центрифугированию в градиенте плотности хлорида цезия. Этот метод позволяет не только очистить вирусы от других компонентов клеточной культуры, но и сконцентрировать его, получив более 10^13 вирусов в 1 мл. Очищенный вирус очень устойчив в различных буферных растворах, а для длительного хранения может быть заморожен без потери активности.
Клетки-мишени. Аденовирусы заражают широкий круг делящихся и неделящихся клеток, поскольку рецепторы для вирусов Коксаки и аденовирусов имеются почти у всех клеток. Лишь у некоторых клеток этих рецепторов мало или они недоступны. Существуют способы изменения тропности аденовирусов (Wickham, 2000). Использование антител двойной специфичности к нитям вируса и мембранным белкам клетки позволяет блокировать естественную тропность вируса и перенаправить его на определенный тип клеток. Для изменения тропности или облегчения взаимодействия с клетками можно с помощью методов генной инженерии модифицировать вирусные нити или их концевые головки (Douglas et al., 1999). Наконец, можно использовать адаптерные белки, например химерный белок, содержащий последовательности эпидермального фактора роста и рецептора вирусов Коксаки и аденовирусов. Это облегчает связывание вируса с клетками, экспрессирующими рецептор эпидермального фактора роста (Dmitriev et al., 2000).
Применение. В настоящее время проводится много клинических испытаний, в которых аденовирусные векторы применяют для лечения как наследственных, так и приобретенных заболеваний. При лечении наследственных заболеваний большим недостатком является непродолжительность экспрессии трансгенов и иммунный ответ на зараженные клетки. Внехромосомная локализация аденовирусного генома в клетке ограничивает продолжительность экспрессии трансгенов в активно делящихся клетках (например, клетках костного мозга или эпителия), так как деление клеток не сопровождается репликацией трансгена. Аденовирусные векторы, как способные, так и не способные к репродукции, могут найти применение в лечении злокачественных новообразований (см. ниже).
Безопасность. Основное побочное действие аденовирусных векторов — иммунный ответ, направленный против зараженных клеток. Обсуждение безопасности аденовирусных векторов особенно стимулировала смерть одного больного во время клинических испытаний (Marshall, 1999). Имеются также сомнения, что в процессе получения вектора полностью исключено образование рекомбинантного вектора, способного к репродукции. Аденовирусные векторы, предназначенные для клинического использования, нуждаются в тщательной проверке. Аденоассоциированные вирусы. Эти маленькие, лишенные оболочки вирусы, содержащие одноцепочечную ДНК, обладают рядом свойств, необходимых хорошему вектору. Они непатогенны, обеспечивают эффективную и стабильную трансдукцию неделящихся клеток, а кроме того, позволяют исключить экспрессию вирусных белков в зараженных клетках. Основные недостатки аденоассо-циированных векторов — маленькая емкость и трудности в концентрировании. Начались клинические испытания аденоассоциированных векторов, и есть основания рассчитывать на их пригодность для генотерапии (Monahan and Samulski, 2000).
Жизненный цикл. Для репродукции аденоассоциированные вирусы нуждаются в генетической информации вируса-помощника. В жизненном цикле аденоассоциированных вирусов выделяют две фазы. Такой вирус заражает клетку, включается в клеточный геном и в отсутствие вируса-помощника (аденовируса) остается там продолжительное время в латентном состоянии. В присутствии аденовирусов начинается активная фаза, приводящая к репродукции аденоассоциированного вируса и лизису клеток. Геном аденоассоциированного вируса содержит две открытые рамки считывания (гер и cap), ограниченные инвертированными концевыми повторами (ITR). Для репродукции вируса нужны только гены гер, кодирующие четыре белка, которые обеспечивают репродукцию аденоассоциированного вируса, транскрипцию вирусной ДНК и эндонуклеазную активность, необходимую для встраивания в клеточный геном. Структурные белки, образующие капсид вируса, кодируются геном cap. В районе инвертированных концевых повторов находятся точки начала репликации; эти повторы содержат сигналы для сборки вирусов, а также участвуют во встраивании вирусной ДНК в клеточный геном. Функция многих белков и другие особенности биологии вируса стали известны после изучения природных немодифицированных вирусов (Kotin, 1994).
Заражение начинается с прикрепления вируса к его основному рецептору на клетке — протеогликану, содержащему гепарансульфат (Summerford and Samulski, 1998). В проникновении вируса в клетку участвуют также рецептор фактора роста фибробластов и сц,Р5-интегрин (Summerford et al., 1999). Интернализация вируса осуществляется путем эндоцитоза через образование покрытых клатрином окаймленных ямок (Bartlett et al., 2000а). Внутри клетки геном аденоассоциированного вируса замыкается в кольцо и образует кольцевые конкатемеры, находящиеся вне хромосом (Yang et al., 1999). Образование этих кольцевых форм вирусного генома сопровождается длительной экспрессией трансгена (Duan et al., 1998). Природный аденоассоциированный вирус может встраиваться в ДНК человека на одном участке 19-й хромосомы (19q 13.3—qter). Рекомбинантный вирус иногда утрачивает эту способность (Rivadeneira et al., 1998). Конструкция и получение вектора. Существующие аденоассоциированные векторы получают с помощью системы трех рекомбинантных плазмид (Xiao et al., 1998). Первая плазмида содержит трансген, расположенный между двумя инвертированными концевыми повторами, вторая — гены гер и cap, а третья — участки генома аденовируса, необходимые для сборки аденоассоциированного вируса. Этот подход позволяет обойтись без дополнительного заражения продуцирующих клеток аденовирусом. Из-за небольшого размера генома аденоассоциированных вирусов в вектор можно включить не более 5200 пар нуклеотидов чужеродной ДНК. Это не только ограничивает размер потенциального трансгена, но и затрудняет использование специальных промоторов и энхансеров, регулирующих его экспрессию в зараженной клетке. При использовании двухвекторной системы можно вдвое увеличить емкость вектора: две половины трансгена соединяются in vivo из двух разных векторов, которые объединяются в кольцевой конкатемер внутри клетки (Sun et al., 2000; Yan et al., 2000). Таким же образом можно собирать большие гены или включать важные регуляторные элементы, слишком большие для одного вектора (Duan et al., 2000). В настоящее время основные проблемы в использовании аденоассоциированных векторов связаны с трудностями получения высокой концентрации вектора и определения его титра. Клетки-мишени. Аденоассоциированные векторы способны заражать различные клетки. В доклинических исследованиях показана эффективная трансдукция клеток скелетных мышц, ЦНС, легких, печени, ЖКТ и глаза.
Применение. Аденоассоциированные векторы начали применять в клинике: сейчас проводятся клинические испытания доставки генов в легкие и в скелетные мышцы. По-видимому, эти векторы подходят для обеспечения длительной экспрессии трансгенов в скелетных мышцах, сердце, ЦНС и других тканях. Первые результаты клинического испытания, в котором с помощью аденоассоциированного вектора осуществляли доставку гена фактора IX в скелетные мышцы больных гемофилией, оказались успешными (см. ниже). Способность этих векторов обеспечивать длительную экспрессию трансгенов, не оказывая токсического действия на клетки и не вызывая иммунного ответа, делает их перспективным инструментом лечения некоторых наследственных заболеваний.
Безопасность. Аденоассоциированные вирусы непатогенны. Первые опыты с использованием соответствующих векторов показали, что они не активируют иммунную систему. Раньше высказывались опасения, что аденоассоциированный вектор может быть загрязнен вирусом-помощником (аденовирусом), но этот риск ликвидировали новые схемы получения векторов (Xiao et al., 1998). Наконец, аденоассоциированные векторы могут встраиваться в геном клетки случайным образом, что теоретически может привести к инсерционному мутагенезу. Вероятно, необходимо сохранить в векторах способность специфического встраивания в 19-ю хромосому (Rivadeneira etal., 1998).
Вирус простого герпеса типа 1[править | править код]
Этот вирус содержит большую (152 000 пар нуклеотидов) молекулу двухцепочечной ДНК, которая реплицируется в ядре зараженной клетки. Вирус заражает различные клетки, как делящиеся, так и неделящиеся; вирусный геном находится вне хромосом. В вирусный геном путем гомологичной рекомбинации или путем делеции и вставки можно встроить до 20 000—30 000 пар нуклеотидов чужеродной ДНК. Вирус простого герпеса типа 1 обладает тропностью к нейронам, поэтому его предложено использовать в качестве вектора для генотерапии нервных болезней, например болезни Паркинсона или злокачественных новообразований мозга (Fink and Glorioso, 1997; Simonato et al.,2000). Основные недостатки такого вектора — цитотоксичность и возможность замолкания трансгена.
Жизненный цикл. Инфекция, вызванная вирусом простого герпеса типа 1, может быть активной, приводящей к лизису клеток, или латентной. При первичном заражении вирус проникает в клетки эпителия (кожи или слизистых), где репродуцируется. Новые вирусы, покидая зараженную клетку путем отпочковывания, получают внешнюю оболочку, состоящую из остатков клеточной мембраны. Затем вирусы внедряются в чувствительные нервы вблизи от очага первичной инфекции и ретроградно транспортируются по волокну в тело нейрона. В прикреплении вируса участвуют молекулы гепарансульфата, расположенные на поверхности клеточной мембраны (Laquerre et al., 1998). Попав в тело нейрона, вирус может продолжить активную репродукцию или перейти в латентное состояние. В последнем случае подавляется экспрессия большинства вирусных генов, но два промотора (LAPI, LAP2) активируют синтез транскриптов, связанных с латентностью (LAT-транскриптов). Позже вирус может реактивироваться, начать активную репродукцию и распространиться на очаг первичной инфекции или ЦНС.
Конструкция и получение вектора. Герпесвирусный вектор не способен к репликации, поскольку у него нет нескольких необходимых для этого генов, таких, как сверхранние гены ICP4, 1СР22и ICP27(Krisky et al., 1998). Удаление этих генов уменьшает также цитотоксичность вектора и увеличивает продолжительность экспрессии трансгена. Были разработаны методы, позволяющие без использования вирусов-помощников получить герпесвирусные векторы, хотя и с невысоким титром. Такие векторы способны заражать нервные клетки in vivo, не повреждая их (Fraefel et al., 1996). Наиболее эффективные способы получения вектора на основе вируса простого герпеса типа 1 позволяют включить в него два независимых трансгена (Krisky et al., 1997).
Большим препятствием к использованию герпесвирусных векторов является кратковременность экспрессии, вызванная замолканием трансгена. Перспективный способ преодоления этой проблемы — использование промоторов, активирующих синтез LAT-транскриптов (Goins et al., 1999; Lachmann and Efstathiou, 1997; Marshall et al., 2000). Иногда для облегчения трансляции трансген сшивают с внутренним сайтом связывания рибосом (IRES) вируса энцефаломиокардита.
Клетки-мишени. Вирус простого герпеса типа 1 способен заражать различные клетки человека, но особенно выражена его тропность к нейронам. Для повышения специфичности удаляют вирусные гены, кодирующие гликопротеид (обеспечивает прикрепление к клетке); их можно заменить на другие аналогичные гены (Anderson et al., 2000).
Применение. Емкость герпесвирусных векторов очень велика. Например, с их помощью в культуру мышечных клеток, полученных от мышей с экспериментальной мышечной дистрофией, была введена полная кДНК дистрофина из 14 000 пар нуклеотидов (Akkaraju et al., 1999). Способные к репродукции герпесвирусные векторы сейчас разрабатываются для лечения злокачественных новообразований мозга и других органов (Martuza, 2000). Безопасность. Основная опасность герпесвирусных векторов — цитотоксичность. Новейшие способы получения векторов, включающие удаление дополнительных вирусных генов, снижают этот риск.