Невирусная доставка генов (генотерапия)
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Невирусная доставка генов[править | править код]
Разработаны и опробованы невирусные способы доставки чужеродной ДНК в клетки: плазмиды, ДНК-липосомные комплексы, ДНК-белковые комплексы и частицы золота, покрытые ДНК. Их получить проще и дешевле, чем вирусные векторы. Однако низкая эффективность и кратковременная экспрессия трансгена существенно ограничивают пригодность невирусных методов доставки ДНК для генотерапии. Более длительная экспрессия может быть получена с помощью транспозонов — естественных подвижных генетических элементов, способных встраиваться в хромосомную ДНК (Yant et al., 2000).
Плазмиды[править | править код]
Как ни странно, очищенная ДНК (или мРНК), введенная непосредственно в ткани, вызывает преходящую экспрессию трансгенов. Это было показано на мышечной ткани, для которой такое прямое введение наиболее эффективно (Wolff et al., 1992). Клетки кожи также способны экспрессировать плазмидные гены после введения ДНК в ткань непосредственно (Hengge et al., 1996) или с помощью баллистической трансфекции — обстрела ткани, например, частицами золота, покрытыми плазмидной ДНК (Lin et al., 2000). Экспрессия чужеродного белка в коже или мышцах после такой процедуры вызывает иммунный ответ, что можно использовать для вакцинации (Davis et al.. 1995). Клинические испытания должны проверить эффективность и безопасность этого способа вакцинации против инфекционных болезней (Le et al., 2000; Tacket et al., 1999). Кроме того, введение чужеродной ДНК в мышцы позволяет вызвать эктопический синтез необходимого больному белка, например эритропоэтина (Tripathy et al., 1996).
Частицы золота, покрытые ДНК[править | править код]
Частицы золота (диаметром приблизительно 1 мкм) с нанесенной плазмидной ДНК можно «выстрелить» в подходящую клетку с помощью электрической искры или сжатого газа. Такую генную пушку используют для введения трансгенов в клетки поверхностного слоя кожи (эпидермиса) или опухолей кожи (меланомы). Экспрессия трансгенов продолжается всего несколько дней, что в большей степени связано со свойствами клеток-мишеней (например, слушиванием клеток эпидермиса), чем со способом доставки генов. Использование генной пушки хорошо подходит для вакцинации (Haynes et al., 1996), где кратковременной экспрессии антигена достаточно для стимуляции иммунной системы.
Липосомы[править | править код]
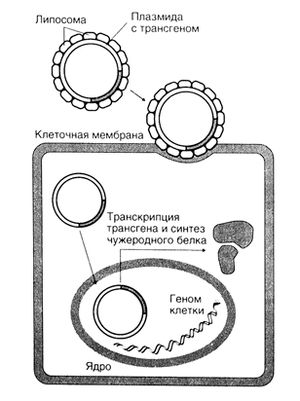
Это однослойные или многослойные мембранные везикулы, полученные из липидов и способные переносить ДНК внутрь клеток. Суть в том, что, окружив гидрофильные молекулы гидрофобными, можно облегчить проникновение первых через мембрану клетки. Схема трансфекции клеток с помощью липосом показана на рис. 5.3. Белки и другие молекулы можно включить в липидные мембраны. Поскольку молекулы, которые следует доставить в клетку, должны быть заключены внутри липосом, процесс получения таких липосом достаточно сложен. Кроме того, большинство молекул ДНК, используемых в генотерапии, по размерам больше липосом, что тоже затрудняет процесс. Липосомы принято делить на анионные (заряженные отрицательно) и катионные (заряженные положительно).
Описание к рисунок 5.3. Доставка ДНК с помощью катионных липосом. Липосомы сливаются с клеточной мембраной таким образом, что ДНК проникает в клетку, избегая разрушения лизосомами. Плазмидная ДНК (показанная здесь) проникает в ядро, где синтезируется мРНК, которая, в свою очередь, переносится обратно в цитоплазму и служит матрицей для синтеза белка. Встраивание ДНК в геном клетки-хозяина происходит очень редко.
Анионные липосомы[править | править код]
Первая трансфекция in vivoc помощью липосом была осуществлена при использовании анионных липосом, в которые включали ген инсулина (Soriano et al., 1983). В крови крыс после трансфекции повышалась концентрация инсулина, а концентрация глюкозы снижалась. Несмотря на этот успех, у метола имеются существенные недостатки. После в/в введения липосомы захватываются в основном купферовскими клетками печени и не попадают к другим клеткам. В наружный слой липосом можно включить различные белки с целью изменить судьбу липосом в организме, в частности направленность доставки. Так удается уменьшить долю липосом, захватываемых клетками ретикулоэндотелиальной системы. Включение в наружный слой липосом белковых лигандов или антител к поверхностным молекулам клетки также способствует избирательному связыванию с мембранными рецепторами клеток определенного типа (Wu and Wu, 1987).
Катионные липосомы[править | править код]
Судьба катионных и анионных липосом in vivo различна. Для многих органов показано, что введение катионного ДНК-липосомного комплекса в приносящий кровоток приводит к экспрессии трансгена в этих органах. Кроме того, для трансфекции клеток легочного эпителия ДНК-липосомные комплексы можно вводить как в/в, так и в виде аэрозоля. В опытах на животных оба эти пути введения были безопасны (Canonico et al., 1994).
ДНК-белковые комплексы[править | править код]
Разработаны методы адресной доставки генов, использующие специфические рецепторы на клетках-мишенях (Michael and Curiel, 1994). Если молекулу чужеродной ДН К связать с лигандом рецептора, то такой комплекс будет избирательно взаимодействовать с рецепторами и подвергаться интернализации в клетку-мишень (Wu and Wu, 1987). ДНК-белковые комплексы привлекают внимание, поскольку теоретически могут обеспечить избирательность доставки трансгена без сопутствующих проблем, присущих вирусным векторам. Сначала были разработаны способы связывания ДНК с лигандом на основе поликатионов, комплексов антиген-антитело или биотин—стрептавидин. Широко применяется поли-L-лизин — поликатион, который можно легко присоединить к различным белковым лигандам. При смешивании конъюгата поли-Ь-лизин—лиганд с ДНК образуются макромолекулярные комплексы, в которых ДНК электростатически связывается с поли-L-лизином. Эти макромолекулярные комплексы представляют собой тороидальные структуры диаметром 50—100 нм; они избирательно связываются с мембранными рецепторами клетки и поглощаются путем эндоцитоза. В экспериментах по трансфекции использовали рецепторы трансферрина (Zenke et al., 1990) и асиалоорозомукоида (Wu and Wu, 1987), а также поверхностные полисахариды (Batra et al.,1994). Особое внимание привлекли рецепторы асиалоорозомукоида: они обнаружены исключительно на гепатоцитах и поэтому могут быть использованы для избирательной доставки генов в печень.