Дыхательная функция
Содержание
Функции легких. Дыхание[править | править код]
Основная функция легких - дыхание, но они также выполняют метаболические функции, например там ангиотензин I превращается в ангиотензин II. Кроме того, легочный круг кровообращения служит буферной емкостью для сохранения в организме постоянного объема крови, там отфильтровываются небольшие сгустки крови из венозного кровообращения, до того как они попадут в артерии, тем самым препятствуя тромбоэмболии (в сердце, мозге).
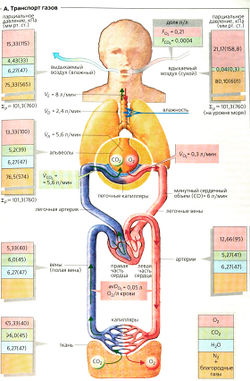
Внешнее дыхание обеспечивает обмен газов между телом и внешней средой. (При внутреннем, или тканевом, дыхании происходит окисление питательных веществ) Конвекция (массовый поток) - это способ транспортировки газов на большие дистанции вместе с потоком воздуха или крови. Оба этих потока обусловлены разностью давлений. Диффузия используется для транспорта газов на короткие расстояния (несколько мкм), например, через клеточные мембраны и другие физиологические барьеры. Газообмен между атмосферой и альвеолами называется вентиляцией легких. При вдохе (воздуха) кислород (O2) попадает в альвеолы за счет конвекции и, проходя сквозь альвеолярную мембрану, диффундирует в кровоток. Затем кислород переносится кровотоком в ткани, где диффундирует из крови к клеткам и, в конечном счете, попадает в митохондрии. Углекислый газ (СO2), образующийся в митохондриях, возвращается в легкие.
Общая легочная вентиляция в единицу времени, VT (минутный объем) - это объем воздуха (V), вдыхаемый или выдыхаемый в единицу времени. Поскольку обычно измеряется объем выдыхаемых газов, используется обозначение VE[от англ, expiratory — выдыхаемый). Для организма человека в покое VE~ 8 л/мин при уровне потребления кислорода (VO2) 0,3 л/мин и уровне удаления углекислого газа (VCO2) 0,25 л/мин. Таким образом, нужно через легкие прокачать (вдох-выдох) примерно 26 л воздуха, чтобы обеспечить 1 л O2. Экскурсирующий объем VT- это объем воздуха, входящий и выходящий из легких за время одного дыхательного цикла. VE равно произведению VT- (примерно 0,5 л в покое) на частоту дыхания f (в покое примерно 16 циклов/мин), только примерно 5,6 л/мин (при f = 16 мин-1) из VE = 8 л/мин достигает альвеол - это альвеолярная вентиляция (VA). Остальной воздух в воздушных путях не дает вклада в газообмен (вентиляция мертвого объема, Vp).
У человека примерно 300 миллионов альвеол (тонкостенных воздушных пузырьков диаметром примерно 0,3 мм), расположенных на концах бронхиол. Альвеолы окружены плотной сетью легочных капилляров и имеют общую площадь своей поверхности примерно 100 м2. По этой причине, а также потому что диффузия из воздуха в кровь происходит здесь на очень близкие расстояния (лишь несколько мкм), даже при 10-кратном увеличении потребности организма в кислороде через альвеолярные стенки в кровь может диффундировать достаточное количество O2, а из крови в альвеолярное пространство - СO2.
В легочной артерии имеющая дефицит кислорода венозная кровь насыщается кислородом (становится артериальной) и выталкивается левым желудочком в большой круг кровообращения.
Минутный объем сердца (= минутный сердечный выброс) (СО)- это объем крови, прокачиваемый через большой и малый круги кровообращения в единицу времени (5-6 л/мин в покое). СО, умноженный на артериально-венозную разницу O2 (аvDO2), т. е. разность между содержанием O2 в артериальной крови в аорте и смешанной венозной крови в правом предсердии (примерно 0,05 л O2 на 1 л крови) дает объем O2 транспортируемого в единицу времени из легких к периферии. В покое 6 * 0,05 = 0,3 л/мин -величина, соответствующая VO2 (см. выше). И наоборот, если измерить величины и аvDO2, то можно рассчитать СО по принципу Фика:
СО = VO2 /avDO2. [5.1]
Ударный объем (УО) получают делением СО на сердечный ритм (частоту пульса).
В соответствии с законом Дальтона, общее давление (Ptotal) смеси газов равно сумме парциальных давлений (P) отдельных газов. Если объемную долю газа (F, в л/л) умножить на Ptotal, то получим парциальное давление; для O2, например, род = FO2 хPtotal Для сухого воздуха на уровне моря [Ptotal = 101,3 кПа = 760 мм рт. ст.) можно рассчитать парциальные давления газов, зная их содержание: FO2 = 0,209, FcO2 = 0,0004, FNa + благородные газы = 0,79 (А, вверху справа).
Если смесь газов «влажная», то парциальное давление водыPH2O нужно вычесть из Ptotal (обычно Ptotal равно атмосферному давлению). Парциальные давления других газов при этом также будут ниже, поскольку Рх = Fy (Ptotal- РH2O). Проходя через дыхательные пути (37 °С), вдыхаемый воздух насыщается влагой. В результате, РH2O возрастает до 6,27 кПа (47 мм рт. ст.), a падает на 1,32 кПа ниже, чем в сухом атмосферном воздухе. Парциальное давление во вдыхаемом воздухе, в артериолах, артериях, венах (смешанная венозная кровь), тканях и выдыхаемом воздухе указано на рис. А.
Механизм дыхания[править | править код]
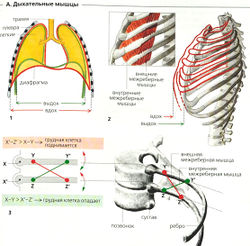
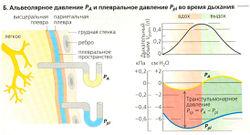
Разность в давлении между альвеолами и окружающей средой является движущей силой газообмена, осуществляемого при вентиляции. Альвеолярное давление (PA - внутрилегочное давление) должно быть ниже, чем атмосферное (барометрическое) давление (PB) во время вдоха и выше во время выдоха. Если атмосферное давление РB взять за точку отсчета (нулевая линия), то альвеолярное давление отрицательно во время вдоха и положительно во время выдоха (Б). Эти разности давления создаются с помощью согласованных движений диафрагмы и грудной клетки (торакс), что приводит к увеличению объема легких (Vpulm) во время вдоха и уменьшению - во время выдоха (А1, 2).
Дыхательная мускулатура состоит из диафрагмы, косых мышц живота и наружных межреберных мышц. Их сокращения опускают (уплощают) диафрагму и поднимают и расширяют грудную клетку, тем самым расширяя легкие. Вдох, таким образом, представляет собой активный процесс. При глубоком дыхании вовлекаются наружные межреберные мышцы и вспомогательные дыхательные мышцы. Во время выдоха диафрагма и другие участвующие во вдохе мышцы расслабляются, поднимая диафрагму и уменьшая объем грудной клетки и легких. Поскольку этот обратный процесс происходит в основном благодаря эластичности легких, выдох в покое является пассивным. При более глубоком дыхании в выдохе могут участвовать также активные механизмы: внутренние межреберные мышцы сокращаются, и диафрагма толкается вверх брюшным давлением, создаваемым мышцами брюшной стенки.
Два близлежащих ребра связаны внутренней и внешней межреберными мышцами. Разнонаправленное сокращение мышц передает на верхнее и нижнее ребра разную силу (АЗ). Расстояние между местом крепления внешней межреберной мышцы к верхнему ребру (Y) и осью вращения верхнего ребра (X) меньше, чем расстояние от места крепления мышцы к нижнему ребру (Z1) и осью вращения нижнего ребра (X1). Таким образом, X'-Z' является более длинным и более мощным рычагом, чем X-Y. Грудная клетка поднимается, когда сокращаются наружные межреберные мышцы, и опускается, когда сокращаются противоположные внутренние межреберные мышцы.
Чтобы использовать движение диафрагмы и грудной клетки для вентиляции, легкие должны иметь возможность следовать этому движению и не быть прикрепленными к диафрагме и груди. Это достигается при помощи плевры - тонкого слоя покрытых 114 жидкостью клеток, которые выстилают каждое легкое [висцеральная плевра), отделяя от близлежащих органов, которые также покрыты плеврой (париетальная, пристеночная плевра).
В нормальном состоянии легкие сжимаются благодаря своей собственной эластичности и под действием сил альвеолярного поверхностного натяжения. Поскольку плевральное пространство не может расширяться, а легкие прикреплены к внутренней поверхности грудной клетки, в результате возникает подсасывание (которое тем не менее не препятствует движению двух плевральных листов по касательной друг к другу). Плевральное давление Ppl. таким образом, отрицательно относительно атмосферного давления. Рpl, также называемое внутриплевральным, или интраторакальным, давлением, можно измерить во время дыхания (динамически) с использованием пищеводного зонда (=Ppl). Интенсивность подсасывания (отрицательное давление) увеличивается, когда грудная клетка расширяется во время вдоха, и уменьшается во время выдоха (Б). Ppl обычно не бывает положительным, за исключением очень сильного выдоха с использованием специальных мышц.
Трансмуральное давление (Ptm) дыхательной системы (разница между внутренним и наружным давлением) вычисляется с использованием РA, Ррl (Б) и барометрического давления (в окружающей среде) (Ра7м, см. выше):
- Ptm: легкие Ра - Рpl = транспульмонарное давление (Б, внизу справа);
- Ptm: грудная клетка + диафрагма Ррl- 0 = Ррl = транстораксикальное давление;
- Рtm: легкие + грудная клетка: Ра - 0 = Ра = трансмуральное давление всей дыхательной системы.
Характеристика дыхательной активности[править | править код]
Термины гиперпноэ и гипопноэ используются для описания ненормального увеличения или уменьшения глубины и скорости дыхательных движений. Тахипноэ (учащенное дыхание) и брадипноэ (слишком медленное дыхание), а также апноэ (асфиксия, удушье) описывают ненормальные изменения в скорости дыхания. Термины гипервентиляция и гиповентиляция подразумевают, что объем выдыхаемого СO2 больше или меньше соответственно, чем уровень продукции СO2, и артериальное парциальное давление СO2 (РaСO2) соответственно снижается или повышается . Диспноэ - термин, описывающий тяжелое или затрудненное дыхание (одышку), тогда как ортопноэ-это состояние, при котором дыхание затруднено в любом положении тела, кроме вертикального.
Очистка вдыхаемого воздуха Вдыхаемые чужеродные частицы захватываются слизью носа, горла, трахеи и бронхов. Захваченные частицы поглощаются макрофагами и возвращаются ресничным эпителием бронхов назад в трахею. Действует цилиарный эскалатор: реснички двигаются со скоростью 5-10 с-1 и проталкивают слизь в ротовую полость со скоростью 1 см/мин на пленку жидкого секрета эпителия. Интенсивное курение, муковисцидоз, генетические дефекты вязкости слизи могут ухудшать ресничный транспорт. Каждый день вырабатывается 10-100 мл слизи, в зависимости от типа и частоты локального раздражения (например, при курении) и стимуляции блуждающего нерва. Слизь обычно проглатывается, и жидкая фракция переваривается в желудочно-кишечном тракте.
Поверхностное натяжение. Сурфактант[править | править код]
Поверхностное натяжение - это основной фактор, определяющий эластичность системы грудная клетка-легкиеи площадь поверхности газ-жидкость, а для легких этот параметр напрямую влияет на осуществление газообмена на поверхности альвеол (примерно 100 м2).
Эффективность этих поверхностных сил можно продемонстрировать при помощи наполнения изолированного, полностью «опавшего» (претерпевшего коллапс) легкого (а) воздухом или (б) жидкостью. В примере (а) легкое проявляет гораздо большее сопротивление, особенно в начале наполнения. Это отражается на начальном давлении, которое при достижении полной емкости легких повышает альвеолярное давление (РA) примерно до 2 кПа, или 15 мм рт. ст.. В примере (б) сопротивление и, таким образом, Ра только на V4 больше. В соответствии с этим в примере (а) для преодоления поверхностного натяжения необходимо более высокое давление.
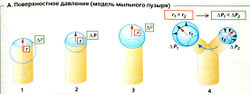
Если газовый пузырек радиуса r находится в жидкости, поверхностное натяжение у (Н * м-1) на границе раздела создает внутри пузыря давление более высокое, чем внешнее давление (пристеночное давление ΔР > 0). По закону Лапласа:
ΔР= 2у/r(Па). [5.3]
Поскольку, как правило, для плазмы у = 10~3 Н • м~1 (постоянная величина), ΔР растет с уменьшением r.
Модель мыльного пузыря. Если мыльный пузырь в виде пленки на горлышке цилиндра имеет достаточно большой радиус r (А1), то возникает небольшое ΔР. (Здесь две поверхности раздела воздух-жидкость, поэтому ΔР = 4у/r.) Чтобы увеличить объем пузырька, надо уменьшить r и увеличить АР 1К2). Поэтому требуется сравнительно высокое «начальное давление». Когда далее пузырек растет, г вновь увеличивается (АЗ) и отношение прирост давления/увеличение объема уменьшается. Альвеолы работают похожим образом. Эта модель демонстрирует, что в случае двух альвеол, соединенных друг с другом (А4), меньшая альвеола (ΔР2 высокое) становится еще меньше, а большая (ΔР1 низкое) - еще больше, чтобы выравнять давление с первой.
Сурфактант (поверхностно-активное вещество, ПАВ), выстилающий внутреннюю поверхность альвеол, предотвращает эту проблему: в меньшей альвеоле у понижается, а в большей альвеоле нет. (Концентрация ПАВ на меньшей поверхности больше.) Сурфактант - смесь белков и фосфолипидов (главным образом, дипальмитоил-лецитина) - секретируется альвеолярными клетками II типа.
Респираторный дистресс-синдром новорожденных-серьезное нарушение газообмена - вызывается тем, что недоразвитое легкое отказывается продуцировать достаточное количество сурфактанта. Легочное повреждение, связанное с токсичностью O2, частично происходит также из-за кислородного разрушения сурфактанта, что ведет к уменьшению эластичности легких. Это необратимо приводит к альвеолярному коллапсу (ателектазу) и отеку легких. Тестирование динамических функций легких
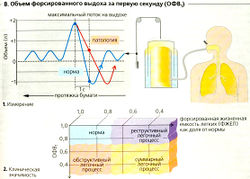
Максимальная вентиляция легких (МВЛ) - это самый большой объем газа, который можно вдохнуть (за 10 с) путем волевого увеличения экскурсирующего объема и частоты дыхания (Б). У здорового человека МВЛ может достигать 70-120 л/мин. Эта величина может быть полезна для обнаружения болезней, воздействующих на дыхательные мышцы, например злокачественной миастении.
Объем форсированного выдоха (ОФВ или тест Тиффно) - это максимальный объем газа, который может быть вытеснен из легких. В клинической медицине обычно измеряется ОФВ за первую секунду (0ФВ1). Отношение ОФВ к форсированной жизненной емкости легких (ФЖЕЛ) называется объемом форсированного выдоха ОФВ1 (обычно 0ФВ1 > 0,7). (ФЖЕЛ - это максимальный объем газа при быстром форсированном выдохе из положения полного вдоха; В.) Обычно это значение немного ниже, чем жизненная емкость ЖЕЛ (с. 118). Максимальная скорость при выдохе при измерениях на пневмотрахографе ФЖЕЛ составляет около 10 л/с.
Тестирование динамических функций легких используется для дифференциации рестриктивной легочной болезни (РЛБ) и обструктивной легочной болезни (ОЛБ). РЛБ характеризуется функциональным уменьшением объема легких, как, например, при отеке легких, пневмонии и ухудшении легочного наполнения при искривлении позвоночника. При ОЛБ происходит сужение воздушных путей, как, например, при астме, бронхите, эмфиземе и параличе голосовых связок (В2).
Как и в случае ЖЕЛ, эмпирические формулы также используются для стандартизации ФЖЕЛ по возрасту, росту и полу пациентов.
Газообмен в легких[править | править код]
Вентиляция альвеол[править | править код]
Только альвеолярная часть (VA) экскурсирующего объема достигает альвеол. Остальной воздух остается в мертвом объеме (VD). VA = VT - VD(л). Произведение объема на частоту дыхания (f мин-1) дает вентиляцию, т. е. VA , Vf (или VT) и VD. Таким образом, VA= VE- VD (л • мин-1). Поскольку величина VD задана анатомически, значение VD (= VD• f) повышается с увеличением f. Если при данной общей вентиляции (VE = VT • f) дыхание становится более частым ( f ↑), хотя и менее глубоким (VT↓), $а будет снижаться, поскольку VD увеличивается.
Пример. Если VE = 8 л • мин-1, VD = 0,15 л, нормальная частота дыхания f = 16 мин-1, то VA = 5,6 л * мин-1, т. е. 70% VE. Когда f удваивается и VT снижается до половинного значения, VA падает до 3,2 л • мин-1, т. е. 40% VT, хотя Ve (8 л • мин-1) остается без изменений.
Таким образом, альвеолярный газообмен может ухудшаться при неглубоком и частом дыхании (например, из-за перелома ребра) или вследствие болезни, или искусственного увеличения VD.
Потребление O2 (VO2) определяется как разность скорости потока вдыхаемого O2 (= VE • FIO2), и скорости выдыхаемого O2 (= VE*FEO2)- Таким образом, VO2 = VE(FIO2-FEO2). В покое VO2 = 8 (0,21 - 0,17) = 0,32 л • мин-1.
Объем удаляемого СO2 (VcO2) определяется как VT+FECO2 = 0,26 л • мин-1 в покое; (FICO2=0). При интенсивной физической работе V)2 и VСO2 увеличиваются примерно в 10 раз. Отношение VСO2/VO2 называется дыхательным коэффициентом (RQ), который зависит от алиментарного статуса человека. RQ варьирует от 0,7 до 1,0.
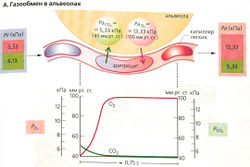
Газообмен между альвеолами и кровью происходит путем диффузии и описывается законом диффузии Фика. В капиллярах легких движущая сила этой диффузии - разность парциальных давлений в альвеолах и эритроцитах (А). Среднее парциальное давление O2 в альвеолах PAO2 «13,3 кПа (100 мм рт. ст.), а парциальное давление СO2 РaСO2 «5,3 кПа (40 мм рт. ст.). В «венозной крови» легочных артерий среднее парциальное давление PvO2 —5,3 кПа (40 мм рт. ст.) и PvСO2 —6,1 кРа (46 мм рт. ст.). Таким образом, средняя разность парциальных давлений в альвеолах и в капиллярах составляет около 8 кПа (60 мм рт. ст.) для O2 и 0,8 кПа (6 мм рт. ст.) для СO2, но в некоторых частях легких эти величины могут варьировать. PAO2 с уменьшением РaСO2 увеличивается 126 (например, это обусловлено гипервентиляцией) и наоборот (газовое уравнение для альвеол).
O2 диффундирует на расстояние примерно 1-2 мкм из альвеол в кровоток (расстояние диффузии). При нормальных условиях, в покое, кровь в легочных капиллярах находится в контакте с альвеолами примерно 0,75 с. Это время контакта (А) является достаточно продолжительным для достижения равновесия между кровью и альвеолярными газами. Таким образом, капиллярная кровь артериализуется. PO2 и PСO2 в артериализованной крови (PaO2 и РaСO2) примерно одинаковы по величине с соответствующими альвеолярными давлениями (РaСO2 и PAСO2). однако венозная кровь входит в артериализованную через артериовенозные шунты в легких, а также из бронхиальных вен (Б). Этот внеальвеолярный шунт, а также вентиляционно-перфузионное неравенство вызывают снижение PaO2 от 13,3 кПа (после прохождения через альвеолы) до 12,0 кПа (90 мм рт. ст.) в аорте (РaСO2 Увеличивается лишь незначительно).
Малая разность давлений, составляющая примерно 0,8 кПа, тем не менее достаточна для альвеолярного обмена СO2, поскольку в тканях коэффициент диффузии Коха %)2 - 2,5 • 10-16 м2 • с-1 • Па-1, что в 23 раза больше, чем для O2. Во время физической работы (высокий минутный объем сердца) время контакта снижается и составляет всего треть величины покоя. Если диффузия ослаблена (см. ниже), уравновешивание парциальных давлений O2 в альвеолах при физической нагрузке менее вероятно, чем в покое.
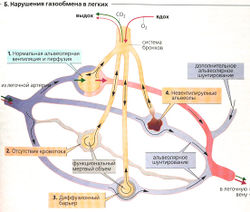
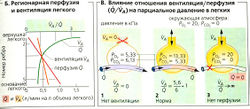
Ухудшение альвеолярного газообмена может произойти по нескольким причинам: (а) при снижении скорости кровотока по альвеолярным капиллярам (например, из-за легочного инфаркта, Б2), (б) при наличии диффузионного барьера (например, из-за утончения капиллярной стенки при отеке легких; БЗ), (в) если ослаблена альвеолярная вентиляция (например, из-за закупорки бронха; Б4). В случаях Б2 и БЗ происходит увеличение функционального мертвого объема, а в случаях БЗ и Б4 - неадекватная артериализация крови (альвеолярный шунт, т. е. смешивание неартериализованной крови с артериальной). Постепенные нарушения Б2 и Б4 могут происходить даже у здоровых людей .
Легочный кровоток, соотношение «вентиляция-перфузия»[править | править код]
Если пренебречь небольшим количеством крови, которая достигает легких по бронхиальным артериям, средняя бронхиальная перфузия МП, или кровоток к легким, эквивалентна минутному объему сердца (СО = 5-6 л/мин). Легочное артериальное давление составляет около 25 мм рт. ст. в систоле и 8 мм рт. ст. в диастоле, и в среднем Р «15 мм рт. ст. Р снижается до 12 мм рт. ст. в прекапиллярном участке (Pprecap, до начала легочных капилляров) и примерно до 8 мм рт. ст. в посткапиллярном участке [Ppostcapl- Эти величины относятся к участкам легких, расположенным на уровне клапана легочного ствола.
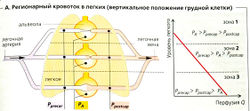
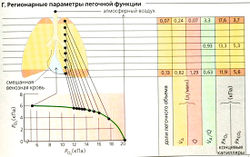
Неравномерное распределение кровотока внутри легкого (А). Благодаря суммарному эффекту гидростатического давления (до 12 мм рт. ст.) Рргесар увеличивается в кровеносных сосудах ниже легочных клапанов (ниже основания легкого), когда грудная клетка расположена вертикально. Вблизи вершины легкого Pprecap снижается в сосудах выше клапана легочной артерии (А, зона 1). При этих условиях Рргесдр может снижаться даже до субатмосферного уровня, а среднее альвеолярное давление [РA] находится на уровне атмосферного и, таким образом, может вызывать распространенную компрессию капилляров (P а > Pprecap > Рpostcap, А). B результате величина Q на единицу легочного объема очень мала. В центральной части легкого (А, зона 2) может произойти сужение просвета капилляра - его венозной части, по крайней мере временно (Рргесар > Ра > Ppostcap), тoгда как участок вблизи основания легкого (А, зона 3) постоянно снабжается кровью (Рргесар > Ppostcap > РА). Таким образом, величина Q на единицу легочного объема снижается от верхушки легкого к основанию (А, В, красная линия).
Неравномерное распределение альвеолярной вентиляции. Альвеолярная вентиляция на единицу объема также увеличивается от верхушки к основанию легких из-за эффекта гравитации (Б, оранжевая линия), хотя и не так значительно, как Q. Таким образом, отношение VA/Q снижается от верхушки к основанию легкого (Б, зеленая кривая и верхняя шкала).
Дисбаланс отношения VA/Q. В среднем для всего легкого отношение VA/Q составляет 0,93 (В). Эта величина вычисляется из средней альвеолярной вентиляции VА (5,6 л/мин) и общей перфузии Q (6 л/мин), что эквивалентно минутному объему сердца (СО). При экстремальных условиях, когда q/ща из частей легкого не вентилируется совсем,
VA/Q = 0 (В1). При другой крайности, когда кровоток отсутствует (VA/Q→ ∞; ВЗ), в альвеолах будет преобладать «свежий» воздух (функциональный 128 мертвый объем). Таким образом, теоретически для отношения VA/Q возможны большие вариации: от 0 до бесконечности. В этом случае PAO2 будет колебаться между смешанной венозной PVO2 и PIO2 г (влажного) свежего воздуха (Г). В здоровом вертикальном легком l)A/Q в покое значительно снижается (от 3,3 до 0,63) от вершины к основанию (Б, зеленая линия). PAO2 (РaСO2) составляет, таким образом, 17,6 (3,7) кПа в «гипервентилируемой» верхушке легкого, 13,3 (5,3) кПа в нормально вентилируемой центральной зоне, и 11,9 (5,6) кПа в гиповентилируемом основании легкого. Эти изменения не так резко выражены во время физических нагрузок, поскольку 0 в зоне 1 также возрастает из-за соответствующего увеличения Рprecap.
Дисбаланс отношения VA/Q снижает эффектность газообмена в легких. Несмотря на высокое давление PAO2 в верхушке легкого (примерно 17,6 кПа; Г, справа) и относительно нормальное среднее значение PAO2, сравнительно небольшая О-фракция зоны 1 вносит небольшой вклад в общее значение О легочных вен. В этом случае PaO2 < PAO2, и поэтому существует альвеолярно-артериальная разность O2 (AaDO2) (обычно около 1,3 кПа).При наличии общего артерио-венозного шунта (VA/Q = 0) пациенту не поможет даже кислородное лечение, поскольку кислород не достигнет ложа легочных капилляров (В1).
Гипоксическая вазокоистрикция регулирует кровоснабжение капилляров и предотвращает развитие экстремальных отношений VA/Q. Когда PAO2 резко снижается, рецепторы в альвеолах производят локальные сигналы, запускающие сокращение подходящих кровеносных сосудов. Это сдавливает шунты в слабовентилируемых или невентилируемых участках легкого, таким образом направляя большие количества крови для газообмена в более продуктивные участки.
Дисбаланс VA/Q может вызывать серьезные осложнения при многих легочных заболеваниях. При легочном шоке, например, шунты могут составлять до 50% от общей величины 0. Опасное для жизни прекращение легочной функции быстро развивается при отеке легкого, альвеолярном диффузионном барьере и нарушениях выделения сурфактанта.
Транспорт СO2 в крови[править | править код]
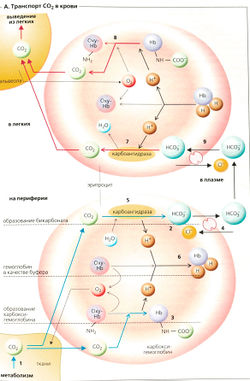
Углекислый газ (СO2) - это конечный продукт энергетического метаболизма. СO2, продуцируемый клетками организма, претерпевает физическое вытеснение и диффундирует в соседние кровеносные капилляры. Небольшое количество СO2 остается растворенным в крови, тогда как в основном он химически связан в форме НСО3 и карбоксигемоглобина (A, нижняя часть рисунка, синие стрелки; артериовенозная разница концентрации СO2 дана в таблице). Кровоток, насыщенный СO2, попадает в легочные капилляры из правого предсердия. В легочных капиллярах СO2 высвобождается (А, красные стрелки), диффундирует в альвеолы и выводится в атмосферу.
Фермент карбоангидраза (карбонатдегидратаза) катализирует реакцию НСО3 + Н+ ⇄ СO2 + Н2О в эритроцитах (A5, 7). Поскольку это ускоряет установление равновесия, краткого времени контакта (< 1 с) между красными кровяными клетками и альвеолами или периферическими тканями достаточно для превращения СO2 ⇄ НСО3.
Диффундирующий из клеток периферической крови СO2 (A, см. внизу «Ткань») увеличивает РСO2 (в артериальной крови —5,3 кПа = 40 мм рт. ст.) до среднего давления в венах РСO2 (—6,3 кПа = = 47 мм рт. ст.). Это также увеличивает концентрацию СO2 в плазме. однако большая часть СO2 диффундирует в красные кровяные клетки, тем самым увеличивая содержание в них СO2. В клетках крови СO2 (+Н2О) превращается в НСО3 (А5, 2) и карбоксиге-моглобин (АЗ). Концентрация НСО3 в эритроцитах, таким образом, становится выше, чем в плазме. В результате около трех четвертей ионов НСО3 выходят из эритроцитов с помощью НСО3/Сl антипортера. Этот анионный обмен также называется переносом хлора (сдвигом Хамбургера) и отображен на A4.
Ионы Н+ высвобождаются, когда СO2 красных кровяных клеток периферической крови превращается в НСО3 и карбоксигемоглобин.
Образование бикарбоната:
СO2 + Н2О ⇄ НСО3 + Н+. [5.4]
Образование карбоксигемоглобина:
Hb-NH2 + СO2 ⇄ Hb-NH-COO- + Н+. [5.5]
Гемоглобин (НЬ) является главным буфером для ионов Н+ в красных кровяных клетках (А6;«Небикарбонатные буферы»). До тех пор пока удаление ионов Н+ в реакциях [5.4] и [5.5] не допускает быстрого установления равновесия, большие количества СO2 могут связываться в НСО3 и карбоксигемоглобин. Деоксигенированный гемоглобин (НЬ) может принять больше ионов Н+, чем окси-гемоглобин (Оху-Hb), поскольку НЬ является более слабой кислотой (Я). Это способствует поглощению СO2 периферической кровью [эффект Холдена) благодаря одновременному высвобождению O2 из эритроцитов, т. е. благодаря дезоксигенации Оху-НЬ до НЬ.
В легочных капиллярах эти реакции протекают в противоположном направлении (Я, верхняя часть рисунка, красные и черные стрелки). Давление РСO2 г в альвеолах ниже, чем в венозной крови, поэтому СO2 диффундирует в альвеолы, и равновесие реакций [5.4] и [5.5] сдвигается влево. СO2 высвобождается из НСО3 и карбамата гемоглобина, за счет чего ионы Н+ (высвобождаемые из НЬ) связываются в обоих реакциях (А7, 8), и направление транспорта в НСОз/Сl-обменнике меняется на обратное (A9). Реоксигенация НЬ в Оху-НЬ в легком способствует этому процессу, поскольку улучшает снабжение ионами Н+ (эффектХолдена).
Таблица
|
Распределение С02 в крови (ммоль/л крови, 1 ммоль = 22,26 мл ССУ | ||||
|
растворенный С02 |
НС03- |
карбамат |
ИТОГО | |
|
Артериальная кровь | ||||
|
Плазма* |
0,7 |
13,2 |
0,1 |
14,0 |
|
Эритроциты** |
0,5 |
6,5 |
1,1 |
8,1 |
|
Кровь |
1,2 |
19,7 |
1,2 |
22,1 |
|
Смешанная венозная кровь | ||||
|
Плазма* |
0,8 |
14,3 |
0,1 |
15,2 |
|
Эритроциты** |
0,6 |
7,2 |
1,4 |
9,2 |
|
Кровь |
1,4 |
21,5 |
1,5 |
24,4 |
|
Артериовенозная разница С02 в крови | ||||
|
0,2 |
1,8 |
0,3 |
2,3 | |
|
Процент от общей артериовенозной разницы | ||||
|
9% |
78% |
13% |
100% | |
|
* Примерно 0,55 л плазмы/л крови. ** Примерно 0,45 л эритроцитов/л крови. | ||||
Связывание СO2 в крови[править | править код]
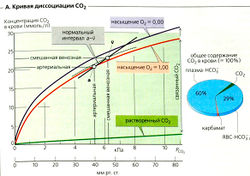
Общая концентрация углекислого газа (= химически связанный СO2 + растворенный СO2) в смешанной венозной крови составляет примерно 24-25 ммоль/л; в артериальной крови - примерно 22-23 ммоль/л. Почти 90% этого количества углекислоты существует в виде НСО3 (А, справа). Парциальное давление СO2 (ЯсоР является основным фактором, определяющим содержание СO2 в крови. Кривая диссоциации СO2 иллюстрирует, как общая концентрация СO2 зависит от %)г (А).
Концентрация растворенного СO2 [СO2] в плазме прямо пропорциональна %)г в плазме и может быть рассчитана следующим образом:
[СO2] = аСO2 * РСO2 (ммоль/л плазмы или мл/л плазмы), [5.6],
где (aCO2г - растворимость СO2 (коэффициент Бунзена). При 37 °С
аСO2 = 0.225 ммоль • л-1 • кПа-1.
После перевO2а количества СO2 в объем СO2 (мл = ммоль • 22,26) получаем aСO2 = 5 мл • л-1 • кПа-1.
Зависимость концентрации растворенного СO2 в крови, таким образом, линейна (А, зеленая линия).
Буферная емкость пары гемоглобин-оксигемоглобин ограниченна, поэтому зависимость содержания «связанного СO2» от РСO2 уже нелинейна. Кривая диссоциации рассчитана для общего содержания СO2 (сумма растворенного и связанного СO2) (А, красная и фиолетовая линии).
Связывание СO2 с гемоглобином зависит от степени насыщения кислородом (SO2) гемоглобина. При одинаковом РСO2 кровь, полностью насыщенная O2, не способна связывать такие же количества СO2, как совсем не содержащая O2 (А, красная и фиолетовая линии). Когда в легких венозная кровь поглощает O2, буферная емкость гемоглобина и, следовательно, уровень химического связывания СO2 снижаются из-за эффекта Холдена. Венозная кровь никогда не может совсем не содержать O2, наоборот, в зависимости от того, о каком органе идет речь, в ней всегда содержатся те или иные количества кислорода. Величина SO2 смешанной венозной крови составляет около 0,75. Кривая диссоциации СO2 для SO2 = 0,75, таким образом, лежит между кривыми для SO2 = 0,00 и SO2 -1,00 (А, прерывистая линия). В артериальной крови РСO2 « 5,33 кПа и « 0,97 (А, точка а). В смешанной венозной крови РСO2 « 6,27 кПа и SO2 « 0,75 (А, точка 7). Нормальный уровень диссоциации СO2 определяется интервалом а-v на физиологической кривой диссоциации СO2, которую можно построить,если провести через точки а и 7 прямую.
Отношение концентраций НСО3 и растворенного СO2 в плазме и красных кровяных клетках различается (примерно 20:1 в плазме и 12:1 в эритроцитах). Это соответствует разным значениям pH в плазме (7,4) и эритроцитах (примерно 7,2).
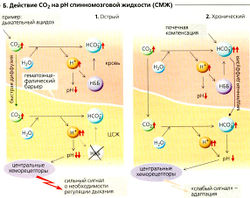
СO2 в спинномозговой жидкости В отличие от НСО3 и Н+, молекула СO2 может относительно легко преодолевать гематоэнцефалический барьер между кровью и спинномозговой жидкостью (СМЖ) (Б1). РСO2 в СМЖ тем самым быстро адаптируется к резким изменениям РСO2 в крови. Связанные с СO2 (респираторные) изменения pH в организме могут быть нейтрализованы только при помощи небикарбонатных буферов (НББ). Поскольку концентрация небикарбонатных буферов в СМЖ очень низкая, резкий рост РСO2 (респираторный ацидоз) ведет к довольно быстрому снижению pH в СМЖ (Б1, pH ↓↓ ) что регистрируется центральными хемосенсорами (хеморецепторами), которые регулируют в соответствии с этим дыхательную активность. (В данной книге чувствительные рецепторы называются сенсорами с целью отличить их от рецепторов гормонов и медиаторов.)
В крови концентрация небикарбонатных буферов (гемоглобин, белки плазмы) высокая. Когда концентрация СO2 растет, высвобождающиеся ионы Н+ эффективно забуфериваются в крови. Реальная концентрация НСО3 в крови при этом довольно медленно растет и результат становится выше, чем в СМЖ. Благодаря этому ионы НСО3 диффундируют (довольно медленно) в СМЖ (Б2), приводя к новому повышению pH в СМЖ, поскольку увеличивается отношение НСО3/СO2. Это, в свою очередь, ведет к уменьшению дыхательной активности (через центральные хемосенсоры); процесс усиливается в почках - pH крови растет благодаря задержке НСO3 . При помощи этого механизма организм в итоге адаптируется к хронически повышенному давлению РСO2, т е хронически повышенное значение РСO2 не будет действовать на дыхание.
Тканевое дыхание[править | править код]
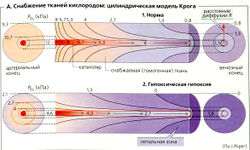
O2 диффундирует из периферической крови к близлежащим тканям, а СO2 - в обратном направлении. Поскольку СO2 диффундирует гораздо быстрее, диффузия O2 является лимитирующим фактором. Достаточное снабжение O2 обеспечивается развитой капиллярной сетью с площадью газообмена —1000 мг. Расстояние диффузии (R) составляет только 10-25 мкм. Движущая сила диффузии - это разность парциальных давлений кислорода (ΔPO2) в капиллярной крови и митохондриях, где PO2 не должно падать ниже 0,1 кПа (1 мм рт. ст.). Поскольку PO2 понижается с расстоянием по ходу капилляров, на удаленном (дистальном) конце капилляра (при входе его в венозное русло) доставка O2 к клеткам (большое R) незначительна, что и показано на цилиндрической модели Крога (А1). Такие клетки первые страдают от дефицита кислорода [гипоксий), поэтому иногда этот участок называют «летальной зоной» (А2).
По принципу Фика потребление кислорода в данном органе, VO2 (в л/мин), определяется как разность между артериальным запасом (Q • [O2]a) и неиспользованным венозным остаточным объемом Ог/время (G * [O2]v, где Q - скорость кровотока в органе (л/мин), [O2] - содержание кислорода (л Ог/л крови):
VO2 = Q([O2]a-[O2]v) [5.7]
Для того чтобы отвечать повышенным потребностям в O2, скорость кровотока 0 может быть увеличена за счет вазодилатации в данном органе и/или путем увеличения извлечения кислорода в тканях (EO2). EO2 - потребление O2 в органе, т. е. отношение Q([O2]a-[O2]v), см. уравнение 5.7) к артериальному запасу O2 (Q • [O2]a). Выражение для О можно упростить,
EO2 = ([O2]a-[O2]v)/[O2]a [5.8]
Еq2 варьирует с типом органа и его функцией в условиях покоя: кожа 0,04 (4%), почки 0,07; мозг, печень и скелетные мышцы в покое —0,3, миокард 0,6. Во время интенсивной физической нагрузки мышц EO2 может увеличиваться до 0,9. Скелетные мышцы при нагрузке отвечают тем, что их потребность в кислороде повышается, т. е. EO2 увеличивается (0,3 => 0,9). Аналогичной способностью обладает и миокард, но в значительно меньшей степени и в случае трех типов гипоксии, описанных ниже (Б1-3), возможна только ограниченная компенсация.