Дыхательная система
Категория:
«Фармакология».
Содержание
- 1 ФИЗИОЛОГИЯ СИСТЕМЫ ДЫХАНИЯ
- 2 ПАТОФИЗИОЛОГИЯ И ЗАБОЛЕВАНИЯ СИСТЕМЫ ДЫХАНИЯ
- 3 Бронхиальная астма
- 4 Хроническая обструктивная болезнь легких
- 5 Респираторный дистресс-синдром
- 6 Муковисцидоз
- 7 Кашель
- 8 Ринит и ринорея
- 9 Респираторные инфекции
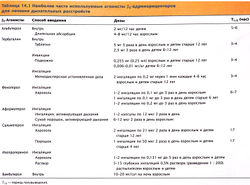
- 10 Антибиотики, используемые для отдельных инфекций респираторного тракта
- 11 Легочная эмболия
- 12 Легочная гипертензия
- 13 Побочные эффекты лекарственных средств для лечения респираторных заболеваний
- 14 Читайте также
- 15 Литература
ФИЗИОЛОГИЯ СИСТЕМЫ ДЫХАНИЯ[править | править код]
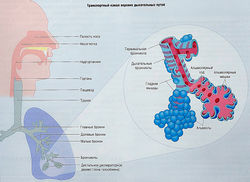
Кровь оксигенируется и удаляет углекислый газ посредством системы дыхания
В организме осуществляется множество метаболических процессов с использованием большого количества кислорода и выделением не меньшего количества углекислого газа. Кислород-поглощающая поверхность легкого (поверхность газообмена) огромна (80 м2). Она сформирована в виде ветвящейся древоподобной системы трубок для проведения воздуха (бронхи и бронхиолы), которые заканчиваются миллионами крошечных мешков, называемых альвеолами (рис. 14.1).
Дыхание контролируют спонтанные ритмические импульсы из дыхательного центра в продолговатом мозге, который регулируют высшие центры регуляции головного мозга и афферентные вагусные сигналы из легких (рис. 14.2). Процесс дыхания зависит от:
- изменений в крови парциального давления углекислого газа (рСO2), активируемых хеморецепторами продолговатого мозга;
- изменений в крови парциального давления кислорода (рO2), активируемых хеморецепторами дуги аорты и каротидных телец.
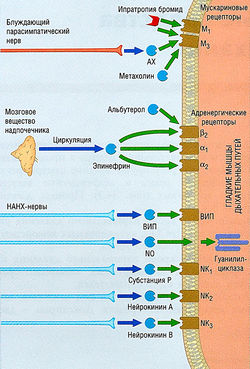
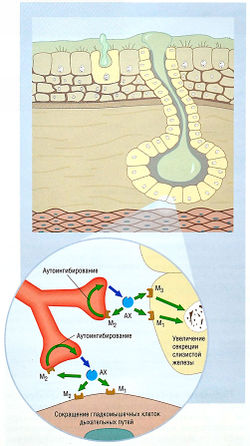
Рис. 14.2 Тонус и иннервация гладких мышц дыхательных путей. Тонус констрикторов обеспечивается блуждающим нервом и выработкой ацетилхолина (АХ). Его блокирует смешанный антагонист мускариновых М,/М3-рецепторов тиотропия бромид. Метахолин, определяющий возбудимость респираторного тракта у пациентов с астмой (см. рис. 14.4), активирует эти рецепторы. Циркулирующий эпинефрин расслабляет гладкие мышцы дыхательных путей, активируя бета2-рецепторы. По этому принципу действуют такие р2-агонисты, как альбутерол. Главное ингибирующее влияние на тонус гладких мышц дыхательных путей оказывает оксид азота (NO), высвобождаемый неадренергическими нехолинергическими (НАНХ) нервами, и в меньшей степени вазоактивный интестинальный пептид (ВИП). НАНХ-нервы также имеют волокна, которые могут выделять сенсорные нейропептиды, такие как субстанция Р и нейрокинины (NK), вызывающие сокращение гладких мышц дыхательных путей.
Дыхание может изменяться под влиянием некоторых лекарственных средств. Доксапрам — дыхательный стимулятор, функционирующий посредством стимуляции каротидных хеморецепторов и хеморецепторов в дыхательном центре; применяют у пациентов с легочной недостаточностью. Некоторые лекарственные средства, содержащие наркотические анальгетики, барбитураты, блокаторы центральных Н1рецепторов и этанол, вызывают угнетение дыхания.
Тонус гладких мышц дыхательных путей регулируют парасимпатические, симпатические и неадренергические нехолинергические нервы и циркулирующий эпинефрин
Гладкие мышцы дыхательных путей иннервируются:
- парасимпатической нервной системой посредством блуждающего нерва IX пара черепно
Лекарственные средства, влияющие на дыхание
- Наркотические анальгетики, барбитураты, некоторые блокаторы Н1рецепторов и этанол вызывают угнетение дыхания
- Доксапрам стимулирует дыхание, его применяют у пациентов с легочной недостаточностью
- Полагают, что стимуляторы дыхания активируют и каротидные хеморецепторы, и дыхательный центр. Их назначают с большой осторожностью из-за нежелательных эффектов со стороны ЦНС (например, судорог), но эффективность препаратов не всегда гарантирована
Неинфекционные заболевания респираторного тракта
- Наиболее распространенные заболевания — астма, аллергический ринит и хронические обструктивные заболевания легких (хронический бронхит и эмфизема)
- Астма — воспалительное заболевание
- Муковисцидоз — наследственное заболевание
- Кашель — основной симптом заболеваний респираторного тракта мозговых нервов) за счет действия ацетилхолина на мускариновые рецепторы (см. рис. 14.2);
- так называемой третьей нервной системой с нейротрансмиттерами — оксидом азота и вазоактивным интестинальным пептидом — с использованием неадренергических нехолинергических нервов этой системы (см. рис. 14.2), вызывающих расслабление гладких мышц бронхов (бронходилатацию).
Дилатацию бронхов вызывает также эпинефрин, связывающийся с β2-адренорецепторами гладких мышц бронхов (см. рис. 14.2). Несмотря на то что у гладких мышц бронхов нет прямой симпатической иннервации или она слабая, существуют дополнительные ингибирующие элементы парасимпатических ганглиев.
Тонус гладких мышц дыхательных путей зависит от баланса между:
- влиянием парасимпатической нервной системы;
- ингибирующим влиянием циркулирующего эпинефрина;
- неадренергическими нехолинергическими тормозными нервами;
- симпатической иннервацией парасимпатических ганглиев.
ПАТОФИЗИОЛОГИЯ И ЗАБОЛЕВАНИЯ СИСТЕМЫ ДЫХАНИЯ[править | править код]
При легочных заболеваниях появляются кашель, хрипы, одышка и нарушения газообмена
Кашель, хрипы, одышка (диспноэ) и нарушения газообмена могут быть результатом:
- изменения тонуса гладких мышц (например, при бронхиальной астме);
- васкулярной гиперемии верхних дыхательных путей (например, при назальной гиперемии);
- закупорки слизью (например, при астме и хроническом бронхите);
- нарушения газообмена (например, при эмфиземе);
- гиперсекреции (при рините, астматическом компоненте).
Бронхиальная астма[править | править код]
Бронхиальная астма — хроническое воспалительное заболевание дыхательных путей, вызывающее острый бронхоспазм и диспноэ
Бронхиальная астма — распространенное заболевание, поражающее до 20% населения некоторых стран. Заболеваемость и смертность в связи с астмой в большинстве стран постоянно возрастают, несмотря на рост использования противоастматических лекарственных средств.
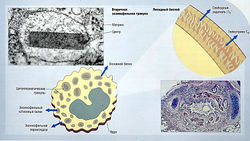
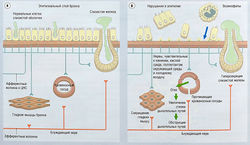
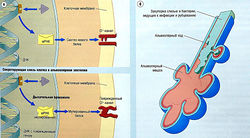
Характеристика клинических симптомов бронхиальной астмы связана с хронической воспалительной реакцией в дыхательных путях с вовлечением местных лимфоцитов и эозинофилов, которые на всем протяжении сопровождают бронхоальвеолярное дерево, на биопсии и аутопсии (рис. 14.3). Считается, что гранулы эозинофилов выделяют цитотоксические медиаторы (см. рис. 14.3), которые разрушают реснитчатый эпителий дыхательной системы. Повреждение тканей связано с повышенной раздражимостью дыхательных путей (гиперчувствительностью бронхов), вызывающей кашель и хрипы в ответ на стимулы, которые обычно не провоцируют такую реакцию у здоровых людей (рис. 14.4).
Рис. 14.3 Цитотоксические медиаторы, выделяемые эозинофилами и разрушающие эпителий. Эозинофилы при инфильтрации выделяют цитотоксические медиаторы из гранул, такие как основной белок, эозинофильную пероксидазу и эозинофильный катионный белок. Некоторые медиаторы воспаления могут выделяться липидным бислоем при активации эозинофилов. Секреция дыхательных путей при астме имеет патофизиологические изменения (предоставлено Alan Stevens, James Lowe).
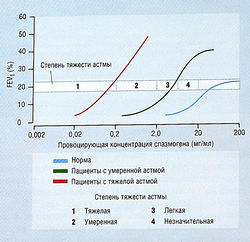
Рис. 14.4 Гиперчувствительность бронхов. У пациентов с бронхиальной астмой наблюдается гиперчувствительность бронхов, приводящая к кашлю и хрипам в ответ на стимулы, которые не вызывают такую реакцию у здорового человека. Клинически такая гиперчувствительность может проявляться изменением дыхательной функции, а именно снижением объема форсированного выдоха за первую секунду (FEV,) в ответ на вдыхание спазмогенов, таких как гистамин или мускариновый агонист метахолин. Прогрессирование болезни сопровождается повышением раздражимости дыхательных путей.
Клинические проявления бронхиальной астмы
- Острые приступы одышки, связанные с острой обструкцией дыхательных путей из-за сокращения гладких мышц бронхов
- Гиперсекреция слизи, которая может привести к закупорке слизью и нарушению газообмена
- Воспаление дыхательных путей
- Гиперчувствительность бронхов
Гиперчувствительность бронхов возникает в результате воздействия на чувствительные нервы, расположенные под поврежденным эпителием (рис. 14.5). Активация этих нервов в ответ на стресс или воздействие раздражителей окружающей среды приводит к местным аксональным и вагусным рефлексам, которые могут приводить к бронхоспазму, секреции слизи и вазодилатации воздухоносных путей (см. рис. 14.5).
При лечении астмы используют бронходилататоры и противовоспалительные лекарственные средства.
Бронходилататоры[править | править код]
Острый обратимый бронхоспазм проявляется характерным свистящим хрипом, что является критерием лечения бронходилататорами трех различных классов: агонистами β2-адренорецепторов, антихолинергическими лекарственными средствами (антагонистами мускариновых рецепторов) и ксантинами.
АГОНИСТЫ β2-АДРЕНОРЕЦЕПТОРОВ. Агонисты β2-адренорецепторов — наиболее широко используемые препараты для лечения бронхоспазма при астме, их применяют ингаляционно установленными дозами или посредством распылителя системно и перорально (табл. 14.1). Агонисты β2-адренорецепторов короткого действия широко используют для облегчения острого бронхоспазма, они содержат альбутерол, тербуталин и фенотерол. Эпинефрин, изопротеренол, изоэтарин и метапротеренол не являются селективными для β2адренорецепторов и имеют различную степень активности по отношению к а- и β1-рецепторам, что, по сути, является их побочным эффектом. Большинство β2-адренорецепторов доступны в форме рацемических смесей, но недавно в клиническую практику был введен одиночный энантиомер R-альбутерола.
Агонисты β2адренорецепторов расслабляют гладкие мышцы дыхательных путей посредством активации G-белок-связанных рецепторов, что приводит к их активации и возрастанию цАМФ в гладких мышцах дыхательных путей. Они являются действенными функциональными (физиологическими) антагонистами бронхоконстрикции, вызванной широким спектром воздействий. Одним из недостатков альбутерола, тербуталина и фенотерола является короткий Т1/2, равный 2-3 час. Но некоторые агонисты β2-адренорецепторов длительного действия, такие как сальметерол, аформотерол и бамбутерол, устраняют бронходилатацию до 15 час. Считается, что длительное действие сальметерола связано с присутствием в молекуле длинного липофильного радикала, который связывается с экзорецептором в непосредственной близости к β2-адренорецептору на гладких мышцах дыхательных путей. Эти лекарственные средства длительного действия предназначены для долгосрочной профилактики приступов астмы, и их не рекомендуют при остром приступе, особенно сальметерол, который начинает оказывать эффект через 15 мин после введения. Данные лекарственные средства особенно эффективны при лечении ночных приступов астмы, но их не рекомендуют в качестве монотерапии и, как правило, применяют в сочетании с ингаляционными глюкокортикостероидами (см. далее). Тем не менее отдельные лекарственные средства, содержащие сальметерол, были внесены в черный список, т.к. их использование может повышать риск смертности у некоторых пациентов.
Рис. 14.5 Механизм гиперчувствительности бронхов. Гиперчувствительность бронхов может возникнуть в результате ответа чувствительных нервов дыхательных путей на поражение эпителиального слоя цитотоксическими медиаторами из проникающих эозинофилов. Гиперчувствительность также может быть ответом на выделение воспалительных медиаторов, таких как простагландины и цитокины. (а) Легкое в норме, (б) Легкое больного астмой. ЦНС — центральная нервная система.
Побочные эффекты агонистов β2-адренорецепторов: тремор, гипокалиемия, а при передозировке — тахикардия. Ингаляция агонистов β2-адренорецепторов или выбор наилучшего альтернативного пути введения уменьшают риск возникновения побочных эффектов.
АНТИХОЛИНЕРГИЧЕСКИЕ СРЕДСТВА. Антихолинергические средства, блокирующие мускариновые рецепторы, вызывают бронходилатацию, связываясь с мускариновыми рецепторами гладких мышц дыхательных путей, тем самым предотвращая действие ацетилхолина, высвобождающегося из парасимпатических окончаний блуждающего нерва. Антихолинергические средства не предотвращают все типы бронхоспазма, но эффективны против нарушений респираторной функции, вызванных различными раздражителями. Антагонисты мускариновых рецепторов также снижают секрецию слизи.
Известные на сегодняшний день антагонисты мускариновых рецепторов не селективны в отношении М2- и М3-рецепторов (рис. 14.6), и аутоантагонизм М2-рецептора на холинергических пресинаптических окончаниях может снизить эффективность антагонизма на М3-рецепторах гладких мышц. Селективные антагонисты М3-рецепторов имеют явное терапевтическое преимущество.
Рис. 14.6 Действие ацетилхолина (АХ) на гладкие мышцы дыхательных путей. Ацетилхолин, выделяемый парасимпатическими нейронами и действующий на мускариновые М,- и М3-рецепторы дыхательного пути и подслизистые железы, влияет на сокращение мышц и секрецию слизи. Также некоторые ацетилхо-лины влияют на пресинаптические мускариновые М2-рецепторы нервных окончаний, снижая дальнейшую продукцию ацетилхолинов. Эти М2-рецепторы называют ауторецепторами.
Лекарственные средства для лечения астмы
- Все агонисты β2-адренорецепторов вызывают бронходилатацию
- Основное действие глюкокортикостероидов — подавление воспалительного ответа
- Ксантины обладают бронходилатирующим и противовоспалительным действиями
- Блокаторы мускариновых рецепторов, вызывающие бронходилатацию, могут быть эффективны для лечения астмы
Антагонисты мускариновых рецепторов включают такие короткодействующие лекарственные средства, как атропин, ипратропия бромид и окситропия бромид, а также длительно действующее средство тиотропия бромид (табл. 14.2). Эти препараты применяют в клинике ингаляционно с целью снижения системных побочных эффектов, так или иначе ассоциированных с антагонистами мускариновых рецепторов. Во время ингаляции препараты в небольших количествах абсорбируются в системном кровотоке легкого, не проникая через гематоэнцефалический барьер и вызывая незначительные побочные эффекты. Максимальная бронходилатация обычно достигается через 30 мин после начала введения и сохраняется до 5 час при сочетании с лекарственными средствами короткого действия и до 15 час в сочетании с тиотропия бромидом. При лечении астмы эффективность данных препаратов сравнивают с эффективностью ингаляционных агонистов β2-адренорецепторов и использование является основополагающим методом лечения хронических обструктивных заболеваний легких (см. далее).
КСАНТИНЫ. Ксантины широко применяют в лечении астмы с начала XX века, когда появились сведения о том, что «крепкий кофе» снимает симптомы астмы. В состав кофе, чая и шоколадных коктейлей входят природные ксантины, такие как кофеин и теобромин. Основным ксантином, используемым в клинике, является теофиллин, который иногда входит в состав смеси, состоящей из теофиллина и этилендиамина (аминофиллин). Также применяют бамифиллин и эликсофеллин. Ксантины обычно вводят перорально, но они быстро метаболизируются и имеют короткий биологический период полувыведения. Это ограничение преодолевается путем использования медленно метаболизирующихся препаратов, которые достигают своей максимальной концентрации в плазме через 16-18 час.
Главная проблема в использовании ксантинов в качестве бронходилататоров — их узкая терапевтическая направленность; концентрация в плазме выше 10 мкг/мл оказывает эффект при бронходилатации, а концентрация выше 20 мкг/мл имеет высокий риск побочных эффектов, таких как тошнота, сердечные аритмии и судороги. Концентрацию ксантинов в плазме необходимо регулярно измерять. Для лечения острой астмы аминофиллин рекомендуют медленно вводить внутривенным путем в соответствующей дозе.
Лекарственные средства, повышающие концентрацию теофиллина в сыворотке крови
- Эритромицин
- Антагонисты Са2+
- Циметидин (но не ранитидин)
Лекарственные средства, снижающие уровень теофиллина в сыворотке крови
- Рифампицин
- Фенобарбитал
- Фенитоин
- Карбамазепин
Для лечения острой астмы пациентам, не применяющим теофиллиновые лекарственные средства, назначают дозу 5 мг/кг и устанавливают на уровне 4 мг/кг каждые 6 час для детей от 1 года до 9 лет, 3 мг/кг каждые 6 час детям 9-16 лет и курящим лицам, 3 мг/кг каждые 8 час некурящим взрослым и 2 мг/кг пожилым.
Важно учитывать взаимодействие препаратов, т.к. в результате этого концентрация теофиллина в сыворотке может быть повышена (барбитуратами, бензодиазепинами) или снижена (циметидином, эритромицином, ципрофлоксацином, аллопуринолом). Эти взаимодействия могут изменять концентрацию теофиллина в сыворотке, поэтому его дозу подбирают индивидуально. Лечение начинают с самой низкой дозы, и, если она переносится нормально и симптомы не проявляются, дозу можно увеличивать поэтапно до максимальной рекомендуемой. В течение 3 сут титрование дозы прекращают, чтобы уровень препарата в сыворотке стабилизировался. У тяжелобольных пациентов уровень препарата в сыворотке крови контролируют каждые 24 час. Доза должна быть скорректирована таким образом, чтобы концентрация в сыворотке составляла 5-15 мкг/мл.
Лекарственные средства длительного действия не приемлемы для терапии острой астмы, которую лечат другими препаратами, в том числе и мгновенного действия.
Для лечения ночной астмы лекарственные средства принимают в 20.00, при этом контролируют уровень теофиллина в сыворотке. Желательно титровать дозу с малым шагом, увеличивая ее каждые 3 дня только в том случае, если пациент ее хорошо переносит, а побочные эффекты отсутствуют.
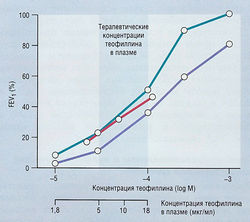
Считается, что ксантины вызывают бронходилатацию путем ингибирования изоферментов фосфодиэстеразы (табл. 14.3). Эти ферменты принимают участие в метаболизме вторичных мессенджеров, вовлеченных в расслабление мышц дыхательных путей (цАМФ и цГМФ). Ингибирование ФДЭ-3 и ФДЭ-4 в гладких мышцах дыхательных путей приводит к внутриклеточной аккумуляции цАМФ и соответственно к расслаблению гладких мышц (рис. 14.7; см. также табл. 14.3).
Рис. 14.7 Эффекты теофиллина в терапевтических концентрациях. Изменение объема форсированного выдоха за первую секунду (FEV,) (красная линия), изменение ингибирования расслабления гладких мышц дыхательных путей (зеленая линия) или ингибирования активности фосфодиэстеразы в этих мышцах (фиолетовая линия) в ответ на концентрацию теофиллина в плазме (мкг/мл) или в ткани (log М в изолированной ткани) [Rabe, et al. Eur Resp I 1995; 289; 600-603].
|
Таблица 14.3 Классификация изоферментов фосфодиэстеразы | |||
|
Семейство |
Изофермент |
Ткань |
Ингибиторы |
|
1 |
Са2+/кальмодулин-зависимый |
Мозг, гладкие мышцы дыхательных путей |
Винпоцетин Теофиллин |
|
2 |
цГМФ-стимулируемые |
Сердце, гладкие мышцы сосудов, тромбоциты, гладкие мышцы дыхательных путей |
Теофиллин |
|
3 |
цГМФ-ингибируемые |
Лимфоциты, тромбоциты, сердце, гладкие мышцы сосудов, гладкие мышцы дыхательных путей |
Милринон Теофиллин |
|
4 |
цAM Ф-селективные |
Клетки воспаления (нейтрофилы, макрофаги, тучные клетки, эозинофилы, лимфоциты), гладкие мышцы дыхательных путей, сердце, мозг, поперечнополосатые мышцы |
Ролипрам Теофиллин Циломиласт Рофлумиласт |
|
5 |
цГМФ-селективные |
Трахея, тромбоциты, гладкие мышцы сосудов |
Запринаст Теофиллин Силденафил |
Противовоспалительные и профилактические лекарственные средства[править | править код]
Противовоспалительные лекарственные средства могут снять существующее бронхиальное воспаление и/или предотвратить сопутствующее воспаление у пациентов с бронхиальной астмой. Большинство противовоспалительных лекарственных средств предотвращает сопутствующее воспаление и поэтому их рассматривают как профилактические противоастматические препараты. Поскольку противовоспалительные лекарственные средства не вызывают бронходилатацию, их не рекомендуют для лечения острых приступов астмы.
ГЛЮКОКОРТИКОСТЕРОИДЫ. Глюкокортикостероиды — самые эффективные из известных противовоспалительных лекарственных средств, применяемые для лечения хронических воспалительных процессов, сопутствующих астме. Они препятствуют проникновению воспалительных клеток в дыхательные пути и формированию отека, воздействуя на эндотелий сосудов. Механизм действия подробно изложен в главе 9.
Глюкокортикостероиды назначают в качестве профилактики, в виде ингаляций, для достижения местного противовоспалительного эффекта, при этом не вызывая системных побочных эффектов. Ингалируемые глюкокортикостероиды при бронхиальной астме: беклометазона дипропионат, будесонид, флутиказона пропионат, триамцинолон, мометазон и циклезонид. Пероральные глюкокортикостероиды необходимы для лечения тяжелой бронхиальной астмы, не чувствительной к ингалируемым глюкокортикостероидам, при этом обычно назначают преднизон, метилпреднизолон или преднизолон (табл. 14.4).
Как пероральные, так и внутривенные глюкокортикостероиды эффективны при лечении острой тяжелой астмы. Так, пероральные глюкокортикостероиды имеют серьезные побочные эффекты, связанные с супрессией гипоталамо-гипофизарных взаимоотношений (табл. 14.4). Постоянное использование может привести в том числе к остановке роста у детей (табл. 14.4).
Комбинацию ингалируемых средств, содержащих глюкокортикостероиды, с агонистами β2-адренорецепторов длительного действия в настоящее время широко используют для оптимального купирования сопутствующего воспаления, а также симптомов бронхоспазма при астме. Наиболее часто назначаемыми сочетаниями являются сальметерол/флутиказона пропионат или будесонид/формотерол. Назначение комбинации этих препаратов в одном ингаляторе позволяет уменьшить дозу приема, что снижает вероятность возникновения побочных эффектов; и в том числе свести к минимуму побочные эффекты глюкокортикостероидов.
КСАНТИНЫ. Ксантины не только вызывают бронходилатацию (см. ранее), но и препятствуют активации воспалительных клеток и проникновению их в дыхательные пути больных бронхиальной астмой. Кроме того, отмена ксантинов после длительного лечения может привести к обострению астмы даже у пациентов, принимающих глюкокортикостероиды. Противовоспалительного эффекта можно достичь меньшей концентрацией лекарственного средства в плазме, чем необходимо для бронходи-латации (5-10 мг/мл). Такие выводы привели к переоценке значения ксантинов в лечении астмы (см. рис. 14.7), в частности потому, что:
- пероральный прием ксантинов значительно удобнее для пациента по сравнению с ингалируемыми лекарственными средствами;
- низкие концентрации теофиллина в плазме дают меньше побочных эффектов. Противовоспалительный эффект ксантинов опосредуется через ингибирование ФДЭ-4 (изоэнзима), находящейся преимущественно в воспалительных клетках (см. табл. 14.3). Последние данные свидетельствуют о том, что теофиллин (средство для лечения острого бронхоспазма у больных астмой) эффективен в малых дозах на длительный период времени и в качестве противовоспалительного препарата.
ИНГИБИТОРЫ ФОСФОДИЭСТЕРАЗЫ-4. Изоэнзимы ФДЭ-4 являются основными ферментами в большинстве воспалительных клеток. Клинические исследования фазы III показали, что рофлумиласт-N-оксид, пероральный активный селективный ингибитор ФДЭ-4, является эффективным препаратом в лечении легкой и умеренной астмы.
Противоаллергические лекарственные средства, содержащие кромолин натрия, кетотифен и недокромил натрия, также используют для профилактики бронхиальной астмы. Кромолин и недокромил натрия эффективны в ингаляциях. Кетотифен действенен при пероральном применении, его используют во всем мире, за исключением США. Другие противоаллергические лекарственные средства содержат эбастин и мизоластин.
Ранее механизмы действия этих профилактических препаратов были недостаточно понятны, но считалось, что кромолин натрия является стабилизатором тучных клеток и, таким образом, препятствует высвобождению гистамина и других медиаторов воспаления. Сейчас известно, что это не единственный их эффект. Профилактические лекарственные средства также способны влиять на многие клетки воспаления, такие как альвеолярные макрофаги, тем самым предотвращая их проникновение в дыхательные пути. Кроме того, кромолин натрия и недокромил натрия могут снижать повышенные нейрональные рефлексы, вызванные раздражением рецепторов дыхательных путей, возможно, путем угнетения ответа раздраженных нервов (см. рис. 14.5). Это делает возможным их использование в лечении астматического кашля.
В последнее время были введены в клиническую практику рекомбинантные гуманизированные моноклональные антитела, которые селективно связываются с иммуноглобулином Е человека (омализумаб). Омализумаб вводят подкожно, он имеет очень большой период полувыведения, что позволяет вводить его 1 раз в месяц для лечения аллергической астмы.
Лекарственные средства, влияющие на синтез и действие лейкотриенов[править | править код]
ЗАФИРЛУКАСТ И МОНТЕЛУКACT. Зафирлукаст и монтелукаст — пероральные активные антагонисты цистеинил-лейкотриеновых рецепторов, блокирующие действие лейкотриенов (ЛТС4 и ATD4) на гладкие мышцы дыхательных путей и сосудистый эндотелий. Наиболее эффективны при лечении аспирин-индуцированной астмы и физически индуцированной астмы, особенно в одноразовой суточной дозировке, которая может повысить приверженность к лечению, что является важнейшей клинической проблемой терапии астмы, особенно у детей. Цилеутон является действенным пероральным ингибитором синтеза цистеинил-лейкотриеновых рецепторов и других метаболитов 5-липооксигеназы, образовавшихся в процессе метаболизма арахидоновой кислоты (см. табл. 14.4), оказывающим умеренный клинический эффект при лечении астмы.
Аналоги циклоспорина[править | править код]
Циклоспорин успешно применяют для лечения иммунных нарушений, связанных с лимфоцитозами. Недавно была доказана его клиническая эффективность в лечении астмы, резистентной к терапии глюкокортикостероидами. Сейчас оценивают побочные эффекты и проводят исследования с целью поиска менее опасного аналога этого лекарственного средства для лечения астмы.
Сейчас противовоспалительные средства применяют на более раннем этапе лечения астмы, чем раньше
С тех пор как стало принятым считать, что астма — хроническое воспалительное заболевание дыхательных путей, а не просто заболевание, связанное с бронхоконстрикцией, многие организации по всему миру, включая National Institutes of Health in the United States, ВОЗ и Canadian Thoracic Society, издали руководства по оптимальному лечению бронхиальной астмы. В основе лежит поэтапный метод лечения, но начинать противовоспалительное лечение следует гораздо раньше, чем считалось ранее, т.к. выявлен положительный эффект ранней терапии на течение болезни.
Побочные эффекты противоастматическнх лекарственных средств
- Агонисты β2-адренорецепторов могут вызвать судороги, длительное применение может ухудшить течение заболевания
- В черный список были включены лекарственные средства, содержащие агонисты β2-адренорецепторов, а именно сальметерол
- Ксантины вызывают тремор, тахикардию и раздражение желудочно-кишечного тракта
- Пероральные глюкокортикостероиды назначают только тем пациентам, которые нечувствительны к другим видам терапии, т.к. пероральные глюкокортикостероиды имеют широкий спектр побочных эффектов
- Аэрозольные глюкокортикостероиды вызывают меньше побочных эффектов, чем пероральные, в основном разрастание грибов Candida в полости рта и хрипоту
Хроническая обструктивная болезнь легких[править | править код]
Хронический бронхит и эмфизема часто встречаются у злостных курильщиков, подобное сочетание рассматривают как хроническую обструктивную болезнь легких. ХОБЛ в основном выявляют у курящих лиц в пожилом возрасте, но также может наблюдаться у молодых пациентов с генетическим дефицитом фермента а1-антитрипсина. Хронический бронхит характеризуется в функциональном плане как заболевание, связанное с повышенным отделением мокроты и дневным (или в основном дневным) кашлем. Обструкция дыхательных путей является результатом сужения их просвета и закупорки слизью, что может привести к вторичному возникновению инфекции (рис. 14.8). Обычно хронический бронхит вызывает альвеолярную гиповентиляцию, гиперкапнию и гипоксию, несмотря на то что некоторые больные дышат учащенно, чтобы избежать острой гипоксии. Возможно развитие вторичной легочной гипертензии, которая может привести к правосердечной недостаточности (легочное сердце). Для пациентов типичен продуктивный кашель, отхождение мокроты, экспираторная одышка и обструкция дыхательных путей. Часто присоединяется инфекция, которая утяжеляет течение болезни. У пациентов, курящих длительное время, может развиться эмфизема с деструктивным распадом альвеолярных структур и последующим нарушение газообмена. Пациенты с эмфиземой имеют не очень благоприятный прогноз, их дыхательная система малоэффективна. Не существует лекарственных средств, которые бы предотвратили или устранили эмфизему, только отказ от курения может остановить ее прогрессирование. Таких пациентов лечат симптоматически различными лекарственными средствами (см. далее), и им часто назначают распыленный кислород.
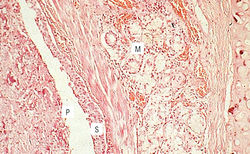
Рис. 14.8 Хронический бронхит. Аномальная гиперсекреция слизи, которая может вызвать закупорку дыхательных путей (Р). Гиперсекреция, связанная с гипертрофией и гиперплазией бронхиальных секретирующих желез (М). Рейд-индекс — пропорция для желез: толщина стенки бронха при хроническом бронхите увеличена. Воспаление обычно отсутствует, несмотря на то что повышенная продукция слизи связана с развитием последующих сопутствующих инфекций дыхательных путей, приводящих к вторичному воспалению. Сквамозная метаплазия (S) часто встречается у пациентов, имеющих хронические инфекции (предоставлено Alan Stevens, James Lowe).
Для лечения симптомов, связанных с хроническим бронхитом и эмфиземой, применяют бронходилататоры, мукокинетики и антибиотики.
Бронходилататоры[править | править код]
АГОНИСТЫ β-АДРЕНОРЕЦЕПТОРОВ. Агонисты β2-адренорецепторов (короткого и длительного действия) используют при лечении обструкции дыхательных путей и экспираторной одышке у пациентов с хроническим бронхитом и эмфиземой, но у таких пациентов они менее эффективны, чем при лечении астмы, т.к. в этом случае сокращение гладких мышц дыхательных путей не является основным компонентом бронхоконстрикции.
Агонисты β2-адренорецепторов длительного действия иногда также применяют в сочетании с ингалируемыми глюкокортикостероидами, несмотря на то что эффективность глюкокортикостероидов при ХОБЛ еще не доказана.
КСАНТИНЫ. Ксантины используют при лечении хронического бронхита, в особенности из-за их влияния на гладкие мышцы дыхательных путей. Они также влияют на ЦНС, приводя к повышенной возбудимости, что важно учитывать при хроническом бронхите, т.к. это может приводить к сокращению диафрагмы.
Мукокинетики[править | править код]
N-АЦЕТИЛЦИСТЕИН. N-Ацетилцистеин разрушает дисульфидные связи, которые связывают гликопротеины слизи, тем самым снижая ее вязкость. N-Ацетилцистеин и сходный препарат амброксол доказали свою эффективность в лечении ХОБЛ. Другие мукокинетики содержат гуайфенезин, йодид калия и обычную соль. Эрдостеин — муколитическое лекарственное средство, ингибитор эластазы; его используют при лечении ХОБЛ.
АНТАГОНИСТЫ МУСКАРИНОВЫХ РЕЦЕПТОРОВ. Антагонисты мускариновых рецепторов являются основными средствами лечения хронического бронхита, т.к. они снимают бронхоспазм, связанный с курением и вдыханием других раздражителей. Препараты также эффективны из-за их способности уменьшать секрецию слизи (они нейтрализуют действие ацетилхолина на мускариновые рецепторы) (см. рис. 14.6). Чаще всего для лечения пациентов с симптомами ХОБЛ используют тиотропия бромид — антагонист мускариновых рецепторов длительного действия.
Антибиотики[править | править код]
У пациентов с хроническим бронхитом часто возникает вторичная инфекция, колонизированная в мокроте. Таким больным обычно назначают антибиотики.
Ингибиторы фосфодиэстеразы-4[править | править код]
Недавние клинические исследования показали, что перорально активные селективные ингибиторы ФДЭ-4 рофлумиласт и циломиласт эффективны при терапии ХОБЛ. а1Антитрипсин назначают на начальных стадиях эмфиземы при его генетической недостаточности. Его также пытаются применять при лечении более поздних стадий заболевания.
Респираторный дистресс-синдром[править | править код]
Респираторный дистресс-синдром взрослых является острым, угрожающим жизни состоянием. Это происходит из-за слабо развитой капиллярной сети, что приводит к гипоксии, снижению объема легкого, пропитыванию альвеол и некардиогенному отеку легкого. Дистресс-синдром часто возникает у пациентов с сепсисом (50%). Смертность при этом синдроме составляет примерно 60-70%.
Современное лечение дистресс-синдрома остается недостаточным
Ни одно лекарственное средство не предотвращает наступление дистресс-синдрома и не снижает сопутствующую смертность. Но исследования, проведенные на животных, свидетельствуют об эффективности неотложного лечения, включающего моноклональные антитела против цитокинов, фактор активации тромбоцитов, фактор некроза опухоли и антагонисты рецепторов IL-1.
Существует также респираторный дистресс-синдром у новорожденных, не имеющих сурфактанта. На практике назначают несколько препаратов сурфактанта (содержат кальфактант и порактант альфа), которые применяют дог того момента, пока организм новорожденного не начинает вырабатывать свой собственный сурфактант.
Муковисцидоз[править | править код]
Муковисцидоз вызван мутациями в специфических белках, обеспечивающих апикальный клиренс Cl~
Муковисцидоз — наследственное заболевание, возникающее в раннем детстве. Поражает дыхательные пути и протоки некоторых органов, особенно легких, поджелудочной железы и потовых желез. У пациентов с муковисцидозом происходят мутации специфических белков, обеспечивающих апикальный клиренс С1" (рис. 14.9). Это приводит к нарушению клиренса С1~, повышенной реабсорбции натрия и, в результате, изменению осмотического давления и повышению реабсорбции воды. Дефект проявляется обильной вязкой секрецией в органах с протоками, особенно в дыхательных путях, а также протоках поджелудочной и потовых желез у гомозигот. В легких это приводит к увеличению областей со слабым кровотоком. Последующее присоединение инфекции (Staphylococcus aureus, Pseudomonas aeruginosa и другие микроорганизмы) приводит к необратимым изменениям в легких (бронхоэктазы). Аналогичный процесс, связанный с изменением секреции, происходит и в других органах.
Рис. 14.9 Патогенез муковисцидоза. (а) Мутации в специфическом белке, ответственном за Ch-канал эпителия респираторного тракта приводит к нарушениям клиренса С1~ и резорбции воды, (б) Это приводит к обильной и вязкой секреции в протоковых органах, которая сопровождается инфекцией. ДНК — дезоксирибонуклеиновая кислота; мРНК — матричная рибонуклеиновая кислота.
Мукокинетические препараты, антисекреторные препараты, антибиотики и физиотерапию применяют при лечении муковисцидоза
Предположительно продолжительность жизни людей с муковисцидозом гораздо меньше, но она может быть продлена с помощью интенсивной терапии лекарственными средствами и физиотерапией (табл. 14.5). Современная терапия легочных проявлений муковисцидоза заключается в:
- уменьшении секреции для поддержания сохранности просвета дыхательных путей и протоков;
- борьбе с оппортунистическими инфекциями.
Таблица 14.5 Возможные терапевтические подходы при лечении муковисцидоза
|
Проблема |
Подход |
|
Поврежденный ген |
Заменить |
|
Выработка мутированного белка |
Добавить |
|
Повышенная реабсорбция Na+ |
Экскретировать Na+ (амилорид) |
|
Застой мокроты |
Отхаркивающие лекарственные средства, муколитики, рекомбинантная ДНК, физиотерапия |
|
Бактериальная инфекция (Staphylococcus aureus, Pseudomonas aeruginosa) |
Антибиотики |
|
Необратимое повреждение легкого |
Трансплантация легкого |
Гнойная слизь при муковисцидозе имеет характерный желтый цвет и богата фрагментами ДНК (из мертвых клеток), которые были использованы для снижения секреции (см. далее).
Мукокинетические и антисекреторные лекарственные средства[править | править код]
Антагонисты мускариновых рецепторов снижают жидкую секрецию респираторного тракта, другие препараты повышают текучесть и снижают вязкость секрета:
- отхаркивающие лекарственные средства повышают текучесть секрета, тем самым улучшая продуктивность кашля. Типичные отхаркивающие лекарственные средства содержат гуайфенезин и назначают перорально или ментол и камфару и назначают ингаляционно, но их эффективность ограничена. Иодид калия обладает лучшими отхаркивающими свойствами;
- муколитики понижают вязкость секрета. N-ацетилцистеин разрушает дисульфидные связи в молекуле муцина, тем самым понижая вязкость, но могут возникать побочные эффекты, такие как тошнота, рвота, стоматит и ринорея;
- недавно была показана эффективность лечения муковисцидоза лекарственными средствами, разрушающими цепи ДНК (например, рекомбинантная ДНК в форме аэрозоля).
Антибиотики[править | править код]
Типичные бактерии, находящиеся в легких при муковисцидозе, — S. aureus (на ранней стадии заболевания) и P. aeruginosa, часто вызывают пневмонию. Основные антибиотики, используемые при лечении, — гентамицин, тобрамицин или амикацин совместно с одним из следующих лекарственных средств: ципрофлоксацином, тикарциллином, имипенемом, цефтазидимом и пиперациллином. Тобрамицин часто применяют в виде аэрозоля. Если легкое сильно повреждено, пациенту может быть проведена операция по трансплантации легкого.
Генетическая терапия находится на стадии разработки.
Кашель[править | править код]
Кашель является полезным рефлексом, но может потребовать лечения, если становится слишком сильным и изнуряющим
Кашель — распространенный респираторный симптом, возникающий и при других респираторных заболеваниях (например, при рините или астме). Иногда он связан с гастроэзофагеальным рефлюксом и прекращается после излечения первичного заболевания. Но иногда кашель появляется без причины или продолжается, несмотря на терапию первичного заболевания, включающую противокашлевую терапию. Кашель — рефлекс, вызываемый механическими или химическими раздражителями, воздействующими на верхние дыхательные пути, или вызываемый центральными стимулами (рис. 14.10). Это защитный механизм, который помогает удалить из дыхательных путей инородные тела и нежелательные вещества. Но иногда кашель становится неэффективным и изнуряющим и может психологически и физически раздражать пациента (табл. 14.6). В таком случае необходимо применять специфическую противокашлевую терапию.
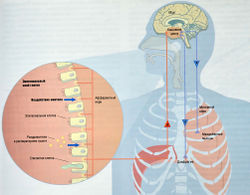
Кашель — рефлекторный механизм, включающий рефлекторную дугу (см. рис. 14.10) с рецептором, центральным и эфферентным компонентами. Недавно был найден кашлевой рецептор, но его природа остается неизвестной. Чувствительные нервы, при раздражении которых возникает кашель, находятся на участке от гортани до разделения сегментарных бронхов. Точный путь афферентных волокон и точная локализация «кашлевого центра» в ЦНС еще не известны, предположительно он включает ядро одиночного пути. Эфферентный путь кашлевого рефлекса включает межреберные и диафрагмальные нервы. Внезапное сокращение мышц дыхательных путей приводит к резкому повышению внутригрудного давления, которое выталкивает воздух из альвеол по дыхательным путям.
Рис. 14.10 Рефлекторная дуга кашля. Кашель может быть вызван механическими, химическими или центральными стимулами, а афферентные нервы; е — эфферентные нервы.
Рецепторные и центральные компоненты рефлекторной дуги являются субстратом для действия лекарственных средств, уменьшающих кашель
Лекарственные средства подавляют либо уменьшают:
- активацию рецептора и тем самым активность афферентных нервов;
- чувствительность «кашлевого центра».
Периферически действующие противокашлевые лекарственные средства[править | править код]
Некоторые лекарственные средства действуют периферически, понижая чувствительность кашлевых рецепторов к химическим раздражителям и аутакоидам, которые активируют рецепторы.
|
Таблица 14.6 Причины кашля | ||||
|
Механические |
Воспалительные |
Экстраторакальные |
Кашлевой рефлекс |
ЦНС |
|
Бронхит Пневмония Муковисцидоз и астма Опухоль, гранулемы, заболевания крови, отек Инородное тело |
Астма Вирусная инфекция Поллютанты АПФ Интерстициальные болезни |
Синдром постназального затекания Гастроэзофагеальный рефлюкс Воспаление среднего уха |
Вирусные инфекции Астма АПФ Идиопатические |
Психогенные |
|
АПФ — ангиотензинпревращающий фермент; ЦНС — центральная нервная система. [Fuller. Cough. In: Crystal and West. The Lung. New York: Raven Press; 1991]. | ||||
МЕНТОЛОВЫЕ ИНГАЛЯЦИИ. Ментоловые ингаляции понижают чувствительность периферических кашлевых рецепторов у животных. Возможно, то же наблюдается и у людей. Рассасывание леденцов с ментолом и эвкалиптом также снижает кашель.
МЕСТНЫЕ АНЕСТЕТИКИ. Местные анестетики, такие как бензокаин, бупивакаин или лидокаин, нанесенные на глотку и гортань, могут снизить чувствительность кашлевых рецепторов в этих областях к химическим или физическим стимулам. Их обычно применяют для снятия кашля, связанного с бронхоскопией, и у пациентов, рефрактерных к другой противокашлевой терапии.
БЕНЗОНАТАТ. Бензонатат применяют перорально; считается, что он влияет на периферические и центральные рецепторы. Возможно, он менее эффективен, чем кодеин (см. далее), и химически схож с локальным анестетиком тетракаином.
Центрально действующие противокашлевые лекарственные средства[править | править код]
Опиоиды являются лекарственными средствами, снижающими чувствительность дыхательного центра. Противокашлевый эффект морфина и кодеина проявляется за счет их блокирующего действия на опиоидные рецепторы в «кашлевом центре». Это действие отлично от других опиоидных эффектов. Кодеин обычно входит в состав противокашлевых микстур в некоторых странах, кроме США.
Декстрометорфан, являющийся d-изомером метилового эфира опиата, и леворфанол лишены обезболивающих свойств. Они эффективны в качестве супрессора кашля, как кодеин, но в очень больших дозах могут вызвать угнетение ЦНС.
Хлофедианол менее эффективен, чем кодеин. Большие дозы могут оказывать влияние на ЦНС, приводя к возбуждению и ночным кошмарам.
Ринит и ринорея[править | править код]
Ринит и ринорея — признаки воспаления слизистой оболочки носа
Ринит — острое или хроническое воспаление слизистой носа. Ринорея характеризуется повышенной секрецией экссудата в полости носа. Оба заболевания могут быть результатом:
- вирусных инфекций слизистой оболочки носа;
- взаимодействия между антигенами и иммуноглобулинами Е на слизистой оболочке носа.
Эти взаимодействия приводят к повышенному кровоснабжению слизистой оболочки носа и/или увеличивают проницаемость сосудов. В результате объем слизистой оболочки увеличивается, а дыхание через нос затрудняется.
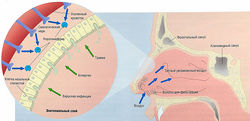
Кровь по сосудистым коллатералям и венозным синусам поступает к слизистой оболочке, чтобы поддерживать ее в теплом и влажном состоянии. Важнейшим физиологическим механизмом, контролирующим носовое кровообращение, является тонус симпатической нервной системы; также играют определенную роль аутакоиды (рис. 14.11). Активация симпатических нервов уменьшает проявления ринита и ринореи, очищает носовые ходы и облегчает дыхание. Симпатолитики (агонисты адренергических нейронов и антагонисты а-адренорецепторов) могут вызвать заложенность носа. Напротив, агонисты а1адренорецепторов приводят к вазоконстрикции, поэтому их применяют при лечении симптомов ринита (см. далее).
Рис. 14.11 Механизмы ринита и ринореи. Симпатическая нервная система является важнейшим контролирующим механизмом, регулирующим усиленный кровоток слизистой носа. Жидкая гиперсекреция может появиться в ответ на различные стимулы.
Антагонисты Н1рецепторов (антигистаминные лекарственные средства), противовоспалительные препараты и назальные вазоконстрикторы используют при лечении ринита и ринореи
Существует множество субстратов, на которые действуют препараты для купирования ринита и контроля ринореи (табл. 14.7). В идеале нужно контролировать причину, вызывающую ринит, но не существует эффективного лечения против вирусов, поэтому лечение симптоматическое. При аллергических реакциях высвобождаются аутакоиды, такие как гистамин и цистеинил-лейкотриены, которые влияют на слизистую оболочку носа. Гистамин может вызывать чихание и зуд.
Табяица 14.7 Мишени лекарственных средств при лечении ринита и ринореи
|
Мишень |
Лекарственные средства |
|
Назальный кровоток |
Вазоконстрикторы |
|
Воспаление |
Глюкокортикостероиды |
|
Угнетение высвобождения медиаторов воспаления |
Кромолин-натрий |
|
Омализумаб | |
|
Блокада медиаторных рецепторов |
Антагонисты Н1-рецепторов |
|
Антагонисты лейкотриенов |
Контролировать симптомы ринита можно несколькими способами:
- воспалительную реакцию можно снизить нанесением глюкокортикостероидов в форме спрея прямо на слизистую оболочку носа;
- предотвратить взаимодействие антител в результате высвобождения аутакоидов путем использования препаратов против иммуноглобулина Е (омализумаб);
- кромолин-натрий можно нанести на слизистую оболочку носа с целью ингибирования высвобождения гистамина и других аутакоидов из тучных клеток и других клеток воспаления.
Гиперсекреторную фазу ринита можно предотвратить или уменьшить использованием вазоконстрикторов и агонистов а-адренорецепторов (симпатомиметиков).
Антагонисты Н1 рецепторов[править | править код]
Самым главным аутакоидом, высвобождаемым в слизистой оболочке носа, является гистамин, который влияет на Н1рецепторы слизистой оболочки. Антагонисты Н1рецепторов (см. главу 9) используют при лечении аллергического ринита. Чаще всего применяют цитиризин, дезлоратадин, фексофенадин, эбастин, олопатадин. Нельзя не упомянуть об участии Н2-рецепторов, но нет данных, что антагонисты Н2-рецепторов эффективны при аллергическом рините, несмотря на то что вазодилатация при рините может иметь и Н2-зависимый компонент.
Противовоспалительные препараты[править | править код]
ГЛЮКОКОРТИКОСТЕРОИДЫ. Глюкокортикостероиды проявляют противовоспалительную активность, но вызывают множество побочных эффектов, в том числе сильное угнетение иммунной системы, обострение инфекций и угнетение адренокортикальных связей. Эти побочные эффекты наблюдаются в основном при пероральном применении (см. главу 11). Большинство этих побочных эффектов можно предотвратить, если препараты использовать местно и в малых дозах. Но в этом случае возможно местное угнетение иммунной реакции, что может привести к присоединению локальной инфекции.
Наиболее часто используемые глюкокортикостероиды, наносимые местно на слизистую оболочку носа: триамцинолон, беклометазона дипропионат, будесонид и флутиказон, которые регулярно впрыскивают с помощью аэрозоля в носовые ходы.
КРОМОЛИН-НАТРИЙ. Кромолин-натрий угнетает высвобождение аутокоидов из клеток воспаления, вовлеченных в аллергическую реакцию (см. главу 9). Его используют для снижения зуда и чихания, связанных с ринитом, и выпускают в виде суспензий, которые необходимо наносить местно на слизистую оболочку носа, используя аэрозольный распылитель. Длительный антиаллергический эффект может быть получен в течение месяца при приеме препарата омализумаб (антииммуноглобулина Е).
Противоотечные симпатомиметики[править | править код]
Воспалительные и гиперсекреторные процессы в слизистой оболочке носа вызывают активную вазодилатацию. Контролировать гиперсекрецию (что приведет к снижению вазодилатации) можно назначением агонистов а1адренорецепторов. Эти вещества действуют на а1адренорецепторы слизистой оболочки носа, уменьшая ее объем и затруднения движению воздуха. Это приводит к активации рецепторов на венозной сети сосудов. Активация а1 и, возможно, а2-адренорецепторов в питающих артериях может привести к вазоконстрикции этих сосудов, и, вероятно, повредит слой слизистой оболочки. Агонисты а1адренорецепторов начали использовать в качестве противоотечных назальных препаратов еще до того, как были выделены подтипы а1адренорецепторов. Попытки оценить селективные агонисты и их эффективность как противоотечных средств могут принести пользу.
Агонисты а1адренорецепторов при приеме внутрь вызывают выраженную назальную вазоконстрикцию и снятие отека, но происходит генерализованное сужение всех сосудов и повышается артериальное давление. Тем не менее, такие лекарственные препараты, как фенилэфрин, входят в состав некоторых пероральных микстур для лечения ринита и ринореи.
Антагонисты лейкотриеновых рецепторов, такие как монтелукаст, эффективны в лечении аллергического ринита.
Срочные лекарственные средства[править | править код]
Селективный ингибитор ФДЭ-4 рофлумиласт показал свою эффективность в срочном лечении ринита.
Респираторные инфекции[править | править код]
Теплая и влажная среда дыхательного пути, выстланного эпителиальной тканью, контактирует с вдыхаемыми микроорганизмами: вирусами, бактериями, грибами и паразитами (см. рис. 14.1).
Наиболее распространенные инфекции дыхательных путей вызваны вирусами и бактериями. Некоторые инфекции относительно безобидны (например, простуда), в то время как другие могут быть угрозой для жизни (например, вирусная или бактериальная пневмония). Та легкость, с которой инфекция проникает в респираторный тракт, зависит от состояния здоровья человека. Например, легочные инфекции, вызванные Pneumocystis carinii, характерны для больных СПИДом. Кроме того, некоторые микроорганизмы могут проникать лишь в определенные части респираторного тракта.
Таблица 14.8 Факторы, обусловливающие использование антибиотиков
- Клинические проявления инфекции
- Вид инфекционного агента и его риск для пациента
- Чувствительность микроорганизма к антибиотикам
- Вероятность возникновения резистентности
- Усвоение препарата организмом
- Пригодность эффективного антибиотика
- Побочные эффекты эффективного антибиотика
- Фармакодинамика и фармакокинетика
- Фармакоэкономика
Антибиотики
- Антибиотики не рекомендуется использовать при лечении вирусных заболеваний респираторного тракта
- Различные антибиотики действуют на разные стадии роста и развития бактерий
- Сочетание антибиотиков может быть синергичным и препятствовать развитию резистентности бактерий
- Полный курс антибиотикотерапии должен быть завершенным, иначе может развиться антибиотикорезистентность
Полость легких подвергается заражению бактериями, вирусами и грибами. Вирусные инфекции, как правило, самоограничены, но делают ткань чувствительной для бактерий и грибов. Candida albicans полости рта является наиболее распространенной грибковой инфекцией и развивается при угнетении иммунного статуса (например, системная иммуносупрессия или применение аэрозолей, содержащих глюкокортикостероиды, при лечении астмы).
Антибиотики могут привести к развитию микробной резистентности
Несмотря на то что многие инфекции респираторного тракта самоограничены и вызывают небольшие повреждения, другие могут привести к серьезным последствиям и снизить жизненную емкость легких. Неправильное использование антибиотиков при лечении легочной бактериальной инфекции (табл. 14.8) создает риск как для пациента, так и для общества, поскольку появляется возможность развития антибиотикорезистентности. В отсутствие угрожающих жизни инфекций выбор антибиотика основан на виде атакующего агента и на его чувствительности к антибиотикам.
Микроорганизм необходимо культивировать и определить его чувствительность к антибиотикам. Некоторые микроорганизмы имеют такие характерные особенности, что клинический диагноз и выбор лечения может быть основан только на клинических симптомах.
Существование целого ряда антибиотиков со схожими свойствами привело к появлению концепции терапии первой, второй и третьей линии, основанной на селективности и специфичности различных бактерий. Терапия первой линии включает препараты первого выбора. Препараты второй линии используют в том случае, если препараты первой линии были неэффективны или пациент их не переносит.
Антибиотики, используемые для отдельных инфекций респираторного тракта[править | править код]
ЭПИГЛОТТИТ. Для лечения эпиглоттита, опасного для жизни, вызванного Haemophilus influenzae (тип В) используют дериваты цефалоспорина (цефуроксим, цефотаксим, цефтриаксон). Хлорамфеникол назначают в качестве лекарственного препарата второй линии. Он достаточно эффективный препарат, но может вызвать фатальную апластическую анемию (1 : 30 ООО случаев).
ФАРИНГИТ. Не существует эффективных лекарственных средств для лечения заболевания, вызванного вирусами, но стрептококки группы А могут вызвать тяжелейшие инфекции. При этом пенициллины (особенно пенициллин V) относят к антибиотикам первой линии. Эритромицин является препаратом второй линии, а цефалексин — препаратом третьей линии (табл. 14.9).
ЛАРИНГИТ И ОСТРЫЙ РИНИТ. Ларингит и острый ринит — частые вирусные инфекции, которые обычно не лечат, но вторичные бактериальные инфекции необходимо лечить антибиотиками. Антибиотики, предназначенные для лечения вирусных инфекций верхних дыхательных путей, в клинической практике назначают редко из-за риска развития резистентности микроорганизмов.
СИНУСИТ. Многие взрослые подвержены синуситам, которые вызывают Streptococcus pneumoniae, Н. influenzae, Micrococcus catarrhalis, стрептококки, грамотрицательные бациллы, анаэробы и респираторные вирусы. Амоксициллин при этом заболевании является антибиотиком первой линии, а триметоприм/сульфаметоксазол, рифампицин, це-фуроксима аксетил, цефаклор, цефиксим и амоксициллин/клавуланат — второй линии. Триметоприм, доксициклин и кларитромицин — третьей линии.
Таблица 14.9 Лекарственные средства для лечения бактериального фарингита
|
Инфекция |
Стрептококк группы А | ||
|
Терапия первой линии |
Терапия второй линии |
Терапия третьей линии | |
|
У взрослых |
Пенициллин V |
Эритромицин |
Цефалексин, кларитромицин |
|
У детей |
Пенициллин V, амоксициллин, пивампициллин |
Эритромицина эстолат |
Цефалексин |
Детям с острым синуситом без перфорации, вызванным S. pneumoniae, Н. influenzae, М. catarrhalis, стрептококками группы A, Staphylococcus aureus, грамотрицательными бациллами или анаэробами, назначают амоксициллин и пивампициллин в качестве средства первой линии, триметоприм/сульфаметоксазол и цефуроксима аксетил — второй линии, триметоприм и кларитромицин — третьей линии.
БРОНХИТ. Не существует эффективной терапии вирусных заболеваний бронхов. Инфекцию бактериального происхождения лечат следующим образом:
- если бронхит средней тяжести и вызван Mycoplasma pneumoniae, S. pneumoniae, Chlamydia pneumoniae, то антибиотиками первой линии являются тетрациклин и эритромицин. Антибиотиками второй линии — доксициклин и кларитромицин;
- если у взрослого бронхит слабой или умеренной степени (обострение хронического бронхита) и он вызван S. pneumoniae, Н. influenzae, М. catarrhalis или М. pneumoniae, антибиотиками первой линии являются тетрациклин, триметоприм/сульфаметоксазол и амоксициллин, антибиотиками второй линии — доксициклин, цефуроксима аксетил, цефаклор, амоксициллин/клавуланат и кларитромицин;
- если бронхит сопровождается умеренным или сильным воспалением легких, вызванным S. pneumoniae, Н. influenzae, М. catarrhalis или М. pneumoniae, антибиотиками первой линии являются тримето-прим/сульфаметоксазол, цефаклор, цефуроксима аксетил, амоксициллин/клавуланат и любой из перечисленных. Антибиотиками второй линии — флоксациллин и ципрофлоксацин;
- если имеется обострение хронического бронхита в форме бронхоэктазов и инфекция вызвана S. pneumoniae, Н. influenzae, М. catarrhalis или P. aeruginosa, антибиотиками первой линии являются тетрациклин и триметоприм/сульфаметоксазол, антибиотиками второй линии — флоксациллин, ципрофлоксацин, цефаклор, цефуроксима аксетил, амоксициллин/клавуланат или любой из перечисленных в комбинации с эритромицином или кларитромицином.
ПНЕВМОНИЯ. Пневмония — воспаление инфекционного происхождения легочной ткани (в частности альвеол и маленьких бронхиол) с вовлечением плевры (плеврит). Данное заболевание может возникать при различных обстоятельствах, соответственно им выбирают терапию (табл. 14.10).
При бронхопневмонии первичная инфекция сконцентрирована в бронхах и распространяется на соседние альвеолы, которые заполняются острым воспалительным экссудатом. Поврежденные области легкого сливаются. Сначала повреждение затрагивает только сегменты, но если не проводить лечение, то очаг поражения захватывает целые доли. Это заболевание часто встречается у маленьких детей и пожилых людей. К факторам риска относят слабость и акинезию. Акинезия приводит к застою секрета, который под действие силы тяжести оседает в легком и происходит инфицирование; бронхопневмония чаще всего поражает нижние доли. Заболевание возникает при наличии предрасположенности к инфицированию вследствие обстоятельств.
При бронхопневмонии поврежденные макроскопические области легкого плотные, безвоздушные и имеют бурую окраску. Гной также может быть и в периферических бронхах. Гистологически в бронхах происходит острое воспаление, альвеолы содержат острый воспалительный экссудат. Когда в процесс вовлекается плевра, развивается плеврит. После лечения на пораженном месте развивается фиброз. Частые осложнения при пневмонии: легочный абсцесс, плевральная инфекция и септицемия.
КОКЛЮШ. Коклюш — заболевание, вызываемое Bordetella pertussis, от которого детей вакцинируют. Эритромицин (для детей предпочтителен эстолат) является антибиотиком первой линии, триметоприм/сульфаметоксазол — второй линии, а тетрациклин, амоксициллин и ампициллин — третьей линии.
Туберкулез[править | править код]
Туберкулез — широко распространенное в мире инфекционное заболевание, вызываемое различными видами микобактерий. Туберкулезная инфекция Mycobacterium tuberculosis (палочка Коха) чаще всего встречается в бедных и густонаселенных регионах мира. В связи с развитием мировой экономики, а также улучшением гигиены количество случаев туберкулеза, особенно в развитых странах, во вторую половину XX в. значительно снизилось, но в последнее время участились случаи туберкулезной инфекции и опасность данного заболевания возросла. Рост заболеваемости связан со СПИДом и развитием резистентности микобактерий к ранее эффективным препаратам.
М. tuberculosis может поражать не только легочную ткань, но и мозг и кишечник, при этом микобактерию можно обнаружить в казеозных полостях и макрофагах. Часто туберкулез самоограничивается, но микобактерия сохраняется в неактивном состоянии в кальцифицированных областях. Это предотвращает распространение инфекции, но усложняет доступ лекарственных средств к микобактериям. Существует риск последующего разрыва в месте, где персистирует микобактерия, и возобновления инфекции. Сложность заключается еще и в том, что лекарственные средства эффективны только против активно растущих микобактерий. Терапию можно продолжать от 9 до 18 мес и комбинировать с другими препаратами. Следует проводить профилактическую терапию людям, которые контактировали с больными в острой фазе заболевания. Главной целью лечения является достижение минимального риска рецидива (в идеале < 5%).
Лечение туберкулеза
- Терапией первой линии является комбинация рифампицина, изониазида и пиразинамида
- Лечение обычно длится 6 мес, прием пиразинамида может быть продолжен еще на 2 мес
Противотуберкулезные лекарственные средства
- Микобактерии быстро приобретают резистентность к лекарственным средствам
- Основными противотуберкулезными препаратами являются изониазид, рифампицин, стрептомицин, этамбутол и пиразинамид
- При лечении туберкулеза следует комбинировать лекарственные средства
Для детального изучения лекарственных средств, используемых при лечении туберкулеза; см. Противотуберкулезные средства (антимикобактериальные).
Говоря кратко, различные комбинации лекарственных средств применяют на протяжении длительного периода. Основными препаратами при лечении нерезистентного туберкулеза являются изониазид, рифампицин, этамбутол, пиразинамид и стрептомицин. Другие препараты содержат в своем составе капреомицин, циклосерин, этионамид и парааминосалициловую кислоту.
Гиперчувствительный пневмонит[править | править код]
Гиперчувствительный пневмонит (аллергический альвеолит) — это лимфоцитарный и гранулематозный интерстициальный пневмонит, вызванный реакциями гиперчувствительности типа III и IV на повторное вдыхание некоторых антигенов. Заболевание, носящее название «легкое фермера», развивающееся в результате повторного вдыхания пыли, которая содержит актиномицеты, является прототипом гиперчувствительного пневмонита. Такую реакцию вызывают термофильные актиномицеты, грибы или белки животного происхождения, вдыхаемые в больших количествах.
Гиперчувствительный пневмонит характеризуется появлением кашля, лихорадки и озноба, недомоганием, диспноэ у ранее сенсибилизированных лиц (через 6-8 час после контакта с антигеном), появляется крепитация при аускультации, отдельные или диффузно расположенные инфильтраты на снимках легких. Страдает функция легких, снижается их объем и объем диффузии и развивается гипоксемия. В ответ на введение антигена наблюдаются нейтрофилия и повышенное содержание С-реактивного белка. В сыворотке больных гиперчувствительным пневмонитом присутствуют перцептивные антитела против антигена, при этом повышено содержание Т-клеток в бронхоальвеолярной жидкости (в основном CD8+ Th-клетки). У пациентов с очень выраженным ответом может быть повышен уровень CD4+ Тс-клеток.
ЛЕЧЕНИЕ. Наиболее эффективное лечение гиперчувствительного пневмонита заключается в прекращении действия антигена и факторов загрязнения окружающей среды. Может помочь контроль за количеством пыли и использование масок. Препаратами выбора являются глюкокортикостероиды, которые значительно снижают легочный воспалительный процесс.
Аллергический бронхолегочный аспергиллез[править | править код]
Аллергический бронхолегочный аспергиллез возникает у больных астмой и является эозинофильной пневмонией, возникающей в ответ на Aspergillus fumigatus. A. fumigatus растет в бронхах и вызывает аллергическую реакцию дыхательных путей и паренхимы. В патогенез данного заболевания вовлечены реакции гиперчувствительности типов I и III (и, возможно, типа IV). Гистопатологические исследования подтвердили, что в паренхиме при этом заболевании присутствуют эозинофильные инфильтрации в области бронхов, а также плазматические клетки и моноциты. Аллергический бронхолегочный аспергиллез характеризуется наличием бронхиальной астмы, легочными инфильтратами, продукцией мокроты, эозинофилией крови, положительным кожным тестом, наличием антител к A. fumigatus и повышенным уровнем общего (и специфичного) иммуноглобулина Е.
ЛЕЧЕНИЕ. Лечение проводят глюкокортикостероидами и другими противоастматическими лекарственными средствами (теофиллин, агонисты бета2адренорецепторов). Они снижают воспалительный процесс и осуществляют освобождение дыхательных путей от закупорки слизью и от A. fumigatus. Глюкокортикостероиды снижают уровень иммуноглобулина Е в сыворотке, и инфильтраты в легком исчезают. Длительное назначение преднизона (7,5-15 мг/сут) может быть эффективно при необратимом тяжелом заболевании. Ингаляции бекломета-зона дипропионата также эффективны. Антимикотические лекарственные средства неэффективны при снятии воспалительного процесса. Иммунотерапия с сывороткой, содержащей A. fumigatus, имеет двойственный эффект (местные реакции и обострение симптомов).
Легочная эмболия[править | править код]
Помимо участия в газообмене большая часть легочных сосудов также служит фильтром крови, поскольку является единственной капиллярной сетью, несущей венозную кровь, и обладает уникальной возможностью задерживать твердые частицы, которые могут попасть в артериальный кровоток. Микрофильтрация происходит, вероятно, регулярно, но в некоторых случаях может возникать легочная эмболия, что может привести к значительным изменениям в легочной и сердечной функции и даже к смерти. Венозная тромбоэмболия провоцирует в США 140 ООО смертей в год. Существуют также лица с хроническим легочным сердцем в результате отсутствия лечения эмболии.
Целью лечения венозной тромбоэмболии является предотвращение рецидивов, а также летального исхода вследствие легочной эмболии. Гепарин используют в дозах, скорректированных для поддержания времени свертывания крови на терапевтическом уровне (см. главу 10). Лечение гепарином, как правило, длится 5-10 сут и его обычно сочетают с варфарином для перорального применения. Сейчас в лечении венозной тромбоэмболии широко применяют низкомолекулярный гепарин вместо нефракционного гепарина из-за преимуществ первого: не нужен контроль вводимой дозы, вводят подкожно, тем самым не создавая риска геморрагии. Анализ некоторых исследований показал, что профилактическое лечение антитромбоцитарными препаратами (см. главу 10) уменьшает вероятность возникновения тромбоза глубоких вен и легочной эмболии.
Легочная гипертензия[править | править код]
Первичная легочная гипертензия — редкое состояние, вторичная легочная гипертензия возникает чаще вследствие разрушения соединительной ткани, легочной эмболии, ХОБЛ, фиброза легкого и из-за приема лекарственных средств, снижающих аппетит (например, аминорекса фумарата или дексфленфлурамина гидрохлорида).
Сосудорасширяющие лекарственные средства[править | править код]
Легочную гипертензию лечат прежде всего вазодилатирующими лекарственными средствами (до сих пор не установлен оптимальный сосудорасширяющий препарат). При лечении первичной легочной гипертензии лучшими блокаторами кальциевых каналов считают нифедипин и дилтиазем (см. главу 13). Эти сильнодействующие препараты помогают выявить пациентов, для которых будет эффективной долговременная терапия вазодилататорами.
У нифедипина и дилтиазема относительно большой период полувыведения (12 час), но при приеме данных лекарственных средств возникают серьезные побочные эффекты (системная вазодилатация и гипотензия) и в первую очередь страдают сосуды. Если блокаторы кальциевых каналов неэффективны, следует начать внутривенное введение эпопростенола (простациклина, простагландина 12).
У ПГ12 период полувыведения 3 мин, что делает его идеальным для предотвращения симптомов легочной гипертензии. ПГ12 вводят на протяжении длительного времени, поэтому такую терапию считают достаточно дорогостоящей. ПГ12 также имеет множество побочных эффектов (системная гипертензия, тошнота, головная боль, лихорадка, боль в области живота), которые исчезают при понижении вводимой дозы. Кроме того, ПГ12 ингибирует агрегацию тромбоцитов, поэтому во время лечения в месте введения могут появиться кровоподтеки и кровотечения.
Подобных побочных эффектов можно избежать, вводя ПП2 в форме аэрозоля (путем вдыхания). ПГ12 вводят из расчета 1 нг/кг/мин и увеличивают до 1-2 нг/кг/мин до появления положительного эффекта или побочных эффектов, при этом максимальная доза для взрослых может составлять 12 нг/кг/мин. Активные пероральные ПГ12, такие как аналоги илопроста и берапроста, доказали свою клиническую эффективность при лечении легочной гипертензии. Агонист простациклинового рецептора трепростинил натрия эффективен при подкожном введении. Трепростинил натрия имеет меньшее, по сравнению с эпопростенолом, количество побочных эффектов, его применяют для лечения более слабых форм легочной гипертензии. Трепростинил подвергается печеночному метаболизму и имеет период полувыведения 2-4 час, что является главным его преимуществом перед эпопростенолом. Можно обеспечить длительное введение трепростинила путем введения под кожу с помощью катетера внутрикожного мини-насоса.
Ингалируемый NO также применяют при лечении легочной гипертензии благодаря эффекту релаксации легочных сосудов. Он имеет огромное преимущество перед остальными вазодилататорами, т.к. оказывает минимальное воздействие на другие сосуды. Он дешев, начинает действовать быстро (и быстро распадается в присутствии кислорода), имеет минимальные побочные эффекты. Необходимо предусмотреть систему дозированной доставки газа и следить за состоянием окружающего воздуха при проведении терапии, т.к. некоторые метаболиты NO, такие как N02, токсичны.
Аденозин — еще один вазодилататор, повышающий содержание цАМФ в сосудах гладких мышц. Он может быть эффективен для лечения первичной легочной гипертензии. Аденозин имеет очень короткий период полувыведения (10 сек) и дешевле ПГ12, но вызывает значительное расширение коронарных сосудов и понижает системное сосудистое сопротивление.
Кислород — селективный легочный вазодилататор, применяемый для лечения всех пациентов с легочной гипертензией, испытывающих гипоксию в покое или десатурацию при нагрузке. Особенно это важно для пациентов с повышенным давлением в легочной артерии вследствие ХОБЛ. Терапия кислородом 15-17 час/сут значительно снижает смертность и прогрессирование болезни у пациентов с ХОБЛ. Этот селективный эффект кислорода заключается в предотвращении вазоконстрикции в ответ на дыхательную гипоксию.
Другие лекарственные средства, используемые для лечения легочной гипертензии[править | править код]
Сердечные гликозиды, такие как дигоксин, широко используют при лечении легочной гипертензии, несмотря на то, что еще точно не установлено, какую пользу они приносят. Симптоматическое положительное влияние оказывает также сублингвальный изопротеренол, а также дофамин и добутамин предположительно эффективны при остром ухудшении функции правого желудочка. Диуретики эффективны при сердечной недостаточности, т.к. они снижают преднагрузку на правый желудочек и снимают отеки, связанные с легочной гипертензией, хотя неизвестно, оказывают ли они влияние на продолжительность жизни. Активный пероральный антагонист рецепторов эндотелия бозентан также используют при лечении легочной гипертензии. Недавние исследования показали, что ингибитор ФДЭ-5 силденафил также может оказывать положительный эффект при лечении легочной гипертензии.
Побочные эффекты лекарственных средств для лечения респираторных заболеваний[править | править код]
Антагонисты β-адренорецепторов[править | править код]
Антагонисты β2-адренорецепторов, такие как пропранолол, который блокирует β2-адренорецепторы, противопоказаны пациентам с бронхиальной астмой, т.к. они вызывают бронхоконстрикцию, которая может привести к летальному исходу. Этот побочный эффект возникает на фоне изменения циркулирующего эпинефрина и/или иннервации ганглиев симпатических нервов, что ингибирует тонус блуждающего нерва и сужает просвет дыхательных путей. Антагонисты β-адренорецепторов в форме глазных капель также могут вызвать угрожающие жизни приступы астмы; все антагонисты β-адренорецепторов при астме противопоказаны.
Побочные эффекты лекарственных средств для лечения респираторных заболеваний (кроме астмы и инфекции)
- Мукокинетики имеют сравнительно небольшие побочные эффекты
- Опиоиды подавляют только кашель, имея при этом значительные побочные эффекты (например, злоупотребление препаратами, социальная изоляция)
Побочные эффекты антибиотиков
- Основной побочный эффект пенициллина и цефалоспорина — аллергия
- Основной побочный эффект аминогликозидов — почечная токсичность
- Основные побочные эффекты сульфонамидов — аллергия и светочувствительность кожи
- Побочные эффекты противотуберкулезных лекарственных средств зависят от препаратов
Ингибиторы ангиотензинпревращающего фермента[править | править код]
Ингибиторы ангиотензинпревращающего фермента, такие как каптоприл и эналаприл, применяют при лечении гипертензии и застойной сердечной недостаточности. Так, каптоприл может уменьшить кашель у некоторых пациентов с сопутствующими аллергическими заболеваниями дыхательных путей. Считается, что его механизм действия заключается в локальной выработке брадикинина, т.к. ингибиторы ангиотензинпревращающего фермента ингибируют пептидил-пептидазные ферменты, вовлеченные в метаболизм брадикинина, а также ингибируют превращение ангиотензина I в ангиотензин II. Концентрация брадикинина в легких может повышать и стимулировать афферентные рецепторы, вызывающие кашель. Такой кашель эффективно лечат кромолином натрия, но самым лучшим лечением является, конечно, исключение ингибиторов ангиотензинпревращающего фермента.
Нестероидные противовоспалительные средства[править | править код]
Примерно 20% больных астмой могут отреагировать бронхоконстрикцией в ответ на введение НПВС. Этот механизм не до конца изучен, но может быть связан с выработкой липооксигеназой метаболитов арахидоновой кислоты, т.к. такой бронхоспазм снимают ингибиторами 5-липооксигеназы и антагонистами цистеинил-лейкотриеновых рецепторов.
Читайте также[править | править код]
- Дыхательная функция
- Респираторная система
- Искусственное дыхание
- Пневмоторакс
- Объем легких и его измерение
- Связывание и транспорт кислорода в крови
- Гипоксия
- Контроль и стимуляция дыхания
- Дыхание при подводном плавании
- Дыхание в условиях высокогорья
Литература[править | править код]
- Barnes PJ. Novel signal transduction modulators for the treatment of airway diseases. Pharmacology & Therapeutics 2006; 109: 238-245. [A perspective on emerging treatment strategies].
- Berti I, Longo G, Visintin S et al. Treatment of mild asthma. N Engl J Med 2005; 353: 424-442.
- Boushey HA, Sorkness CA, King TS et al. The national heart, lung, and blood institute’s asthma clinical research network. Daily versus as-needed corticosteroids for mild persistent asthma. N Engl J Med 2005; 352: 1519-1 528.
- Cazzola M, Matera MC, Page CP. Novel approaches for the treatment of pneumonia. Trends Pharmacol Sci 2003; 29: 306-318.
- Dinwiddie R. Anti-inflammatory therapy in cystic fibrosis. Journal of Cystic Fibrosis 2005, 4(Suppl 2): 45-48.
- Griffiths MJD, Evans TW. Drug therapy: inhaled nitric oxide therapy in adults. N Engl J Med 2005; 353: 2683-2695.
- Leath TM, Singla M, Peters SP. Novel and emerging therapies for asthma. Drug Discovery Today 2005; 10: 1647-1655.
- Minasian C, McCullagh M, Bush A. Cystic fibrosis in neonates and infants. Early Human Development 2005; 81: 997-1004.
- Page CP, O’Connor B, Spina D (eds) Drugs for the Treatment of Respiratory Diseases, Cambridge: Cambridge University Press; 2003. [An account of drugs used in the treatment of respiratory diseases.]
- Reynolds SM, Mackenzie AJ, Spina D, Page CP. Pharmacology of cough. Trends Pharmacol Sci 2004; 25: 569-576. [An overview of the pharmacology of cough.]
- Sears MR, Greene JM, Willan AR et al. A longitudinal, population-based, cohort study of childhood asthma followed to adulthood. N EnglJ Med 2003; 349: 1414-1422.
- Sutherland ER, Cherniack RM. Current concepts: management of chronic obstructive pulmonary disease. N Engl J Med 2004; 350: 2689-2697.
- Thomas CF Jr, Limper AH. Medical progress: pneumocystis pneumonia. N Engl J Med 2004; 350: 2487-2498.