Препараты, влияющие на иммунитет
Источник:
Клиническая фармакология по Гудману и Гилману том 3.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Средства, влияющие на иммунную систему[править | править код]
Эта статья начинается с краткого обзора механизмов иммунного ответа, без знания которых нельзя понять, как действуют иммуномодуляторы. Обсуждение основ иммуносупрессивной терапии включает описание вероятных механизмов действия, основных показаний и возможного побочного действия четырех основных классов иммунодепрессантов: глюкокортикоидов (см. Кортикостероиды), ингибиторов кальциневрина, цитостатиков, включая антиметаболиты, и антител. Заветная цель иммуносупрессивной терапии — создание и поддержание специфической иммунологической толерантности, то есть активного состояния нечувствительности к определенным антигенам. В главе обсуждаются также способы преодоления таких нежелательных последствий иммуносупрессии, как высокий риск инфекционных заболеваний и злокачественных новообразований. Среди этих новых направлений — блокада костимуляции Т-лимфоцитов, индукция донорского химеризма, введение растворимых антигенов HLA и других толерогенов. И в завершение приводятся общие сведения о некоторых иммуностимуляторах, об активной и о пассивной иммунизации. Новые подходы в иммунотерапии не только направлены на повышение эффективности и снижение токсичности препаратов, но и будут иметь важные экономические последствия и отразятся на качестве жизни.
Иммунный ответ[править | править код]
Появление иммунной системы обусловлено необходимостью распознавания своего и чужого. Многоклеточные организмы должны уничтожать возбудителей инфекций или вышедшие из-под контроля опухолевые клетки без вреда для нормальных клеток. Для этого существует надежная система распознающих и эффекторных механизмов, обеспечивающих разные виды иммунитета. Механизмы неспецифического иммунитета достаточно примитивны, он не требует предварительной активации, а его эффекторы обладают низким сродством к чужеродному и широким спектром действия. Напротив, специфический иммунитет направлен на определенные антигены, нуждается в предварительной активации, а его эффекторы могут иметь очень высокое сродство к антигенам. На первых этапах зашиты от чужеродного действует в основном неспецифический иммунитет, и лишь со временем начинает преобладать специфический иммунный ответ. К основным факторам неспецифического иммунитета относятся комплемент, гранулоциты (включая базофилы), моноциты, макрофаги, NK-лимфоциты и тучные клетки. Специфический иммунный ответ осуществляется В- и Т-лимфоцитами. В-лимфоциты вырабатывают антитела, а Т-лимфоциты действуют как вспомогательные (Т-хелперы), цитолитические (Т-киллеры) и регуляторные (Т-супрессоры) клетки. Эти клетки не только обеспечивают нормальный иммунный ответ на инфекцию или опухолевые клетки, но и опосредуют реакцию отторжения трансплантата и аутоиммунные расстройства (Janeway etal., 1999; Paul, 1999). Молекулы иммуноглобулинов, расположенные на поверхности В-лимфоцитов, играют роль рецепторов и способны распознавать огромное число антигенов. В отличие от В-лимфоцитов Т-лимфоциты распознают антигены только в виде пептидных фрагментов в комплексе с молекулами Н LA на поверхности антигенпредставляющих клеток, таких, как дендритные клетки, макрофаги и другие клетки, несущие на своей поверхности молекулы HLA класса 1 (HLA-A, HLA-В и HLA-С) и класса II (HLA-DR, HLA-DP и HLA-DQ). Клетки каждого клона Т- и В-лимфоцитов имеют одинаковые рецепторы к определенному антигену. При активации этих рецепторов лимфоциты начинают быстро пролиферировать, высвобождая цитокины, играющие роль регуляторов иммунного ответа.
От состояния иммунной системы в значительной степени зависят развитие и исход многих заболеваний. Разработка вакцин против таких распространяющихся возбудителей, как ВИЧ и вирус лихорадки Эбола, — насущная задача, стоящая перед учеными. Рост числа заболеваний, связанных с нарушением функции иммунной системы, часто принимающий характер эпидемии, требует разработки новых действенных методов лечения. К таким заболеваниям относятся: аутоиммунные расстройства (ревматоидный артрит, сахарный диабет, системная красная волчанка, рассеянный склероз), солидные опухоли и гемоблас-тозы, инфекционные болезни, бронхиальная астма, различные аллергические реакции. Трансплантация органов — действенный метод лечения многих заболеваний. Однако отторжение трансплантата, опосредованное иммунной системой, по-прежнему остается серьезным препятствием к широкому применению этого метода лечения. Углубленное изучение механизмов иммунного ответа привело к появлению новых методов лечения. В этой главе даны основные сведения о препаратах, действующих на иммунный ответ, — иммунодепрессантах, индукторах иммунологической толерантности и иммуностимуляторах.
Иммуносупрессия[править | править код]
Иммунодепрессанты успешно применяют для подавления иммунного ответа при трансплантации органов (особенно в случае острого отторжения трансплантата) и для лечения тяжелых аутоиммунных заболеваний. Сегодня при трансплантации органов и тканей применяют следующие основные классы лекарственных средств: 1) глюкокортикоиды, 2) ингибиторы кальциневрина, 3) цитостатики. Однако лечение подобных состояний требует пожизненного приема перечисленных средств и вызывает подавление иммунитета в целом, что повышает риск развития инфекций и опухолей. Нефротоксичность и сахарный диабет, возникающие при длительном применении ингибиторов кальциневрина и глюкокортикоидов, ограничивают использование этих препаратов.
Препараты моноклональных и поликлональных антител, направленные против активированных Т-лимфоцитов, являются важным дополнением к другим способам лечения. Эти препараты действуют только на определенные клетки иммунной системы, что обеспечивает высокую избирательность лечения. Арсенал иммунодепрессантов недавно пополнился новыми средствами, такими, как сиролимус и антитела к рецептору ИЛ-2, которые блокируют пути внутриклеточной передачи сигнала от факторов роста в уже активированных Т-лимфоцитах, тем самым в значительной степени ограничивая пролиферацию клонов и вызывая толерантность. Ниже приведены основные сведения о наиболее известных иммунодепрессантах. Близка к завершению разработка новых лекарственных средств, действующих избирательно и призванных, возможно уже в следующем десятилетии, существенно изменить подходы к иммунотерапии.
Трансплантация органов[править | править код]
Общие положения[править | править код]
Трансплантация органов базируется на пяти основных принципах. Первый принцип — тщательная подготовка больного и подбор донора, наиболее совместимого по антигенам систем АВО и HLA (Legendre and Guttman, 1989). Второй принцип — применение комбинированной иммуносупрессивной терапии, подобно тому как это делается при полихимиотерапии опухолей. Одновременно назначают несколько препаратов, подавляющих иммунный ответ на трансплантат путем действия на разные молекулярные мишени (табл. 53.1; Krenskyetal., 1990; Hong and Kahan, 2000a). Одновременное назначение нескольких препаратов в относительно низких дозах позволяет достигнуть максимальной иммуносупрессии и уменьшить побочное действие. Третий принцип — назначение высоких доз иммунодепрессантов во время индукционной иммуносупрессивной терапии с последующей длительной поддерживающей иммуносупрессивной терапией меньшими дозами. Четвертый принцип — тщательное исследование каждого нарушения функции трансплантата. Необходимо установить, вызвано ли нарушение реакцией отторжения, побочным действием препаратов или инфекцией, помня, что эти причины могут сосуществовать. Пятый принцип обязывает снизить дозу или полностью отменить препарат, если его побочное действие неоправданно велико.
Таблица 53.1. Механизм действия некоторых иммунодепрессантов на активацию Т-лимфоцитов
|
Препарат |
Мишень |
|
Глюкокортикоиды |
Глюкокортикоидчувствительные регуляторные элементы генома (регулируют транскрипцию генов) |
|
Муромонаб-СОЗ |
CD3 — компонент антигенраспознающего рецептора Т-лимфоцитов (блокирует распознавание антигена) |
|
Циклоспорин |
Кальциневрин (ингибирует фосфатазную активность) |
|
Такролимус |
Кальциневрин (ингибирует фосфатазную активность) |
|
Азатиоприн |
ДНК (включение аналогов естественных нуклеотидов) |
|
Микофеноловая кислота |
ИМФ-дегидрогеназа (ингибирует активность) |
|
Даклизумаб и |
Рецептор ИЛ-2 (блокируют активацию |
|
базиликсимаб |
Т-лимфоцитов, опосредованную ИЛ-2) |
|
Сиролимус |
Киназа mTOR, участвующая в регуляции клеточного цикла (ингибирует активность) |
Индукционная иммуносупрессивная терапия. Во многих клиниках моноклональные антитела (муромонаб-СОЗ, антитела к рецептору ИЛ-2) или поликлональные антилимфоцитарные антитела применяют сразу после трансплантации в качестве индукционной иммуносупрессивной терапии (Wilde and Goa, 1996; Brennan et al., 1999). Это обеспечивает начало приживления трансплантата без использования высоких доз нефротоксичных ингибиторов кальциневрина. Такое лечение снижает риск раннего отторжения, поэтому оно особенно важно при исходно высоком риске отторжения (при значительной исходной сенсибилизации больного, при повторных трансплантациях, при трансплантации у детей и темнокожих).
Поддерживающая иммуносупрессивная терапия. В большинстве клиник одновременно назначают несколько препаратов — ингибитор кальциневрина, глюкокортикоиды, микофеноловую кислоту (ингибитор пуринового обмена), — действующих на разные этапы активации Т-лимфоцитов (Suthanthiran et al., 1996; Perico and Remuzzi, 1997). Глюкокортикоиды, азатиоприн, циклоспорин, такролимус, микофеноловая кислота, сиролимус и разнообразные моноклональные и поликлональные антитела одобрены ФДА к применению при трансплантации.
Лечение отторжения трансплантата. Преднизон в низких дозах, ингибиторы кальциневрина, ингибиторы пуринового обмена и сиролимус успешно применяют для профилактики острой реакции отторжения, однако такое лечение слабо действует на активированные Т-лимфоциты, а потому малопригодно для лечения начавшегося острого отторжения или для полного предотвращения хронического отторжения (Monaco et al., 1999). Для лечения отторжения необходимо применять средства, направленные против активированных Т-лимфоцитов: глюкокортикоиды в высоких дозах (пульс-терапия), поликлональные антилимфоцитарные антитела или моноклональные антитела муромонаб-СDЗ.
Глюкокортикоиды[править | править код]
Применение глюкокортикоидов в качестве иммунодепрессантов в 1960-х гг. сыграло ключевую роль в развитии трансплантации органов и тканей. Химическое строение, фармакокинетика и лекарственные взаимодействия глюкокортикоидов изложены в Кортикостероиды. Преднизон, преднизолон и другие глюкокортикоиды применяются как в качестве монотерапии, так и в сочетании с другими иммунодепрессантами для подавления реакции отторжения трансплантата и при аутоиммунных заболеваниях.
Механизм действия. Иммуносупрессивный эффект глюкокортикоидов известен давно, но точный механизм этого эффекта до конца не раскрыт (Rugstad, 1988; Beato, 1989). Глюкокортикоиды быстро вызывают преходящую лимфопению за счет лизиса и перераспределения лимфоцитов. Более длительное действие глюкокортикоидов опосредуют внутриклеточные рецепторы. Комплексы глюкокортикоид—рецептор проникают в ядро и связываются с глюкокортикоидчувствительными элементами ДНК, регулирующими транскрипцию некоторых генов (гл. 60). Важную роль играет также взаимодействие этих комплексов с факторами транскрипции. Повышение под действием глюкокортикоидов экспрессии белка 1кВ препятствует активации факторов транскрипции NFkB и приводит к усилению апоптоза активированных клеток (Auphan et al„ 1995). Основное действие глюкокортикоидов заключается в подавлении синтеза важнейших провоспалительных цитокинов, таких, как ИЛ-1 и ИЛ-6. В Т-лимфоцитах подавляется синтез ИЛ-2 и замедляется их пролиферация. Угнетается активация цитотоксических Т-лимфоцитов. Хемотаксис нейтрофилов и моноцитов замедляется, снижается высвобождение лизосомальных ферментов. Таким образом, глюкокортикоиды оказывают сильное противовоспалительное действие, угнетая клеточный иммунитет. При этом они сравнительно мало влияют на гуморальный иммунитет.
Применение. Глюкокортикоиды показаны во многих ситуациях (Zoorob and Cender, 1998). В сочетании с другими иммунодепрессантами эти препараты обычно применяют для профилактики и лечения отторжения. Пульс-терапия метилпреднизолоном используется для подавления острой реакции отторжения и лечения тяжелых обострений некоторых аутоиммунных заболеваний (Shinn et al., 1999; Laan et al., 1999). Глюкокортикоиды эффективно подавляют реакцию «трансплантат против хозяина» после трансплантации костного мозга. Их чрезвычайно широко применяют при аутоиммунных заболеваниях: ревматоидном и других артритах, системной красной волчанке, дерматомиозите, псориазе и иных кожных поражениях, бронхиальной астме и прочих аллергических заболеваниях, неспецифическом язвенном колите, воспалительных заболеваниях глаз, аутоиммунных гематологических заболеваниях и тяжелом обострении рассеянного склероза. Кроме того, глюкокортикоиды нивелируют аллергические реакции, вызванные другими иммунодепрессантами, и применяются после трансплантации для предупреждения выброса цитокинов при первом введении муромонаба-СОЗ (см. ниже).
Побочные эффекты. Поскольку к глюкокортикоидам чувствительны клетки многих тканей, а число генов, регулируемых глюкокортикоидами, огромно, то применение высоких доз этих препаратов привело к инвалидизации и развитию угрожающих жизни состояний у многих больных. Побочные эффекты глюкокортикоидов включают замедление роста, ишемические некрозы костей, остеопороз, повышенный риск инфекций, плохое заживление ран, катаракту, гипергликемию и артериальную гипертонию (Кортикостероиды - побочные эффекты). Сочетание с циклоспорином позволяет уменьшить дозу глюкокортикоидов, но, несмотря на это, побочное действие глюкокортикоидов остается одной из главных проблем трансплантологии.
Ингибиторы кальциневрина[править | править код]
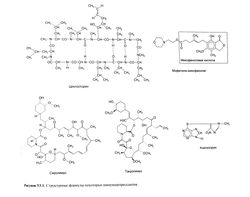
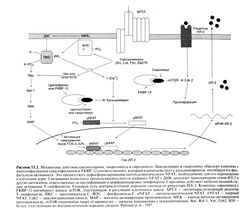
Наиболее эффективные иммунодепрессанты, широко применяемые в клинике, — это ингибиторы кальциневрина циклоспорин и такролимус. Они действуют на пути внутриклеточной передачи сигнала от активированных рецепторов Т-лимфоцитов (Schreiberand Crabtree, 1992). Несмотря на то что циклоспорин и такролимус имеют разное химическое строение (рис. 53.1) и связываются с различными (но родственными) молекулярными мишенями, механизм подавления ими передачи сигнала от рецепторов Т-лимфоцитов одинаков: оба препарата образуют комплекс с иммунофилинами (соответственно с циклофилином и белком FKBP-12), который связывается с кальциневрином и блокирует его фосфатазную активность (рис. 53.2). В норме кальциневрин катализирует дефосфорилирование цитоплазматического NFAT, необходимое для перемещения этого фактора транскрипции из цитоплазмы в ядро, где тот, в свою очередь, активирует гены ряда цитокинов, в том числе ген ИЛ-2 — главного фактора роста и дифференцировки Т-лимфоцитов.
Циклоспорин[править | править код]
Химические свойства. Циклоспорин (циклоспорин А), продуцируемый грибами Beauveria nivea, представляет собой циклический полипептид из 11 аминокислотных остатков (Borel et al., 1976). Его структура имеет следующие особенности: амидные группы в составе пептидных связей либо метилированы, либо образуют водородные связи; содержит одну D-аминокислоту (аланин); одна из пептидных связей находится в цис-, а остальные — в транс-положении (рис. 53.1). Так как циклоспорин — липофильное соединение, перед введением его необходимо растворить в модифицированном касторовом масле.
Механизм действия. Циклоспорин несколько угнетает гуморальный иммунитет, но в основном действует на Т-лимфоциты, участвующие в отторжении трансплантата и некоторых аутоиммунных заболеваниях (Kahan, 1989). Препарат преимущественно подавляет запускаемую антигеном внутриклеточную передачу сигнала в Т-лимфоцитах, тормозит экспрессию ряда цитокинов, включая ИЛ-2, а также экспрессию белков, подавляющих апоптоз. Циклоспорин образует комплекс с циклофилином — рецепторным белком, находящимся в цитоплазме клеток-мишеней. Этот комплекс связывается с кальциневрином, ингибируя тем самым Са -зависимое дефосфорилирование цитоплазматического NFAT (Schreiber and Crabtree, 1992). В норме дефосфорилированный цитоплазматический NFAT перемещается в ядро, где образует комплекс с ядерным NFAT или другими факторами, необходимыми для активации Т-лимфоцитов, и усиливает транскрипцию гена ИЛ-2 и генов других цитокинов. Комплекс циклоспорина и циклофилина подавляет фосфатазную активность кальциневрина, в результате цитоплазматический NFAT остается фосфорилированным и не может попасть в ядро, усиления транскрипции не происходит и Т-лимфоциты не отвечают на антигенную стимуляцию. Кроме того, циклоспорин повышает экспрессию трансформирующего фактора роста Р — белка, подавляющего пролиферацию Т-лимфоцитов поддействием ИЛ-2 и продукцию цитотоксических Т-лимфоцитов (Khanna et al., 1994).
Фармакокинетика. Циклоспорин применяют как внутрь, так и в/в. Препарат для в/в введения выпускается в виде концентрированного раствора, содержащего полиоксиэтилированное касторовое масло и этанол. Непосредственно перед инъекцией препарат разводят в 0,9% NaCl или 5% глюкозе. Препарат для приема внутрь выпускается в виде желатиновых капсул и растворов. Циклоспорин в мягких желатиновых капсулах всасывается медленно, его биодоступность составляет 20—50%. Для улучшения всасывания был разработан препарат в виде микроэмульсии, одобренный ФДА в 1995 г. (Noble and Markham,1995). Биодоступность этой лекарственной формы препарата выше и не подвержена таким индивидуальным колебаниям, как у обычного препарата. Микроэмульсия циклоспорина выпускается в виде желатиновых капсул (по 25 и 100 мг) и раствора для приема внутрь (100 мг/мл). Так как биодоступность разных лекарственных форм циклоспорина неодинакова, замена одной формы на другую должна проводиться под наблюдением врача и при тщательном контроле за концентрацией циклоспорина в крови. Для сравнения измеренных концентраций с данными литературы необходимо знать особенности метода измерения. Появились несколько препаратов циклоспорина, не защищенных торговой маркой (Hallo-ran, 1997), но недавно продажа одного из таких препаратов была запрещена ФДА из-за неподтвержденной биоэквивалентности (гл. 1).
Как упоминалось выше, при приеме внутрь циклоспорин всасывается не полностью. Всасывание препарата зависит от нескольких факторов, в том числе от особенностей больного и от лекарственной формы. Элиминация циклоспорина обычно двухфазная; конечный составляет 5—18ч (Faulds etal., 1993; Noble and Markham, 1995). При в/в введении клиренс циклоспорина составляет приблизительно 5—7 мл/мин/кг у взрослых с переменной почкой, но возможны колебания в зависимости от возраста и категории больных. Так, клиренс ниже при трансплантации сердца и заметно выше у детей. При использовании терапевтических доз зависимость между введенной дозой и ПФК (гл. 1) имеет линейный характер, однако из-за значительных индивидуальных различий в каждом случае необходимо измерение концентрации в крови (Faulds etal., 1993; Noble and Markham, 1995).
При приеме микроэмульсии циклоспорина внутрь максимальная концентрация в крови достигается через 15—2 ч (Faulds et al., 1993; Noble and Markham, 1995). Прием во время еды замедляет всасывание и снижает биодоступность. Прием пищи (как с высоким, так и низким содержанием жиров) в течение 30 мин после циклоспорина уменьшает ПФК препарата примерно на 13%, а максимальную концентрацию в крови — на 33%. В связи с эти необходим индивидуальный подбор дозы и режима приема циклоспорина у амбулаторных больных.
Циклоспорин широко распределяется во внесосудистом пространстве. У больных с пересаженными органами объем распределения циклоспорина, введенного в/в, достигает 3—5 л/кг.
Лишь 0,1% циклоспорина выводится в неизмененном виде с мочой (Faulds et al., 1993). В основном препарат окисляется в печени при участии изоферментов подсемейства II1A цитохрома Р450 и в меньшей степени — в кишечнике и почках (Fahr, 1993). Хотя циклическая пептидная структура циклоспорина относительно устойчива, боковые цепи активно метаболизируются. У человека в желчи, кале, крови и моче найдены по меньшей мере 25 метаболитов циклоспорина (Christians and Sewing, 1993). Все метаболиты обладают меньшей, чем циклоспорин, биологической активностью и токсичностью. Циклоспорин и его метаболиты экскретируются преимущественно с желчью, и только 6% — с мочой. Циклоспорин выводится также с молоком. При нарушении функции печени необходима коррекция дозы. При почечной недостаточности, атакже больным, находящимся на гемодиализе, назначают обычные дозы.
Применение. Циклоспорин применяют при трансплантации почки, печени, сердца и других органов, а также при ревматоидном артрите и псориазе (Faulds et al., 1993).
Использование циклоспорина в дерматологии обсуждается в гл. 65. Открытие циклоспорина стало началом новой эры в трансплантологии: снизилось число ранних отторжений, повысилась выживаемость почечных трансплантатов, и стали возможными трансплантации сердца и печени. Циклоспорин обычно назначают в сочетании с другими препаратами, особенно с глюкокортикоидами, азатиоприном или микофеноловой кислотой, а в последнее время — с сиролимусом. Дозы циклоспорина существенно различаются и зависят от того, какой орган пересаживается и какие еще препараты входят в схему лечения. Перед трансплантацией циклоспорин обычно не назначают из-за нейротоксичности. При трансплантации почки назначение циклоспорина стараются отсрочить, пока СКФ не достигнет некоего минимального уровня. В каждом отдельном случае начальные и поддерживающие дозы столь различны, что единых рекомендаций быть не может. При подборе дозы руководствуются выраженностью симптомов отторжения трансплантата; учитывают выраженность симптомов отторжения (слишком низкая доза), симптомов нарушения функции почек и других проявлений побочного действия (слишком высокая доза) и концентрацию циклоспорина в крови. При трансплантации почки важно отличить отторжение трансплантата от нарушения функции почек вследствие побочного действия циклоспорина. Поскольку риск побочного действия выше при в/в введении препарата, то такое введение прекращают, как только больной сможет принимать препарат внутрь.
При тяжелом ревматоидном артрите циклоспорин применяют при неэффективности метотрексата. Циклоспорин можно назначать вместе с метотрексатом, тщательно следя за концентрациями в крови обоих препаратов (Ва-raldo et al., 1999). Циклоспорин показан взрослым с нормальным иммунитетом при тяжелом псориазе, если другое лечение неэффективно (Linden and Weinstein, 1999). Механизм действия циклоспорина предполагает возможность использования его и при других заболеваниях,патогенезе которых участвуют Т-лимфоциты (Faulds et jl 1993). Имеются сообщения об успешном применении циклоспорина в случае неэффективности стандартного лечения при остром поражении глаз на фоне болезни Бехчета, эндогенных увеитах, диффузном нейродерте) неспецифическом язвенном колите и гломерулонефрите.
Побочные эффекты. Основные осложнения при лечении циклоспорином — нарушения функции почек, тремор, гирсутизм, артериальная гипертония, гиперлипопротеи-пемия и гиперплазия десен (Burke et al., 1994). Нефроток-сическое действие наблюдается у большинства больных к служит основным показанием к отмене препарата или коррекции дозы. Артериальная гипертония наблюдается почти в 50% случаев трансплантации почки и практически всегда при трансплантации сердца. Сочетанное применение ингибиторов кальциневрина (особенно такро-димуса) и глюкокортикоидов повышает риск сахарного диабета.
Лекарственные взаимодействия. Назначение циклоспорина одновременно с другими препаратами требует особой осторожности, так как он взаимодействует со многими распространенными лекарственными средствами. Вещества, влияющие на активность микросомальных ферментов, особенно на изоферменты подсемейства IIIA цитохрома Р450, изменяют концентрацию циклоспорина в крови (Faulds et al., 1993). Препараты, ингибирующие эти изоферменты, замедляют метаболизм циклоспорина и, соответственно, повышают его концентрацию. К ним относятся антагонисты кальция (верапамил, никардипин), противогрибковые препараты (флуконазол, кетоконазол), антибиотики (эритромицин), глюкокортикоиды (метилпреднизалон), ингибиторы протеазы ВИЧ (индинавир) и другие препараты (аллопуринол, метоклопрамид). Кроме того, ингибирующим действием обладают виноградный и грейпфрутовый соки, а потому во время лечения циклоспорином их употреблять не следует. Напротив, вещества, активирующие изоферменты подсемейства IIIA цитохрома Р450, ускоряют метаболизм циклоспорина и снижают его концентрацию в крови. Подобным образом действуют ряд антибиотиков (нафциллин и рифампицин), противосудорожных (фенобарбитал, фенитоин) и некоторых других лекарственных средств. Циклоспорин и сиролимус не следует назначать одновременно из-за усиления побочного действия — сиролимус усиливает нарушения функции почек, вызванные циклоспорином, а циклоспорин, в свою очередь, усугубляет вызванные сиролимусом гиперлипопротеидемию и угнетение кроветворения. Кроме того, поражение почек усиливается при одновременном приеме циклоспорина с Н П ВС и другими нефротоксичными препаратами. Прием циклоспорина способствует снижению клиренса метотрексата и некоторых других препаратов, таких, как преднизолон, дигоксин и ловастатин.
Такролимус[править | править код]
Это антибиотик из группы макролидов, продуцируемый Streptomyces tsukubaensis (Goto et al., 1987). Его структурная формула приведена на рис. 53.1.
Механизм действия. Такролимус, подобно циклоспорину, ингибирует кальциневрин, подавляя активацию Т-лимфоцитов (Schreiber and Crabtree, 1992). Такролимус связывается с внутриклеточным белком FKBP-12 (РК506-связывающий белок-12), который, как и родственный ему по структуре циклофилин, относится к иммунофилинам. При образовании комплекса из такролимуса, FKBP-I2, кальция, кальмодулина и кальциневрина фосфатазная активность последнего падает. Как уже сказано выше, подавление активности кальциневрина препятствует дефосфорилированию цитоплазматического NFAT и переносу последнего внутрь ядра, что блокирует активацию Т-лимфоцитов (рис. 53.2). В связи с этим, несмотря на связывание с разными внутриклеточными рецепторами, механизмы иммуносупрессивного действия циклоспорина и такролимуса одинаковы (Plosker and Foster, 2000).
Фармакокинетика. Такролимус выпускается в виде капсул для приема внутрь (по 0,5, 1 и 5 мг) и раствора для инъекций (5 мг/мл). Всасывание в ЖКТ неполное и подвержено значительным индивидуальным колебаниям. Прием пищи замедляет и снижает всасывание. Из-за значительных различий в фармакокинетике такролимуса необходим индивидуальный подбор дозы (Fung and Starzl, 1995). Для определения фармакокинетических параметров лучше использовать цельную кровь, а не плазму. Примерно на 75—99% такролимус связывается с белками плазмы, главным образом с альбумином и кислым а,-гликопротеидом. Т1/2 такролимуса составляет около 12 ч. Такролимус в значительной степени метаболизируется в печени изоферментами подсемейства III А цитохрома Р450. Некоторые из метаболитов активны, но иммуносупрессивное действие оказывает в основном исходный препарат. Большая часть такролимуса и его метаболитов выделяется с калом. Менее 1% выводится в неизмененном виде с мочой.
Применение. Такролимус, как и циклоспорин, показан для профилактики отторжения трансплантированных органов, а также для лечения отторжения, развившегося несмотря на лечение циклоспорином (Mayer et al., 1997; The U.S. Multicenter FK506 Liver Study Group, 1994). Рекомендуемая начальная доза для в/в введения — 0,03— 0,05 мг/кг/сут в виде длительной инфузии. Рекомендуемая начальная доза внутрь для взрослых при трансплантации почки составляет 0,2 мг/кг/сут, при трансплантации печени — 0,1—0,15 мг/кг/сут. Детям, как правило, требуются более высокие дозы, чем взрослым (Shapiro,1998); при трансплантации печени детям рекомендуемая суточная доза равна 0,15—0,2 мг/кг/сут в 2 приема (каждые 12ч).
Побочные эффекты. Такролимус вызывает поражение почек, ЦНС (тремор, головную боль, двигательные расстройства, эпилептические припадки), ЖКТ, артериальную гипертонию, гиперкалиемию, гипергликемию и сахарный диабет (Plosker and Foster, 2000). Как и в случае с циклоспорином, нефротоксичность такролимуса ограничивает его применение (Mihatsch et al., 1998; Henry, 1999). Действие такролимуса на |3-клетки островков поджелудочной железы вызывает снижение толерантности к глюкозе и развитие сахарного диабета. При трансплантации органов у взрослых эти осложнения нередки. Применение такролимуса, как и любых других иммунодепрессантов, повышает риск вторичных опухолей и оппортунистических инфекций.
Лекарственные взаимодействия. Концентрацию такролимуса в крови и функцию почек необходимо регулярно контролировать, особенно при назначении совместно с другими нефротоксичными препаратами. Циклоспорин и такролимус усиливают нефротоксическое действие друг друга, поэтому при переходе с циклоспорина на такролимус необходим перерыв не менее 24 ч. Так как такролимус метаболизируется изоферментами подсемейства IIIA цитохрома Р450, лекарственные взаимодействия такролимуса и циклоспорина сходны (Venkataramanan et al., 1995; Yoshimura et al., 1999).
Цитостатики[править | править код]
Сиролимус[править | править код]
Сиролимус (рапамицин) — макролид, вырабатываемый грибами Streptomyces hygroscopicus (Vezina et al., 1975). Его структурная формула представлена на рис. 53.1.
Механизм действия. Сиролимус блокирует пути внутриклеточной передачи сигнала от рецепторов ИЛ-2 и других факторов роста, препятствуя активации и пролиферации Т-лимфоцитов (рис. 53.2) (Kuo et al., 1992). Сиролимус, аналогично циклоспорину и такролимусу, образует в клетке комплекс с иммунофилином — белком FKBP-12. Однако комплекс сиролимуса с FKBP-12 ингибирует не кальциневрин, а киназу mTOR (mammalian target of rapamycin — мишень рапамицина у млекопитающих), ключевой фермент регуляции клеточного цикла (Brown et al., 1994). В результате этого ингибирования клеточный цикл останавливается на границе периодов G) и S. Эксперименты на животных показали, что сиролимус не только препятствует отторжению трансплантата, подавляет реакцию «трансплантат против хозяина» и эффективен при ряде аутоиммунных заболеваний, но и обладает длительным иммуносупрессивным действием, длящимся несколько месяцев после отмены препарата, что предположительно связано с развитием иммунологической толерантности (см. ниже, «Иммунологическая толерантность») (Groth et al., 1999).
Фармакокинетика. У здорового человека при приеме внутрь сиролимус быстро всасывается и достигает максимальной концентрации в крови через 1 ч после однократного приема. При трансплантации почки сиролимус [назначают дробно, и его максимальная концентрация в крови достигается через 2 ч (Napoli and Kahan, 1996; Zimmerman and Kahan, 1997). Биодоступность сиролимуса составляет примерно 15%, а концентрация в крови прямо пропорциональна дозе в диапазоне 3—12 мг/м2. Богатая жирами пиша снижает максимальную концентрацию сиролимуса в крови на 34%, поэтому следует выбрать постоянный режим приема по отношению к еде и регулярно определять концентрацию сиролимуса в крови. Около 40% сиролимуса связано с белками плазмы, в основном с альбумином. Сиролимус проникает в клетки крови, и у больных с пересаженной почкой его концентрация в цельной крови в 38 раз превышает концентрацию в плазме. Сиролимус метаболизируется изоферментами подсемейства IVA цитохрома Р450 и выводится из клеток Р-гликопротеидом. В крови обнаружено семь основных метаболитов сиролимуса (Salm et al., 1999). Метаболиты выводятся преимущественно с калом и в небольшом количестве — с мочой. Некоторые из метаболитов активны, но иммуносупрессивное действие на 90% обеспечивается самим сиролимусом. После дробного приема сиролимуса на фоне стабильной функции трансплантированной почки его Т1/2 в крови достигает 62 ч (Napoli and Kahan, 1996; Zimmerman and Kahan, 1997). Насыщающая доза сиролимуса (в 3 раза выше поддерживающей) в большинстве случаев обеспечивает постоянную концентрацию препарата в крови в течение суток.
Применение. Сиролимус в сочетании с блокаторами ка-льциневрина и глюкокортикоидами применяется для профилактики отторжения трансплантата (Kahan et al., 1999а). При нарушении функции почек или высоком риске такого нарушения в ответ на прием ингибиторов кальциневрина во избежание необратимого поражения почек сиролимус назначают вместе с глюкокортикоидами и микофеноловой кислотой. Начальная доза препарата для лиц старше 13 лет и весом менее 40 кг рассчитывается в зависимости от площади поверхности тела (поддерживающая доза — 1 мг/м2/сут, насыщающая доза — 3 мг/м2). Рекомендаций по применению сиролимуса у детей и пожилых пока нет (Kahan, 1999). При нарушении функции печени поддерживающую дозу снижают на треть (Watson etal., 1999).
Побочные эффекты. Применение сиролимуса при трансплантации почки сопряжено с дозозависимым повышением концентрации холестерина и триглицеридов в сыворотке, что может потребовать специального лечения (Murgia et al., 1996). Несмотря на то что сиролимус сам по себе не обладает нефротоксичностью, его применение вместе с циклоспорином сильнее влияет на функцию почек, чем прием циклоспорина с азатиоприном или плацебо. Поэтому при назначении сиролимуса вместе с циклоспорином необходимо регулярно контролировать функцию почек. Сиролимус дозозависимо увеличивает риск такого хорошо известного хирургического осложнения при трансплантации почки, как образование лимфатической кисты, что требует тщательного наблюдения в послеоперационном периоде. Другие побочные эффекты — анемия, лейкопения, тромбоцитопения (Hong and Kahan, 2000b), гипо- или гиперкалиемия, лихорадка, желудочно-кишечные нарушения. Сиролимус, как и все иммунодепрессанты, повышает риск злокачественных новообразований (особенно лимфом) и инфекций. При назначении сиролимуса следует проводить профилактику пневмоцистной пневмонии и цитомегаловирусной инфекции (Groth et al., 1999).
Лекарственные взаимодействия. Так как сиролимус является субстратом изоферментов подсемейства IVA цитохрома Р450 и выводится из клеток Р-гликопротеидом, необходимо особое внимание при одновременном применении с препаратами, имеющими те же пути метаболизма и транспорта (Yoshimura et al., 1999). Как было отмечено ранее, следует избегать одновременного применения циклоспорина и сиролимуса. При назначении вместе с циклоспорином, дилтиаземом или рифампицином может потребоваться коррекция дозы сиролимуса. При приеме таких препаратов, как ацикловир, дигоксин, глибенкламид, нифедипин, этинилэстрадиол/норгестрел, преднизолон, триметоприм/сульфаметоксазол, сиролимус назначают в обычных дозах. Так как не все лекарственные взаимодействия сиролимуса известны, необходимо помнить о такой возможности и регулярно определять концентрацию сиролимуса в крови.
Азатиоприн[править | править код]
Будучи имидазольным производным 6-мер-каптопурина (рис. 53.1), азатиоприн ингибирует пуриновый обмен (Elion, 1993).
Механизм действия. Под воздействием нуклеофильных соединений, таких, как глутатион, азатиоприн расщепляется до меркаптопурина, который, в свою очередь, превращается в метаболиты, непосредственно подавляющие синтез пуринов (Bertino, 1973). Аналог естественных нуклеотидов, 6-тио-ИМФ, превращается в 6-тио-ГМФ и затем в 6-тио-ГГФ, который встраивается в ДНК, препятствуя экспрессии генов (Chan et al., 1987). При этом прекращается пролиферация и подавляются различные функции лимфоцитов. Азатиоприн более сильный иммунодепрессант, чем меркаптопурин, что, видимо, обусловлено различиями во всасывании препаратов и фармакокинетике их метаболитов.
Фармакокинетика. Азатиоприн хорошо всасывается при приеме внутрь, и его сывороточная концентрация достигает максимума через 1—2 ч после приема. Т1/2азатиоприна составляет примерно 10 мин, в то время как Т1/2 меркаптопурина — около 1 ч. Т1/2 других метаболитов достигает 5 ч. Определение сывороточной концентрации препарата малоинформативно из-за высокой скорости метаболизма, быстрого проникновения в ткани и значительной активности многих производных азатиоприна. Азатиоприн и меркаптопурин умеренно связываются с белками плазмы и частично выводятся при диализе. Подвергаясь окислению и метилированию в печени и эритроцитах, азатиоприн и меркаптопурин быстро удаляются из крови. Изменение почечного клиренса мало влияет на терапевтические и побочные эффекты препарата, но все же при почечной недостаточности дозу азатиоприна обычно снижают.
Применение. Азатиоприн был впервые применен в качестве иммунодепрессанта в 1961 г., что сделало возможной аллотрансплантацию почки (Murray et al., 1963). Азатиоприн применяют в сочетании с другими препаратами доя профилактики отторжения трансплантированных органов и для лечения тяжелого ревматоидного артрита (Hong and Kahan, 2000а; Gaffney and Scott, 1998). Дозы азатиоприна, достаточные для профилактики отторжения при минимальных побочных эффектах, существенно различаются, начальная доза обычно составляет 3— 5мг/кг/сут. Для лечения ревматоидного артрита начальная доза ниже — 1 мг/кг/сут. Во время лечения регулярно проводят общий анализ крови и определяют биохимические показатели функции печени.
Побочные эффекты. Главный из них — нарушение кроветворения; обычно развивается лейкопения, реже — тромбоцитопения, еще реже — анемия. Другие важные побочные эффекты — предрасположенность к инфекциям (особенно герпесу и инфекциям, вызванным вирусом va-ricella-zoster), нарушение функции печени, алопеция, желудочно-кишечные нарушения, панкреатит и повышенный риск злокачественных новообразований.
Лекарственные взаимодействия. Аллопуринол ингибирует ксантиноксидазу, главный фермент в катаболизме метаболитов азатиоприна (Venkat Raman et al., 1990). При одновременном назначении азатиоприна и аллопуриноладоза азатиоприна должна быть снижена на 25—33%, однако лучше не применять эти препараты вместе. Прием азатиоприна в сочетании с другими средствами, вызывающими подавление кроветворения, или с ингибиторами АПФ также может вызывать лейкопению, тромбоцитопению и анемию.
Микофеноловая кислота[править | править код]
Этот препарат обычно применяют в виде мофетила микофенолата, представляющего собой 2-морфолиноэтиловый эфир микофеноловой кислоты (Allison and Eugui, 1993). Структурная формула мофетила микофенолата приведена на рис. 53.1
Механизм действия. Мофетила микофенолат сам по себе не активен, но быстро гидролизуется и превращается в активное вещество — микофеноловую кислоту — избирательный, неконкурентный и обратимый ингибитор ИМФ-дегидрогеназы (Natsu-meda and Carr, 1993), необходимой для синтеза гуаниновых нуклеотидов. Пролиферация В- и Т-лимфоцитов в значительной степени зависит от этого фермента, в то время как другие клетки могут использовать иные пути синтеза. Таким образом, микофенолован кислота избирательно подавляет пролиферацию лимфоцитов, а также синтез антител, адгезию и миграцию лимфоцитов. Добавление гуанозина или дезоксигуанозина в культуральную среду останавливает действие микофеноловой кислоты на клетки.
Фармакокинетика. Мофетила микофенолат после приема внутрь или в/в введения быстро и полностью гидролизуется до микофеноловой кислоты, которая затем превращается в неактивный глюкуронид. Мофетила микофенолат исчезает из крови в считанные минуты, в то время какТ1/2 микофеноловой кислоты составляет примерно 16 ч. Выводится препарат с мочой, в основном в виде глюкуронида микофеноловой кислоты (87%), и лишь незначительное количество (< 1%) — в виде микофеноловой кислоты (Bardsley-Elliot et al., 1999). При почечной недостаточности сывороточные концентрации микофеноловой кислоты и ее глюкуронида возрастают. В первые недели после трансплантации почки (до 40 сут) сывороточная концентрация микофеноловой кислоты после однократного приема мофетила микофенолата в два раза меньше, чем у здоровых добровольцев или реципиентов с нормализовавшейся функцией трансплантата. Данные о применении микофеноловой кислоты у детей крайне ограничены, а эффективность и риск побочного действия не известны (Butani et al., 1999).
Применение. Микофеноловую кислоту применяют для профилактики отторжения трансплантата, обычно в со-четании с другими иммунодепрессантами, чаще с глюкокортикоидами и ингибиторами кальциневрина, но не с азатиоприном(Kimballetal., 1995;Ahsanetal., 1999;Kreis et al., 2000). Можно назначить микофеноловую кислоту вместе с сиролимусом, но из-за лекарственного взаимодействия необходимо тщательно следить за концентрацией обоих препаратов. При трансплантации почки микофеноловую кислоту назначают по 1 г внутрь или в/в (инфузия в течение 2 ч) 2 раза в сутки. Темнокожим при трансплантации почки и всем реципиентам при трансплантации сердца показаны более высокие дозы — по 1,5 г 2 раза в сутки. Изучается возможность использования микофеноловой кислоты для лечения других заболеваний.
Побочные эффекты. Микофеноловая кислота оказывает токсическое действие в основном на ЖКТ и костный мозг (Fulton and Markham, 1996; Bardsley-Elliot etal., 1999), что проявляется лейкопенией, поносом и рвотой. Повышается риск инфекций, особенно цитомегаловирусного сепсиса.
Лекарственные взаимодействия. Были изучены лекарственные взаимодействия микофеноловой кислоты с несколькими препаратами, часто используемыми при трансплантации (Bardsley-Elliot et al., 1999). При одновременном применении микофеноловой кислоты с циклоспорином, триметопримом/сульфаметоксазолом или перо-ральными контрацептивами каких-либо неблагоприятных эффектов не выявлено. Взаимодействие микофеноловой кислоты с азатиоприном не изучено. Антациды, содержащие гидроксид алюминия или магния, снижают всасывание микофеноловой кислоты, поэтому их не следует назначать одновременно. Микофеноловую кислоту не следует применять вместе с холестирамином и другими препаратами, нарушающими кишечно-печеночный кругооборот. Такие препараты снижают сывороточную концентрацию микофеноловой кислоты, вероятно, за счет связывания ее в тонкой кишке. Ацикловир и ганцикловир конкурируют с глюкуронидом микофеноловой кислоты за системы секреции в почечных канальцах, что приводит к повышению сывороточной концентрации и этого глюкуронида, и указанных противовирусных средств. Этот эффект усиливается при почечной недостаточности.
Другие цитостатики[править | править код]
Многие из цитостатиков, применяемых при химиотерапии злокачественных новообразований, оказывают иммуносупрессивный эффект, действуя на лимфоциты и другие клетки иммунной системы. Метотрексат, циклофосфамид, талидомид и хлорамбуцил применяют в качестве иммунодепрессантов. Метотрексат назначают не только как противоопухолевый препарат, но и для подавления реакции «трансплантат против хозяина», лечения ревматоидного артрита и псориаза (Grosflam and Weinblatt, 1991). Аналогично, циклофосфамид и хлорамбуцил применяют не только при злокачественных новообразованиях, но и для лечения гломерулонефрита у детей (Neuhaus et al., 1994). Циклофосфамид широко используют при тяжелой системной красной волчанке (Valeri et al., 1994). Ингибитор синтеза пиримидинов лефлуномид показан при ревматоидном артрите у взрослых (Prakash and Jarvis,1999). Препарат подавляет дигидрооротатдегидрогеназу, участвующую в синтезе пиримидиновых оснований. Он гепатотоксичен, а при назначении беременным может оказывать неблагоприятное действие на плод.
Антитела[править | править код]
Как поликлональные, так и моноклональные антитела против поверхностных антигенов лимфоцитов широко применяются для профилактики и лечения отторжения трансплантированных органов. Путем повторных введений человеческих тимоцитов (для получения антитимоцитарного глобулина) или лимфоцитов (для получения антилимфоцитарного глобулина) лошадям, кроликам, овцам или козам получают сыворотку, содержащую поликлональные антитела, из которой затем выделяют фракцию иммуноглобулинов (Mannick et al., 1971). Несмотря на хорошее иммуносупрессивное действие, разные партии препаратов, полученных таким путем, значительно различаются по эффективности и токсичности. Разработка метода получения моноклональных антител с помощью гибридом стала значительным успехом в иммунологии (Kohler and Milstein, 1975) и позволила получать неограниченное количество антител одной специфичности (рис. 53.3). Моноклональные антитела решили проблему значительных различий в эффективности и специфичности, свойственных поликлональным антителам, однако пока получены моноклональные антитела к ограниченному числу специфических мишеней. В связи с этим в современной иммуносупрессивной терапии находят применение как поликлональные, так и моноклональные антитела.
Антитимоцитарный иммуноглобулин[править | править код]
Это очищенный иммуноглобулин из сыворотки кролика, иммунизированного человеческими тимоцитами (Regan et al., 1999). Он выпускается в виде стерильного лиофилизированного препарата, предназначенного для растворения в стерильной воде и последующего в/в введения.
Механизм действия. Антитимоцитарный иммуноглобулин содержит цитотоксические антитела, связывающиеся с молекулами CD2, CD3, CD4, CD8, CD1 la, CD18, CD25, CD44, CD45 и HLA классов I и II на поверхности человеческих Т-лимфоцитов (Bourdage and Hamlin, 1995). Антитела способствуют разрушению лимфоцитов (путем активации комплемента и путем клеточной цитотоксичности). Кроме того, они подавляют активность оставшихся лимфоцитов, связываясь с молекулами клеточной мембраны, участвующими в активации этих клеток.
Применение. Антитимоцитарный иммуноглобулин в комбинации с другими иммунодепрессантами применяют на стадии индукционной иммуносуппрессивной терапии и для лечения острой реакции отторжения при трансплантации почки (Mariat etal., 1998). Высокая эффективность препарата позволяет назначать антитимоцитарный иммуноглобулин вместо нефротоксичных ингибиторов кальциневрина тем больным, у которых функция трансплантированной почки после ишемического и реперфузионного повреждений восстанавливается медленно. Рекомендуемая доза при остром отторжении трансплантированной почки составляет 1,5 мг/кг/сут (инфузия в течение 4—6 ч) в течение 7—14 сут. Среднее число Т-лимфоцитов снижается ко вторым суткам лечения. Антитимоцитарный иммуноглобулин применяют также для профилактики и лечения острой реакции отторжения при трансплантации других органов (Wall, 1999). Изучается целесообразность его введения во время операции (Szczech and Feldman, 1999).
Побочные эффекты. При применении антитимоцитарного иммуноглобулина могут наблюдаться лихорадка и озноб, велик риск артериальной гипотонии. Для предотвращения побочного действия применяют глюкокортикоиды. парацетамол или Нгблокаторы, а антитимоцитарный иммуноглобулин вводят медленно (в течение 4— 6ч) в крупную вену. После введения антитимоцитарного иммуноглобулина могут развиться сывороточная болезнь игломерулонефрит, реже наблюдаются аллергические реакции немедленного типа. Возможны гематологические осложнения — лейкопения и тромбоцитопения. Как и другие иммунодепрессанты, антитимоцитарный иммуноглобулин повышает риск инфекций и злокачественных новообразований, особенно при комбинированном применении с другими иммунодепрессантами. Лекарственных взаимодействий не выявлено, но могут появляться антитела против антитимоцитарного иммуноглобулина, ограничивающие его многократное применение (как и других препаратов на основе кроличьих антител). Например, в одном исследовании антитела к кроличьим антителам были выявлены у 68% больных.
Моноклональные антитела[править | править код]
Антитела к CD3[править | править код]
Антитела к поверхностному антигену Т-лимфоцитов CD3 используют при трансплантации с начала 1980-х гг. Они оказались необычайно эффективными иммуносупрессивными средствами. Первый препарат, муромонаб-СОЗ (мышиные моноклональные антитела IgG к человеческому CD3), по-прежнему применяют при отторжении трансплантата, устойчивого к действию глюкокортикоидов (Соsimi et al., 1981).
Механизм действия. Муромонаб-СБЗ связывается с CD3 — неизменным компонентом антигенраспознающего рецептора Т-лимфоцитов, участвующего в распознавании антигенов и запускающего внутриклеточную передачу сигнала и пролиферацию Т-лимфоцитов (Hooks et al., 1991). Действие антител вызывает немедленную интернализацию антигенраспознающих рецепторов Т-лимфоцитов, что препятствует последующему распознаванию антигенов. Введение муромонаба-СОЗ приводит к быстрому уменьшению числа Т-лимфоцитов в крови и в лимфоидных органах — лимфоузлах и селезенке. Это происходит за счет гибели Т-лимфоцитов в результате активации комплемента, атакже за счет их прилипания к эндотелию и перераспределения в нелимфоидные органы, в частности легкие. Кроме того, муро-монаб-СОЗ подавляет активность оставшихся Т-лимфоцитов — в них не вырабатывается ИЛ-2 и существенно снижена выработка других цитокинов, вероятно, за исключением ИЛ-4 и ИЛ-10.
Применение. Муромонаб-СОЗ применяют для лечения острого отторжения трансплантата (Ortho Multicenter Transplant Group, 1985; Woodle et al., 1999; Rostaing et al.,1999). Муромонаб-СОЗ выпускается в виде стерильного раствора, в ампуле содержится 5 мг препарата. Рекомендуемая доза для взрослых — 5 мг/сут (у детей дозы ниже) струйно в/в один раз в сутки на протяжении 10—14 сут. Уровень антител возрастает в течение первых трех дней, оставаясь затем на постоянном уровне. Т-лимфоциты исчезают из крови в первые минуты введения и вновь появляются приблизительно через неделю после окончания терапии. Повторное использование муромонаба-СОЗ приводит к иммунизации против мышиных детерминант антител, что может привести к нейтрализации этих антител и потере иммуносупрессивного действия (Jaffers et al., 1983). Поэтому повторное использование муромонаба-СОЗ и других мышиных моноклональных антител противопоказано большинству больных.
Побочные эффекты. Основной побочный эффект муромонаба-СОЗ — так называемый синдром высвобождения цитокинов (Wilde and Goa, 1996; Ortho Multicenter Transplant Study Group, 1985). В основе этого осложнения лежит активация Т-лимфоцитов и высвобождение ряда цитокинов в результате связывания антител с Fc-pe-цептором, ассоциированным с комплексом антигенраспознающего рецептора Т-лимфоцитов. Взаимодействие антител с CD3, образующим комплекс с антигенраспоз-нающим рецептором Т-лимфоцитов, и последующая их перекрестная сшивка, обусловленная взаимодействием с рецепторами Fc-фрагментов, приводят к активации Т-лимфоцитов и высвобождению цитокинов. Синдром высвобождения цитокинов обычно возникает через 30 мин и более после инфузии антител и может длиться несколько часов. Тяжесть симптомов наибольшая при первом введении; как риск синдрома, так и тяжесть симптомов уменьшаются при последующих введениях. Обычно наблюдаются высокая лихорадка, озноб, головная боль, тремор, тошнота или рвота, понос, боль в животе, общее недомогание, миалгия, артралгия, общая слабость. Реже встречаются кожные реакции, поражение сердечно-сосудистой и дыхательной систем, а также ЦНС, включая серозный менингит. Описаны и смертельно опасные осложнения — тяжелый отек легких, РДСВ, шок, аритмии и остановка кровообращения. При синдроме высвобождения цитокинов повышаются сывороточные концентрации ФНОа, ИЛ-2, ИЛ-6, интерферона у, которые вырабатываются активированными Т-лимфоцитами и моноцитами. Несколькими исследователями была показана главенствующая роль ФНОа в развитии этого синдрома (Herbelin etal., 1995). Перед началом лечения тщательно исследуют водный баланс и назначают глюкокортикоиды (их прием перед введением муромонаба-СОЗ предупреждает выброс цитокинов и значительно снижает реакцию на первое введение препарата) и другие средства профилактики. При первом введении антител к CD3 необходимо быть готовым к проведению реанимационных мероприятий. Среди других побочных эффектов — аллергическая реакция немедленного типа, а также характерное для иммуносупрессивной терапии повышение риска инфекций и злокачественных новообразований. После прекращения лечения муромонабом-СОЗ сильно повышается риск отторжения трансплантата (Wilde and Goa, 1996).
Антитела к CD3 нового поколения[править | править код]
Недавно с помощью генной инженерии были получены новые моноклональные антитела к CD3. Чтобы уменьшить выработку антител к ним у больного, эти моноклональные антитела теперь в значительной степени состоят из участков IgG человека. Кроме того, структура антител была изменена так, чтобы предотвратить связывание с рецептором Fc-фрагмента (Friend et al., 1999). Целью создания моноклональных антител к CD3 нового поколения было обеспечить избирательность действия и свести к минимуму побочные эффекты. Первые клинические испытания показали, что гуманизированные моноклональные антитела к CD3, не связывающиеся с рецептором Fc-фрагмента, останавливают острое отторжение трансплантата без синдрома высвобождения цитокинов в ответ на первое введение (Woodle et al., 1999). Изучается применение таких антител при аутоиммунных заболеваниях.
Антитела к рецептору ИЛ-2[править | править код]
Даклизумаб и базиликсимаб— гуманизированные моноклональные антитела, состоящие из активного центра антител мыши и IgG, человека. — получают с помощью генной инженерии (Wiseman and Faulds, 1999). Антитела даклизумаба на 90% состоят из константного участка IgG, человека и фрагментов вариабельного участка человеческих антител, продуцируемых миеломой Ей, и на 10% — из активного центра мышиных антител к а-субъединице рецептора ИЛ-2.
Механизм действия. Антитела прочно связываются с а-субъ-единицей рецептора ИЛ-2 (другое название этой субъединицы р55а, или CD25), присутствующего на поверхности активированных, но не покоящихся Т-лимфоцитов, и блокируют активацию Т-лимфоцитов под действием ИЛ-2. Даклизумаб обладает несколько меньшим сродством к рецептору ИЛ-2, чем базиликсимаб.
Применение. Моноклональные антитела к рецептору ИЛ-2 применяют у взрослых для профилактики острой реакции отторжения в сочетании с другими иммунодепрессантами — глюкокортикоидами, ингибиторами каль-циневрина, иногда — с азатиоприном или микофеноловой кислотой (Kovarik et al., 1999; Hong and Kahan, 1999; Kahan et al., 1999b; Hirose et al., 2000). Даклизумаб и базиликсимаб выпускаются в виде стерильного концентрированного раствора, который перед в/в введением необходимо развести. У больных, которым после трансплантации почки вводили даклизумаб по 1 мг/кг в/в 1 раз в 2 нед, после 5 введений рецептор ИЛ-2 был блокирован, причем блокада рецептора продолжалась в течение 120 сут с момента трансплантации (Vincenti et al., 1998). Заметных изменений в составе лимфоцитов крови не обнаружено. Базиликсимаб назначают по 20 мг за 2 ч до операции и через 4 сут после нее.
Побочные эффекты. Данные антитела не вызывают синдрома высвобождения цитокинов. При их приеме могут наблюдаться анафилактические реакции. Такие осложнения, как лимфопролиферативные заболевания и оппортунистические инфекции, при использовании антител к рецептору ИЛ-2 возникают значительно реже, чем при использовании других иммунодепрессантов. Лекарственных взаимодействий этих антител с другими препаратами пока не выявлено (Hong and Kahan, 1999). Инфликсимаб содержит химерные моноклональные антитела к ФНОа, состоящие из константного участка IgG, человека и вариабельного участка мышиных антител. Эти высокоаффинные антитела связываются с ФНОа и препятствуют его взаимодействию с рецептором.
При ревматоидном артрите повышен уровень ФНОа в суставах, а при болезни Крона — в кале. Клинические испытания показали, что сочетание метотрексата с инфликсимабом при ревматоидном артрите эффективнее, чем назначение одного метотрексата. При активной болезни Крона, устойчивой к лечению другими иммунодепрессантами, введение инфликсимаба приводило к улучшению, в частности уменьшению числа свишей. Инфликсимаб в комбинации с метотрексатом разрешен ФДА для лечения ревматоидного артрита при неэффективности монотерапии метотрексатом. Инфликсимаб разрешен также для лечения умеренной и тяжелой болезни Крона в случае неэффективности стандартного лечения, а также для уменьшения числа свищей при этом заболевании (гл. 39). Приблизительно у каждого шестого больного через 1—2 ч после введения антител проявляется побочное действие в виде лихорадки, крапивницы, артериальной гипотонии и одышки. После лечения инфлик-симабом описано развитие тяжелых инфекций, преимущественно инфекций верхних дыхательных путей и мочевых путей. Есть сообщения о появлении антинуклеар-ных антител и развитии волчаночного синдрома. Этанерцепт сходен с инфликсимабом по механизму действия, однако не является антителом, а представляет собой химерный белок, содержащий лиганд-связывающий участок человеческого рецептора ФНОа и Fc-фрагмент человеческого IgG,. Подобно инфликсимабу, этанерцепт связывается с ФНОа и препятствует его взаимодействию с рецептором. Препарат разрешен ФДА для лечения ревматоидного артрита при неэффективности других лекарственных средств. Этанерцепт применяют вместе с метотрексатом в случае безуспешности монотерапии последним. Применение этанерцепта, как и инфликсимаба, может приводить к серьезным инфекциям. Более чем в трети случаев наблюдается местная реакция на введение препарата — покраснение, зуд, боль и отек.
Иммунологическая толерантность[править | править код]
Иммуносупрессивная терапия повышает риск оппортунистических инфекций и вторичных опухолей. Поэтому главная задача исследований, посвященных трансплантации органов и аутоиммунным заболеваниям, — индукция и поддержание иммунологической толерантности, то есть активного состояния нечувствительности к определенным антигенам (Krensky and Clayberger, 1994; Нас-kett and Dickler, 1999). Достижение толерантности означало бы возможность излечения описанных выше состояний без побочных эффектов иммуносупрессивной терапии. В некоторых доклинических испытаниях показано, что ингибиторы кальциневрина препятствуют развитию толерантности (Wood, 1991; Van Parijs and Abbas,1998). Напротив, сиролимус на тех же моделях не только не препятствовал развитию толерантности, но и в некоторых случаях стимулировал ее (Li et al., 1998). Некоторые другие многообещающие подходы в настоящее время проверяются в клинических испытаниях. Все они остаются пока экспериментальными и поэтому обсуждаются здесь очень кратко.
Блокада костимуляции Т-лимфоцитов[править | править код]
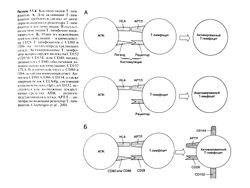
Для развития специфического иммунного ответа Т-лимфоцитам требуется два сигнала: антиген-специфический сигнал от антигенраспознаюшего рецептора Т-лимфоцитов и костимуля-ция, которую обеспечивают в основном молекулы CD28 Т-лим-фоцитов, взаимодействуя с CD80 или CD86, расположенными на поверхности антигенпредставляющих клеток (рис. 53.4) (Khoury et al., 1999). В экспериментальных исследованиях для блокады костимуляции применяли химерный белок CTLA4Ig и моноклональные антитела к СD80 и к СD86. Белок СТLA4Ig содержит связывающий участок молекулы CTLA-4 (CD 152), гомолога CD28, и константный участок IgG, человека. CTLA41g — конкурентный ингибитор CD28. Как CTLA4lg, так и лизирую-щие моноклональные антитела к CD80 сейчас проходят клинические испытания. Исследуется возможность воздействия и на другие пути костимуляции, в частности на молекулы, участвующие во взаимодействии CD40, расположенного на поверхности Т-лимфоцитов, с С040-лигандом (CD 154) на поверхности В-лимфоцитов, эндотелиальных и антигенпредставляющих клеток. Известно, что антитела к CD154 блокируют экспрессию CD80 в процессе иммунного ответа. Другие блокаторы костимуляции Т-лимфоцитов, такие, как моноклональные антитела к CD2, к ICAM-1 (CD54) и к а,Ь2-интегрину (CD1 la/CD18), также дали обнадеживающие результаты в доклинических испытаниях (Salmela et al., 1999).
Донорский химеризм[править | править код]
Один из многообещающих способов достижения иммунологической толерантности к трансплантату связан с установлением так называемого донорского химеризма, то есть сосуществования в организме реципиента клеток иммунной системы как самого реципиента, так и донора. Для индукции донорского химеризма применяют разные схемы, но все они основаны на частичном подавлении иммунной системы реципиента (с помощью ионизирующей радиации, циклофосфамида или антител к Т-лимфоцитам) с последующей трансплантацией костного мозга или стволовых клеток крови от донора (Starzl et al., 1997; Fuc-himotoetal., 1999; Spitzeretal., 1999; Haleetal., 2000). После восстановления иммунитета реципиент больше не распознает новые антигены, полученные при трансплантации, как чужие. Такая толерантность сохраняется надолго, и применения ингибиторов кальциневрина обычно не требуется. Хотя наиболее перспективным подходом в этой области является индукция так называемого смешанного хименизма, или макрохимеризма, при котором в крови присутствует значительное количество донорских клеток, разрабатываются также способы, позволяющие добиться иммунологической толерантности с помощью небольшого числа донорских клеток (микрохимеризм).
Растворимые молекулы HLA[править | править код]
Много лет назад, когда циклоспорин еще не применяли, было замечено, что переливания крови уменьшают риск отторжения почечного трансплантата (Opelz and Terasaki, 1978). Это наблюдение дало начало переливаниям крови от специально подобранных доноров для улучшения результатов трансплантации почки (Opelz et al., 1997). С началом применения циклоспорина этот эффект исчез, вероятно, из-за того, что циклоспорин эффективно подавляет активацию Т-лимфоцитов. Тем не менее влияние переливаний крови на индукцию иммунологической толерантности неоспоримо. Возможно, этот эффект опосредован расположенными на поверхности клетки или растворенными молекулами HLA. В опытах на животных показано, что растворимые молекулы Н LA и синтетические пептиды с той же последовательностью аминокислотных остатков, что и линейные участки молекул HLA, многими путями индуцируют иммунологическую толерантность (Murphy and Krensky, 1999).
Толерогены[править | править код]
Толерогены — специфические антигены, обычно в виде пептидов, индуцирующие иммунологическую толерантность в экспериментальных моделях сахарного диабета, ревматоидного артрита и рассеянного склероза. Сейчас некоторые из толерогенов проходят клинические испытания. В последнее десятилетие наши знания о механизмах иммунологической толерантности значительно расширились. Теперь хорошо известно, что комплекс антигена с молекулами HLA антигенпредставляющих клеток,взаимодействуя с комплексом антигенраспознающего рецептора Т-лимфоцитов и молекул CD3, вместе с растворимыми и мембраносвязанными костимулирующими молекулами запускают каскад событий, ведущих к развитию иммунного ответа. Помимо этого существуют механизмы подавления иммунного ответа, влияющие на выживание и пролиферацию клеток. В экспериментах как in vitro, так и in vivo уже показано, что можно избирательно подавить иммунный ответ на определенные антигены, не прибегая к известным методам иммуносупрессивной терапии, чреватым побочными эффектами (Van Parijs and Abbas. 1998). Эти открытия породили уверенность, что в будущем с помощью специфической иммунотерапии удастся излечить большинство заболеваний, опосредованных иммунной системой, включая аутоиммунные заболевания и отторжение трансплантата. Новые подходы могут включать комбинации препаратов, действующих в основном на Т-лимфоциты и блокирующих клеточные рецепторы или начальные этапы внутриклеточной передачи сигнала. Одновременно с ними можно будет назначать средства, которые эффективно блокируют костимуляцию, препятствуя пролиферации и дифференцировке Т-лим-фоцитов, а также выбросу провоспалительных цитокинов.
Рисунок 53.4. Костимуляция Т-лимфоцитов. А. Для активации Т-лимфоцитов требуются сигнал от анти-генраспознающего рецептора Т-лимфоцитов и костимуляция. В отсутствие костимуляции Т-лимфоцит инактивируется. Б. Один из важнейших путей костимуляции — взаимодействие CD28 Т-лимфоцитов с CD80 и CD86 на антигенпредставляющих клетках. Активированные Т-лимфоциты экспрессируют молекулы CD 152 и CD154. CD154, или ССЙО-лиганд, связывается с С1340, обеспечивая дополнительную костимуляцию. CD 152 (CTLA-4) взаимодействует с CD80 и CD86, ослабляя иммунный ответ. Антитела к CD80, CD86, CD 154, а также химерный белок CTLA4lg, состоящий из участков молекул lgG( и CD 152, исследуются как возможные лекарственные средства. АПК — антиген -представляющая клетка, АРТЛ — ан-тигенраспознаюший рецептор Т-лимфоцитов. Clayberger et al., 2001.
Иммуностимуляция[править | править код]
Основные принципы[править | править код]
В противоположность иммунодепрессантам, предназначенным для подавления иммунного ответа при отторжении трансплантата и аутоиммунных заболеваниях, препараты, стимулирующие иммунный ответ, применяют при инфекциях, иммунодефицитных состояниях и злокачественных новообразованиях. К сожалению, эффективность препаратов этой группы пропорциональна выраженности их побочного действия.
Иммуностимуляторы[править | править код]
Левамизол. Первоначально левамизол был получен как антигельминтный препарат, но затем обнаружилась его способность восстанавливать угнетенную функцию В- и Т-лимфоцитов, моноцитов и макрофагов. Единственное его применение — назначение вместе с фторурацилом в качестве адъювантной химиотерапии после хирургической операции при стадии С (по классификации Дьюкса) рака толстой кишки (Moertel etal., 1990; Figu-eredo et al., 1997). Левамизол может вызвать агранулоцитоз, иногда смертельный.
Талидомид больше известен как препарат, вызывавший тяжелые пороки развития у детей, чьи матери принимали его во время беременности (Smithells and Newman, 1992; Laryetal., 1999). По этой причине его применение ограничено специальными программами, и его могут назначить лишь врачи, имеющие специальную лицензию и полностью осознающие риск его тератогенного действия. Талидомид категорически противопоказан беременным и женщинам, которые могут забеременеть во время лечения. Показанием к назначению талидомида служит лепрозная узловатая эритема (Sampaio et al., 1993). Механизм действия талидомида не известен (Tseng et al., 1996). Его действие на иммунную систему в значительной степени зависит от конкретных условий. Есть сообщения, что при лепрозной узловатой эритеме талидомид снижает уровень ФНОа в крови, а при ВИЧ-инфекции — повышает его (Jacobson etal., 1997). Возможно, талидомид действует на ангиогенез (Miller and Stromland,1999). Снижение уровня ФНОа под действием талидомида позволяет надеяться, что он будет эффективен при тяжелом ревматоидном артрите, устойчивом к другим методам лечения (Ке-esaletal., 1999).
Вакцина БЦЖ. Это живая вакцина, полученная из аттенуированного штамма Mycobacterium bovis Кальметтом и Гереном. Вакцина БЦЖ стимулирует образование гранулемы в месте введения. Механизм противоопухолевого действия этого препарата не известен. Вакцину БЦЖ применяют для лечения и предотвращения рецидивов рака мочевого пузыря in situ, а также для предотвращения рецидивов после трансуретральной резекции первичных и рецидивирующих папиллярных опухолей на стадиях Та и Т1 (Morales et al., 1981; Paterson and Patel, 1998; Patard et al., 1998). Вакцина БЦЖ может вызвать аллергию, озноб, лихорадку, общее недомогание, шок; иногда развивается иммунокомплексная аллергическая реакция.
Цитокины и интерфероны. Помимо первоначально открытой противовирусной активности интерфероны а, β и γ обладают и выраженными свойствами иммуномодуляторов (Johnson et al., 1994; Tilg and Kaser, 1999; Ranso-hoff, 1998). Интерфероны связываются с мембранными рецепторами, что запускает ряд внутриклеточных процессов: индуцируются некоторые ферменты, подавляется пролиферация, активируется фагоцитоз макрофагов, повышается специфическая цитотоксичность Т-лимфоцитов (Tompkins, 1999). Методы генной инженерии позволяют получать рекомбинантный интерферон а-2Ь из культуры Escherichia coli. Это один из небольших белков с молекулярной массой 15 000—27 600, секретируемых клетками в ответ на вирусную инфекцию и некоторые стимулы. Интерферон а-2Ь применяют для лечения злокачественных новообразований, в том числе волосатоклеточного лейкоза, меланомы, лимфомы из клеток центра фолликула, а также саркомы Капоши при СПИДе (Punt, 1998; Bukowski, 1999; Sinkovicsand Horvath, 2000). Его назначают также при инфекционных заболеваниях, таких, как хронический гепатит В и остроконечные кондиломы. Кроме того, его применяют в комбинации с рибавирином для лечения хронического гепатита С у больных с компенсированной функцией печени, не получавших ранее интерферон а-2Ь, или при развитии рецидива после лечения этим препаратом (Lo Iacono et al., 2000). После введения интерферона а-2Ь иногда возникаютли-хорадка, озноб и головная боль. Реже наблюдается действие на сердечно-сосудистую систему (артериальная гипотония, аритмии, изредка — дилатационная кардиомиопатия и инфаркт миокарда) и ЦНС (депрессия, спутанность сознания).
Интерферон у-lb представляет собой рекомбинантный белок, отличающийся от других интерферонов тем, что он активирует фагоциты и способствует накоплению в них активных форм кислорода, токсичных для ряда микроорганизмов. Его применяют для снижения риска и тяжести инфекций, сопровождающих хроническую гранулематозную болезнь. Побочные эффекты включают лихорадку, головную боль, сыпь, быструю утомляемость, желудочно-кишечные нарушения, потерю аппетита, потерю веса, миалгию и депрессию.
Интерферон β-la (рекомбинантный гликопротеид из 166 аминокислотных остатков) и интерферон β-lb (рекомбинантный белок из 165 аминокислотных остатков) обладают противовирусным и иммуномодулирующим действием. Их применение одобрено ФДА для снижения частоты обострений при ремиттирующем течении рассеянного склероза. Наиболее распространенные побочные эффекты — гриппоподобные симптомы (лихорадка, озноб, миалгия) и реакция в месте инъекции.
Подробности применения интерферонов для лечения вирусных инфекций приведены в гл. 50.
Альдеслейкин. Этот препарат, представляющий собой человеческий рекомбинантный ИЛ-2, получают из культуры Escherichia coli (Taniguchi and Minami, 1993). В отличие от нативного ИЛ-2 альдеслейкин не гликозилиро-ван, не имеет аланина на N-конце, а в положении 125 находится серин вместо цистеина (Doyle et al., 1985). Активность препарата выражают в МЕ, определяемых по усилению пролиферации лимфоцитов, причем 1,1 мг альдеслейкина соответствует 18 млн МЕ. Альдеслейкин in vitro проявляет следующие свойства нативного ИЛ-2: усиливает пролиферацию лимфоцитов и рост ИЛ-2-за-висимых клеточных линий; усиливает цитотоксичность Т-лимфоцитов и активность NK-лимфоцитов; индуцирует синтез интерферона у (Winkelhake et al., 1990; Whittington and Faulds, 1993). У животных отмечено разнообразное дозозависимое действие препарата на иммунную систему, в том числе активация клеточного иммунитета, сопровождающаяся лимфоцитозом, эозинофилией, тромбоцитопенией и высвобождением большого количества цитокинов (ФНОа, ИЛ-1, интерферона у). Альдеслейкин назначают взрослым при метастазирующем раке почки и меланоме. Лечение иногда сопровождается серьезными нарушениями сердечно-сосудистой системы из-за повышения проницаемости капилляров, сопровождающегося потерей сосудистого тонуса и выходом белков плазмы во внесосудистое пространство. Снижается АД, возникает ишемия органов, возможен смертельный исход. В результате нарушения функции нейтрофилов возрастает риск генерализованных инфекций.
Иммунизация[править | править код]
Иммунизация может быть активной и пассивной. Активная иммунизация заключается в стимуляции иммунной системы определенным антигеном для развития эффективного иммунного ответа при последующей встрече с этим антигеном. При пассивной иммунизации вводятся готовые антитела непосредственно после контакта или перед контактом с вероятным антигеном.
Вакцины[править | править код]
При активной иммунизации (вакцинации) человеку вводят либо убитые, либо живые, но ослабленные (аттенуированные) микроорганизмы, либо белки или пептиды, характерные для определенного микроорганизма.
Часто необходимо проведение повторных вакцинаций,особенно при использовании убитых микроорганизмов. В США вакцинация позволила значительно снизить, вплоть до полного исчезновения, заболеваемость рядом тяжелых инфекций, таких, как дифтерия, корь, эпидемический паротит, коклюш, краснуха, столбняк и инфекция, вызванная Haemophilus influenzae типа В (Dorner and Barrett, 1999; The National Vaccine Advisory Committee, 1999).
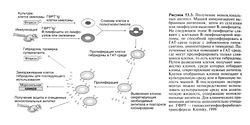
Хотя большая часть разрабатываемых вакцин направлена на борьбу с инфекционными заболеваниями, человечество стоит на пороге получения вакцин, направленных против злокачественных новообразований и аутоиммунных заболеваний (Lee et al., 1998; Del Vecchio and Parmiani, 1999; Simone et al., 1999). Такая иммунизация может обеспечить полную или частичную защиту от болезни. Раньше для получения противоопухолевых вакцин в качестве источника антигенов использовали целые опухолевые клетки или лизат из этих клеток, которые вводили вместе с различными адъювантами, предполагая, что антигенпредставляющие клетки, расщепив введенные белки, представят специфичные опухолевые антигены Т-лимфоцитам (Sinkovicsand Horvath, 2000). Эти вакцины иногда дают лечебный эффект, и сейчас их проверяют в клинических испытаниях. Основу противоопухолевых вакцин второго поколения составляют антиген представляющие клетки больного, инкубированные ex vivo с антигеном или экспрессирующие опухолевый антиген в результате трансфекции. Показано, что при введении лабораторным животным дендритных клеток, которые были предварительно инкубированы с пептидами опухолевых антигенов, обладающими сродством к молекулами HLA класса 1, наблюдается противоопухолевый ответ, обусловленный цитотоксическими Т-лимфоцита-ми (Tarte and Klein, 1999). Наконец, в многочисленных исследованиях на животных показана эффективность ДНК-вакцин при инфекционных заболеваниях и злокачественных новообразованиях (Lewis and Babiuk, 1999; Liljeqvist and Stahl, 1999). Преимущество ДНК-вакцин перед иммунизацией пептидами в том, что в первом случае отбор антигенных детерминант из синтезированного чужеродного белка происходит в самом организме, что позволяет не заботиться о соответствии пептидов и аллелей HLA, имеющихся в организме. Существуют определенные сомнения в безопасности применения этой технологии из-за риска встраивания плазмидной ДНК в геном клетки человека и инсерционного мутагенеза, иногда приводящего к злокачественной трансформации клетки. И наконец, последний способ вызвать или усилить иммунный ответ против специфических антигенов заключается в трансфекции клеток рекомбинантными вирусами, кодирующими интересующий антиген. Для трансфекции клеток млекопитающих используют, например, вирусы осповакцины, авипоксвирусы, лентивирусы или аденовирусы.
Иммуноглобулины[править | править код]
Пассивная иммунизация применяется в случае дефицита собственных антител при врожденном или приобретенном иммунодефиците, при высокой вероятности контакта с определенным антигеном, если времени для активной иммунизации недостаточно (корь, бешенство, гепатит В), атакже в случаях, когда иммуноглобулины могут оказать лечебное действие при уже развившемся заболевании (ботулизм, дифтерия, столбняк). Пассивная иммунизация может быть осуществлена разными препаратами (табл. 53.2). В зависимости от показаний можно использовать неспецифические (нормальный иммуноглобулин) или, наоборот, специфические иммуноглобулины. Защитный эффект обычно длится 1—3 мес. Нормальный иммуноглобулин получают из объединенной плазмы взрослых путем фракционирования охлажденным этанолом. Он содержит преимущественно IgG (95%) и показан при заболеваниях, сопровождающихся дефицитом антител, при инфекциях, например гепатите А и кори, и таких заболеваниях, как тромбоцитопеническая пурпура и синдром Гийена—Барре (Ballow, 1997; Jordan et al., 1998a; Jordan et al., 1998b). Наоборот, специфические иммуноглобулины (гипериммунный глобулин) отличаются от остальных препаратов иммуноглобулинов тем, что для их получения отбирают доноров с наивысшим титром данных антител. Специфические иммуноглобулины имеются для гепатита В, бешенства, столбняка, вируса varicella-zoster, цитомегаловируса и респираторного синцитиального вируса. AHTH-Rh0(D)-иммуноглобулин — специфический иммуноглобулин для профилактики гемолитической болезни новорожденных при несовместимости матери и плода по антигену D системы Rh. При использовании любых препаратов имеется риск передачи инфекции.
Таблица 53.2. Некоторые препараты иммуноглобулинов
- Нормальный иммуноглобулин для в/в введения
- Иммуноглобулин против цитомегаловируса
- Иммуноглобулин против респираторного синцитиального вируса
- Иммуноглобулин против вируса гепатита В
- Антирабический иммуноглобулин
- Анти-Rh0(D)-иммуноглобулин
- Противостолбнячный иммуноглобулин
Анти-Rh0(D)-иммуноглобулин. Этот препарат содержит высокий титр антител (IgG) к антигену D системы Rh, расположенному на поверхности эритроцитов. нти-Rh0(D)-HMMyHonio6ynHH получают из донорской плазмы с помощью фракционирования охлажденным этанолом с последующим проведением через систему очистки от вирусов (Bowman, 1998; Contreras, 1998; Lee, 1998). Всех доноров тщательно обследуют для уменьшения риска передачи инфекции. Механизм действия. Анти-Rh0(D)-иммуноглобулин связывает антиген D и предотвращает аллоиммунизацию организма (Ре-terec. 1995). Rh-отрицательная женщина может быть иммунизирована к чужеродному ей антигену D эритроцитов плода во f время родов, самопроизвольного аборта, внематочной беременности или любой фето-материнской трансфузии. Если в организме женщины развился первичный иммунный ответ, то при последующих беременностях антитела к антигену D могут проникать через плаценту и разрушать эритроциты плода. Этот смертельно опасный синдром назван гемолитической болезнью новорожденных. Введение анти-Rh0(D)-иммуноглобулина в большинстве случаев предупреждает развитие этой болезни, если ее причиной является несовместимость по антигену D.
Применение. Aнти-Rh0(D)-иммyнorлoбyлин вводят в/м Rh-отрицательной матери, если известно или предполагается, что эритроциты Rh-положительного плода попадают в кровоток матери. Т1/2 препарата составляет 21—29 сут.
Побочные эффекты. Возможны неприятные ощущения в месте введения, легкая лихорадка. Системные реакции крайне редки, однако есть сообщения о развитии миалгии, сонливости и анафилактического шока. Как и при использовании других препаратов плазмы, имеется риск передачи инфекций.
Перспективы[править | править код]
На протяжении 1990-х гг. большинство клиник при трансплантации использовали различные иммунодепрессанты в сочетании с индукционной иммуносупрессивной терапией антилимфоцитарными препаратами моноклональных или поликлональных антител. Для поддерживающей иммуносупрессивной терапии применяют ингибиторы кальциневрина (циклоспорин или такролимус), глюкокортикоиды и антиметаболиты (азатиоприн или микофеноловую кислоту). Микофеноловая кислота заменила азатиоприн в стандартных схемах лечения после трансплантации. В настоящее время ряд клиник проводят исследования новых комбинаций препаратов, включающих циклоспорин или такролимус в сочетании с глюкокортикоидами и микофеноловой кислотой, иногда в комбинации с индукционной иммуносупрессивной терапией препаратами антител. Ряд новых препаратов более эффективно предотвращает отторжение и делает трансплантацию почки, печени, поджелудочной железы или сердца более доступной. Эффективность новых комбинаций препаратов возрождает идею отмены глюкокортикоидов. Современная иммуносупрессивная терапия направлена на предотвращение отторжения, снижение повреждающего действия на трансплантат и других побочных эффектов. Разработка иммунодепрессантов продолжается, но главная цель трансплантологии — достижение иммунологической толерантности. Для успешной борьбы с отторжением трансплантата и с аутоиммунными заболеваниями необходимо создать такие препараты и схемы лечения, чтобы «обмануть» иммунную систему и вынудить ее принять чужое за свое или «переучить» клетки, повреждающие собственные ткани. Другое направление — разработка вакцин, которые оказались бы эффективными не только при многочисленных инфекциях (таких, как туберкулез и ВИЧ-инфекция), но и при злокачественных новообразованиях и аутоиммунных заболеваниях. Новые подходы в иммунотерапии не только направлены на повышение эффективности и снижение токсичности препаратов, но и будут иметь важные экономические последствия и отразятся на полноценности жизни.