Ингибиторы синтеза белка
Источник:
Клиническая фармакология по Гудману и Гилману том 3.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Ингибиторы синтеза белка[править | править код]
В этой статье рассматриваются следующие антимикробные средства: 1) бактериостатические ингибиторы синтеза белка, действующие главным образом путем связывания с рибосомами, 2) препараты, подавляющие синтез неточной стенки (кроме бета-лактамных антибиотиков), 3) антимикробные средства, применяемые только по особым показаниям. К первой группе относятся тетрациклины, хлорамфеникол, макролиды, клиндамицин, стрептограмины и линезолид. Тетрациклины — антибиотики широкого спектра действия, активные в отношении грамположительных и грамотрицательных бактерий (как аэробных, так и анаэробных), риккетсий, микоплазм и хламидий. Однако за последние 10 лет терапевтическая ценность этих препаратов значительно снизилась из-за широкого распространения устойчивых штаммов. Хлорамфеникол назначают только при угрожающих жизни состояниях (например, при риккетсиозах, больным с бактериальным менингитом, которым нельзя назначить другой препарат), так как обмажет вызвать апластическую анемию. Макролиды (эритромицин, кларитромицин, азитромицин) применяют в первую очередь при пневмонии, так как они активны в отношении Streptococcus pneumoniae и возбудителей атипичной пневмонии. Кларитромицин и азитромицин используют для профилактики и лечения инфекций, вызванных атипичными микобактериями. Клиндамицин, антибиотик из группы линкозамидов, оказывает выраженное бактериостатическое действие на стрептококки, стафилококки и анаэробные микроорганизмы, включая Bacteroides fragilis. Кроме того, клиндамицин эффективен при пневмоцистозе и токсоплазмозе. Хинупристин/дальфопристин — комбинацию двух стрептограминов — применяют парентерально при инфекциях, вызванных полирезистентными грамположительными бактериями, в частности устойчивыми к ванкомицину штаммами Enterococcus faecium. Линезолид, препарат из группы оксазолидинонов, активен в отношении энтерококков, устойчивых к ванкомицину, и Staphylococcus aureus, устойчивых к метициллину. Перекрестная устойчивость для линезолида не характерна, так как он действует на более ранних этапах синтеза белка, чем другие препараты с подобным механизмом действия. Ванкомицин активен в отношении стрептококков, энтерококков, всех штаммов Staphylococcus aureus, исключая редко встречающиеся умеренно устойчивые штаммы, и почти всех штаммов коагулазотрицательных стафилококков. Это единственный гликопептидный антибиотик, разрешенный к применению в США. В Европе применяют и другой гликопептидный антибиотик, тейкопланин; его единственное преимущество перед ванкомицином — возможность в/м введения. Бацитрацин действует на аэробные грамположительные бактерии. Бацитрацин используют только местно, поскольку при системном применении он нефротоксичен. Спектиномицин. представитель аминоциклитолов, назначают только больным с гонококковой инфекцией, которым противопоказаны препараты первого ряда. Полимиксин В активен в отношении аэробных грамотрицательных палочек, включая Pseudomonas aeruginosa. Из-за высокой нефротоксичности при системном введении препарат выпускают только в виде мазей и растворов для промывания. Настоящая глава посвящена фармакологическим свойствам и клиническому применению перечисленных выше препаратов.
Спектиномицин[править | править код]
Химические свойства и источники[править | править код]
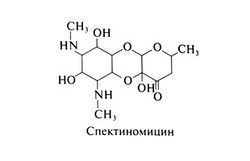
Спектиномицин — антибиотик, продуцируемый Streptomyces spectabilis. По структуре препарат представляет собой аминоциклитол. Структурная формула спектиномицина следующая:
Антимикробная активность и механизм действия[править | править код]
Спектиномицин действует на ряд грамотрицательных бактерий, но уступает в этом отношении другим препаратам, к которым эти микроорганизмы чувствительны (Schoutens et al., 1972). Спектиномицин применяют при гонорее, вызванной устойчивыми к препаратам первого ряда штаммами, а также при наличии противопоказаний к этим препаратам. Устойчивость к спектиномицину встречается редко (Clendennen et al., 1992).
Спектиномицин избирательно подавляет синтез белка у грамотрицательных бактерий. Препарат связывается с 30S-субъединицей рибосом и действует подобно аминогликозидам, но, в отличие от них, не оказывает бактерицидного действия и не нарушает считывание мРНК. Устойчивость к спектиномицину обусловлена изменением мишени препарата вследствие мутации или его инактивацией бактериальным ферментом (Clarket I al., 1999).
Фармакокинетика[править | править код]
Спектиномицин быстро всасывается при в/м введении. После введения в дозе 2 г максимальная сывороточная концентрация достигается через 1 ч и составляет 100 мкг/мл. Через 8 ч после инъекции она снижается примерно до 15 мкг/мл. Спектиномицин почти не связывается с белками плазмы и полностью выводится с мочой в течение 48 ч.
Применение[править | править код]
Согласно рекомендациям Центра по контролю заболеваемости, для лечения неосложненной гонококковой инфекции применяют цефтриаксон, цефиксим, ципрофлоксацин или офлоксацин. Спектиномицин назначают в случае непереносимости бета-лактамных антибиотиков и фторхинолонов или аллергии к этим препаратам. Спектиномицин назначают также беременным, которые плохо переносят β-лактамные антибиотики, так как фторхинолоны при беременности противопоказаны. Препарат вводят в дозе 2 г глубоко в/м однократно. Один из недостатков спектиномицина состоит в том, что он не действует на возбудителей сифилиса и хламидиоза. Кроме того, этот препарат малоэффективен при гонококковом фарингите, поэтому излечение должно быть подтверждено посевом.
Побочные эффекты[править | править код]
Однократное в/м введение спектиномицина редко сопровождается побочными эффектами (Duncan et al., 1972). Возможны крапивница, озноб, лихорадка, тошнота, головокружение и бессонница. Инъекции бывают болезненными.
Полимиксин В и колистин[править | править код]
При парентеральном введении эти препараты очень нефротоксичны, поэтому в настоящее время их обычно назначают местно.
Химические свойства и источники[править | править код]
Полимиксины — близкие по строению антибиотики, вырабатываемые некоторыми штаммами аэробной спорообразующей палочки Bacillus polymyxa, обнаруженной в почве. Они были открыты в 1947 г. Колистин (полимиксин Е) продуцируется Paenibacillus polymyxa (Bacillus nolymyxa)— микроорганизмом, который был выделен из пробы почвы, взятой в префектуре Фукусима (Япония). Полимиксины представляют собой основные полипептиды с молекулярной массой около 1000. Полимиксин В (смесь полимиксинов В1 и В2) имеет следующую структурную формулу:
Колистин (полимиксин Е) по строению сходен с полимиксином В. Колистин выпускают не только для местного применения, но и для приема внутрь (колистина сульфат) и парентерального введения (колистина мезилат).
Антимикробная активность и механизм действия[править | править код]
Полимиксин В и колистин активны в отношении грамотрицательных бактерий, включая Enterobacter spp., Esherichia coli, Klebsiella spp., Salmonella spp., Pasteurella spp., Bordetella spp. и Shigella spp., в концентрации 0,05—2 мкг/мл. In vitro рост большинства штаммов Pseudomonas aeruginosa подавляется при концентрации менее 8 мкг/мл.
Полимиксины представляют собой амфифильные (содержат и гидрофильные, и гидрофобные группы) катионные поверхностно-активные соединения. Взаимодействуя с фосфолипидами, полимиксины нарушают структуру бактериальных мембран и повышают их проницаемость. Изменение проницаемости мембраны происходит сразу после контакта бактериальной клетки с препаратом. Чувствительность к полимиксину В, видимо, определяется содержанием фосфолипидов в клеточной стенке бактерий (Brown and Wood, 1972). У некоторых устойчивых к полимиксину В микроорганизмов клеточная стенка защищает цитоплазматическую мембрану от действия препарата.
Полимиксин В связывается с липидом А (компонент эндотоксина, представляющего собой липополисахарид наружной мембраны грамотрицательных бактерий) и инактивирует его. Поданным экспериментальных исследований, препарат ослабляет выраженность патофизиологических изменений, вызванных высвобождением эндотоксина (Shenep et al., 1984; Tauber et al., 1987), хотя клиническое значение этого пока не установлено.
Фармакокинетика[править | править код]
Ни полимиксин В, ни колистин не всасываются при приеме внутрь. Кроме того, они плохо всасываются со слизистых и с поверхности обширных ожогов.
Применение[править | править код]
Полимиксина В сульфат используют местно (в том числе при болезнях глаз и уха), комбинируя его с другими препаратами для местного применения. Парентеральное введение не рекомендуется, хотя соответствующие лекарственные формы до сих пор выпускаются.
При инфекциях кожи, слизистых, глаз и уха, вызванных чувствительными к полимиксину В микроорганизмами, препарат применяют в виде раствора или мази. Полимиксин В эффективен при наружном отите, возбудителем которого чаще всего бывают Pseudomonas spp. Язвы роговицы, вызванные Pseudomonas aeruginosa, обычно излечиваются при местном нанесении препарата или инъекциях под конъюнктиву.
Побочные эффекты[править | править код]
При нанесении на кожу и слизистые, даже поврежденные, полимиксин В почти не всасывается и потому не вызывает системных побочных эффектов. Аллергические реакции при местном применении редки. Побочные эффекты, возникающие после парентерального введения полимиксина В и колистина.
Тейкопланин[править | править код]
Химические свойства и источники[править | править код]
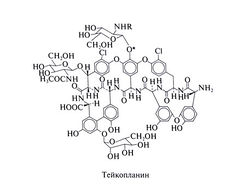
Тейкопланин — гликопептидный антибиотик, вырабатываемый Actinoplanes teichomyetius. Препарат представляет собой смесь шести близких по строению соединений, различающихся радикалом у атома кислорода, помеченного звездочкой (см. ниже). У одного из них этот атом соединен с водородом, у пяти других — с радикалами, в которых символом R обозначен остаток н-8,9-диметилдекановой кислоты или 8-метилнонановой кислоты. Тейкопланин применяется только в Европе, в США он пока не одобрен. По химическому строению, механизму действия, антимикробному спектру и путям элиминации тейкопланин подобен ванкомицину. Структурная формула тейкопланина следующая:
Механизм действия и устойчивость[править | править код]
Тейкопланин, как и ванкомицин, нарушает синтез клеточной стенки и активен только в отношении грамположительных бактерий. На чувствительные микроорганизмы он оказывает бактерицидное действие (на энтерококков — бакгериостатическое). Тейкопланин активен в отношении чувствительных и устойчивых к метициллину стафилококков (МПКдля них обычно ниже 4 мкг/мл; Wiedemann and Atkinson, 1991). Для Listeria monocytogenes, Corynebacterium spp., Clostridium spp. и анаэробных грамположительных кокков МПК колеблется от 0,25 до 2 мкг/мл. Рост стрептококков (в том числе зеленящих и Streptococcus pneumoniae) и энтерококков подавляется при концентрации 0,01—1 мкг/мл. Некоторые штаммы стафилококков (в том числе Staphylococcus aureus), энтерококков и других бактерий, обладающих природной устойчивостью к ванкомицину (Lactobacillus spp. и Leuconos-toc spp.), устойчивы и к тейкопланину.
Механизмы устойчивости стафилококков к тейкопланину не изучены. Чувствительный штамм может приобрести устойчивость в процессе лечения (Kaatz et al., 1990). Энтерококки с фенотипом Van А устойчивы и к ванкомицину, и к тейкопланину. Механизм устойчивости тот же, что и для ванкомицина: изменение мишени (клеточной стенки), препятствующее связыванию антибиотика. Штаммы энтерококков с фенотипом Van В часто чувствительны к тейкопланину, так как последний лишь слабо индуцирует ферменты, изменяющие строение клеточной стенки. Штаммы энтерококков с фенотипом Van С, обычно не патогенные для человека, чувствительны к тейкопланину (Arthur and Courvalin, 1993).
Фармакокинетика[править | править код]
По сравнению с ванкомицином тейкопланин в большей степени связывается с белками плазмы (на 90—95%) и гораздо медленнее элиминируется (Ту2 до 100 ч при нормальной функции почек). Кроме того, тейкопланин можно вводить в/м. Взрослым его назначают в дозе 6—30 мг/кг/сут (более высокие дозы используют только при тяжелых стафилококковых инфекциях). Благодаря медленной элиминации в большинстве случаев препарат можно вводить 1 раз в сутки. При почечной недостаточности дозу тейкопланина, как и дозу ванкомицина, уменьшают. Больным с нефункционирующими почками (находящимся на диализе) тейкопланин можно вводить I раз в неделю. При этом необходимо следить, чтобы сывороточная концентрация препарата находилась в пределах терапевтического диапазона (в частности, минимальная концентрация должна составлять 15—20 мкг/мл).
Применение[править | править код]
Тейкопланин применяют при многих инфекциях, включая остеомиелит и эндокардит, вызванные стафилококками (метициллиноустойчивыми и метициллиночувствительными), стрептококками и энтерококками (Bibleret al., 1987; Glup-czynski et al., 1986). По эффективности тейкопланин сравним с ванкомицином. Однако при тяжелых инфекциях лечение низкими дозами безуспешно (Calain etal., 1987). При сепсисе и эндокардите, вызванных метициллиночувствительными штаммами Staphylococcus aureus, тейкопланин уступает пенициллинам, активным в отношении стафилококков (частота излечения составляет соответственно 60—70 и 85—90%). Чтобы добиться усиления антимикробной активности в отношении Staphylococcus aureus, тейкопланин комбинируют с аминогликозидами (например, гентамицином), поскольку с ними препарат действует синергично. При нормальной функции почек гентамицин назначают в дозе 1 мг/кг каждые 8 ч. К тейкопланину чувствительны все стрептококки. Назначение препарата 1 раз в сутки достаточно для излечения стрептококкового остеомиелита и эндокардита (Leport et al., 1989). Тейкопланин — один из самых активных препаратов в отношении энтерококков. Опыт его применения пока невелик, но тем не менее позволяет заключить, что тейкопланин эффективен при тяжелых энтерококковых инфекциях (например, эндокардите). Для достижения бактерицидного эффекта препарат комбинируют с гентамицином.
Побочные эффекты[править | править код]
Основной побочный эффект тейкопланина — сыпь. Чаше всего она возникает при использовании больших доз. Возможны также аллергические реакции, лихорадка и нейтропения. Изредка возникает ототоксический эффект.
Бацитрацин[править | править код]
Историческая справка[править | править код]
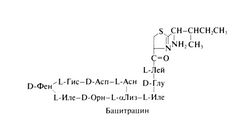
Бацитрацин — антибиотик, вырабатываемый Bacillus subtilis, штаммом Tracy-1. Этот штамм был выделен в 1943 г. из материала (смесь уличной грязи и поврежденных тканей), полученного при хирургической обработке открытого перелома удевочки по фамилии Трейси. И выделенный штамм, и сам антибиотик (bacitracin) названы в ее честь. История открытия, свойства и применение бацитрацина были описаны в 1949 г. Мелени и Джонсоном (Meleney and Johnson, 1949). Химические свойства. Бацитрацины — это группа полипептидных антибиотиков. В состав выпускаемых в настоящее время препаратов входят несколько соединений. Основной компонент — бацитрацин А Одна единица бацитрацина эквивалентна 26 мкг. Предполагаемая структурная формула бацитрацина А следующая:
Антимикробная активность и механизм действия[править | править код]
В концентрации 1 ед/мл бацитрацин действует на ряд грамположительных кокков и палочек, Neisseria spp., Haemophilus influenzae и Treponema pallidum. Рост Actinomyces spp. и Fusobacterium spp. подавляется при концентрации препарата 0,5—5 ед/мл. Энтеробакге-рии, Pseudomonas spp., Candida spp. и Nocardia spp. устойчивы к нему. Бацитрацин угнетает синтез клеточной стенки бактерий.
Применение[править | править код]
Раньше бацитрацин назначали парентерально. Хотя лекарственные формы для парентерального введения выпускают до сих пор, в настоящее время препарат применяют преимущественно местно. Существуют мази с бацитрацином (в том числе глазная), а также порошок, из которого готовят раствор для местного применения. Мазь наносят непосредственно на пораженные участки не реже 1 раза в сутки. Выпускают также комбинированные препараты для местного применения, содержащие помимо бацитрацина неомицин, полимиксин В и гидрокортизон.
При фурункулезе, пиодермии, карбункуле, импетиго и абсцессах эффективность местного применения бацитрацина (самого по себе или в сочетании с другими антимикробными средствами) не доказана. Если инфицированная поверхность открытая (например, при язвах, вторичных инфекциях на фоне зудящих дерматитов), бацитрацин уничтожает чувствительные к нему микроорганизмы. Даже в виде мази он редко вызывает аллергические реакции, что выгодно отличает его от других антимикробных средств для местного применения. Местное применение бацитрацина эффективно при гнойном конъюнктивите и инфицированных язвах роговицы (если возбудителями служат чувствительные к препарату бактерии). При носительстве стафилококков в носоглотке препарат малоэффективен. Есть сведения об успешном применении бацитрацина внутрь при псевдомембранозном колите (Dudley et al., 1986).
Побочные эффекты[править | править код]
При парентеральном введении бацитрацин оказывает выраженное нефротоксическое действие. При местном применении изредка возникают аллергические реакции.
Читайте также[править | править код]
- Тетрациклины
- Левомицетин(хлорамфеникол)
- Макролиды (эритромицин, кларитромицин, азитромицин)
- Клиндамицин