Местные анестетики
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Местные анестетики[править | править код]
Местные анестетики уменьшают или устраняют боль, блокируя распространение возбуждения по нервам. Они взаимодействуют со специфическими рецепторами в просвете быстрых натриевых каналов, препятствуя току ионов через эти каналы. Обычно действие местных анестетиков ограничено зоной введения и быстро прекращается за счет диффузии в окружающие ткани. Химические и фармакологические свойства каждого препарата определяют показания к его клиническому применению. В зависимости от способа введения местного анестетика различают поверхностную, инфильтрационную, инфильтрационно-проводниковую (блокаду обширных полей), проводниковую, в/в регионарную, спинномозговую и эпидуральную анестезию. В этой главе обсуждаются механизм действия местных анестетиков, показания к их применению, пути введения и побочные эффекты.
Общие сведения[править | править код]
В достаточной концентрации местные анестетики обратимо подавляют генерацию потенциала действия, блокируя распространение возбуждения по нервам. Они могут действовать на любые отделы нервной системы и на все виды нервных волокон, вызывая как потерю чувствительности, так и местный паралич. Эффекты местных анестетиков, введенных в терапевтических дозах, полностью обратимы: функция нерва восстанавливается, а признаки повреждения нервных волокон или нейронов отсутствуют.
Историческая справка. Анестезирующие свойства первого местного анестетика — кокаина — были открыты случайно во второй половине XIX века. Кокаин в большом количестве содержится в листьях коки (Erythroxylum coca). Жители Анд еще много веков назад использовали экстракт этих листьев, оказывающий психостимулирующее действие и вызывающий эйфорию. Кокаин был впервые выделен Альбертом Ниманом в 1860 г. Как это было принято среди химиков в то время, Ниман попробовал новое вещество на вкус и заметил, что при этом немеет язык. Физиологические свойства кокаина изучал Зигмунд Фрейд, а Карл Коллерв 1884 г. стал использовать кокаин в качестве местного анестетика при офтальмологических операциях. Вскоре Халстед предложил применять кокаин для инфильтраиионной и проводниковой анестезии. Эти открытия привели к созданию множества местных анестетиков, применяемых в настоящее время.
Химические свойства[править | править код]
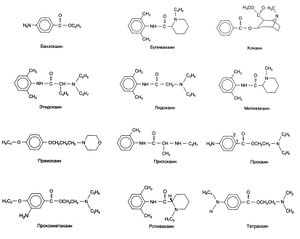
Структурно-функциональная зависимость. Кокаин — сложный эфир бензойной кислоты и 3-гидрокси-2-карбометокситропана (рис. 15.1). Высокая токсичность кокаина и его способность вызывать зависимость (гл. 24) ограничивают его применение, и поэтому уже в 1892 г. Эйнгорн и сотр. начали искать его синтетические аналоги. В 1905 г. был синтезирован прокаин, ставший на протяжении почти полувека основным и эталонным местным анестетиком. В настоящее время наиболее распространены прокаин, лидокаин, бупивакаин и тетракаин.
Из рис. 15.1 видно, что у типичных местных анестетиков имеются гидрофильная и гидрофобная части, соединенные эфирной или амидной связью. Вещества самых разных химических групп, обладающие таким строением, могут действовать как местные анестетики. Гидрофильная часть часто представляет собой третичный амин, хотя может быть и вторичным амином, гидрофобная часть должна иметь ароматическую структуру. фармакологические свойства местного анестетика определяются характером связи между гидрофильной и гидрофобной частями. Например, препараты с эфирной связью легко гидролизуются эстеразами плазмы.
Подробно о физико-химических свойствах местных анестетиков и о взаимосвязи их структуры и активности можно прочитать, например, в обзоре Courtney and Strichartz (1987). В целом, чем препараты гидрофобнее, тем выше их активность и продолжительность действия. Это объясняется тем, что связывание таких препаратов с гидрофобными структурами тканей увеличивает их концентрацию в тканях и предохраняет от разрушения эстеразами плазмы и печеночными ферментами. Кроме того, полагают, что участки натриевых каналов, с которыми взаимодействуют местные анестетики, также гидрофобны (см. ниже); следовательно, гидрофобные препараты характеризуются большим сродством к рецептору. Однако с увеличением гидрофобности возрастает и токсичность местных анестетиков, и соответственно сужается их терапевтический диапазон.
Размер молекул местного анестетика также определяет длительность его взаимодействия с рецептором (Courtney and Strichartz, 1987). Чем меньше молекула, тем быстрее она отсоединяется от рецептора. Эффект таких препаратов существенно зависит от частоты импульсации в ткани, на которую они действуют (см. ниже, «Частотозависимость и потенциалзависимость действия местных анестетиков»).
Механизм действия[править | править код]
Местные анестетики блокируют возникновение и проведение нервного импульса. Точкой их приложения служит клеточная мембрана: блокаду проведения нервного импульса можно вызвать и в перфузируемом гигантском аксоне кальмара (в этом препарате аксоплазма заменена на солевой раствор).
В основе действия местных анестетиков лежит уменьшение или полное подавление временного увеличения натриевой проницаемости, в норме вызываемого небольшой деполяризацией (гл. 12; Strichartz and Ritchie, 1987). Это свойство местных анестетиков обусловлено их прямым взаимодействием с быстрыми натриевыми каналами. По мере действия анестетика на нерв порог возбудимости постепенно возрастает, скорость нарастания потенциала действия уменьшается, проведение замедляется и фактор надежности проведения понижается. Все это затрудняет распространение потенциала действия и в конечном счете вызывает блокаду проведения.
Помимо быстрых натриевых каналов местные анестетики могут взаимодействовать и с другими мембранными белками (Butterworth and Strichartz, 1990), в частности блокировать калиевые каналы (Strichartz and Ritchie, 1987). Однако, поскольку этот эффект возникает лишь при высокой концентрации местного анестетика, блокада проведения не сопровождается существенными изменениями потенциала покоя.
Четвертичные аналоги местных анестетиков блокируют проведение лишь при введении внутрь перфузируе-мого гигантского аксона кальмара; при воздействии на аксон снаружи проведение не нарушается. Это позволяет предположить, что точка приложения местных анестетиков достижима лишь со стороны цитоплазмы (Narahashi and Frazier, 1971; Strichartz and Ritchie, 1987). Таким образом, для того, чтобы эти препараты оказывали свое действие, они должны пройти через мембрану.
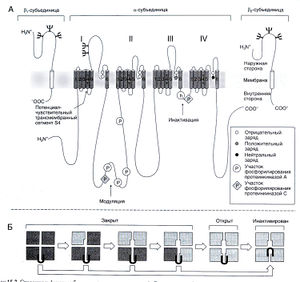
Существовали различные гипотезы молекулярного механизма действия местных анестетиков (Courtney and Strichartz, 1987). Однако в настоящее время общепринято, что местные анестетики взаимодействуют с одним или более специфическими рецепторами внутри быстрых натриевых каналов (Butterworth and Strichartz, 1990). Биохимические, биофизические и молекулярно-биологические исследования двух последних десятилетий существенно расширили представления о строении и функции этих и других потенциалзависимых каналов (гл. 12; Catterall,2000). Натриевые каналы головного мозга млекопитающих — это гетеротримерные комплексы гликозилированных белков. В этих комплексах, общая молекулярная масса которых превышает 300 000, различают а-субъединицу (молекулярная масса — 260 000), β1субъединицу (молекулярная масса — 36 000) и β2-субъединицу (молекулярная масса — 33 000). Альфа-субъединица состоит из четырех гомологичных доменов (I—IV), каждый из которых содержит шесть трансмембранных а-спирапьных сегментов (SI—S6; рис. 15.2) и внутримембранную петлю. Полагают, что собственно натриевый канал (трансмембранная пора, избирательно пропускающая ионы натрия) располагается в центре почти симметричной структуры, образованной четырьмя указанными доменами. Канал открывается за счет смещения потенциалчув-ствительных (воротных) структур в ответ на изменение мембранного потенциала. Потенциалчувствительные структуры входят в состав четвертых сегментов (S4) всех доменов. Эти сегменты гидрофобны и несут положительный заряд, поскольку содержат положительно заряженные остатки лизина или аргинина в каждом третьем положении. Полагают, что при изменениях мембранного потенциала эти остатки смещаются перпендикулярно плоскости мембраны, запуская ряд последовательных конформационных изменений во всех четырех доменах; это в конечном счете ведет коткрыванию канала (рис. 15.2; Catterall, 1988).
Описание к рис. 15.2. Строение и функция быстрого Натриевого канала. А. Двумерное изображение быстрого натриевого канала головного мозга млекопитающих. Вне- и внутриклеточные петли изображены непрерывными линиями соответствующей длины; трансмембранные сегменты представлены в виде цилиндров. Знаком Щ обозначены участки гликозилирования. Видно, что строение всех четырех гомологичных доменов а-субъединицы одинаково. Активация. Сегменты S4 каждого домена а-субъединицы служат по-тенциалчувствительными структурами. Они несут положительный заряд (обозначен «+»), поскольку содержат положительно заряженные аминокислотные остатки в каждом третьем положении. Электрический заряд внутри клетки в покое отрицателен, и поэтому эти остатки притягиваются в направлении внутриклеточной поверхности мембраны. Пора. Трансмембранные сегменты S5 и S6, а также короткая внутримембранная петля между ними (сегменты SS1 и SS2 на рис. 15.3) формируют стенки поры в центре почти симметричного четырехугольника, образованного четырьмя доменами а-субъединицы (см. также рис. 15.2, Б). Аминокислотные остатки, обозначенные кружками в сегменте SS2, играют ключевую роль для проницаемости и избирательности канала, а также для связывания и действия блокаторов натриевых каналов тетродотоксина и сакситоксина. Инактивация. Короткая внутриклеточная петля между доменами 111 и IV играет роль инактивационных ворот. Полагают, что эта петля закрывает внутреннее устье канала через несколько миллисекунд после его открывания. Видимо, основное значение имеют три гидрофобных остатка (Иле— Фен—Мет), отмеченные на рисунке буквой «И»: они проникают во внутреннее устье канала и связываются со специфическим рецептором. Модуляция. Функция быстрого натриевого канала может меняться при фосфорилировании его структур. Так, фосфори-лирование протеинкиназой С инактивационных ворот между доменами III и IV замедляет инактивацию, а фосфорилирование участков внутриклеточной петли между доменами I и II протеинкиназой А или С уменьшает активацию. Б. Схематичное изображение четырехугольного расположения четырех доменов а-субъединицы (вид сверху). Представлена последовательность конфор-мационных изменений натриевого канала во время активации и инактивации. Во время деполяризации каждый из четырех доменов претерпевает конформационные изменения, приводящие к его активации. Как только все четыре домена активированы, канал открывается. Спустя несколько миллисекунд инактивационные ворота между доменами III и IV закрывают внутреннее устье канала, препятствуя дальнейшему току натрия. Catterall, 1988.
Трансмембранная пора натриевого канала, по-видимому, образована сегментами S5 и S6, а также короткими сегментами SS1 и SS2, расположенными между ними и формирующими внутримембранную петлю. Аминокислотные остатки этих коротких сегментов играют ключевую роль в проводимости и избирательности канала.
Через несколько миллисекунд после открывания натриевые каналы закрываются. Этот процесс называется инактивацией. Инактивационные ворота образованы короткой внутриклеточной петлей, соединяющей домены III и IV (рис. 15.2). При инактивации эта петля прикрывает внутреннее устье канала — возможно, связываясь с рецептором в области краев этого устья.
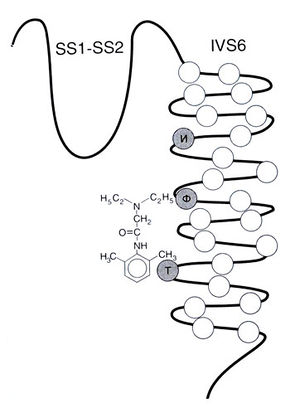
Аминокислотные остатки, участвующие во взаимодействии с местными анестетиками, обнаружены в сегменте S6 IV домена (Ragsdale et al., 1994). Гидрофобные аминокислотные остатки, расположенные в центре и в области внутриклеточного конца сегмента S6, могут непосредственно связываться с местным анестетиком (рис. 15.3). В эксперименте замена большего гидрофобного аминокислотного остатка (изолейцина) на меньший (аланин) в области внеклеточного конца сегмента S6 позволяет ионизированным молекулам местного анестетика пройти из внеклеточной жидкости к рецептору. Все это позволяет предположить, что рецептор, с которым взаимодействует местный анестетик, находится в области внутриклеточного конца натриевого канала и по крайней мере часть его образована аминокислотными остатками сегмента S6IV домена.
Описание к рис. 15.3. Рецептор местных анестетиков. Са-спиральным трансмембранным сегментом S6 IV домена (IVS6) соединены короткие сегменты SS1 и SS2, участвующие в формировании наружного устья канала. Кружками обозначены аминокислотные остатки в сегменте IVS6. Серым выделены три аминокислотных остатка, которым принадлежит основная роль во взаимодействии с местным анестетиком. Изображен местный анестетик лидокаин, связанный с двумя из этих остатков — Фен1764 (Ф) и Тир1771 (Т). Третий, отмеченный серым, остаток — Иле1760 (И). Его замещение меньшим аминокислотным остатком аланином с помощью направленного мутагенеза позволяет местным анестетикам проникать к рецептору снаружи; следовательно, Иле1760 формирует наружную границу рецептора. Ragsdale et al., 1994.
Частотозависимость и потенциалзависимость действия местных анестетиков. Выраженность блокады нерва под действием местного анестетика зависит от параметров раздражения нерва и от потенциала покоя. В состоянии покоя нерв намного менее чувствителен к местному анестетику, чем при непрерывной стимуляции. Чем выше частота стимуляции нерва и меньше (положительнее) потенциал покоя, тем сильнее действие анестетика на нерв.
Такая частото- и потенциалзависимость действия местного анестетика объясняется следующими моментами:
- ионизированные молекулы этих веществ достигают рецептора внутри быстрого натриевого канала только тогда, когда этот канал пребывает в открытом состоянии,
- местные анестетики прочнее связываются с рецепторами при инактивированном состоянии натриевого канала и стабилизируют его в этом состоянии (Courtney and Strichartz, 1987; Butterworth and Strichartz, 1990).
Эти свойства местных анестетиков зависят от их рКа липофильности и размера молекулы. Так, частотозависимость действия местного анестетика определяется скоростью его диссоциации из комплекса с рецептором, а эта скорость тем выше, чем мельче и гидрофобнее молекула. Дело в том, что быстро диссоциирующие препараты активнее при высокой частоте раздражения нерва, поскольку только при такой частоте связывание с рецептором во время потенциала действия преобладает над диссоциацией в состоянии покоя. Частотозависимость блокады ионных каналов особенно важна для антиаритмических средств (гл. 35).
Зависимость чувствительности к местным анестетикам от типа нервного волокна[править | править код]
Несмотря на значительные индивидуальные особенности, в большинстве случаев после введения местного анестетика сначала исчезает болевая чувствительность, затем температурная, тактильная, проприоцептивная и, в последнюю очередь, развивается парез (табл. 15.1). Классические эксперименты на целых нервных стволах показали, что волна А5 составного потенциала действия, отражающая проведение возбуждения по медленным тонким миелиновым волокнам, уменьшается раньше и при меньших концентрациях кокаина, чем волна Аа, отражающая проведение по быстрым толстым волокнам (Gasser and Erlanger, 1929). В целом вегетативные волокна, тонкие безмиелиновые волокна группы С (болевая чувствительность) и тонкие миелиновые волокна группы А5 (болевая и температурная чувствительность) блокируются местными анестетиками раньше, чем толстые миелиновые волокна групп Ау, Ар и Аа (тактильная и проприоцептивная чувствительность и управление скелетными мышцами) (Raymond and Gis-sen, 1987). Различная скорость блокирования нервных волокон, отвечающих за проведение разных видов чувствительности, имеет большое практическое значение.
Точная причина различной чувствительности нервных волокон к местным анестетикам не известна. На сегодняшний день есть несколько предположений. Согласно классической гипотезе, основанной на экспериментах с целыми нервными стволами, чувствительность нервных волокон к местным анестетикам уменьшается с увеличением их толщины. В результате тонкие волокна, проводящие боль, характеризуются высокой чувствительностью к анестетикам, а толстые волокна, обеспечивающие движение, — низкой (Gasser and Erlanger, 1929). Однако при электрофизиологических исследованиях одиночных нервных волокон, выделенных из нервных стволов, установить зависимость чувствительности к местному анестетику от толщины волокна не удается (Franz and Perry, 1974; Fink and Cairns, 1984; Huang et al., 1997). Таким образом, толщина нервного волокна сама по себе вряд ли определяет его чувствительность к местным анестетикам. Однако с увеличением толщины нервного волокна увеличивается и расстояние между перехватами Ранвье. Поскольку для того, чтобы подавить проведение возбуждения по нерву, необходимо блокировать определенное количество перехватов Ранвье, тонкие волокна, где перехваты Ранвье располагаются ближе друг к другу, более чувствительны к местным анестетикам (Franz and Perry, 1974). Еще одной причиной могут быть различия в тканевых барьерах и особенности расположения в нервном стволе тонких волокон групп С и А8.
Роль pH[править | править код]
В неионизированном виде (то есть в виде сводобных аминов) местные анестетики плохо растворимы. В связи с этим они обычно выпускаются в виде водорастворимых солей, в основном гидрохлоридов. Поскольку местные анестетики — слабые основания (pK;, обычно составляет 8—9), их гидрохлориды — слабые кислоты. Это повышает стабильность эфиров местных анестетиков и вводимых вместе с ними сосудосуживающих средств. В обычных условиях pH растворов местных анестетиков быстро становится равным pH внеклеточной жидкости.
Через мембрану могут проходить только неионизированные формы местных анестетиков, но с натриевыми каналами они взаимодействуют в виде катионов. Об этом говорят данные опытов на безмиелиновых нервных волокнах млекопитающих (Ritchie and Greengard, 1966).
Оказалось, что проведение возбуждения можно блокировать и восстанавливать изменением pH омывающего нерв раствора соответственно до 7,2 и 9,6. Ведущая роль катионных форм была также продемонстрирована в опытах с добавлением третичных и четвертичных аминов местных анестетиков в раствор, омывающий гигантский аксон кальмара изнутри и снаружи (Narahashi and Frazier, 1971). Впрочем, даже неионизированные формы местных анестетиков обладают некоторой анестезирующей активностью (Butterworth and Strichartz, 1990).
Удлинение действия местных анестетиков с помощью сосудосуживающих средств[править | править код]
Длительность действия местного анестетика прямо пропорциональна времени, в течение которого препарат взаимодействует с нервом. Следовательно, увеличение этого времени удлиняет анестезию. Кокаин сам по себе сужает сосуды, усиливая действие норадреналина (гл. 6 и 10) и тем самым предотвращая собственное всасывание. Местные анестетики часто смешивают с сосудосуживающими средствами, обычно с адреналином; такие средства замедляют всасывание анестетика. При этом, с одной стороны, действие анестетика ограничивается местом введения, с другой — весь всасывающийся препарат успевает элиминироваться, и в результате уменьшаются системные побочные эффекты. В то же время адреналин расширяет сосуды скелетных мышц, стимулируя β2-адренорецепторы, и может усиливать побочные эффекты анестетика, введенного в мышцу.
Некоторые сосудосуживающие средства сами могут оказывать системные побочные эффекты (см. ниже). Кроме того, они замедляют заживление ран, могут вызвать отек или некроз после местной анестезии. Эти побочные эффекты отчасти обусловлены тем, что адренергические средства увеличивают потребление кислорода тканями, что в сочетании с сужением сосудов вызывает гипоксию и повреждение тканей. Введение местных анестетиков в сочетании с сосудосуживающими средствами в участки с недостаточным коллатеральным кровотоком чревато необратимым гипоксическим повреждением, некрозом и гангреной и потому противопоказано.
Побочные эффекты[править | править код]
Местные анестетики не только блокируют проведение по нервам, но и действуют на все возбудимые органы и ткани: ЦНС, вегетативные ганглии, нервно-мышечные синапсы и мышцы (Covino, 1987; Garfield and Gugino, 1987; Gintant and Hoffman, 1987). Опасность такого воздействия прямо пропорциональна количеству местного анестетика, попавшего в кровь.
ЦНС. Местные анестетики оказывают возбуждающее действие на ЦНС, вызывая беспокойство, тремор, а иногда и клонические судороги. В целом, чем активнее препарат, тем выше риск судорог. Таким образом, вероятность центральных побочных эффектов определяется свойствами самого анестетика и его концентрацией в крови. Вслед за возбуждением наступает угнетение ЦНС. Причиной смерти обычно становится остановка дыхания.
Как возбуждение, так и последующее угнетение ЦНС под действием местных анестетиков объясняется торможением нейронов; при этом возбуждение возникает в результате избирательного торможения тормозных нейронов. Быстрое в/в введение местного анестетика может привести к смерти без предшествующего возбуждения ЦНС или после лишь кратковременного возбуждения. Это обусловлено одновременным угнетением все* нейронов при высокой концентрации препарата. Лечение на поздней стадии отравления местными анестетиками заключается в обеспечении проходимости дыхательных путей и ИВЛ. На ранней стадии для предотвращения и устранения судорог в/в вводят бензодиазепины или быстродействующие барбитураты (гл. 17).
Хотя самый частый из центральных побочных эффектов местных анестетиков — сонливость, лидокаин может вызвать дисфорию или эйфорию, а также подергивания мышц. Более того, лидокаин и прокаин могут привести к потере сознания, которой предшествует лишь сонливость (Covino, 1987). Настроение и поведение может меняться под действием любого местного анестетика, но в особенности кокаина. Эти свойства кокаина, а также его способность вызывать зависимость обсуждаются в гл. 24.
Сердечно-сосудистая система. Попадая в кровоток, местные анестетики могут оказывать побочные эффекты на сердечно-сосудистую систему (Covino, 1987). Прежде всего они действуют на миокард, снижая его возбудимость, проводимость и сократимость. Кроме того, большинство местных анестетиков расширяют артериолы. Побочное действие на сердечно-сосудистую систему обычно наблюдается лишь при высокой концентрации анестетика в крови и сочетается с побочным действием на ЦНС. Изредка шок и летальный исход возможны и при меньшей концентрации анестетика, что можно объяснить действием на ведущий водитель ритма сердца или внезапной фибрилляцией желудочков. Впрочем, желудочковая тахикардия и фибрилляция желудочков — относительно редкие побочные эффекты местных анестетиков, за исключением бупивакаина. Действие лидокаина и прокаинамида, которые применяются в качестве антиаритмических препаратов, обсуждается в гл. 35. Необходимо отметить, что побочные эффекты местных анестетиков на сердечно-сосудистую систему могут возникать вследствие случайного внутрисосудистого введения препарата, особенно вместе с адреналином.
Гладкомышечные органы. Местные анестетики уменьшают сокращения интактного кишечника и изолированных полосок кишки (Zipf and Dittmann, 1971). Кроме того, они вызывают расслабление гладких мышц сосудов и бронхов, хотя в низких концентрациях могут сначала вызвать их сокращение (Covino, 1987). Спинномозговая или эпидуральная анестезия, а также введение местного анестетика в брюшную полость приводит к угнетению симпатической нервной системы, что сопровождается повышением тонуса органов ЖКТ (см. ниже). Местные анестетики увеличивают тонус покоя и уменьшают сократимость изолированных полосок миометрия. Однако сократимость матки при регионарной анестезии во время родов снижается редко.
Нервно-мышечные и вегетативные межнейронные синапсы. Местные анестетики нарушают нервно-мышечную передачу. Например, прокайн подавляет сокращение скелетной мышцы в ответ на максимальное ритмическое раздражение двигательного нерва и на введение ацетилхолина; введенный в той же концентрации прокаин не препятствует сокращению мышцы в ответ на ее прямое электрическое раздражение. В высоких концентрациях местные анестетики нарушают передачу возбуждения в вегетативных ганглиях вследствие блокады ионных каналов, сопряженных с N-холинорецепторами (Neher and Stein-bach, 1978; Chamet et al., 1990).
Аллергические реакции[править | править код]
Такие реакции на местные анестетики редки. Они могут проявляться аллергическим дерматитом или приступом бронхиальной астмы (Covino, 1987). Аллергические реакции необходимо отличать от побочных эффектов местных анестетиков и вводимых вместе с ними сосудосуживающих средств. Аллергические реакции возникают почти исключительно при использовании препаратов из группы эфиров. Среди анестетиков этой группы возможны перекрестные аллергические реакции: например, при аллергии к прокаину возможна и аллергия к тетракаину, поскольку в процессе их обмена образуются одинаковые метаболиты. Средства из группы амидов сами по себе почти не вызывают аллергические реакции, однако их растворы могут содержать консерванты (например, метилпарабен), к которым возможна аллергия (Covino, 1987). Растворы местных анестетиков с сосудосуживающими средствами также могут вызывать аллергию, поскольку содержат сульфит.
Метаболизм[править | править код]
Большое практическое значение имеет метаболизм местных анестетиков, поскольку их токсичность определяется главным образом равновесием между их всасыванием и элиминацией. Выше уже отмечалось, что всасывание анестетика можно уменьшить, добавляя в раствор сосудосуживающее средство. Скорость метаболизма местных анестетиков существенно различается и во многом определяет безопасность их применения. Поскольку токсичность зависит от концентрации свободного препарата в крови, связывание его с белками плазмы и тканей уменьшает токсичность. Так, при в/в регионарной анестезии конечности около половины введенного анестетика остается связанным с белками тканей через 30 мин после снятия жгута. Легкие также могут связывать большое количество анестетика (Arthur, 1987).
Местные анестетики из группы эфиров (например, тетракаин) инактивируются путем гидролиза эстеразами плазмы, возможно псевдохолинэстеразой. Печень также участвует в гидролизе местных анестетиков. Поскольку в СМЖ эстераз почти нет, при интратекальном введении анестезия сохраняется до тех пор, пока препарат не всосется в кровь.
Местные анестетики из группы амидов метаболизируются в основном микросомальными ферментами печени путем N-деалкилирования и последующего гидролиза (Arthur, 1987). Исключение составляет прилокаин: он сначала гидролизуется, в результате чего образуется ортотолуидин, способный вызвать метгемоглобинемию. Местные анестетики из группы амидов с осторожностью применяют при тяжелых заболеваниях печени. Эти препараты активно (на 55—95%) связываются с белками плазмы, преимущественно с кислым а,-гликопротеидом. Уровень этого белка повышается при онкологических заболеваниях, хирургических вмешательствах, травмах, инфаркте миокарда, курении, уремии и уменьшается, например, при приеме пероральных контрацептивов. В зависимости от концентрации белков плазмы меняется количество местного анестетика, поступающего в печень, и, следовательно, его токсичность. Кроме того, связывание местных анестетиков с белками плазмы меняется с возрастом. У новорожденных относительно мало белков, с которыми связываются эти препараты, поэтому выше вероятность побочных эффектов. На метаболизм анестетиков влияют не только белки плазмы. Важную роль в распределении местных анестетиков из группы амидов может играть их захват легкими (Arthur, 1987).
Лидокаин[править | править код]
Лидокаин (рис. 15.1) создан в 1948 г. и в настоящее время является самым распространенным местным анестетиком.
Фармакологические свойства. Основные фармакологические свойства лидокаина такие же, как и у других местных анестетиков. По сравнению с прокаином (в равных концентрациях) анестезия под действием лидокаина наступает быстрее, бывает более выраженной и продолжается дольше. В отличие от прокаина, лидокаин представляет собой аминоэтиламид и является типичным представителем местных анестетиков из группы амидов. Лидокаин — препарат выбора при аллергии к местным анестетикам из группы эфиров.
Фармакокинетика. Лидокаин быстро всасывается из ЖКТ, дыхательных путей, а также при парентеральном введении. Он эффективен и без сосудосуживающих средств, однако адреналин уменьшает всасывание лидокаина, тем самым уменьшая побочные эффекты и увеличивая продолжительность действия препарата. Помимо инъекционных форм лидокаина существует система для введения лидокаина и адреналина методом электрофореза, применяемая в основном в дерматологии. Глубина анестезии при электрофорезе достигает 10 мм. Лидокаин деалкилируется в печени под действием микросомальных ферментов с образованием глицил(н)ксилидида и моноэтилглицил(н)ксилидида, которые далее превращаются в моноэтилглицин и ксилидид. Как глицил(н)ксилидид, так и моноэтилглицил(н)ксилидид обладают местноанестезирующим действием. У человека 75% ксилидида выделяется с мочой в виде 4-гидрокси-2,6-ди-метиланилина (Arthur, 1987).
Побочные эффекты. В высоких дозах лидокаин может вызвать сонливость, шум в ушах, нарушения вкуса, головокружение и подергивания мышц. По мере увеличения дозы развиваются эпилептические припадки, кома и угнетение дыхания. Клинически значимые сердечно-сосудистые нарушения возникают при такой сывороточной концентрации лидокаина, при которой имеются значительные расстройства ЦНС. Некоторые побочные эффекты обусловлены действием метаболитов лидокаина глицил(н)ксилидида и моноэтилглицил(н)ксилидида.
Применение. Лидокаин может использоваться во всех случаях, когда требуется местная анестезия средней продолжительности. Кроме того, он применяется в качестве антиаритмического средства (гл. 35).
Бупивакаин[править | править код]
Фармакологические свойства. Бупивакаин, внедренный в практику в 1963 г., представляет собой широко распространенный местный анестетик из группы амидов. От лидокаина он отличается лишь строением аминосодержащей группы, которая у бупивакаина представлена бутилпиперидином (рис. 15.1). Бупивакаин — сильный анестетик длительного действия. Большая продолжительность действия в сочетании с преимущественным воздействием на чувствительные, а не двигательные волокна делают его препаратом выбора для анестезии во время родов и в послеоперационном периоде. Вводя бупивакаин путем постоянной инфузии через катетер, можно обеспечить обезболивание на несколько суток.
Побочные эффекты. Бупивакаин (и этидокаин, см. ниже) обладает большей кардиотоксичностью, чем лидокаин. Кардиотоксическое действие проявляется тяжелыми желудочковыми аритмиями и угнетением сократимости миокарда после случайного внутрисосудистого введения больших доз бупивакаина. Высокую кардиотоксичность бупивакаина можно объяснить несколькими обстоятельствами. Как лидокаин, так и бупивакаин быстро связываются с натриевыми каналами кардиомиоцитов во время фазы деполяризации потенциала действия, однако бупивакаин значительно медленнее отсоединяется от этих каналов после реполяризации. Вследствие этого многие натриевые каналы (при нормальной ЧСС) остаются связанными с бупивакаином к началу очередного потенциала действия (Clarkson and Hondeghem, 1985); в результате блокируется все больше натриевых каналов, а кардиотоксическое действие оказывается большим, чем можно предположить, исходя из местноанестезирующей активности бупивакаина. Кроме того, кардиотоксическое действие бупивакаина может быть обусловлено влиянием на ЦНС, поскольку в эксперименте введение небольшого количества этого препарата в ствол мозга способно вызвать угрожающую жизни желудочковую аритмию (Thomas et al., 1986). Нарушения, вызванные кардиотоксическим действием бупивакаина, очень плохо поддаются лечению. Тяжесть их возрастает при ацидозе, гиперкапнии и гипоксии.
Другие синтетические местные анестетики[править | править код]
Количество синтетических местных анестетиков так велико, что описывать их все не имеет смысла. Некоторые из них имеют слишком много побочных эффектов и применяются только для поверхностной анестезии глаз (гл. 66), слизистых или кожи (гл. 65). Другие используют для инфильтрационной, проводниковой, а иногда и поверхностной анестезии. Ниже приведены основные группы местных анестетиков; препараты перечислены в алфавитном порядке.
Средства для инъекционного введения[править | править код]
Мепивакаин. Это препарат средней продолжительности действия из группы амидов (рис. 15.1). Он был внедрен в практику в 1957 г. По фармакологическим свойствам мепивакаин напоминает лидокаин, однако оказывает более сильное токсическое действие у новорожденных и потому не используется в акушерстве. Это действие объясняется скорее задержкой этого препарата в крови в ионизированной форме (pH крови новорожденного сравнительно низкий, а мепивакаин представляет собой слабое основание), чем более медленным его метаболизмом у новорожденного. У взрослых терапевтический диапазон мепи-вакаина, видимо, несколько шире, чем лидокаина. Мепивакаин начинает действовать так же быстро, как лидокаин, но в отсутствие сосудосуживающих средств действует несколько дольше (примерно на 20%). Мепивакаин не подходит для поверхностной анестезии.
Прилокаин. Это местный анестетик средней продолжительности действия из группы амидов (рис. 15.1), по фармакологическим свойствам сходный с лидокаином. Основное отличие при-локаина в том, что он почти не обладает сосудорасширяющими свойствами и потому может использоваться без сосудосуживающих средств. Кроме того, он имеет больший объем распределения и, вследствие этого, обладает меньшим нейротоксиче-ским действием. Это позволяет использовать его при в/в регионарной анестезии. Прилокаин — единственный местный анестетик, способный вызывать метгемоглобинемию. Это объясняется расщеплением в процессе метаболизма ароматического кольца до ортотолуилина. Метгемоглобинемия носит дозозависимый характер и обычно возникает при дозе выше 8 мг/кг. У здоровых лиц метгемоглобинемия, как правило, не опасна. Лечение состоит во введении метиленового синего, 1—2 мг/кг в/в. Метгемоглобинемия ограничивает использование прилокаина в акушерстве, так как затрудняет оценку состояния новорожденного. Кроме того, у новорожденных риск метгемоглобинемии выше из-за большей чувствительности фетального гемоглобина к окислителям и незрелости ферментов, участвующих в восстановлении метгемоглобина в гемоглобин.
Прокаин. Этот препарат из группы эфиров (рис. 15.1) появился в 1905 г. и стал первым синтетическим местным анестетиком. В прошлом он применялся чрезвычайно широко, но в настоящее время используется только для инфильтрационной анестезии и, иногда, для блокады нервов в диагностических целях. Это объясняется малой активностью, медленным началом и короткой продолжительностью действия прокаина. Он редко вызывает побочные эффекты. Прокаин гидролизуется с образованием парааминобензойной кислоты, снижающей активность сульфаниламидов. В связи с этим больным, принимающим эти средства, прокаин в высоких дозах противопоказан.
Ропивакаин. Кардиотоксичность бупивакаина способствовала поискам менее токсичного местного анестетика длительного действия. В результате был разработан новый препарат из группы амидов — ропивакаин (рис. 15.1). Он представляет собой чистый S-изомер 1-пропил-1,6’-пипеколоксилидида. S-изомер был выбран потому, что, как и у большинства местных анестетиков с хиральным центром, он менее токсичен, чем R-изомер (McClure, 1996). Полагают, что это объясняется более медленным всасыванием и, следовательно, меньшей сывороточной концентрацией препарата. Ропивакаин несколько слабее бупивакаина. В экспериментах на животных ропивакаин обладал меньшим кардиотоксическим действием по сравнению с бупи-вакаином. По данным клинических испытаний, ропивакаин подходит и для эпидуральной, и для проводниковой и инфильтрационной анестезии. Продолжительность действия его такая же, как у бупивакаина. Интересно, что ропивакаин еще меньше, чем бупивакаин, влияет на двигательные волокна. Тетракаин. Это препарат длительного действия из группы эфиров (рис. 15.1). Он был внедрен в практику в 1932 г. Посравнению с прокаином он значительно активнее и действует дольше. Тетракаин метаболизируется медленнее, чем другие представители группы эфиров, и потому имеет больше побочных эффектов. В настоящее время он широко используется для спинномозговой анестезии, когда необходим местный анесте-тикдлительного действия. Кроме того, тетракаин входит в состав некоторых препаратов для поверхностной анестезии. С появлением бупивакаина тетракаин стал реже применяться для проводниковой блокады из-за необходимости введения более высоких доз, медленного наступления эффекта и большей токсичности.
Хлоропрокаин. Это местный анестетик из группы эфиров, представляющий собой хлорированное производное прокаина (рис. 15.1). Он был внедрен в практику в 1952 г. Его основные преимущества: быстрое начало и короткая продолжительность действия, а также малое число побочных эффектов из-за быстрого метаболизма (Т1/2, около 25 с). Применять хлоропрокаин стали значительно осторожнее после того, как появились сообщения о продолжительных чувствительных и двигательных нарушениях при эпидуральном или субарахноидальном введении больших доз препарата. Такие побочные эффекты, по-видимому, объясняются низким pH и использованием метабисульфита натрия в качестве консерванта в выпускаемых ранее препаратах. Современные препараты хлоропрокаина, содержащие в качестве консерванта кальциевую соль ЭДТА, не обладают нейротоксическим действием, однако их все же не рекомендуют вводить интратекально. Сообщалось также, что после эпидуральной анестезии чаще, чем ожидалось, наблюдалась боль в спине (Stevens et al., 1993). Последняя может бытьь обусловлена длительным напряжением глубоких мышц спины вследствие связывания Са2+ с ЭДТА. Частота боли в спине прямо пропорциональна объему лекарственного средства, используемому для инфильтрации кожи во время анестезии.
Этидокаин. Это анестетикдлительного действия из группы амидов (рис. 15.1). Он был внедрен в практику в 1972 г. Этидокаин начинает действовать быстрее, чем бупивакаин, и примерно так же быстро, как л идо каин. При этом продолжительность действия этидокаина такая же, как у бупивакаина. В отличие от бупивакаина, этидокаин преимущественно блокирует проведение нервных импульсов по двигательным волокнам. В связи с этим он применяется при хирургических вмешательствах, требующих выраженного расслабления мышц, и не используется для анестезии во время родов и в послеоперационном периоде. Этидокаин обладает такой же кардиотоксичностью, как и бупивакаин (см. выше).
Средства для поверхностной анестезии кожи и слизистых[править | править код]
Некоторые анестетики обладают выраженным раздражающим действием или недостаточно эффективны для анестезии глаз, но могут использоваться для поверхностной анестезии кожи и слизистых. Они применяются, например, в качестве симптоматических средств при анальном зуде, зуде в области половых органов, остром или хроническом дерматите, в том числе вызванном ядоносным сумахом. Имеются комбинированные препараты, содержащие помимо местного анестетика глюкокортикоид или Нрблокатор.
Цинхокаин — производное хинолиновой кислоты. Из-за высокой токсичности применение его в качестве инъекционного анестетика в США запрещено, однако в других странах он по-прежнему широко используется для спинномозговой анестезии. Крем и мазь, содержащие цинхокаин, применяются для поверхностной анестезии кожи.
Диклонин характеризуется быстрым началом действия. По продолжительности действия он сходен с прокаином. Диклонин хорошо всасывается через кожу и слизистые. Он применяется в виде 0,5 и 1% растворов для поверхностной анестезии во время эндоскопии, при стоматите после лучевой и химиотерапии, а также для обезболивания промежности.
Прамокаин применяется для поверхностной анестезии. По структуре он отличается от других местных анестетиков (рис. 15.1), что позволяет снизить риск перекрестных аллергических реакций при непереносимости других препаратов. Прамокаин обладает удовлетворительным анестезирующим действием и хорошо переносится при нанесении на кожу и слизистые, однако он не применяется для анестезии глаз или слизистой носа из-за выраженного раздражающего действия. Наиболее распространены препараты на основе 1% раствора прамокаина.
Малорастворимые местные анестетики[править | править код]
Некоторые местные анестетики малорастворимы, медленно всасываются и, следовательно, имеют мало побочных эффектов. Такие препараты можно непосредственно наносить на раны и изъязвленные поверхности; они долго остаются в месте введения и обеспечивают продолжительную анестезию. Эти анестетики представляют собой эфиры парааминобензойной кислоты, но, в отличие от описанных выше препаратов, лишены аминогруппы. Наиболее распространенный представитель малорастворимых анестетиков — бензокаин. Он отличается от прокаина лишь отсутствием диэтиламиногруппы (рис. 15.1). Бензокаин входит в состав многочисленных препаратов для поверхностной анестезии. Есть сообщения о том, что бензокаин, как и прилокаин, может вызвать метгемоглобинемию, поэтому следует избегать его передозировки.
Офтальмологические средства[править | править код]
Местные анестетики можно использовать для обезболивани; роговицы и конъюнктивы, но большинство описанных вышпрепаратов обладают для этого слишком выраженным раздражающим действием. Первый анестетик, который стали применять в офтальмологии, — кокаин — имел серьезные недостатки: он вызывал мидриаз и слущивание эпителия роговицы. В связи с этим его перестали использовать. В настоящее время чаще всего в офтальмологии применяют проксиметакаин и тетракаин (рис. 15.1). Проксиметакаин не только обладает лишь слабым раздражающим действием, но и почти не вызывает перекрестных аллергических реакций с другими местными анестетиками из группы эфиров. В связи с этим его можно использовать при аллергии к таким препаратам.
Для обезболивания сначала закапывают в глаз одну каплю местного анестетика. Если анестезия недостаточна, закапывание повторяют до тех пор, пока не будет достигнуто нужное обезболивание. Продолжительность анестезии определяется главным образом кровоснабжением тканей. При здоровой роговице анестезия продолжается дольше, чем при воспаленной; в последнем случае необходимо своевременно повторять закапывание анестетика. Длительная анестезия замедляет заживление роговицы, способствует ее изъязвлению и слущиванию эпителия, а также увеличивает риск случайного повреждения глаза. В связи с этим местные анестетики можно закапывать в глаза лишь под контролем врача. Пути введения, фармакокинетика и побочные эффекты препаратов, используемых в офтальмологии, обсуждаются в гл. 66.
Тетродотоксин и сакситоксин[править | править код]
Это наиболее сильные из известных ядов: их минимальная летальная доза для мышей составляет 8 мкг/кг. Оба они могут вызвать смертельное отравление у человека. Тетродотоксин содержится в половых железах и других внутренних органах некоторых рыб отряда Tetraodontiformes (к которому принадлежит обитающая у берегов Японии рыба фугу, или иглобрюх), а также в коже некоторых тритонов семейства саламандровых и лягушек рода ателопов, обитающих в Коста-Рике. Сакситоксин и, возможно, некоторые подобные ему яды вырабатываются динофлагеллятами Gonyaulax catanella и Gonya-ulax tamarensis и накапливаются в тканях моллюсков и ракообразных, питающихся этими водорослями. При оптимальном освещении и температуре водоросли Gonyaulax могут размножаться так быстро, что окрашивают воду в красный цвет. Это явление называют красным приливом. В такие периоды моллюски, питающиеся этими водорослями, становятся крайне ядовитыми для человека, в связи с чем возникают вспышки к так называемого паралитического отравления (Као, 1972; Ritc-l\ hie, 1980). Хотя химическая структура тетродотоксина и сакси-токсина различна, механизм действия этих ядов сходен (Ritchie, 1980): в наномолярных концентрациях они блокируют быстрые натриевые каналы в области наружных устьев. В результате полностью подавляется возникновение потенциала действия. Рецепторы тетродотоксина и сакситоксина образованы аминокислотными остатками сегмента SS2 а-субъединицы быстрого натриевого канала (рис. 15.2) во всех четырех доменах (Terlau et al., 1991; Catterall, 2000). He все быстрые натриевые каналы одинаково чувствительны ктетродотоксину: так, к нему устойчивы быстрые натриевые каналы кардиомиоцитов и денервированных скелетных мышц. Смерть при отравлении тетродотоксином и сакситоксином наступает из-за паралича дыхательных мышц, поэтому лечение должно включать ИВЛ. Артериальная гипотония, характерная для отравления тетродотоксином, обусловлена блокадой проведения по сосудодвигательным нервам, а также расслаблением гладких мышц сосудов (Као, 1972). Лечение помимо ИВЛ включает промывание желудка и мероприятия по поддержанию кровообращения. Если при паралитическом отравлении смерть не наступает в первые сутки, то прогноз можно считать благоприятным (Ogura, 1971; Schantz, 1971).
Читайте также[править | править код]
- Анестезиология
- История анестезиологии
- Анестезия в предоперационный период
- Анестезия в интраоперационный период
- Местная анестезия
- Анестезия в послеоперационный период
- Общие анестетики
- Средства для наркоза
- Препараты для анестезии
Литература[править | править код]
- Caplan, R.A., Ward, R.J., Posner, К., and Cheney, F.W. Unexpected cardiac arrest during spinal anesthesia: a closed claims analysis of predisposing factors. Anesthesiology, 1988,68:5—11
- Catterall, W.A. Structure and function of voltage-sensitive ion channels. Science, 1988,242:50—61.
- Chamet, P., Labarca, C., Leonard, R.J., Vogelaar, N.J., Czyzyk, L., Gouin, E., Davidson, N., and Lester, H.A. An open-channel blocker interacts with adjacent turns of alpha-helices in the nicotinic acetylcholine receptor. Neuron, 1990,4:87—95.
- Clarkson, C.W., and Hondeghem, L.M. Mechanism for bupivacaine depression of cardiac conduction: fast block of sodium channels during the action potential with slow recovery from block during diastole. Anesthesiology, 1985,62:396-405.
- Huang, J.H., Thalhammer, J.G., Raymond, S.A., and Strichartz, G.R. Susceptibility to lidocaine of impulses in different somatosensory fibers of rat sciatic nerve. J. Pharmacol. Exp. Ther., 1997,292:802—811.
- Narahashi, Т., and Frazier, D.T. Site of action and active form of local anesthetics. Neurosci> Res. (N.Y.), 1971,4:65—99.
- Stevens, R.A., Urmey, W.F., Urquhart, B.L., and Kao, T.C. Back pain after epidural anesthesia with chloroprocaine. Anesthesiology, 1993, 78: 492-497.
- Stone, L.S., MacMillan, L.B., Kitto, K.F., Limbird, L.E., and Wilcox, G.L. The alpha 2a adrenergic receptor subtype mediates spinal analgesia evoked by alpha 2 agonists and is necessary for spinal adrener-gic-opioid synergy. J. Neurosci., 1997, 37:1255—1260.
- Hicker, G.T., Boyes, R.N., Bridenbaugh, P.O., and Moore, D.C. Binding of anilide-type local anesthetics in human plasma. 11. Implications in vivo, with special reference to transplacental distribution. Anesthesiology, 1970,33:304-314.
- Willcockson, W.S., Kim, J., Shin, H.K., Chung, J.M., and Willis, W.D. Actions of opioid on primate spinothalamic tract neurons. J. Neurosci., 1986,6:2509-2520.
- Winnie, A.P., Tay, C.H., Patel, K.P., Ramanmurthy, S., and Durrani, Z. Pharmacokinetics of local anesthetics during plexus blocks. Anesth. Analg., 1977, 56:852-861.
- Yaksh, T.L., and Rudy, T.A. Analgesia mediated by a direct spinal action of narcotics. Science, 1976, 192:1357—1358.