Отравление ртутью. Лечение
Источник:
Клиническая фармакология по Гудману и Гилману, том 4.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Отравление ртутью. Лечение[править | править код]
Ртуть столетиями широко применялась в медицине. Она входила в состав разнообразных препаратов: диуретиков, антимикробных средств (в том числе антисептиков), мазей, слабительных. В последние десятилетия вместо соединений ртути стали использовать более избирательные, эффективные и безопасные лекарственные средства, и теперь ятрогенные отравления ртутью стали редкостью. Однако ртуть достаточно широко применяется в промышленности (табл.), поэтому производственные отравления и отравления, обусловленные загрязнением промышленными отходами окружающей среды, по-прежнему представляют серьезную проблему. Во многих странах наблюдались массовые отравления ртутью среди населения и диких животных. За редкими исключениями, такие отравления в силу ряда причин (незаметное начало заболевания, стертые ранние клинические проявления, плохая осведомленность врачей о симптомах отравления) оставались нераспознанными в течение многих месяцев или (даже лет (Gerstner and Huff, 1977).
Химическое состояние ртути и ее источники[править | править код]
Ртуть может существовать в виде металлической ртути (пары), неорганических солей и органических соединений, которые различаются по своей токсичности. В табл. представлено суточное поступление соединений ртути в организм из разных источников.
Контакты с ртутью в быту и на производстве
|
Источник |
Доля от общего количества контактов с ртутью, % |
|
Производство едких щелочей и хлора (например, отбеливателей) и его отходы |
25 |
|
Электронная промышленность |
20 |
|
Краски |
15 |
|
Термометры |
10 |
|
Зубные пломбы |
3 |
|
Научно-исследовательские лаборатории |
2 |
Среднее суточное поступление ртути в организм в отсутствие профессионального контакта с ртутью
|
Источник |
Среднее суточное поступление ртути, мкг | ||
|
Металлическая ртуть (пары) |
Неорганические соли ртути |
Метил ртуть | |
|
Воздух |
0,024 |
0,001 |
0,0064 |
|
Пиша | |||
|
Рыба |
0 |
0,04 |
2.3 |
|
Другие продукты |
0 |
0,23 |
0 |
|
Питьевая вода |
0 |
0,0035 |
0 |
|
Зубные пломбы |
3-17 |
0 |
0 |
|
Всего |
3—17 |
0,3 |
2,31 |
Металлическая ртуть — самое летучее из неорганических соединений ртути. Отравление парами ртути чаще всего связано с профессиональной деятельностью и известно еще с античных времен. Золотодобытчики широко использовали ртуть для извлечения золота из руды, а полученную таким образом амальгаму нагревали для выпаривания ртути. В некоторых развивающихся странах этот способ применяют до сих пор. Причиной отравления может стать длительный контакт с парами ртути, случайно разлитой в плохо вентилируемом помещении (такое нередко бывает в научно-исследовательских лабораториях). Для большей части населения основным источником ртути служат пломбы из ртутной амальгамы, из которых выделяются пары ртути. Однако количество металла, попадающего при этом в организм, по-видимому, не опасно для здоровья (Eley and Сох, 1993); исключение составляют редкие случаи аллергического контактного дерматита.
Из всех соединений ртути ее неорганические соли оказывают самое сильное раздражающее действие и могут вызвать тяжелое острое отравление. В состав неорганических солей может входить как одно-, так и двухвалентная ртуть. Каломель (хлорид одновалентной ртути, Hg2Cl2) — наиболее известное соединение ртути — применялась как антисептик (в качестве компонента некоторых косметических кремов), диуретик и слабительное. Более 400 лет назад в производстве фетровых шляп широко использовали нитрат ртути. Производственные отравления этим веществом приводили к неврологическим и поведенческим расстройствам, запечатленным Льюисом Кэрроллом в образе Сумасшедшего Шляпника из «Алисы в Стране Чудес». Сулема (хлорид двухвалентной ртути, HgCI2), распространенный когда-то антисептик, часто использовалась с целью самоубийства. Неорганические соли ртути до сих пор находят широкое применение в промышленности; попадание их с промышленными отходами в реки стало причиной загрязнения окружающей среды во многих странах. В настоящее время эти соединения используют главным образом в производстве едких щелочей и хлора, а также в электронной промышленности. Кроме того, ртуть применяется при изготовлении пластмасс, фунгицидных и бактерицидных средств и входит в состав зубных пломб.
В используемых сегодня органических соединениях ртути металл связан ковалентной связью с одним атомом углерода. Это разнородная группа соединений, различающихся по своей токсичности. Наиболее опасны алкильные производные ртути (самое распространенное из них — метил ртуть). Соли алкильных производных ртути применялись в качестве фунгицидов и нередко становились причиной отравлений. Так, отравления, обусловленные употреблением в пищу обработанных такими соединениями семян злаков, наблюдались в Ираке, Пакистане, Гане и Гватемале. Самое массовое отравление произошло в Ираке в 1972 г. В конце 1971 г. Ирак закупил за границей большое количество обработанных метил ртутью семян пшеницы и ячменя, которые раздали населению для весенней посадки. Несмотря на официальные предупреждения, зерно было использовано для выпечки хлеба. В результате в больницы попали 6530 человек, 500 человек умерли (Bakir etal., 1973,1980).
Минаматская болезнь тоже была следствием отравления метилртутью. Минамата — маленький город в Японии, где находится химический завод, спускающий свои отходы прямо в залив Минамата. Неорганическая ртуть использовалась на заводе как катализатор. Часть ее попала в отходы в виде метилртути, часть — в виде неорганических соединений, которые под действием водных и почвенных микроорганизмов тоже превращаются в метил ртуть. Последняя быстро поглощается планктонными водорослями и затем накапливается в питающейся ими рыбе. Жители Минаматы, чей рацион в основном состоит из рыбы, стали первыми жертвами отравления. В итоге пострадал 121 и умерли 46 человек (McAlpine and Araki, 1958; Smith and Smith, 1975; Tamashiro etal., 1985). В США отмечались случаи отравления ртутью, обусловленные употреблением в пишу мяса свиней, которых кормили обработанным фунгицидом зерном. Химические свойства и механизм действия. Большинство биологических эффектов ртути обусловлено тем, что она легко образует ковалентные связи с серой. При взаимодействии с сульф-гидрильной группой двухвалентная ртуть замешает атом водорода, образуя меркаптиды, X— Hg—SR и Hg(SR)2, где X — отрицательно заряженный радикал, a R — белок. Органические соединения ртути образуют тиолы, RHg—SR'. Даже в низких концентрациях производные ртути способны инактивировать ферменты, содержащие сульфгидрильную группу, нарушая таким образом клеточные функции и метаболизм. Высокое сродство ртути к тиолам позволяет лечить отравление ртутью такими препаратами, как димеркапрол и пеницилламин. Кроме того, ртуть вступает в реакции с другими группами, имеющими важное физиологическое значение (фосфорильные, карбоксильные, амидо- и аминогруппы).
Разные токсические свойства соединений ртути обусловлены наличием разных замещающих групп, которые влияют на растворимость, степень диссоциации, сродство к клеточным рецепторам, а также характер распределения и экскреции этих соединений.
Всасывание, распределение, метаболизм и выведение[править | править код]
Металлическая ртуть плохо всасывается в ЖКТ, так как она присутствует там в виде капель и не взаимодействует с биологически активными молекулами. Поэтому при проглатывании металлическая ртуть не слишком токсична. В то же время пары ртути полностью всасываются в легких, после чего ртуть окисляется до двухвалентного состояния каталазой эритроцитов (Magos et al., 1978). Через несколько часов после вдыхания паров ртути ее распределение в организме такое же, как и после попадания в ЖКТ солей ртути, с одним заметным отличием. Поскольку пары ртути проходят через мембраны значительно легче, чем двухвалентная ртуть, большое количество металла, не успев окислиться, проникает в головной мозг. В результате при отравлении парами ртути ЦНС поражается гораздо сильнее, чем при отравлении соединениями, содержащими двухвалентную ртуть.
Неорганические соли ртути[править | править код]
Растворимые неорганические соли двухвалентной ртути всасываются в кишечнике примерно на 10—15%; значительная часть ртути остается связанной со слизистой кишечника и его содержимым. Нерастворимые неорганические соединения ртути, такие, как каломель, всасываются Ж хуже, но при окислении превращаются в растворимые. Неорганические соединения ртути распределяются в организме очень неравномерно. Соли двухвалентной ртути накапливаются преимущественно в почках, где они сохраняются дольше, чем в Я других органах. Концентрация неорганических соединений ртути в цельной крови и плазме одинакова. Неорганическая ртуть с трудом проходит через гематоэнцефалический барьер и плаценту, а выводится в основном с мочой и калом; Т1/2 составляет около 60 сут (Fribergand Vostal, 1972). Поданным исследований на животных, с калом выводится больше ртути, чем с мочой (Klaassen, 1975).
Органические соединения ртути[править | править код]
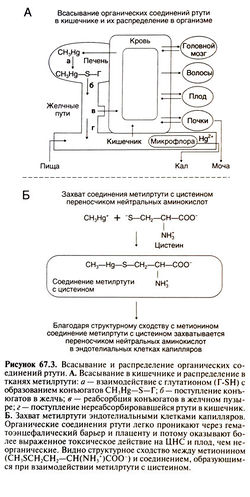
Благодаря более высокой растворимости в жирах органические соединения ртути всасываются в ЖКТ значительно лучше, чем неорганические, и меньше раздражают слизистую кишечника. Всасывание и распределение органических соединений ртути представлено на рис. 67.3, А. Метилртуть всасывается в ЖКТ более чем на 90%. Органические соединения ртути легко проникают через гематоэнцефалический барьер и плаценту и потому вызывают более сильные неврологические нарушения и оказывают большее тератогенное действие, чем неорганические. Метилртуть, взаимодействуя с цистеином, образует соединение, которое сходно по структуре с метионином. Это соединение захватывается присутствующим в эндотелиальных клетках капилляров переносчиком нейтральных аминокислот (рис. 67.3, Б; Clarkson, 1987). Органические соединения ртути более равномерно распределены в организме, чем неорганические (Klaassen, 1975). Значительная часть органических соединений ртути находится в эритроцитах. Соотношение концентраций метилртути в эритроцитах и в плазме составляет примерно 20:1; для прочих органических соединений ртути оно может быть несколько иным (Kershaw et al., 1980). Ртуть накапливается в волосах благодаря высокому содержанию в них сульфгидрильных групп. В некоторых органических соединениях ртути связь между атомами ртути и углерода после всасывания этих соединений разрывается; в случае метилртути это происходит довольно медленно, и образующиеся неорганические соединения ртути вносят незначительный вклад в токсические эффекты. В ароматических соединениях ртути, таких, как гидроксимеркур-о-нитрофенол, связь между углеродом и ртутью легко распадается, поэтому их токсичность такая же, как и у неорганических соединений ртути. Метилртуть выводится преимущественно с калом в виде конъюгата с глутатионом; почками экскретируется менее 10% (Bakir et al., 1980). Т1/7 метилртути колеблется от 40 до 105 суг (Bakir et al., 1973).
Токсичность[править | править код]
Металлическая ртуть. При кратковременном воздействии паров ртути симптомы отравления — слабость, озноб, металлический вкус во рту, тошнота, рвота, понос, одышка, кашель, чувство стеснения в груди — могут появиться уже в течение нескольких часов. Поражение легких может привести к интерстициальному пневмониту и тяжелой дыхательной недостаточности. Выздоровление обычно полное, хотя возможен пневмосклероз.
Хроническое отравление парами ртути проявляется в иной, менее острой форме, с преобладанием неврологических расстройств (Friberg and Vostal, 1972). Оно характеризуется астенией в сочетании с тремя или более из перечисленных ниже симптомов (Goyer and Clarkson, 2001): зоб, увеличение поглощения радиоактивного йода щитовидной железой, тахикардия, лабильный пульс, гингивит, красный дермографизм, повышение концентрации ртути в моче. Впоследствии, если контакт с парами ртути продолжается, возникают тремор и так называемый ртутный эретизм, для которого характерны психические (депрессия, раздражительность, патологическая стеснительность и пугливость, бессонница, неуверенность в себе, эмоциональная неуравновешенность, забывчивость, нетерпеливость) и вазомоторные (повышенная потливость, внезапное покраснение лица) нарушения. Типичны слюнотечение и гингивит. Сочетание трех симптомов — повышенной возбудимости, тремора и гингивита — считалось основным признаком отравления парами ртути еще с тех времен, когда нитрат ртути использовался для обработки фетра (например, при изготовлении фетровых шляп) и меха. При длительном контакте с парами ртути на производстве возникает поражение почек. На рис. 67.4 представлены симптомы ртутного отравления и концентрация ртути в моче при разных концентрациях паров ртути в воздухе. Неорганические соли ртути. Ионизированная ртуть (например, в виде сулемы) может вызывать тяжелое острое отравление. Из-за осаждения неорганическими солями ртути белков слизистые рта, глотки и кишечника приобретают пепельно-серый цвет, возникает сильная боль, иногда сопровождающаяся рвотой. С рвотными массами из желудка удаляется невсосавшаяся ртуть, поэтому, если больной в сознании, рвоту не подавляют. Вследствие местного разъедающего действия ионизованной ртути на слизистую ЖКТ в кале появляются спущенный эпителий и большое количество неизмененной крови. В отсутствие лечения возможны гиповолемический шок и смерть. Своевременно начатое лечение позволяет предотвратить местные токсические эффекты неорганической ртути.
Системные проявления развиваются спустя несколько часов после попадания неорганических солей ртути в ЖКТ и продолжаются несколько дней. Вначале появляется сильный металлический вкус во рту, затем — гингивит и неприятный запах изо рта; выпадают зубы. Распространенное и самое опасное последствие отравления неорганическими соединениями ртути — поражение почек. При остром отравлении возникает острый канальцевый некроз, приводящий колигурии и анурии. При длительном воздействии неорганических соединений ртути преобладают изменения в клубочках, обусловленные как прямым влиянием ртути на базальную мембрану клубочков, так и повреждающим действием иммунных комплексов (Goyer and Clarkson, 2001).
Для хронического отравления неорганическими соединениями ртути характерна акродиния — синдром, проявляющийся гиперемией конечностей, груди и лица, светобоязнью, потливостью, снижением аппетита, тахикардией, а также поносом или запором. Акродиния была зарегистрирована в 1980 г. в Аргентине у грудных детей, подвергшихся воздействию содержащего фенил ртуть фунгицида, который использовался коммерческой службой проката пеленок (Gotelli et al., 1985). Акродиния развивается почти исключительно при поступлении ртути через ЖКТ и считается проявлением аллергической реакции на это вещество (Matheson et al., 1980).
Органические соединения ртути. Источником большинства данных об отравлении органическими соединениями ртути послужили несколько случаев массового отравления метилртутью. Для отравления метилртутью характерна неврологическая симптоматика: нарушения зрения (скотома и сужение полей зрения), атаксия, парестезия, неврастения, снижение слуха, дизартрия, нарушения интеллекта, тремор, двигательные расстройства, а в тяжелых случаях — параличи и смерть (табл. 67.4). Морфологические изменения обнаруживают в коре больших полушарий, преимущественно в шпорной борозде (затылочные доли), прецентральной, постцентральной и поперечных височных извилинах; в коре мозжечка уменьшается число зернистых клеток (Eto, 1997). На плод метилртуть действует даже в тех случаях, когда у матери отравление протекает бессимптомно; у детей впоследствии наблюдаются умственная отсталость и нервно-мышечные нарушения.
Рисунок 67.4. Симптомы ртутного отравления и концентрация ртути в моче при разных концентрациях паров ртути в воздухе.
Диагностика ртутного отравления[править | править код]
Важное диагностическое значение имеют данные анамнеза о контакте с ртутью в быту или на производстве. В отсутствие таких сведений диагноз подтверждают с помощью лабораторных исследований. Предельной концентрацией ртути в цельной крови, при которой не возникает токсических эффектов, обычно считается 3—4 мкг% (0,15— 0,2 мкмоль/л). Если у взрослого эта концентрация превышает 4мкг% (0,2 мкмоль/л), необходимо установить источник отравления и провести обследование. Так как метилртуть накапливается в эритроцитах, а неорганические соединения ртути — нет, по распределению ртути между эритроцитами и плазмой можно судить о том, какое соединение послужило причиной отравления — органическое или неорганическое. В первом случае более информативным показателем общего содержания ртути в организме служит ее концентрация в эритроцитах, во втором — в плазме. Частота тех или иных симптомов отравления метил-ртутью при разных концентрациях ртути в цельной крови представлена в табл. 67.4. Однако клиническая картина служит лишь приблизительным ориентиром, только на нее полагаться нельзя. Взаимосвязь между общим содержанием неорганической ртути в организме и ее концентрацией в плазме изучена недостаточно, возможно, потому, что последняя сильно зависит от времени, прошедшего с момента контакта со ртутью. К тому же токсические эффекты неорганической ртути зависят от ее химического состояния: например, при отравлении парами ртути концентрация металла в головном мозге в 10 раз выше, чем при отравлении неорганическими солями ртути в эквивалентной дозе.
О содержании ртути в организме можно судить и по концентрации ртути в моче (верхняя граница нормы — 5 мкг/л). При отравлении парами ртути ее концентрация в плазме прямо пропорциональна почечной экскреции. В то же время при отравлении метилртутью уровень ртути в моче не отражает ее содержания в крови, поскольку метилртуть выводится преимущественно с калом (Bakir et al., 1980).
Концентрация ртути в волосах приблизительно в 300 раз выше, чем в крови, поскольку в них содержится много сульфгид-рильных групп. За год волосы отрастают примерно на 20 см; таким образом, исследуя разные участки волос, можно судить о том, как давно произошло отравление.
Лечение ртутного отравления[править | править код]
При отравлении ртутью (независимо от ее химического состояния) как можно скорее определяют ее концентрацию в крови.
Пары ртути (металлическая ртуть). Обязательное условие — немедленное прекращение контакта со ртутью и тщательное наблюдение за функцией легких. На короткое время может потребоваться ИВЛ. Терапию комплексобразующими средствами (см. ниже) начинают немедленно, а решение о ее прекращении принимают, руководствуясь состоянием больного и концентрацией ртути в крови и моче.
Симптомы отравления метилртутью при разных концентрациях ртути в крови
|
Концентрация ртути в крови, мкг/мл (мкмоль/л) |
Частота симптома, % | |||||
|
Парестезия |
Атаксия |
Нарушения зрения |
Дизартрия |
Нарушения слуха |
Смерть | |
|
0,1-0,5 (0,5-2,5) |
5 |
0 |
0 |
5 |
0 |
0 |
|
0,5-1 (2,5-5) |
42 |
11 |
21 |
5 |
5 |
0 |
|
1-2 (5-10) |
60 |
47 |
53 |
24 |
5 |
0 |
|
2-3(10-15) |
79 |
60 |
56 |
25 |
13 |
0 |
|
3-4(15-20) |
82 |
100 |
58 |
75 |
36 |
17 |
|
4-5 (20-25) |
100 |
100 |
83 |
85 |
66 |
28 |
Неорганические соли ртути. При тяжелом и умеренном отравлении, обусловленном попаданием неорганических солей ртути в ЖКТ, решающую роль играет поддержание водно-электролитного баланса и гемостаза. Если больной находится в сознании, можно вызвать рвоту (при повреждении слизистой ЖКТ этого делать не следует). Если с момента проглатывания ртути прошло более 30—60 мин, рвота малоэффективна. При отравлении соединениями, обладающими разъедающим действием, показаны эндоскопия и коагулограмма. Некоторые авторы рекомендуют применять активированный уголь, хотя эффективность этого метода не доказана. К тому же активированный уголь затрудняет проведение эндоскопии или делает его вообще невозможным.
Терапия комплексобразующими средствами. Для лечения отравления металлической ртутью или ее неорганическими солями обычно используют димеркапрол либо пеницилламин. Первый применяют при воздействии больших доз ртути и наличии клинических признаков отравления, второй — при воздействии небольших доз в отсутствие симптомов. Первая доза димеркапро-ла составляет 5 мг/кг в/м. Затем вводят по 2,5 мг/кг в/м каждые 12—24 ч в течение 10 сут. Пеницилламин в дозе 250 мг внутрь каждые 6 ч можно применять сам по себе или после курса лечения димеркапролом. Продолжительность лечения комплексобразующими средствами может быть разной, об его эффективности судят по концентрации ртути в моче и крови. При отравлении ртутью эффективен и сукцимер — новое комплексобра-зующее средство для приема внутрь (Campbell et al., 1986; Fournier et al., 1988; Bluhm et al., 1992). Правда, его применение в этих целях пока не одобрено ФДА.
Хелатный комплекс димеркапрол—ртуть выводится с желчью и мочой, в то время как комплекс пеницилламин—ртуть только с мочой. Поэтому при нарушении функции почек пеницилламин назначают крайне осторожно. Больным с почечной недостаточностью может потребоваться гемодиализ. Тем не менее комплексобразующие средства можно назначать даже в этом случае, так как хелатный комплекс димеркапрол—ртуть удаляется при диализе (Giunta et al., 1983).
Органические соединения ртути. Органические соединения ртути с длинными радикалами, особенно метилртуть, выводятся из организма хуже всего, вероятно потому, что они слабо реагируют с комплексобразующими средствами. При отравлении метилртутью димеркапрол противопоказан, так как в экспериментах на животных этот препарат повышает содержание метилртути в головном мозге. Пеницилламин ускоряет экскрецию метилртути, хотя его клиническая эффективность невелика (Bakir et al., 1980). В дозах, рекомендуемых для лечения отравлений неорганическими солями ртути (1 г/сут), пеницилламин лишь незначительно уменьшает концентрацию метилртути в крови; для достижения более выраженного эффекта дозу необходимо увеличить до 2 г/сут. В первые 3 сут лечения пени-цилламином концентрация ртути в крови сначала увеличивается и лишь затем падает. Возможно, это обусловлено более высокой скоростью мобилизации ртути из тканей в кровь по сравнению со скоростью выведения этого вещества с мочой и калом.
В экспериментах на животных показано, что производные метилртути подвергаются интенсивному кишечно-печеночному кругообороту. Следовательно, прием невсасываюшихся в ЖКТ веществ, способных связывать соединения ртути, например политиоловых смол, облегчает удаление этих соединений из организма (Bakir etal., 1973). По сравнению с комплексобразующими средствами политиоловые смолы обладают некоторыми преимуществами. Во-первых, они не вызывают перераспределения ртути в организме, а следовательно, увеличения ее концентрации в крови. Во-вторых, димеркапрол и пеницилламин дают больше побочных эффектов, так как они всасываются в кишечнике и содержат активные сульфгидрильные группы. Опыт использования разных методов лечения при отравлении метилртутью в Ираке показал, что и пеницилламин, и N-аце-тилпеницилламин, и политиоловые смолы уменьшают концентрацию ртути в крови, однако четкой взаимосвязи между снижением содержания метилртути в организме и улучшением состояния больных не прослеживается (Bakir et al., 1980).
Обычный гемодиализ при отравлении метилртутью малоэффективен, поскольку она накапливается в эритроцитах (в плазме ее концентрация невелика). Однако показано, что при введении L-цистеина в артериальную кровь на входе в диализатор метилртуть взаимодействует с этим веществом, образуя соединение, которое, как и сам цистеин, диффундирует в анализирующий раствор. Эффективность этого метода у человека доказана (Al-Abbasi et al., 1978), но эксперименты на животных свидетельствуют, что удаление комплекса метилртути с сукцимером путем гемодиализа может оказаться еще эффективнее (Kostyni-ak, 1982).