Токсикология
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Содержание
Основы токсикологии[править | править код]
Важнейшими характеристиками лекарственных средств служат их эффективность и безопасность. К сожалению, все вещества могут оказывать нежелательное действие. Поэтому при разработке новых препаратов большое значение имеет широта терапевтического диапазона, то есть диапазон доз от минимальной терапевтической до минимальной токсической. В ряде случаев больные превышают рекомендуемую дозу, что часто служит причиной отравлений. Особенно это касается препаратов с узким терапевтическим диапазоном.
Врач должен быть готов к встрече с токсическим действием лекарственного средства или любого другого вещества. Настоящая глава посвящена обсуждению токсического действия химических веществ и принципам лечения отравлений.
Предмет токсикологии[править | править код]
Токсикология — это наука, изучающая вредное воздействие химических веществ на живые организмы. В ней часто выделяют несколько разделов. Предметом токсикометрии служит проведение токсикологических тестов (см. ниже), на основе которых оценивают риск контакта данного вещества с человеческим организмом и с окружающей средой. Токсикодинамика изучает механизмы, лежащие в основе токсического действия различных веществ. Токсикодинамические характеристики необходимы для разработки токсикологических тестов, для облегчения поиска более безопасных веществ и рациональных способов лечения отравлений. Именно токсиколог определяет риск применения лекарственных средств и прочих веществ для тех или иных целей и дает рекомендации на их выпуск.
В США за безопасностью поступающих в продажу лекарственных и косметических средств, медицинских устройств и пищевых добавок следит ФДА. Для пищевых добавок ФДА устанавливает допустимое суточное потребление, то есть количество добавки, которое человек может потреблять в сутки в течение всей жизни без всякого вреда. Нормы для пестицидов, токсических веществ, вредных отходов и токсических загрязнителей атмосферы и воды принимает Агентство по охране окружающей среды. За соблюдением безопасности условий труда на предприятиях следит Управление охраны труда, а в обязанности работодателя входит поддержание концентрации всех химических веществ на рабочих местах ниже предельно допустимых. Наконец, Комиссия по безопасности товаров широкого потребления отвечает за безопасность всех прочих товаров для дома, школы и отдыха.
Два раздела токсикологии особенно важны для медицины. Судебная токсикология, стоящая на стыке аналитической химии и фундаментальной токсикологии, изучает отравления применительно к задачам судебно-медицинской экспертизы; она необходима для установления причин или обстоятельств смерти. В рамках клинической токсикологии изучаются и совершенствуются средства и методы диагностики и лечения острых отравлений, а также особенности течения болезней, вызванных действием химических веществ на организм.
Врач должен знать, какие симптомы могут сопутствовать отравлениям лекарственными средствами и веществами, присутствующими в окружающей среде. Побочные эффекты лекарственных средств часто сходны с симптомами заболеваний. Знакомство с основами токсикологии помогает врачу распознать эти симптомы и выбрать правильное лечение.
Зависимость эффекта от дозы[править | править код]
Первостепенное значение для токсиколога имеет изучение зависимости эффекта от дозы. Существуют два способа ее отображения (гл. 3, рис. 3.3). Первый — это кривая доза—эффект: она показывает, как зависит от дозы выраженность эффекта. Второй способ заключается в построении характеристической кривой, отражающей зависимость от дозы частоты развития эффекта в изучаемой популяции (или группе экспериментальных животных): при этом учитывают не выраженность эффекта, а только его наличие либо отсутствие (по принципу «все или ничего»). Такие кривые в токсикологии особенно важны; именно их используют для определения LD50 лекарственных средств и прочих химических веществ.
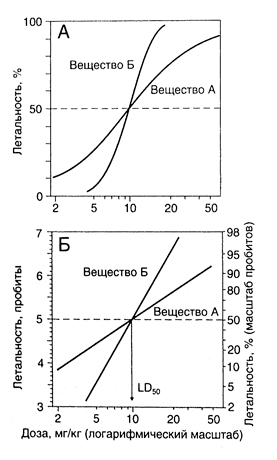
LD50 определяют экспериментально. Изучаемое вещество обычно вводят мышам или крысам (через рот или внутрибрюшинно) в нескольких дозах (обычно четырех или пяти), почти смертельных (рис. 4.1, А). Если на вертикальной оси отложить долю погибших животных, а на горизонтальной — дозу в логарифмическом масштабе, то получится характеристическая кривая (она была описана в гл. 3), имеющая S-образную форму. Чтобы превратить ее в прямую (рис. 4.1, Б), единицы на вертикальной оси преобразуют в так называемые пробиты (от англ. probability units — единицы вероятности). Один пробит равен одному стандартному отклонению; пятый пробит принимается равным среднему арифметическому. Таким образом, например, четвертый пробит равен 16-му процентилю (то есть 16-процентной смертности животных), а шестой — 84-му процентилю (соответствует смерти 84% животных). Из точки пересечения полученной прямой с горизонтальной линией, соответствующей пятому пробиту (то есть 50-процентной гибели животных), опускают перпендикуляр. Он и указывает на LD50. Существенна не только LD50, но и наклон полученной прямой. Так, у двух веществ (рис. 4.1, Б) LD50 одинакова (10 мг/кг), однако наклон прямых разный. Поэтому в дозе, равной половине LD50 (5 мг/кг), вещество А вызовет гибель 30% животных, а вещество Б — лишь 5%.
Описание к рисунок 4.1. Определение LDM. А. Для оценки токсического действия вещества его вводят в нескольких дозах, в том числе заведомо летальных. LD» определяют по точке пересечения кривой смертности с горизонталью, соответствующей 50-про-центной смертности (пунктирная линия). Б. Для удобства вычислений S-образную кривую смертности преобразуют в прямую, используя специальные единицы — пробиты.
К эффектам типа «все или ничего» относится не только смертельный исход. Сходные кривые могут быть построены для любого эффекта, вызываемого химическими веществами (гл. 3).
Факторы токсического действия[править | править код]
LD50 для разных веществ сильно различаются. Для некоторых смертельные дозы составляют доли микрограмма (LD50 для ботулотоксина составляет 10 пг/кг); другие относительно безопасны в дозах, превышающих несколько граммов. Хотя для оценки токсического действия веществ предложен ряд методов (они основаны на определении смертельной дозы), провести границу между токсичными и нетоксичными веществами часто довольно трудно. Парацельс (1493—1541) говорил: «Все есть яд. Ничто не лишено ядовитости. И только доза отличает яд от лекарства». В рамках токсикологии невозможно разделить вещества на ядовитые и неядовитые, как бы ни хотело этого общество. Задача токсикологии состоит в том, чтобы оценить риск, который представляет то или иное вещество, — а не отнести его к ядовитым или неядовитым. При оценке риска, связанного с применением того или иного вещества в соответствии с рекомендациями производителя, следует учитывать не только прямые токсические эффекты, но и вредное действие, которое может быть опосредовано влиянием на окружающую среду. Малотоксичное вещество при неправильном применении и хранении может принести больше вреда, чем высокотоксичное.
В настоящее время особую тревогу вызывают вещества, оказавшиеся канцерогенными для экспериментальных животных. Канцерогенность большинства из них для человека не изучена. Органы государственного регулирования разделяют потенциальные канцерогены на три группы, и подходы к оценке связанного с этими веществами риска разные. В отношении пищевых добавок ФДА проявляет особую осторожность, поскольку они касаются огромного числа людей, а никакой существенной пользы не приносят. В отношении лекарственных средств ФДА старается соотнести их риск и пользу. Например, канцерогенный для экспериментальных животных препарат ФДА, скорее всего, не разрешит использовать для лечения легких недугов, но может одобрить его применение для лечения тяжелого заболевания. На самом деле большинство противоопухолевых средств являются химическими канцерогенами.
В отношении канцерогенов Агентство по охране окружающей среды старается ограничить дозу, которую человек может получить в течение жизни. При этом онкологическое заболевание, вызванное данным веществом, не должно возникать чаще, чем в одном случае из миллиона. Допустимую суточную дозу для человека определяют с помощью математических моделей, экстраполируя дозу вещества, вызывающего рост опухоли у определенного процента экспериментальных животных (обычно у 10—20%). Эти модели, по-видимому, вполне пригодны для защиты людей от контакта с потенциальными канцерогенами.
Острые и хронические токсические эффекты[править | править код]
Токсические эффекты, вызываемые одним и тем же веществом при его остром, подостром и хроническом действии на организм, нередко различаются. Об острых эффектах говорят в случае получения дозы вещества за один раз. Хронические эффекты, как правило, вызваны многократным получением небольших доз вещества в течение длительного времени; при этом вещество обычно медленно накапливается в организме. В окружающей среде имеется много веществ природного и искусственного происхождения, которые в низких дозах могут воздействовать на организм человека в течение длительного времени, и в настоящее время все больше внимания уделяют оценке кумулятивных токсических эффектов таких веществ.
Непрямое токсическое действие лекарственных средств[править | править код]
Часто лекарственные средства выпускаются в виде именно того вещества, которое и оказывает лечебное действие; оно же, как правило, вызывает и основные побочные эффекты. Вместе с тем токсические эффекты химических веществ (а в случае лекарственных средств — и лечебное действие) могут быть обусловлены их метаболитами или свободными радикалами кислорода.
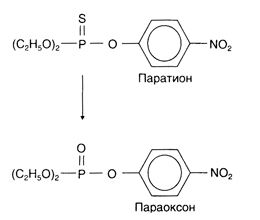
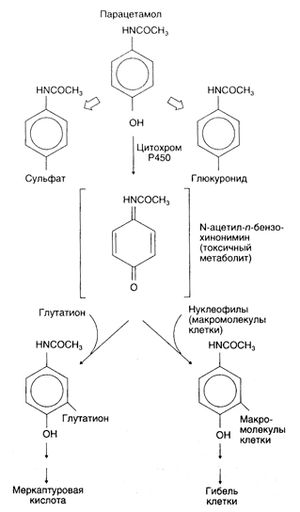
Токсические метаболиты. Токсические эффекты многих веществ обусловлены их метаболитами. Так, токсические метаболиты образуются из большинства фосфор-органических инсектицидов при участии микросомальных ферментов печени. Примером может быть образование из паратиона стабильного метаболита параоксона (рис. 4.2) — ингибитора АХЭ. Некоторые метаболиты химически нестабильны; обычно их называют реакционноспособными промежуточными продуктами. Примером служит метаболит парацетамола N-ацетил-n-бензохинонимин (рис. 4.3) — очень реакционноспособное соединение, реагирующее с глутатионом и другими нуклеофилами. При истощении запасов глутатиона в печени этот метаболит связывается с макромолекулами гепатоцитов, что и вызывает гибель последних. Токсические эффекты паратиона и парацетамола возрастают при повышении активности микросомальных ферментов печени, так как при этом увеличивается и образование активных метаболитов (гл. 1); это наблюдается, в частности, на фоне приема этанола или фенобарбитала.
Фототоксические и фотоаллергические реакции. Для многих веществ образование токсических метаболитов опосредуют печеночные ферменты. Однако в ряде случаев такие метаболиты могут образовываться в коже под действием излучения ультрафиолетового или видимого диапазонов. Если при этом из лекарственного препарата (например, сульфаниламида) образуется более сильный аллерген, чем сам препарат, говорят о фотоаллергической реакции. Фототоксические реакции обусловлены не аллергией, а тем, что проникающие в кожу вещества (как извне, так и через системный кровоток) либо вызывают фотосенсибилизацию. либо усиливают обычное действие светового излучения. Примерами служат тетрациклины, сульфаниламиды, хлорпромазин и налидиксовая кислота; как правило, в отсутствие светового излучения они безвредны.
Свободные радикалы кислорода. Гербицид паракват вызывает тяжелое поражение легких. Его токсическое действие опосредовано свободными радикалами кислорода, образование которых сопряжено с восстановлением молекулы параквата (рис. 4.4).
Токсикологические испытания на животных[править | править код]
В основе всех токсикологических испытаний на животных лежат два принципа. Во-первых, правильная оценка эффекта исследуемого вещества у экспериментальных животных позволяет сделать вывод о его токсичности для человека. В расчете на единицу поверхности тела сходные дозы вещества оказывают примерно одинаковое токсическое действие на человека и животных (если рассчитывать дозы на единицу веса, то при сходных дозах токсический эффект у человека выше). Данные токсикологических испытаний используют для подбора доз новых лекарственных средств в клинических испытаниях, а также для установления допустимых концентраций вредных веществ в окружающей среде.
Второй принцип состоит в том, что воздействие на животных высокими дозами токсического вещества служит необходимым и надежным методом выявления риска, которому может подвергаться человек при гораздо меньших дозах. В таких исследованиях изучают не выраженность, а частоту развития токсического эффекта (см. выше). Очевидно, что количество участвующих в испытаниях животных, как правило, намного меньше количества людей, которые могут подвергаться воздействию данного вещества. Так, тяжелые токсические эффекты (например, канцерогенные) могут встречаться в 25 ООО случаев из 25 млн, то есть с частотой 0,01%. Для человека такая частота недопустимо высока, однако для выявления подобных эффектов в экспериментальном исследовании должно участвовать не менее 30 ООО животных. Поэтому для того, чтобы оценить риск воздействия вещества в малых дозах, на относительно небольшие группы животных воздействуют высокими дозами. Очевидно, что применяемая в таких случаях экстраполяция не всегда правомочна.
Первым этапом токсикологических испытаний служит определение LD50 на животных двух видов с использованием двух способов введения вещества, один из которых должен соответствовать ожидаемому пути попадания данного вещества в человеческий организм. При этом отмечают число животных, погибших в течение 14 сут после введения однократной дозы. Обращают также внимание на симптомы отравления, сонливость, изменения в поведении и заболеваемость.
Затем проводят испытания на подострую токсичность, как правило, в течение 90 сут, на животных двух видов, с использованием как минимум трех доз и одного способа введения, соответствующего ожидаемому пути попадания вещества в человеческий организм. Во время испытаний регистрируют множество параметров, а в конце проводят патологоанатомическое исследование.
Испытания на хроническую токсичность проводят одновременно с клиническими испытаниями (гл. 3). На продолжительность испытаний лекарственных средств влияет то, как средство предполагается использовать в клинике. Так, если его планируют применять в течение короткого времени и под медицинским наблюдением (как в случае антибактериальных препаратов), испытания могут длиться не более 6 мес. Если же препарат собираются использовать в течение длительного времени, могут потребоваться испытания продолжительностью 2 года.
Испытания на хроническую токсичность часто проводят с целью определить возможное канцерогенное действие вещества. В этом случае опыты обычно проводят на крысах и мышах в течение половины средней продолжительности жизни животных данного вида. Для оценки действия вещества на плод и репродуктивную функцию, а также перинатальных и постнатальных токсических эффектов применяют другие подходы. Так, для изучения тератогенного действия препарат обычно вводят беременным крысам и кроликам в период органогенеза.
Помимо канцерогенного и тератогенного действия изучают также мутагенное действие лекарственных средств. Для этого чаще всего применяют разработанный Эймсом мутационный тест на штамме Salmonella typhimurium, содержащем мутантный ген фермента, необходимого для синтеза гистидина (Ames et al., 1975). Такой штамм сможет размножаться в среде, не содержащей гистидина, лишь в том случае, если произойдет обратная мутация. Поскольку многие вещества становятся мутагенными или канцерогенными лишь после активации ферментами эндоплазматического ретикулума, в среду помимо мутантного штамма и лекарственного препарата добавляют микросомы печени крысы. К достоинствам теста Эймса относятся быстрота и высокая чувствительность. Однако он пригоден лишь для выявления генотоксичных канцерогенов, но не промоторов.
Распространенность острых отравлений[править | править код]
Истинная распространенность отравлений в США точно не известна. В 1998 г. в Американскую ассоциацию центров отравлений сообщили более чем о 2 млн случаев. Однако нет сомнений, что истинное число отравлений намного больше.
В США от отравлений ежегодно умирают более 775 человек. За последние 30 лет удалось существенно снизить смертность от отравлений среди детей младше 5 лет. Например, в 1998 г. не зафиксировано ни одного случая смерти ребенка от отравления аспирином, хотя в начале 1960-х гг. таких случаев было около 140 в год. Вероятно, здесь сыграли роль несколько факторов: более безопасная упаковка лекарственных средств и средств бытовой химии; улучшение подготовки врачей и качества врачебной помощи; просветительная работа среди населения.
В табл. 4.1 приведен список основных причин отравлений. Видно, что из трех самых частых причин две относятся не к лекарственным средствам, а к косметическим и чистящим средствам. Вместе с тем основными причинами смертельных отравлений служат именно лекарственные средства (табл. 4.2). К веществам, отравления которыми особенно часто приводят к смерти, относятся трициклические антидепрессанты, парацетамол, салицилаты, опиоиды, кокаин, дигоксин, угарный газ и антагонисты кальция. В основном от отравлений умирают взрослые, причем нередко они принимают токсические вещества намеренно. На детей младше 6 лет приходится 53% всех случаев отравления и лишь 2% смертельных исходов. На детей в возрасте 1 —2 лет приходится самая высокая частота случайных отравлений. К счастью, большинство веществ, доступных детям этого возраста, не слишком токсичны. Основные источники случайных смертельных отравлений у детей — препараты железа и пестициды.
Согласно недавно опубликованным данным, в больницах США очень велика распространенность тяжелых, в том числе смертельных, побочных эффектов лекарственных средств (Lazarou et al., 1998; Institute of Medicine, 1999). Полагают, что тяжелые побочные эффекты ежегодно отмечаются примерно у 2 млн госпитализированных больных; из них около 100 000 заканчиваются смертельным исходом. Если эти оценки верны, то ежегодно от врачебных ошибок умирает больше людей, чем от дорожно-транспортных происшествий, рака молочной железы или СПИДа.
Основные источники информации об отравлениях[править | править код]
В учебниках по фармакологии приводятся сведения о лечении лекарственных отравлений, но обычно в них говорится об отравлениях прочими веществами. Более подробную информацию об отравлениях можно найти в изданиях по токсикологии (Ellenhorn, 1997; Goldfrank et al., 1998; Haddad etal., 1998; Klaassen, 2001).
Таблица 4.1. Наиболее частые причины отравлений
|
Причины |
Число отравлений |
Доля отравлений, % |
|
Чистящие средства |
229 500 |
10,2 |
|
Анальгетики |
215 067 |
9,6 |
|
Косметические средства и средства личной гигиены |
210 224 |
9,4 |
|
Растения |
122 578 |
5,5 |
|
Инородные тела |
103 696 |
4,6 |
|
Противокашлевые средства и средства от простуды |
99 924 |
4,5 |
|
Укусы и ужаления |
92 182 |
4,1 |
|
Инсектициды и пестициды (в том числе родентициды) |
86 289 |
3,9 |
|
Лекарственные средства для местного применения |
83 455 |
3,7 |
|
Пищевые отравления |
78 690 |
3,5 |
|
Транквилизаторы, снотворные и нейролептики |
70 982 |
3,2 |
|
Антидепрессанты |
67 872 |
3 |
|
Углеводороды |
66 623 |
3 |
|
Антибактериальные препараты |
62 034 |
2,8 |
|
Химические реагенты |
61 061 |
2,7 |
|
Спирты |
55 246 |
2,5 |
Таблица 4.2. Наиболее частые причины смертельных отравлений
|
Причины |
Число смертельных исходов |
Доля контактов с веществами данной группы, % |
|
Анальгетики |
264 |
0,108 |
|
Антидепрессанты |
152 |
0,224 |
|
Психостимуляторы и наркотики |
118 |
0,345 |
|
Сердечно-сосудистые средства |
118 |
0,279 |
|
Транквилизаторы, снотворные и нейролептики |
89 |
0,125 |
|
Спирты |
56 |
0,101 |
|
Химические продукты |
45 |
0,074 |
|
Газы и дымы |
38 |
0,092 |
|
Чистящие средства |
24 |
0,01 |
|
Противосудорожные средства |
20 |
0,09 |
|
Препараты для лечения бронхиальной астмы |
18 |
0,114 |
|
Н1-блокаторы |
18 |
0,036 |
|
Углеводороды |
18 |
0,027 |
|
Средства, используемые автомобилистами |
16 |
0,108 |
|
Гормональные средства и антагонисты гормонов |
16 |
0,043 |
|
Инсектициды и пестициды (в том числе родентициды) |
16 |
0,024 |
Ценный источник информации по лечению острых отравлений бытовыми веществами — монография Clinical Toxicology of Commercial Products (Gosselin, 1984). В одном из семи ее разделов приведены более 17 500 торговых названий продуктов, которые человек может принять случайно или с целью самоубийства. Указаны производители и состав каждого продукта, а также компоненты, которые, скорее всего, оказывают токсическое действие. Имеется также система поиска информации о токсических веществах POISINDEX (Micromedex, Inc., Denver, Colorado).
В США около 120 центров отравлений, которые подчиняются Отделу отравлений ФДА. Кроме того, имеется 34 местных центра отравлений, созданных Американской ассоциацией центров отравлений. Эти центры предоставляют необходимую информацию по телефону.
Тяжелые металлы и их антидоты[править | править код]
Источник:
Клиническая фармакология по Гудману и Гилману, том 4.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Свинец, ртуть, мышьяк и кадмий — важнейшие источники отравлений в быту и на производстве. В прошлом свинцовые краски применяли в жилых помещениях, а при прокладке водопроводов использовали свинцовые трубы и свинецсодержащий припой, поэтому многие люди до сих пор подвергаются риску свинцового отравления. Постоянный контакт со свинцом особенно опасен для детей. Со ртутью человек тоже сталкивается повседневно: она содержится в рыбе, зубных пломбах из ртутной амальгамы. В некоторых географических областях питьевая вода содержит мышьяк в высоких концентрациях. Согласно недавним исследованиям, кадмий обладает канцерогенными свойствами. Настоящая глава посвящена токсическому действию этих веществ и их антидотам — комплексобразующим средствам.
Человек контактировал с тяжелыми металлами и мышьяком во все времена. Причиной отравлений могло быть попадание этих веществ в пищу и питьевую воду из природных источников или из кухонной посуды. С наступлением индустриальной эры и развитием горнодобывающей промышленности стали встречаться производственные отравления металлами и мышьяком. Угрозу представляют содержащие эти вещества пестициды и лекарственные средства (например, антимикробные). Важнейшей причиной отравления тяжелыми металлами стало загрязнение окружающей среды, обусловленное сжиганием содержащего их ископаемого топлива, добавлением тетраэтилсвинца в бензин и широким применением тяжелых металлов в промышленности.
Токсическое действие тяжелых металлов и мышьяка обусловлено их взаимодействием с реакционноспособными группами (лигандами), несущими важные физиологические функции. Тяжелые металлы, особенно переходные, могут реагировать с лигандами, содержащими кислород (—ОН, —СОО, —ОРО3Н~, >С=0), серу (—SH, — S—S—I и азот (—NH2 и >NH). В результате реакции между металлом и лигандом формируется координационная связь, в которой оба электрона предоставляются лигандом, и образуется комплексное, или координационное, соединение.
Все обсуждаемые в данной главе антидоты тяжелых металлов и мышьяка относятся к комплексобразующим средствам и способны образовывать с металлами хелатные комплексы. Последние представляют собой комплексные соединения, в которых катион металла связан с двумя или более донорными атомами лиганда, в результате чего замыкается гетероцикл. Наиболее стабильны пяти- и шестичленные циклы, поэтому в качестве комплексобразующих средств обычно используют полидентатные (имеющие несколько донорных атомов), а не монодентатные (имеющие лишь один донорный атом) лиганды. Конкурируя с эндогенными лигандами, комплекс-образующие средства препятствуют связыванию с ними катионов металлов или разрывают уже образовавшиеся связи, предотвращая или нейтрализуя токсическое действие металлов и ускоряя их выведение из организма.
Стабильность хелатного комплекса зависит и от того, какие металл и лиганд его образуют. Например, свинец и ртуть имеют большее сродство к лигандам, содержащим серу и азот, чем к кислородсодержащим лигандам, а кальций — наоборот. Эти различия лежат в основе избирательного действия комплексобразующих средств.
Эффективность комплексобразующего средства зависит от его относительного сродства к токсичному металлу (по сравнению со сродством к эндогенным металлам), распределения комплексобразующего средства и токсичного металла, а также способности препарата усиливать выведение последнего.
Идеальное комплексобразующее средство хорошо растворимо в воде, не подвергается метаболизму, сохраняет комплексобразующую активность при pH, свойственном биологическим жидкостям, легко проникает в места накопления токсичного металла и образует с последним нетоксичные комплексы, которые быстро выводятся. Кроме того, желательно, чтобы препарат обладал низким сродством к кальцию, так как кальций плазмы легко связывается комплексобразующими средствами, что может привести к гипокальциемии даже при высоком сродстве лекарственного средства к токсичным металлам. Главное требование к комплексобразующему средству более высокое, чем у эндогенных лигандов, сродство к токсичным металлам. Из-за большого числа эндогенных лигандов эффективность комплексобразующих средств in vivo гораздо ниже, чем in vitro. Поэтому о целесообразности клинического применения этих препаратов можно судить только по результатам испытаний in vivo.
В первой части данной главы рассмотрены токсические эффекты свинца, ртути, мышьяка, кадмия и радиоактивных тяжелых металлов, а также лечение отравлений этими веществами. Вторая часть главы посвящена химическим свойствам и применению некоторых антидотов тяжелых металлов и мышьяка.
Читайте также[править | править код]
- Токсические эффекты
- Лечение отравлений лекарственными средствами
- Растительные препараты
- Отравление свинцом. Лечение
- Отравление ртутью. Лечение
- Отравление мышьяком. Лечение
- Отравление кадмием. Лечение
- Антидоты
- Антидоты тяжелых металлов и железа
- Атмосферные загрязнители воздуха
- Летучие органические вещества