Зависимость доза-эффект — различия между версиями
Zabava (обсуждение | вклад) (→Отношение доза-ответ) |
Dormiz (обсуждение | вклад) (→Читайте также) |
||
| (не показано 5 промежуточных версий этого же участника) | |||
| Строка 1: | Строка 1: | ||
| − | == | + | == Зависимость доза-эффект (отношение доза-ответ) == |
Ранее в этой главе связывание лекарства с рецептором обсуждалось как простой тип взаимодействия. Установлено, что модели на основе таких предположений имеют недостатки при исследовании взаимосвязи между ответом и концентрацией лекарств в тканях и органах или между ответом и дозой для всей популяции животных или человека. Эта область исследований известна как связь доза-ответ (dose-response, DR). | Ранее в этой главе связывание лекарства с рецептором обсуждалось как простой тип взаимодействия. Установлено, что модели на основе таких предположений имеют недостатки при исследовании взаимосвязи между ответом и концентрацией лекарств в тканях и органах или между ответом и дозой для всей популяции животных или человека. Эта область исследований известна как связь доза-ответ (dose-response, DR). | ||
| Строка 268: | Строка 268: | ||
=== Клинические реакции === | === Клинические реакции === | ||
| − | Клинические реакции на препараты оценивают с помощью разнообразных методов: от измерения физиологических функций (частота сердечных сокращений, артериальное давление) до уровней излечиваемости или смертности пациентов в популяции | + | Клинические реакции на препараты оценивают с помощью разнообразных методов: от измерения физиологических функций (частота сердечных сокращений, артериальное давление) до уровней излечиваемости или смертности пациентов в популяции. Однако, поскольку цель лекарственной терапии состоит в излечении или облегчении течения заболевания для улучшения и продления жизни, увеличиваются попытки напрямую измерить эти эффекты. Как уже упоминалось, большое количество пациентов желает иметь эту информацию, для чего и проводятся клинические наблюдения. Альтернативным способом изучения новых препаратов, попадающих на рынок, является мониторирование всех назначений (в разумных пределах), повлекших фатальные или нежелательные реакции. |
| − | Клинически использование любого препарата зависит от знания подходящей дозы, которая в свою очередь зависит от данных кривой доза-ответ относительно как основных, так и нежелательных (побочных) эффектов. Изначально кривую доза-ответ для новых препаратов получают на основе изучения культуры ткани, затем животных и только потом — человека. Иногда невозможно получить полную терапевтическую кривую доза-ответ у | + | Клинически использование любого препарата зависит от знания подходящей дозы, которая в свою очередь зависит от данных кривой доза-ответ относительно как основных, так и нежелательных (побочных) эффектов. Изначально кривую доза-ответ для новых препаратов получают на основе изучения культуры ткани, затем животных и только потом — человека. Иногда невозможно получить полную терапевтическую кривую доза-ответ у человека вследствие высокой токсичности препарата при увеличении дозы. Как правило, такие исследования сложны и требуют больше времени, чем в клинической практике. Например, эффект определенной дозы препарата для снижения болевого порога у человека может быть оценен с помощью визуальной аналоговой шкалы, на которой указывают субъективное ощущение боли от 0 (нет боли) до 10 (максимально возможная боль). Однако ощущения боли варьируют у разных людей, степень болевых ощущений часто колеблется, кроме того, боль может возникать вследствие разных патологических процессов. В результате для определения окончательной кривой доза-ответ у человека для новых анальгетиков нужно сотни наблюдаемых и длительные исследования, что нецелесообразно. С другой стороны, на животных моделях (крысы или мыши) снижение боли может быть определено по среднему времени облизывания животным лапы, в которую было введено вещество, вызывающее воспаление. Для получения таким методом данных для кривой доза-ответ может потребоваться от 100 до 200 животных и несколько часов наблюдения. Обычно до этого строятся упрощенные кривые доза-ответ, полученные на разных тканевых препаратах, для определения отсутствия фармакологического действия, которое могло бы мешать клиническому использованию препарата. |
| − | |||
| − | |||
С точки зрения трудности получения истинной связи доза-ответ у человека часто проводят корреляции. Например, хронически повышенное артериальное давление неизвестной этиологии (первичная гипертензия) статистически ассоциировано с повышенной заболеваемостью и смертностью, поэтому идеальным измерением антигипертензивных препаратов является степень, на которую они снижают заболеваемость и смертность, против возможности побочных эффектов. Это требует проспективного клинического наблюдения тысяч пациентов в течение многих лет, поэтому обычно эффект антигипертензивных средств оценивают с позиции их эффективности и силы, используя заменитель снижения артериального давления, которое легко измерить. Взаимосвязь доза-ответ для истинной клинической эффективности для большинства широко используемых антигипертензивных препаратов до сих пор не получена, хотя большое внимание уделяется их способности уменьшать смертность. Интересно, что, несмотря на доступность многих антигипертензивных препаратов, относящихся к разным классам, сравнительно немногие доказанно уменьшают смертность пациентов с эссенциальной гипертензией. | С точки зрения трудности получения истинной связи доза-ответ у человека часто проводят корреляции. Например, хронически повышенное артериальное давление неизвестной этиологии (первичная гипертензия) статистически ассоциировано с повышенной заболеваемостью и смертностью, поэтому идеальным измерением антигипертензивных препаратов является степень, на которую они снижают заболеваемость и смертность, против возможности побочных эффектов. Это требует проспективного клинического наблюдения тысяч пациентов в течение многих лет, поэтому обычно эффект антигипертензивных средств оценивают с позиции их эффективности и силы, используя заменитель снижения артериального давления, которое легко измерить. Взаимосвязь доза-ответ для истинной клинической эффективности для большинства широко используемых антигипертензивных препаратов до сих пор не получена, хотя большое внимание уделяется их способности уменьшать смертность. Интересно, что, несмотря на доступность многих антигипертензивных препаратов, относящихся к разным классам, сравнительно немногие доказанно уменьшают смертность пациентов с эссенциальной гипертензией. | ||
| Строка 280: | Строка 278: | ||
Разные люди по-разному реагируют на действие лекарств. В результате возникает необходимость в проведении мероприятий для определения эффектов препаратов в популяции. Опыт показал, что данные должны быть собраны согласно протоколу, а не в ходе рутинной работы. | Разные люди по-разному реагируют на действие лекарств. В результате возникает необходимость в проведении мероприятий для определения эффектов препаратов в популяции. Опыт показал, что данные должны быть собраны согласно протоколу, а не в ходе рутинной работы. | ||
| − | Данные, полученные в фазах II и III клинического наблюдения (см. | + | Данные, полученные в фазах II и III клинического наблюдения (см. [[Этапы разработки лекарственных препаратов]]), являются важным источником информации для оценки действия препаратов в популяции. Эти данные могут быть использованы не только для определения токсичности препарата, но и для увеличения его эффективности. Главной проблемой, связанной с получением информации в регистрационных исследованиях, может быть недостаток выборки группы. |
| − | Эта проблема может усугубиться различной степенью тяжести заболевания у разных пациентов. Но эти трудности частично преодолеваются разработкой исследований с вовлечением большого количества пациентов. В долгосрочной перспективе постоянный сбор информации о действии лекарств в популяции может служить условием для оптимизации дозы в целях уменьшения токсичности и увеличения фармакотерапевтической выгоды | + | Эта проблема может усугубиться различной степенью тяжести заболевания у разных пациентов. Но эти трудности частично преодолеваются разработкой исследований с вовлечением большого количества пациентов. В долгосрочной перспективе постоянный сбор информации о действии лекарств в популяции может служить условием для оптимизации дозы в целях уменьшения токсичности и увеличения фармакотерапевтической выгоды. |
При изучении эффекта препарата в популяции необходимо учитывать образ жизни пациентов. Например, курящий пациент — представитель определенной популяции. | При изучении эффекта препарата в популяции необходимо учитывать образ жизни пациентов. Например, курящий пациент — представитель определенной популяции. | ||
Это означает, что врачу, назначающему препарат, понадобится приспосабливать значения, полученные в общей популяции, для конкретного пациента. Такие детали играют важную роль в решении врача, назначающего препарат. | Это означает, что врачу, назначающему препарат, понадобится приспосабливать значения, полученные в общей популяции, для конкретного пациента. Такие детали играют важную роль в решении врача, назначающего препарат. | ||
| + | |||
| + | == Читайте также == | ||
| + | *[[Кумулятивный эффект]] | ||
| + | *[[Соотношение доза-эффект]] | ||
| + | *[[Кривая концентрации]] | ||
| + | *[[Концентрация лекарственных веществ]] | ||
| + | *[[Механизмы действия лекарственных средств|Что делают лекарства и каким образом]] | ||
| + | *[[Молекулярное действие лекарств (молекулярные мишени)]] | ||
| + | *[[Действие лекарств на клетки]] | ||
| + | *[[Тканевое и системное действие лекарств]] | ||
| + | *[[Рецепторы|Рецепторы - виды и классификация]] | ||
| + | *[[Регуляция рецепторов]] | ||
| + | *[[Взаимодействие лекарственных средств с рецепторами]] | ||
== Литература == | == Литература == | ||
Текущая версия на 18:39, 24 октября 2014
Содержание
Зависимость доза-эффект (отношение доза-ответ)[править | править код]
Ранее в этой главе связывание лекарства с рецептором обсуждалось как простой тип взаимодействия. Установлено, что модели на основе таких предположений имеют недостатки при исследовании взаимосвязи между ответом и концентрацией лекарств в тканях и органах или между ответом и дозой для всей популяции животных или человека. Эта область исследований известна как связь доза-ответ (dose-response, DR).
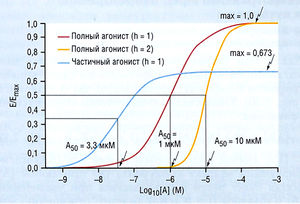
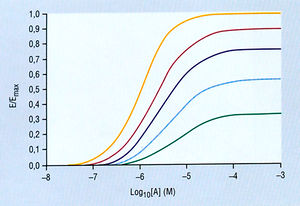
Связь между концентрацией (логарифмом дозы) препарата-агониста и ответом, выраженным в виде кривой, своей формой напоминает сигмовидную кривую, сходную с показанной на рис. 2.29, которая, в свою очередь, очень напоминает форму кривой лекарство-рецептор, показанную ранее. Эффект (Е) — это ответ ткани или, реже, ингибирование спонтанной активности (например, урежение сердечных сокращений ацетилхолином). При концентрации агониста (А) ниже определенных значений Е слишком мал для измерения. При более высоких концентрациях эффект становится заметным и растет при дальнейшем увеличении концентрации. Когда концентрация станет достаточно высокой, Е прекращается, достигая асимптоты при Еmах (максимальный эффект агониста). Кривую log доза-ответ характеризуют три параметра:
- Еmax
- концентрация А, при которой Е составляет 50% от Еmах (обозначают [А50]). В данном случае — [ED50], где ED — это эффективная доза, или [ЕС50], где ЕС — эффективная концентрация. ЕС50 — это мера потенциала лекарства: чем ниже ЕС50 лекарства, тем больше его эффективность.
Описание к рис. 2.29 Кривые доза-ответ различных агонистов (А) с различными значениями Aso, максимума и кривизны (h). Следует отметить, что по оси Y ответ агониста дан в виде Е/Етах. Приведены три агониста; чем больше концентрация А50, тем сильнее кривая уходит вправо. В случае полных агонистов максимум одинаков, а для частичных агонистов максимум меньше. Чем выше значение h, тем круче наклон кривой доза-ответ. Е — эффект; Етах — максимальный эффект; М — молярная концентрация.
Потенциал лекарства, как правило, не связан с максимальным ответом. Следует учесть, что в клинических исследованиях эти концепции могут быть смешаны. Этот параметр находится в центре кривой доза-ответ на кривой log дозы или log концентрации;
- параметр наклона (коэффициент Хилла, h); описывает крутизну кривой. Его вычисляют путем сравнения Е - [А] кривой с другой формой уравнения доза-ответ, описываемой следующей log функцией:
E/Emax= [A]h/([A]h + A50h) (ф. 2.7)
В некоторых случаях агонист, химически тесно связанный с другим агонистом, может иметь Еmах ниже, несмотря на то что оба препарата действуют на один и тот же рецептор. Такой агонист называют частичным агонистом.
Кривые доза-ответ
- Взаимосвязь между ответом на лекарство и дозой (концентрацией) лекарства называют кривой доза-ответ (DR)
- Количественный анализ действия лекарства зависит от интерпретации кривой доза-ответ
- В кривых доза-ответ обычно используют полулогарифмические графики (ось дозы представлена в log форме)
- Конкурентные антагонисты смещают кривую доза-ответ вправо
Для описания кривой DR используют термины «крутизна», «потенциал», «внутренняя активность» и «эффективность»[править | править код]
Как следует из сказанного ранее, кривую DR точно описывают три параметра. Значения крутизны могут быть больше и меньше 1,0, а значение 1,0 означает простейшую модель А + R = AR. Термин «потенциал» описывает локализацию кривой на оси доз. Важно помнить, что ED50, ЕС50 и сходные характеристики потенциала обычно не соответствуют КА, рассчитанной при исследовании связывания. Потенциал имеет четкое значение, но, к сожалению, его не всегда используют правильно.
Вычисление потенциала и крутизны не представляет трудностей, в то время как определение максимального эффекта для определенного препарата зачастую затруднено. Термин «эффективность» широко используют для описания потенциала препарата оказывать желаемый терапевтический эффект. Под фармакологической эффективностью (е) понимают способность агониста вызывать ответ. Таким образом, антагонист обладает нулевой эффективностью, а полный агонист — максимальной. Частичные агонисты характеризуются средней эффективностью. Схожим термином является «внутренняя активность», которая для полных агонистов равна 1,0. Следовательно, параметры частичных агонистов имеют значения менее 1,0.
Фактически термин «потенциал» равен значению А50. Чем ниже А50, тем меньшая концентрация препарата необходима для эффекта, равного 50% от максимального ответа, и тем выше потенциал. Таким образом, наивысший Еmах иногда равен внутренней активности или эффективности. Следовательно, агонист А может быть более мощным, чем агонист В, даже если не достигает максимальной эффективности В (т.е. Еmах для В больше, чем для А).
Определения
- Аффинитет — это способность связываться с рецепторами
- Эффективность — это взаимосвязь между оккупацией рецепторов и способностью вызывать ответ на молекулярном, клеточном, тканевом или системном уровне
- Внутренняя активность — способность одного комплекса лекарство-рецептор вызывать ответ
Связь между тканевым ответом и количеством комплексов препарат-рецептор обычно нелинейная
Поскольку типичная кривая log[A] против ответа (Е) сходна с теоретической кривой [DR] против log[D], считается, что ответ Е напрямую отражает количество комплексов агонист-рецептор [AR]. В частности, считается, что Е/Еmах эквивалентно [AR]/[RJ. Однако данное тождество встречается редко, и соотношение между Е и [AR] может быть нелинейным и сложным.
Очень часто Еmах просто отражает способность системы производить ответ Е. Например, если А -это агонист, действующий на рецептор, снижающий артериальное давление, максимальным эффектом А будет снижение давления до 0 мм рт. ст. Даже в случае неприемлемых показателей ответа, как у агонистов с различным Еmах в одной культуре ткани, Е, составляющий 50% Еmах, обычно достигается у агонистов со значением [AR]/[Rt] намного меньшим, чем 50% от Rt.
Эти выводы были сделаны, когда стало возможным получать достоверные значения констант диссоциации для агонистов, используя необратимые антагонисты, как было предложено Р. Фурчготтом в 1966 г. Как только установлена константа диссоциации агониста [Кa], график Е против [А] может быть перенесен на график Е против [AR]/[Rt], что дает информацию о системе трансдукции (клеточный ответ), связывая [AR] с Е.
Конкурентные антагонисты таких эндогенных агонистов, как нейротрансмиттеры, нейрогормоны и аутакоиды[править | править код]
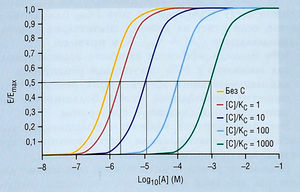
Конкурентные антагонисты смещают кривую доза-ответ вправо
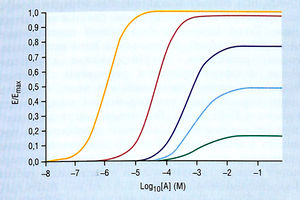
Как и при связывании, обратимые конкурентные антагонисты вызывают параллельный сдвиг вправо графиков Е (эффект) против log[A], где А — агонист (рис. 2.30). Такая связь автоматически образуется из уравнения:
[AR] = [Rt] [А]/([А] + КА (1 + [С]/Кс)) (ф. 2.8)
При любом соотношении между Е и [AR] ингибирующий эффект конкурента (К) при любой [А] всегда будет расти и уменьшаться при увеличении [А] и фактора (1 + [С]/Кс), равного отношению доз (DR). Другими словами, ингибирование заметно при любом уровне ответа и Еmах не уменьшается. Существует простой способ проверить, соответствуют ли экспериментальные данные теории. Поскольку DR - 1 = [С]/Кс, следовательно:
log(DR - 1) = log[C] - logKc (ф. 2.9)
Описание к рис. 2.30 Кривые доза-ответ агонистов (А) в присутствии конкурентных антагонистов (С) при различных концентрациях, таких как [С]/Кс, равное 1, 10, 100 или 1000. При сравнении с рис. 2.7 можно заметить, что ось X одинакова на обоих рисунках, а ось Y в данном случае представляет отношение эффектов (Е), вызванных различными концентрациями агонистов к максимальному эффекту (Emax). М — молярная концентрация.
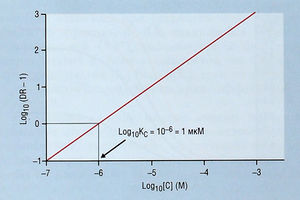
Данное уравнение носит название «закон Шильда» (рис. 2.31). Согласно закону Шильда, пересечение log10 (DR - 1) = 0 (где DR = 2) является значением Кс. По аналогии с измерением pH отрицательный log10 Кс является рА2.
В некоторых случаях уравнение (DR - 1) = [С]/Кc не подходит для агонистов, даже если антагонисты полностью конкурентны и вызывают сдвиг вправо. Отклонения от этого уравнения могут быть в случае, когда рецептор несет больше одного связывающего центра для агониста и активируется только при связывании двух и более молекул агониста. Примером такого феномена является никотиновый рецептор к ацетилхолину в скелетных мышцах.
Описание к рис. 2.31 Кривая Шильда для конкурентного антагониста (С). На этом графике DR — это отношение доз, т.е. значение А50 в присутствии определенной концентрации С, разделенное на А50 без наличия С. Здесь данные совпадают с таковыми для построения кривой Шильда. Линейный вид графика позволяет легко рассчитать Кс и кривизну. При этом изучение может проводиться в широком диапазоне концентраций. М — молярная концентрация.
Не все антагонисты конкурентные
Не все лекарственные препараты изменяют связывание агонистов конкурентным образом, прежде всего из-за того, что рецептор содержит более одного центра, распознающего лекарство, и связывание в одном центре изменяет аффинитет другого. Такой тип взаимодействия называют «аллостерическим взаимодействием», которое при экспериментальном насыщении рецепторов на 50% максимального связывания определяется как D50b (KD) и постоянно варьирует между двумя пределами. Одним пределом является отсутствие аллостерического агента, а другим — наличие практически полного связывания всех рецепторов с аллостерическим агентом. Если антагонист связывается подобным образом, он считается неконкурентоспособным.
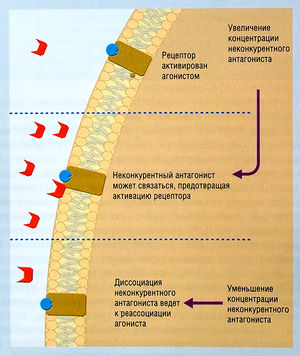
Другой теоретической моделью является связывание антагониста только с одним комплексом лекарство-рецептор (DR). Оно имеет место в случае, когда связывание D вызывает изменение конформации рецептора (рис. 2.32) таким образом, что он может связываться с антагонистом. В этом случае антагонист обозначают как неконкурентное лекарство (U). Вследствие динамики взаимодействия между лекарством (D), неконкурентным лекарством (U) и рецепторами сродство рецептора к лекарству D увеличивается в присутствии U. Это обычно происходит из-за того, что форма DR не может существовать и DRU прежде должен диссоциировать на DR и U до образования свободной формы R. В итоге D заключено в форме DRU.
Неконкурентные антагонисты снижают Еmах
Если антагонист (D) снижает Еmах, его обычно (и ошибочно) называют неконкурентным (рис. 2.33). Такой антагонизм приводит к заметным отклонениям закона Шильда от log(DR - 1) против log[D] у конкурентных антагонистов. Примером неконкурентного антагонизма является блокада ионных каналов, в которой лекарство нацелено на ионный канал, уже открытый агонистом.
Многие препараты, используемые в клинической практике, являются конкурентными антагонистами для эндогенных агонистов, таких как нейрогормоны и аутакоиды, например:
- пропранолол (β-адренорецепторы);
- галоперидол (рецепторы дофамина);
- налоксон (опиоидные рецепторы);
- фентоламин (а-адренорецепторы);
- циметидин (гистаминовые Н2-рецепторы);
- атропин (М-холинорецепторы);
- курареподобные соединения (никотиновые холинорецепторы скелетных мышц).
Описание к рис. 2.33 Кривые доза-ответ агонистов (А) в присутствии неконкурентных антагонистов (D) при различных концентрациях. Данный график сходен с графиком конкурентного антагониста на рис. 2.30. Следует отметить сдвиг вправо кривой доза-ответ с увеличением концентрации D и падением максимума. Е — эффект; Етах — максимальный эффект; М — молярная концентрация.
В этих случаях природа антагонизма и эффективность соединений (и значения Kd) установлены методами, упомянутыми ранее.
В терапии эффекты, наблюдаемые при применении конкурентных антагонистов, в действительности представляют ингибирование ответа на экзогенные или эндогенные агонисты, например подавление циметидином эндогенной кислотной секреции в желудке, регулируемой гистамином. В данном случае кривая доза-ответ характеризуется: (1) Еmах; (2) дозой, вызывающей 50% эффект (ЕС50); (3) уровнем крутизны (h). Как и кривая доза-ответ для агонистов, форма таких кривых полностью зависит от системы трансдукции, которая связывает активный комплекс агонист-рецептор (AR*) с тканевым ответом, поскольку в случае с конкурентными антагонистами любая концентрация антагониста соотносится со снижением [А]. Тем не менее показано, что ЕС50 в общем случае близка к константе диссоциации Kd, умноженной на (1 + [А]/А50). То есть ЕС50 одинакова в случае, если ответ на агонист значительно меньше максимального ([А] < А50). Как правило:
- 50% блокада эффектов агониста ассоциирована как минимум с 50% оккупацией рецепторов;
- для максимального эффекта конкурентных антагонистов необходимо, чтобы большинство рецепторов были связаны с препаратом.
Это противоречит эффектам большинства агонистов, когда максимальные ответы возникают при низкой оккупации рецепторов.
Если конкурентные антагонисты применяют для блокады действия эндогенных агонистов (например, нейротрансмиттеров), ЕС50 может быть намного меньше, чем Kd. Это объясняется тем, что [А] в районе рецептора высока относительно А50. Кроме этого, такое явление может возникать вследствие того, что физиологически [А] далеко непостоянна и типы равновесных уравнений здесь неприемлемы.
Кривые доза-ответ для неконкурентных антагонистов, иллюстрирующие подавление ответа на эндогенные или экзогенные агонисты, схожи с показанными на рис. 2.30. Поскольку эти вещества действуют через разные механизмы, можно сделать вывод о том, что, в отличие от конкурентных антагонистов, ЕС50 не соответствует пропорции
1 + [А]/А50.
Действие необратимых антагонистов сохраняется
Необратимые антагонисты характеризуются антагонизмом, который сохраняется, несмотря на исчезновение свободного антагониста. Необратимый антагонизм, производимый таким препаратом, меньше при наличии высоких концентраций агониста, инкубируемого с антагонистом.
После открытия необратимых антагонистов их эффекты на кривой доза-ответ оказались неожиданными, поскольку ранее фармакологи предполагали, что ответ на препарат прямо пропорционален [AR]. Необратимые антагонисты вызывают необратимое подавление ответов на агонисты в соответствии с уменьшением доли доступных рецепторов. Однако при этом часто не происходит заметных изменений Еmах. Типичные данные представлены на рис. 2.34, на котором при коротких периодах инкубации с необратимым антагонистом кривые смещаются параллельно увеличению значений А50 без уменьшения Еmах, что характерно для конкурентной блокады. После достаточного периода инкубации Еmах снижается, а сдвиг А50 уменьшается. Объяснением данного феномена служит то, что максимальный ответ обычно требует активации только небольшой части рецепторов. Наличие большего числа рецепторов, чем необходимо для достижения максимального ответа, часто называют резервом рецепторов.
Описание к рис. 2.34 Кривые доза-ответ агонистов (А) в присутствии необратимых антагонистов при различных концентрациях. Чем больше кривая сдвигается вправо, тем дольше ткань инкубировалась с необратимым антагонистом. Е — эффект; Еmах — максимальный эффект; М — молярная концентрация.
Резерв рецепторов указывает, что А50 (значение [А] для 50% ответа) меньше, чем КА ([А] для оккупации 50% рецепторов). Отношение Кд/А50 отражает резерв рецепторов. Этот параметр варьирует у агонистов, действующих на один и тот же рецептор. Следовательно, изменение резерва рецепторов у родственных аналогов агонистов является еще одной характеристикой рецепторов. Резерв рецепторов также определяется типом ткани, например активация нескольких доступных рецепторов может привести к максимальному клеточному или тканевому ответу вследствие заметной амплификации активируемых рецепторами сигнальных путей.
Простейшее и общепризнанное объяснение различий между агонистами (что называют внутренней эффективностью) состоит в том, что только определенная конформация комплекса AR (AR*) является активной и вызывает ответ. Агонисты с низкой внутренней активностью (А50 близка к КА при небольшом резерве рецепторов), включая частичные агонисты, формируют AR с небольшим количеством форм AR* в то время как агонисты с высокой внутренней активностью (А50 « Кд) формируют AR в основном в форме AR*. Кривые доза-ответ, показанные на рис. 2.34, содержат информацию для расчета КА агониста (не показан).
Простая модель эффективности, введенная Стивенсоном
Простая модель эффективности, введенная Стивенсоном, удобна для понимания того, как могут получаться результаты, приведенные на рис. 2.34. Предположим, что AR вызывает импульс (S), пропорциональный [AR], и что ответ (Е) — это функция S, которая не бесконечна. В этом случае;
S = е [AR]/[Rt], (ф. 2.10)
где е — константа пропорциональности, называемая эффективностью, которая может изменяться у разных агонистов, и
Е = E'S/(1 + S),(ф. 2.11)
где Е — эффект, Е' — гипотетический максимум, который возникает при бесконечном S. Если агонисты во фракции (f) AR, являющейся активной конформацией (AR*), различаются, е будет пропорциональна f. Если е бесконечна, то она будет пропорциональна [Rt] (или q[Rt], если не все рецепторы действующие). Внутренняя эффективность равна e/Rt.
На основе данной модели можно проводить сравнение агонистов относительно значений е, что равносильно внутренней эффективности. Трудность состоит в том, что реальные значения е зависят от взаимосвязи между предполагаемыми Е и S, а это может быть и не типично для любой системы трансдукции.
Агонизм
- Агонизм — это проявление молекулярного и клеточного ответа при взаимодействии между препаратом (агонистом) и рецептором, активируемым препаратом. Внутренняя активность полного агониста принимается за 1
- Частичный агонизм возникает при взаимодействии препарата с рецептором, вызывающим молекулярный ответ менее 1. Усредненная внутренняя активность лежит между О и 1
- Антагонизм возникает, если препарат взаимодействует с рецептором, ингибируя действие агониста. Внутренняя активность равна О
- Обратный агонизм возникает, если препарат взаимодействует с рецептором, снижая нормальный уровень внутренней активности. Внутренняя активность равна -1
- Частичный обратный агонизм возникает, если препарат взаимодействует с рецептором, уменьшая нормальный уровень внутренней активности. Внутренняя активность лежит между О и -1
Частичные агонисты — это агонисты с низкой внутренней эффективностью и е немногим больше 1
Частичные агонисты можно рассматривать как агонисты с низкой эффективностью и е немногим больше 1. Эксперименты с необратимыми антагонистами показали, что частичные агонисты характеризуются значениями А50, близкими к КА, и отсутствием резерва рецепторов. Как уже было указано, небольшую е частичных агонистов (по сравнению с полными агонистами) можно объяснить только тем, что небольшая фракция комплексов AR образует активную конформацию (AR*) с частичными агонистами.
При наличии высоких концентраций полных агонистов частичные агонисты действуют как антагонисты
Поскольку ответ на частичные агонисты возникает при высокой оккупации рецепторов, становится ясно, что частичные агонисты работают как антагонисты полных агонистов. Следовательно, частичные агонисты можно использовать для блокирования эффектов эндогенных агонистов (например, норадреналина), вызывая при этом небольшой стойкий эффект активации рецепторов при отсутствии полного агониста. Классическим примером частичного агонизма служат β-блокаторы (например, пиндолол), являющиеся скорее частичными агонистами, чем конкурентными антагонистами. Пиндолол становится более эффективным β-блокатором при повышении активности симпатической иннервации сердца. Таким образом, если симпатическая иннервация сердца низкая, пиндолол увеличивает частоту сердечных сокращений, блокируя эффект симпатических нервов в сердце. Классический β-блокатор ни при каких условиях не увеличивает частоту сердечных сокращений (ЧСС).
Изменение ответа на препарат при десенсибилизации
Ответ организма на препарат часто непостоянен во времени, даже если концентрации препарата в рецепторном центре достигают стабильных значений. В различных ситуациях ответы на лекарство могут со временем угасать. К потере лекарством эффективности на уровне органа или на системном уровне ведут многие факторы — от прогрессирования заболевания до физиологической адаптации. Если потеря ответа на лекарство возникает на молекулярном уровне (т.е. на рецепторе), это называют десенсибилизацией. Многие механизмы способствуют десенсибилизации, функционируя на таких уровнях клеточной регуляции, как транскрипция, трансляция и белки. Эти механизмы могут работать быстро (от нескольких секунд до нескольких минут) или относительно медленно (в течение нескольких часов или дней).
Механизмы, вовлеченные в быстро развивающуюся десенсибилизацию, широко изучаются на уровне молекул, особенно G-белок-связанные рецепторы и, в частности, β-адренорецепторы. На клеточном уровне стимуляция β-адренорецепторов таким агонистом, как изопротеренол, ведет к активации аденилилциклазы и быстрому росту внутриклеточной концентрации вторичного мессенджера цАМФ. Однако во многих клетках способность изопротеренола активировать адеиилилциклазу со временем уменьшается, что ведет к падению концентрации цАМФ в клетке. Фосфорилирование β-адренорецепторов, их ассоциация с другими белками и изменение субклеточной локализации рецепторов могут способствовать уменьшению способности изопротеренола вызывать аккумуляцию цАМФ.
Десенсибилизация β-адренорецепторов (и других G-белок-связанных рецепторов) может возникать именно вследствие фосфорилирования рецепторов, связанных с агонистом — G-белок-связанным рецептором киназы (GRK). GRK образуют семейство киназ. GRK2, изначально известный как βARK, был открыт вследствие способности фосфорилировать β-адренорецепторы, связанные с агонистом. Такой механизм был назван гомологичной десенсибилизацией, поскольку в него вовлекаются только рецепторы, оккупированные агонистом. После фосфорилирования рецепторы связывают белок из группы аррестинов, что ведет к стерическому торможению взаимодействия между рецепторами и G-белками. Рецепторы могут в дальнейшем отделяться от плазменной мембраны и проникать в цитоплазму. Недавно полученные данные указывают, что интернализированные рецепторы могут способствовать новым механизмам работы β-адренорецепторов.
Другой механизм десенсибилизации рецепторов состоит в обратной связи с вторичными мессенджерами, что ведет к десенсибилизации не только рецепторов, активированных агонистом, но и других рецепторов на той же клетке. Эту форму десенсибилизации называют гетерогенной, поскольку функция многих типов рецепторов может одновременно изменяться после активации одного типа рецепторов. β-Адренорецепторы стимулируют аккумуляцию цАМФ, что ведет к активации протеинкиназы А; активированная субъединица протеинкиназы А может фосфорилировать не только β-адренорецепторы, нарушая их функцию, но и множество других рецепторов в той же клетке в соответствующих центрах фосфорилирования протеинкиназы А.
Физиологический антагонизм[править | править код]
Физиологические антагонисты препятствуют агонистам за счет механизмов, не зависящих от взаимодействия агонист-рецептор
Ранее антагонисты, ингибирующие действие агонистов, рассматривали как вызывающие ингибирование. Они действуют на рецепторы так же, как и агонисты. Но лекарственные препараты могут противодействовать эффектам агонистов и посредством других механизмов.
Препараты могут противодействовать эффектам других лекарств, воздействуя на различные молекулярные мишени
Это часто происходит при действии двух препаратов на разные рецепторы, обладающие противоположным действием на уровне ткани или органа. В этом случае препараты рассматриваются как физиологические, или функциональные, антагонисты друг друга (первый термин более правильный). Яркими примерами являются физиологический антагонизм адреналина и ацетилхолина, которые, соответственно, ускоряют и урежают сердечные сокращения, а также глюкагона и инсулина, которые, соответственно, повышают и понижают уровень глюкозы в крови.
Более сложным примером антагонизма служит нервно-мышечная блокада антидеполяризующими миорелаксантами, такими как панкуроний, и антихолинэстеразными средствами, такими как неостигмин. Кривая доза-ответ нервно-мышечной
блокады при действии неостигмина сдвигается вправо по неконкурентной модели в сравнении с панкуронием. Это происходит потому, что оба препарата действуют на совершенно разные молекулярные мишени: панкуроний — на никотиновый рецептор, а неостигмин — на фермент ацетилхолинэстеразу. Блокада активности фермента может только удвоить потенциал концевой пластинки, в результате антихолинэстераза не может снять нервно-мышечную блокаду, вызванную избыточной дозой панкурония.
Оценка ответа и практическое применение кривых доза-ответ[править | править код]
Ответы на препараты измеряют различными способами
Лекарства оказывают свое начальное действие на молекулярном уровне, например связываясь с рецептором. В итоге это приводит к клеточным, тканевым ответам и ответам на уровне органов и организма в целом, которые можно измерить. Биохимические методы часто используют для оценки внутриклеточных ответов на лекарство, в то время как ответ на уровне тканей или органов может быть измерен с помощью физических (электрических, оптических, механических) способов — как in vitro, так и in vivo. Для исследования in vitro ткани и органы изолируют от организма и погружают в физиологический буфер, обычно в стеклянном сосуде. Исследования на интактных животных или человеке называют in vivo.
До настоящего момента термины «эффект» и «ответ» использовали как синонимы, но не были даны их определения, поскольку существует множество способов действия лекарств и определения их эффектов. Следует помнить, что при достаточно высоких концентрациях лекарства могут оказывать заметные эффекты, которые не соотносятся с их ожидаемым клиническим действием.
Кривые доза-ответ почти всегда выглядят, как на рис. 2.29 и 2.30, за исключением случаев, когда лекарства действуют более чем на один тип рецепторов. Ниже определенной дозы или концентрации эффект незаметен, а при увеличении дозы ответ возрастает, достигая максимума. Дозу агониста, вызывающую полумаксимальный эффект, обычно называют ED50. Соответственно, ED10 — это доза, вызывающая 10% максимального ответа, ED25 — 25%, ED75 — 75% и т.д. Если известна концентрация агониста [А], то ей соответствуют термины «ЕС10», «ЕС25», «ЕС50» и т.д.
Терапевтическое соотношение: экспериментальный параметр между риском и пользой
- LD50 (letal dose) — доза препарата, вызывающая гибель 50% экспериментальных животных
- EDS0 (effect dose) — доза препарата, эффективная у 50% экспериментальных животных
- Отношение LD50 к ED50 — терапевтический индекс, экспериментальная мера полезности препарата
- Другие терапевтические индексы для оценки риска и пользы используют нелетальные эффекты
Соотношение ED75/ED25 (или ЕС75/ЕС25) дает простой способ оценки крутизны кривой доза-ответ на S-образном участке, который при точном измерении равняется h — коэффициенту Хилла:
Е = Еmax [А]h(ЕС50h + [А]h) (ф. 2.12)
Это еще один вариант уравнения доза-ответ, в котором [А] — концентрация лекарства, и h теоретически равняется целому числу — 1 или 2. У лекарств с h > 1 (ЕС75/ЕС25 < 9) ответ резко увеличивается соответственно дозе, что может представлять опасность. Например, глубокая анестезия, вызванная ингаляционными средствами для наркоза, может возрасти до критического уровня при очень незначительном увеличении концентрации препарата.
Иногда ответ на лекарство является квантовым («все или ничего»)
В некоторых случаях ответ на лекарство определяется не по степени выраженности, а является квантовым: ответ либо есть, либо нет, т.е. препарат лечит или не лечит, смертелен или несмертелен. С учетом таких данных на оси «ответ» на кривой доза-ответ отражается процент людей, животных или клеток, которые реагируют, поэтому такую кривую называют квантовой кривой доза-ответ. Классическая квантовая кривая доза-ответ — кривая летальности, на которой процент животных, погибших после приема лекарства или яда, указан для разных доз. Дозу, летальную для 50% животных, обозначают LD50 (летальная доза). Значение LD50 для конкретного препарата зависит от пути введения и видов, на которых испытывали лекарство. LD50 аналогична ED50 — дозе, вызывающей желаемый эффект у 50% животных.
О лекарствах судят по их терапевтическим и нежелательным эффектам (отношение польза-риск)
Терапевтический индекс, классический показатель безопасности лекарства, определяется экспериментально как отношение LD50/ED50. Данный параметр полезен, но может привести к ошибке, если кривая log доза-ответ не параллельна кривой летальности (кривые имеют разный наклон h). Некоторые фармакологи предпочитают использовать отношения LD25/ED75 или LD10/ED90, отражающие предположение Эрлиха (» в 1900 г.) о том, что лучше судить о лекарстве по отношению его максимально допустимой дозы к минимальной лечебной дозе.
Параметры оценки летальных доз могут быть определены только на животных. Однако для клиническои оценки отношения польза-риск можно использовать другие методы измерения токсичности. Например, кривую доза-ответ для положительного эффекта можно сравнить с таковой для нежелательного, но не летального эффекта и вычислить терапевтический индекс. Желание уменьшить количество животных для оценки летальности привело к росту использования подобных параметров. В клинических наблюдениях важно попытаться сравнить кривые доза-ответ для желательных эффектов с таковыми для нежелательных. К сожалению, часто отсутствует информация, необходимая для расчета обоснованных параметров. В клинической практике можно получить только ограниченные данные доза-ответ, поскольку можно назначать только небольшое количество различных доз (если проявляются нежелательные эффекты, большие дозы не назначают).
При квантовых ответах крутизна h кривой доза-ответ непосредственно отражает изменчивость тестируемой популяции. Если все животные были одинаковы, то, согласно кривой летальности, они все погибают от одной и той же дозы. В соответствии с экстенсивной статистической теорией такие результаты должны быть обработаны (с использованием «пробитов»), а также для надежности оценки ED50, LD50 и т.д. Но квантовые результаты должны подходить под вариант стандартной формулы доз:
E/Emax= Dh/(LD50h + Dh), (ф. 2.13)
где D — доза, Еmах = 100%, h — коэффициент наклона.
Иногда то, что выглядит как зависимый ответ ткани, в действительности отражает скрытые квантовые ответы, т.е. одно значение является суммой ответов многих отдельных клеток, причем каждая клетка отвечает по типу «все или ничего». Иногда это объясняет крутизну кривой доза-ответ, например, у миорелаксантов, ингибирующих сокращения скелетных мышц. В данном случае отдельные нервно-мышечные контакты в волокнах скелетных мышц при определенных концентрациях препарата либо блокируются, либо нет, а сокращения отдельных мышечных волокон либо есть, либо их нет. В гладких мышцах происходит наоборот: сокращение каждого волокна угасает соответственно дозе препарата.
Взаимосвязь доза-ответ является основой для изучения рецепторов, разработки новых лекарств и понимания их действия
При разработке и изучении лекарств основная цель состоит в классификации их по биологическим системам, на которые они действуют, и по взаимодействию с молекулярными мишенями: являются ли они агонистами, частичными агонистами, полными обратными агонистами, конкурентными или неконкурентными, обратимыми или необратимыми антагонистами. Подход состоит в измерении эффектов лекарств на различные ферментные системы и культуры ткани, содержащие различные типы молекулярных мишеней. Так, соединение может быть определено как Н1агонист (1-й тип гистаминового рецептора), если оно действует так же, как гистамин, и его действие ингибируется конкурентным антагонистом Н1рецепторов. Неустановленное активное вещество в ткани является адреналином, если его эффективность равна таковой адреналина в препаратах, содержащих различные количества адренорецепторов, и подходящий конкурентный антагонист сдвигает кривую доза-ответ неизвестного агента так же, как и кривую доза-ответ адреналина. Если лекарство или химическое соединение обладает эффектами, которые не могут быть объяснены воздействием на известные рецепторы, то можно обнаружить новые рецепторы, и если это соединение встречается в ткани, это может быть новый аутакоид. Подобные исследования привели к пониманию действия большинства лекарств, открытию эндогенных трансмиттеров и их рецепторов.
До сих пор при фармакологических исследованиях принято определять эффекты лекарств in vitro путем измерения специфических ответов препаратов гладкомышечных органов, таких как участок кишечника, артерии, вены, мочевой пузырь или уретра и т.п. Такие ткани обычно отвечают на различные агенты сокращением или расслаблением, их ответ коррелирует с концентрацией, быстро возникает и исчезает при добавлении или удалении лекарства. Таким образом, можно быстро определить взаимосвязь концентрации и ответа и ее изменение другим лекарством. Биохимический ответ на лекарство (накопление или расход вторичных мессенджеров) часто может служить более точной мерой действия лекарства и необходим в случаях, когда исследуемое лекарство действует на молекулярные мишени, которых нет в препарате ткани, что позволяет легко получить заметный физический ответ.
Определение новых молекулярных мишеней[править | править код]
Для выявления молекулярных мишеней используют опосредованные методы
Появление теории рецепторов (предположение о том, что препарат взаимодействует со специфической мишенью для инициации эффекта) в начале XX в. породило интерес к структурной и функциональной идентификации молекулярных мишеней. В конце XX в. для определения и идентификации молекулярных мишеней и их функций использовали косвенные методы. В частности, существование групп рецепторов и их подтипов могло быть показано с помощью сходных ответов различных тканей на действие разных агонистов, ингибирования этих ответов обратимыми и необратимыми антагонистами и изменения физических условий, таких как температура. Так были успешно выявлены основные известные классы рецепторов, нейромедиаторов и гормонов. Выявление других молекулярных мишеней, таких как ферменты, значительно проще, поскольку им присуща внутренняя биологическая активность.
Молекулярная биология играет важную роль в развитии молекулярной фармакологии
Достижения молекулярной биологии оказывают большое влияние на фармакологию. Техника связывания лиганда (см. ранее) позволяет локализовать и идентифицировать молекулярные мишени, проводить их очистку и устанавливать аминокислотную последовательность. Это дало возможность клонировать гены молекулярных мишеней и определить генетический код, ответственный за структуру аминокислот, и путем сравнения установить связи между группами молекулярных мишеней. Идентификация ДНК-кода для молекулярных мишеней облегчает непосредственный доступ к мРНК, несущей информацию, которая в итоге соответствует данным об экспрессии молекулярных мишеней. Эти сведения очень схожи с классической теорией рецепторов, определяющей специфическое связывание препаратов. В то же время появлялись данные о внутриклеточных механизмах трансдукции комплекса препарат-рецептор в тканевый ответ. Развитие молекулярной биологии определило третью фазу понимания молекулярных мишеней и механизмов действия лекарств.
Открытие новых препаратов[править | править код]
Методики разработки новых препаратов во многом (но не полностью) зависят от техник молекулярной биологии
Фармакология — это наука о лекарственных веществах и их действии на организм. Следовательно, фармакология также является важной частью процесса разработки препаратов. Многие новые средства были открыты фармацевтическими компаниями, которым необходимо постоянное увеличение ассортимента для обеспечения экономического выживания. Техники молекулярной биологии способны произвести чистые формы целевых биомолекул, с которыми могут взаимодействовать потенциальные препараты. Эти молекулярные мишени впоследствии могут быть объединены в удобные системы, указывающие на то, являются ли лиганды агонистами или антагонистами. Из-за большого количества потенциальных лигандов, которые могут быть быстро определены, технику такого типа называют высокопроизводительным скринингом (ВПС). Современный ВПС позволяет изучить до 100 тыс. химических соединений в день, т.е. миллионы соединений природного или синтетического происхождения могут быть исследованы относительно связывания и активации целевых молекул. Данная техника лучше всего применима к рецепторам гормонов и нейромедиаторов, хотя ее также используют для ферментов ионных каналов и других молекулярных мишеней.
Кроме большого количества существующих «библиотек» лигандов есть потребность в быстрых методах синтеза новых соединений. Достижения синтетической органической химии (например, комбинаторной химии) позволяют производить большое количество соединений, соответствующих требованиям ВПС. Более того, техники ВПС также используют для изучения потенциальных препаратов с желаемыми фармакокинетическими характеристиками.
Комбинации систем ВПС позволяют определять соединения, действующие на изученные молекулярные мишени с достаточной эффективностью, селективностью и подходящими фармакокинетическими параметрами, в результате их фармакотерапевтический потенциал может быть изучен непосредственно у человека.
Однако оптимизм по поводу того, что данный подход позволит разработать новые препараты для каждого заболевания, должен быть подтвержден результатами. Трудность состоит в том, что почти никогда нет полного представления о роли доступных молекулярных мишеней в физиологии и патологии и о комплексном воздействии на гомеостаз каскадов клеточных реакций, инициируемых ими.
Таким образом, пока молекулярно-биологический подход в фармакологии обеспечивает быстрые пути разработки препаратов, надежные методы оценки терапевтического потенциала новых препаратов требуют функционального анализа действия препаратов в культуре ткани, системах органов и организме в целом (включая животные модели с целевой патологией). Кроме того, организм представляет собой интегральную единицу, которая значительно больше, чем сумма ее частей.
Клинические реакции[править | править код]
Клинические реакции на препараты оценивают с помощью разнообразных методов: от измерения физиологических функций (частота сердечных сокращений, артериальное давление) до уровней излечиваемости или смертности пациентов в популяции. Однако, поскольку цель лекарственной терапии состоит в излечении или облегчении течения заболевания для улучшения и продления жизни, увеличиваются попытки напрямую измерить эти эффекты. Как уже упоминалось, большое количество пациентов желает иметь эту информацию, для чего и проводятся клинические наблюдения. Альтернативным способом изучения новых препаратов, попадающих на рынок, является мониторирование всех назначений (в разумных пределах), повлекших фатальные или нежелательные реакции.
Клинически использование любого препарата зависит от знания подходящей дозы, которая в свою очередь зависит от данных кривой доза-ответ относительно как основных, так и нежелательных (побочных) эффектов. Изначально кривую доза-ответ для новых препаратов получают на основе изучения культуры ткани, затем животных и только потом — человека. Иногда невозможно получить полную терапевтическую кривую доза-ответ у человека вследствие высокой токсичности препарата при увеличении дозы. Как правило, такие исследования сложны и требуют больше времени, чем в клинической практике. Например, эффект определенной дозы препарата для снижения болевого порога у человека может быть оценен с помощью визуальной аналоговой шкалы, на которой указывают субъективное ощущение боли от 0 (нет боли) до 10 (максимально возможная боль). Однако ощущения боли варьируют у разных людей, степень болевых ощущений часто колеблется, кроме того, боль может возникать вследствие разных патологических процессов. В результате для определения окончательной кривой доза-ответ у человека для новых анальгетиков нужно сотни наблюдаемых и длительные исследования, что нецелесообразно. С другой стороны, на животных моделях (крысы или мыши) снижение боли может быть определено по среднему времени облизывания животным лапы, в которую было введено вещество, вызывающее воспаление. Для получения таким методом данных для кривой доза-ответ может потребоваться от 100 до 200 животных и несколько часов наблюдения. Обычно до этого строятся упрощенные кривые доза-ответ, полученные на разных тканевых препаратах, для определения отсутствия фармакологического действия, которое могло бы мешать клиническому использованию препарата.
С точки зрения трудности получения истинной связи доза-ответ у человека часто проводят корреляции. Например, хронически повышенное артериальное давление неизвестной этиологии (первичная гипертензия) статистически ассоциировано с повышенной заболеваемостью и смертностью, поэтому идеальным измерением антигипертензивных препаратов является степень, на которую они снижают заболеваемость и смертность, против возможности побочных эффектов. Это требует проспективного клинического наблюдения тысяч пациентов в течение многих лет, поэтому обычно эффект антигипертензивных средств оценивают с позиции их эффективности и силы, используя заменитель снижения артериального давления, которое легко измерить. Взаимосвязь доза-ответ для истинной клинической эффективности для большинства широко используемых антигипертензивных препаратов до сих пор не получена, хотя большое внимание уделяется их способности уменьшать смертность. Интересно, что, несмотря на доступность многих антигипертензивных препаратов, относящихся к разным классам, сравнительно немногие доказанно уменьшают смертность пациентов с эссенциальной гипертензией.
Популяционные эффекты[править | править код]
Разные люди по-разному реагируют на действие лекарств. В результате возникает необходимость в проведении мероприятий для определения эффектов препаратов в популяции. Опыт показал, что данные должны быть собраны согласно протоколу, а не в ходе рутинной работы.
Данные, полученные в фазах II и III клинического наблюдения (см. Этапы разработки лекарственных препаратов), являются важным источником информации для оценки действия препаратов в популяции. Эти данные могут быть использованы не только для определения токсичности препарата, но и для увеличения его эффективности. Главной проблемой, связанной с получением информации в регистрационных исследованиях, может быть недостаток выборки группы.
Эта проблема может усугубиться различной степенью тяжести заболевания у разных пациентов. Но эти трудности частично преодолеваются разработкой исследований с вовлечением большого количества пациентов. В долгосрочной перспективе постоянный сбор информации о действии лекарств в популяции может служить условием для оптимизации дозы в целях уменьшения токсичности и увеличения фармакотерапевтической выгоды.
При изучении эффекта препарата в популяции необходимо учитывать образ жизни пациентов. Например, курящий пациент — представитель определенной популяции.
Это означает, что врачу, назначающему препарат, понадобится приспосабливать значения, полученные в общей популяции, для конкретного пациента. Такие детали играют важную роль в решении врача, назначающего препарат.
Читайте также[править | править код]
- Кумулятивный эффект
- Соотношение доза-эффект
- Кривая концентрации
- Концентрация лекарственных веществ
- Что делают лекарства и каким образом
- Молекулярное действие лекарств (молекулярные мишени)
- Действие лекарств на клетки
- Тканевое и системное действие лекарств
- Рецепторы - виды и классификация
- Регуляция рецепторов
- Взаимодействие лекарственных средств с рецепторами
Литература[править | править код]
- Delmas Р, Coste В, Gamper N, Shapiro MS. Phosphoinositide lipid second messengers: new paradigms for calcium channel modulation. Neuron 2005; 47: 179-182.
- Felix R. Molecular regulation of voltage-gated Ca2+ channels. J Recept Signal Transduct Res 2005; 25: 57-71.
- Gainetdinov RR, Premont RT, Bohn LM, Lefkowitz RJ, Caron MG. Desensitization of G protein-coupled receptors and neuronal functions. Annu Rev Neurosci 2004; 27: 107-144.
- Gouaux E, Mackinnon R. Principles of selective ion transport in channels and pumps. Science 2005; 310: 1461-1465.
- Hawrylyshyn KA, Michelotti GA, Coge F, Guenin SP, Schwinn DA. Update on human alphal-adrenoceptor subtype signaling and genomic organization. Trends Pharmacol Sci 2004; 25: 449-455.
- Kass RS. The channelopathies: novel insights into molecular and genetic mechanisms of human disease. J Clin Invest 2005; 115: 1986-1989.
- Lefkowitz RJ, Shenoy SK. Transduction of receptor signals by beta-arrestins. Science 2005; 308: 512-517.
- Ray WA. Population-based studies of adverse effects. New Engl J Med 2004; 349: 1 592-1 594.
- Summers RJ, Broxton N, Hutchinson DS, Evans BA. The Janus faces of adrenoceptors: factors controlling the coupling of adrenoceptors to multiple signal transduction pathways. Clin Exp Pharmacol Physiol 2004; 31(11): 822-827.
- Thompson MD, Burnham WM, Cole DE. The G protein-coupled receptors: pharmacogenetics and disease. Crit Rev Clin Lab Sci 2005; 42(4): 31 1-392.
- Wray S, Burdyga T, Noble K. Calcium signalling in smooth muscle. Cell Calcium 2005; 38(3-4): 397-407.