Катехоламины — различия между версиями
Dormiz (обсуждение | вклад) (→Типы адренорецепторов и действие катехоламинов) |
Dormiz (обсуждение | вклад) (→Читайте также) |
||
| Строка 99: | Строка 99: | ||
*[[Адренергические рецепторы и синапсы]] | *[[Адренергические рецепторы и синапсы]] | ||
*[[Адренергический синапс]] | *[[Адренергический синапс]] | ||
| − | |||
*[[Симпатомиметики]] | *[[Симпатомиметики]] | ||
*[[Адреномиметики]] | *[[Адреномиметики]] | ||
Версия 23:15, 26 октября 2014
Содержание
Типы адренорецепторов и действие катехоламинов
Источник: «Наглядная фармакология».
Автор: X. Люльман. Пер. с нем. Изд.: М.: Мир, 2008 г.
Биологический эффект адреналина и норадреналина обусловлен адренорецепторами (а1А,В,D, a2A,B,C, β1,β2, β3)- Ранее в терапии адренорецепторы классифицировались как a1, а2, β1 и β2.
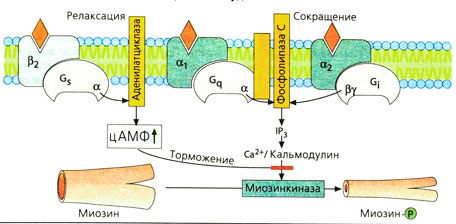
Влияние на гладкие мышцы. Противоположные эффекты, возникающие при стимуляции a1- и β2-адренорецепторов клеток гладких мышц, объясняются различиями внутриклеточных механизмов передачи сигнала. Стимуляция a1 -адренорецептора посредством внутриклеточного инозитол-трифосфата (1Р3) приводит к высвобождению ионов кальция. Кальций совместно с белком кальмодулином активирует миозин-киназу, что приводит к фосфорилированию сократительного белка миозина и повышению сосудистого тонуса (вазоконстрикция). а2-Адренорецепторы могут одновременно вызывать сокращение клеток гладких мышц и активировать фосфолипазу С (ФЛС) с помощью βу-субъединиц Gj-белка.
цАМФ блокирует активацию миозинкиназы. β2-Рецепторы активируют Gs-белки, что ведет к повышению уровня образования цАМФ и вазодилатации.
Сосудосуживающий эффект адреномиметиков используется при назначении адреналина вместе с местными анестетиками или при изготовлении капель в нос (нафазолин, оксиметазолин, ксилометазолин). Адреналин применяется системно для повышения артериального давления при анафилактическом шоке и экстренной реанимации.
Бронходилатация. При стимуляции β2-рецепторов (например, фенотеролом, сальбутамолом, тербуталином) происходит расширение просвета бронхов. Этот эффект используется при лечении бронхиальной астмы и хронического обструктивного бронхита, причем лучше использовать препараты для ингаляции, чтобы избежать нежелательного системного воздействия.
Токолитическое действие. Блокирующий эффект β2-адреномиметиков (например, фенотерола) на сократимость мышц матки используется для предотвращения схваток при угрозе выкидыша. Вазодилатация, возникающая при стимуляции β2-рецепторов, приводит к рефлекторной тахикардии на фоне уже имеющейся тахикардии, вызванной стимуляцией β1-адренорецепторов.
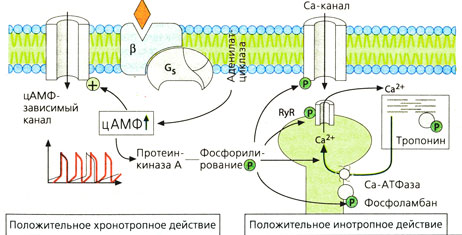
Влияние на работу сердца. Катехоламины через β1 -адренорецепторы усиливают все функции сердца: силу сокращений (положительное инотропное действие), частоту сокращений (хронотропное), возбудимость (батмотропное), проводимость (дромотропное). В проводящей системе активируются цАМФ-зависимые каналы, которые ускоряют диастолическую деполяризацию, и порог для активации потенциала действия достигается раньше (Б). цАМФ активирует протеинкиназу А, которая фосфорилирует различные Са2+-транспортные белки. Возбуждение сердечной мышцы ускоряется; при возбуждении из внеклеточного пространства в клетки через Са2+-каналы L-типа поступает больше Са2+, а также усиливается высвобождение Са2+ из саркоплазматического ретикулума (благодаря рецепторам рианодина, RyR). Быстрое расслабление сердечной мышцы осуществляется через фосфорилирование тропонина и фосфоламбана (активирует Са-зависимую АТФа-зу). При острой сердечной недостаточности можно вводить β-миметики, при хронической недостаточности они не вводятся.
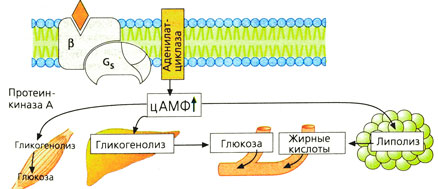
Влияние на обмен веществ. Стимуляция β2-адренорецепторов в печени и скелетных мышцах посредством увеличения уровня цАМФ приводит к распаду гликогена с образованием глюкозы (гликогенолизу). Из печени глюкоза поступает в кровь. В жировой ткани происходит распад триглицеридов с образованием жирных кислот (липолиз, опосредованный β2 и β3-рецепторами), которые также поступают в кровь.
Катехоламины и средства, влияющие на адренергическую передачу
Источник:
Клиническая фармакология по Гудману и Гилману том 1.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
Катехоламины выделяются симпатическими нервами и клетками мозгового вещества надпочечников. Эти вещества участвуют в регуляции множества физиологических функций; в частности, именно они отвечают за единую реакцию организма на стресс, направленную на поддержание гомеостаза. Норадреналин служит главным медиатором симпатической нервной системы, а адреналин — основным гормоном мозгового вещества надпочечников. Симпатическая нервная система активируется при самых различных физиологических и патологических состояниях — физической нагрузке, эмоциональном напряжении, кровопотере и многих других. Функции этой системы многообразны, и поэтому препараты, воспроизводящие, изменяющие или блокирующие эти функции, применяют при целом ряде заболеваний. К ним относятся, в частности, артериальная гипертония, гемодинамический шок, аритмии, бронхиальная астма, анафилактические реакции. Лечение некоторых из этих заболеваний обсуждается в гл. 28, 32, 33, 34 и 35.
У млекопитающих физиологические и биохимические реакции на симпатические влияния в большинстве случаев опосредованы норадреналином, хотя определенный вклад вносят и котрансмиттеры, например пептиды. При стрессе происходит также выброс из мозгового вещества надпочечников гормона адреналина. Эффекты норадреналина и адреналина в одних органах почти одинаковые, в других — существенно различаются. Так, оба они оказывают стимулирующее действие на сердце, однако адреналин вызывает расширение сосудов скелетных мышц, а норадреналин — сужение сосудов кожи, слизистых и почек.
Третий эндогенный катехоламин — это дофамин. Он содержится преимущественно в базальных ядрах, однако окончания дофаминергических нервов и дофаминовые рецепторы найдены и в других отделах ЦНС и в периферических органах. Роль катехоламинов в ЦНС подробно обсуждается в 12-й и других главах.
Естественно, что средства, влияющие на адренергическую передачу, — адренергические средства, с одной стороны, адреноблокаторы — с другой, — относятся к наиболее изученным фармакологическим препаратам. Многие особенности их действия легко понять, зная эффекты эндогенных катехоламинов. Сами по себе эти катехоламины также иногда применяются в качестве лекарственных средств, однако чаще в качестве адреностимуляторов используют их синтетические аналоги. Такие препараты обладают рядом преимуществ: большими биодоступностью при приеме внутрь и длительностью действия, избирательностью по отношению к разным подтипам адренорецепторов и другими. Все это делает их более эффективными и уменьшает выраженность и вероятность побочных реакций. Здесь мы рассмотрим структуру, молекулярные механизмы действия и физиологические эффекты всех этих средств.
Эндогенные катехоламины и адренергические средства
Большинство эффектов эндогенных катехоламинов и адренергических средств можно разделить на несколько категорий: 1) возбуждающее действие на некоторые гладкомышечные органы (например, сосуды кожи, почек и слизистых) и железы (например, слюнные и потовые), 2) тормозное действие на другие гладкомышечные органы (например, кишечник, бронхи, сосуды скелетных мышц), 3) возбуждающее действие на сердце (повышение частоты и силы сокращений), 4) метаболическое действие (усиление гликогенолиза в печени и мышцах, мобилизация свободных жирных кислот из жировой ткани), 5) влияния на эндокринные железы, в частности модуляция (усиление или ослабление) секреции инсулина, ренина и гормонов гипофиза, 6) центральное действие (например, возбуждение дыхательного центра, а у некоторых веществ — общее возбуждающее и анорексигенное действие), 7) пресинаптическое действие — торможение или облегчение высвобождения ряда медиаторов, например норадреналина и ацетилхолина (тормозящие влияния играют большую физиологическую роль, чем облегчающие). Многие из этих влияний и рецепторы, которыми они опосредуются, приведены в табл. 6.1 и 6.3. Разные адренергические средства могут в большей степени оказывать либо те, либо другие из перечисленных эффектов. Однако многие из таких различий носят чисто количественный характер, и поэтому разбирать в деталях влияния каждого из средств этой группы было бы лишним. Мы ограничимся подробным рассмотрением наиболее типичного из них — адреналина.
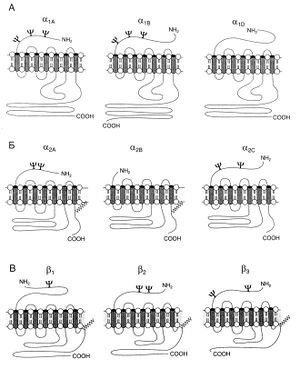
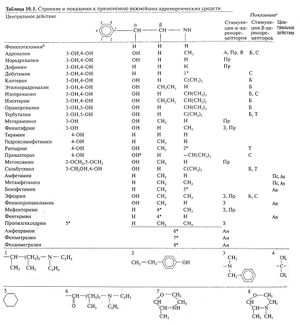
Эффекты препаратов, вмешивающихся в адренергическую передачу, невозможно понять, не зная классификацию, распределение и функции разных типов, подтипов и подгрупп адренорецепторов. Строение этих рецепторов приведено на рис. 10.1, а подробно они разбираются в гл. 6
Описание к рис. 10.1. Строение различных у адренорецепторов. Каждый из трех основных видов адренорецепторов— a,, Oj и р, в свою очередь, де- I лится на три разновидности. Стимуляция всех подтипов Р-адренорецепторов приводит к активации аденилатциклазы. Альфа^адрено-рецепторы всех подгрупп также сопряжены с одинаковыми системами вторых посредников и внутриклеточными эффекторными структурами — их стимуляция сопровождается ингибированием аденилатциклазы, открыванием зависимых от G-белков калиевых каналов, снижением вероятности открывания медленных кальциевых каналов. Напротив, разные подгруппы а-адренорецепторов, видимо, связаны с разными механизмами внутриклеточной передачи сигнала. у — участки N-гликозилирова-ния, wwa— участки тиоаципирова-ния.
Историческая справка
Прессорное действие экстракта надпочечников было впервые обнаружено Оливером и Шефером в 1895 г. (Oliver and Shafer, 1895). В 1899 г. Абель предложил назвать действующее начало таких экстрактов эпинефрином. Эпинефрин, или адреналин, был синтезирован независимо Штшцем и Дейкином (Hartung, 1931). Развитие представлений об эндокринной и медиаторной функции адреналина и норадреналина рассмотрено в гл. 6. В 1910 г. Баргер и Дейл (Bargerand Dale, 1910) описали эффекты большого числа близких кадреналину синтетических аминов и назвали эти эффекты симпатомиметическими. В этой работе были заложены представления о том, какие структурные особенности определяют действие адренергических средств. В дальнейшем было показано, что введение кокаина и хроническая денервация подавляют реакции на эфедрин и тирамин, но усиливают действие адреналина. Из этого следовало, что различия между симпатомиметическими аминами не всегда бывают чисто количественными. Появилась точка зрения, согласно которой адреналин действует непосредственно на эффекторные органы, а эфедрин и тирамин — на адренергические окончания. Далее было обнаружено, что резерпин истощает запасы норадреналина (Bertler etal., 1956), а тира мин и некоторые другие симпатомиметические амины не действуют на фоне резерпинизации. Из этого следовало, что действие подобного рода веществ сводится к высвобождению эндогенного норадреналина (Bum and Rand, 1958).
Химические свойства
Структурно-функциональная зависимость. В основе строения всех адренергических веществ (табл. 10.1) лежит структура, состоящая из бензольного кольца и этиламиновой боковой цепи. Множество соединений с адренергическим действием образуются путем замен в бензольном кольце,а также при а- и β-атомах углерода и в аминогруппе этилаыиновой цепи. Норадреналин, адреналин, дофамин, изопреналини некоторые другие вещества имеют гидроксильные группы в 3-й и 4-й позициях бензольного кольца. Поскольку о-дигидроксибензол называется также катехолом, адренергические вещества с гидроксильными группами в бензольном кольце были названы катехоламинами.
Многие адренергические вещества влияют непосредственно на адренорецепторы (адреностимуляторы), но соотношение между их сродством к а- и β-адренорецепторам различно —от преимущественно а-адреностимулирующего (норадреналин) до преимущественно β-адреностимулирующего (изопреналин) действия. Точки приложения адренергических веществ многообразны, однако разные вещества из этой группы применяются по разным показаниям (табл. 10.1).
Расстояние от бензольного кольца до аминогруппы. Адренергическая активность резко повышается, если бензольное кольцо и аминогруппа разделены двумя углеродными атомами. Это правило применимо почти ко всем адренергическим веществам.
Замены в аминогруппе. Роль таких замен особенно ярко видна на примере избирательности к а- и β-адренорецепторам: чем длиннее алкильный радикал (например, у изопреналина), тем выше сродство к β-адренорецепторам Бета2-адреностимулируюшее действие норадреналина довольно слабое, а при добавлении в аминогруппу адреналина замещающей метильной группы это действие резко усиливается. Важное исключение — фенилэфрин: у этого вещества также имеется замещающая метильная группа в аминогруппе, однако он является избирательным а-адреностимулятором. Для β2-адреностимулирующего действия необходим длинный замещающий радикал, однако для того чтобы препарат обладал избирательностью к β2-адренорецепторам (по сравнению с β1-адренорецепторами), требуются и другие замены. Как правило, чем короче замещающий радикал, тем выше сродство к а-адренорецепторам, но а-адреностимулирующая активность веществ с метильной замещающей группой выше, чем у незамещенных соединений. Так, эта активность максимальна у адреналина, ниже — у норадреналина и почти отсутствует у изопреналина.
Замены в бензольном кольце. Для максимальной активности в отношении как а-, так и β-адренорецепторов необходимы гидроксильные группы в положениях 3 и 4 бензольного кольца. Если одной или обеих этих групп нет и отсутствуют другие заместители в ароматическом кольце, то адреностимулирующая активность снижается. Поэтому фенилэфрин слабее адреналина и как а-, и как β-адреностимулятор, а β2-адреностимулирующим действием почти не обладает. Исследования структуры и функции β-адренорецепторов показали, что гидроксильные группы при Сеβ204 и Сеβ207 могут образовывать водородные связи с гидроксильными группами катехоламинов в положениях 3 и 4 соответственно (Strader et al., 1989). Возможно также, что Асп113 электростатически взаимодействует с аминогруппой катехоламинов. Поскольку Сеβ204 и Сеβ201 располагаются в пятом трансмембранном домене β-адренорецептора (гл. 6), а Асп"3 — в третьем, можно предположить, что катехоламины при связывании располагаются параллельно мембране, образуя мостик между указанными доменами. Впрочем, данные исследования дофаминовых рецепторов позволяют предположить и другие варианты (Hutchins, 1994).
Избирательность по отношению к β2-адренорецепторам у соединений с длинным радикалом при аминогруппе зависит от наличия гидроксильных групп в положениях 3 и 5 бензольного кольца. Так, орципреналин, тербуталин и сходные препараты вызывают расслабление гладких мышц бронхов у больных бронхиальной астмой, но по сравнению с неизбирательными средствами оказывают гораздо меньшее влияние на сердце. Эффекты некатехоламиновых производных фенилэтиламина частично обусловлены высвобождением норадреналина из пресинаптических окончаний. Поскольку норадреналин слабо действует на β2-адренорецепторы, действие таких веществ опосредовано преимущественно активацией а- и β1-адренорецепторов. Те же из подобных соединений, которые не имеют гидроксильных групп не только в бензольном кольце, но и при β-атоме углерода боковой цепи, действуют исключительно через высвобождение норадреналина.
Поскольку наличие полярных замещающих групп в молекуле фенилэтиламина приводит к снижению жирорастворимости, незамещенные или алкилированные соединения легче проникают через гематоэнцефалический барьер и, следовательно обладают центральным действием. Это характерно, например для эфедрина, амфетамина и метамфетамина. Кроме того, как уже говорилось, отсутствие полярных гидроксильных групп приводит к снижению адреностимулирующего действия.
Действие катехоламинов короткое. При приеме внутрь они неэффективны, так как полностью разрушаются в слизистой кишечника и в печени (гл. 6). На вещества с негидроксильными группами в положениях 3 и 4 (или хотя бы в одном из этих положений) КОМТ не действует, и поэтому как длительность их действия, так и биодоступность при приеме внутрь выше.
У соединений с негидроксильными замещающими группами в бензольном кольце, как правило, α-адреностимулирующее действие снижено, а β-адреностимулирующее — почти отсутствует; более того, такие соединения могут быть даже β-адреноблокаторами. Так, метоксамин служит избирательным α-адреностимулятором, а в высоких дозах — β-адреноблокатором. Важным исключением является сальбутамол — избирательный β2-адреностимулятор с заместителем в положении 3:
Замены при α-атоме углерода. На соединения с такими заменами не действует МАО. Если же подобные замены имеются у некатехоламиновых производных фенилэтиламина, на которые не действует и КОМТ (см. выше), то T1/2 резко повышается. Именно поэтому длительность действия, например, эфедрина и амфетаминов измеряется не в минутах, а в часах. По той же причине препараты с метильной группой в a-положении (например, метараминол) долго сохраняются в нервных окончаниях, вызывая высвобождение из них норадреналина.
Замены при β-атоме углерода. Наличие гидроксильной группы при этом атоме уменьшает центральное действие — в основном из-за снижения жирорастворимости. Однако одновременно существенно возрастает а- и бета-адреностимулирующее действие. Для примера можно сравнить эфедрин и метамфетамин: первый вызывает гораздо более выраженное расширение бронхов и повышение АД и ЧСС, но гораздо слабее как психостимулятор.
Оптическая изомерия. Оптические изомеры образуются в результате введения заместителей при а- или β-атоме углерода. Левовращающие продукты замещения при β-атоме обладают большей активностью в отношении периферических органов (естественные изомеры /-адреналин и /-норадреналин в 10 раз активнее синтетических d-адреналина и d-норадреналина). Напротив, правовращающие (d-) продукты замещения при а-атоме углерода более активны, чем левовращающие (l-): d-амфетамин обладает более мощным центральным (но не периферическим) действием, чем l-амфетамин.
Активация адренорецепторов и физиологические эффекты
Важным фактором, определяющим реакцию того или иного органа на адренергические средства, служит плотность и соотношение α- и β-адренорецепторов. Так, в гладких мышцах бронхов имеются в основном β2-адренорецепторы, и поэтому норадреналин почти не снижает сопротивление дыхательных путей; напротив, изопреналин и адреналин — мощные бронходилататоры. В кожных сосудах присутствуют почти исключительно а-адренорецепторы; следовательно, норадреналин и адреналин вызывают сужение этих сосудов, а изопреналин на них почти не действует. В сосудах же скелетных мышц имеются как α-, так и β2-адренорецепторы; активация первых вызывает сужение сосудов, вторых — расширение. Порог активации β2-адренорецепторов адреналином ниже, чем а-адренорецепторов, и поэтому в физиологических концентрациях адреналин вызывает преимущественно расширение сосудов скелетных мышц. В высоких концентрациях адреналин активирует оба типа адренорецепторов, и преобладает эффект α-адренорецепторов (то есть сужение сосудов).
Конечная реакция на адренергические средства зависит не только от их прямого действия, но и от компенсаторных гомеостатических механизмов. Один из самых ярких примеров — прессорное действие а-адреностимуляторов. Это действие сопровождается активацией барорецепторов дуги аорты и каротидного синуса; в результате рефлекторно снижается симпатический и повышается парасимпатический тонус, что приводит к уменьшению ЧСС. Эта рефлекторная реакция особенно важна в случае веществ, не обладающих β-адреностимулирующим действием. При состояниях, сопровождающихся нарушением барорефлекса (например, атеросклерозе), влияния адренергических средств могут оказаться усиленными (Chapleau et al., 1995).
Непрямое симпатомиметическое действие
В течение многих лет считалось, что эффекты адренергических средств обусловлены только прямой стимуляцией адренорецепторов. Однако от таких представлений пришлось отказаться, когда выяснилось, что эффекты тирамина и многих других некатехоламиновых производных фенилэтиламина уменьшаются или исчезают после хронической десимпатизации, резерпинизации или введения кокаина. Напротив, влияния экзогенного адреналина, и особенно норадреналина, в этих условиях часто усиливались. Все это привело к предположению о том, что тирамин и подобные ему вещества оказывают непрямое действие — захватываются адренергическими окончаниями и вытесняют норадреналин из синаптических пузырьков или экстравезикулярных депо. При этом норадреналин высвобождается из окончания и действует на постсинаптические рецепторы; этим и объясняется адренергическое действие тирамина и сходных соединений. Резерпинизация приводит к истощению депо катехоламинов, а десимпатизация — к гибели симпатических окончаний; разумеется, в этих условиях тирамин действовать не может. Кокаин же ингибирует высокоаффинный нейрональный переносчик катехоламинов и некоторых родственных им соединений; при этом тирамин и сходные с ним средства не могут поступить в адренергическое окончание. Именно поэтому кокаин блокирует действие препаратов непрямого действия (симпатомиметиков), но усиливает эффекты веществ прямого действия (адреностимуляторов): когда страдает их обратный захват, они дольше остаются в синаптической щели и действуют на постсинаптические рецепторы.
Самый распространенный метод количественной оценки прямого и непрямого действия адренергических средств — это сравнение кривых доза—эффект для того или иного эффекторного органа до и после резерпинизации (Trendelenburg, 1972). Если эти кривые не изменяются, то препараты относят к средствам прямого действия, или адреностимуляторам; примеры — норадреналин и фенилэфрин. Если же эффекты препаратов устраняются резерпинизацией, то говорят от средствах непрямого действия, или симпатомиметиках; типичный пример — тирамин. Эффект же некоторых веществ на фоне резерпинизации уменьшается, но не устраняется полностью (то есть для достижения прежнего эффекта необходимы большие дозы). Это смешанные (обладающие и прямым, и непрямым действием) симпатомиметики. В разных органах и у разных животных соотношение между прямым и непрямым действием может сильно различаться. У человека это соотношение известно не всегда.
Поскольку норадреналин стимулирует преимущественно α- и β1-адренорецепторы, но гораздо слабее — β2-адренорецепторы, многие симпатомиметики (напомним, что эти средства действуют через высвобождение норадреналина) влияют в основном на органы с преобладанием а-адренорецепторов и на сердце. В то же время ряд некатехоламиновых соединений обладают довольно сильным β2-адреностимулирующим действием и порой именно из-за этого действия применяются. Так, эффекты эфедрина во многом обусловлены высвобождением норадреналина, однако он способен устранять бронхоспазм в связи с прямым действием на β2-адренорецепторы бронхов; норадреналин же такое действие не оказывает. Наконец, некоторые некатехоламиновые соединения (например, фенилэфрин) оказывают преимущественно прямое действие на адренорецепторы. Таким образом, невозможно предугадать эффект подобных соединений только на основании того, что они способны в большей или меньшей степени вызывать высвобождение норадреналина.
Ложные медиаторы
Как уже говорилось, симпатомиметики захватываются симпатическими окончаниями и вытесняют норадреналин из депо. Производные фенилэтиламина без гидроксильной группы при β-атоме углерода боковой цепи быстро удаляются из окончаний, но те соединения, которые имеют эту группу либо приобретают ее под действием дофамин-β-монооксигеназы, задерживаются в окончаниях относительно надолго — вытесняя при этом норадреналин. В результате в синаптических пузырьках накапливаются сравнительно малоэффективные вещества; поскольку количество пузырьков, изливающих свое содержимое в синаптическую щель при возбуждении симпатического окончания, остается прежним, адренергическая передача затрудняется.
Эта так называемая гипотеза ложных медиаторов позволяет объяснить некоторые необычные эффекты ингибиторов МАО. В ЖКТ под действием бактериальной тирозингидроксилазы образуются производные фенилэтиламина. Одним из них является тирамин, который подвергается окислительному дезаминированию как в ЖКТ, так и в печени и в системный кровоток попадает лишь в незначительных количествах. Ингибиторы МАО подавляют метаболизм тирамина; в результате его содержание в крови повышается, он захватывается адренергическими окончаниями (здесь его распад на фоне ингибиторов МАО также снижен), превращается под действием дофамин-β-монооксигеназы в октопамин и в таком виде накапливается в синаптических пузырьках, постепенно вытесняя норадреналин. В результате при возбуждении адренергического окончания из него выделяется уменьшенное количество норадреналина вместе с октопамином — веществом, обладающим лишь слабым а- и β-адреностимулирующим действием. Таким образом, длительный прием ингибиторов МАО приводит к нарушению адренергической передачи. В то же время у получающих эти препараты больных употребление сыра, пива или красного вина может вызвать тяжелый гипертонический криз. Эти и некоторые другие продукты, при изготовлении которых используется брожение, содержат большое количество тирамина (и, в меньшей степени, других производных фенилэтиламина). Когда МАО в клетках ЖКТ и печени подавлена, значительная часть тирамина поступает в системный кровоток, вызывая быстрый и массивный выброс норадреналина. В результате АД резко возрастает — вплоть до развития таких осложнений, как инфаркт миокарда или инсульт.