Цитостатики
Источник: «Наглядная фармакология».
Автор: X. Люльман. Пер. с нем. Изд.: М.: Мир, 2008 г.
Содержание
Цитостатики
Противоопухолевые средства
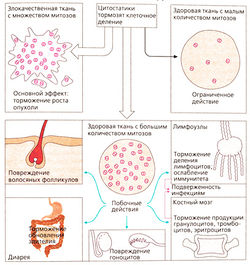
Опухоль (новообразование) состоит из клеток с неуправляемым делением. Злокачественная опухоль (рак) разрушает соседние ткани, и ее клетки распространяются по организму, образуя метастазы. Лечение направлено на уничтожение всех злокачественных клеток в организме. Если это невозможно, то пытаются затормозить рост опухоли и тем самым продлить жизнь больного (паллиативное лечение). Трудности терапии связаны с тем, что опухолевые клетки не имеют специфического обмена и являются частью организма.
Цитостатики повреждают клетки (цитотоксическое действие), находящиеся в стадии митоза. Быстро размножающиеся клетки опухоли подвергаются действию препаратов в первую очередь. Нарушение течения стадий деления препятствует пролиферации, а также приводит к апоптозу (самоуничтожению клетки). Ткани, имеющие меньшую скорость клеточного деления, т. е. большинство здоровых тканей, не подвергаются действию препаратов. Однако это же относится и к низкодифференцированным опухолям с редко делящимися клетками. В то же время клетки некоторых здоровых тканей имеют физиологически обусловленную высокую частоту деления и повреждаются под действием цитостатической терапии, вследствие которой наблюдаются следующие типичные побочные эффекты.
Выпадение волос происходит из-за повреждения волосяных фолликулов. Нарушения функции желудочно-кишечного тракта, например диарея, развиваются вследствие нарушения восстановления эпителиальных клеток кишечника, продолжительность жизни которых составляет около двух суток. Тошнота и рвота возникают из-за возбуждения хеморецепторов рвотного центра. Повышенная частота возникновения инфекционных заболеваний обусловлена ослаблением иммунной системы. Кроме того, цитостатики угнетают костный мозг. В первую очередь это сказывается на короткоживущих гранулоцитах (нейтропения), затем на тромбоцитах (тромбоцитоления) и в конечном итоге на эритроцитах (анемия). Бесплодие обусловлено торможением сперматогенеза или созревания яйцеклетки. Большинство цитостатиков влияют на метаболизм ДНК, поэтому имеется опасность повреждения генетического материала здоровых клеток (мутагенное действие). Возможно, по этой же причине через несколько лет после терапии развивается лейкемия (канцерогенное действие). Если цитостатики назначаются во время беременности, то нарушается развитие плода (тератогенное действие).
Механизмы действия цитостатиков
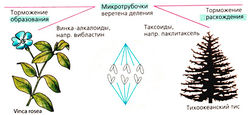
Нарушение клеточного деления. Перед делением клетки веретено деления растягивает удвоенные хромосомы. На этот этап воздействуют так называемые «анти-митотические яды» (колхицин). Одним из элементов веретена деления являются микротрубочки, образование которых блокируют винбластин и винкристин. Микротрубочки состоят из белков а- и β тубулина. Ненужные трубочки разрушаются, а их составные части снова преобразуются для повторного использования. Винкристин и винбластин относятся к винка -алкалоидам, так как производятся из вечнозеленых растений Vinca rosea. Они ингибируют полимеризацию компонентов тубулина в микротрубочки. Побочным действием является повреждение нервной системы (из-за нарушения аксонного транспорта, зависящего от микротрубочек).
Паклитаксел получают из коры тихоокеанского тиса. Препарат ингибирует разборку микротрубочек и индуцирует образование атипичных микротрубочек, блокируя тем самым преобразование тубулина в микротрубочки с нормальными функциями. Доцетаксел — полусинтетическое производное паклитаксела.
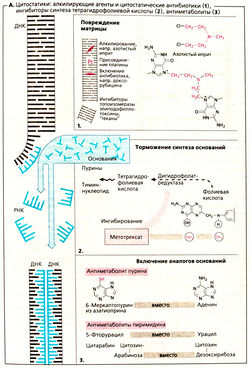
Ингибирование синтеза РНК и ДНК. Митозу предшествует удвоение хромосом (синтез ДНК) и усиление синтеза белков (синтез РНК). ДНК клетки (серый цвет на рисунке) представляет собой матрицу для нового синтеза (синий цвет) ДНК и РНК. Блокада синтеза может осуществляться перечисленными ниже способами.
Повреждения ДНК-матрицы (1). Алкилирующие цитостатики — это реакционноспособные соединения, предоставляющие свой алкильный остаток, который связывается с ДНК ковалентной связью. Например, атомы хлора из молекулы азотистого иприта могут обмениваться на азотистые основания, в результате чего образуются сшивки между нитями ДНК. Нарушается считывание информации. К алкилирующим цитостатикам относятся хлорамбуцил, мефалан, циклофосфамид, ифосфамид, ломустин, бисульфан. Особые побочные эффекты: повреждение легких бисульфаном, повреждение слизистой мочевого пузыря метаболитом циклофос-фамида акролеином (защищают с помощью 2-меркаптоэтансульфоната натрия). Соединения платины цисплатин и карбопла-тин высвобождают платину, которая связывается с ДНК.
Цитостатические антибиотики ковалентно связываются с ДНК, что приводит к обрыву цепи (блеомицин). Антрациклино-вые антибиотики даунорубицин и адриами-цин (доксорубицин) могут оказать побочное действие — повреждение сердечной мышцы. Блеомицин, по-видимому, может привести к развитию фиброза легких.
Ингибиторы топоизомеразы индуцируют обрыв цепи ДНК. Эпиподофиллотоксины этопозид и тенипозид взаимодействуют с топоизомеразой II, которая в норме поддерживает суперспирализацию ДНК путем разрывов и сшивок двунитевой ДНК. Топотекан и иринотекан являются производными камптотецина, получаемого из плодов китайского дерева. Они блокируют топоизомеразу I, которая расщепляет одно-нитевую ДНК.
Ингибирование синтеза оснований (2). Для синтеза пуриновых оснований и тимидина необходима тетрагидрофолиевая кислота (ТГФК). Она образуется из фолиевой кислоты при помощи фермента дищцрофо-латредуктазы. Аналог фолиевой кислоты метотрексат блокирует фермент и таким образом создает дефицит ТГФК в клетках. Восстановить этот дефицит можно путем введения фолиновой кислоты (5-формил-ТГФК; лейковорил или цитроворум-фактор). Гидроксимочевина (гидроксикарбамщ) ингибирует рибонуклеотидредуктазу — фермент, в норме преобразующий рибонуклеотиды в дезоксирибонуклеотиды, из которых построены молекулы ДНК.
Включение аналогов оснований (3). Аналоги оснований (6-меркаптопурин, 5-фторурацил) или нуклеозиды с аномальными сахарами (цитарабин) действуют как антиметаболиты. Они блокируют синтез ДНК/РНК или способствуют синтезу аномальных нуклеиновых кислот.
6-Меркаптопурин образуется в организме из предшественника азатиоприна (см. формулу на рис. 3). Аллопуринол блокирует распад 6-меркаптопурина, и поэтому при их комбинированном назначении нужна меньшая доза азатиоприна.
Для повышения эффективности терапии и улучшения лекарственной переносимости цитостатики часто применяют в комплексной терапии.
Поддерживающая терапия. Химиотерапия может сопровождаться приемом других лекарств. Хороший эффект для профилактики индуцированных цитостатиками и сильными мутагенными препаратами (например, цисплатином) нарушений могут давать антагонисты 5-НТ3-рецептора серотонина, например ондансетрон. Угнетение костного мозга можно предотвратить с помощью колониестимулирующих факторов гранулоцитов или гранулоцитов и макрофагов (рекомбинантные факторы филграстим, ленограстим, мол-грамостим).
Принципы целевой противоопухолевой терапии
При злокачественном перерождении стволовых клеток образуется неопластический клон, который подменяет нормальные клетки в процессах обмена. Для борьбы с этим явлением возможно целевое медикаментозное лечение.
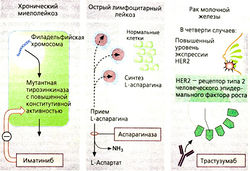
Иматиниб. Хронический миелоидный лейкоз (ХМЛ) обусловлен генетическим дефектом гематопоэтических ретикулоцитов костного мозга. Почти у всех пациентов с ХМЛ обнаруживается филадельфийская хромосома (Ph), представляющая собой хромосому 22, в которой один из фрагментов заменен на фрагмент хромосомы 9, содержащий онкоген. Вследствие этого хромосома 22 содержит рекомбинантный ген (bcr-abl). Этот ген кодирует мутант с нерегулируемой (конститутивной) повышенной тирозинкиназной активностью, что ускоряет клеточное деление. Иматиниб — ингибитор тирозинкиназ, особенно данной киназы, но может тормозить ферментативную активность и других. Больные с ХМЛ, у которых обнаружена филадельфийская хромосома, могут применять препарат перорально.
Аспарагиназа расщепляет аспарагиновую кислоту на аспартат и аммиак. Определенные клетки, например лейкозные клетки при остром лимфолейкозе, нуждаются в аспарагине для белкового синтеза. Они должны брать аспарагин из межклеточного пространства, многие же клетки других видов производят его сами. При приеме фермента, расщепляющего аспарагин, снабжение клеток аминокислотами ухудшается, ингибируется синтез белков и пролиферация неопластических клеток. Аспарагиназа производится из клеток бактерий Е coli или имеет растительное происхождение (из Erwinia chrysanthem'r, этот фермент поэтому также называют хризантаспазой). При пероральном приеме этого фермента могут возникать аллергические реакции.
Трастузумаб — терапевтический препарат на основе моноклональных антител, применяемый при злокачественных неоплазиях. Эти антитела действуют на поверхностный белок, который особенно активно способствует злокачественным перерождениям клеток. Трастузумаб связывается на HER2 — рецепторе эпидермального фактора роста. При раке молочной железы концентрация этих рецепторов намного выше. Вследствие связывания антител клетки иммунной системы становятся отличными от клеток, которые должны быть удалены. Антитела кардиотоксичны; есть сообщения, что блокирование HER2 может привести к нарушению активности сердечной мышцы.
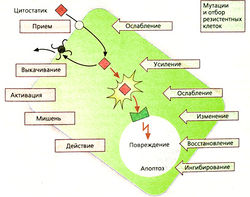
Механизмы устойчивости к цитостатикам
После успешного лечения вначале эффект от приема препарата может снизиться, так как в опухоли появляются резистентные клетки. Существует несколько механизмов развития резистентности:
Ослабление захвата препарата клеткой, например вследствие снижения синтеза транспортных белков, необходимых для проникновения метотрексата через клеточную мембрану.
Усиление защитного транспорта из клетки: увеличение продукции Р-гликопротеина, который осуществляет транспорт антрациклинов, винка-алкалоидов, эпиподофиллотоксинов и паклитаксела из клетки (множественная лекарственная устойчивость, ген mdr-1).
Ослабление биоактивации пролекарства, например цитарабина, которому для проявления цитотоксического эффекта необходимо внутриклеточное фосфорилирование.
Изменение места действия, например из-за повышения продукции дигидрофолат-редуктазы для компенсации действия метотрексата.
Восстановление повреждений, например повышение эффективности механизмов восстановления ДНК при ее повреждении цисплатином.