Лечение боли в спине
Содержание
- 1 Консервативное лечение пояснично-крестцового болевого синдрома у спортсменов
- 1.1 ПАРАВЕРТЕБРАЛЬНАЯ БЛОКАДА
- 1.1.1 Внутримышечная блокада
- 1.1.2 Проводниковая блокада
- 1.1.3 Эпидуральная блокада по Кателену
- 1.1.4 Перидуральная блокада
- 1.1.5 Блокада симпатического ствола
- 1.1.6 Блокада задних ветвей спинномозговых нервов
- 1.1.7 Блокада межпозвонкового сустава
- 1.1.8 Блокада остистых связок
- 1.1.9 Блокада пояснично-подвздошной связки
- 1.1.10 Блокада крестцово-бугорной связки
- 1.1.11 Блокада крестцово-остистой связки
- 1.1.12 Блокада крестцово-подвздошных связок
- 1.1.13 Блокада крестцово-подвздошного сочленения
- 1.1.14 Блокада грушевидной мышцы
- 1.1.15 Блокада пояснично-подвздошной мышцы
- 1.1.16 Блокада при вертельном бурсите и тендините большого вертела
- 1.1 ПАРАВЕРТЕБРАЛЬНАЯ БЛОКАДА
- 2 ЛОКАЛЬНАЯ ОЗОНОТЕРАПИЯ
- 3 МАЛОИНВАЗИВНЫЕ ХИРУРГИЧЕСКИЕ ВМЕШАТЕЛЬСТВА ПРИ ПОЯСНИЧНОКРЕСТЦОВОМ БОЛЕВОМ СИНДРОМЕ У СПОРТСМЕНОВ
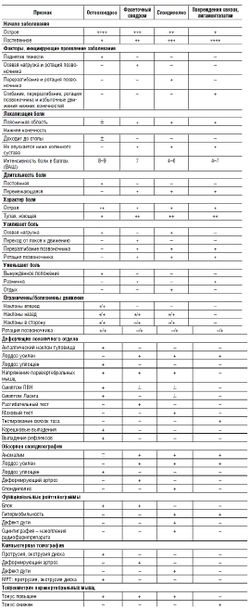
- 4 Дифференциальная диагностика пояснично-крестцового болевого синдрома у спортсменов
- 5 Читайте также
Консервативное лечение пояснично-крестцового болевого синдрома у спортсменов
В комплексном лечении различных клинических вариантов ПКБС важное место занимает использование медикаментозных средств. Среди них ведущее место занимают НПВП.
В настоящее время в области спортивной травматологии применяют большой спектр этих препаратов. К ним предъявляют два основных требования:
- эффективность, под которой понимают быстрый регресс и ликвидацию болевого синдрома и раннюю функциональную (спортивную) реабилитацию;
- безопасность, под которой понимают отсутствие нежелательных побочных действий, аллергических реакций и эффектов, входящих в конфликт с нормами международного антидопингового комитета.
Несмотря на большое разнообразие НПВП, все стандартные препараты этого класса лекарственных средств обладают общими положительными и отрицательными свойствами. Это связано с универсальным молекулярным механизмом их фармакологической активности, а именно угнетением фермента циклооксигеназы (ЦОГ), регулирующей синтез простагландинов (ПГ). Существует две изоформы ЦОГ: структурный фермент (ЦОГ-1), регулирующий продукцию ПГ, обеспечивающих нормальную (физиологическую) активность клеток, и индуцируемый изофермент (ЦОГ-2), принимающий участие в синтезе ПГ в зоне воспаления. Полагают, что анальгетические эффекты НПВП определяет угнетение ЦОГ-2, а наиболее часто встречаемые побочные эффекты (поражение ЖКТ, нарушение функции почек и агрегации тромбоцитов) - угнетение ЦОГ-1.
В последние годы получены новые факты о роли ЦОГ-1 и ЦОГ-2 в норме и при патологии, а также о ЦОГ-независимых механизмах эффективности действия НПВП: угнетение провоспалительных цитокинов; образование супероксидных радикалов оксида азота, фосфолипазы С, фактора транскрипции NF-kB, участвующего в регуляции синтеза провоспалительных цитокинов и молекул адгезии, что служит дополнительным (пусть пока на уровне эксперимента) обоснованием применения НПВП. Обоснованно предположение, что препараты со сбалансированной ингибирующей активностью в отношении ЦОГ-1 и ЦОГ-2 могут иметь преимущество перед специфическими ингибиторами ЦОГ-2 (коксибами), поскольку есть данные, что в развитии воспаления и боли участвует не только ЦОГ-2, но и ЦОГ-1, и установлена физиологическая роль ЦОГ-2-зависимого синтеза ПГ в заживлении язв верхних отделов ЖКТ, овуляции, образовании простациклина (ПГ-2) клетками сосудистого эндотелия (снижение антитромботического эффекта). Углубление знаний и накопление клинических данных о механизмах действия НПВП позволили сформировать рабочую классификацию и разделить все существующие НПВП на четыре группы:
- селективные ингибиторы ЦОГ-1 (низкие дозы ацетилсалициловой кислоты);
- неселективные ингибиторы ЦОГ (большинство стандартных НПВП - диклофенак, ибупрофен, лорноксикам и др.);
- преимущественно селективные ингибиторы ЦОГ-2 (ацеклофенак, мелоксикам, нимесулид);
- специфические (высокоселективные) ингибиторы ЦОГ-2 (целекоксиб, рофекоксиб).
При назначении НПВП необходимо учитывать данную классификацию, поскольку основная цель терапии - достижение максимального лечебного эффекта и минимизация частоты и тяжести побочных реакций, т.е. безопасность лечения.
Наряду с ингибицией синтеза ПГ имеются данные о других механизмах анальгетической активности НПВП, прежде всего о центральном опиоидноподобном антиноцицептивном действиии. У разных больных наблюдают определенные различия в ответе на тот или иной препарат, что диктует необходимость индивидуального подбора НПВП. Тем не менее в целом НПВП в эквивалентных дозах обладают примерно одинаковой анальгетической активностью, но существенно различаются по выраженности побочных эффектов, особенно в отношении ЖКТ. При этом более сильные ингибиторы ЦОГ-1 (пироксикам, индометацин) чаще вызывают побочные эффекты, чем препараты, обладающие более сбалансированной активностью в отношении ингибиции изоферментов ЦОГ (ибупрофен, кетопрофен, диклофенак). Особенно высокий риск тяжелых гастроэнтерологических побочных эффектов наблюдают на фоне лечения одним из наиболее мощных анальгетиков - кеторолаком (кетанов, кеторол).
Важно учитывать токсическое действие НПВП на хрящ, что особенно характерно для индометацина. Пироксикам, наряду с сильным угнетением ЦОГ-1, обладает и очень длительным периодом полужизни (32 ч).
К более безопасным относят короткоживущие (быстро всасываемые и быстро элиминируемые) препараты - диклофенак и производные пропионовой кислоты (ибупрофен, кетопрофен, напроксен).
Диклофенак, сочетающий в себе высокую эффективность и безопасность, считают «золотым стандартом» среди НПВП. Для всех препаратов группы диклофенака характерно отсутствие отрицательного влияния на метаболизм суставного хряща и, следовательно, межпозвонкового диска, относимого к хрящевой ткани.
Серьезными преимуществами перед стандартными НПВП обладает комбинация диклофенака и мизопростола (артротек), использование которой (как и специфических ингибиторов ЦОГ-2) позволяет снизить риск ЦОГ-зависимых побочных эффектов. Кроме того, мизопростол способен потенцировать анальгетический эффект диклофенака.
Производные пропионовой кислоты применяют при умеренном болевом синдроме. Особенно хорошая переносимость отличает ибупрофен, что позволяет много лет считать его эталоном безопасности. Поскольку побочные реакции возникают достаточно редко, ибупрофен можно применять длительно, что важно при лечении хронического ПКБС. Среди относительно безопасных НПВП с хорошей анальгетической активностью, особенно при парентеральном введении, выделяют кетопрофен, который также ингибирует синтез ПГ. Предполагают, что высокая обезболивающая способность кетопрофена связана также с его влиянием на таламические центры болевой чувствительности. Поэтому препарат можно применять для лечения умеренной и сильной боли, как острой, так и хронической. К особенностям фармакокинетики препарата относят быстрое достижение максимальной концентрации в плазме (1-2 ч после приема внутрь) вследствие быстрой абсорбции в ЖКТ. Общая частота побочных эффектов на фоне лечения кетопрофеном не зависит от кумулятивной дозы препарата. Кетопрофен относят к стандартным НПВП, но характеризуют относительно сбалансированным угнетением изоферментов ЦОГ. Это способствует снижению побочных реакций. Кетопрофен (после диклофенака и ибупрофена) занимал третье место по общей безопасности и одно из последних мест по частоте смертельных побочных эффектов в США.
Последние годы спектр неселективных НПВП расширился за счет лекарственных средств, которые обеспечивают быстрое развитие анальгетического эффекта и удовлетворительную переносимость. К ним относят лорноксикам (ксефокам).
Лорноксикам отличает от других оксикамов короткий период полувыведения (3-5 ч), что объясняет отсутствие кумуляции, снижает риск передозировки и повышает безопасность его применения. Потенциал лекарственного воздействия в 10 раз выше, чем пироксикама. Анальгетические свойства препарата связаны с мощным угнетением ЦОГ, а также торможением образования интерлейкина-6 и синтеза оксида азота. Подавляющее действие на синтез оксида азота дозозависимо и значительно более выражено, чем у диклофенака, пироксикама, напроксена, ибупрофена и кеторолака. Лорноксикам вызывает локальную блокаду синтеза ПГ в таламических центрах болевой чувствительности. Он стимулирует выработку эндогенного динорфина и эндорфина, что ведет к физиологической активации путей угнетения болевой чувствительности. Анальгезирующее действие связано также со снижением концентрации биогенных аминов, обладающих алгогенными свойствами, увеличением порога болевой чувствительности рецепторного аппарата. Лорноксикам обладает настолько выраженным анальгетическим эффектом, что в определенных ситуациях может заменять опиоидные анальгетики при лечении умеренной и сильной боли. Быстрота наступления обезболивающего действия служит основанием для назначения этих средств в первую очередь для купирования острых болевых синдромов различной интенсивности. При достаточно длительном применении (12 нед) препарат не повышает систолическое АД и оказывает стабилизирующее действие на частоту сердечных сокращений и сердечный ритм. При высокой анальгетической активности лорноксикаму присуща относительно низкая токсичность. Побочные эффекты при его применении аналогичны тем, которые вызывают другие НПВП, чаще со стороны ЖКТ.
Наиболее детально изучен первый селективный ингибитор ЦОГ-2 - мелоксикам (мовалис). Его селективность в отношении ЦОГ-2, продемонстрированная с использованием всех существующих экспериментальных методов, сопоставима с коксибами. Очень важно, что результаты применения мелоксикама в широкой клинической практике, в том числе у больных с факторами риска возникновения побочных реакций (пожилой возраст, язвенная болезнь желудка и/или двенадцатиперстной кишки в анамнезе, одновременный прием кардиопротективных доз ацетилсалициловой кислоты и др.), подтвердили, что препарат обладает оптимальным соотношением польза/риск.
Терапия мелоксикамом позволяет уменьшить риск возникновения желудочнокишечных осложнений на 36%, снизить частоту тяжелых поражений (язвы, перфорации, кровотечения) на 48% по сравнению с диклофенаком, пироксикамом и напроксеном. Кроме того, в последнее время получены очень интересные данные о возможном кардиопротективном действии мелоксикама у больных с острым коронарным синдромом. Это исследование подтверждает принципиальное отличие мелоксикама от других ингибиторов ЦОГ-2, назначение которых может, по некоторым данным, приводить к увеличению частоты инфаркта миокарда и тромботических осложнений. Фармакокинетические свойства мелоксикама дают возможность принимать препарат раз в день. При внутримышечном введении обезболивающий и противовоспалительный эффекты проявляются через 30-50 мин и сохраняются, как минимум, 5-6 ч. Системные побочные реакции при назначении мелоксикама по частоте и спектру не отличались от плацебо. Последовательное, ступенчатое, назначение мелоксикама внутримышечно, затем per os - эффективная схема лечения обострения хронической боли и может быть альтернативой применения стандартных НПВП. Преимущество мелоксикама - отсутствие отрицательного влияния на суставной хрящ, так как в терапевтических концентрациях он не подавляет образование полноценных протеогликанов в отличие от других НПВП, снижает уровень ряда ферментов, разрушающих хрящ, и может рассматриваться как хондронейтральный и даже как хондропротективный препарат. Ряд авторов изучали эффективность этого препарата в спортивной травматологии. Они установили, что он обладает выраженным анальгезирующим действием, позволяет проводить лечение, не прерывая тренировочный и соревновательный процесс, сократить сроки реабилитации спортсменов, не вызывает чувства дискомфорта в месте внутримышечного введения препарата.
Весьма перспективны специфические ингибиторы ЦОГ-2 - коксибы. Результаты исследования CLASS (Celecoxib Long-term Arthritis Safety Study), в которое было включено 8000 больных с остеоартрозом и ревматоидным артритом, свидетельствуют об очень высокой безопасности и эффективности целекоксиба (целебрекс). Анализ полученных результатов продемонстрировал достоверное снижение частоты симптоматических и тяжелых гастроэнтерологических побочных эффектов (эндоскопически выявляемые язвы) и осложнений (перфоративные язвы, обструкция, кровотечение) на фоне лечения целекоксибом по сравнению с такими безопасными НПВП, как диклофенак и ибупрофен. Отмечена крайне низкая частота печеночных и почечных побочных эффектов, которые нередко служат причиной отмены лечения.
Несмотря на то что целекоксиб не ингибирует тромбоцитарную ЦОГ-1 и, следовательно (в отличие от стандартных НПВП), не снижает агрегацию тромбоцитов, анализ базы данных, включавшей более 13 тыс. пациентов, леченных целекоксибом, и результатов исследования CLASS, не выявил какого-либо увеличения частоты инфаркта миокарда, инсульта.
Однако существующие на сегодняшний день работы предполагают, что селективные ингибиторы ЦОГ-2 (рофекоксиб, целекоксиб) все-таки могут увеличивать риск неблагоприятных сердечно-сосудистых эффектов, о чем свидетельствовало несколько подобных осложнений во время приема данных препаратов в США. Однако речь шла о приеме препаратов в достаточно высоких дозах в течение длительного времени у пациентов с ревматоидным артритом.
Как уже указывалось, НПВП - препараты выбора при ПКБС. Лечение начинают с назначения наиболее безопасных препаратов (короткого действия) в минимально эффективной дозе, поскольку побочные эффекты имеют зависимый от дозы характер (ибупрофен, лорноксикам, кетопрофен, диклофенак). Лорноксикам назначают в начальной дозе 16 мг в сутки с последующим переходом на поддерживающую терапию в дозе 4 мг 2-3 раза в сутки. У пациентов с факторами риска побочных эффектов лечение начинают сразу с мелоксикама, целекоксиба или мизопростола. Применение индометацина ограничивают купированием острого приступа боли в спине у молодых людей без факторов риска побочных эффектов. Кроме того, учитывают, что парентеральный и ректальный пути введения НПВП не предохраняют больных от возможности развития гастроэнтерологических и других побочных эффектов. Наличие инъекционных форм многих НПВП позволяет использовать принцип ступенчатой терапии болевых синдромов при дегенеративных заболеваниях позвоночника (спондилезе, спондилоартрозе): в остром периоде показано внутримышечное введение НПВП (в течение 3 дней) с последующим переходом на пероральную терапию данным препаратом в той же дозе в течение 2 нед. Дозировки наиболее распространенных НПВП приведены в табл. 14.
Таблица 14. Суточные дозы наиболее распространенных нестероидных противовоспалительных препаратов
|
Препарат |
Доза, мг/суг |
|
Диклофенак |
100-150 |
|
Ибу профен |
1200-2400 |
|
Кетопрсфен |
200-300 |
|
Индометацин |
75-150 |
|
Пироксикам |
20 |
|
Лорноксикам |
8-16 |
|
Целекоксиб |
200 |
Регуляции и подавления ноцицептивной импульсации в ЦНС и усиления деятельности антиноцицептивной системы достигают применением анальгетиков центрального действия. Основной препарат этой группы - трамадол.
Трамадол - рацемическая смесь двух энантиомеров, обладает двойным механизмом действия. Его правовращающий энантиомер связывается с ?-опиатными рецепторами и ингибирует обратный захват серотонина, а левовращающий энантиомер ингибирует обратный захват норадреналина. В результате активации норадренергической и серотонинергической систем трамадол угнетает передачу болевых импульсов на спинальном уровне. В обычных дозах он не вызывает угнетения дыхания и кровообращения, нарушения моторики ЖКТ и мочевых путей, при длительном применении не приводит к развитию лекарственной зависимости. Его важное преимущество - минимальный наркогенный потенциал. Трамадол не внесен в Конвенцию о наркотиках, находящихся под международным контролем, и не подлежит специальному учету как наркотик. Согласно данным изучения трамадола гидрохлорида с использованием контролируемых (в том числе двойных слепых) рандомизированных иссследований показано, что он купирует сильную и умеренную боль при лечении остеоартроза крупных суставов в такой же степени, как и диклофенак и мелоксикам, не оказывая при этом побочных действий, присущих НПВП. Трамадол быстро и на 90% всасывается с достижением максимальной концентрации в крови через 2 ч после приема. Особый интерес вызывают результаты успешного сочетанного применения трамадола и НПВП, позволяющего не только достичь адекватного анальгетического эффекта с минимальными побочными реакциями, но и уменьшить дозы НПВП. Препарат не имеет побочных эффектов, характерных для НПВП, и может применяться у пациентов с лекарственной гастропатией, язвенной болезнью желудка, а также печеночной, сердечной и почечной недостаточностью. Следует отметить, что в онкологической практике препарат применяют длительно, в течение 2-3 лет, без развития привыкания.
Согласно данным литературы использование трамадола показано при:
- непереносимости НПВП;
- противопоказаниях к применению НПВП;
- недостаточном эффекте терапии НПВП, когда увеличение их дозы нежелательно;
- обострении болевого синдрома на фоне приема НПВП;
- назначении глюкокортикоидов, так как применение трамадола не увеличивает риск развития желудочно-кишечных расстройств.
Побочные эффекты: седация, головокружение, тошнота и рвота, снижение аппетита, сухость во рту, запор. Медленное, в течение 2-3 дней, увеличение дозы в начале терапии помогает избежать неприятных последствий при приеме этого препарата. Нередко побочные эффекты трамадола постепенно исчезают в течение первых дней терапии. Все изложенное позволяет рассматривать трамадол как перспективное средство в лечении ПКБС. Трамадол обычно назначают по 50 мг (при сильной боли по 100 мг) до 2 раз в день.
В остром периоде поясничного болевого синдрома (дискорадикулярный конфликт, фасеточный синдром) как НПВП, так и широкий спектр анальгетических препаратов могут быть малоэффективны, так как они не устраняют рефлекторный мышечный спазм, роль которого в развитии и прогрессировании ПКБС в настоящее время считают доказанной. В связи с этим в комплексной терапии используют миорелаксанты, которые способствуют прерыванию описанного выше порочного круга боль-мышечный спазм-боль. Это толперизон и тизанидин. Толперизон блокирует моно- и полисинаптические спинномозговые рефлексы, избирательно снижает активность каудальной части ретикулярной формации головного мозга, уменьшая спастичность. Обладает центральными н-холинолитическим эффектом, также приводящим к миорелаксации. Вследствие химического родства с лидокаином снижает болевую чувствительность в периферических нервных путях, оказывает местно-анестезирующее действие. Его сосудорасширяющий эффект объясняют блокирующим воздействием на ?-адренорецепторы, локализованные в сосудах. Его назначают по 1 таблетке (0,05 мг) 3 раза в день в течение всего острого периода, но не более 3-4 нед. Препарат тизанидин также обладает спазмолитическим и анальгетическим действием. Он уменьшает выброс возбуждающих аминокислот из промежуточных нейронов спинного мозга, тем самым обеспечивая снижение повышенного мышечного тонуса, при этом не меняя сократительную способность мышц. Имеет существенное значение то, что тизанидин защищает слизистую оболочку желудка от действия НПВП, и при их одновременном назначении эффективность лечения значительно повышается. Препарат назначают в течение всего острого периода, обычно в течение 5-10 дней в дозе от 6-8 мг в сутки.
Одновременно назначают спазмолитики, в частности баралгетас. Действие этих препаратов обусловлено входящими в его состав компонентами: анальгетиком (метамизол натрия), спазмолитиком (питофенона) и ганглиоблокатором (фенпиверина), который оказывает дополнительное расслабляющее воздействие на гладкую мускулатуру. В остром периоде при выраженной боли, обусловленной дискорадикулярным конфликтом, его вводят в дозе 5 мл внутривенно капельно вместе с глюкозо-новокаиновой смесью (200 мл 5% раствора глюкозы с 200 мл 0,25% раствора прокаина). При подостром болевом синдроме баралгетас применяют в сочетании с НПВП, например с диклофенаком - внутримышечно 1-2 раза в день.
Из сосудистых препаратов применяют пентоксифиллин. Он хорошо переносится пациентами. При приеме внутрь возможно развитие диспептических расстройств, тошноты (очень редко), при парентеральном введении - падение АД. Пентоксифиллин улучшает микроциркуляцию и реологические свойства крови. Оказывает сосудорасширяющее действие и улучшает снабжение тканей кислородом. Уменьшает агрегацию тромбоцитов и приводит к их дезагрегации, снижает вязкость крови. Обычная доза по 0,1 г 2 раза в день, в острых случаях вводят внутривенно 5 мл 2% раствора в 250-500 мл раствора 0,9% натрия хлорида или в 5% растворе декстрозы.
В ряде случаев необходимо назначение транквилизаторов (хлордиазепоксид, диазепам) в ежедневной дозе 5-10 мг/сут. Они угнетают аффективные компоненты боли без изменения порога болевой чувствительности, повышают устойчивость организма к хроническому болевому воздействию, разрывая порочный круг боль- тревога-боль. Иными словами, они оказывают успокаивающее действие на ЦНС, вызывают мышечную релаксацию, обладают противосудорожной активностью, потенцируют действие снотворных и анальгетиков. Транквилизаторы назначают коротким курсом на 2 нед с постепенным снижением дозы.
При признаках депрессии и тревожной озабоченности о дальнейшей профессиональной карьере, что часто наблюдают у спортсменов с острым и хроническим ПКБС, целесообразно назначение антидепрессантов. Антидепрессанты, помимо основного эффекта, оказывают и обезболивающее действие. Полагают, что анальгетический и противоспалительный эффекты этих препаратов могут быть обусловлены подавлением синтеза таких медиаторов боли и воспаления, как ПГ-Е2 и оксид азота. Кроме того, антидепрессанты усиливают анальгетический эффект других обезболивающих препаратов. В то же время следует иметь в виду, что лечение антидепрессантами умеренно увеличивает риск желудочных кровотечений (относительный риск 2,6), особенно при их сочетанном применении с НПВП (относительный риск 15,6). При необходимости используют амитриптилин, который назначают в дозе 12,5 мг в сутки перед сном. Клинический эффект антидепрессантов обычно наблюдают не ранее чем через 2 нед от начала приема препарата. Поэтому их применяют достаточно длительный период времени, обычно не менее 6 нед.
Для стимуляции процессов регенерации применяют витамины группы В.
- Тиамин (витамин В1) - стимулирует обмен веществ и стабилизирует нервнорефлекторную регуляцию, оказывает влияние на проведение нервного возбуждения в синапсах, т.е. вызывает умеренное ганглиоблокирующее и курареподобное действие.
- Пиридоксин (витамин В6) - необходим для нормального функционирования центральной и периферической нервной системы. Активно участвует в обмене аминокислот (триптофана, метионина, цистеина, глутаминовой и других аминокислот), а также в жировом обмене.
- Цианокобаламин (витамин В12) характеризует высокая биологическая активность. Достоверное уменьшение ПКБС наблюдают при использовании больших доз цианокобаламина. Это действие связывают с повышением содержания и усилением эффекта норадреналина и 5-гидроокситриптамина, которые являются ингибирующими трансмиттерами для ноцицептивной системы. В экспериментах на животных высокие дозы цианокобаламина подавляли ноцицептивное поведение и уменьшали ноцицептивную активность, индуцированную в нейронах спинного мозга и гипоталамуса. В клинике высокие дозы цианокобаламина снижают интенсивность острой боли и потенцируют эффект НПВП.
Обычно доза витаминов группы В составляет 1 мл ежедневно в течение 10 дней. При наличии корешковой симптоматики разовая доза цианокобаламина увеличивается до 1000 мкг.
Более удобен для пациентов препарат мильгамма, который представляет комбинацию витаминов группы В и лидокаина. Для купирования боли в острый период вводят внутримышечно по 2 мл ежедневно в течение 5-10 дней.
Мощный противовоспалительный эффект глюкокортикоидов также используют в лечении острого ПКБС. Они уменьшают воспалительные являения как при спондилоартрозе, так и при корешковом синдроме. Однако их терапевтическое действие не ограничено влиянием на воспалительный процесс. Короткие курсы гормональной терапии могут уменьшать проявления нейрокомпрессионных синдромов и посредством других механизмов, в частности за счет прямого нейропротективного воздействия.
Один из комбинированных препаратов, которые могут быть полезны в острых ситуациях, - амбене. В его состав входят дексаметазон, фенилбутазон, салициламид, лидокаин и цианокобаламин. Сочетание дексаметазона и фенилбутазона обеспечивает быстрое наступление эффекта и продолжительное обезболивающее и противовоспалительное действие. Потенцирование эффектов компонентов препарата дает возможность снизить дозу дексаметазона. Добавление цианокобаламина способствует улучшению микроциркуляции и нервного проведения в зоне повреждения. Салициламид обеспечивает хорошую растворитмость препарата, что снижает риск постинъекционных осложнений. Наличие в составе амбене лидокаина делает инъекцию безболезненной. Амбене вводят внутримышечно 1 раз в день через 1-3 дня до 5 инъекций. Назначение его на более длительный срок нежелательно, поскольку связано с повышением риска побочных реакций, прежде всего со стороны ЖКТ и кроветворения. Повторные курсы можно проводить с интервалом в несколько месяцев.
С целью нормализации обменных процессов назначают биологически активные вещества (румалон, хондроитина сульфат). Эти препараты содержат экстракт хряща и костного мозга молодых животных, обладают ферментной активностью. Они улучшают обмен веществ в хрящевой ткани и стимулируют его регенерацию, способствуя дифференцированию хондробластов в хондроциты и увеличению пролиферации камбиального слоя хряща; улучшают репаративные процессы в мышечной ткани, нормализуя углеводный обмен, улучшают микроциркуляцию. Обычно эти препараты назначают в виде внутримышечных инъекций в под остром периоде поясничного болевого синдрома. К этой же группе относят и дискус композитум. Среди его составных частей - экстракты межпозвонковых дисков и костного мозга, эмбриональные ткани, витамины группы В, соединения серы, цинка, меди, серебра и т.д. Применяют дискус композитум подкожно или внутримышечно по 2,2 мл 1-3 раза в неделю.
Основной препарат для коррекции нарушений минерального обмена у пациентов с усталостными переломами дужек поясничных позвонков - альфакальцидол (оксидевит). Действующее начало этого препарата - предшественник кальцитриола, который, в свою очередь, является основным регулятором гомеостаза кальция. В костной ткани основная точка приложения кальцитриола - остеобласты, в которых он стимулирует синтез местных ростовых факторов, а также коллагена 1-го типа и матричных протеинов - остеокальцина и остеопонтина. Эти процессы способствуют ослаблению костной резорбции, репарации микроструктурных повреждений в костях, улучшению качества костной ткани, однако не обеспечивают минерализации коллагеновых фибрилл костей. Повышая всасывание кальция в ЖКТ, альфакальцидол подавляет секрецию ПТГ, увеличивающуюся в ответ на снижение концентрации кальция в плазме. Положительный момент - снижение уровня ЩФ в плазме крови, указывающее на уменьшение интенсивности костного ремоделирования на фоне терапии альфакальцидолом.
Альфакальцидол не оказывает прямого анальгетического эффекта, однако, по некоторым данным, обладает способностью индуцировать синтез кальцитонина, который обладает анальгетической активностью. Все это обусловливает быстрое купирование костной боли. Альфакальцидол улучшает также функцию скелетных мышц - органов-мишеней активных метаболитов витамина D3.
Необходимое условием поддержания ремоделирования костной ткани на нормальном уровне - достаточное потребление кальция. Даже кратковременный дефицит кальция, как показали экспериментальные исследования, может привести к нарушению механизмов, регулирующих метаболизм костной ткани. Дефицит пищевого кальция - один из факторов, способствующих нарушению минерального обмена. Поэтому кальций - обязательная составная часть медикаментозного лечения. Минимальная суточная доза кальция - 1,5 г. Один из современных препаратов кальция - кальций-сандоз форте, состоящий из лактата, глюконата и карбоната кальция с содержанием в одной шипучей таблетке 500 мг ионизированного кальция. Повышение на фоне терапии уровня кальция в плазме крови объясняют увеличением абсорбции кальция в кишечнике за счет активации под воздействием альфакальцидола синтеза кальцийсвязывающих белков.
Болевой синдром - основа дегенеративно-дистрофических заболеваний позвоночника. Его следствие - спазм паравертебральных мышц, ограничения движения позвоночника и т.д. Применение обезболивающих блокад патогенетически оправданно. Они - едва ли не самые эффективные лечебные средства, приносящие пациенту облегчение уже в ближайшее после их выполнения время. Кроме того, оценка эффективности блокады оказывает существенную помощь в постановке или подтверждении правильного диагноза, позволяет более полно представить пути формирования болевого синдрома, определить источники его продуцирования.
Блокады противопоказаны при:
- непереносимости анестетика или составляющих компонентов;
- общей и местной инфекции.
Для осуществления лечебных блокад в большинстве случае используют прокаин. Основное его действие - нейротропное. Прокаин препятствует повышению проницаемости мембраны нервных клеток при раздражении, восстанавливает нормальную проводимость и функцию нервов, нервных окончаний и спинальных ганглиев, деятельность которых нарушена в связи с патологической афферентацией из различных патологических очагов. Кроме того, он способствует нормализации деятельности вышерасположенных отделов нервной системы. В частности, прокаин способствует ликвидации очагов застойного возбуждения в ЦНС, восстановлению нейродинамики ретикулярной формации ствола мозга, снижает возбудимость моторных зон коры головного мозга. Особенность действия прокаина - он не вызывает непосредственного перерыва нервных путей, а облегчает перестройку внутриневральных отношений, действуя как более слабый адекватный раздражитель.
В результате этого уменьшается или прекращается боль, улучшается микроциркуляция вследствие нормализации проницаемости капиллярной стенки, ликвидируется сосудистый и мышечный спазм, уменьшается отек, улучшается трофика.
Образованием в процессе распада прокаина парааминобензойной кислоты, которая связывается с гистамином, объясняют его антигистаминное, антитоксическое и десенсибилизирующее действие. Из других местных анестетиков используют лидокаин, бупивакаин и т.д.
ПАРАВЕРТЕБРАЛЬНАЯ БЛОКАДА
Показания для выполнения этих блокад: остеохондроз, проявляющийся люмбалгией и люмбоишиалгией, спондилолиз.
Внутримышечная блокада
Блокаду осуществляют в положении больного лежа на животе с подложенным под живот валиком для выпрямления поясничного лордоза. После двукратной обработки кожи антисептиком проводят внутрикожную анестезию на расстоянии 4-5 см сбоку от верхнего края остистого отростка на уровне соответствующего межпозвонкового промежутка. Затем иглой длиной 10-12 см, предпосылая вперед раствор прокаина и постепенно углубляясь, проникают через паравертебральные мышцы до упора в поперечный отросток позвонка. Это обычно происходит на глубине 5-8 см. После чего направление иглы меняют, кончик ее продвигают ниже поперечного отростка и после предварительной аспирации вводят оставшийся раствор. Необходимо отметить, что отрицательная аспирационная проба не гарантирует от возможности попадания анестетика в сосудистое русло, по отдельным данным, это происходит в 8,5% случаев.
Проводниковая блокада
При наличии корешковой симптоматики выполняют паравертебральные провод никовые блокады, в результате которых осуществляют местную анестезию вокруг межпозвонкового отверстия, при этом анестезируют не только спинальные, но и менингеальные нервные веточки. Эту блокаду выполняют аналогичным образом, но после упора в поперечный отросток его обходят иглой сверху. Иглу направляют под углом 45° и продвигают до упора в край межпозвонкового отверстия.
В клинике спортивной и балетной травмы ЦИТО для подобных блокад обычно используют раствор, состоящий из 100 мл 0,5% раствора прокаина с добавлением 2 мл метамизола натрия, 2 мл дротаверина, 200 мкг цианокобаламина. При наличии ирритации нервного корешка дозу цианокобаламина увеличивают до 1000 мкг. В конце блокады вводят 1 мл дексаметазона. Эффект от первой блокады обычно кратковременный - 3-4 ч, после следующих блокад безболевой период увеличивается. Блокады обычно проводят два раза в неделю через 3-4 дня.
Вместо этих препаратов после введения прокаина можно использовать препарат амбене, содержащий витамин В12, противовоспалительные, обезболивающие компоненты (лидокаин, фенилбутазон), в том числе и дексаметазон. Последний оказывает немедленное действие, фенилбутазон обеспечивает пролонгированный эффект. Дексаметазон и фенилбутазон потенцируют действие друг друга. Кумулятивное действие составных частей препарата позволяет уменьшить дозу гормона, что существенно в профилактике возможных нарушений гомеостаза. Необходимо помнить об общих противопоказаниях для введения гормональных препаратов: заболевания ЖКТ - гастриты, язвенная болезнь; сердечная недостаточность; выраженные нарушения функции почек, печени, щитовидной железы; наличие инфекции, в том числе и хронической вирусной; аутоиммунные заболевания (системная красная волчанка и др.); глаукома; детский возраст; беременность и грудное кормление.
При выполнении проводниковой блокады обычно вводят 40-50 мл вышеупомянутого раствора и 1 мл дексаметазона или только 5% раствор прокаина с амбене .
Побочный эффект проводниковой блокады - усиление или появление корешковой боли, обусловленное местным увеличением давления после введения раствора. Специального лечения не требует. Через несколько часов эти явления самопроизвольно проходят.
Эпидуральная блокада по Кателену
Эпидуральное пространство находится между твердой мозговой оболочкой и стенками позвоночного канала. В нем расположены переднее и заднее венозные сплетения и жировая клетчатка.
Эпидуральную блокаду относят к проводниковым, параневральным блокадам. Показание к ее применению - ПКБС с корешковым синдромом. Блокаду выполняют следующим образом.
Больной лежит на боку с приведенными к животу бедрами. Нащупав рогообразные отростки крестца с обеих сторон крестцовой щели, иглой строго по средней линии прокалывают кожу, подкожную клетчатку, мембрану, закрывающую вход в крестцовый канал. Затем иглу поворачивают по ходу позвоночника и продвигают краниально на 3-4 см. При неправильном положении иглы она упрется в крестец, что препятствует введению анестезирующего раствора. Обычно объем анестетика составляет 40-60 мл.
Перидуральная блокада
Перидуральное пространство расположено между надкостницей и твердой мозговой оболочкой. Вентрально расположен дуральный мешок с его содержимым, дорсально - желтая, остистые связки, подкожная клетчатка, кожа.
Пациент лежит на боку или сидит. Делают прокол кожи, подкожной клетчатки, остистой связки по верхнему краю нижележащего остистого отростка. Конец иглы направлен краниально на 5-7?, как при выполнении спинномозговой пункции. Под поршнем шприца следует оставлять пузырек воздуха над уровнем анестезирующего раствора. Продвигая иглу вперед, ей предпосылают анестезирующий раствор. Пока игла идет в твердых тканях, пузырек воздуха сжимается; как только игла входит в перидуральное пространство, где давление отрицательное, пузырек расширяется. Для контроля шприц снимают с иглы, на канюлю «навешивают» каплю; если игла в перидуральном пространстве, капля втягивается внутрь. Объем вводимого раствора 10-20 мл.
Блокада симпатического ствола
При апофизите вследствие передней грыжи верхних поясничных межпозвонковых дисков возможно раздражение симпатического ствола. Боли при этом достаточно сильные, ноющие, глубокие. В этих случаях требуется блокада симпатического узла. Симпатический ствол расположен у медиального края большой поясничной мышцы на переднебоковой поверхности тела позвонка. Справа и спереди от левого ствола расположена брюшная аорта, слева и спереди от правого симпатического ствола - нижняя полая вена.
Блокаду симпатического ствола проводят так же, как паравертебральную проводниковую, только иглу продвигают глубже под углом 30°. На глубине 8-10 см достигают переднебоковой поверхности тела позвонка и после пробной аспирации вводят 10-20 мл 0,5% прокаина. Раствор проникает в щель между большой поясничной мышцей и телом позвонка до симпатической цепочки. В большинстве случаев достаточно одной блокады для купирования болевого синдрома.
Блокада задних ветвей спинномозговых нервов
Эта блокада позволяет прервать патологическую импульсацию, исходящую не только из фасеточных суставов, но также из мышц и связок соответствующей области.
Положение больного - лежа на животе. Вкол иглы осуществляют на три поперечника пальца латерально от нижнего края остистого отростка и на один поперечник пальца каудально. После прокола кожи иглу наклоняют под углом 15-20° в сагиттальной плоскости, располагая канюлю латерально, проводят в тканях до упора кончика иглы в основание поперечного отростка. Вводят 3-4 мл анестетика, а затем, перемещая иглу веерообразно, вводят еще 6-7 мл в область межпоперечной связки.
Таким образом, поочередно блокируют медиальную, срединную и латеральную веточки задней ветви спинномозгового нерва, иннервирующие суставы, мышцы и связки дорсальной поверхности туловища.
При выполнении этой блокады, если неправильно выбрана точка вкола, кончик иглы может проникнуть в зону межпозвоночных отверстий, что приводит к стреляющим болям и парестезиям в зонах иннервации соответствующего спинномозгового нерва. Кроме того, при проникновении иглы в межпозвоночное отверстие анестетик может попасть в субарахноидальное пространство, т.е. результатом блокады может стать спинальная анестезия.
Блокада межпозвонкового сустава
Показание для блокады - острый или хронический болевой синдром, обусловленный патологией межпозвонковых суставов.
Из-за перекрытия зон иннервации инъекции обычно осуществляют на актуальном уровне, а также на выше- и нижележащем. В связи с тем что не обнаружено данных перехода иннервации через среднюю линию у пациентов с односторонними жалобами, блокируют фасеточные суставы только с одной стороны.
При выполнении внутрисуставных инъекций необходим рентгеноскопический контроль. Пациента при этом укладывают в положение, при котором проблемный межпозвонковый сустав переводится в профиль. Это может быть и косое положение до 30-45°. После обычной обработки кожи проводят анестезию кожи, подкожной клетчатки, паравертебральных мышц. Затем иглу направляют таким образом, чтобы ее кончик вошел в нижний заворот сустава. Для уточнения глубины кончика иглы нужна только переднезадняя проекция. По мнению ряда авторов, одна из наиболее вероятных ошибок при пункции фасеточного сустава - попытка ввести иглу в среднюю часть сустава при фронтальном расположении его плоскости. В таких случаях игла соскальзывает латерально в сторону межпозвонкового отверстия, что может привести к возникновению парестезий и стреляющей боли в зоне иннервации спинномозгового нерва.
После выполнения пункции сустава в его полость вводят 0,5-1,0 мл анестетика (2% лидокаина, 0,5% бупивакаина) в смеси с глюкокортикоидом - дексаметазоном. При точном внутрисуставном положении иглы в момент введения лекарственного вещества, как правило, ощущают пружинистое сопротивление. О внутрисуставном расположении иглы также свидетельствует и репродукция отраженного болевого синдрома. При разрыве капсулы сустава ощущения сопротивления нет, и введение раствора осуществляется свободно, причем в больших, чем обычно, количествах. Емкость сустава в норме составляет 0,7-1,0 мл, однако в некоторых случаях она уменьшается до 0,3 мл или увеличивается до 2 мл.
При параартикулярных инъекциях рентгеновский контроль не требуется. Положение больного - лежа на животе. Иглу при этом вводят на 2 см сбоку от средней линии на уровне остистого отростка до костного контакта. Вводят анестетик (10-20 мл), затем дексаметазон (суммарная доза 1 мл). После блокады в течение 2 ч соблюдают постельный режим.
Курс лечения состоит из 3-4 инъекций с интервалом 3-7 дней.
У большинства пациентов лечебный эффект наблюдают после первой блокады. Это проявляется уменьшением болевого синдрома уже через 10-15 мин после инъекции. Затем боль может возобновляться и через 5-6 ч снова постепенно исчезать. Зачастую успешный результат блокады можно прогнозировать уже в момент ее выполнения, а также в ближайшие 10-15 мин после. Наиболее эффективное воздействие внутрисуставного введения лекарственных веществ отмечают у тех больных, у которых во время блокады репродукция болевого синдрома включает все его основные компоненты. Второй благоприятный прогностический признак - положительный ближайший результат. У пациентов, наряду со снижением интенсивности или устранением болевого синдрома, отмечают уменьшение напряжения паравертебральных мышц и увеличение амплитуды движений в поясничном отделе позвоночника.
В качестве осложнения или побочного действия подобной блокады ряд авторов отмечают парестезии или слабость в ногах, связанные с попаданием анестетика в перидуральное пространство. Эти нарушения самостоятельно проходят через 1-1,5 ч.
Блокада остистых связок
Показания для проведения такой блокады - острые и хронические повреждения остистых связок.
В положении больного лежа на животе с подложенным под живот валиком проводят пункцию в соответствующем межостистом промежутке. Иглу проводят на глубину примерно 3 см и вводят до 5 мл 0,5% раствора прокаина. В норме в остистую связку можно ввести 0,5-0,7 мл раствора. При частичном ее повреждении количество введенного прокаина такое же, как в норме, при разрыве остистой связки количество анестетика увеличивается. При попадании иглы в участок здоровой ткани ощущают значительное сопротивление. Смещая иглу, определяют участок связки, куда прокаин поступает более свободно. После введения прокаина связка становится безболезненной при пальпации. В соседние межостистые промежутки вводят по 0,5 мл прокаина. Блокады выполняют каждые 2-3 дня в течение 2-2,5 нед.
Кроме блокад с анестетиками при повторных травмах межостистых связок, а также при межостистом лигаментозе (синдроме Баструпа ) вводят вещества, уплотняющие соединительную ткань, усиливающие пролиферацию соединительнотканных элементов (60% натрия амидотризоат или урографин). После анестезии мягких тканей в межостистый промежуток вводят 1-2 мл 0,5% прокаина, затем 1-2 мл склерозирующего раствора. Такие блокады со склерозирующими растворами проводят 1 раз неделю в количестве 1-2.
Блокада пояснично-подвздошной связки
Положение больного - лежа на животе. При блокаде проксимального прикрепления ППС пункцию осуществляют в области поперечных отростков IV и V посяничных позвонков до костного контакта (это обычно происходит на глубине 3-8 см). При патологии дистального прикрепления связки блокаду осуществляют в области крыла подвздошной кости также после костного контакта. В связи с большой протяженностью прикрепления связки к подвздошной кости блокируют участок длиной 3-4 см, а также обе (переднюю и заднюю) ножки этой связки.
Дополнительно проводят блокаду крестцово-подвздошных связок, стабилизирующих дистальные 2/3 КПС. Необходимость этого обусловлена тем, что ППС принимает участие в стабилизации верхней части крестцово-подвздошного сочленения и при ее патологии зона перевозбуждения проприорецепторов распространяется и на эти связки. Общее количество 0,5% раствора прокаина составляет 50-70 мл.
Блокада крестцово-бугорной связки
Медиальное прикрепление крестцово-бугорной связки расположено на боковой поверхности нижней половины крестца. При блокаде КБС иглу направляют плоско под углом 30° и после костного контакта с крестцом вводят анестезирующий раствор.
Дистальное прикрепление связки расположено в области седалищного бугра. Блокада этой области осуществляется двумя способами.
В положении «лягушки» на спине - анестезирующий раствор вводят после костного контакта с пальпаторно определяемым седалищным бугром.
В положении больного лежа на животе. Область блокады дистального прикрепления КБС определяют следующим образом: мысленно или йодом соединяют три точки - заднюю верхнюю ость подвздошной кости, седалищный бугор и большой вертел бедра. Из вершины угла от задней верхней ости проводят биссектрису, которую делят на три части. Иглу длиной 12 см вводят в нижнюю треть упомянутой биссектрисы на глубину 5-6 см до костного контакта - места прикрепления связки к кости. После этого вводят анестезирующий раствор (прокаин 0,5% - 50-60 мл).
Блокада крестцово-остистой связки
В положении больного на животе после пальпации болезненной точки на боковой поверхности нижней части крестца вводят 30-40 мл 0,5% раствора прокаина. При этом иглу постепенно продвигают глубже в связи с тем, что прикрепление КОС находится на передненаружной поверхности крестца.
Блокада крестцово-подвздошных связок
Для осуществления этой блокады определяют заднюю верхнюю ость подвздошной кости. Ниже ее после анестезии кожи иглу направляют под углом 30° на глубину 1,0-1,5 см и по ходу суставной щели КПС вводят 50-60 мл 0,5% раствора прокаина.
Для усиления лечебного действия при блокаде связок таза в раствор прокаина добавляют метамизол натрия, дротаверин, цианокобаламин. При выраженном болевом синдроме допускают однократное применение глюкокортикоидов (гидрокортизон, бетаметазон), что осуществляют после введения анестетика. Эти препараты, обладая выраженным противоотечным и противовоспалительным действием, уменьшают боль, отек, улучшают микроциркуляцию и тем самым способствуют регенерации. Однако, будучи введенными повторно, они, наоборот, тормозят заживление, предрасполагают к повторным повреждениям.
Блокада крестцово-подвздошного сочленения
Вкол иглы осуществляют на 1 см медиальнее нижнего края КПС. Иглу вводят кнаружи и кверху в нижнюю часть сустава. Кончиком иглы манипулируют для входа в сустав. Вход может быть установлен по неровности суставного контура, ощущаемого иглой. Вслед за этим вводят анестетик в количестве 5-10 мл.
Блокада грушевидной мышцы
Показание: синдром грушевидной мышцы.
Положение больного - лежа на животе. Мысленно соединяют заднюю верхнюю ость седалищной кости, седалищный бугор и большой вертел. Из угла в области задней верхней ости проводят биссектрису, делят на три части. Иглу вводят на границе средней и нижней трети ее до костного контакта. Затем иглу извлекают на 1,0-1,5 см и в толщу мышечного брюшка вводят 20-30 мл 0,5% раствора прокаина.
Блокада пояснично-подвздошной мышцы
Эту блокаду применяют для уточнения диагноза илиопсоалгии и лечения этого состояния. Она может быть выполнена тремя способами.
В брюшко m. iliopsoas, расположенное в области малого таза. Точка вкола иглы длиной 15-20 см - 6 см ниже паховой складки на уровне средней и латеральной ее трети, направление иглы под углом 30° к поверхности бедра в направлении к задней верхней ости подвздошной кости через lacuna musculorum в полость малого таза до появления сопротивления мышечной фасции. Правильность введения определяют по мере появления парестезии в проекции иннервации бедренного нерва и устранения мышечного компонента сгибательной контрактуры в тазобедренном суставе.
Паравертебрально (отступя от остистого отростка на 5-6 см) на уровне I-II поясничных позвоноков вводят пункционную иглу длиной 15-20 см до упора в поперечный отросток позвонка и, огибая его по верхнему краю, до ощущения провала на глубину 5 см в направлении кпереди. При технически правильном проведении блокады в момент введения раствора возникает ощущение тепла в конечности, парестезии, ликвидация боли в области тазобедренного сустава.
В область бедренного треугольника, ограниченного паховой связкой, портняжной и длинной приводящей мышцами, кнаружи от сосудистого пучка.
Объем вводимого раствора 50-100 мл (на 100 мл 0,5% раствора прокаина 2 мл дротаверина, 2 мл метамизола натрия, 2 мл цианокобаламина).
Блокада при вертельном бурсите и тендините большого вертела
Определяют точки наибольшей болезненности над областью большого вертела бедренной кости. При тендините эта точка находится тотчас над верхушкой большого вертела. В найденную точку вводят смесь, состоящую из 5-7 мл раствора местного анестетика и 1 мл раствора глюкокортикоида длительного действия. Иногда с интервалом 6-12 мес проводят еще 1-2 повторные инъекции.
После лечебной или диагностической блокады в течение 4-6 ч соблюдают постельный режим.
При строгом учете показаний, обоснованном выборе вида лечебной блокады и лекарственных препаратов, соблюдении правил проведения инъекций и техники избранной лечебной блокады осложнения встречают редко. При выполнении медикаментозных блокад могут отмечаться следующие осложнения (ранние и поздние).
Ранние осложнения (при проведении блокады или непосредственно после нее):
- непереносимость лекарственных препаратов, чаще всего прокаина, выражается коллаптоидным состоянием вследствие снижения тонуса симпатической нервной системы;
- крапивница, как реакция на прокаин или другие препараты, входящие в состав используемого раствора.
Поздние осложнения:
- токсико-аллергические реакции отмечают после 3-4 блокад и связаны с кумуляцией анестетика. В этих случаях наблюдают возбуждение, спутанность сознания, учащение пульса, дыхания, судороги. Для купирования реакции необходимы трансфузионная дезинтоксикационная терапия, введение противосудорожных препаратов;
- локальная инфекция в виде ограниченного абсцесса;
- осложнения, связанные с травмами нервных стволов, проколами сосудов с образованием гематом твердой мозговой оболочки;
- рефлекторные реакции в виде спазма церебральных, спинальных и периферических сосудов, мышц, внутренних органов.
ЛОКАЛЬНАЯ ОЗОНОТЕРАПИЯ
В последнее время наблюдают повышение интереса к различным немедикаментозным методам лечения. Это обусловлено возросшей частотой аллергических реакций на лекарственные препараты, наличием большого числа других противопоказаний к сильнодействующим препаратам, а также высокими ценами на лекарства. Один из таких немедикаментозных методов лечения - озонотерапия.
Озон (О3) - трехатомная аллотропная модификация кислорода, образующаяся из кислорода (О2) при электрическом разряде или при действии ультрафиолетового облучения. Озон - значительно более сильный окислитель, чем кислород. Растворимость озона в воде в 7 раз выше растворимости кислорода. При этом он распадается на свободные радикалы, пероксиды, супероксиды, озониды, гидроксильные группы. Они взаимодействуют с мембраной клеток крови, сосудов, мышц. В клетках происходит активизация кислородзависимых реакций, цикла Кребса и оксилительного фосфорилирования в митохондриях с накоплением АТФ и креатинфосфата.
В результате многочисленных экспериментальных исследований выявлен широкий диапазон биологического действия озона. Он обладает иммуномодулирующим, бактерицидным, антисептическим, фунгицидным, противовоспалительным, болеутоляющим действием, ускоряет обмен веществ.
Согласно данным ряда исследовательских организаций озонотерапию с разной степенью успеха применяют более чем при 50 различных заболеваниях. В некоторых случаях ее используют как единственный метод лечения, в других - в дополнение к традиционным медицинским процедурам, хирургическому лечению или химиотерапии. В мировой лечебной практике в настоящее время озон применяют несколькими способами с использованием различных методик: локальной местной терапии, ректального введения газообразного озона, большой и малой аутогемотерапии с озонированной кровью, внутриартериальным, внутривенным, внутрисуставным и параартикулярным введением озоно-кислородной смеси.
Существуют немногочисленные сообщения о применении озона при лечении поясничного болевого синдрома.
Ряд авторов провели лечение 66 больных с применением внутримышечных инъекций озоно-кислородной смеси и 30 больных, которым вводили только кислород. Интересно, что отличные и хорошие результаты наблюдались у 86% больных из обеих групп, но в первой группе было отмечено статистически значимое улучшение некоторых клинических параметров. Это позволяет предположить, что игла и кислород вместе уже обладают терапевтическим действием, которое усиливается озоном.
Другие исследователи вводили озоно-кислородную смесь в область межпозвонкового отверстия 200 пациентам с радикулопатией, обусловленной протрузией диска. При КТ-исследовании через 3 мес после озонотерапии у 55,5% пациентов с «мягкими» грыжами отмечена регрессия дискового выпячивания. В группе пациентов с «твердыми» грыжами, т.е. частично или полностью кальцифицированными дисковыми выпячиваниями, несмотря на значительное клиническое улучшение, размеры их при КТ остались прежними. И хотя некоторые «озонотерапевты» верят в то, что озон достигает участка грыжевого выпячивания и подвергает его лизису, эта идея маловероятна, поскольку озон имеет очень короткий период полураспада и немедленно растворяется в интерстициальной жидкости, распадаясь на свободные радикалы. По мнению отдельных авторов, озон обладает обезболивающим и противовоспалительным эффектом с последующим сокращением дискового отека. Однако более сложным остается вопрос лечения дисковой грыжи. Авторы считают, что озонотерапия определяющим образом воздействует на замыкательные пластинки тел позвонков, через центральные отделы которых осуществляется питание межпозвонкового диска, который у взрослых неваскуляризирован. Проницаемость замыкательных пластинок уменьшается с годами, и, начиная с 18-20 лет, происходит постепенное отложение кальциевых солей при прогрессирующей дистрофии хрящевых поверхностей позвонков и замещение их костной тканью. Дегенеративно-дистрофические изменения развиваются и в позвоночном сосудистом сплетении - уплотняются стенки сосудов, снижается их проницаемость, что ведет к недостаточному кровоснабжению и питанию тел позвонков и, следовательно, замыкательных пластинок и диска. Пульпозное ядро диска теряет свою эластичность и устойчивость к механическим нагрузкам. Иначе говоря, проводя озонотерапию, мы тем самым улучшаем микроциркуляцию на уровне спинальных корешков. Это замедляет дегенерацию сосудистого сплетения позвоночника и обеспечивает необходимый уровень метаболических процессов в дисках.
В подавляющем большинстве отечественных работ по клиническому применению озона при ПКБС сообщается об успешном применении процедур малой аутогемотерапии с озонированной кровью (концентрация озона 5 мг/л) в сочетании с паравертебральными введениями озоно-кислородной смеси в такой же концентрации. Есть сообщения о высокой эффективности введения озоно-кислородной смеси в триггерные точки паравертебральных мышц.
Согласно данным литературы при регионарной озонотерапии происходит следующее:
- уменьшение раздражения окончаний синувертебрального нерва за счет ослаб ления действия дисциркуляторного фактора и уменьшения отека окружающих тканей;
- уменьшение дислокационного фактора в связи с частичным восстановлением амортизационных свойств поврежденного диска в результате улучшения обменных процессов;
- уменьшение асептического воспаления вследствие блокирования синтеза ПГ как медиаторов воспаления и активации клеточного иммунитета;
- уменьшение болевых ощущений - антиноцицептивное действие процедур обусловлено непосредственным окислением алгопептидов, ускорением элиминации недоокисленных веществ, накапливаемых в спазмированных мышцах и вызывающих возбуждение болевых рецепторов, повышением порога возбудимости мембран болевых рецепторов (мембраностабилизирующий эффект);
- улучшение функционирования сегментарного аппарата спинного мозга, проявляемое в ускорении формирования нового двигательного стереотипа, активации спинальных механизмов контроля боли, нормализации вегетативнотрофического обеспечения двигательного акта.
Противопоказания к озонотерапии (по данным литературы):
- алкогольное опьянение;
- кровотечение из любого органа;
- беременность;
- гипертиреоз;
- тромбоцитопения;
- судорожный синдром в анамнезе;
- непереносимость озона.
Методика локальной озонотерапии. Процедуру выполняют в положении больного на животе. После обработки кожи в область напряженного участка m. erector spinae обычной иглой для внутримышечных инъекций медленно вводят 20 мл озоно-кислородной смеси с концентрацией озона 5 мг/л. Оптимальная концентрация озона в смеси с кислородом для внутримышечного введения установлена экспериментальным путем. Большая концентрация озона ведет к некрозу мышечных волокон. При двустороннем болевом синдроме 20 мл озоно-кислородной смеси вводят и с другой стороны. Инъекция озоно-кислородной смеси вызывает незначительную боль, которая проходит через несколько минут, остается лишь чувство распирания в поясничной области, которое тоже самостоятельно проходит через 15-20 мин. На область инъекции накладывают стерильную повязку.
После блокады рекомендуют в течение часа умеренную двигательную активность, например ходьбу. В зависимости от выраженности болевого синдрома инъекции газовой смеси проводят каждый день или через день в количестве 5-10.
При проведении процедур озонотерапии можно наблюдать следующие побочные явления: мидриаз, интенсивное потоотделение, преходящее снижение АД, брадикардию, давящую боль за грудиной, диспноэ, аллергические реакции, остановку сердца (вазовагальная реакция). По данным ряда авторов, по отношению к общему числу процедур уровень осложнений составляет 0,006%. По сравнению с другими видами лечения - ничтожная величина. Чаще всего побочные эффекты озонотерапии проявляются при внутривенных процедурах, особенно при внутривенном введении озоно-кислородной смеси, от которого сейчас практически отказались. Причины осложнений включают неправильную технику введения и неверно выбранную дозировку. Наиболее опасны в отношении токсического влияния на блуждающий нерв и возникновения вазовагальной реакции с падением АД и угнетением дыхательного центра перекисные радикалы. Несмотря на низкую частоту осложнений, врач, занимающийся озонотерапией, должен быть готов к таким экстренным ситуациям, которые крайне редко, но все-таки могут возникать.
Озонотерапию сочетают с приемом любых фармпрепаратов, кроме антикоагулянтов, и с проведением любых физиопроцедур. При этом часто оказывается, что можно снизить дозировку лекарств, например обезболивающих, седативных, антибактериальных, гипотензивных препаратов, так как озон усиливает их действие. Эффект комплексного применения озонотерапии с другими видами лечения больше, чем арифметическая сумма эффектов каждого их этих видов. Озонотерапия - дешевый и безопасный способ лечения.
На основании изложенного заключим, что для восстановления спортивной и профессиональной работоспособности при лечении пояснично-крестцового болевого синдрома существенное значение имеет дифференцированный подход, исходя из клинического варианта ПКБС, рациональное сочетание методов консервативной терапии (медикаментозные препараты, физиопроцедуры, лечебная гимнастика и т.д.) с хирургическими методами (лечебные обезболивающие блокады, инъекции озоно-кислородной смеси) в зависимости от фазы, стадии заболевания и степени функциональных нарушений.
МАЛОИНВАЗИВНЫЕ ХИРУРГИЧЕСКИЕ ВМЕШАТЕЛЬСТВА ПРИ ПОЯСНИЧНОКРЕСТЦОВОМ БОЛЕВОМ СИНДРОМЕ У СПОРТСМЕНОВ
Разработка и совершенствование комплексной программы реабилитации спортсменов с патологией позвоночника с использованием современных методик - одно из приоритетных направлений современной спортивной травматологии. Один из ее элементов - малотравматичная хирургия. К подобным хирургическим вмешательствам относят чрескожную лазерную декомпрессию межпозвонковых дисков и чрескожную радиочастотную деструкцию фасеточных нервов. Экстракорпоральная ударно-волновая терапия занимает промежуточное положение между хирургическим и консервативным методами лечения.
Чрескожная лазерная декомпрессия диска
ЧЛДД имеет четкие показания, которые можно установить только после тщательного обследования пациента. Лазерная вапоризация поясничных дисков показана при боли в спине с иррадиацией в нижние конечности, обусловленной протрузией диска до 8 мм включительно, по данным КТ или МРТ, не купируемой в течение 6 нед консервативной терапией, а также при соответствии клинической картины данным КТ и МРТ и при отсутствии грубой неврологической симптоматики (парезов мышц, нарушений функции тазовых органов).
По данным литературы, выполнение ЧЛДД показано после безуспешного в течение 3-8 мес консервативного лечения. Однако длительная неэффективная физиотерапия способствует развитию гипертрофии и оссификации желтой связки, варикозным изменениям эпидуральных вен, образованию рубцово-спаечных сращений между задней продольной связкой и твердой мозговой оболочкой, приводящих к деформации дурального мешка, изменению расположения сосудов и нервов не только в данном позвоночном сегменте, но и в соседних. Причем наиболее рубцовообразующим действием обладают локальные электропроцедуры. С учетом специфики нашего контингента больных - спортсменов - мы сократили сроки проведения консервативного лечения в случае его недостаточной успешности до 6 нед с последующим выполнением ЧЛДД.
Для успешного проведения оперативного вмешательства и получения положительного результата необходимо учитывать следующие противопоказания (по данным литературы):
- экструзия, секвестр диска, по данным КТ, МРТ;
- стеноз позвоночного канала (врожденный или приобретенный вследствие деформации костных структур);
- нестабильность позвоночного сегмента;
- выраженный спондилез;
- выраженный спондилоартроз с деформацией межпозвонковых отверстий;
- спондилолистез более I степени;
- предыдущее оперативное лечение или нуклеолиз на уровне рассматриваемого диска;
- вакуум-феномен межпозвонкового диска;
- геморрагический диатез;
- местная и общая инфекция;
- общесоматические противопоказания (активный ревматический процесс, психические расстройства, беременность и т.д.).
Относительные противопоказания к проведению ЧЛДД включают многократные сеансы мануальной терапии, усугубившие болевой синдром, травмы позвоночника на этом же уровне в анамнезе.
На обязательно выполняемых обзорных рентгенограммах можно исключить другую патологию позвоночника, которая также сопровождает ПКБС, обнаружить поражение позвоночника на нескольких уровнях, вакуум-феномен, детализировать такие важные моменты, как наличие спондилолиза, уровень стояния крыльев подвздошных костей, а также проявлений дисплазии (наличие переходного позвонка, незаращение дуг, нарушение тропизма межпозвонковых суставов и т.д.).
При подозрении на нестабильность поясничного отдела проводят функциональные рентгенограммы в положении максимального сгибания и разгибания позвоночника
МРТ выявляет выпячивание диска, позволяет уточнить размеры этого выпячивания. По данным литературы, точность МРТ при диагностике грыж дисков достигает 97% с совпадением дооперационного диагноза с интраоперационными данными в 100% на уровне диска IV-V поясничных позвонков. Но даже высококачественная МРТ не может помочь отдифференцировать экструзию диска от его протрузии у 10% пациентов, что очень важно при проведении ЧЛДД. Именно невозможностью отличить экструзию от протрузии диска даже при выполнении МРТ объясняют вероятность отсутствия улучшения после лазерной вапоризации диска.
Более перспективна в этом плане разработанная в последнее время МРТ с контрастным усилением (непосредственно перед сканированием внутривенно вводят парамагнетики - гадопентетовую кислоту, гадолиниум? в дозе 0,1 ммоль/кг).
Этот метод исследования позволяет отдифференцировать экструзию диска от протрузии и, кроме того, выявить секвестры диска. Как показали морфологические исследования, аваскулярный дисковый секвестр покрыт грануляционной тканью с большим количеством сосудов. При МРТ с контрастированием отделившийся фрагмент диска четко определим на фоне хорошо контрастированной грануляционной ткани.
КТ выявляет грыжевое выпячивание, но даже самый лучший прибор не может отдифференцировать пульпозное ядро от фиброзного кольца, поэтому нельзя четко отличить сублигаментарную грыжу от транслигаментарной, даже при контрастном усилении. КТ более полезна при выявлении степени спондилоартроза, стеноза на уровне дискорадикулярного конфликта.
Реконструкция тел позвонков в коронарной проекции помогает обнаружить шиповидные костные разрастания в сторону спинномозгового канала, а также уточнить степень снижения высоты диска.
В нашей стране продолжают широко использовать при обследовании пациентов с дискорадикулярным конфликтом контрастные методы исследования: миелографию и дискографию.
Миелография позволяет обнаружить грыжевое выпячивание дисков и нарушение ликвородинамики. Однако результаты этого исследования также не помогают ответить на вопрос (важный в плане возможного проведения лазерной вапоризации диска) - наблюдается протрузия или экструзия диска, даже при последующей КТ. Кроме того, она значительно уступает МРТ по визуализации содержимого спинномозгового канала. И вдобавок, эта процедура инвазивная, после нее можно наблюдать ряд осложнений: тошноту, рвоту, головную боль, инфекции, арахноидит. Необходимость в проведении миелографии может возникнуть в случаях, когда требуется определить степень компрессии «корешковой манжетки», а при многоуровневом поражении - выявить «диск-виновник».
Другой рентгеноконтрастный метод - дискография. Она дает исчерпывающую информацию о характере дискового выпячивания, наличии секвестров. Кроме того, дискография - единственный метод исследования, при котором анатомическая информация сочетается с провокационной болью при введении контраста в поврежденный диск. Однако если ранее считалось, что дискография более чувствительна, чем КТ или МРТ, в диагностике ранних стадий дегенерации дисков в случаях дискогенных болей без радикулопатии, то в настоящее время доказано, что дегенерация диска не является предиктором воспроизведения боли. Анализ показал, что воспроизведение характерной боли во время дискографии зачастую связано с затеканием контрастного вещества в наружную часть фиброзного кольца. В настоящее время данный метод почти полностью заменен МРТ. Основная причина этого - дискография - инвазивный метод, который может усилить дегенерацию пульпозного ядра и ослабить прочность фиброзного кольца. После дискографии необходим временной интервал перед проведением ЧЛДД, иначе лазерное излучение будет выпаривать контрастное вещество, а не пульпозное ядро. Поэтому следует согласиться с мнением ряда авторов, что пациентам, подвергающимся малоинвазивным вмешательствам, необходимо проводить как можно меньше инвазивных диагностических процедур.
Таким образом, алгоритм лучевых методов исследования пациентов - кандидатов для ЧЛДД состоит в следующем:
- исследование костной структуры - спондилография, КТ, МРТ;
- исследование функционального состояния позвоночного сегмента - функциональная спондилография;
- исследование состояния межпозвонкового диска - МРТ, КТ, МРТ с контрастным усилением.
Операцию осуществляют под местной анестезией (10-15 мл 1% раствора лидокаина, 20 мл 0,25% раствора бупивакаина) в положении пациента на здоровом боку. Пункцию диска осуществляют со стороны протрузии, в связи с тем что именно эта зона диска, как было установлено в эксперименте, наиболее изменчива и способна уменьшаться при падении внутридискового давления в результате лазерной вапоризации.
Конечности пациента максимально подтягивают к груди, под поясничный отдел помещают мягкий цилиндрический валик. После обработки операционного поля осуществляют маркировку крыльев подвздошных костей, гребня крестца и срединной линии, отмечают точку введения иглы. Стерильной спицей под рентгеновским контролем намечают пораженный диск.
В случае протрузии диска IV-V поясничных позвонков пункцию проводят классическим боковым доступом Де Сезе-Лаверне. Место введения иглы, как правило, соответствует точке Маккалоха, находящейся на пересечении линии, параллельной оси позвоночника, и отстоящей от остистых отростков на 8-10 см, с линией, соединяющей гребни подвздошных костей. Угол введения иглы - 45-50° к сагиттальной плоскости.
При наличии выраженной дисплазии пояснично-крестцового отдела позвоночника уровень диска IV-V поясничных позвонков находится значительно ниже крыла подвздошной кости. В таких случаях боковой доступ не подходит. Пункцию диска осуществляют экстрадурально аналогично пункции диска V поясничного и I крестцового позвонков.
Пункцию диска V поясничного и I крестцового позвонков осуществляют несколькими способами. Наиболее часто используют экстрадуральный доступ. Точка введения иглы находится на расстоянии 1,5-2,0 см от средней линии и ниже дуги, образованной нижними ножками V поясничного позвонка. Иглу вводят под углом 5° к сагиттальной плоскости. При этом необходимо помнить, что нервный корешок чаще всего распластан на дисковом выпячивании. В связи с этим во избежание повреждения корешка пункцию выполняют очень осторожно, иглу проводят медленно.
Иногда можно использовать трансдуральный доступ Чу - на уровне нижнего края остистого отростка по средней линии. При прохождении дурального мешка пациенты ощущают кратковременную радикулярную боль. После операции, проведенной из этого доступа, вследствие повреждения дурального мешка возможно появление сильной головной или радикулярной боли. В этом случае необходимо более длительное соблюдение постельного режима.
Для пункции диска используют специальную иглу диаметром 1,2 мм с троакаром и газоотводным отверстием. Введение иглы в диск контролируют с помощью рентгеновского аппарата с электронно-оптическим преобразователем в двух проекциях. Сначала проведение иглы отслеживают в боковой проекции. После вхождения кончика иглы в фиброзное кольцо, что определяют по эластичному сопротивлению, осуществляют рентгеновский контроль в прямой проекции. При нахождении кончика иглы в пределах фиброзного кольца дальнейшее проведение иглы осуществляют под рентгеновским контролем в боковой проекции. После прохождения фиброзного кольца возникает ощущение провала вследствие снижения сопротивляемости тканей. Иглу вводят на глубину 2/3 диска по его продольной оси параллельно замыкательным пластинкам тел позвонков. Последнее условие необходимо обязательно соблюдать, чтобы исключить термическое поражение замыкательных пластинок и развитие в последующем спондилита.
Корреляция между прямой и боковыми проекциями гарантирует правильное положение иглы. Иногда необходимо бывает выполнение третьей проекции, при которой рентгеновский луч перпендикулярен игле.
С больным постоянно поддерживают вербальный контакт для уточнения возникающих у него ощущений в процессе операции. Появление радикулярной боли при введении иглы свидетельствует о близком расположении ее к нервному корешку. В этом случае иглу подтягивают на 1,5-2,0 см и вводят немного в другом направлении. Чтобы исключить возможность повреждения иглой нервного корешка, все эти манипуляции осуществляют только под рентгеновским контролем.
После пункции диска обтуратор иглы меняют на световод, который во избежание нежелательного смещения жестко фиксируют в игле специальной насадкой. Длина выступающего из иглы кончика световода составляет 2 мм. Затем световод подключают к лазерной установке, на дисплее которой предварительно устанавливают следующие рабочие параметры: мощность импульса 15 Вт, время импульса 1 с.
Между импульсами соблюдают паузы длительностью примерно 5-10 с. При появлении у пациента чувства жжения и боли в пояснице, что чаще всего обусловлено избыточной аккумуляцией тепла, длительность паузы увеличивают.
Через каждые 300 Дж осуществляют контроль световода. При этом его извлекают из иглы, оценивают внешний вид кончика, степень его обугленности, проверяют характер свечения. На плоской белой поверхности он должен давать круглое равномерное пятно. В конце операции, как правило, вид светового пятна меняется: оно становится неправильной формы с рваными краями, неравномерной окраски. В таких случаях его проводимость отличается от исходной. При выраженных изменениях кончика световода и проводимости до окончания операции его необходимо заменить на новый. Одновременно с контролем световода у пациента проверяют симптом ПВН. Почти во всех случаях в среднем после 12-18 импульсов симптом ПВН становится менее выраженным, и пациент ощущает явное облегчение.
В ходе операции через каждые 500-600 Дж положение иглы меняют за счет поэтапного смещения ее к позвоночному каналу для денатурации ядерной пульпы большего объема.
На диск оказывают энергетическое воздействие в пределах от 1200 до 2100 Дж в зависимости от высоты межпозвонкового промежутка, реакции больного на течение операции и интенсивности, характера выделяемого из иглы газа. В начале операции, когда диск еще достаточно гидратирован, из газоотводного отверстия иглы выделяется пар, возможно, с капельками прозрачной жидкости. Появление темного дыма с запахом горящего белка свидетельствует об окончании выпаривания жидкой части пульпозного ядра и начале термического воздействия на фиброзное кольцо, что служит сигналом для окончания операции.
Величина требуемой для вапоризации энергии, как уже указывалось, зависит от объема диска, который, в свою очередь, зависит не от массы тела, а от роста пациента. Например, для пациентов ростом 160 см и ниже достаточно будет 1000 Дж, при росте выше 180 см - 2000 Дж.
В конце операции сначала извлекают оптическое волокно, еще раз проверяют кончик электрода. Затем удаляют иглу. Длительность операции составляет 20-40 мин (29?2,15 мин). На область пункции накладывают асептическую повязку.
У большинства пациентов (70%) боль в нижней конечности и выраженность симптомов ПВН и Ласега заметно уменьшается к концу операции. Через 7-10 дней отмечают частичный регресс неврологической симптоматики - значительное ослабление симптомов натяжения нервных стволов, уменьшение зоны нарушения кожной чувствительности. Большинство пациентов легко встают к концу операционного дня, не испытывая при этом усиления боли в нижних конечностях. Более постоянна жалоба на ощущение тяжести в поясничном отделе позвоночника.
Вставать в ортопедическом поясе разрешают через 4-6 ч после операции, а садиться - через 2-3 нед.
В программе реабилитации условно выделяют три периода.
- Первый период (1-я неделя после операции) - ограничение осевой нагрузки и устранение болевого синдрома с помощью НПВП, анальгетиков, лечебная гимнастика в положении лежа для укрепления мышц нижних конечностей, массаж мышц нижних конечностей.
- Второй период (2-3-я неделя после операции) - укрепление мышцстабилизаторов - упражнения на укрепление мышц спины и брюшной стенки в положении разгрузки, укрепляющий массаж.
- Третий период - восстановление выносливости к статическим и динамическим нагрузкам, координации движений, в том числе и специфичных для спорта и балета двигательных навыков, более активные упражнения на укрепление мышц спины и брюшной стенки, укрепляющий массаж, дозированное восстановление подвижности позвоночника, плавание в бассейне. На заключительном этапе спортсмены постепенно приступают к специальным тренировкам, первое время ограничивая осевую нагрузку на позвоночник (упражнения со штангой стоя, прыжки, единоборства с партнерами и т.д.).
Стационарный период после операции составляет от 1 до 3 сут. Восстановительное лечение пациенты заканчивают в амбулаторных условиях. К работе разрешают приступать через 2 нед, к тренировкам - через 4 нед. Фиксацию поясничного отдела ортопедическим поясом осуществляют не более месяца со дня операции.
Если больной оперировался на фоне обострения дискорадикулярного конфликта, болевые ощущения купируются медленнее. В таких случаях дополнительно назначают пентоксифиллин, спазмолитики. Вставать и ходить в ортопедическом поясе также разрешают через 4-6 ч, однако в зависимости от интенсивности болевого синдрома восстановительное лечение начинают позднее. При сохранении не менее 50% болевого синдрома к лечению добавляют инъекции озоно-кислородной смеси в поясничные паравертебральные мышцы.
Клинико-неврологический контроль осуществляют на следующий день, через 1 нед, 1, 3, 6, 12 мес.
Согласно данным литературы ЧЛДД - хирургическое вмешательство с небольшим риском осложнений. Тем не менее эту операцию нельзя считать абсолютно безопасной. Встречаемые осложнения можно разделить на две группы: аналогичные тем, которые наблюдают при выполнении дискографии, и специфичные только для ЧЛДД.
К первой группе относят прежде всего дисциты асептические и инфекционные, клинически выражающиеся высокой температурой после операции, сохранением или появлением боли в области оперированного диска, увеличением СОЭ, повышением числа лейкоцитов крови, сдвигом лейкоцитарной формулы. Со временем появляются эрозии замыкательных пластинок при рентгенологическом обследовании или МРТ, положительные данные радионуклидного исследовании. Частота инфекционных дисцитов после ЧЛДД составляет около 0,1%, после открытых оперативных вмешательств колеблется от 0,2 до 8,5%. Профилактика этого осложнения состоит в тщательном предоперационном обследовании больного, выявлении очагов хронической инфекции, профилактическом введении перед операцией антибиотиков широкого спектра действия.
Зарегистрировано несколько случаев клинически незначимых гематом в m. psoas в результате повторных попыток пункции диска боковым доступом (для сравнения: при эндоскопических вмешательствах подобные гематомы встречают в 1,7% случаев).
Вследствие прокола дурального мешка при трансдуральном доступе всегда и при эктрадуральном иногда возникает головная боль. Причинами головной боли в постпункционном периоде могут быть понижение ликворного давления и раздражение мозговых оболочек. В большинстве случаев их купируют цитрамоном , реже необходимы внутривенные капельные введения магния сульфата.
Ко второй группе осложнений относят прежде всего повреждение замыкательных пластинок и подлежащей кости в результате теплового воздействия лазерного луча. При этом на МРТ определяют характерную картину полукруглого дефекта замыкательной пластинки тела позвонка уже через месяц после операции. Клинически имеются симптомы спондилита, хотя в ряде случаев патологическая симптоматика отсутствует. Это осложнение чаще наблюдают при проведении ЧЛДД лазером системы КТР (калий-титан-фосфат), в котором используют световоды с односторонней заточкой кончика световода. При использовании других лазерных систем также можно наблюдать это осложнение. Во избежание его необходимо отбирать пациентов для ЧЛДД с достаточно высоким междисковым промежутком и вводить иглу параллельно замыкательным пластинкам.
При использовании лазеров, генерирующих значительное тепло (например, гольмиевого), ранее была необходима система охлаждения, поэтому внешний диаметр канюли составляет 2,7 мм. Кроме того, при этом виде лазера применяют многоэтапную систему введения световода (спица-направитель, трефан и т.д.). При неправильном положении или смещении оболочек была возможна термическая травма мягких тканей или околопозвоночных мышц, о чем были сообщения в литературе. Для профилактики подобных осложнений необходим постоянный рентгенологический контроль на каждом этапе операции.
Внутрибрюшные повреждения - перфорации кишечника описаны в трех случаях. При этом обычно на вторые сутки после ЧЛДД возникают признаки острой патологии брюшной полости. Для исключения этого осложнения необходимы точная разметка точки введения иглы, постоянный рентгенологический контроль, осторожное медленное проведение иглы.
В редких случаях в литературе упоминают о возникновении после ЧЛДД (на фоне клинико-неврологического улучшения) гиперпатических болей в области коленного сустава, голени и стопы без четкой радикулярной симптоматики. Причины возникновения гиперпатии не ясны. Можно предположить, что гиперпатия - следствие реиннервации у пациентов с длительным анамнезом радикулопатии. По данным литературы, длительность этого осложнения от 6 до 12 нед, хорошо поддается консервативному лечению с использованием обезболивающих, сосудистых препаратов, витаминов.
Падение АД вследствие вазовагальной реакции - очень редкое, но серьезное осложнение лазерной вапоризации дисков. Описано два случая этого осложнения при выполнении ЧЛДД на поясничном уровне. У одного пациента падение АД отмечено после воздействия 300 Дж лазерной энергии, у другого - сразу после начала операции.
Тромбоэмболия легочной артерии после ЧЛДД описана у трех человек, имевших в анамнезе заболевания вен нижних конечностей. Сроки возникновения этого осложнения через 1, 2 и 6 нед после операции. Частота тромбоэмболических осложнений после открытых вмешательств на поясничных дисках достигает 26,5%. В плане профилактики необходимо учитывать сопутствующие заболевания сосудов нижних конечностей, осуществлять эластичное тугое бинтование конечностей во время и после операции, мобилизировать пациентов уже в первые сутки после ЧЛДД.
Чрескожная радиочастотная деструкция фасеточных нервов
ЧРДФН имеет несколько названий, имеющих одинаковое значение:
- радиочастотная деструкция фасеточных нервов;
- радиочастотная дерецепция фасеточных суставов;
- радиочастотная денервация фасеточных суставов.
Сущность этой операции состоит в том, что происходит денервация межпозвонкового сустава в результате разрушения медиальной веточки задней ветви спинального нерва, иннервирующей межпозвонковый сустав. Повреждающий эффект оказывает тепловая энергия, образуемая в тканях при прохождении через них токов ультравысокой частоты. Показанием выступает отсутствие стойкого эффекта от проводимой в течение 3 мес консервативной терапии поясничной боли, обусловленной фасеточным синдромом.
Пациентов для этой операции отбирают по следующим критериям:
- поясничная боль более 3 мес;
- усиление боли при разгибании поясничного отдела позвоночника, длительном нахождении в положении стоя или сидя;
- боль при глубокой пальпации в области межпозвонкового сустава;
- отсутствие неврологических нарушений;
- отсутствие улучшения после консервативной терапии;
- положительный эффект диагностической блокады.
Всем больным наряду с клинико-неврологическим обследованием проводят рентгенологическое обследование, включающее поясничную спондилографию в двух проекциях с функциональными пробами. Для уточнения состояния суставных отростков проводят рентгенограммы в косых проекциях или КТ.
Решающее значение при определении необходимости проведения радиочастотной денервации поясничных фасеток имеет положительный, но недостаточный обезболивающий эффект одной-двух параартикулярных диагностических блокад. При полном отсутствии эффекта после обезболивающих блокад диагноз «синдром поясничных фасеток» сомнителен, радиочастотная деструкция тогда не проводится.
Противопоказания для радиочастотной деструкции (по данным литературы):
- радикулярная боль (признак корешковой компрессии);
- перенесенные ранее операции на позвоночнике на этом же уровне;
- возраст моложе 18 и старше 72 лет;
- нарушение восприятия боли в силу социальных или психологических факторов;
- зависимость от наркотических и седативных препаратов, алкоголя;
- геморрагический синдром;
- общая или местная инфекция;
- общие заболевания (гипертоническая болезнь, сахарный диабет, коллагенозы и т.д.);
- беременность;
- нарушение мозгового или спинального кровообращения в анамнезе.
Наличие признаков корешковой компрессии в большинстве случаев свидетельствует или об экструзии диска, или о выраженных дегенеративных изменениях межпозвонковых суставов со значительной гипертрофией суставных концов и их деформацией. При наличии симптомов корешковой дисфункции необходима декомпрессия нервных корешков путем дискэктомии или резекции суставов.
Перенесенные ранее операции на позвоночнике приводят к значительным изменениям топографии фасеточных нервов, развитию рубцов и спаек. В таких случаях предпочтительно консервативное лечение.
Положение пациента - лежа на животе. Премедикация седативными препаратами необходима только эмоционально лабильным больным.
Для дерецепции фасеточных суставов используют различные радиочастотные генераторы. Контроль осуществляют автоматически, и при превышении температуры в области кончика электрода показания прибора дублируются звуковым сигналом. Благодаря соблюдению постоянства выбранных параметров (температура нагрева активного кончика электрода, сила и напряжение тока, время манипуляции, сопротивление биологических тканей в области кончика электрода) получают контролируемый объем деструкции. В эксперименте был определен объем деструкции при температуре 80 ?С и радиочастотном воздействии в течение 60 с: диаметр зоны коагуляции составил 3 мм.
В зависимости от комплекции больного для операции на поясничных фасетках применяют иглы SMK 100 или 150 с рабочим неизолированным кончиком длиной 2 мм.
Уровень деструкции определяют по соответствующей клинической картине и результатам диагностической блокады. Однако к интерпретации результатов блокады следует подходить с осторожностью, поскольку возможно затекание анестетика в соседние сегменты. Кроме того, во время блокады тормозится проведение всех волокон афферентных нервов, в то время как при радиочастотном воздействии можно избирательно блокировать достаточно мелкие волокна.
Сначала проводят анестезию кожи 0,25% раствором бупивакаина в местах введения игл. В зависимости от клинической картины, учитывая при этом, что каждая задняя ветвь иннервирует, по крайней мере, два фасеточных сустава и каждый фасеточный сустав получает иннервацию как минимум от двух спинальных уровней, деструкции подвергают нервы, идущие к межпозвонковым суставам на нескольких уровнях с одной или обеих сторон (обычно не больше 6-8 суставов).
Под рентгеноскопическим контролем иглу проводят до соприкосновения с верхним краем поперечного отростка. Ориентир - изображение корня дужки позвонка на экране монитора. Кончик иглы не должен смещаться за пределы поперечного отростка, что исключает возможность случайного повреждения корешка или ганглия. Затем угол введения иглы несколько меняют, кончик ее соскальзывает с поперечного отростка, и продвигают на 1-2 мм в подсуставную ямку, где проходит фасеточный нерв. Этот последний этап пункции иногда вызывает у пациентов кратковременные болезненные ощущения, но в большинстве случаев введение иглы безболезненно.
Введение иглы обязательно контролируют рентгенологически в двух, а для лучшей визуализации края поперечного отростка - и в косых проекциях (5-15° краниально).
При денервации сустава V поясничного и I крестцового позвонков иглу проводят до задней поверхности крыла крестца и смещают чуть выше в подсуставную ямку. Другую иглу подводят к верхнелатеральному краю первого заднего крестцового отверстия до соприкосновения с надкостницей (там проходит ветвь нерва к суставу V поясничного и I крестцового позвонков). Для облегчения этой манипуляции на уровне I крестцового позвонка его нужно отклонить краниально, чтобы лучше визуализировать заднее отверстие I крестцового позвонка. Дополнительным ориентиром может служить задняя верхняя ость подвздошной кости. Если от нее провести линию медиально под углом 45° к горизонтали, то на расстоянии 2 см от среднего гребня крестца она окажется над задним отверстием I крестцового позвонка.
Убедившись, что игла занимает оптимальное положение, мандрен заменяют на электрод и осуществляют контроль положения иглы с помощью электростимуляции.
Сначала проводят сенсорную стимуляцию нерва с частотой 50 Гц путем увеличения напряжения тока от 0 до 1 В. При этом у пациентов появляются или усиливаются обычные болезненные ощущения в поясничном отделе позвоночника, ягодичной области, бедре, области седалищного бугра, вдоль седалищного нерва, иногда дистальнее коленного сустава. Локализацию считают правильной, если чувствительный ответ наблюдают при напряжении менее 1 В.
Затем проводят моторную стимуляцию с частотой 2 Гц также путем увеличения напряжения тока. При отсутствии в зоне кончика электрода двигательных нервных веточек увеличение напряжения тока до 3 В не вызывает фасцикулярных сокращений паравертебральных мышц или мышц нижних конечностей (при этом болевая реакция может присутствовать), что также подтверждает корректное положение иглы.
Во время операции с пациентом поддерживают постоянный вербальный контакт, уточняют локализацию болевых ощущений и наличие мышечных сокращений. Если кончик электрода расположен близко к первичной спинальной ветви, пациент ощущает сильную радикулярную боль в соответствующем дерматоме. Это означает, что электрод расположен слишком глубоко и его необходимо после рентгенологического контроля извлечь и перепровести. При отсутствии болевой реакции во время чувствительной электростимуляции денервацию не проводят.
При правильном расположении иглы в нее вводят 1 мл 0,25% раствора бупивакаина, а на панели генератора устанавливают режим деструкции - температура 80 ?С, экспозиция - 60-90 с. После чего производят непосредственное радиочастотное воздействие. Как правило, деструкция проходит безболезненно.
Во время проведения процедуры проводят и постоянный контроль сопротивления тканей, расположенных вокруг активного кончика иглы. При правильном положении иглы в области нервных веточек сопротивление (импеданс) находится в пределах 300-700 Ом.
Подобным образом осуществляют стимуляцию и деструкцию фасеточных нервов на всех необходимых уровнях. Затем все иглы извлекают и накладывают стерильную повязку.
Ряд авторов указывают на отсутствие прогрессирования дегенеративных изменений межпозвонковых суставов после проведенной радиочастотной деструкции фасеточных нервов. Кроме того, несмотря на частичную денервацию многораздельной мышцы при этой операции, нет ни одного сообщения в литературе о нарушении ее функции.
Послеоперационное ведение
Если непосредственно после деструкции больной предъявляет жалобы на чувство легкой слабости в ногах вследствие инфильтрации зоны нервного корешка анестетиком, то показан постельный режим в течение 1-2 ч. В большинстве случаев пациенту разрешают вставать и ходить через 30 мин после операции. Выписывают больных вечером этого же дня или на следующий день. В первые дни возможны ощущение тяжести в поясничных мышцах, умеренная боль в области проколов кожи.
Пациентам рекомендуют в течение 7 дней принимать НПВП, носить поясничнокрестцовый ортопедический пояс. Прекращать иммобилизацию следует постепенно, сокращая продолжительность пользования корсетом на протяжении 1-2 нед.
В программе реабилитации выделяют три периода.
- Первый период (1-я неделя после операции). Больным рекомендуют умеренную ходьбу, лечебную гимнастику в положении лежа для укрепления мышц нижних конечностей, проводят массаж мышц нижних конечностей.
- Второй период (2-я неделя после операции). Рекомендуют укрепление мышц-стабилизаторов, дозированное восстановление подвижности позвоночника, проводят массаж мышц спины и нижних конечностей, разрешают плавание в бассейне.
- Третий период - восстановительный - восстановление выносливости позвоночника к статическим и динамическим нагрузкам, координации движений, в том числе и специфичных для спорта и балета двигательных навыков.
Через 2-3 нед после операции разрешают приступить к основной деятельности при условии соблюдения принципа постепенного дозированного увеличения нагрузок.
В литературе встречают данные о наблюдаемых в единичных случаях осложнениях при радиочастотной деструкции фасеточных нервов.
В начальный период разработки этой методики автор сообщал о небольших поверхностных ожогах кожи (4 пациента на 380 человек) в области прохождения электрода. Это было обусловлено несовершенством радиочастотного генератора и недостаточной изоляцией электрода. Как побочный эффект можно упомянуть онемение кожи в соответствующих денервации дерматомах или соседних участках. Эти явления гипестезии, как правило, проходили спустя несколько недель.
Таким образом, чрескожная радиочастотная деструкция фасеточных нервов - патогенетически обоснованный, эффективный и безопасный малоинвазивный метод лечения фасеточного синдрома поясничного отдела позвоночника. Преимущества его перед другими методами разрушения нервной ткани (химической, крио-, электро-, термодеструкцией, хирургической деструкцией) - контролируемый объем деструкции, постоянный мониторинг температуры и сопротивления тканей в области расположения кончика электрода, возможность подтверждения точной локализации иглы путем электростимуляции, выполнение под местной анестезией, короткий восстановительный период, низкая частота осложнений, возможность повторного применения.
Экстракорпоральная ударно-волновая терапия
Принцип действия этого метода основан на преобразовании электромагнитных колебаний в звуковые волны с фокусировкой их акустической линзой.
Фокус ударной волны имеет эллиптическую сигарообразную форму, продольная ось которой расположена по направлению распространения ударной волны. Глубина проникновения фокуса регулируется степенью наполнения водой контактной подушки - чем меньше наполнение, тем больше глубина. Максимальная глубина проникновения ударных волн составляет 60 мм.
Ударно-волновая установка EPOS позволяет осуществлять терапевтическое воздействие на девяти энергетических уровнях с плотностью энергии 0,03- 0,5 мДж/мм2, давлением 147-500 бар и частотой 60-240 импульсов в минуту. Эффективная энергия в фокусе 0,6-12,0 мДж.
Гибкая карданная подвеска терапевтической головки позволяет осуществлять оптимальное подведение ее к любому участку тела пациента. Для визуального облегчения позиционирования на контактной водяной подушке имеется маркировка, что делает наглядным прохождение ударных волн и позицию фокуса ударной волны по продольной оси. Расположенный сбоку лазерный указатель обозначает центр фокуса ударной волны по горизонтальной оси и одновременно служит для контроля глубины проникновения.
Показания для проведения ЭУВТ следующие.
- Лигаментопатия связок пояснично-крестцового отдела позвоночника и таза:
- пояснично-подвздошной (дистальное прикрепление);
- крестцово-бугорной (проксимальное и дистальное прикрепление);
- крестцово-остистой (проксимальное прикрепление).
- Тракционный апофизит крыла подвздошной кости.
- Традиционный метод лечения данных состояний, кроме изменения двигательного стеореотипа, - блокады с локальным введением глюкокортикоидных препаратов, которые уменьшают болезненные ощущения, но вместе с тем тормозят регенераторные процессы.
Противопоказания для проведения ударно-волновой терапии непосредственно вытекают из механизма действия ударных волн. Большая часть энергии ударной волны высвобождается при прохождении через ткани различной консистенции. Решающую роль при этом играют применяемая доза энергии и вид среды, через которую проходит ударная волна.
Нельзя осуществлять ударно-волновое воздействие в проекции крупных сосудов, нервных стволов, костей черепа, позвоночника, органов, содержащих воздух (легкие, кишечник). При воздействии ударной звуковой волны на крупные сосуды (переход ткань/жидкость) возможно повреждение стенки сосудов с возникновением кровотечения или индуцированием тромбоза. При переходе ударной волны из ткани в воздух, как это имеет место в зоне легких, кишечника, высвобождается большое количество энергии, что может привести к разрыву тканей. Вследствие поверхностного воздействия при лечении энтезопатий в зоне выхода на поверхность кожи (зона перехода ткань/воздух) возможно образование гематом.
Обязательное условие для проведения ударно-волновой терапии - окончание традиционных методов консервативной терапии не позднее 2 нед перед началом курса ЭУВТ. После локального воздействия рентгенотерапии должно пройти не менее 6 мес, после локальных инъекций глюкокортикоидов - не менее 2 мес. Именно в эти сроки, которые были определены экспериментальным путем, отмечено восстановление иммунного или гормонального статуса, нарушенного вследствие применения этих видов терапии. В результате восстанавливаются и местные регенераторные возможности.
Процедуру ударно-волновой терапии проводят в положении больного на животе. При лигаментопатии КБС в ее дистальном отделе с целью более точного позиционирования терапевтической головки необходимо увеличить сгибание в тазобедренных суставах для лучшего выведения седалищного бугра путем подкладывания под живот валика.
При проведении ЭУВТ анестезии не требуется. При лигаментопатиях связок таза используют прямое позиционирование терапевтической головки. При этом головку располагают над областью патологии, затем ее центр совмещают с точкой наибольшей болезненности, определяемой по способу обратной связи. После нанесения контактного геля головку прибора плотно прижимают к болезненному участку и осуществляют ударно-волновое воздействие. Обычная глубина проникновения ударных волн составляет 0,5-2,0 см. Однако для озвучивания более глубоко расположенного прикрепления ППС на крыле подвздошной кости необходима глубина 2,5-3,3 см. То же самое относится и к дистальному прикреплению КБС в области седалищного бугра. В последнем случае процедуру проводят особенно осторожно в связи с близостью седалищного нерва, который может реагировать на ударно-волновое воздействие. При появлении характерной стреляющей боли энергию воздействия уменьшают и меняют положение терапевтической головки.
Область ударно-волнового воздействия соответствует области прикрепления связки.
При патологии ППС в связи с широким прикреплением на крыле подвздошной кости постепенно осуществляют озвучивание всей этой области и верхней трети крестцово-подвздошного сочленения в связи с тем, что волокна ППС укрепляют верхнюю крестцово-подвздошную связку. При тракционном апофизите осуществляют ударно-волновое воздействие в области апофиза крыла подвздошной кости.
При лигаментопатии проксимального отдела КБС озвучивают боковую поверхность крестца и нижние 2/3 КПС, при лигаментопатии дистального отдела этой связки - медиальную поверхность седалищного бугра.
Область озвучивания при лигаментопатии КОС расположена на боковой поверхности крестца.
Количество импульсов за процедуру составляет 2000.
Лечение обычно начинают с самого низкого - первого энергетического уровня. В зависимости от анальгетического эффекта и переносимости процедуры с переходом с одного уровня на следующий увеличивают энергию воздействия. Частота импульсов в процессе процедуры также дозированно увеличивается с 60 до 180-240 ударов в минуту. С помощью пульта ручного управления, который с учетом требований эргономики расположен рядом с терапевтической головкой, обеспечивают контроль над всеми необходимыми параметрами ударно-волнового воздействия и пуск ударной волны.
После первой процедуры обычно наблюдают значительное облегчение, вплоть до полного исчезновения боли. Повторные процедуры проводят с интервалом в 7 дней. Боль к этому времени возникает вновь, но уже меньшей интенсивности. При повторных процедурах применяют более высокий энергетический уровень. Например, если в течение первой процедуры из-за сильного болевого синдрома удалось воздействовать ударными волнами только первого энергетического уровня, при повторной процедуре применяют уже второй и так далее.
Отмечено, что наибольший анальгетический эффект наблюдают при работе на 3-6-м уровнях ударно-волнового воздействия с частотой 90-180 импульсов в минуту, при явлениях тракционного апофизита крыла подвздошной кости энергию ударно-волнового воздействия увеличивают до 7-9-го уровня, а частоту ударов - до 240 импульсов в минуту. Количество процедур в зависимости от терапевтического эффекта составляет от трех до пяти.
Во время лечения пациентам разрешают тренироваться, рекомендуют только исключить движения, вызывающие боль.
Терапевтическое воздействие ударных волн при лигаментопатиях заключено в следующем.
Анальгетический эффект. Считают, что прохождение звуковых волн приводит к разрушению нервных окончаний либо к перераздражению (гиперстимуляции) их. Все эти процессы в конечном итоге имеют один и тот же результат, а именно прерывается рефлекторная дуга передачи болевого импульса из патологического участка. Этот вид реакции нервной системы, известный также под названием «пороговое управление» (gate control), инициирует активацию безмякотных волокон типа С и миелиновых волокон типа А-дельта. Сигналы, поступающие с С-волокон в задние рога спинного мозга, попадают в серое вещество, окружающее канал, и передаются назад в задние рога в виде информации, оказывающей тормозящее действие. При этом вновь поступающие болевые сигналы игнорируются. Волокна типа А-дельта препятствуют проведению сигналов от С-волокон. Другими словами, удается разорвать circulus vitiosus (порочный круг) боль - обработка болевой информации ЦНС - предотвращение болевых ощущений за счет использования замещающей схемы движения - возникновение патологической схемы движения - возникновение болевых ощущений вследствие реадаптационного изменения нейрональных включений.
Таким образом, ударно-волновое воздействие приводит к исчезновению памяти болезненного ощущения, вновь используется обычная схема выполнения движения и отпадает необходимость в нервных и мышечных замещающих механизмах.
Метаболическое действие обусловлено изменением мембранной проницаемости клеток вследствие кратковременного расширения межмолекулярных расстояний. Это способствует восстановлению внутриклеточного и внеклеточного ионного обмена. Обеспечивается отвод и всасывание продуктов катаболического разложения, т.е. ударно-волновое воздействие выводит процесс из «застывшего» состояния, растормаживает хронически воспаленную ткань.
Воздействие ударных волн, в отличие от ультразвуковых волн, не приводит к сколь-либо существенному изменению температуры внутри ткани. По этой причине эффект изменения мембранной проницаемости следует, скорее всего, рассматривать как результат механического воздействия.
Рассматривают также и другие анальгетические и противовоспалительные обменные реакции, которые связаны с активизацией свободных радикалов (изменение химической среды и торможение неврологических медиаторов) и стимуляцией макрофагов.
Эффект кавитации. При высокоэнергетическом ударно-волновом воздействии за фазой повышенного давления следует фаза разрежения. Уже при разрежении в несколько МПа в жидкой среде начинается образование разрывов непрерывности. Это приводит к формированию кавитационных пузырьков. Последние в результате повторного воздействия ударных волн могут схлопываться, что приводит к образованию локальных, крайне высоких давлений. Существует прямая взаимосвязь образования кавитационных пузырьков с интенсивностью энергии и частотой импульсов. В результате эффекта кавитации происходят дезинтеграция очагов кальциевых отложений в области энтезопатии, микропереломы в области костных фрагментов при замедленно срастающихся переломах и ложных суставах, образование вторичных гематом.
Именно эффектом кавитации можно объяснить те остеогенные процессы, которые происходят в результате высокоэнергетического ударно-волнового воздействия в области тракционных апофизитов и способствуют их ассимиляции. Ударные волны приводят к:
- измельчению остеогенных агрегационных ядер с освобождением кристаллов фосфата кальция и созданию с участием макрофагов новых остеогенных агрегационных ядер;
- активации стимулятора остеогенеза - костного протеина остеонектина;
- увеличению регионального кровенаполнения в результате временного симпатического паралича;
- фрагментации базальных мембран капилляров и миграции эндотелиальных клеток в интерстициальное пространство с образованием новых капилляров;
- активации вследствие капиллярного стресса стимулятора ангиогенеза, способствующего размножению эндотелиальных клеток и фибробластов, что также приводит к образованию новых капилляров;
- ускорению роста и дифференциации остеобластоподобных клеток (дозозависимый эффект).
Кроме того, образующиеся в результате эффекта кавитации в зоне ударноволнового воздействия биологически активные вещества также нарушают ноцицептивную функцию нервных окончаний и индуцируют регенераторные процессы.
Эффект действия ударных волн в зависимости от энергетического уровня представлен в табл. 15.
Таблица 15. Эффект действия ударных волн в зависимости от уровня и плотности энергии
|
Лечение |
Действие ударной волны |
Плотность энергии. мДж/мм-1 |
Уровень энергии |
|
Переломы постен Ложные суставы Апофизиты |
Кавитация |
>0.6 |
6-9 |
|
Метаболический |
0.28-0.6 |
1-7 | |
|
Анальгетический |
0.08-028 |
1-5 | |
|
Кальцификация |
Кавитация |
>0.6 |
6-9 |
|
Метаболический |
0.23-0.6 |
1-7 | |
|
Анальгетический |
0.08-028 |
1-5 | |
|
Тендопатия Лигаментопатия |
Метаболический |
0.28-0.6 |
1-7 |
|
Анальгетический |
0.08-028 |
1-5 |
Соблюдение противопоказаний, однозначное определение показаний, оптимальная локализация и правильное позиционирование терапевтической головки исключают тяжелые осложнения вследствие проведения ударно-волновой терапии.
На основании данных литературы и собственных клинических наблюдений можно сделать вывод о несомненных преимуществах экстракорпоральной ударноволновой терапии перед другими видами лечения:
- амбулаторный метод;
- неинвазивная терапия;
- небольшая продолжительность лечения;
- не применяется анестезия;
- отсутствуют опасности, присущие для оперативного вмешательства;
- исключено применение глюкокортикоидов;
- не образуются рубцы;
- нет осложнений;
- лечение проводят без освобождения от работы или тренировок.
Таким образом, представленные высокотехнологичные методы лечения, а именно чрескожные лазерная декомпрессия дисков и радиочастотная деструкция фасеточных нервов, а также экстракорпоральная ударно-волновая терапия, перспективны при лечении пояснично-крестцового болевого синдрома у спортсменов. Это связано с их малотравматичностью, отсутствием необходимости длительного пребывания больного в стационаре, достаточно быстрым восстановлением спортивной и профессиональной работоспособности.
Дифференциальная диагностика пояснично-крестцового болевого синдрома у спортсменов
Хронический пояснично-крестцовый болевой синдром - наиболее частая причина обращения больных к врачам разных специальностей. Источниками боли в спине могут быть различные элементы позвоночного столба, поскольку все они содержат нервные окончания.
Успешное лечение ПКБС невозможно без целенаправленного воздействия на продуцирующие боль структуры. Поскольку пояснично-крестцовый болевой синдром может быть проявлением целого ряда дегенеративно-дистрофических заболеваний позвоночных сегментов и окружающих мягких тканей, чрезвычайно важно знать особенности развития данного заболевания у каждого конкретного больного. Использование инструментальных методов диагностики, методов лучевой диагностики помогает в уточнении диагноза. Дифференциальная диагностика проводится между остеохондрозом, фасеточным синдромом, спондилолизом и связочной патологией пояснично-крестцового отдела позвоночника.
Острое начало заболевания характерно прежде всего для дискорадикулярного конфликта. Наиболее частый «пусковой механизм» - поднятие тяжести. Такое острое развитие клинической симптоматики большинство авторов объясняют резким повышением внутридискового давления и устремлением элементов диска (пульпозного ядра) в сторону позвоночного канала. Интенсивность болевого синдрома по ВАШ составляет 8-9 баллов. При этом зачастую развивается анталгический наклон туловища, ограничиваются движения в позвоночнике во всех направлениях.
При фасеточном синдроме острое начало наблюдают реже. «Пусковой механизм» - резкое движение в поясничном отделе позвоночника в сочетании с осевой нагрузкой. Считают, что при этом происходит ущемление менискоидов межпозвонковых суставов или богато иннервируемой капсулы сустава. Вследствие рефлекторного напряжения мышц развивается также функциональный блок, однако он ограничен несколькими позвоночными сегментами. Возможны осторожные наклоны вперед, при наклоне назад и в здоровую сторону боли резко усиливаются. Интенсивность болевого синдрома - до 7 баллов (ВАШ).
Еще реже острое начало заболевания наблюдают при спондилолизе. Наиболее частая причина усталостного перелома дуги позвонка - значительное переразгибание поясничного отдела позвоночника в сочетании с ротацией. Интенсивность боли при спондилолизе составляет 4-6 баллов (многие спортсмены и артисты балета, несмотря на боль, продолжают свою профессиональную деятельность). Присутствуют ограничение наклонов вперед, болезненность наклонов назад и в сторону пораженной дуги.
Остро могут возникать и повреждения остистых связок в результате форсированных движений поясничного отдела позвоночника в сагиттальной плоскости. Интенсивность болевых ощущений составляет 4-7 баллов (ВАШ).
При всех этих заболеваниях отмечают не только локальную боль в поясничном отделе позвоночника. При остеохондрозе с наличием дискорадикулярного конфликта присутствует симптоматика поражения соответствующего спинномозгового нерва с характерными зоной иррадиации боли, двигательными, чувствительными, рефлекторными нарушениями и симптомами натяжения корешков. По характеру боль при дискорадикулярном конфликте острая, хорошо локализованная, подобна разряду электрического тока, отличается постоянством.
У больных с фасеточным синдромом, спондилолизом и патологией связок при неврологическом обследовании не выявляют признаков корешковой дисфункции. В ряде случаев у пациентов со спондилолизом и начинающимся спондилолистезом отмечают ложный симптом Ласега, обусловленный напряжением задней группы мышц бедра. При фасеточном синдроме возможен положительный симптом ПВН при поднятии конечности под углом более 70° к горизонтальной плоскости вследствие передачи движения на поясничный отдел.
Для фасеточного синдрома, спондилолиза и связочной патологии характерна отраженная боль, которая, на первый взгляд, сходна с проявлением корешкового синдрома. Однако отраженную боль отличает меньшая интенсивность, она глубокая, ноющая, сверлящая, имеет определенную локализацию при каждом виде патологии, но редко опускается ниже коленного сустава. Например, при синдроме Минье - дисфункции межпозвонковых суставов грудопоясничного отдела перехода - боль ощущается в области крыла подвздошной кости той же стороны, при этом отмечают гиперчувствительность кожи в области крыла подвздошной кости при щипке или перекатывании кожи при исследовании. Вследствие того что внимание всегда привлечено к болезненному месту, источник боли зачастую не определяют.
Если боль при дискорадикулярном конфликте постоянная, то при других видах патологии она носит перемежающийся характер, зависит от двигательной нагрузки. При фасеточном синдроме и связочной патологии болевые ощущения уменьшаются при движениях, при спондилолизе же боль, наоборот, усиливается.
Дискорадикулярный конфликт сопровождают анталгический наклон туловища и уплощение поясничного лордоза, при связочной патологии и спондилолизе лордоз, как правило, усилен.
Выраженное напряжение и повышенный тонус мышц спины определяют при дискогенной патологии, при спондилолизе напряжены мышцы поясничной области, при фасеточном синдроме - локальное напряжение над пораженным суставом. При хронической микротравме связок таза мышечный тонус, напротив, снижен.
В дифференциальной диагностике помогает и ряд специфических для каждой патологии тестов: разгибательный тест при фасеточном синдроме, маховый тест при спондилолизе, тесты на натяжение связок таза - ППС, КБС, КОС, ротационный тест и т.д.
Один из методов специального обследования, позволяющий уточнить диагноз, - диагностическая блокада, временное купирование боли в результате анестезии межпозвонкового сустава или поврежденной связки.
Наряду с клинико-неврологическим обследованием большое значение для установления правильного диагноза имеют методы лучевой диагностики: спондилография (стандартные проекции, косые в 3/4, с функциональными пробами), КТ, МРТ, а также радионуклидное исследование, УЗИ, термография.
Основные дифференциально-диагностические признаки остеохондроза, синдрома фасеток, спондилолиза и патологии связок пояснично-крестцового отдела позвоночника и таза приведены в табл. 16.
Апофизит - изменения верхнепоясничного отдела позвоночника у спортсменов - часто трактуют как остеохондропатию, тогда как на самом деле это два различных патологических состояния.
При остеохондропатии чаще всего поражается нижнегрудной отдел позвоночника с образованием протяженного равномерного кифоза. Основу его составляют увеличенные в переднезаднем направлении клиновидные позвонки. Межпозвонковые диски в ранней стадии заболевания мало изменены, затем отмечают небольшое их уплощение, возникают множественные узелки Шморля. В замыкательных пластинах наблюдают аномальные участки со сниженным содержанием гликопротеидов и нарушением агрегации коллагена. Кроме того, остеохондропатия - генетически детерминированное заболевание с аутосомно-доминантным типом наследования.
В отличие от остеохондропатии апофизит - приобретенное заболевание спортсменов в результате специфической профессиональной нагрузки. Поражается верхнепоясничный отдел позвоночника с формированием локального кифоза. Высота межпозвонковых дисков снижена вследствие образования передней грыжи. Отмечают смещение апофиза кпереди с его оссификацией.
Мышечные синдромы также могут быть источником пояснично-крестцового болевого синдрома. Отраженная боль при этом может имитировать корешковую боль при остеохондрозе или отраженную боль при спондилоартрозе, нестабильности пояснично-крестцового отдела позвоночника или патологии связок. В мышцах образуются триггерные точки, которые характеризуют локальные уплотнения мышечной ткани, определяемые пальпаторно и при ЭМГ, болезненные при пассивном растяжении мышцы. Для мышечных синдромов нехарактерны неврологические нарушения, отраженная боль в нижние конечности в большинстве случаев не опускается ниже коленного сустава.
В плане дифференциальной диагностики острого дискорадикулярного конфликта необходимо упомянуть острый приступ илиопсоалгии, при котором возникает сильная боль в пояснице, и анталгический наклон туловища.
Основные причины рефлекторного спазма и укорочения поясничноподвздошной мышцы:
- прямое давление на мышцу или раздражение двигательных нервов при переднелатеральной экструзии дисков между I и II и II и III поясничными позвонками;
- стимуляция двигательных ветвей 1-3 спинномозговых нервов, возникающая в результате передачи (посредством белых соединительных ветвей) возбуждения симпатических волокон крестцового автономного сплетения переднелатеральной экструзией диска между V поясничным и I крестцовым позвонками.
При илиопсоалгии, кроме боли в поясничной области, могут быть болезненные ощущения в паху и ягодице - одноили двусторонние, альтернирующие или все время только с одной стороны. Никогда не бывают по средней линии, за исключением сопутствующей дисковой патологии. Боли усиливаются в положении на животе, при ходьбе, наклоне вперед, вперед и в сторону, противоположную боли, поворотах туловища в здоровую сторону. Наклон назад невозможен. Боль уменьшается в положении сидя.
Пациент может предъявлять жалобы на боль в пояснице с одной стороны и боль в верхнепоясничном отделе с другой стороны и плечевом суставе. Это можно объяснить наличием перекреста волокон большой ягодичной мышцы с одной стороны с волокнами m. latissimus dorsi другой стороны через грудопоясничную фасцию.
Вследствие пояснично-подвздошной миофиксации уплощается поясничный лордоз и возникает кифоз. Положителен симптом Вассермана (появление боли в паху и пояснице при разгибании бедра). Отмечают наклон корпуса вперед или в больную сторону при ходьбе.
Пальпация пояснично-подвздошной мышцы из-за ее глубокого расположения затруднена, однако небольшой ее участок около места прикрепления к малому вертелу бедренной кости можно пропальпировать. Для этого надо отвести бедро пациента и согнуть коленный сустав. Пояснично-подвздошную мышцу пальпируют в латеральной части дна бедренного треугольника, образованного паховой связкой сверху, портняжной мышцей латерально и длинной приводящей мышцей медиально.
Боль иррадиирует по передней и внутренней поверхностям бедра обычно до коленного сустава без неврологического дефицита. На рентгенограммах в прямой проекции иногда можно увидеть уплотнение тени поясничной мышцы на больной стороне. Уточняют диагноз с помощью обезболивающей блокады мышцы.
Одна из достаточно частых причин люмбоишиалгии - синдром грушевидной мышцы, который может быть вторичным рефлекторным или самостоятельным болевым синдромом.
При занятиях спортом и балетом возникают сначала рабочая гипертрофия грушевидной мышцы, затем хроническая перегрузка при длительной статической нагрузке (например, длительном пребывании в антифизиологической позе), и повторные микротравмы при высокоамплитудных движениях нижних конечностей приводят к фиброзу мышечной ткани. И в том, и в другом случае седалищный нерв подвергается механической компрессии. Последняя приводит к нарушению кровоснабжения седалищного нерва с последующей демиелинизацией и изменению нервной проводимости, что характерно для разрушения оболочки нерва. Поэтому в отличие от пролапса диска при синдроме грушевидной мышцы отмечают ирритативный корешковый синдром.
Кроме того, в результате прямой травмы ягодичной области образуются кровоизлияния с выделением биологически активных веществ (серотонина, брадикинина). Воспалительные медиаторы приводят не только к образованию отека и освобождению мукополисахаридов, но и к раздражению nervi nervorum оболочки седалищного нерва.
При синдроме грушевидной мышцы боль локализована как в самой мышце, так и в поясничной области. Она усиливается при ходьбе, в положении стоя, при полуприседании на корточках, в положении конечность на конечность, уменьшается в положении лежа, сидя с разведенными ногами. Усиление боли происходит при внутренней ротации бедра в тазобедренном суставе за счет натяжения грушевидной мышцы (симптом Фрайберга ), при наружной ротации бедра с сопротивлением. Боль усиливается и при приведении бедра. Положителен симптом Виленкина : перкуссия в точке грушевидной мышцы приводит к появлению боли по задней поверхности конечности. Возможно некоторое ограничение сгибания в тазобедренном суставе. Грушевидная мышца часто болезненна при пальпации, напряжена. Однако движения в позвоночнике свободные, в полном объеме.
Между спазмированной грушевидной мышцей и КОС может сдавливаться седалищный нерв вместе с нижней ягодичной артерией. Основной симптом раздражения седалищного нерва - боль в области ягодицы, задней поверхности бедра, подколенной ямки, стопы. Как правило, боль имеет выраженную вегетативную окраску, сочетается с ощущением зябкости или жжения. Боль усиливается при ходьбе, перемене погоды, стрессовых ситуациях. Положителен псевдосимптом Ласега. При длительной компрессии развиваются симптомы нарушения функции седалищного нерва: снижаются сила в мышцах голени и стопы, ахиллов рефлекс. Выпадение чувствительности чаще отмечают в зоне иннервации малоберцового нерва, так как его волокна наиболее уязвимы при ухудшении кровоснабжения.
Вследствие поражения вегетативных волокон седалищного нерва возникают каузалгии, гиперестезия, вазомоторные нарушения (стопа становится цианотичной, холодной на ощупь), трофические нарушения (гиперкератоз, изменение формы, цвета и роста ногтей, нарушения потоотделения).
Сдавление нижней ягодичной артерии и сосудов седалищного нерва приводит к развитию «подгрушевидной» перемежающейся хромоты. Вследствие рефлекторного спазма артерий нижней конечности при ходьбе возникает резкая боль, локализующаяся чаще всего в задней группе мышц голени, вынуждающая пациента останавливаться, сгибать больную конечность в коленном суставе или садиться. При возобновлении ходьбы подобная картина повторяется.
Вторичный синдром грушевидной мышцы возникает при заболеваниях крестцово-подвздошного сочленения, органов малого таза, дискогенных радикулопатиях V поясничного и I крестцового позвонков.
Для уточнения уровня компрессии седалищного нерва необходимо неврологическое исследование дополнить электронейромиографией, исследованием сосудов нижней конечности, МРТ поясничного отдела позвоночника, эхографией ягодичной области, диагностической блокадой грушевидной мышцы.
Другая причина пояснично-крестцового болевого синдрома - синдром подколенного сухожилия. В результате повторных резких махов ногой вперед при спринте или беге с барьерами, при ударе по мячу в футболе происходят микронадрывы и микрокровоизлияния в месте прикрепления задней группы мышц бедра (двуглавая мышца бедра, полусухожильная и полуперепончатая мышцы) в области седалищного бугра. Это приводит к образованию рубцовых спаек с лежащим рядом седалищным нервом. При данной патологии также наблюдают пояснично-крестцовую боль, распространяющуюся до подколенной ямки, и может быть положителен симптом Ласега . В отличие от дискорадикулярного конфликта при синдроме подколенного сухожилия отсутствуют напряжение мышц спины и другие симптомы поражения позвоночника. Боль при пальпации в области седалищного бугра усиливается при подъеме конечности вперед (симптом растяжения). Кроме того, характерный симптом - боль в области седалищного бугра при длительном сидении. Неврологических нарушений не бывает.
Синдром ягодичных мышц возникает вследствие однократной или повторяющейся хронической перегрузки, разной длины ног, дисфункции КПС, неправильной походки. Характеризуется упорной болью в пояснично-крестцовой области, зоне ягодиц, по наружной или задней поверхности больной конечности. Усиливается боль чаще всего при длительном сидении, при перемене положения тела, в положении конечность на конечность, при переохлаждении. При пальпации выявляют значительное мышечное напряжение.
Тестирование средней и малой ягодичных мышц: пациент, лежащий на спине с вытянутыми и приведенными ногами, отводит бедро, врач оказывает сопротивление этому движению и пальпирует напряженные болезненные мышцы.
Достаточно часто встречают тендинит сухожилия средней ягодичной мышцы и вертельный бурсит. Характерна боль по латеральной поверхности бедра, возникающая при ходьбе, игре в теннис. Подобно тендиниту сухожилия надостной мышцы и подакромиальному бурситу тендинит сухожилия средней ягодичной мышцы и вертельный бурсит возникают в результате дегенеративных изменений и постоянной травматизации. Дифференцировать тендинит сухожилия средней ягодичной мышцы и вертельный бурсит трудно, по-видимому, эти заболевания нередко сопутствуют друг другу. Боль при вертельном бурсите обычно возникает ночью, а при тендините - во время длительной ходьбы. Но, в отличие от рассматриваемого в нашей работе контингента, вертельным бурситом в основном страдают пожилые люди. Помогает в установлении правильного диагноза эхография вертельной области, в некоторых случаях - рентгенография тазобедренного сустава, лечебно-диагностическая блокада.
Причиной поражения большой ягодичной мышцы может стать избыточная нагрузка при беге, прыжках, вставании из сидячего положения, особенно с весом, например со штангой, подъеме по лестнице, длительной ходьбе с наклоненным вперед туловищем, падении. Наряду с болями в поясничной и ягодичной областях присутствует и отраженная боль по задней поверхности бедра.
Тестирование большой ягодичной мышцы: пациент лежит на животе с согнутой голенью, поднимает бедро, доктор оказывает сопротивление этому движению и пальпирует напряженную болезненную мышцу.
Синдром квадратной мышцы поясницы характеризует возникновение боли в области КПС, в глубине ягодиц, вдоль латеральной границы подвздошного гребня и до большого вертела бедренной кости. Из-за глубокой боли в поясничной области пациент может терять способность стоять с выпрямленным позвоночником или ходить. Болевые ощущения может вызвать даже попытка повернуться в постели на другой бок. При пальпаторном исследовании выявляют болезненные участки миофиброза в местах прикрепления квадратной мышцы поясницы к поперечным отросткам трех верхних поясничных позвонков и XII ребру. Причина этого состояния - избыточная нагрузка при поднятии тяжестей с согнутой в пояснице спиной, длительное и повторяющееся напряжение мышц спины.
Хронический компартмент-синдром мышц спины - относительно редкая причина пояснично-крестцового болевого синдрома. Он возникает вследствие длительного защитного мышечного напряжения при нестабильности, изменении рабочего стереотипа, а также активных занятий с тяжестями и на тренажерах. Именно у представителей силовых видов спорта компартмент-синдром возникает чаще всего. При этом гипертрофированные мышцы как бы зажаты в футляре нерастяжимой фасции. Это и обусловливает появление хронической одноили двусторонней паравертебральной боли при физических упражнениях. При пальпации отмечают значительное повышение тонуса паравертебральных мышц. Важные диагностические признаки включают уменьшение боли в покое и отсутствие неврологических нарушений.
Патология крестцово-подвздошного сочленения вызывает боль в пояснице, ягодице и бедре, характерную для радикулопатии корешка 1 крестцового спинномозгового нерва. Боль усиливается при ходьбе, наклонах, длительном сидении или стоянии. При ходьбе больной наклоняется на один бок, щадит конечность. Болевые точки отмечают сбоку от крестца, под задней остью подвздошной кости и в ягодичной области. Кроме того, наблюдают судорожные подергивания в икроножной мышце той же стороны, усиливающиеся в ночное время. Патология КПС может формироваться в результате блока сочленения, который нередко возникает при «косом» и «скрученном» тазе, а также при деформирующем артрозе, патологической костной перестройке в области КПС, воспалительных (ревматизм, туберкулез, бруцеллез) и системных заболеваниях (болезнь Бехтерева ). Симптомов неврологических выпадений не наблюдают. Характерен псевдосимптом Ласега с возникновением боли преимущественно в области подколенной ямки или изолированно в пояснице. Существует ряд тестов, при выполнении которых появление боли в КПС подтверждает его патологию.
- Сжатие таза - пациент лежит на боку, на верхнее крыло подвздошной кости осуществляют давление перпендикулярно вниз. При этом растягиваются задние крестцово-подвздошные связки или возникает компрессия переднего отдела КПС.
- Дистракция - осуществляют давление спереди назад и кнаружи на обе передние верхние ости подвздошной кости лежащего на спине пациента, как бы пытаясь растянуть таз. Объект растягивания - передние крестцовоподвздошные связки.
- Тест Генслена - положение больного на здоровом боку, конечность максимально согнута и подтянута к животу, исследуемая конечность сверху и разогнута, врач переразгибает ее в тазобедренном суставе. При этом происходит ротационное движение в КПС, ощущаемое исследователем, и резко усиливается боль в КПС при его патологии.
- Тест Патрика (коленно-пяточный) - положение больного на спине с фиксированным тазом: крайнее отведение конечности, согнутой в тазобедренном и коленном суставах и ротированной кнаружи (пятка касается бедра выпрямленной другой конечности), приводит к возникновению боли в одноименном КПС, определяют ограничение отведения в тазобедренном суставе. В норме колено согнутой конечности должно лечь на поверхность кушетки.
- Тест Кэмпбелла - при разгибании туловища возникает боль в области пораженного КПС.
- Тест бедренного толчка - положение больного на спине, усилие прилагают к КПС путем внезапного давления на согнутое под углом 90° бедро в нейтральном положении.
- Тест крестцового толчка - положение больного на животе, давление осуществляют на крестец.
- Краниальный срезывающий тест - осуществляют давление на копчиковый конец крестца в краниальном направлении.
- Феномен «опережения», асимметрия движений крестца. В положении пациента стоя врач устанавливает большие пальцы обеих рук на задние верхние ости подвздошной кости. При наклоне вперед в норме обе ости смещаются вперед симметрично. Если тонус крестцово-подвздошных связок повышен, при наклоне крестца раньше вовлекается в движение половина таза с укороченными связками. В этом случае расположенная ниже задняя верхняя ость поднимается выше, «опережает» заднюю верхнюю ость другой стороны. Через 20-30 с натянутые связки расслабляются, симметрия таза восстанавливается.
Кроме этих тестов при функциональной патологии таза («косой» и «скрученный» таз, блокады КПС) имеются характерные симптомы.
- Симптом «бокового хода» - больные отмечают, что при ходьбе боком мелким шагом боли беспокоят значительно меньше, особенно это проявляется в остром периоде заболевания.
- Симптом «лестницы» - подниматься вверх по лестнице легче, чем спускаться.
- Симптом «жесткого ложа» - больные не переносят жесткой постели (на щите в положении на спине).
Эти дифференциально-диагностические признаки обобщены в табл. 17.
Таблица 17. Дифференциально-диагностические признаки патологии пояснично-крестцового отдела позвоночника и крестцово-подвздошного сочленения
|
Симптом |
Патология пояснично-крестцового отдела позвоночника |
Патология крестцово-подвздошного сочленения |
|
Боль | ||
|
Локализация |
LS-S1 |
Ягодичная область в проекции тазобедренного сустава |
|
Иррадиация |
Наружная поверхность голени, тыл стопы-подошва |
Задняя поверхность бедра, паховый сгиб |
|
Затруднено нахождение в положении лежа |
На спине с разогнутыми ногами |
На боку пораженной стороны |
|
Боль при надавливании |
На остистый отросток V. реже IV поясничных или I крестцового позвонков, пояснично-подвздошную связку |
На крестцово-подвздошное сочленение. большую седалищную вырезку |
|
Движения позвоночника | ||
|
Стоя |
Ограниченны |
Свободны все. кроме наклонов в здоровую сторону; ограничена крайняя степень сгибания кпереди |
|
Сидя |
Ограниченны |
Наклоны вперед свободны при расслабленных сгибателе бедра |
|
Лежа |
Ограниченны |
Свободны |
|
Специальные симптомы | ||
|
Подъем выпрямленной конечности |
Ограничен с обеих сторон, крайняя степень подъема |
Ограничен с одной стороны незначительно |
|
Тестирование КПС | ||
|
Сжатие таза Дистракция таза Тест Генслена Тест Патрика Тест Кэмпбелла Тест бедренного толчка Тест крестцового толчка |
- |
Боль с пораженной стороны |
|
Краниальный срезывающий тест |
- |
+ |
|
Феномен «опережения» |
- |
+ |
|
Симптом «бокового хода» |
- |
+ |
|
Симптом «лестницы» |
- |
+ |
|
Симптом «жесткого ложа» |
- |
+ |
При рентгенологическом обследовании выявляют изменения в области КПС - сужение суставной щели, краевые остеофиты (деформирующий артроз), остеопороз с кистовидными просветлениями и эрозированными суставными поверхностями (воспалительные процессы), субхондральный склероз, уплотнение кости, гиперостоз крыла подвздошной кости, очаги уплотнения (конденсирующий сакроилеит - патологическая функциональная перестройка).
На обзорной рентгенограмме таза при его функциональной патологии в положении пациента лежа выявляют следующее:
- асимметрию линий, соответствующих суставным поверхностям КПС;
- отсутствие параллельности линий, проходящих через наиболее высокие точки гребня подвздошной кости и две корреспондирующие точки контура вертлужной впадины, которые в норме параллельны;
- ступенеобразную деформацию симфиза;
- деформацию ветвей симфиза и запирательного отверстия вследствие ротации таза.
На функциональных рентгенограммах таза, выполняемых в положении пациента стоя попеременно на одной и другой конечности в течение нескольких минут, усиливается ступенеобразная деформация симфиза, деформация лонных костей и запирательного отверстия. При разной длине нижних конечностей линии, проходящие через наиболее высокие точки гребня подвздошной кости и две корреспондирующие точки контура вертлужной впадины, кроме того что они не параллельны между собой, они не параллельны и полу.
Значительные диагностические трудности возникают при клинических признаках патологии КПС и появлении неврологической симптоматики. Это объясняют тем, что при обострении деформирующего артроза и синовита крестцовоподвздошного сочленения воспалительные медиаторы, а также краевые остеофитов воздействуют на невральные элементы в области трех слабых мест КПС, обнаруженных с помощью контрастной артрографии. Эти слабые места расположены в следующих отделах КПС:
- заднем - в области дорсального крестцового отверстия;
- верхнем - на уровне крыла подвздошной кости вблизи от корешка 5 поясничного спинномозгового нерва;
- переднем - в области пояснично-крестцового сплетения.
В таких случаях для уточнения диагноза необходима электродиагностика.
Из дополнительных методов обследования большое значение имеют лабораторные данные, свидетельствующие о воспалительном процессе.
Источником поясничной боли могут быть бурситы в области большого вертела, грушевидной, ягодичной и внутренней запирательной мышц.
Внутренняя запирательная сумка является постоянной. Ее расположение легко определяют в положении больного на боку. При подтягивании коленного сустава к груди легко пальпируют седалищный бугор. Пальпирующий палец затем движется к верхнему заднему краю выпуклости седалищного бугра и скользит кверху в углубление малой седалищной вырезки, на верхушке которой лежит сумка. Над ней расположена внутренняя запирательная мышца, прикрепляющаяся вместе с близнецовыми мышцами на медиальной поверхности большого вертела. Сумка расположена медиальнее седалищного нерва в непосредственной близости от крестцово-остистой связки. Болезненность пальпации в этой зоне указывает на бурсит либо лигаментопатию КОС. В случае бурсита максимальное отведение и ротация кнутри поднятой вверх прямой конечности вызывает боль вследствие натяжения внутренней запирательной и грушевидной мышц, под которыми расположена воспаленная сумка. Провокационный тест для крестцово-остистой связки: появление боли при приведении согнутой конечности к противоположному плечу.
При патологии тазобедренного сустава характерна боль в области сустава с иррадиацией в поясницу и бедро. Боль провоцируют движения в суставе, характерна боль после продолжительного покоя («стартовая» боль), после длительной ходьбы, при ношении тяжестей, при перемене погоды, сопровождается ограничением движений в суставе. Определяют болезненный спазм всех мышц, принимающих участие в движении сустава, что приводит к формированию сгибательно-приводящей контрактуры. При ходьбе таз смещается вверх и вперед, возникает компенсаторный поясничный гиперлордоз, что обусловливает своеобразную «кланяющуюся» походку. Помогают в распознавании истинной причины болевого синдрома методы лучевой диагностики: обзорная рентгенография позвоночника и тазобедренных суставов, МРТ, КТ.
Большие трудности для диагностики представляют инфекционные поражения позвоночного столба. Инфекция может затрагивать как дисковые пространства (дисцит), так и сами позвонки (спондилит). Обычная рентгенография, как правило, малоинформативна, если, конечно, нет паравертебрального абсцесса или остеомиелита; намного более чувствительны для выявления инфекции КТ и МРТ. Формирование эпидурального абсцесса следует заподозрить в том случае, когда у пациента с предполагаемой или доказанной бактериемией возникают и постепенно усиливаются разлитые боли по всей поясничной области, продолжающиеся на протяжении дней и недель. Быстрое прогрессирование боли, корешковых симптомов и слабости в нижних конечностях также указывает на наличие эпидурального абсцесса. Туберкулез начинается в теле позвонка и в конечном счете приводит к его коллапсу.
В ряде случаев необходимо проводить исследование на ревматоидный артрит, а также на специфические инфекции: хламидиоз, урео- и микоплазмоз, лаймскую болезнь.
Кроме этого, боль, исходящая от внутренних органов и глубоко лежащих рецепторных структур, также может проецироваться на поясничную область. Консультации специалистов (уролога, гинеколога, гастроэнтеролога, проктолога) помогут уточнить источник ПКБС.
Таким образом, представленный дифференциально-диагностический алгоритм при обследовании пациентов с пояснично-крестцовым болевым синдромом будет способствовать раннему и точному выявлению пораженных структур позвоночного двигательного сегмента, и, следовательно, своевременному проведению адекватной терапии.
Лечебный алгоритм при пояснично-крестцовом болевом синдроме у спортсменов
На основании клинических наблюдений и лечения пациентов-спортсменов с пояснично-крестцовым болевым синдромом в ЦИТО разработаны следующие схемы лечения (табл. 18-20-23).
Таблица 18. Лечебный алгоритм при спондилогенной пояснично-крестцовой боли
Таблица 19. Лечебный алгоритм при пояснично-крестцовой боли с корешковым (ирритативным или компрессионным) синдромом
Таблица 20. Лечебный алгоритм при синдроме фасеток
Таблица 21. Лечебный алгоритм при спондилолизе поясничных позвонков
Таблица 22. Лечебный алгоритм при патологии остистых связок
Таблица 23. Лечебный алгоритм при лигаментопатиях связок таза
Читайте также
- Тренировка пресса при боли в спине
- Спортивная травма позвоночника - лечение
- Растяжение связок позвоночника в поясничном отделе
- Боль в спине
- Боль в пояснице
- Грыжа межпозвоночного диска
- Спондилолиз
- Спондилолистез (лечение)
- Переломы позвоночника в поясничном отделе
- Реабилитация при болях в спине
- Массаж при остеохондрозе
- Массаж при радикулите
- Массаж при межреберной невралгии