Противовирусные средства (препараты)
Содержание
Противовирусные средства[править | править код]
Источник: «Наглядная фармакология».
Автор: X. Люльман. Пер. с нем. Изд.: М.: Мир, 2008 г.
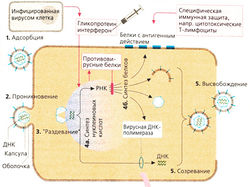
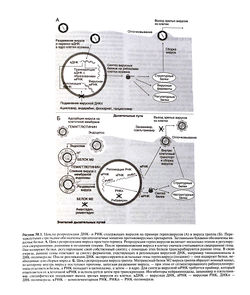
Вирусы состоят в основном из генетического материала (нуклеиновые кислоты, ДНК, на рис. А изображены зеленым цветом), заключенного в оболочку — капсид (синий шестиугольник); чаще всего это двухслойная фосфолипидная мембрана (серое кольцо) со встроенными белками (синие черточки). У вирусов нет собственного обмена веществ, они размножаются за счет пораженной ими клетки-хозяина. Для лечения вирусных заболеваний необходимо ингибировать обменные процессы в инфицированных клетках, которые участвуют в размножении вирусов.
Размножение вирусов на примере вируса простого герпеса (Herpes simplex) (А). Вирус простого герпеса содержит двухцепочечную ДНК.
1. Вирусная частица прикрепляется (адсорбируется) на поверхности клетки-мишени, при этом гликопротеины оболочки вируса взаимодействуют со специальными структурами клеточной мембраны.
2. Оболочка вируса встраивается в клеточную мембрануклетки-мишени и нуклео-капсид (нуклеиновые кислоты + капсид) входит внутрь клетки (проникновение).
3. Капсид раскрывается («раздевание вируса») — у вируса герпеса этот процесс происходит на порах ядра — и ДНК вируса проникает в ядро; с этого момента генетический материал вируса может управлять метаболизмом клетки.
4а. Синтез нуклеиновых кислот: генетический материал вируса (в данном случае ДНК) многократно реплицируется, далее образуется РНК, необходимая для синтеза белка.
46. Вирусные белки представляют собой ферменты, необходимые для размножения (например, ДНК-полимераза и тимидинки-наза), а также материал для построения капсида или вирусной мембраны (они могут также встраиваться в мембрану клетки).
5. Сборка компонентов вирусной частицы.
6. Высвобождение дочерних вирусов, которые могут распространяться внутри организма и вне его.
Размножение вируса герпеса приводит к гибели клетки-мишени; при этом проявляются симптомы заболевания.
Защита организма от вирусов (А). Организм защищается от размножения вирусов с помощью цитотоксических Т-лимфоцитов, которые узнают клетки, продуцирующие вирусы (по наличию на поверхности клеток индуцированных вирусом белков) и уничтожают их. Кроме того, организм защищается с помощью антител, которые инактивируют вирусные частицы, находящиеся вне клетки. Профилактические противовирусные прививки имеют своей целью активировать механизм специфической иммунной защиты организма.
Интерфероны (ИНФ) представляют собой гликопротеины, высвобождаемые инфицированными вирусом клетками. Интерфероны стимулируют в соседних клетках продукцию антивирусных белков, которые тормозят синтез вирусных белков путем разрушения вирусной РНК или вызывают нарушение трансляции. Действие интерферонов не направлено на определенный вирус. Однако они специфичны в отношении организмов, т. е. для лечения людей нужен человеческий интерферон. Интерфероны получают из лейкоцитов (ИНФ-а), фибробластов (ИНФ- β ) или лимфоцитов (ИНФ-у). Интерфероны применяют для лечения некоторых вирусных заболеваний, злокачественных новообразований и аутоиммунных заболеваний: ИНФ-а — для лечения хронического гепатита С и волосатоклеточного лейкоза, ИНФ- β — для лечения тяжелых форм герпеса и рассеянного склероза.
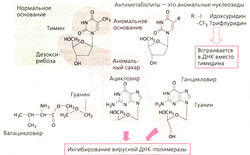
Вирусостатические актиметаболиты — аналоги нуклеозидов (Б). Нуклеозид (например, тимидин) состоит из основания (тимина) и сахара дезоксирибозы. В антиметаболите один из компонентов имеет аномальную структуру. Аномальный нуклеозид после присоединения трех фосфатных групп блокирует дальнейший синтез ДНК.
Идоксуридин и аналогичные соединения встраиваются в ДНК и повреждают ее. Синтез ДНК человека при этом также нарушается, поэтому данные препараты применяют только местно (например, при герпетическом кератите).
Ацикловир является самым эффективным препаратом среди вирусостатических антиметаболитов и лучше всех переносится. Ацикловир активируется только в инфицированных клетках, блокируя в них синтез вирусной ДНК.
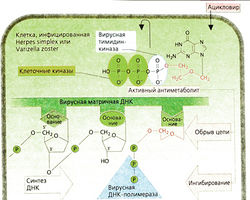
1. Первый этап фосфорилирования осуществляет тимидинкиназа, имеющаяся только у вируса Herpes simplex и Varicella zoster,; две другие фосфатные хруппы переносят клеточные киназы.
2. Трифосфат ацикловира как полярное соединение не может проникать через мембраны и накапливается в инфицированной клетке.
3. Трифосфат ацикловира воспринимается вирусной ДНК-полимеразой в качестве субстрата, происходит ингибирование фермента, а также обрыв цепи вирусной ДНК, так как отсутствует З’-гидроксигруппадезоксирибозы, необходимая для присоединения последующих нуклеотидов. Ацикловир высокоэффективен при тяжелых герпетических инфекциях (например, энцефалите, генерализованной инферкции) и инфекциях, вызванных вирусом Varicella zoster (например, тяжелые формы опоясывающего лишая). В этих случаях ацикловир назначается внутривенно. Препарат может также применяться перорально, однако всасывание происходит не полностью (15-30%). Кроме того, имеются лекарственные формы для местного применения. Ацикловир не действует на ДНК человека, не вызывает угнетения костного мозга. Препарат выводится почками в неизмененном виде.
В валацикловире гидроксильная группа связана эфирной связью с аминокислотой L-валином. Благодаря этому всасывание увеличивается в два раза по сравнению с ацикловиром. В стенке кишечника и в печени остаток валина отщепляется эстеразами, и в результате образуется ацикловир.
Фамцикловир — антигерпетическое пролекарство (действующее вещество пенцикловир), обладает хорошей биодоступностью при пероральном применении.
Ганцикловир применяется для инфузионного введения при тяжелых инфекциях, вызванных цитомегаловирусом (относится к группе вирусов герпеса). Механизм действия не связан с тимидинкиназой. Препарат не очень хорошо переносится: нередко наблюдается лейкопения и тромбоцитопения. Вводится инфузионно или перорально в форме валинового эфира (вал ганцикловир).
Фоскарнет представляет собой аналог дифосфата. При встраивании нуклеотида в ДНК отщепляется дифосфатный остаток. Фоскарнет блокирует ДНК-полимеразу, поскольку он конкурирует за места связывания дифосфатных остатков. Показания: системное лечение тяжелой формы цитомегаловирусной инфекции, СПИДа, местное лечение герпетической инфекции.
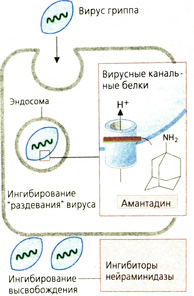
Средства против гриппа. Амантадин специфически блокирует размножение вируса гриппа А (РНК-вирус, возбудитель истинного гриппа). Вирусы попадают в клетку путем эндоцитоза. Для высвобождения РНК необходимо, чтобы из кислого содержимого эндосом протоны попадали внутрь вируса. Амантадин блокирует канал в вирусной оболочке, через который проходят протоны. Поэтому «раздевание» вируса становится невозможным. Препарат применяется для профилактики, иногда для уменьшения симптомов заболевания. Амантадин является также противопаркинсоническим средством.
Ингибиторы нейраминидазы препятствуют высвобождению вирусов гриппа А и В. Вирусная нейраминидаза отщепляет N-ацетилнейраминовую (сиаловую) кислоту от поверхности клетки и таким образом помогает вирусной частице отделиться от клетки-мишени. Занамивир применяется ингаляционно, озелтамивир назначают перорально, так как этот эфир является предшественником действующей формы лекарства. Возможные области применения — лечение и профилактика гриппа.
История противовирусных средств[править | править код]
Источник:
Клиническая фармакология по Гудману и Гилману том 3.
Редактор: профессор А.Г. Гилман Изд.: Практика, 2006 год.
За последние десять лет появилось много новых противовирусных препаратов — большинство из них для борьбы с ВИЧ-инфекцией и ее осложнениями (Hayden, 2000; Balfour, 1999). В настоящей главе собраны сведения о препаратах, применяемых для лечения инфекций, вызванных ДНК- и РНК-содержащими вирусами. Препараты, действующие на ретровирусы, в частности на ВИЧ, рассмотрены отдельно (гл. 51). Многие противовирусные препараты избирательно действуют на один из этапов вирусной инфекции и жизненного цикла вирусов. Здесь же рассматриваются и интерфероны — цитокины, обладающие противовирусным, иммуномодулирующим и антипролиферативным эффектом. Особое внимание уделено препаратам, действующим на герпесвирусы и вирусы гриппа. Обсуждаются также вопросы эффективности противовирусной терапии и устойчивости вирусов. Многие противовирусные препараты являются аналогами пуриновых и пиримидиновых нуклеозидов.
Все вирусы содержат одно- или двухцепочечную РНК или ДНК, заключенную в белковую оболочку — капсид. У некоторых вирусов есть также внешняя оболочка из липопротеидов, на поверхности которой, как и на поверхности капсида, могут располагаться белковые антигены. Большинство вирусов содержат ферменты (или гены для их синтеза), необходимые для репродукции в клетке-хозяине. У вирусов нет собственного обмена веществ, и они используют метаболические пути клетки-хозяина, которой может служить бактерия, клетка растения или животного. Более глубокое изучение жизненного цикла вирусов позволит создать новые противовирусные препараты, действующие на ту или иную его стадию (табл. 50.1). Противовирусные средства должны избирательно подавлять синтез вирусных (но не клеточных) нуклеиновых кислот и белков. В настоящей главе представлены сведения о противовирусной активности, фармакокинетике и клиническом применении отдельных противовирусных препаратов. Те из них, которые прошли клинические испытания и разрешены к применению, перечислены в табл. 50.2.
На рис. 50.1 схематически показаны циклы репродукции ДНК- и РНК-содержащих вирусов. К ДНК-содержащим вирусам относятся поксвирусы (натуральная оспа), герпесвирусы (ветряная оспа, опоясывающий лишай), аденовирусы (вирусный конъюнктивит и фарингит), гепаднавирусы (гепатит В) и вирус папилломы человека (бородавки и остроконечные кондиломы). Геном большинства ДНК-содержащих вирусов транскрибируется в ядре клетки-хозяина при участии ее РНК-полимеразы, при этом сначала на вирусной ДНК синтезируется мРНК, затем происходит трансляция мРНК и синтез вирусных белков. Исключение составляют поксвирусы, у которых есть собственная РНК-полимераза, поэтому их репродукция может происходить в цитоплазме клетки-хозяина.
РНК-содержащие вирусы либо синтезируют мРНК с помощью собственных ферментов, либо функции мРНК начинает выполнять вирусная РНК. На ней синтезируются вирусные белки, в том числе РНК-полимераза, под действием которой затем образуется собственная мРНК вируса (рис. 50.1, Б). Транскрипция генома некоторых РНК-содержащих вирусов, например вируса гриппа, происходит только в ядре клетки-хозяина. К РНК-содержащим вирусам относятся вирус краснухи, рабдовирусы (бешенство), пикорнавирусы (полиомиелит, менингит, острые респираторные вирусные инфекции), аренавирусы (менингит, лихорадка Ласса), арбовирусы (желтая лихорадка, арбовирусные энцефалиты), ортомиксовирусы (грипп) и парамиксовирусы (корь, эпидемический паротит).
Таблица 50.1. Препараты, действующие на разных стадиях вирусной инфекции
|
Стадии вирусной инфекции |
Препараты и их механизм действия |
|
Заражение |
Растворимые ложные рецепторы; антитела к мембранным рецепторам; ингибиторы слияния вируса с клеточной мембраной |
|
Адсорбция на клеточной мембране | |
|
Проникновение в клетку | |
|
Раздевание |
Блокаторы ионных каналов; стабилизаторы капсида |
|
Высвобождение нуклеиновой кислоты | |
|
Транскрипция вирусного генома* |
Ингибиторы вирусных ДНК-полимераз, РНК-полимераз, обратной транскриптазы, геликазы, праймазы, интегразы |
|
Транскрипция вирусной мРНК | |
|
Репликация вирусного генома | |
|
Трансляция вирусных белков |
Интерфероны; антисмысловые олигонуклеотиды, рибозимы |
|
Регуляторные белки (ранние) |
Ингибиторы регуляторных белков |
|
Структурные белки (поздние) |
Нет |
|
Посттрансляционные модификации |
Нет |
|
Протеолитическое расщепление |
Ингибиторы протеаз |
|
Присоединение миристиновой кислоты; гликозилирование |
Нет |
|
Сборка вируса |
Интерфероны; ингибиторы структурных белков |
|
Выход из клетки |
Ингибиторы нейраминидазы; противовирусные антитела; цитотоксические лимфоциты |
|
Отпочковывание, лизис клетки |
Зависит от особенностей репродукции данного вируса, но всегда протекает при участии вирусных ферментов.
Особого внимания заслуживает семейство ретровирусов, которые также относятся к РНК-содержащим вирусам. Ретровирусы вызывают такие заболевания, как ВИЧ-инфекция (гл. 51) и Т-клеточный лейкоз-лимфома взрослых (Т-лимфотропный вирус человека типа 1). У этих вирусов есть обратная транскриптаза — фермент, под действием которого на основе вирусной РНК синтезируется комплементарная ей ДНК — провирус, которая затем встраивается в геном клетки-хозяина. В дальнейшем при транскрипции образуется как клеточная РНК, так и мРНК вируса. На вирусной мРНК, в свою очередь, синтезируются вирусные белки для сборки новых вирусов.
При разработке новых противовирусных препаратов были вскрыты некоторые практически значимые общие закономерности.
- Большинство соединений, обладающих противовирусной активностью in vitro, в организме нарушают жизнедеятельность клеток и слишком токсичны для человека.
- Эффективные препараты, как правило, имеют узкий спектр действия, и мишенями их являются отдельные вирусные белки — чаще всего ферменты (полимераза или транскриптаза), участвующие в синтезе нуклеиновых кислот вируса.
- Для появления устойчивости к препарату бывает достаточно замены одной пары нуклеотидов, приводящей к изменению аминокислотной последовательности в вирусном белке-мишени. Отбор штаммов вируса, устойчивых к тому или иному препарату, свидетельствует об избирательности действия этого препарата.
- Современные препараты подавляют репродукцию вируса, но после их отмены вирус может вновь начать размножаться. В связи с этим при вирусных инфекциях важнейшую роль играет иммунный ответ; лечение может оказаться безрезультатным как при появлении устойчивых штаммов вируса, так и при тяжелых нарушениях иммунитета. Устойчивые штаммы (например, герпесвирусы, ВИЧ-1) выделяют в основном от больных с ослабленным иммунитетом и активной репродукцией вируса, которые получали повторные или продолжительные курсы противовирусной терапии. Исключение составляет вирус гриппа, геном которого и сам по себе характеризуется высокой изменчивостью.
- На вирусы, находящиеся в латентном состоянии, современные препараты не действуют, хотя некоторые из этих препаратов способны в течение длительного времени сдерживать рецидив заболевания.
- Эффективность препарата определяется его концентрацией в клетках, которая должна быть достаточно высокой, чтобы подавить репродукцию вирусов. Например, аналоги нуклеозидов начинают действовать только после их захвата клетками и фосфорилирования, поэтому эффективность лечения зависит от концентрации необходимых ферментов и конкурирующих субстратов, а следовательно, от типа клетки и особенностей ее метаболизма.
- Пробы на чувствительность к противовирусным препаратам in vitro не стандартизованы, и их результат зависит от метода анализа, типа клеток, штамма вируса и лаборатории. Поэтому для большинства противовирусных средств не установлено четких закономерностей между эффективной концентрацией in vitro, концентрацией в крови и других биологических жидкостях и клинической эффективностью.
Таблица 50.2. Разрешенные к применению противовирусные препараты
|
Препарат |
Синонимы |
Путь введения |
|
Препараты, действующие на герпесвирусы | ||
|
Ацикловир Валацикловир Видарабин Ганиикловир Докозанол Идоксуридин Пенцикловир Трифлурндин Фамцикловир Фомивирсен Фос карнет Цидофовир |
ACV, ациклогуанозин АраА, аденин арабинозид GCV, DHPG IDUR PCV TFT, трифтортимидин FCV ISIS-2922 PFA, фос фоноформат НРМРС |
В/в; внутрь; М; глазная мазь, глазной крем Внутрь Глазной гель, глазная мазь; в/в* В/в; внутрь; раствор для инъекций в стекловидное тело; глазной гель М Глазная мазь, глазные капли М; в/в* Глазные капли Внутрь Раствор для инъекций в стекловидное тело В/в; внутрь* В/в; М* |
|
Препараты, действующие на вирус гриппа | ||
|
Амантадин Занамивир Озельтамивмр Римантадин |
GC-167 GS-4I04 |
Внутрь Ингаляции Внутрь Внутрь |
|
Прочие противовирусные препараты | ||
|
Имиквимод Интерферон а (а-2а, а-2Ь, а-пЗ; ал ьфакон -1; a-n 1) Ламивудин Пегинтерферон а-2а' Пегинтерферон а-2Ь Рибавирин |
М П/к, в/м, в/в, введение в кондилому Внутрь П/к П/к Внутрь, ингаляции, в/в* | |
Другие противовирусные препараты[править | править код]
Интерфероны[править | править код]
Классификация и противовирусная активность[править | править код]
Интерфероны — это мошные цитокины, обладающие противовирусным, иммуномодулируюшим и антипролиферативным действием (Baron et ai., 1992; см. также гл. 53). Они синтезируются клетками под воздействием различных факторов и запускают биохимические механизмы защиты клеток того же вида животных от вирусов. В ор ганизме человека вырабатываются три группы интер. феронов, обладающих противовирусным действием- а(более 18 представителей), бета и у. Применяемые в клинической практике рекомбинантные интерфероны а -это негликозилированные белки с молекулярной массой около 19 500 (табл. 50.2).
Синтез интерферонов аир может идти почти во всех клетках. Пусковыми стимулами для образования интерферонов могут служить вирусы, двухцепочечная РНК некоторые цитокины (в том числе ИЛ-1, ИЛ-2, ФНО) другие факторы. Интерферон у вырабатывается только Т- и NK-лимфоцитами при их стимуляции антигенами митогенами и некоторыми цитокинами. Функции интерферонов а и р разнообразны: они обладают противовирусным и антипролиферативным действием; усиливают цитотоксическую активность Т-лимфоцитов, NK-лим-фоцитов и макрофагов; повышают экспрессию антигенов HLA класса I и других поверхностных антигенов. Интерферон у менее активен в отношении вирусов, но оказывает более сильное иммуномодулирующее действие: активирует макрофаги, стимулирует экспрессию антигенов HLA класса II и опосредует местные воспалительные реакции.
Интерфероны подавляют репродукцию большинства вирусов животных, но на многие ДНК-содержащие вирусы действуют слабо. Данные о противовирусной активности интерферонов сильно различаются в зависимости от вируса и метода анализа. Биологическую активность интерферонов определяют обычно по их противовирусному действию в культуре клеток и выражают в международных единицах (ME) в соответствии с общепринятыми стандартами.
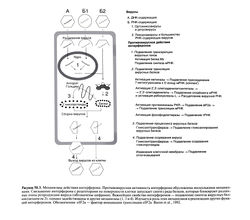
Механизм действия[править | править код]
Связывание интерферонов со специфическими клеточными рецепторами активирует внутриклеточную передачу сигнала, в которой участвуют Янус-киназы и факторы транскрипции STAT. В результате комплекс белков STAT отщепляется от рецептора и перемещается в клеточное ядро, где взаимодействует с генами, несущими интерферон-чувствительный регуляторный элемент. Тем самым запускается синтез более двух десятков белков, действие которых направлено на подавление вируса (Stark etal., 1998; рис. 50.3). Интерфероны действуют на все основные этапы репродукции вируса: проникновение в клетку и раздевание, синтез вирусной мРНК, трансляцию вирусных белков, сборку и выход вируса из клетки. Самое грозное для многих вирусов свойство интерферонов — подавление синтеза вирусных белков. Интерфероны индуцируют выработку 2',5'-олигоаденилат-синтетаз и протеинкиназы PKR. В присутствии двухцепочечной РНК под действием 2',5'-олигоаденилатсинтетаз образуются 2',5'-олигоаденилаты, которые, в свою очередь, активируют рибонуклеазу L, расщепляющую как вирусные, так и клеточные одноцепочечные РНК. Протеинкиназа PKR избирательно фосфорилирует и тем самым блокирует фактор инициации трансляции eIF2a, без которого невозможен синтез вирусных белков. Кроме того, она может запускать апоптоз. Интерфероны индуцируют также фосфодиэстеразу, которая отщепляет часть молекулы тРН К, что препятствует элонгации полипептидной цепи. В зависимости от вида вируса интерфероны могут действовать на различных этапах его репродукции. Некоторые вирусы способны подавлять выработку индуцируе мых интерферонами ферментов или снижать их активность. Так, один из механизмов устойчивости вируса гепатита С к интерферонам обусловлен способностью этого вируса подавлять протеинкиназу PKR (Francois et al., 2000).
Между интерферонами и другими компонентами иммунной системы существуют сложные взаимодействия. Интерфероны могут действовать на вирус напрямую или опосредованно — за счет изменения иммунного ответа. Например, повышая экспрессию антигенов HLA, они стимулируют лизис зараженных клеток цитотоксическимиТ-лимфоцитами. Помимо собственно противовирусного действия интерфероны участвуют в некоторых общих реакциях организма на вирусную инфекцию, в том числе в патологических иммунных реакциях, сопровождающихся повреждением тканей.
фармакокинетика[править | править код]
При приеме интерферонов внутрь обнаружить их в плазме не удается, а уровень 2',5'-олигоаденилатсинтетазы в лимфоцитах почти не повышается (Wills, 1990). Зато при в/м или п/к введении интерферон а всасывается более чем на 80%. Сывороточная концентрация интерферона а зависит от дозы; через 4—8 ч после введения она достигает максимума, а через 18—36 ч возвращается к исходному уровню. При однократном введении уровень 2',5'-олигоаденилатсинтетазы в лимфоцитах крови (показатель биологической активности интерферона) начинает возрастать через 6 ч и остается выше исходного уровня в течение 4 сут. Через 24 ч после введения интерферона а противовирусная активность лимфоцитов крови становится максимальной, а затем медленно (в течение 6 сут) возвращается к исходному уровню. Всасывание интерферона у при в/м или п/к введении менее постоянно, а сывороточная концентрация интерферона при таком введении невелика, хотя уровень 2',5'-олигоаденилатсинтетазы в лимфоцитах крови может повышаться. Объем распределения интерферона а составляет в среднем 31л. При системном применении низкие концентрации интерферона о обнаруживают в секретах дыхательных путей, СМЖ, водянистой влаге и головном мозге.
Поскольку действие интерферонов длится достаточно долго, то судить о нем на основании обычных фармакокинетических показателей сложно. При в/в введении динамика элиминации интерферона а из плазмы сложна и описывается несколькими экспоненциальными функциями (Bocci, 1992). Т1/2 интерферона а составляет около 40 мин, а рекомбинантных интерферонов Риу — около 4 ч и 30 мин соответственно. Элиминация интерферонов из плазмы зависит от их распределения в организме, захвата клетками и распада, который происходит главным образом в печени и почках. С мочой выводится лишь очень незначительное количество интерферонов.
Присоединение к интерферонам инертного полимера поли-этиленгликоля значительно замедляет их элиминацию из плазмы. Получаемые при этом интерфероны длительного действия (конъюгированные интерфероны, или пегинтерфероны) можно вводить всего 1 раз в неделю. Кроме того, присоединение полиэтиленгликоля снижает иммуногенность белковых препаратов. С ростом молекулярной массы полиэтиленгликоля возрастает Т1/2 препарата, уменьшаются его почечный клиренс и относительная противовирусная активность. В крупных клинических испытаниях изучена эффективность двух конъюгированных интерферонов. Пегинтерферон а-2Ь получен присоединением к интерферону а-2Ь линейной молекулы полиэтиленгликоля с молекулярной массой 12000. Т1/2 такого препарата увеличен с 2—3до54ч (Glueetal., 2000). Пегинтерферона-2а содержит эфир разветвленного полиэтиленгликоля с молекулярной массой 40 000; его Т1/2 еще выше — в среднем 77 ч. Около 70% пегинтерферона а-2Ь и большая часть пегинтерферона а-2а элиминируются путем печеночного метаболизма. Побочные эффекты. Через несколько часов после введения интерферонов (в дозе 1—2 млн МЕ и больше) часто возникает гриппоподобный синдром с лихорадкой, ознобом, головной болью, миалгией, артралгией, тошнотой, рвотой и поносом (Dus-heiko, 1997). Лихорадка обычно длится не более 12 ч, при приеме жаропонижающих препаратов перед введением интерферона она выражена слабее. В большинстве случаев со временем переносимость интерферона улучшается. Гриппоподобное состояние, неприятные ощущения в месте инъекции и лейкопения возникали почти у половины больных с остроконечными кондиломами при введении интерферона в кондилому.
При системном применении интерферон может вызывать угнетение кроветворения (нейтропению и тромбоцитопению), нарушения со стороны ЦНС (сонливость, спутанность сознания, изменение поведения, редко — эпилептические припадки), тяжелую астению с повышенной утомляемостью и потерей веса, аутоиммунные нарушения (в том числе хронический лимфоцитарный тиреоидит), реже — сердечно-сосудистые нарушения (артериальную гипотонию и тахикардию). Эти побочные эффекты препятствуют повышению дозы. Иногда отмечаются повышение активности печеночных ферментов и уровня триглицеридов в крови, алопеция, протеинурия и азотемия, интерстициальный нефрит, образование аутоантител. У детей при лечении интерфероном нередко возникают изменения личности и алопеция (Sokal et al., 1998). Изредка при введении интерферонов к ним вырабатываются нейтрализующие антитела, и тогда дальнейшее лечение становится бесполезным (Antonelli et al., 1991). Введение интерферонов может отрицательно сказываться на репродуктивной функции. Их безопасность при беременности не установлена.
Интерфероны замедляют инактивацию некоторых препаратов (например, теофиллина) микросомальными ферментами печени. В результате сывороточная концентрация таких препаратов повышается. Угнетение кроветворения, вызванное другими препаратами (например, зидовудином), на фоне введения интерферонов может усиливаться.
Переносимость конъюгированных интерферонов не хуже, чем обычных: отменять лечение приходится в 6—11% случаев. Тем не менее, по данным некоторых исследований, конъюгированные интерфероны несколько чаще вызывают лихорадку, тошноту и воспалительную реакцию в месте инъекции. Не ясно пока, представляет ли опасность накопление и длительное пребывание полиэтиленгликоля в организме.
Применение[править | править код]
В США разрешены рекомбинантные, природные и конъюгированные интерфероны а (табл. 50.2). Их используют для лечения остроконечных кондилом, хронических гепатитов С и В,саркомы Капошиу ВИЧ-инфицированных, злокачественных новообразований, рас сеянного склероза.
Гепатит В. При парентеральном введении интерферо. нов у 25—50% больных хроническим гепатитом В исчезают вирусная ДНК и HBeAg (е-антиген вируса гепатита В), начинается выработка антител к HBeAg, улучшаются биохимические показатели функции печени и гистологическая картина (Haria and Benfield, 1995; Main and Thomas, 1997). Длительная ремиссия возможна лишь при продолжительном назначении интерферона а-2Ь в довольно высоких дозах (обычно 5 млн МЕ/сут или 10 млн МЕ 3 раза в неделю взрослым и 6 млн МЕ/мг Зраза в неделю детям п/к или в/м в течение 4—6 мес) (Sokal et al., 1998). У большинства больных уровень вирусной ДНК и активность ДНК-полимеразы в плазме быстро снижаются, но перестают они определяться только в 30% случаев. Хорошие прогностические признаки — низкий уровень вирусной ДНК и высокая активность аминотрансфераз до лечения. При вертикальном пути передачи инфекции, наличии в крови антител к HBeAg и снижении иммунитета (например, при сопутствующей ВИЧ-инфекции) вероятность длительной ремиссии ниже. На 2— 3-м месяце лечения может наступить сероконверсия (исчезает HBeAg и появляются антитела к нему). Часто при этом повышается активность аминотрансфераз и возникает синдром, сходный с гепатитом, — эти изменения по-видимому, связаны с разрушением иммунной системой зараженных гепатоцитов. При тяжелой печеночной недостаточности интерферон в высоких дозах может угнетать кроветворение, что ухудшает состояние больного.
При лечении интерфероном длительной ремиссии удается достичь более чем у 80% больных хроническим гепатитом В. При этом часто исчезает HbsAg (поверхностный антиген вируса гепатита В), улучшается или стабилизируется гистологическая картина, снижается частота печеночных осложнений и летальность (Lau et al., 1997). В ряде случаев интерферон помогает при нефротическом синдроме и гломерулонефрите, возникающем на фоне хронического гепатита В. При хроническом гепатите D интерферон эффективен в 50% случаев, однако если в плазме сохраняется HbsAg, то почти всегда возникают рецидивы (Farci et al., 1994). При остром гепатите В или D интерферон малоэффективен.
Гепатит С. При монотерапии хронического гепатита С интерфероном а-2Ь (3 млн МЕ п/к 3 раза в неделю) активность аминотрансфераз в 50—70% случаев снижается до нормы и из плазмы исчезает вирусная РНК. Тем не менее частота рецидивов высока, и при лечении интерфероном в течение 6 мес длительной ремиссии удается добиться лишь у 10—25% больных (Main and Thomas, 1997). При введении интерферона в течение 12—18 меси, возможно, при назначении его в более высоких дозах вероятность длительной ремиссии выше. Длительная ремиссия сопровождается устойчивым улучшением гистологической картины и, возможно, снижением риска печеночноклеточного рака (Yoshida et al., 1999). Результат лечения зависит от генотипа вируса и уровня вирусной РНК до начала лечения. Раннее исчезновение вируса-хороший прогностический признак (Civeira and Prieto,1999). Если через 3 мес от начала лечения вирусная РНК не определяется, то введение интерферона следует продолжать еше 12 мес или даже дольше (Gish, 1999).
У ранее нелеченных больных при лечении конъюгированными интерферонами длительная ремиссия наступает чаше, чем при лечении обычными интерферонами по стандартной схеме (3 раза в неделю п/к). Так, при лечении пегинтерфероном а-2а (180 мг п/к 1 раз в неделю в учение 48 нед) длительная ремиссия наступала в 2 раза чаше (Zeuzem et al., 2000), в том числе у больных с хроническим гепатитом С, осложненным циррозом печени /Heathcote et al., 2000). Эффективность пегинтерферона а-2Ь зависит от дозы, вводить его рекомендуется из расчета 1,5 мкг/кг/нед. Проводятся широкомасштабные исследования лечения гепатита С конъюгированными ин-терферонэми в сочетании с рибавирином. По предварительным данным, эффективность препаратов при этом возрастает, а частота длительных ремиссий превышает 50% (Manns et al., 2000). Изучают и эффективность поддерживающей терапии (в течение 4 лет) конъюгированными интерферонами.
Если монотерапия интерфероном не дала результата, назначать ее повторно не имеет смысла. Однако введение интерферона совместно с рибавирином может оказаться эффективным (см. ниже). При рецидиве может помочь повторный курс интерферона, но еще более эффективно одновременное назначение рибавирина. Интерферон может принести улучшение при криоглобулинемии и гломерулонефрите, развившихся на фоне гепатита С, а при остром гепатите С — снизить риск хрониза-ции.
Инфекции, вызываемые вирусом папилломы человека. При устойчивых к лечению остроконечных кондиломах применяют различные природные и рекомбинантные интерфероны. Их введение непосредственно в кондиломы приводит к полному излечению у 36—62% больных (Frazer and McMillan, 1997). Рецидивы возникают у 20—30% больных, получавших интерфероны. Такой путь введения применяют и при лечении простых бородавок интерферонами а. При в/м или п/к введении интерферонов бородавки уменьшаются, но побочные эффекты при этом более выражены. Показано также, что при назначении интерферонов в/м или п/к одновременно с введением их в бородавки частота наступления полной ремиссии не возрастает. Системное применение интерферонов может послужить хорошим дополнением к лечению папил-ломатоза гортани как у детей младшего возраста, так и у взрослых.
Другие вирусные инфекции. Установлено, что интерфероны эффективны при инфекциях, вызванных герпесвиру-сами, в том числе герпесе половых органов; опоясывающем лишае (с ограниченными высыпаниями) при злокачественных новообразованиях и у пожилых больных; цитомегаловирусной инфекции у реципиентов почек. Однако по сравнению с традиционными противовирусными препаратами интерферон обычно действует слабее и дает больше побочных эффектов. При герпесе кожи и слизистых, устойчивом к препаратам, действующим на герпесвирусы, может быть эффективным местное применение интерферона с трифлуридином (Birch et al., 1992).
При ВИЧ-инфекции интерфероны оказывают антиретровирусное действие. Однако на поздних стадиях заболевания интерферон в сочетании с зидовудином давал лишь временное улучшение и вызывал выраженное угнетение кроветворения. Интерферон а (3 млн МЕ п/к 3 раза в неделю) эффективен при иммунной тромбоцитопе-нии, развившейся на фоне ВИЧ-инфекции и не поддающейся лечению зидовудином (Marroni et al., 1994).
In vitro интерфероны действуют почти на все респираторные вирусы, за исключением аденовирусов. Однако закапывание интерферона а в нос оправдано лишь для профилактики риновирусной инфекции, причем длительное применение ограничено побочными эффектами со стороны слизистой носа. При развившейся риновирусной инфекции такое лечение не помогает.
Ламивудин[править | править код]
Ламивудин — левовращающий изомер 2\3'-дидезокси-3'-тиацитидина — нуклеозидный аналог, ингибирующий обратную транскриптазу ВИЧ и ДНК-полимеразу вируса гепатита В. Применение его в качестве антиретровирусного средства подробно описано в гл. 51. В концентрациях 4—7 нг/мл он подавляет репродукцию вируса гепатита В in vitro на 50%, почти не оказывая цитотоксического действия. Под действием клеточных ферментов ламивудин превращается в ламивудинтрифосфат, который конкурентно ингибирует ДНК-полимеразу вируса гепатита В и останавливает репликацию его ДНК. T1/2 ламиву-динтрифосфата в инфицированных клетках составляет 17—19 ч, поэтому ламивудин можно принимать с большими интервалами.
Концентрации, в которых ламивудин эффективен в отношении устойчивых штаммов, превышают концентрации для чувствительных штаммов в 40—10 000 раз. Устойчивость штаммов, выделенных от больных, получавших лечение ламивудином, обусловлена мутациями вирусной ДНК-полимеразы — в основном за счет замен аминокислот в положениях 526—528 и 550—552 на участке Тир—Мет—Асп—Асп (YMDD). Некоторые из мутантных штаммов размножаются in vitro медленнее, чем дикие, у других репродукция прекращается в отсутствие лами-вудина (Yeh et al., 2000).
При приеме внутрь ламивудин быстро всасывается; у взрослых биодоступность составляет 80% (Johnson et al., 1999). Максимальная сывороточная концентрация достигается через 0,5— 1,5 ч после приема и при дозе 100 мг составляет в среднем 1000 нг/мл. У детей с гепатитом В сходную сывороточную концентрацию дает прием 3 мг/кг ламивудина 1 раз в сутки (Sokal et al., 2000). Объем распределения ламивудина приближается к общему объему жидкости в организме. Т1/2 составляет в среднем 9 ч; около 70% принятой дозы выводится с мочой в неизмененном виде. Около 5% метаболизируется с образованием неактивного транс-сульфоксида. При умеренной почечной недостаточности (СКФ < 50 мл/мин) дозу уменьшают. При одновременном приеме триметоприма выведение ламивудина замедляется.
При хроническом гепатите В длительный прием ламивудина (100 мг/сут в течение года и более) приводит к снижению уровня вирусной ДНК (обычно более чем на 2 порядка), нормализации биохимических показателей функции печени и улучшению гистологической картины (Lai etal., 1998; Dienstag etal., 1999).Однако сероконверсия (HBeAg исчезает, и появляются антитела к нему) наступает лишь у меньшей части больных, хотя и может сохраняться довольно долго. В большинстве же случаев после отмены ламивудина виремия возникает вновь, иногда — с обострением гепатита. При декомпенсированном циррозе печени ламивудин может отдалить необходимость трансплантации. Эффективность ламивудина в сочетании с интерфероном а не выше, чем при лечении каждым препаратом в отдельности, хотя в случае комбинации сероконверсия возникает чаще, и, возможно, реже возникает устойчивость (Schalm et al., 2000).
У 14—32% больных с нормальным иммунитетом через год лечения ламивудином (100 мг/сут) обнаруживают устойчивые штаммы вируса, а в крови вновь появляется вирусная ДНК. Через 3 года этот показатель возрастает до 50% и выше. Клиническое значение мутаций, приводящих к устойчивости, изучается. Появление устойчивых штаммов часто протекает бессимптомно, но может сопровождаться изменением биохимических показателей функции печени и ухудшением состояния больного. Несмотря на более высокие дозы (300 мг/сут), устойчивость к ламивудину часто возникает и при лечении гепатита В у ВИЧ-инфицированных. При лечении гепатита В у реципиентов печени также нередко обнаруживают устойчивые штаммы — иногда при этом ухудшается гистологическая картина.
Рибавирин[править | править код]
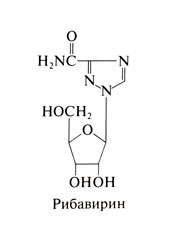
Строение и противовирусная активность[править | править код]
Рибавирин, или 1-/3-D-рибофуранозил-1Н-1,2,4-триазол-3-карбоксамид, — это синтетический аналог пуриновых нуклеозидов, в котором модифицированы азотистое основание и остаток D-рибозы. Его структурная формула следующая:
Рибавирин подавляет репродукцию многих РНК- иДНК-содержаших вирусов, в том числе ортомиксовирусов, парамиксовирусов, аренавирусов, буньявирусов, флавивирусов, герпес-вирусов, аденовирусов, поксвирусов и ретровирусов (Gilbert [and Knight, 1986; Huggins, 1989). In vitro на вирусы гриппа, парагриппа и респираторный синцитиальный вирус рибавирин действует в концентрациях 3—10 мкг/мл. Он обратимо подавляет синтез нуклеиновых кислот и пролиферацию неинфицированных клеток, угнетает иммунный ответ (Heagy et al., 1991) и нарушает выработку цитокинов in vitro.
Механизм действия и устойчивость[править | править код]
Механизм противовирусного действия рибавирина точно не установлен, но очевидно, что он препятствует синтезу гуаниновых нуклеотидов и вирусной мРНК (Gilbert and Knight, 1986). Под действием клеточных ферментов рибавирин фосфорилируется до моно-, ди-, а затем трифосфата. В свободных от вирусов и инфицированных респираторным синцитиальным вирусом клетках рибавирин содержится главным образом в виде трифосфата (> 80%). Т1/2 последнего внутри клетки составляет менее 2 ч.
Конкурентно ингибируя клеточную И МФ-дегидрогеназу, ри-бавиринмонофосфат препятствует синтезу ГТФ и, тем самым — синтезу нуклеиновых кислот в целом. Рибавиринтрифосфат (тоже конкурентно) ингибирует присоединение 7-метилгуано-зина к 5'-концу вирусной мРНК (кэппинг), а у вируса гриппа он замедляет транскрипцию. По-вндимому, существует несколько мишеней рибавирина, причем действие на одну из них (например, на синтез ГТФ) может повлечь действие на другие (например, на ГТФ-зависимые ферменты).
Устойчивые к рибавирину штаммы вирусов пока не выделены, хотя in vitro удавалось получить клетки, в которых рибавирин не фосфорилировался до активных метаболитов. Фармакокинетика. Рибавирин активно всасывается с участием нуклеозидных переносчиков в проксимальном отделе тонкой кишки. Биодоступность его при приеме внутрь составляет в среднем около 50% (Glue, 1999). Сывороточная концентрация рибавирина возрастает постепенно, достигая стационарного состояния к 4-й неделе лечения. Целесообразно принимать рибавирин во время еды, так как при этом сывороточная концентрация его заметно повышается (Glue, 1999). При приеме 600 и 1200 мг рибавирина максимальная сывороточная концентрация составляет соответственно 0,8 и 3,7 мкг/мл; при введении 500 и 1000 мг препарата в/в сывороточная концентрация равна в среднем 17 и 24 мкг/мл. При ингаляциях сывороточная концентрация зависит от длительности лечения, достигая к 5-м суткам 0,2—1 мкг/мл (Englundetal., 1994). Концентрация рибавирина в секретах дыхательных путей намного выше сывороточной, но непостоянна — значения ее могут различаться в 1000 раз.
За счет захвата рибавирина клетками объем его распределения довольно велик (около 10 л/кг). С белками плазмы он почти не связывается. Элиминация рибавирина сложна: при однократном приеме Т|/2 в плазме составляет в среднем 30—40ч,но по достижении стационарного состояния увеличивается до 200—300 ч. Рибавиринтрифосфат накапливается в эритроцитах после отмены рибавирина концентрация трифосфата в эритроцитах постепенно падает с Т1/2 около 40 сут. Основные пути элиминации — печеночный метаболизм и почечная экскреция В печени от рибавирина отщепляется рибоза, затем оставшийся триазолкарбоксамид гидролизуется с образованием триазоль-ного карбоксильного метаболита. В дальнейшем и сам рибавирин, и его метаболиты выводятся с мочой. При тяжелой почечной недостаточности (СКФ 10—30 мл/мин) клиренс рибавирина уменьшается втрое. При СКФ < 50 мл/мин препарат следует принимать с осторожностью.
Побочные эффекты[править | править код]
Ингаляции рибавирина могут вызвать сыпь конъюнктивит, преходящий бронхоспазм, иногда — обратимое нарушение функции внешнего дыхания. При назначении ингаляций во время ИВЛ нужно помнить, что рибавирин может оседать на клапанах и закупоривать трубки. Поэтому во время ингаляции необходимо наблюдать за состоянием больного и следить за исправностью аппарата. Не менее важно и предусмотреть меры по защите медицинских работников от вынужденного вдыхания рибавирина (Shults et al., 1996).
При системном применении рибавирин вызывает дозозависимую обратимую анемию за счет внесосудистого гемолиза и угнетения кроветворения (Huggins, 1989). При этом повышается содержание ретикулоцитов в крови, возрастают уровни билирубина, железа и мочевой кислоты. В высоких концентрациях рибавиринтрифосфат может повреждать мембраны эритроцитов за счет свободнорадикального окисления, что приводитк эритрофагоцитозу клетками ретикулоэндотелиальной системы (De Franceschi et al., 2000). При в/в струйном введении рибави рина возможен потрясающий озноб. Около 20% больных хро ническим геЛатитом С, получающих рибавирин в сочетании интерфероном а, из-за побочных эффектов вынуждены пре кратить прием препаратов на раннем этапе. Вдобавок к побоч ным эффектам самого интерферона при комбинированной те рапии чаше возникают утомляемость, кашель, сыпь, зуд, тош нота, бессонница, одышка, подавленное настроение и — восо бенности — анемия. Из-за последней в 8% случаев дозу рибави рина приходится уменьшать.
Поданным доклинических испытаний, рибавирин оказыва ет тератогенное, эмбриотоксическое, канцерогенное и, возмож но, гонадотоксическое действие. После длительного курса лечения тератогенное действие рибавирина сходит на нет лишь через 6 мес после отмены, когда препарат полностью выводится из организма (Glue, 1999). По классификации лекарственных средств, применяемых во время беременности (ФДА), рибавирин относится к категории X, то есть к абсолютно противопоказанным препаратам. Беременных медсестер и врачей не допускают к работе с больными, получающими ингаляции рибавирина.
In vitro рибавирин подавляет фосфорилирование и противовирусную активность аналогов пиримидиновых нуклеозидов (например, зидовудина и ставудина), действующих на обратную транскриптазу ВИЧ. Вместе с тем он усиливает активность пуриновых ингибиторов обратной транскриптазы (например, диданозина).
Применение[править | править код]
В США рибавирин в форме аэрозоля разрешен для лечения госпитализированных детей сбронхио-литом и пневмонией, вызванными респираторным синцитиальным вирусом. Ингаляции рибавирина (20 мг/мл в течение 18 ч I раз в сутки) облегчают некоторые симптомы инфекции; пока не ясно, однако, насколько оправдано его применение. He доказано положительное влияние рибавирина на сроки госпитализации и длительность ИВЛ, а также на смертность и отдаленные последствия со стороны легких (Randolph and Wang, 1996; Long etal., 1997). Менее длительные ингаляции рибавирина в большей дозе (60 мг/мл в течение 2 ч 3 раза в сутки) давали тот же результат, что и ингаляции по стандартной схеме (20 мг/мл в течение 18 ч 1 раз в сутки) (Englund et al., 1994). Рибавирин может быть назначен грудным детям и детям младшего возраста, госпитализированным с тяжелой инфекцией, вызванной респираторным синцитиальным вирусом, а также детям с высоким риском тяжелого течения этой инфекции (в том числе детям с врожденными пороками сердца, хроническими заболеваниями легких, иммунодефицитами, недоношенным и детям младше 6 нед) (Committee on Infectious Diseases, 1996). Есть данные о том, что лечение рибавирином совместно с нормальным иммуноглобулином для в/в введения снижает смертность от инфекции, вызванной респираторным синцитиальным вирусом у реципиентов костного мозга и других больных со сниженным иммунитетом (Ghosh et al., 2000).
Прием рибавирина внутрь в сочетании с п/к введением интерферона а-2Ь эффективен при хроническом гепатите С. При монотерапии рибавирином в течение 6—12 мес у 30% больных временно нормализуются активности аминотрансфераз, но на уровень вирусной РНК такое лечение не влияет. При сочетании интерферона а-2Ь (3 млн МЕ п/к 3 раза в неделю) и рибавирина (по 500 мг, а при весе более 75 кг — по 600 мг внутрь 2 раза в сутки) в течение 24—48 нед вероятность успеха (устойчивое улучшение биохимических показателей функции печени и снижение уровня вирусной РНК) может возрасти до 40%, в зависимости от генотипа вируса (Battaglia and Hagmey-er, 2000). Комбинированное лечение эффективнее и монотерапии интерфероном как у больных, не получавших ранее интерферон (McHutchison and Poynard, 1999), так и у больных, у которых монотерапия оказалась безрезультатной или после отмены интерферона возник рецидив (Barbara et al., 1999). Более длительный курс лечения (48 нед), по-видимому, оправдан при гепатите С, вызванном вирусом с генотипом 1, при высоком уровне вирусной РНКдо начала лечения, атакже при выраженном фиброзе печени. Комбинированную терапию применяли для лечения рецидивов гепатита С после трансплантации печени (Lavezzo and Rizzetto, 1999).
Изредка рибавирин (как в виде ингаляций, так и в/в) назначают при тяжелом гриппе, а также — у больных с ослабленным иммунитетом — при инфекциях, вызванных вирусами осповакцины, парагриппа, кори и аденовирусами. У детей, госпитализированных по поводу гриппа, ингаляции рибавирина уменьшали продолжительность лихорадки, в остальном же на течение заболевания они не влиял и (Rodriguez etal., 1994). Рибавирин в/в снижает летальность при лихорадке Ласса. Его применяли и для лечения других геморрагических лихорадок, вызванных аренавирусами. Рибавирин помогает при геморрагической лихорадке с почечным синдромом, вызванной хантавирусом Хантаан (Huggins et al., 1991). Изучается эффективность рибавирина при хантавирусном легочном синдроме. Рибавирин внутрь применяли для лечения конго-крымской геморрагической лихорадки. В США рибавирин для в/в введения проходит испытания.
Имиквимод[править | править код]
Имиквимод — 1-(2-метилпропил)-1Н-имидазо[4,5-с]хи-нолин-4-амин — новый иммуномодулятор для наружного применения при остроконечных кондиломах (Miller et al., 1999). Не оказывая прямого противовирусного или антипролиферативного действия in vitro, имиквимод стимулирует выработку интерферона а, ФНОа и других цитокинов. В экспериментах на животных показана противовирусная активность имиквимода при местном и системном применении. Имиквимод применяют в виде 5% крема, который наносят непосредственно на кондиломы. Он способствует выработке интерферонов а, Р и у и ФНОа в окружающих тканях, снижению концентрации вирусной ДНК и уменьшению кондилом (Tyring et al.,1998). При применении крема с имиквимодом 3 раза в неделю в течение 16 нед у 50% больных кондиломы исчезали без следа (в половине случаев уже через 8— 10 нед), причем у женщин препарат был более эффективен, чем у мужчин (Slade et al., 1998). После отмены препарата кондиломы нередко появляются вновь. Из побочных эффектов отмечены эритема (у 20% больных), экскориации и шелушение (18—26%), зуд (10—20%), жжение (5—12%) и — реже igэрозии и изъязвление.
Новые противовирусные средства[править | править код]
В табл. 50.5 перечислены противовирусные средства, нахолящиеся на стадии разработки (за исключением препаратов для лечения ВИЧ-инфекции). Наиболее перспективные из них описаны ниже — их испытания почти завершены.
Адефовир[править | править код]
Адефовир — 9-(2-фосфонилметоксиэтил)аденин — аналог аденозина, содержащий фосфонатную группу. Он действует на гепаднавирусы, герпесвирусы и ретровирусы. При гепатите В и ВИЧ-инфекции принимают внутрь адефовира дипивоксил, который под действием эстераз метаболизируется в кишечнике и крови до адефовира. На вирус гепатита В (в том числе на штаммы, устойчивые к ламивудину и фамцикловиру) адефовир in vitro действует в концентрациях 0,2—1,2 мкмоль/л. Под действием клеточных ферментов из адефовира образуется адефовир-дифосфат, избирательно подавляющий вирусные полимеразы. Он медленно выводится из клеток (Т1/2 12—30 ч), поэтому адефовир можно принимать один раз в сутки. Встраиваясь в ДНК, адефовир останавливает ее репликацию. Устойчивые к нему штаммы вируса гепатита В пока не обнаружены.
Сам по себе адефовир всасывается плохо, но благодаря хорошему всасыванию адефовира дипивоксила биодоступность адефовира превышает 50%. Он почти не связывается с белками плазмы, а объем его распределения приближается к общему объему жидкости в организме. При в/в введении кривая сывороточной концентрации адефовира имеет две фазы с конечным Т,/2всреднем 1,6 ч (Cundy etal., 1995а). При приеме внутрь в виде дипивоксила Т, ,2 адефовира составляет 5—7 ч. Адефовир выводится почками в неизмененном виде, при этом на 60% путем канальцевой секреции.
Адефовира дипивоксил может оказывать дозозависимое нефротоксическое действие и нарушать функцию почечных канальцев, что проявляется гипофосфатемией и азотемией. При приеме адефовира в дозе 30 мг/сут и выше нефротоксическое действие развивается лишь через 6—9 мес лечения, но большинство больных хроническим гепатитом В, которым назначали адефовир по 10 мг/сут внутрь, переносили препарат хорошо. У некоторых больных прием адефовира вызывает головную боль,слабость, тошноту и понос. Продукт гидролиза адефовира дипивоксила — пивалиновая кислота — связывает карнитин (с образованием сложного эфира), поэтому прием больших доз адефовира может вызвать дефицит карнитина. Доклинические испытания показали, что у некоторых видов животных большие дозы адефовира оказывали мутагенное и эмбриотоксическое действие, вызывали поражение лимфатической системы, нарушение функции ЖКТ и почечных канальцев, повышение активности аминотрансфераз и КФК.
В дозе 60—120 мг/сут внутрь адефовир эффективен при ВИЧ-инфекции, но из-за токсичности препарата клинические испытания приостановлены. У больных гепатитом В уровень вирусной ДНК снижается и при невысоких дозах адефовира. Изучается эффективность адефовира при хроническом гепатите В (при приеме 10 и 30 мг/сут внутрь). Показано, что in vitro адефовир в сочетании с ламивудином активнее в отношении вируса гепатита В, чем каждый из препаратов в отдельности (Colledge et al., 2000), и в ближайшем будущем начнутся клинические испытания этой комбинации.
Энтекавир[править | править код]
Энтекавир — это циклопентильный аналог гуанозина. Энтекавир активно подавляет репродукцию вируса гепатита В — в культуре клеток печени в концентрациях 3—5 нмоль/л, что примерно в 30 раз ниже, чем для ламивудина (Innaimo et al., 1997). В отношении герпесвирусов активность энтекавира гораздо ниже. Под действием клеточных ферментов из энтекавира образуется энтекавиртрифосфат, который медленно выводится из клеток с Т1/2 около 15 ч. Энтекавиртрифосфат конкурентно ингибирует полимеразу вируса гепатита В, что препятствует началу репликации и элонгации цепи ДНК. Биодоступность энтекавира при приеме внутрь высока; у лабораторных животных он подавлял репродукцию гепаднавирусов даже при приеме в небольших дозах. Лесные сурки, инфицированные гепатитом В, хорошо переносили длительное лечение энтекавиром. По-видимому, энтекавир предотвращал развитие у них печеночноклеточного рака. Больные хроническим гепатитом В, как правило также хорошо переносят короткие курсы энтекавира (0,1—1 внутрь I раз в сутки в течение 28 сут); при этом значительно снижается уровень вирусной Д Н К в плазме (de Man et al., 2000) Клинические испытания препарата продолжаются.
Плеконарил[править | править код]
Плеконарил — 3-[3,5-диметил-4[[3-(3-метил-5-изоксазоил)пропил]окси]фенил]-5-(трифторметил)-1,2,4-оксадиазол — препарат для приема внутрь, подавляющий пикорнавирусы. Клинические испытания его почти завершены (Rogers et al., 1999ч Плеконарил связывается с гидрофобным карманом на поверхности капсида пикорнавирусов и препятствует их адсорбции на клеточной мембране и высвобождению вирусной РНК. In vitro в концентрации ниже 0,07 мкг/мл плеконарил подавляет репродукцию более 90% наиболее часто выделяемых серотипов энтеровирусов (Pevearet al., 1999), а в концентрации 1 мкг/мл и ниже — около 90% серотипов риновирусов. В опытах на животных плеконарил эффективен при энтеровирусном поражении ЦНС и инфекции дыхательных путей, вызванной вирусом Коксаки A2I, патогенным для человека.
У взрослых при приеме плеконарила внутрь максимальная сывороточная концентрация достигается через 1,5—5 ч, а конечный Т1/2 составляет в среднем 25 ч. Прием 200 и 400 мг плеонарила внутрь дает максимальные сывороточные концентрации 1,1—1,6 и 2—2,4 мкг/мл соответственно (Abdel-Rahman and Kearns, 1999). При приеме во время еды, особенно с жирной пишей, сывороточная концентрация плеконарила существенно выше. У детей при однократном приеме внутрь в дозе 5 мг/кг максимальная сывороточная концентрация составляет 1 3 мкг/мл. При этом за счет большего объема распределения и более быстрого выведения (Т1/2 5,7 ч) ПФК у детей на 40% ниже чем у взрослых (Kearns et al., 1999). Обычно плеконарил хорошо переносится, но иногда может вызывать головную боль, тошноту, понос и неприятные ощущения в животе.
Таблица 50.5. Противовирусные средства на стадии клинических испытаний
|
Вирусы |
Препарат |
Группа; механизм действия |
Путь введения |
|
Вирус гепатита В |
Адефовир |
Нуклеозид, аналог аденозина; подавляет вирусную ДНК-полимеразу |
Внутрь |
|
Клевудин (L-FMAN) |
Нуклеозид, аналог уридина; подавляет вирусную ДНК-полимеразу |
Внутрь | |
|
Энтекавнр (BMS-200475) |
Нуклеозид, циклопентильный аналог гуанозина; подавляет вирусную ДНК-полимеразу |
Внутрь | |
|
Эмтрицитабин (FTC) |
Нуклеозид, аналог цитидина; подавляет вирусную ДНК-полимеразу |
Внутрь | |
|
Бета - L-дезокситимидин (L-dT) |
Нуклеозид, аналог тимидина; подавляет вирусную ДНК-полимеразу |
Внутрь | |
|
Цитомегаяовируе |
Марибавир |
Бензимидазольный рибонуклеозид; подавляет вирусную протеинкиназу, кодируемую геном UL97 |
Внутрь |
|
BDCRB (2-бром-5,6-ди-хлор-1 - (р - D - рибофуранозил )бензнмилазол) |
Бензимидазольный рибонуклеозид; подавляет вирусную шелочную нуклеазу, кодируемую геном UL98 |
Внутрь | |
|
Лобукавир |
Нуклеозид, аналог гуанозина; подавляет вирусную Д Н К-полимеразу |
Внутрь | |
|
Вирус папилломы человека |
Афовирсен |
Антисмысловой олигонуклеотид |
В кондиломы |
|
Риновирусы |
sICAM-l |
Растворимый ложный рецептор |
И нтраназально |
|
Плеконарил |
Связывается с капсидом пикорнавирусов |
Внутрь | |
|
AG-7088 |
Ингибитор протеазы ЗС риновирусов |
И нтраназально | |
|
Респираторный синцитиальный вирус |
VP-14637 |
Ингибитор слияния внешней оболочки вируса с клеточной мембраной |
Местно (интраназально, ингаляции) |
|
R-170591 |
Ингибитор слияния внешней оболочки вируса с клеточной мембраной |
Местно (интраназально, ингаляции) | |
|
Энтеровирусы |
Плеконарил |
Связывается с капсидом пикорнавирусов |
Внутрь |
|
Вирус гриппа |
RWJ-270701 |
Ингибитор нейраминидазы |
Внутрь |
При энтеровирусном менингите прием плеконарила уменьшает продолжительность заболевания и сокращает прием анальгетиков (Rogers et al., 1999). Помогает плеконарил и при простуде, вызванной риновирусами. Ведутся клинические испытания плеконарила при инфекциях дыхательных путей, вызванных пикорнавирусами; при тяжелых и угрожающих жизни энтеровирусных инфекциях (например, хроническом энтеровирусном менингоэнцефалите у больных с агаммаглобулинемией); при сепсисе у новорожденных.
Марибавир[править | править код]
Марибавир — это бензимидазольный рибонуклеозид, избирательно действующий на цитомегаловирусы in vitro в концентрациях (0,1—0,6 мкмоль/л), в 4—10 раз меньших, чем ганцикловир (Chulay et al., 1999). В концентрациях 0,2—1,1 мкмоль/л он подавляет также репродукцию вируса Эпштейна—Барр, но на вирусы простого герпеса и varicella-zoster не действует. Особенность марибавира в том, что он не фосфорилируется в зараженных клетках и не влияет на вирусную ДНК-полимеразу. Именно поэтому он активен в отношении штаммов цитомегаловируса, устойчивых к ганцикловиру, фоскарнету и цидофовиру. Предполагают, что марибавир блокирует фосфорилирование ряда белков, препятствуя тем самым репликации вирусной ДНК.
У штаммов, устойчивых к марибавиру in vitro, обнаружена мутация гена протеинкиназы UL97: по-видимому, подавление этого фермента и лежит в основе действия марибавира.
Доклинические исследования показали, что марибавир не оказывает мутагенного действия и обладает высокой биодоступностью. На 98,5% препарат обратимо связывается с белками плазмы. При приеме внутрь он быстро и хорошо всасывается; однократный прием 400 мг марибавира создает сывороточную концентрацию в среднем около 18 мкг/мл. В водянистую влагу (у лабораторных животных) марибавир проникает лишь в небольших количествах. Т1/2 составляет 3—5 ч. Большинство испытуемых переносили марибавир хорошо, однако с увеличением дозы у многих появлялся горький или металлический привкус во рту. Реже возникали головная боль, повышенная утомляемость и нарушения со стороны ЖКТ. В клинических испытаниях установлено, что с увеличением дозы марибавира (с 300 до 1200 мг/сут) концентрация цитомегаловируса в сперме и моче снижается.
Перспективы[править | править код]
Противовирусные препараты нового поколения будут обладать большей активностью и давать меньше побочных эффектов. Усовершенствование путей введения улучшит фармакокинетику препаратов и обеспечит доставку точно к органам-мишеням. Особое внимание уделяется разработке лекарственных средств, которые поступают в организм в виде предшественников и высвобождают действующее вешество в процессе метаболизма. Такие препараты хорошо всасываются при приеме внутрь и в то же время зашишают содержашееся в них активное вещество от быстрого распада.
Как и другие антимикробные средства, противовирусные препараты пытаются применять в сочетании друг с другом, чтобы повысить эффективность, снизить дозы и уменьшить побочные эффекты, а также предотвратить появление устойчивых штаммов. Среди выделенных от больного вирусов встречаются и чувствительные, и устойчивые, причем устойчивость может быть вызвана различными мутациями — именно поэтому комбинации препаратов действуют намного лучше, чем те же препараты в отдельности. Так, один из препаратов может снижать частоту мутаций вируса, уменьшать его способность к репродукции или повышать чувствительность к другим препаратам.
Понимание механизмов вирусной инфекции на молекулярном уровне, возможно, откроет пути к разработке новых противовирусных средств. Особый интерес представляют препараты, действующие на геном вирусов (антисмысловые олигонуклеотиды, рибозимы и др.). Такие препараты позволяют не только подавить репродукцию вируса, но, возможно, и уничтожить латентную вирусную инфекцию. Первый антисмысловой олигонуклеотид — фомивирсен — уже применяется для лечения цитомегаловирусного ретинита, однако фармакологические свойства антисмысловых нуклеотидов, в том числе активность и избирательность, еще требуют изучения. Много интересного таит в себе генотерапия. Можно, например, ввести в клетку мутантные гены, «заставив» ее синтезировать дефектные белки, нарушающие репродукцию вирусов; можно также добиться выработки в этих клетках фрагментов антител к важнейшим вирусным белкам. Перспективными могут оказаться средства для подавления патологических иммунных реакций и иммуномодуляторы, а также иммунотерапия моноклональными антителами, вакцинами и др.