Регуляция секреции гормонов
Регуляция секреции гормонов[править | править код]
Источник:
Эндокриная система, спорт и двигательная активность.
Перевод с англ./под ред. У.Дж. Кремера и А.Д. Рогола. - Э64
Издательство: Олимп. литература, 2008 год.
Степень воздействия гормона на ткань-мишень пропорциональна его концентрации в крови. Содержание любого биологически активного гормона в системе кровообращения определяется сочетанием нескольких факторов. К этим факторам относятся:
- скорость секреции в кровь эндокринной железой;
- для некоторых гормонов, в частности тиреоидных, скорость активации (превращения Т4 в Т3) в крови;
- для липофильных гормонов, а именно стероидных и тиреоидных, степень связывания белками плазмы крови;
- скорость инактивации и удаления из крови (клиренса).
Из всех этих факторов первый — скорость секреции в кровь — является основным, определяющим содержание гормона в системе кровообращения, в частности в условиях отсутствия физической нагрузки (Sherwood, 2004).
Существуют два типа секреции гормона в кровь (Kelly, 1985). Конститутивная секреция представляет собой непрерывное выделение эндокринного вещества в кровь с некоторой базовой скоростью. При таком механизме секреции гормон выделяется клеткой по мере его синтеза, поскольку железа не способна его накапливать, поэтому при получении стимулирующего сигнала происходит увеличение активности синтеза и вновь синтезированный гормон выделяется непосредственно в кровяное русло путем пассивной диффузии через клеточную мембрану. Такой тип секреции характерен для стероидных и тиреоидных гормонов, которые по своим свойствам являются липофильными, как и плазматическая мембрана клетки. Конститутивная секреция регулируется изменениями уровня фосфорилирования белков, которые выступают в роли ферментов пути биосинтеза.
Регулируемая секреция представляет второй тип высвобождения гормона из эндокринной железы в кровь. В этом случае между скоростью синтеза белка и его высвобождением в кровь нет прямой зависимости, как в случае конститутивной секреции. Вместо этого эндокринные железы, которые способны к регулируемой секреции, обладают способностью накапливать синтезированный гормон. Следует отметить, что и в этом случае накопительные способности железистой клетки ограничены. На самом деле для любого отдельно взятого гормона его запас в эндокринных тканях редко превышает суточную потребность организма (Baulieu, 1990).
В случае регулируемой секреции стимулирующее воздействие приводит к высвобождению путем экзоцитоза накопленных везикул, содержащих гормон. В большинстве случаев для обеспечения постоянной готовности клеток к выделению гормона сигнал, вызывающий высвобождение гормона, активизирует ферментативные системы его синтеза. Обычно высвобождению запасенного гормона и активации синтетических процессов предшествует поступление в клетку ионов кальция. Такая регулируемая форма секреции наблюдается для белково-пептидных гормонов и катехоламинов.
Как при конститутивной, так и при регулируемой секреции гормонов стимулом, регулирующим скорость секреции, обычно является: 1) изменение в плазме концентрации питательных веществ или ионов; 2) выделение нейронами нейротрансмиттеров, воздействующих на эндокринные клетки; 3) связывание клеточными рецепторами гормонов, выделяемых другими эндокринными железами. Как правило, все эти события взаимосвязаны между собой определенным образом. С другой стороны, изменения в секреции гормонов обычно являются результатом воздействия нескольких факторов.
Ответ эндокринных желез на стимулирующее воздействие определяется чувствительной и эффективной системой обратной связи, которая передает информацию от ткани-мишени обратно к органу, выделяющему гормон. Наиболее распространенной формой регуляции скорости секреции в эндокринной системе является негативная обратная связь. Этот тип обратной связи можно наблюдать в случае, когда активность одной системы (эндокринная железа) модифицируется негативным образом, т. е. подавляется активностью другой системы (ткани-мишени), что позволяет поддерживать гомеостаз. Например, повышение концентрации глюкозы в крови стимулирует секрецию инсулина поджелудочной железой. Повышение содержания инсулина в крови способствует поглощению глюкозы мышечными клетками ткань-мишень для инсулина, а также превращению глюкозы в жир, результатом чего является нормализация содержания глюкозы в крови.
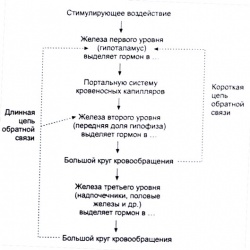
Существует несколько различных видов регуляции секреции гормонов путем негативной обратной связи. Управление секрецией нескольких важных гормонов осуществляет гипоталамо-гипофизарная система. Небольшой участок в основании мозга — гипоталамус — продуцирует несколько рилизинг-гормонов или либеринов, которые переносятся портальной системой кровеносных капилляров в переднюю долю гипофиза. В этом примере нейроэндокринной функции гипоталамус выделяет гормоны-либерины, которые, попадая в переднюю долю гипофиза, изменяют там скорость секреции ряда гормонов в систему кровообращения, которая обеспечивает их транспорт ко всем тканям организма. Эти гипофизарные гормоны могут оказывать непосредственное влияние на ткани-мишени, либо активировать железы третьего уровня этой системы регуляции, стимулируя секрецию их специфических гормонов в кровеносное русло.
Что касается негативной обратной связи, в этой нейроэндокринной системе можно выделить “короткую” и “длинную" регуляторные цепи (Vander et al., 2001). В качестве примера действия короткой цепи негативной обратной связи можно привести ситуацию, когда высокий уровень пролактина в крови детектируется гипоталамусом, в ответ на это там происходит выделение допамина, который направляется в гипофиз и ингибирует секрецию гипофизом пролактина в кровеносное русло. В случае системы, состоящей из трех органов, показано существование длинной петли обратной связи. В качестве иллюстрации такого механизма обратной связи рассмотрим регуляцию синтеза кортизола. Рассматриваемая система состоит из гипоталамуса, гипофиза и коры надпочечников. Гипоталамус выделяет кортиколиберин или кортикотропин-рилизинг-гормон (КРГ) в портальную систему кровеносных капилляров, по которой это вещество попадает в переднюю долю гипофиза. После связывания кортиколиберина с клеточными рецепторами гипофиз выделяет в кровеносное русло АКТГ, который по большому кругу кровообращения попадет к клеткам надпочечников. В тканях коры надпочечников (напомним, что мозговое вещество надпочечников продуцирует катехоламины) АКТГ индуцирует высвобождение в кровь кортизола, который оказывает специфическое воздействие на ткани-мишени печени, скелетных мышц и жировых отложений. В этом случае негативная регуляция наблюдается, когда повышение содержания кортизола в крови подавляет выделение АКТГ гипофизом и/или КРГ гипоталамусом. Этот пример показывает, насколько совершенной в эндокринной системе является интеграция подаваемых и принимаемых сигналов, которая позволяет регулировать секрецию гормонов в эндокринной системе из нескольких органов с помощью короткой и длинной цепей обратной связи (Vander et al., 2001).
Несмотря на то что негативная обратная связь является преобладающим механизмом регуляции, для изменения уровня секреции гормонов в организме используется также позитивная обратная связь. В случае позитивной обратной связи эндокринная железа, продуцирующая гормон, контролирует индуцированные этим гормоном изменения биологической активности ткани-мишени. Если ткань-мишень реагирует недостаточно интенсивно, эндокринная железа выделяет дополнительное количество гормона до тех пор, пока активность биологического процесса, который он регулирует, не достигнет адекватного уровня. Примером позитивной обратной связи является регуляция эндокринной функции во время родов. Окситоцин, выделяемый задней долей гипофиза, стимулирует сокращение матки. По мере прохождения родового процесса и увеличения потребности в более сильных родовых схватках активность матки сигнализирует гипофизу о потребности увеличения секреции окситоцина, что приводит к усилению силы и частоты сокращений матки и позволяет родам завершиться благополучно.
Хотя основной функцией эндокринной системы является поддержание гомеостаза, изменения внутренней среды организма и внешних условий не единственный регулятор секреции гормонов. Концентрация большинства гормонов в крови подвергается прогнозируемым флуктуациям или ритмическим колебаниям, происходящим на протяжении определенного периода времени. Наиболее хорошо изучены циркадные или суточные ритмы эндокринной системы. Циркадный ритм характеризует периодические колебания, происходящие в течение 24 ч солнечных суток, тогда как суточный ритм относится к колебаниям уровня секреции гормона, связанным со сменой дня и ночи. Часто эти термины используются как синонимы. Такие естественные, запрограммированные ритмы активности эндокринных желез поддерживаются супрахиазматическими ядрами гипоталамуса. Этот пейсмекер (ритмоводитель) регулирует секрецию гормонов на основании собственных внутренних часов и задаст специфический характер секреции для каждого гормона, например, содержание кортизола в крови выше всего утром, тогда как максимальное содержание гормона роста наблюдается в ночные часы (Illnerova ct al., 2000).
Наряду с суточными колебаниями уровня секреции гормонов, часто наблюдаются и регулярные пульсации с более коротким периодом, которые называются ультралианным ритмом и накладываются на циркадный ритм. Эти периодические повышения секреции гормонов, вероятно, являются следствием возрастания активности гипоталамуса и имеют важное физиологическое значение. Так, было показано, что при одном и том же общем количестве выделяемого гормона усвоение глюкозы было более эффективным в случае, когда кривая продукции инсулина имела волнообразный вил, по сравнению с ситуацией, когда его уровень в крови был постоянным (Porksen, 2002).
Известно также, что секреция гормонов изменяется и на протяжении года, хотя здесь основная масса данных была получена на животных. Годовые ритмы соответствуют изменению продолжительности светового дня, которая регистрируется шишковидной железой центральной нервной системы (Short, 1985). Эта железа, которую за фоточувствительность часто называют еще "третьим глазом", в ответ на изменение продолжительности светового дня регулирует количество выделяемого ею мелатонина (Tamarkin ct al., 1985). Другие сезонные изменения поведения, такие, как зимняя спячка, миграции и даже изменения окраски меха, управляются прогнозируемыми изменениями уровня мелатонина в крови. У человека усиление продукции мелатонина, происходящее при сокращении продолжительности светового дня, может вызывать изменения настроения и даже депрессию (Lcwy et al., 1987). Ранее было показано, что у всех млекопитающих, не исключая и человека, мелатонин играет главную роль в поддержании циркадных ритмов, оказывая влияние на клетки супрахиазматичсских ядер (Pcvct ct al., 2002).