Сердечно-сосудистая патология
Содержание
- 1 Сердечно-сосудистая патология
- 2 Аритмии
- 3 Острый инфаркт миокарда
- 3.1 Раннее паллиативное вмешательство при остром инфаркте миокарда
- 3.2 Раннее терапевтическое вмешательство при остром инфаркте миокарда
- 3.3 Другие лекарственные средства, используемые для лечения острого инфаркта миокарда
- 3.4 Лечение синдромов, имеющих отношение к острому инфаркту миокарда (острые коронарные синдромы)
- 4 Застойная сердечная недостаточность
- 5 Лечение острой сердечной недостаточности
- 6 Гипертензия
- 7 Неотложная терапия гипертензии
- 8 ПАТОФИЗИОЛОГИЯ И ЗАБОЛЕВАНИЯ КРОВЕНОСНЫХ СОСУДОВ
- 9 Заболевания периферических сосудов
- 10 Васкулит
- 11 Болезнь Рейно
- 12 Варикозное расширение вен
- 13 Тромбоз вен («красные сгустки»)
- 14 Атеротромбоз
- 15 ИНФЕКЦИИ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ
- 16 Инфекционный эндокардит
- 17 Инфекционный миокардит (в том числе болезнь Чагаса)
- 18 Инфекционный перикардит
- 19 Болезнь Кавасаки
- 20 Ревматическая лихорадка
- 21 Читайте также
- 22 Литература
- 23 Источники
Сердечно-сосудистая патология[править | править код]
Закрытые повреждения сердца[править | править код]
Ушиб миокарда — серьезное осложнение тупой травмы грудной клетки, проявляющееся обычно болью в груди и синусовой тахикардией. Возможны другие аритмии. III тон сердца, шум трения перикарда и влажные хрипы в легких. Метод выбора для выявления выпота в полость перикарда и нарушений сократимости миокарда — ЭхоКГ. На ЭКГ можно обнаружить нарушения проводимости, смещение сегмента ST или инверсию зубца Т. Исследование активности сердечных изоферментов в динамике (МВ-фракции КФК и тропонина 1) также может помочь в постановке диагноза. В большинстве случаев ушиб миокарда полностью излечивается, лишь изредка он осложняется, например, дисфункцией желудочков или тромбозом коронарных артерий. Отсутствие изменений на ЭКГ и нормализация активности сердечных изоферментов позволяют с большой долей вероятности исключить поздние осложнения. Физические нагрузки противопоказаны до нормализации ЭхоКГ (обычно в течение нескольких месяцев); после этого необходимо пользоваться защитными приспособлениями для грудной клетки.
Внезапная смерть[править | править код]
Внезапная смерть редко встречается у спортсменов, но каждый такой случай доставляет тяжелые переживания. Среди причин преобладают сердечно-сосудистые (85% из 185 случаев гибели спортсменов в США с 1985 по 1995 г.). Самая частая причина — гипертрофическая кардиомиопатия (примерно 36% всех внезапных смертей у спортсменов). Гипертрофическая кардиомиопатия — это наследственная патология кардиомиоцита на уровне саркомера, приводящая к гипертрофии левого желудочка без расширения его полости. Течение заболевания крайне вариабельно: от полного отсутствия симптомов до тяжелой сердечной недостаточности или преждевременной смерти. Проявления могут включать одышку, стенокардию, аритмии или обмороки, однако для детей и молодых людей очень характерна внезапная смерть во время тяжелой физической нагрузки. Осмотр и обычные инструментальные исследования ненадежны для диагностики гипертрофической кардиомиопатии и определения риска внезапной смерти. Среди физикальных признаков необходимо отметить грубый мезосистолический веретенообразный шум, усиливающийся при уменьшении преднагрузки (например, при пробе Вальсальвы). На ЭКГ можно обнаружить признаки гипертрофии левого желудочка и увеличения левого предсердия или нарушения проводимости. Диагноз ставят с помощью ЭхоКГ, обычно по асимметричной гипертрофии более 15 мм. Важно отметить, что у детей младше 15 лет может не быть выраженной гипертрофии и заболевание может остаться недиагностированным. К тому же только с помощью ЭхоКГ невозможно точно оценить риск внезапной смерти. Вопрос о возможности занятий спортом решают индивидуально с учетом факторов риска, перечисленных в табл. 1.3. Состязательные виды спорта при гипертрофической кардиомиопатии обычно противопоказаны.
Таблица 1.3. Факторы риска внезапной смерти при гипертрофической кардиомиопатии
- Желудочковая тахикардия
- Отягощенный семейный анамнез: внезапная смерть родственников, страдавших гипертрофической кардиомиопатией
- Обмороки
- Тяжелые гемодинамические нарушения: динамическая обструкция (внутрижелудочковый градиент давления > 50 мм рт. ст.), снижение АД при физической нагрузке, умеренная или тяжелая митральная недостаточность
- Размер левого предсердия > 50 мм
- Пароксизмы мерцательной аритмии
- Признаки ишемии миокарда
Врожденные аномалии коронарных артерий — вторая по частоте причина внезапной смерти спортсменов моложе 30 лет. Врожденные аномалии коронарных артерий обычно никак не проявляются, хотя возможны неприятные ощущения в груди или обмороки. При подозрении на врожденную аномалию коронарных артерий показаны пробы с физической нагрузкой для выявления ишемии миокарда. Если подтвердилась ишемия, ограничивают спортивные нагрузки и проводят операцию. К соревнованиям допускаются только те спортсмены, которым успешно проведено хирургическое лечение и у которых подтверждено отсутствие ишемии при физической нагрузке.
Ишемия миокарда вследствие коронарного атеросклероза служит основной причиной внезапной смерти при физической нагрузке у спортсменов старше 30 лет. В большинстве случаев у них есть факторы риска ИБС (гиперхолестеринемия, сахарный диабет, заболевания сердца в семье, курение) и нередко отмечается боль в груди. В каждом случае острой сердечно-сосудистой недостаточности у спортсмена 35 лет и старше следует заподозрить инфаркт миокарда. Проявления его те же, что и у людей, не занимающихся спортом: боль или стеснение в груди, потливость, тошнота, одышка, страх смерти. Неотложные меры включают ингаляцию кислорода, аспирин, нитроглицерин, вызов реанимационной бригады и госпитализацию во избежание осложнений и летального исхода. Немедленно начатый мониторинг ЭКГ и проведение на месте реанимационных мероприятий и автоматической дефибрилляции позволяют спасти жизнь спортсмена. Врачи должны быть по возможности готовы к такому развитию событий. Важно отметить, что отсутствие симптомов у тренированных людей не означает отсутствие коронарного атеросклероза. Поэтому при наличии факторов риска показано обследование. При подтвержденной ИБС не рекомендуются состязательные виды спорта с большой нагрузкой независимо от наличия или отсутствия симптомов, инфаркта миокарда или полной реваскуляризации. Допускаются менее интенсивные физические нагрузки, однако в каждом случае вопрос должен решаться индивидуально после обследования и оценки риска.
Редкое, но крайне опасное повреждение при тупой травме груди — сотрясение сердца. Оно проявляется внезапной потерей сознания и остановкой кровообращения. Почти две трети всех случаев приходятся на бейсболистов, получивших удар мячом в грудь. Считается, что у детей и подростков риск сотрясения сердца выше вследствие большей податливости грудной клетки. Профилактика заключается в использовании надежных защитных средств, особенно игроками, всегда находящимися «под ударом»: принимающими в бейсболе, хоккейными вратарями. Причиной внезапной смерти, вероятно, служит фибрилляция желудочков или острая брадикардия; таким образом, при сотрясении сердца могли бы помочь своевременная диагностика, сердечно-легочная реанимация и автоматическая дефибрилляция непосредственно на игровом поле, хотя на сегодняшний день не доказана польза ни одного из этих вмешательств. Другие причины внезапной смерти перечислены в табл. 1.4.
Таблица 1.4. Причины внезапной смерти спортсменов
- Кардиомиопатии: гипертрофическая, дилатационная, миокардит, аритмогенная дисплазии правого желудочка
- Врожденные аномалии коронарных артерий ИБС
- Разрыв аорты: синдром Марфана, коарктация аорты
- Клапанные пороки сердца: аортальный стеноз, пролапс митрального клапана
- Нарушения ритма сердца и проводимости: синдром WPW, врожденное удлинение интервала QT, идиопатическая желудочковая тахикардия
- Сотрясение сердца
- Допинг: анаболические стероиды, амфетамины, кокаин, эфедрин (Ephedra sinica, ма-хуан)
Аритмии[править | править код]
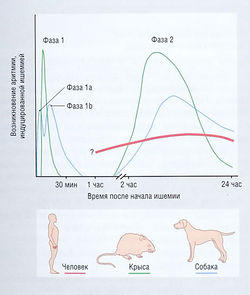
Аритмия буквально означает отсутствие ритма, а дисритмия — это аномальный ритм. На практике оба термина взаимозаменяемы и обозначают аномальное или нерегулярное сердцебиение, причем в США отдают предпочтение термину «аритмия». Существует множество видов аритмии, связанной с патологическими процессами, например острым инфарктом миокарда (ОИМ). Кроме того, аритмии могут возникать как побочный эффект при использовании лекарственных средств, причем парадоксально, что в их число входят многие антиаритмические препараты. Аритмии при ишемии/инфаркте могут иметь характерное временное течение (рис. 13.9).
Рис. 13.9 Развитие аритмии во время острого инфаркта миокарда (ОИМ). Характеристики аритмий при ОИМ у человека очевидны. Течение желудочковой аритмии, приводящей к летальному исходу, после ОИМ показано в часах в сравнении с экспериментальными данными, полученными на животных.
Причины сердечных аритмий
- Острый инфаркт миокарда (острая ишемия и последующий некроз/апоптоз)
- Сердечная недостаточность (гипертрофия, высокая преднагрузка и диастолическое растяжение миокарда)
- Гипертиреоз (аритмия полностью обратима при нормализации функции щитовидной железы)
- Гипокалиемия (особенно при анорексии)
- Вегетативная дисфункция (включая феохромоцитому)
- Лекарственные средства (включая многие антиаритмические средства)
- Наследуемые мутации ионных каналов сердца (например, наследственный синдром удлиненного интервала QT)
- Лихорадка
Аритмии можно классифицировать соответственно их анатомическому происхождению:
- наджелудочковая аритмия (источник возникновения — СА- или АВ-узлы или предсердия);
- желудочковая аритмия (возникает в желудочках). Аритмии варьируют по своей значимости.
В недавно проведенном исследовании, ученые из Монако обнаружили, что чрезмерное потребление кока-колы увеличивает риск развития аритмии, тахикардии и отмиранию мышц. Как объясняют авторы исследования, кукурузный сироп, содержащийся в коле, может затруднять всасывание воды в пищеварительной системе и при этом вызывать диарею, что ведет к большим потерям жидкости, «вымывающей» калий из организма. Кроме того, кофеин, содержащийся в коле, вероятно, уменьшает количество калия, всасываемого почками. Калий необходим для нормального сокращения сердечной мышцы, и его недостаток может тормозить работу желудочков, приводя к аритмии.[1]
Они могут быть как неопасными (некоторые наджелудочковые аритмии), так и приводящими к летальному исходу (например, асистолия и некоторые быстро возникающие желудочковые аритмии). Желудочковые аритмии — наиболее распространенная причина летального исхода в США и других экономически развитых странах: только в США от аритмии ежегодно умирают около 350 000 человек.
Внезапная сердечная смерть (летальный исход в отсутствие предшествующих симптомов или при наличии симптомов продолжительностью < 30 мин) обусловлена главным образом желудочковыми аритмиями: фибрилляцией желудочков (чаще всего) или асистолией (в редких случаях). Внезапная сердечная смерть часто наступает без предвестников и почти всегда вне больницы.
Острый инфаркт миокарда — важная причина тяжелых желудочковых аритмий
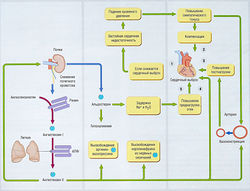
Острый инфаркт миокарда представляет собой клинический синдром, включающий ишемию миокарда (прекращение кровотока в участке сердца), приводящую к некрозу (инфаркту) миоцитов или апоптозу. ОИМ происходит, в частности, при закрытии просвета коронарной артерии сгустком крови (тромбом) или при расслоении аневризмы аорты. В результате закупорки сосуда миокард получает недостаточное количество крови, чтобы покрыть потребности тканей в кислороде и питательных веществах и удалить продукты метаболизма. Причина аритмий при ОИМ неясна. Возможно, что аритмию вызывает накопление внеклеточного К+ (вызывающего диастолическую деполяризацию и аномальную реполяризацию) и циклического аденозинмонофосфата, способного вызывать спонтанные потенциалы действия.
Реперфузия (возобновление кровоснабжения области ишемии) крайне важна, чтобы восстановить кровоснабжение ткани и избежать инфаркта. Ранняя реперфузия, особенно после короткого периода ишемии, сама по себе может вызвать аритмию, и это явление иногда расценивают как показатель удачной терапевтической реперфузии.
Аритмию диагностируют по характеристикам ЭКГ
Аритмии (см. рис. 13.8) диагностируют по ЭКГ:
- ЭКГ в виде ровной линии указывает на асистолию;
- СА-аритмии ассоциированы с нормальной конфигурацией ЭКГ, однако изменяется частота сердцебиений (тахи- или брадикардия) и симптомы часто отсутствуют;
- предсердные экстрасистолы проявляются на ЭКГ как несвоевременно появляющиеся зубцы Р; они часто бессимптомны;
- в случае трепетания предсердий частота сокращений повышена (> 300 в мин) и наблюдается частичная АВ-блокада (вследствие неспособности нормального АВ-узла проводить каждый импульс от предсердия), поэтому не каждый предсердный импульс поступает в желудочки. На ЭКГ зубцы Р повторяются. Трепетание предсердий относительно часто встречается у пожилых людей;
- при фибрилляции предсердий они сокращаются асинхронно, в связи с чем нарушается активная насосная функция. На ЭКГ обычно отсутствует зубец Р. Фибрилляция предсердий часто встречается у лиц пожилого возраста и людей, страдающих заболеванием митрального клапана;
- пароксизмальная наджелудочковая тахикардия — это аритмия, возникающая в АВ-узле. Она может появиться в результате ретроградного проведения возбуждения в узле и вызвать предсердную тахикардию. Сама по себе она не является жизнеугрожающей, однако может стать таковой, если сохраняется высокая частота возбуждений желудочков;
- желудочковые экстрасистолы (ЖЭС) (см. рис. 13.86) иногда относят к эктопическому возбуждению желудочков. На ЭКГ их идентифицируют как дискретное преждевременное появление измененных комплексов QRS. Они часто возникают при ОИМ;
- желудочковую тахикардию (ЖТ) (см. рис. 13.8в) определяют как последовательные ЖЭС (как минимум две). Продолжающаяся тахикардия может вызвать у некоторых пациентов заметные гемо-динамические эффекты, например гипотензию. Встречается при многих заболеваниях;
- фибрилляция желудочков (см. рис. 13.8г) обычно заканчивается летально, поскольку координированных сокращений желудочков нет и сердечный выброс отсутствует. На ЭКГ отдельные зубцы время от времени варьируют по амплитуде и форме. Вероятно, эта аритмия является главной причиной летального исхода у пациентов с ОИМ;
- ЖТ torsades de pointes проявляется на ЭКГ характерной картиной — «пляской пиков» (пируэтная тахикардия). Эта серьезная аритмия подобна фибрилляции желудочков — с быстрыми асинхронными комплексами и ундулирующей базовой линией на ЭКГ. Как правило, эта аритмия спонтанно обратима, поэтому не обязательно будет летальной (в отличие от фибрилляции желудочков). Фактором риска ЖТ torsades de pointes является удлиненный интервал QJ, который может быть врожденным (при наследственном синдроме удлиненного QT) или лекарственно индуцированным (например, антиаритмическими средствами классов 1а и III; см. табл. 13.3). Развитию torsades de pointes способствуют различные предрасполагающие факторы, включая гипокалиемию, брадикардию и многочисленные лекарства;
- синдром Вольфа-Паркинсона-Уайта обусловлен врожденным дополнительным анатомическим путем проведения между предсердием и желудочком (пучок Кента). Этот путь дает возможность быстрой передачи импульсов от предсердий желудочкам в обход АВ-узла. На ЭКГ это проявляется в виде короткого интервала PR, за которым следует дельта-волна на широком комплексе QRS. Может возникнуть фибрилляция предсердий.
Ишемия
- Ишемию, возникающую в результате уменьшения кровотока, диагностируют в связи с недостаточностью сократимости, аномалиями ЭКГ и болью в груди
- Бессимптомная ишемия характеризуется недостаточностью сократимости и аномалиями ЭКГ при отсутствии боли в груди
- Инфаркт миокарда возникает, если длящаяся ишемия приводит к гибели клеток миокарда
- «Оглушение» представляет собой обратимое нарушение функций сердца или сосудов, определяемое в течение нескольких часов или суток после начала реперфузии
- «Спящий» миокард возникает вследствие супрессии его функции при относительной ишемии. При этом сохраняются энергетические субстраты, что способствует восстановлению при проведении реперфузии
- Короткий период ишемии обусловливает прекондиционирование, т.е. состояние защиты сердца от эффектов более длительного периода ишемии (т.е. аритмии, инфаркта и нарушения сократительной функции)
- При возникновении признаков и симптомов, наиболее распространенным является давление в груди или боль, как правило, на левой стороне тела. Другие признаки и симптомы - с которыми чаще всего сталкиваются женщины, пожилые люди и люди с диабетом - включают в себя: боль в челюсти и шее, боли в плечах, быстрое сердцебиение, одышка, тошнота и рвота, потение, усталость.[2]
Механизмы возникновения и поддержания аритмий
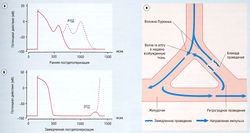
Аритмии инициируются и поддерживаются комбинацией возникновения аномального импульса (потенциала действия) и проведения аномального импульса. Генерация нормального и аномального импульсов известна как автоматизм. Проведение импульса называют нормальным или аномальным в зависимости от пути его передачи: ортоградный путь — нормальное проведение; по механизму reentry — аномальное, или блокированное, проведение (рис. 13.10). Автоматизм может инициировать аритмию, если он возникает эктопически (вне места обычной локализации, т.е. не в СА-узле).
Рис. 13.10 Основные механизмы аритмогенеза. (а) Ранняя постдеполяризация (РПД) возникает во время фазы реполяризации потенциала действия. Пунктирная линия обозначает повторную РПД. (б) Замедленная постдеполяризация (ЗПД) возникает после реполяризации потенциала действия во время фазы диастолы. Пунктирная линия показывает потенциал действия, генерированный в результате ЗПД.(в) Однонаправленная блокада. Возбуждение поступает в волокна Пуркинье, откуда оно должно передаваться в желудочковую ткань. Однако проведение в определенном участке однонаправленно блокировано, импульс идет ретроградно из желудочка обратно в волокна Пуркинье и повторно возбуждает ткань, которая уже не рефрактерна, а является вновь возбудимой.
Примерами аритмий, вызываемых, по всей видимости, автоматизмом, могут служить:
- узловая тахикардия.
- ЖЭС, ассоциированные с развивающимся инфарктом миокарда.
Таблица 13.1 Механизмы аритмогенеза
- Возникновение аномального импульса
- Автоматизм
- Усиленный нормальный автоматизм
- Аномальный автоматизм
- Триггерный автоматизм
- Ранняя постдеполяризация
- Замедленная постдеполяризация
- Проведение аномального импульса
- Блокада проведения
- Блокады I-III степени
- Механизм re-entry
- Циркуляция волны возбуждения
- Отражение
Существует три типа автоматизма, которые могут привести к аритмии (табл. 13.1):
- усиленный нормальный автоматизм встречается в тканях (АВ-узле и пучке Гиса), способных к медленной автоматической генерации импульсов, которая в нормальных условиях перекрывается более частыми импульсами из СА-узла. Нормальный автоматизм может усиливаться под влиянием лекарственных средств и заболеваний;
- аномальный автоматизм возникает в тканях, неспособных в нормальных условиях к автоматической генерации импульсов (т.е. предсердной или желудочковой). В ходе патологических процессов (например, при инфаркте миокарда) аномальный автоматизм часто возникает в волокнах Пуркинье. Катехоламины могут усиливать автоматизм этого типа;
- триггерный автоматизм (известный как триггерная активность) подобен аномальному автоматизму, однако здесь аберрантные импульсы генерируются предшествующим нормальным импульсом. Существуют два типа триггерной активности. Ранняя постдеполяризация (РПД) возникает во время фазы реполяризации потенциала действия (т.е. в течение фазы 2 или 3). РПД усиливается под влиянием брадикардии и лекарственных средств, увеличивающих продолжительность потенциала действия (например, антиаритмических средств класса III). Механизм, лежащий в основе РПД, неизвестен. Замедленная постдеполяризация (ЗПД) (см. рис.13.10) возникает после окончания потенциала действия (т.е. во время фазы 4). В типичных случаях ЗПД появляется как результат внутриклеточной перегрузки ионами Са2+, что может произойти в течение ОИМ, реперфузии или интоксикации дигиталисом. Перегрузка Са2+ приводит к пульсирующему высвобождению Са2+ из саркоплазматического ретикулума и генерации входящего тока (что и ведет к ЗПД), переносимого Ка+/Са2+-обменником.
Механизм re-entry и блокада проведения — условия возникновения аритмий
Чаще всего местом сердечной блокады является АВ-узел:
- при АВ-блокаде I степени проведение через АВ-узел замедлено, что проявляется на ЭКГ в виде удлинения интервала PR;
- для АВ-блокады II степени характерно отсутствие проведения некоторых импульсов в желудочки (т.е. их сокращения не происходит). На ЭКГ комплекс QRS не всегда следует за зубцом Р;
- АВ-блокада III степени (полная) клинически протекает наиболее тяжело. Полностью прекращается проведение импульсов на уровне АВ-узла. Это ведет к замедлению (запаздыванию) ритма сокращений желудочков, не обеспечивающего адекватного сердечного выброса. Аберрантное проведение этого типа может демаскировать ЖЭС.
Механизм re-entry поддерживает (и может инициировать) желудочковую тахикардию и фибрилляцию желудочков
Механизм re-entry — это циркуляция проведения с многократным повторным возбуждением ткани в отсутствие диастолического интервала. В 1914 г. Майне выявил условия возникновения re-entry: наличие участка однонаправленной блокады импульса, что дает возможность обратного (ретроградного) проведения с повторным возбуждением ткани в обход блока. На существование механизма reentry указывают следующие критерии:
- длина проводящего пути больше, чем длина волны (со), определяемая эффективным рефрактерным периодом (ERP) и скоростью проведения (CV), т.е. (О = ERP X CV;
- наличие однонаправленной блокады проведения.
Однонаправленная блокада проведения может быть анатомической (как при синдроме Вольфа-Паркинсона-Уайта) или функциональной (например, удлиненная рефрактерность, возникшая в результате ишемии); оба фактора могут быть одновременно. Re-entry может быть прервана преждевременной активацией, искусственным ускорением сердечного ритма и введением лекарственных средств. Механизм re-entry играет роль в поддержании, а возможно, и в инициации предсердной тахикардии, фибрилляции предсердий, АВ-узловой тахикардии, синдрома Вольфа-Паркинсона-Уайта, желудочковой тахикардии и фибрилляции желудочков.
Существуют и другие аритмогенные механизмы (детальнее с ними можно ознакомиться, обратившись к списку литературы в конце главы).
Лечение аритмий[править | править код]
Автоматизм и проведение — мишени антиаритмической терапии
Цели лечения аритмий:
- восстановление ритма сердцебиений до нормы;
- предотвращение рецидива аритмии;
- устранение гемодинамические последствий аритмий;
- снижение риска возникновения более тяжелых аритмий, таких как фибрилляция желудочков.
Хотя наиболее желательной целью является восстановление нормального синусового ритма, это не всегда необходимо. Так, при фибрилляции предсердий контроль частоты сокращений желудочков — такая же важная цель лекарственной терапии, как и восстановление нормального синусового ритма. Терапию аритмий проводят лекарствами, а также используют нефармакологические методы: электрическую дефибрилляцию, хирургическое вмешательство и имплантацию искусственного водителя ритма. Значение нефармакологических способов лечения возрастает. Главная цель лекарственной терапии — восстановить синусовый ритм, не вызывая побочных эффектов. Многие лекарственные средства не отвечают полностью этой цели. Стандартные антиаритмические средства, используемые в США, перечислены в табл. 13.2. При назначении многих из этих препаратов необходим мониторинг их концентрации в плазме (см. табл. 13.2).
Классификация антиаритмических средств, разработанная Воганом Уильямсом[править | править код]
Теоретически антиаритмические лекарственные средства можно классифицировать по механизму их действия на молекулярном, клеточном и тканевом уровнях. Со времени открытия первого антиаритмического препарата Венкебахом в 1914 г. перечень антиаритмических средств значительно расширился, однако система классификации долгое время оставалась несовершенной. Первая система классификации, разработанная Воганом Уильямсом в 1970 г. (табл. 13.3), описывает отличительные свойства лекарственных средств, используемых в качестве антиаритмических препаратов, хотя эти свойства не обязательно соответствуют механизму действия.
Предполагается, что классификация антиаритмических средств поможет выбрать необходимый для лечения препарат. Однако лишь для небольшого числа аритмий средством выбора являются лекарственные средства только одного класса. Отчасти это обусловлено тем, что лекарственные средства не всегда эффективны. Для наджелудочковых аритмий это не так существенно, поскольку если препарат неэффективен, то можно применить другой. Выбор эффективного лекарственного средства становится более сложной проблемой в случае желудочковых аритмий, т.к. они могут серьезно осложнять состояние пациента или приводить к летальному исходу. Антиаритмические средства особенно неэффективны при желудочковых аритмиях, поэтому выбор препарата часто основывается на данных последовательного тестирования способности лекарственных средств подавлять аритмии, индуцированные «запрограммированной» электростимуляцией желудочков у данного пациента в условиях клиники. Проведенные исследования показывают, что этот метод — не очень хороший предиктор улучшения выживаемости в отдаленном периоде. Тем не менее его продолжают использовать как ориентир при выборе терапии. Для профилактики желудочковых аритмий часто используют комбинацию антиаритмических средств разных классов. Наиболее важный нефармакологический метод лечения жизнеугрожающих желудочковых аритмий — применение автоматического имплантируемого дефибриллятора (АИД).
|
Таблица 13.2 Средняя концентрация в плазме и пути введения антиаритмических средств, используемых в США | ||
|
Лекарственные средства |
Средняя эффективная концентрация в плазме (мкг/мл) |
Путь введения |
|
Дизопирамид |
3 |
в/в, п/о |
|
Лидокаин |
3 |
в/в |
|
Прокаинамид |
7 |
в/в, п/о |
|
Хинидин |
4 |
в/в, п/о |
|
Мексилетин |
в/в, п/о | |
|
Токаинид |
7 |
в/в, п/о |
|
Фенитоин |
15 |
в/в, п/о |
|
Флекаинид |
0,7 |
в/в, п/о |
|
Энкаинид |
0,75 |
в/в, п/о |
|
Пропафенон |
1,5 |
в/в, п/о |
|
Бретилий |
1 |
в/в, п/о |
|
Амиодарон |
1,5 |
в/в, п/о |
|
Верапамил |
0,1 |
в/в, п/о |
в/в — внутривенно; п/о — перорально.
Таблица 13.3 Классификация антиаритмических средств, разработанная Воганом Уильямсом
|
Класс |
Тип лекарственного средства |
Электрофизиологическое действие |
Примеры |
|
la |
Блокатор Nа+-каналов, блокирует также К+-каналы |
Блокирует проведение, повышает ERP |
Хинидин Дизопирамид |
|
lb |
Блокатор Nа+-каналов; более эффективны при высокой частоте |
Блокирует проведение, снижает ERP |
Лидокаин Мексилетин |
|
Ic |
Блокатор Nа+-каналов; эффект не зависит от частоты |
Блокирует проведение, не влияет или повышает ERP |
Флекаинид Энкаинид |
|
II |
Антагонист β-адренорецепторов |
Снижает автоматизм синусового узла, симпатолитическая активность |
Пропранолол Соталол |
|
III |
Препарат, увеличивающий продолжительность потенциала действия |
Не влияет на проведение, замедляет реполяризацию |
Бретилий Амиодарон Соталол |
|
IV |
Антагонист Са2+ |
Замедляет скорость проведения в АВ-узле |
Верапамил Дилтиазем |
Классификация, разработанная Воганом Уильямсом, не помогает выбрать лекарственное средство, основываясь на механизме его действия. Так, РПД и re-entry могут быть мишенями для лекарственной терапии, однако препараты (в том числе и некоторые антиаритмические) могут содействовать появлению аритмии (проаритмии). Преобладающий эффект (про- или антиаритмический) лекарственного средства зависит от конкретного заболевания и дозы лекарства. В экспериментах на животных можно вызвать РПД с помощью антиаритмических средств класса III, но удается предотвратить reentry, применяя те же самые препараты. Лекарственные средства класса I содействуют возникновению re-entry, замедляя скорость проведения, и блокируют re-entry, превращая однонаправленную блокаду проведения в двунаправленную. Таким образом, сложно предсказать, каким будет конечный эффект антиаритмического средства — положительным или отрицательным.
Механизм действия антиаритмических средств класса I на молекулярном уровне заключается в блокаде Nа+-каналов сердца
Доминирующим молекулярным механизмом действия лекарственных средств класса I является блокада Nа+-каналов. Это приводит к блокаде входящего (деполяризующего) тока Na+ (клеточное действие). Механизм антиаритмической активности на тканевом уровне менее ясен, однако эксперименты на животных показали, что превращение однонаправленной блокады в двунаправленную способно предотвратить возникновение re-entry. Некоторые лекарства класса I обладают также дополнительным молекулярным эффектом, т.е. блокируют К+-каналы и, соответственно, реполяризующие токи К+. Это удлиняет эффективный рефрактерный период и может способствовать действию средств на re-entry (см. ранее).
Хинидин, идентифицированный Фреем в 1918 г., был первым антиаритмическим средством. С тех пор были синтезированы многие другие лекарственные средства класса I.
В конце 1970-х гг. антиаритмические средства были подразделены Харрисоном на 3 группы в зависимости от их действия на эффективный рефрактерный период желудочков (см. табл. 13.3). Все препараты класса I обладают общим свойством замедлять желудочковое проведение (что проявляется на ЭКГ широким комплексом QRS). Хинидин относят к лекарственным средствам группы Iа — он увеличивает интервал QJ (поскольку блокирует токи К+), а также замедляет проведение в терапевтических дозах. У хинидина, как и у других препаратов класса Iа, отсутствует избирательность действия на Na+- и К+-каналы, поэтому в настоящее время некоторые исследователи приписывают антиаритмические эффекты хинидина не блокаде Na+-Ka-налов, а его способности расширять интервал QT путем блокады К+-каналов сердца. Этот факт служит иллюстрацией того, что классификация лекарственных средств, разработанная Воганом Уильямсом, не всегда точно описывает молекулярный механизм действия, а позволяет лишь определить его на тканевом уровне.
Стандартная пероральная доза хинидина варьирует от 200 до 300 мг каждые 3-4 час вследствие индивидуальных различий фармакокинетики. Хинидин используют при терапии фибрилляции и трепетания предсердий (восстановление синусового ритма), синдрома Вольфа-Паркинсона-Уайта и желудочковой тахикардии, однако он не является препаратом первой линии. Подобно другим препаратам группы Iа, хинидин не снижает частоту внезапной сердечной смерти (т.е. фибрилляции желудочков) после ОИМ. Его атропиноподобные эффекты могут вызвать синусовую тахикардию. Предполагают, что менее частый побочный эффект — хинидино-вый обморок — возникает в результате индуцированной хинидином ЖТ torsades de pointes, особенно у пациентов с гипокалиемией, и может быть связан с расширением QT под влиянием хинидина. Метаанализ (см. главу 3) показывает, что назначение хинидина для лечения предсердных аритмий может повысить вероятность внезапной сердечной смерти. При использовании хинидина характерным (30% случаев) является раздражение ЖКТ, в более редких случаях появляется синдром «хинхонизма» (глухота, шум в ушах, неясное зрение, приливы крови и тремор). Хинидин повышает концентрацию дигоксина в крови, потенциально приводя к нежелательному лекарственному взаимодействию. Вместе с другими лекарственными средствами класса Iа хинидин противопоказан пациентам с АВ-блокадой, удлинением интервала QT или ЖТ torsades de pointes в анамнезе.
Побочные эффекты хинидина
- Тошнота
- Лихорадка
- Обморок
- Гемодискразия
- ЖТ torsades de pointes
Прокаинамид обладает сходными с хинидином электрофизиологическими и фармакологическими свойствами. Отличия состоят в более быстрой абсорбции при пероральном приеме, а также доступности препаратов для в/в и в/м введения. Его активный метаболит, N-ацетилпрокаинамид, обладает относительно избирательными антиаритмическими свойствами, характерными для класса III. В отличие от хинидина, прокаинамид в США разрешен для лечения только желудочковых, но не наджелудочковых аритмий. Его применяют в качестве препарата первой линии, нацеленной на подавление и профилактику желудочковой тахикардии, особенно при в/в введении в неотложных случаях. Отсутствуют данные о том, что прокаинамид снижает смертность от фибрилляции желудочков после ОИМ. Необходимость частого введения прокаинамида вследствие его быстрого метаболизма нередко является причиной нарушения пациентом схемы лечения, что может ослабить терапевтический эффект.
Побочные эффекты со стороны ЖКТ такие же, как при использовании хинидина. Прокаинамид может вызвать лейкопению и агранулоцитоз (иногда приводящий к летальному исходу), поэтому рекомендуется мониторинг числа клеток крови в первые 12 нед терапии. Редко встречаются тромбоцитопения и положительный тест Кумбса. Длительное применение (> 6 мес) ассоциировано с развитием волчаночноподобного синдрома, который отличается от системной красной волчанки лишь отсутствием поражения почек, меньшей тяжестью и более высокой обратимостью.
Дизопирамид, лекарственное средство класса Iа, сходен с хинидином по свойствам и показаниям для применения. Он оказывает особенно выраженные атропиновые эффекты. Антихолинергическое побочное действие включает неясное зрение, сухость во рту и задержку мочи у пожилых мужчин. Преимущество дизопирамида перед хинидином состоит в том, что отсутствует его нежелательное взаимодействие с дигоксином.
Этмозин (известный также как морицизин) относят к антиаритмическим средствам класса Iа. При ежедневном пероральном приеме в дозе 600-900 мг вызывает дозозависимое снижение частых ЖЭС и уменьшает частоту возникновения неустойчивой и устойчивой желудочковой тахикардии у пациентов с органическими заболеваниями сердца или без таковых. В клинических исследованиях было установлено, что этмозин, подобно ди-зопирамиду, пропранололу и хинидину, в исследованных дозах обладает антиаритмической активностью, которая сохранялась при длительном применении. Этмозин может оказаться эффективным в случаях, когда другие антиаритмические средства не дают положительного эффекта, являются непереносимыми и/или противопоказаны. Однако этот препарат не нашел широкого применения.
Лидокаин — прототипичное антиаритмическое средство класса lb. От других представителей этого класса он отличается тем, что предназначен исключительно для в/в введения и поступает в сердце в высоких концентрациях. Быстрый метаболизм лидокаина в печени делает его пероральное применение неприемлемым. Лидокаин мало влияет на нормальную ЭКГ, что характерно для лекарственных средств класса lb. Его электрофизиологические эффекты избирательно проявляются в случае ишемии миокарда и желудочковой тахикардии. Многие годы его использовали в ранней фазе ОИМ для снижения частоты возникновения фибрилляции желудочков. Однако, несмотря на его способность снижать частоту ЖЭС и даже фибрилляцию желудочков в этих условиях, лидокаин не оказывает благоприятного влияния на выживаемость в отдаленном периоде. При передозировке он действует на нервную систему, вызывая парестезии и судороги. Это особенно опасно для пациентов с гипотензией, у которых ослаблен кровоток через печень, что снижает элиминацию лидокаина. Для безопасного применения лидокаина необходим мониторинг терапии. Внутривенный способ введения обусловливает использование лидокаина при неотложной помощи, а не в качестве поддерживающей терапии. Также лидокаин используют как местный анестетик.
Мексилетин представляет собой антиаритмическое средство класса lb, активное при пероральном приеме. Ранее его использовали как антиконвульсант. Его применение ограничено исключительно подавлением ЖЭС и желудочковой тахикардии. Мексилетин не влияет на выживаемость после ОИМ, как и другие препараты класса lb. Неврологические побочные эффекты, не являющиеся строго дозозависимыми, носят общий характер (головокружение, парестезии, атаксия и тремор).
Благодаря своим фармакокинетическим свойствам мексилетин взаимодействует с антацидами, которые повышают желудочную абсорбцию мексилетина. Из-за незначительного связывания мексилетина с белками плазмы не происходит вытеснения лекарственных средств, обладающих высокой степенью связываемости с белками плазмы. Комбинация мексилетина с антагонистом β1адренорецепторов более эффективна, чем использование каждого из препаратов в отдельности, что позволяет снизить их дозы при подавлении желудочковых аритмий.
Токаинид — антиаритмическое средство класса lb, активное при пероральном применении. Используют реже, чем мексилетин.
Фенитоин представляет собой антиконвульсант, активный при пероральном применении, обладающий антиаритмическими свойствами лекарственных средств класса lb (например, лидокаина). Общие и антиконвульсивные свойства фенитоина представлены в главе 8. Как антиаритмическое средство фенитоин используют для лечения желудочковых аритмий, аритмий, индуцированных передозировкой дигиталиса, и ЖТ torsades de pointes.
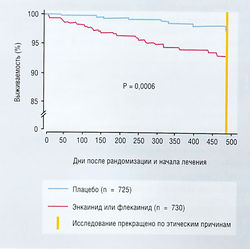
Флекаинид — прототипичное антиаритмическое средство класса Iс, характерными свойствами которого являются высокая активность и избирательность действия на Na+-каналы с медленной диссоциацией лекарства из них. Это вызывает определенные электрокардиографические эффекты (расширение QRS), связанные с замедленным проведением в нормальной ткани сердца при нормальной частоте сердцебиений (потенциально это опасно; см. далее). Флекаинид используют исключительно для лечения наджелудочковых аритмий (пароксизмальная наджелудочковая тахикардия, трепетание и фибрилляция предсердий). Он противопоказан пациентам с органическими заболеваниями сердца. Основанием для этого послужили результаты исследования Cardiac Arrhythmia Suppression Trial (CAST), показавшие, что флекаинид способен удваивать вероятность летального исхода у пациентов с инфарктом миокарда (рис. 13.11).
Рис. 13.11 Выживаемость пациентов по данным исследований с применением лекарственных средств, подавляющих аритмию. Обратите внимание, что пациенты были распределены на группы рандомизированным слепым методом и причиной летального исхода в каждом случае было заболевание сердца, п — число пациентов.
Предполагают, что этот побочный эффект обусловлен главным образом парадоксальным про-аритмическим действием: препарат подавляет не летальные ЖЭС, однако способствует возникновению аритмий (особенно фибрилляции желудочков), приводящих к летальному исходу. В настоящее время считают, что это происходит вследствие замедленного проведения в здоровых участках желудочка. Другие побочное эффекты флекаинида несущественны.
Энкаинид относится к лекарственным средствам класса Iс, сходным по своим свойствам и риску развития проаритмий с флекаинидом.
Пропафенон представляет собой мало используемый препарат класса Iс. По фармакологическим и проаритмическим свойствам сходен, по-видимому, с флекаинидом и энкаинидом. В исследовании CAST пропафенон не оценивали, поэтому сложно судить о строгом противопоказании к его применению при органических заболеваниях сердца и инфаркте миокарда. Пропафенон обладает слабой активностью антагониста β1адренорецепторов, которая может нейтрализовать проаритмические эффекты.
Таким образом, лекарственные средства класса I имели широкое применение, однако вследствие увеличения данных об их ограниченной эффективности в настоящее время их используют гораздо реже. Можно считать, что мексилетин, хинидин, дизопирамид и прокаинамид одинаково эффективны как средства, подавляющие желудочковые аритмии. Ни одно из лекарственных средств класса I не уменьшает вероятности летального исхода после ОИМ, и многие из них являются проаритмическими.
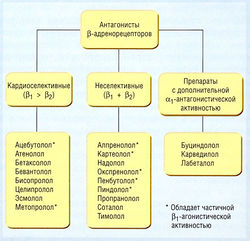
При действии антиаритмических средств класса II снижается активность симпатической нервной системы
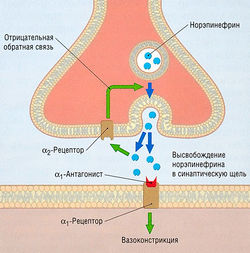
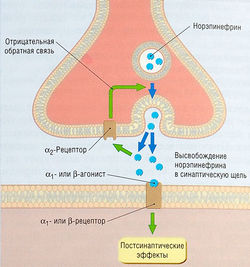
Антагонисты β-адренорецепторов (β-блокаторы) относят к числу наиболее широко применяемых лекарственных средств для лечения сердечно-сосудистых заболеваний. Их использование в качестве антиаритмических средств весьма ограничено по сравнению с терапевтическим применением при гипертензии, стенокардии и застойной сердечной недостаточности (ЗСН). В экспериментах на животных норэпинефрин и эпинефрин способны вызывать или усиливать аритмии, стимулируя β1, β2- и a1-адренорецепторы миокарда. Неадекватная активация адренорецепторов сердца (особенно β1) может способствовать развитию аритмогенеза, хотя это происходит лишь в период физической нагрузки или во время эмоционального стресса (когда тонус симпатической нервной системы высокий) либо у лиц с заболеваниями сердца. Прототипичным лекарственным средством класса II является пропранолол, неселективный β1 и β2-антагонист. β1-Антагонизм считают молекулярным механизмом действия антиаритмических средств класса II, хотя свой вклад также может вносить β2- и даже a1-антагонизм. Метопролол и эсмолол — кардиоселективные средства класса II, т.е. они являются сравнительно избирательными β1антагонистами (избирательность не 100% и уменьшается при повышении дозы).
Лекарственные средства класса II, в частности пропранолол, применяют с целью подавления фибрилляции и трепетания предсердий, связанных с физической нагрузкой и эмоциональным стрессом. Установлено, что некоторые β-блокаторы уменьшают смертность среди пациентов с инфарктом миокарда — преимущество, которое отсутствует при использовании антиаритмических средств любого другого класса. Такое благоприятное действие β-блокаторов может быть не связано с подавлением аритмии. Дозы, способы применения и побочные эффекты антагонистов βадренорецепторов см. далее («Стенокардия»).
Заболевания, при которых следует избегать применения β-блокаторов
- Астма
- Сахарный диабет с гипогликемическими реакциями
- Тяжелая перемежающаяся хромота
Побочные эффекты пропранолола
- Брадикардия
- Утомляемость
- Холодные конечности
Антиаритмические эффекты лекарственных средств класса III связаны с увеличением продолжительности потенциалов действия
Увеличение продолжительности потенциалов действия сердца антиаритмическими средствами класса III проявляется на ЭКГ удлинением интервала QT. Это ведет к подавлению re-entry, хотя может усилить РПД (см. ранее). Таким образом, возможны и анти-, и проаритмические эффекты в зависимости от механизма возникновения аритмии (РПД или re-entry). Бретилий, амиодарон, соталол (являющийся также β-блокатором), d-соталол (не β-блокатор) и дофетилид относят к препаратам класса III.
Бретилий — самое старое, но наименее эффективное средство класса III. Его адренергические нейронблокирующие эффекты свидетельствуют об отсутствии молекулярной избирательности и объясняют его побочные эффекты, например гипотензию.
Амиодарон был предложен в качестве коронарного вазодилататора, а его антиаритмические эффекты были обнаружены случайно. Хотя амиодарон обычно относят к антиаритмическим средствам класса III, он также блокирует Na+- и Са2+-каналы и в некоторой степени a-адренорецепторы. Он способен снижать экспрессию β1-адренорецепторов в миоцитах сердца, однако прямо с этими рецепторами не взаимодействует. Такое отсутствие селективности означает, что его молекулярные механизмы действия неясны и классификация его как препарата класса III вызывает сомнения. При в/в введении действие наступает довольно быстро (в течение 1 час), однако при пероральном применении его следует назначать по крайней мере за 3 нед до появления ожидаемого терапевтического эффекта. Т1/2 амиодарона очень длителен (> 50 сут), в связи с чем невозможно быстро повлиять на действие препарата путем изменения дозы.
Показано, что амиодарон эффективен в случае предсердных и желудочковых аритмий. Он намного эффективнее хинидина, препарата класса II, а также верапамила и дигиталиса подавляет пароксизмальную наджелудочковую тахикардию, связанную с синдромом Вольфа-Паркинсона-Уайта. Его эффективность при наджелудочковой тахикардии повышается при использовании в комбинации с дигоксином, хотя необходимо соблюдать осторожность, т.к. концентрация дигоксина в сыворотке быстро повышается в результате лекарственного взаимодействия.
Сочетание с антиаритмическими средствами класса IV может оказаться благоприятным при лечении тяжелой наджелудочковой тахикардии, однако необходимо принять меры, чтобы избежать АВ-блокады. Амиодарон способен предотвращать внезапную сердечную смерть, но побочные эффекты делают его длительное применение опасным. Одно из преимуществ амиодарона перед β-блокаторами — отсутствие противопоказаний для пациентов с общими заболеваниями, например астмой, диабетом, заболеванием коронарных артерий или почечной недостаточностью. В настоящее время амиодарон — наиболее распространенное антиаритмическое средство при жизнеугрожающих желудочковых аритмиях. Клинические исследования с участием реанимированных и переживших фибрилляцию желудочков пациентов показали, что амиодарон уступает автоматическому имплантируемому дефибриллятору по показателю 3-летней выживаемости. В более позднем исследовании с участием пациентов с дилатационной кардиомиопатией применяли следующую схему введения амиодарона: 400 мг 2 раза в день в течение 1 нед, затем 400 мг/сут в течение 51 нед и далее 300 мг/сут. Исследование было остановлено, поскольку результаты получить не удалось. Выживаемость пациентов без аритмии, при приеме амиодарона была выше, чем при использовании АИД (аритмии устранялись, но не предотвращались), а общая смертность за 4 года была одинаковой независимо от способа лечения — амиодароном или АИД. В исследовании MADIT II применение АИД улучшало выживаемость по сравнению со стандартной терапией амиодароном. Более широкое использование амиодарона, чем АИД, при их сходной эффективности отчасти объясняется более простым способом применения. Пациенты предпочитают принимать препарат, а не подвергаться хирургическому вмешательству для имплантации устройства.
Действие амиодарона на функции щитовидной железы сложное и терапевтически важное; у 14-18% пациентов отмечены гипер- или гипотиреоз. В печени амиодарон ингибирует 5-дейодиназную активность типа I фермента, дейодинирующего гормон щитовидной железы Т4, превращая его в Т3. В результате у эутиреоидных индивидов в сыворотке повышается концентрация Т4 и снижается уровень Т3. Амиодарон способен также изменять содержание TSH в сыворотке. Дозы выше 400 мг/сут повышают концентрацию TSH, которая затем возвращается к норме. Амиодарон может прямо влиять на синтез и секрецию TSH гипофизом. В ходе длительного лечения амиодароном у клинически эутиреоидных пациентов может произойти умеренное повышение или снижение концентрации TSH в сыворотке, что отражает состояние гипо- или гипертиреоза соответственно. Амиодарон снижает также число β-адренорецепторов и эффект Т3 на них. Кроме того, амиодарон вызывает снижение в печени транскрипции отвечающего на Т3 гена, который кодирует рецепторы липопротеинов низкой плотности и уменьшает экспрессию рецепторов гормонов щитовидной железы. Индуцированный амиодароном тиреотоксикоз встречается чаще в географических областях со сниженным уровнем употребления йода, тогда как гипотиреоз более распространен в местностях, где количество принимаемого йода в норме. Индуцированный амиодароном тиреотоксикоз типа II представляет собой деструктивный тиреоидит, приводящий к высвобождению переформированных тиреоидных гормонов из поврежденных фолликулярных клеток щитовидной железы. Это наиболее распространенная форма тиреотоксикоза, индуцированного амиодароном, в областях с нормальным содержанием йода в пище. Поскольку амиодарон назначают по жизненно важным показаниям (при аритмии), следует избегать прекращения его приема. Альтернативный подход состоит в лечении тиреотоксикоза типа II преднизоном в дозе 30-40 мг (или равноценным препаратом) в течение 3 мес, а тиреотоксикоза типа I — метимазолом и перхлоратом калия в течение 30-40 сут. Часто трудно отдать предпочтение одному из этих препаратов, в этом случае можно использовать тионамид, перхлорат калия и глюкокортикостероиды. Если отмена амиодарона недопустима, а лечение не дает эффекта, может потребоваться тиреоидэктомия. У некоторых пациентов индуцированный амиодароном гипотиреоз включает аутоиммунный компонент и ассоциирован с тиреоидитом Хашимото (установленный фактор риска). Он встречается чаще тиреотоксикоза и лучше поддается лечению (с помощью Т4).
Считают, что используемые в клинике лекарственные средства класса III обладают общим молекулярным механизмом действия, т.е. блокируют К+-каналы сердца. Однако другие эффекты на молекулярном уровне могут вести к удлинению потенциалов действия. Эти эффекты включают агонизм к a1-адренорецепторам и подавление инактивации Na+-каналов, которое может способствовать молекулярному механизму действия ибутилида — препарата, применяемого в США для лечения наджелудочковой тахикардии.
DL-соталол (обычно его называют просто соталол) относят к препаратам, сочетающим свойства лекарственных средств классов II и III. Он является блокатором β-адренорецепторов и К+-каналов. С этого препарата в 1980-х гг. началось активное применение более избирательно действующих (чистых) лекарственных средств. Предпосылкой послужило предположение: чем выше избирательность, тем сильнее эффект.
Применение препаратов класса III второго поколения началось с d-соталола — оптического изомера соталола, который действует на К+-каналы как препарат класса III, не влияя на адренергические (β1рецепторы. Он был первым чистым и сильнодействующим лекарственным средством класса III, не влияющим на К+-каналы в субмикромолярных концентрациях. Несмотря на это, он менее эффективен, чем DL-соталол, при лечении наджелудочковых аритмий и противопоказан пациентам с инфарктом миокарда. В клиническом исследовании Survival With Oral D Sotalol (SWORD) было показано, что этот препарат увеличивает смертность после инфаркта миокарда. Большинство используемых в настоящее время лекарственных средств класса III (например, дофетилид и клофилиум) избирательно блокируют изоформу замедленного реполяризующего быстрого тока — IКr. Это важный реполяризующий ток К+ в предсердиях и желудочках. К этим средствам относят и амиодарон (хотя он блокирует другие, не К+-каналы и рецепторы; см. ранее). Иные лекарственные средства класса III влияют на IКr и другие токи К+, воздействуя на каналы, ответственные за проведение кратковременного выходящего тока К+ (Ito; тедисамил), входящего тока К+ (IК1; терикалант) или АТФ-зависимого тока К+ (IК(атф); глибурид). Ни одно из этих лекарственных средств не используют в клинике из-за их побочных эффектов. Опасение, что ЖТ torsades de pointes может быть побочным эффектом, свойственным препаратам класса III, привело к тому, что большинство IКг-избирательных лекарственных средств класса III второго поколения (так же как большинство неселективных блокаторов К+-каналов) было изъято из обращения. Исключение составляет дофетилид, все еще широко используемый в клинике исключительно для лечения предсердных аритмий.
Побочные эффекты амиодарона
- Нарушения функций щитовидной железы
- Отложение в роговице
- Легочные заболевания
- Кожная пигментация
Побочные эффекты верапамила
- Брадикардия
- Тошнота и рвота
- Запоры
Антиаритмические средства класса IV являются антагонистами Са2+
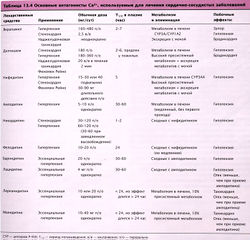
Блокаторы Са2+-каналов (Са2+-антагонисты) представляют собой лекарственные средства, блокирующие Са2+-каналы L-типа. Существует три типа препаратов этого класса, для которых прототипичными являются верапамил (фенетилалкиламиновое производное папаверина), дилтиазем (производное бензотиазепина) и нифедипин (производное 1,4-дигидропиридина). Эти средства используют для лечения различных сердечно-сосудистых заболеваний, включая гипертензию, стенокардию (все три типа препаратов) и аритмии (только верапамил и дилтиазем).
Верапамил является прототипичным антиаритмическим средством класса IV (табл. 13.4). Его эффекты:
- снижение скорости проведения в АВ-узле;
- снижение частоты импульсов в СА-узле;
- отрицательный инотропный эффект;
- расширение коронарных и периферических сосудов.
Дилтиазем обладает сходными с верапамилом фармакологическими свойствами. Оба антиаритмических средства применяют для лечения наджелудочковых аритмий. Клинические исследования антагонистов Са2+ с участием пациентов с заболеванием коронарных артерий не выявили эффективной супрессии желудочковых аритмий или снижения смертности. В связи с вазоселективной природой этих лекарственных средств максимальные безопасные дозы оказались недостаточными для подавления желудочковых аритмий. Несмотря на то что верапамил и дилтиазем оказывают достаточно выраженный эффект на АВ-узел и, в отличие от дигидропиридинов, обладают высокой сосудистой избирательностью, они не вызывают антиаритмический эффект. Механизмы избирательности действия антагонистов Са2+ на сосуды см. далее («Стенокардия»).
Аденозин как антиаритмическое средство выпадает из классификации, разработанной Воганом Уильямсом
Аденозин неактивен при пероральном приеме, однако может быть чрезвычайно эффективным, если его вводят в/в при лечении пароксизмальной наджелудочковой узловой тахикардии. Он имеет крайне короткий Т1/2, исчисляемый секундами, и его эффекты блокируют часто используемые препараты (теофиллин) и кофеин. Он является агонистом на уровне А1рецепторов аденозина в СА- и АВ-узле и предсердиях. После стимуляции рецепторов запускается каскад с активацией ингибирующего G-белка (Gi), который ведет к подавлению активности аденилилциклазы и другим эффектам, опосредуемым Gi, включая ослабление токов Са2+-каналов L-типа. Активация А1-рецепторов приводит к открытию К+-каналов, на которые действует ацетилхолин посредством того же трансдуцирующего каскада. Поскольку эти каналы отсутствуют в желудочках, указанные механизмы действия аденозина не влияют на желудочковые аритмии. Эффекты аденозина на тканевом уровне — гиперполяризация и уменьшение продолжительности потенциалов действия, что ведет к прекращению re-entry. Этим объясняются возможные эффекты: замедление желудочкового ритма во время фибрилляции предсердий, прекращение синусовой реципрокной тахикардии (редкое расстройство re-entry в СА-узле), прекращение пароксизмальной наджелудочковой тахикардии с re-entry через АВ-узел и устранение синдрома Вольфа-Паркинсона-Уайта, включая ретроградное проведение через АВ-узел (однако в последнем случае предпочтительнее применять препараты классов Iа и Iс, т.к. аденозин может увеличить тахикардию вследствие способности укорачивать предсердный рефрактерный период). Кроме того, посредством менее изученных механизмов стимуляция A1-рецепторов аденозином активирует КАТФ-каналы, что объясняет антиишемические эффекты аденозина в желудочках, отмеченные в доклинических исследованиях.
Побочные эффекты аденозина
- Ускорение тахикардии при синдроме Вольфа-Паркинсона-Уайта
- Фибрилляция предсердий при синдроме Вольфа-Паркинсона-Уайта
- Бронхоспазм и гипотензия
Аденозин может вызывать бронхоспазм у пациентов с астмой, поэтому таким пациентам этот препарат противопоказан.
CVT-510 (текаденосон) — избирательный А1агонист, проходящий клинические исследования как средство лечения наджелудочковой тахикардии. Он обладает большей избирательностью по отношению к АВ-узлу, чем аденозин.
Существует 4 типа рецепторов аденозина: A1, А2А, А2В и А3. Активация А2А-рецепторов коронарных сосудов вызывает их расширение, однако в клинической практике (например, при стенокардии) этот эффект не используют.
Сердечные гликозиды дигиталиса используют главным образом для лечения сердечной недостаточности с дополнительным антиаритмическим эффектом
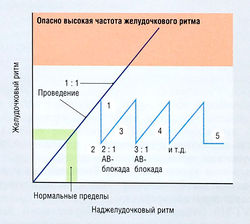
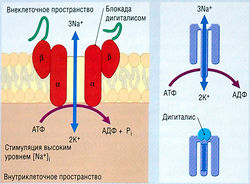
Дигиталис применяют для лечения предсердных аритмий. Механизм его действия необычен. Предсердные аритмии могут так ускорить желудочковый ритм, что он станет слишком быстрым для эффективного диастолического наполнения, и сердечный выброс уменьшается. Дигиталис превращает трепетание предсердий в фибрилляцию за счет укорочения рефрактерного периода предсердий, но в действительности он замедляет желудочковый ритм, воздействуя на АВ-узел (рис. 13.12).
Рис. 13.12 Необычный механизм, посредством которого дигиталис устраняет наджелудочковую тахикардию. (1) Дигиталис удлиняет рефрактерный АВ-период, вызывая высвобождение ацетилхолина блуждающим нервом. (2) Это вызывает АВ-блокаду 2 : 1.(3) Дигиталис также укорачивает рефрактерный период предсердий, усиливая наджелудочковую тахикардию. (4) Это углубляет АВ-блокаду (т.к. время АВ-восстановления снижено). (5) Возникает АВ-диссоциация, приводящая к восстановлению более безопасного желудочкового ритма. АВ — атриовентрикулярный.
Как только желудочковый ритм стабилизируется, фибрилляция предсердий может быть устранена с помощью электроразряда. Однако в зависимости от предполагаемой длительности фибрилляции предсердий может оказаться необходимым предварительное введение пациенту гепарина или варфарина: при фибрилляции предсердий (особенно хронической) вследствие стаза в полости предсердий может образоваться тромб, который после восстановления синусового ритма может быть вытолкнут в сосудистое русло и вызвать инсульт. Дигиталис нельзя использовать при желудочковой тахикардии, вызванной синдромом Вольфа-Паркинсона-Уайта, т.к. дополнительный путь проведения позволяет желудочкам «следовать» за предсердиями и фибриллировать. Антиаритмическим средством выбора служит сердечный гликозид дигоксин.
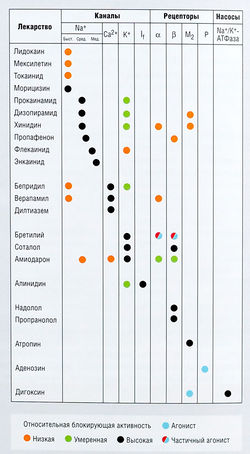
Классификация антиаритмических лекарственных средств «Сицилианский гамбит», предложенная Task Force of the Working Group on Arrhythmias of the European Society of Cardiology, представляет собой подход, альтернативный классификации, разработанной Воганом Уильямсом (рис. 13.13). Неясно, дает ли эта классификация более правильное и точное описание механизма действия антиаритмических средств, поэтому классификация, разработанная Воганом Уильямсом, все еще остается ведущей.
Рис. 13.13 Классификация антиаритмических средств «Сицилианский гамбит». Это альтернативная классификация антиаритмических средств, предложенная Task Force of the Working Croup on Antiarrhythmias of the European Society of Cardiology. Ha этой схеме представлено действие разнообразных антиаритмических средств на ионные каналы, рецепторы и ионные насосы. If — активированный гиперполяризацией ток; М2 — мускариновые рецепторы подтипа 2; Р — пуринергические рецепторы [Circulation 1991; 84: 1831. Copyright 1994 American Heart Association].
Острый инфаркт миокарда[править | править код]
При патологических процессах, лежащих в основе стенокардии (особенно нестабильной), могут возникнуть потенциально необратимая сосудистая непроходимость и сохраняющаяся ишемия. Это начало острого инфаркта миокарда. Кроме того, ОИМ может возникнуть внезапно и неожиданно у пациентов, которые до этого чувствовали себя хорошо. Клинические признаки и симптомы ОИМ подробно описаны. Термином «инфаркт» обозначают погибшую (рубцовую) ткань. Прежде чем возникнет инфаркт, ткань миокарда должна подвергнуться тяжелой ишемии в течение более 60 мин. В клинике термин «инфаркт» используют для обозначения тяжелой необратимой региональной ишемии миокарда. Хотя ОИМ включает процессы (например, стенокардию и желудочковую аритмию), которые уже были описаны в данной главе, его лечение требует специального рассмотрения. Поставить диагноз «инфаркт» помогает ЭКГ, на которой наиболее ранние признаки ишемии проявляются как подъем или депрессия сегмента ST, а последующее развитие инфаркта определяют по появлению зубца Q в отведениях от конечностей.
Раннее паллиативное вмешательство при остром инфаркте миокарда[править | править код]
Раннее паллиативное вмешательство начинают сразу после поступления пациента в больницу или раньше, если возможно: пациенту в/в вводят морфин для устранения боли в груди.
Морфин оказывает благоприятные системные эффекты
- Успокаивает боль в груди благодаря анальгетическим свойствам (см. главу 8).
- Обладает относительной избирательной способностью снижать преднагрузку (венозный тонус) и постнагрузку (артериальный тонус).
- Уменьшает страх у возбужденного пациента, повышает симпатический тонус.
Переадресованная активность симпатической нервной системы снижает потребность миокарда в кислороде, тем самым способствуя уменьшению боли в груди и, возможно, замедляя прогрессирование ишемических поражений.
Раннее терапевтическое вмешательство при остром инфаркте миокарда[править | править код]
Ограничить гибель клеток сердца у пациентов с ОИМ — самая важная задача раннего терапевтического вмешательства. Для ее решения необходима реперфузия ишемического миокарда, которую проводят с помощью механического вмешательства, включая ЧКВ (т.е. катетеризации сердца), и назначения соответствующих лекарственных средств (см. ранее). В более поздние сроки, после стабилизации, можно прибегнуть к искусственной замене пораженной коронарной артерии (агентированию) в комбинации с лекарственной терапией. Для выбора тактики лечения необходим индивидуальный подход к каждому пациенту.
Тромболитические средства способствуют реперфузии и снижают риск реокклюзии и вторичного ОИМ
Тромболитики обладают различным механизмом действия (см. главу 10). Их нужно ввести в/в, п/к или внутрикоронарно как можно раньше после появления первых симптомов ОИМ. К тромболитикам, вводимым в/в, относят тканевый активатор плазминогена, рекомбинантный tPA (алтеплаза), стрептокиназу и гепарин. Они наиболее эффективны для реперфузии при ОИМ, т.к. тромбоз — наиболее частая причина коронарной окклюзии в случае ОИМ. В/в введение гепарина как вспомогательного средства при реперфузии так же снижает частоту возникновения вторичного ОИМ и летального исхода (см. рис. 13.19), как и введение стрептокиназы (внутрикоронарно на протяжении 1 час). Аспирин (перорально) снижает риск вторичного ОИМ и летального исхода, если начать его прием немедленно и продолжать длительное время (см.рис. 13.18). Оптимальной является комбинация стрептокиназы и аспирина, тогда как гепарин в качестве монотерапии (вводимый п/к или в/в) не дает дополнительного преимущества ни как вспомогательное средство, ни как заменитель стрептокиназы. Было отмечено, что п/к введение пациентам с ОИМ гепарина, который абсорбируется непредсказуемо, способно привести к летальному исходу в результате кровоизлияния в мозг. Стрептокиназа, вызывая расстройства, связанные с кровотечением, еще и антигенна и может индуцировать аллергические реакции у некоторых пациентов.
tPA более эффективен как тромболитик, чем стрептокиназа, для лечения ОИМ, а его рекомбинантная форма (алтеплаза) не аллергенна. tPA представляет собой эндогенный фермент, инициирующий каскад внеклеточных процессов (см. главу 10). Он активирует плазминоген (профермент) с образованием плазмина (фермент). Плазмин способен гидролизовать фибрин — неотъемлемый компонент структуры тромба. При ускоренном в/в введении 100 мг алтеплазы в течение 90 мин пациентам с ОИМ клиренс (выведение) лекарственного средства из плазмы происходит с конечным Т1/2, равным 72 мин. Клиренс алтеплазы опосредован главным образом печенью. Начальный объем распределения приближается к объему плазмы. Алтеплазу используют также при ишемическом инсульте (см. ранее). В США ее применяют в качестве препарата первой линии, а в других странах алтеплаза вытеснила стрептокиназу, которая дешевле и почти так же эффективна. Однако образование антител к стрептокиназе (в результате предшествующей инфекции, вызванной стрептококками, или ее применения ранее с лечебной целью) ограничивает использование алтеплазы. И стрептокиназу, и алтеплазу для получения наибольшего эффекта следует вводить в кровеносный сосуд. Внутрикоронарное введение стрептокиназы более эффективно, чем в/в, тогда как алтеплаза достаточно эффективна и при в/в инъекции.
Одна из форм стрептокиназы имеет в 4 раза больший Т1/2 в плазме по сравнению с исходным препаратом. Это АПСК, или антистреплаза. Одно из преимуществ АПСК по сравнению со стрептокиназой и алтеплазой — удобство применения. Благодаря более длительному Т1/2 АПСК при однократном болюсном в/в введении дает такой же реперфу-зионный эффект, как внутрикоронарная или в/в инфузия стрептокиназы или алтеплазы. Два других активатора плазминогена, тенектеплазу и ретеплазу, используют в США. Лечение должно быть начато как можно раньше, после появления первых симптомов ОИМ. Ретеплаза — негликозилированный аналог алтеплазы с более длительным, чем у алтеплазы, Т1/2 назначают 2 болюсные инъекции по 10 миллионов единиц с интервалом 30 мин. Тенекте-плаза тоже аналог алтеплазы, более стойкий к деградации активатором-ингибитором-1 плазминогена, чем алтеплаза или ретеплаза, т.е. имеет более длительный Т1/2, поэтому тенектеплазу можно назначать в виде однократной болюсной в/в инъекции (30, 40 или 50 мг, 200 ЕД/мг). Она снижает уровень циркулирующих фибриногена (на 4-15%) и плазминогена (на 11-24%). Клиническое значение избирательности лекарственного средства по отношению к фибрину с учетом риска кровотечения или эффективности не было определено, однако имеющиеся данные указывают на небольшое снижение риска по сравнению с алтеплазой. Чтобы снизить риск кровотечения, рекомендуют дозировать тенектеплазу по массе тела — 0,5-0,6 мг/кг. При введении тенектеплазы также необходимо предусмотреть возможность проведения антиаритмической терапии в случае возникновения брадикардии, индуцированной реперфузией, и/или желудочковой аритмии. При лечении пожилых пациентов важно тщательно оценить соотношение пользы лекарства (снижение смертности) и риска возникновения побочных эффектов, включая кровотечение. Примерно у 5% пациентов регистрируют значительное кровотечение, вызывающее необходимость проведения гемотрансфузии или ведущее к нарушению гемодинамики.
Ингибиторы тромбина — это другой класс антитромботических средств, используемых при ОИМ
Ингибиторы тромбина блокируют рецепторы тромбина или его действие. Молекулы некоторых ингибиторов имеют сложную структуру (например, НМГ), и их концентрацию в крови трудно измерить. В связи с этим их дозировку выражают в ME активности антифактора Ха (анти-Ха). НМГ как класс частично метаболизируется путем десульфатирования и деполимеризации. Ревипарин — недавно появившийся НМГ, который при п/к введении в пределах 12 час после появления симптомов ОИМ и 2 раза в день в течение 7 сут снижает основные общие показатели (повторный инфаркт миокарда или инсульт на протяжении по меньшей мере 30 сут, летальный исход), однако его влияние на выживаемость в отдаленном периоде не установлено. Существует небольшое повышение абсолютного числа опасных для жизни кровотечений, но польза применения препарата превосходит его риск.
Применение нитратов для лечения ОИМ
Спазм сосудов в отсутствие тромбоза редко бывает единственной причиной ОИМ, но дополнительное назначение нитратов пациентам с тромботической окклюзией полезно, т.к. это уменьшает преднагрузку и боли в груди, особенно при повышенном кровяном давлении. Однако вклад нитратов в повышение длительности выживаемости как следствие их способности содействовать реперфузии незначителен.
Другие лекарственные средства, используемые для лечения острого инфаркта миокарда[править | править код]
Разнообразные лекарственные средства, применяемые для лечения ОИМ, не устраняют ишемию миокарда как таковую, а влияют на эффекты, вызываемые ишемией. К этим препаратам относят β-блокаторы, аспирин, антиаритмические средства и (при особых обстоятельствах) симпатомиметические средства:
- симпатомиметические средства используют лишь для экстренного лечения кардиогенного шока и обсуждаются в первую очередь;
- антиаритмические средства могут вызвать немедленный благоприятный эффект (подавление аритмии); они не улучшают показатели выживаемости в отдаленном периоде;
- β-блокаторы и аспирин могут не оказать немедленного эффекта, однако они улучшают выживаемость в отдаленном периоде;
- как только состояние пациента стабилизируется, настоятельно рекомендуется продолжать прием аспирина и β-блокаторов.
Симпатомиметические средства используют для лечения кардиогенного шока при ОИМ
Кардиогенный шок может осложнить ОИМ. Шок возникает при тяжелом нарушении минутного объема сердца и обычно обусловлен обширным поражением сердечной мышцы. Прогноз очень плохой, с высоким процентом летального исхода. Неотложное лечение (до хирургического вмешательства; см. далее) состоит во в/в введении агонистов адренорецепторов, активирующих β1-рецепторы сердца (норэпинефрин, дофамин или добутамин). Целью является использование наименьшей дозы, достаточной для улучшения состояния ЦНС и коронарного кровотока без повышения пред- или постнагрузки. Терапевтический интервал узкий; частые побочные эффекты — отек легких и усиление сердечной недостаточности. Важно как можно быстрее провести поддерживающее хирургическое вмешательство с применением внутриаортального баллона (который расправляется и спадается синхронно с циклом сердца, таким образом минутный сердечный выброс в коронарные и сонные артерии увеличивается).
Антиаритмические средства используют для устранения аритмии в острой фазе ОИМ
Желудочковую аритмию, не угрожающую жизни пациента, можно устранить в/в введением лидокаина. Если при поступлении в больницу у пациента присутствует желудочковая тахикардия, используют прокаинамид (в/в). При фибрилляции желудочков необходима электрическая кардиоверсия. Для лечения и профилактики часто возникающих рецидивов фибрилляции желудочков и гемодинамически нестабильной желудочковой тахикардии применяют в/в введение амиодарона пациентам, рефрактерным к другим способам терапии. Использование этих лекарственных средств значительно варьирует в разных странах и лечебных учреждениях. Ускоренный идиовентрикулярный ритм, возникающий в результате аномального автоматизма в пораженных инфарктом волокнах Пуркинье (через 2 час или более после острой фазы), можно подавить введением атропина, который, блокируя мускариновые М2-рецепторы в СА-узле и повышая его активность, восстанавливает синусовый ритм.
Применение антиаритмических средств для повышения выживаемости после ОИМ после стабилизации состояния пациента нельзя оценить однозначно
С помощью метаанализа было показано, что в/в введение лидокаина не влияет на одногодичную выживаемость пациентов, однако в некоторых странах его продолжают вводить непосредственно после ОИМ (даже если желудочковая аритмия отсутствует или минимальна). Хотя лидокаин способен сразу же подавить не угрожающие жизни аритмии, он не увеличивает длительность выживания, и его применение может оказаться нежелательным из-за побочного действия на ЦНС (в частности, парестезии) и сердечно-сосудистую систему (асистолия).
Длительное применение антиаритмических средств класса I (прокаинамид, хинидин) или класса III (соталол, амиодарон) после острой фазы ОИМ спорно, поскольку препараты не купируют фибрилляцию желудочков и имеют побочные эффекты (включая проаритмии) (см. ранее). Другие антиаритмические средства классов I и III можно применять длительно, однако их влияние на выживаемость не изучено (исследования CAST и SWORD; см. ранее). Препараты класса II — единственные антиаритмические средства, способность которых снижать смертность от ОИМ в течение года после выписки пациента из больницы доказана, хотя механизм действия этих лекарственных средств неясен (и даже может быть не связанным с подавлением аритмии).
Рестеноз и стенты, элюирующие лекарственные средства, после ОИМ и при нестабильной стенокардии
Хирургическая операция на коронарных артериях возможна непосредственно после ОИМ, а также при нестабильной стенокардии. Стенты представляют собой искусственные кровеносные сосуды, используемые для замены пораженных атеросклерозом артерий, особенно коронарных, которые невозможно восстановить другими способами. Стенты, элюирующие лекарственные средства, высвобождают препараты из своего матрикса. Стент обеспечивает высокую концентрацию местно высвобождаемого препарата. Такой способ доставки лекарственного средства можно использовать для эффективных средств, но способных вызывать серьезные побочные эффекты при их распределении по организму после системного введения. В настоящее время существуют многочисленные разнообразные стенты, элюирующие лекарственные средства, которые оказывают антитромботическое, антипролиферативное и противовоспалительное действие: сиролимус, такролимус, эверолимус, АВТ-578, биолимус, паклитаксел, QP2, дексаметазон, 17β-эстрадиол, батимастат, актиномицин D, метотрексат, ангиопептин, ингибиторы тирозинкиназ, винкристин, митомицин, циклоспорин и антисмысловые препараты С-тус (Resten-NG, AVI-4126). Только для трех из этих лекарственных средств их эффективность доказана в рандомизированных исследованиях — паклитаксела, сиролимуса и эверолимуса. Существенный эффект при конечной ангиографической оценке не обязательно равноценен существенному клиническому эффекту. Безопасность и эффективность ЧКВ в незащищенных левых главных коронарных артериях все еще являются спорными. В США применение стентов, элюирующих лекарственные средства, остается предметом исследований.
Сиролимус (ранее известный как рапамицин) и такролимус ингибируют активацию Т-лимфоцитов, как полагают, разными способами, хотя точный механизм их действия неизвестен.
Экспериментально установлено, что такролимус связывается с внутриклеточным белком FKBP-12. Затем образуется комплекс такролимус-БКВР-12 с Са2+, кальмодулином и кальцинейрином, и фосфатазная активность кальцинейрина подавляется. Этот эффект предотвращает дефосфорилирование и транслокацию NFAT — ядерного компонента, предположительно инициирующего транскрипцию генов, ответственных за образование лимфокинов (таких как IL-2, у-интерферон). В итоге подавляется активация Т-лимфоцитов, т.е. происходит иммуносупрессия. Хотя сиролимус напоминает такролимус, связываясь с FKBP-12, такролимус блокирует транскрипцию генов цитокинов (например, IL-2).
Сиролимус действует позднее, блокируя IL-2-зависимую пролиферацию Т-клеток и стимуляцию, обусловленную перекрестным связыванием CD28, возможно подавляя активацию киназы, которая у млекопитающих служит мишенью для рапамицина или mTOR. Это серин-треонинкиназа, играющая важную роль в клеточном цикле. Таким образом, считают, что сиролимус действует синергично с такролимусом, супрессируя иммунную систему. Такролимус используют также при атопическом дерматите, а сиролимус — для профилактики отторжения аллотрансплантата почки. Цилостазол (см. далее «Тромбоз вен») применяют для предотвращения рестеноза у пациентов, перенесших коронарную ангиопластику и имплантацию стента, а также у пациентов, имеющих в анамнезе инсульт, для профилактики повторного инфаркта мозга.
Лечение синдромов, имеющих отношение к острому инфаркту миокарда (острые коронарные синдромы)[править | править код]
Хотя существуют разнообразные методы лечения ОИМ, общий результат (т.е. выживаемость) остается плохим. Снижение одногодичной смертности при оптимальном использовании всех доступных вмешательств составляет 20-30%. К несчастью, у многих пациентов первым симптомом ОИМ является фибрилляция желудочков, и 35-50% пациентов погибает при первом ОИМ вне больницы, еще до получения медицинской помощи. Таким образом, пациенты с наивысшим риском летального исхода в большинстве случаев не попадают в статистку, учитывающую эффективность вмешательств. В отдаленный период предотвращение коронарной болезни сердца посредством соответствующей диеты, а также исключением факторов риска, например курения, в сочетании с применением АИЛ для пациентов группы высокого риска острой коронарной обструкции, вероятно, будет более эффективным, чем фармакологическое вмешательство после острого процесса.
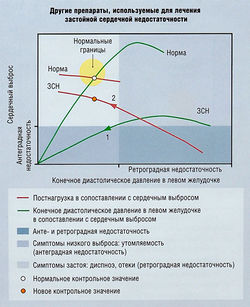
Застойная сердечная недостаточность[править | править код]
ЗСН является наиболее частой причиной госпитализации лиц старше 65 лет в США с ежегодной регистрацией более 400 000 новых случаев. Диагноз ставят на основании нарушения сердечной функции и ухудшения переносимости физической нагрузки. Основные причины ЗСН — ишемическая болезнь сердца, гипертензия, заболевание сердечных клапанов и кардиомиопатия. Установление причины влияет на выбор лекарственной терапии.
Сердечная недостаточность — неспособность сердца обеспечить сердечный выброс, достаточный для потребностей организма
Термин «застойный» относится к переполнению венозной системы кровью и связанному с ним тканевому отеку. Центральное венозное давление, определяющее отечность, известно как преднагрузка. Сердце может не обеспечивать достаточного сердечного выброса по различным причинам, в том числе из-за:
- утраты жизнеспособных миоцитов (кардиомиопатия) вследствие инфаркта, инфекции или действия химических/лекарственных средств (например, кобальта/адриамицина);
- избыточной резистентности при сердечном выбросе (известной как постнагрузка) в результате артериальной гипертензии или стеноза аорты;
- дефектов клапанов (например, регургитации крови при недостаточности митрального клапана) и тахикардии (в частности, при тиреотоксикозе), снижающих ударный объем сердца.
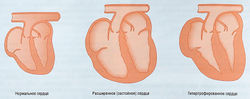
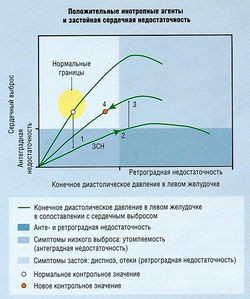
В любом случае вслед за острым нарушением сердечного выброса наступает прогрессирующее ухудшение гемодинамики. Это происходит потому, что рефлекторный ответ на изменение сердечного выброса вынуждает жизнеспособный миокард работать сильнее. Данное обстоятельство может привести к гипертрофии и утолщению стенки желудочков (неблагоприятное ремоделирование). Такое сердце изначально работает в качестве насоса менее эффективно. ЗСН становится симптоматической, если органы начинают получать недостаточно оксигенированную кровь или если центральное венозное давление повышается настолько, что возникают отеки (табл. 13.9).
Таблица 13.9 Симптомы, ассоциированные с застойной сердечной недостаточностью
|
Острая ЗСН |
Хроническая ЗСН |
|
Тахикардия |
Различные аритмии |
|
Одышка (диспноэ) |
Гипертензия |
|
Отек (периферический и/или легочный) |
Кардиомегалия |
|
Сниженная устойчивость к физическим нагрузкам |
Отек (периферический и/или легочный) |
Острая ЗСН возникает при воздействии лекарственных средств в токсических дозах на сердечную мышцу или вследствие окклюзии коронарной артерии, обычно в результате тромбоза.
Хроническая ЗСН возникает при повреждении сердца патологическими процессами, например вследствие первичной гипертензии или ишемии миокарда и ОИМ, или при воздействии лекарственных средств (например, адриамицина и кобальта); выжившие миоциты часто гипертрофируются.
Кардиомиопатическая ЗСН может быть острой или хронической и обычно поражает оба желудочка. Классификация кардиомиопатий основана на физиологических и анатомических признаках (рис. 13.20, 13.21). Кардиомиопатический миокардит, вызываемый бактериальной инфекцией, может привести к гибели миоцитов и недостаточности процессов возбуждения-сокращения выживших миоцитов.
Заболевания, способствующие развитию застойной сердечной недостаточности
- Кардиомиопатия
- Ишемия и инфаркт миокарда
- Гипертензия
- Заболевания клапанов сердца
- Врожденные заболевания сердца
- Коронарная болезнь
Левожелудочковая сердечная недостаточность (наиболее частая форма) характеризуется уменьшением сердечного выброса и снижением кровяного давления, а также отеком легких
Левожелудочковая недостаточность, сопровождающаяся снижением его препульсивной силы, приводит к уменьшению сердечного выброса и снижению кровяного давления (антеградная недостаточность), а уменьшение присасывающей силы — к венозному застою в легких (ретроградная недостаточность). Кровяное давление падает не всегда, т.к. задержка жидкости может компенсировать нарушение сердечного выброса, однако, если это происходит, возможно развитие отека.
Правожелудочковая сердечная недостаточность характеризуется диспноэ, отеками и усталостью
Признаки правожелудочковой сердечной недостаточности (диспноэ, отеки и усталость) возникают вследствие ретроградной недостаточности. В этих условиях и центральное венозное давление, и давление в правом предсердии повышены, что приводит к общему венозному застою. Любое препятствие поступлению крови в правый желудочек или избыточная нагрузка на правый желудочек могут утяжелить это состояние. В результате возникает левожелудочковая недостаточность, т.к. потребность левого желудочка в оксигенированной легочной венозной крови не может быть восполнена.
Клинические признаки застойной сердечной недостаточности
- Уменьшение силы сокращения сердца
- Снижение минутного объема сердца
- Ухудшение кровоснабжения тканей
- Повышение периферической сосудистой резистентности
- Отеки
Компенсаторные рефлексы сначала облегчают, а затем утяжеляют симптомы сердечной недостаточности
Независимо от типа сердечной недостаточности и сердечный выброс, и кровяное давление (часто, но не всегда) снижаются. Сердечно-сосудистая система компенсирует это снижение, поначалу поддерживая адекватное кровоснабжение органов и тканей. Обычно происходят два процесса:
- активация внешних нейрогуморальных рефлексов;
- внутренняя сердечная компенсация (рис. 13.22). Совместно оба эти процесса улучшают функцию сердца. Однако при длительном существовании симптомов тяжесть сердечной недостаточности нарастает вследствие неблагоприятного ремоделирования.
Внешние нейрогуморальные рефлексы первоначально способствуют поддержанию величины сердечного выброса и кровяного давления при ЗСН
Гипотензия активирует барорецепторы, которые повышают активность симпатической нервной системы, приводя к учащению сердцебиений и сужению сосудов, поэтому сократимость сердечной мышцы и артериолярная резистентность возрастают. Артериолярная резистентность повышает постнагрузку сердца, определяемую как сопротивление, которое должна преодолеть сердечная мышца, чтобы вытолкнуть кровь из желудочков. Когда сопротивление повышается, выбрасываемая фракция (количество крови, выталкиваемой из желудочков при каждом сердечном сокращении) и перфузия печени, почек и других органов снижаются. Уменьшение кровоснабжения почек активирует ренин-ангиотензиновую систему, вызывая секрецию ренина, повышающего образование ангиотензина II плазмы. Вслед за этим ангиотензин II высвобождает альдостерон из коры надпочечников.
Ангиотензин II вызывает периферическую вазоконстрикцию, тогда как альдостерон повышает задержку Na+, приводя к определенной последовательности событий:
- увеличению задержки воды;
- повышению венозного и артериального кровяного давления;
- увеличению объема сосудистой и интерстициальной жидкости;
- повышению системного и легочного застоя и отека;
- увеличению сердечной преднагрузки (см. рис. 13.22).
Рис. 13.22 Основные внешние нейрогуморальные компенсаторные механизмы при застойной сердечной недостаточности. (1) Начальным процессом является снижение сердечного выброса. (2) Рефлекторная симпатическая компенсация может увеличить сердечный выброс, однако (3) ассоциированное с этим повышение постнагрузки способно снизить сердечный выброс. Каскад других процессов может привести к гипертрофии сердца (4) в результате действия ангиотензина II на сердце, повышающего сердечный выброс и задержку Na+. Минутный объем сердца возрастает (5) вследствие увеличения преднагрузки и конечного диастолического давления в левом желудочке, однако это может привести к летальному исходу в результате развития отека легких. АПФ#- ангиотензинпревращающий фермент.
Внутренние компенсаторные механизмы сердца активируются под влиянием увеличения сердечной преднагрузки
Возникающие изменения сердца включают:
- расширение желудочков. Объем желудочковой камеры возрастает как следствие растяжения, а также гипертрофии и ремоделирования, опосредованных нейрогуморальными механизмами. Сначала это увеличивает объем крови, выталкиваемой при каждом сокращении сердца;
- увеличение давления, генерируемого желудочками.
По мере нарастания преднагрузки увеличиваются наполнение желудочков и конечное диастолическое давление, что первое время поддерживает величину сердечного выброса за счет повышения силы мышечного сокращения (инотропный эффект). Развиваемое в камерах сердечной мышцы давление зависит от степени растяжения мышечного волокна в покое (т.е. преднагрузки в начале сокращения). Это соотношение описывают кривой длина-напряжение сердечной мышцы, эквивалентом которой в интактном сердце является кривая Франка-Старлинга желудочковой функции (ем. рис. 13.26).
Гипертрофия и растяжение, развивающиеся как следствие ЗСН, увеличивают массу сердечной мышцы, что облегчает желудочковую систолу и повышает эффективность выброса крови из желудочков. Этот адаптивный механизм снижает напряжение стенки желудочков.
Соотношение между напряжением (стрессом) стенки сердца и давлением в желудочковой камере носит название закона Лапласа: Т = (Р X r)/w (где Т — напряжение, развивающееся в стенке сердечной мышцы; Р — трансмуральное давление; г — радиус желудочка; w — толщина стенки). Если не облегчить напряжение стенки желудочка, возникает тяжелое повреждение. Но из закона Лапласа следует, что между изменением напряжения стенки желудочка и ее толщиной существует обратная зависимость, и гипертрофия желудочка может уменьшить развивающееся напряжение стенки по мере увеличения преднагрузки. Однако этот адаптивный процесс не в состоянии долго компенсировать ЗСН. Со временем желудочки обычно становятся гораздо менее работоспособными, чем в норме, и сердечный выброс уменьшается.
Компенсаторные механизмы, активируемые во время ЗСН, проявляются в виде положительной инотропии
Повышение силы сокращения мышц ([+dP/dt]max) носит название положительной инотропии. Она возникает как следствие усиленной симпатической стимуляции сердца и активации β1-адренорецепторов желудочков и ведет к повышению эффективности систолического выброса. Но благоприятный эффект этого компенсаторного механизма не может поддерживаться долго. Развивается недостаточность в результате перегрузки желудочков, возникающей вследствие повышения давления в желудочках при их наполнении, систолического стресса стенки и повышенной потребности миокарда в энергии.
Лечение застойной сердечной недостаточности[править | править код]
Существует две фазы ЗСН: острая и хроническая. Лекарственная терапия должна не только облегчить симптомы заболевания, но и снизить смертность. Эффект лекарственной терапии наиболее благоприятен в тех случаях, когда ЗСН возникла вследствие кардиомиопатии или артериальной гипертензии. Цель лечения состоит в том, чтобы:
- уменьшить застой (отеки);
- улучшить систолическую и диастолическую функции сердца (табл. 13.10). Для достижения этой цели используют различные лекарственные средства (рис. 13.23).
Рис. 13.23 Лекарственные средства, используемые для лечения застойной сердечной недостаточности на разных стадиях. Медленное падение функции желудочков с возрастом усиливается в результате заболевания. АПФ — ангиотензинпревращающий фермент.
Сердечные гликозиды используют для лечения сердечной недостаточности более 200лет
Дигоксин — прототипичный сердечный гликозид, экстрагируемый из листьев пурпурной и белой наперстянки (Digitalis purpurea и D. lanata соответственно). Дигоксин — наиболее распространенный препарат из группы сердечных гликозидов, применяемых в США.
Все сердечные гликозиды обладают сходной химической структурой. Дигоксин, дигиталис и оубаин содержат агликоновое стероидное ядро, имеющее значение для фармакологической активности, а также ненасыщенное, связанное с С17 лактоновое кольцо, обладающее кардиотоническим действием, и связанный с СЗ углеводный компонент (сахар), влияющий на активность и фармакокинетические свойства гликозидов.
Таблица 13.10 Лекарственная терапия застойной сердечной недостаточности
|
Проблема |
Подход |
|
Утомляемость |
Отдых, положительные инотропные средства |
|
Отек |
Диета (ограничение соли), диуретики, гликозиды |
|
Плохая сократимость миокарда |
Положительные инотропные средства |
|
Одышка |
Диуретики (тиазиды/цикл) |
|
Застой |
Нитровазодилататоры |
|
Увеличение сердечной пред- и постнагрузки |
Ингибиторы АПФ, венодилататоры, сосудорасширяющие средства |
|
Необратимая сердечная недостаточность |
Пересадка сердца |
Лекарства, оказывающие положительный инотропный эффект, улучшающий сократимость сердца
- Сердечные гликозиды (например, дигоксин)
- Ингибиторы фосфодиэстеразы (например, инамринон)
- β1-Агонисты (например, добутамин)
Сердечные гликозиды ингибируют мембраносвязанную Na+/K+-ATФазу, улучшая симптоматику ЗСН
Эффекты сердечных гликозидов на молекулярном уровне обусловлены ингибированием мембраносвязанной Na+/K+-ATФaзы (рис. 13.24). Этот фермент участвует в создании мембранного потенциала покоя большинства возбудимых клеток посредством выведения трех ионов Na+ из клетки в обмен на поступление двух ионов К+ в клетку против градиента концентрации, тем самым создавая высокую концентрацию К+ (140 мМ) и низкую концентрацию Na+ (25 мМ). Энергию для этого насосного эффекта дает гидролиз АТФ. Ингибирование насоса приводит к повышению внутриклеточной цитоплазматической концентрации Na+.
Рис. 13.24 Механизм действия гликозидов дигиталиса. Участок, связывающий дигиталис, расположен на внеклеточной части a-p-гетеродимерной структуры фермента Ма+/К+-АТФазы. Ингибирование этого фермента приводит к повышению концентрации внутриклеточного Na+, что влечет за собой повышение концентрации внутриклеточного Са2+ и опосредует положительное инотроп-ное действие сердечных гликозидов. АДФ — аденозиндифосфат; АТФ — аденозинтрифосфат.
Повышение концентрации Na+ ведет к ингибированию мембраносвязанного Nа+/Са2+-обменника и как следствие — к повышению концентрации цитоплазматического Са2+. Обменник представляет собой АТФ-независимый антипортер, вызывающий в обычных условиях вытеснение Са2+ из клеток. Повышение концентрации Na+ в цитоплазме пассивно снижает обменную функцию, и из клетки вытесняется меньше Са2+. Затем Са2+ в повышенной концентрации активно нагнетается в саркоплазматический ретикулум (СР) и становится доступным для высвобождения в течение последующей клеточной деполяризации, тем самым усиливая связь возбуждение-сокращение. Результатом является более высокая сократимость, известная как положительная инотропия (рис. 13.25).
Рис. 13.25 Кривая Франка-Старлинга, положительные инотропные средства и застойная сердечная недостаточность. Нормальный сердечный выброс определяется конечным диастолическим давлением в левом желудочке. При застойной сердечной недостаточности (ЗСН) контрольное значение сердечного выброса снижено, и сердечный выброс падает (1). Активируется компенсаторный нейрогуморальный ответ, который повышает конечное диастолическое давление и улучшает сердечный выброс, однако это может привести к ретроградной недостаточности (2). Положительные инотропные средства повышают сердечный выброс (3). Улучшение сердечного выброса уменьшает потребность в повышенном конечном диастолическом давлении, и происходит декомпенсация с установлением нового контрольного значения (4).
При сердечной недостаточности положительное инотропное действие сердечных гликозидов изменяет кривую Франка-Старлинга желудочковой функции. На рис. 13.26 показано влияние положительных инотропных средств на сердечный выброс.
Рис. 13.26 Механизм действия других лекарственных средств, используемых для лечения застойной сердечной недостаточности (ЗСН). Венодилататоры, диуретики и ингибиторы АПФ уменьшают ретроградную недостаточность и симптомы отека и застоя путем снижения конечного диастолического давления. Однако в случае применения препаратов по отдельности они могут вызвать антеградную недостаточность посредством того же механизма (1). Вазодилататоры и ингибиторы АПФ улучшают сердечный выброс, уменьшая сердечную постнагрузку, возникающую в результате повышенной периферической вазоконстрикции и легочного застоя, тем самым создавая новое контрольное значение в зоне анте- и ретроградной недостаточности (2).
Несмотря на широкое применение дигиталиса, отсутствуют убедительные доказательства того, что он благоприятно влияет на отдаленный прогноз при ЗСН. У многих пациентов дигиталис улучшает симптоматику, однако не снижает смертность от ЗСН.
Сердечные гликозиды изменяют электрическую активность в сердце
В дополнение к повышению силы сокращения сердечные гликозиды изменяют электрическую активность в сердце и прямым, и опосредованным способами.
Сердечные гликозиды опосредованно изменяют частоту сердцебиений, повышая активность блуждающего нерва (вагус, X пара черепно-мозговых нервов) в результате стимуляции афферентных элементов в паравертебральном (узелковом) ганглии и рефлекторного повышения активности дуги блуждающего нерва. Повышенная вагусная импульсация доминирует в наджелудочковой области и вызывает:
- замедление импульсации в СА-узле;
- замедление скорости проведения в АВ-узле (расширение интервала PR на ЭКГ);
- укорочение предсердного потенциала действия.
В токсических дозах сердечные гликозиды повышают тонус эфферентных симпатических нервов сердца. Однако частота нервных разрядов неодинакова, что может привести к неравномерности возбудимости миокарда и аритмии, включая блокаду АВ-узла, атриовентрикулярную пароксизмальную тахикардию и экстрасистолы желудочков.
Прямые эффекты сердечных гликозидов на ткань сердца наиболее выражены при высоких дозах и обусловлены потерей цитоплазматического К+ вследствие ингибирования Nа+/К+-АТФазы. Продолжающийся выход цитоплазматического К+ во внеклеточное пространство снижает мембранный потенциал покоя клетки, в результате:
- повышается автоматизм;
- снижается скорость проведения в сердце;
- повышается рефрактерный период АВ-узла.
С повышением концентрации сердечных гликозидов концентрация свободного Са2+ достигает токсического уровня, насыщая механизм секвестрации СР, что вызывает колебания уровня свободного Са2+ в клетке вследствие Са2+-индуцированного высвобождения Са2+ из СР и колебания мембранного потенциала (колебательные постпотенциалы). Последние могут вызвать аритмии, включая одиночные и множественные экстрасистолы желудочков и тахиаритмии.
Сердечные гликозиды увеличивают периферическое сосудистое сопротивление в результате прямой вазоконстрикции и центрально опосредованного повышения симпатического тонуса. При ЗСН существующее повышенное периферическое сосудистое сопротивление уменьшается по мере продолжения лечения. Улучшение гемодинамики, происходящее в результате увеличения сердечного выброса, проявляется в диурезе (из-за увеличения почечного кровотока).
Все сердечные гликозиды имеют низкий терапевтический индекс, поскольку их фармакотерапевтическое и токсическое действие связано с повышением концентрации цитоплазматического Са2+. Наиболее тяжелым побочным эффектом являются сердечные аритмии.
Помимо сердца, токсические эффекты сердечных гликозидов затрагивают другие органы и системы, однако обычно это происходит только при длительной терапии. Наиболее частыми побочными эффектами, не относящимися к сердцу, могут быть:
- действие на ЖКТ (раздражение желудка);
- действие на ЦНС вследствие стимуляции вагусной афферентации и хеморецепторной триггерной зоны (тошнота, рвота, диарея, анорексия);
- другие влияния на ЦНС (нарушения зрения, головная боль, головокружение, утомляемость, галлюцинации). Особенно часто эти явления возникают у пожилых пациентов.
К редким побочным эффектам относятся эозинофилия и кожная сыпь, а также гинекомастия у мужчин (предполагают, что она возникает вследствие либо гипоталамической стимуляции, либо периферического эстрогенного действия сердечных гликозидов).
Определению причин токсичности помогает мониторинг концентрации сердечных гликозидов в плазме. Фармакокинетика отдельных сердечных гликозидов варьирует в зависимости от их липофильности.
Токсичность сердечных гликозидов изменяется под влиянием К+ в крови
Токсичность сердечных гликозидов усиливается под влиянием гипокалиемии (которая может быть связана с применением диуретиков или вторичным альдостеронизмом). Сердечные гликозиды и ионы К+ конкурируют за общие участки связывания на Nа+/К+-АТФазе. Гипокалиемия повышает связывание сердечных гликозидов с ферментом, тем самым усиливая в равной степени и фармакологическую активность, и токсические эффекты.
Для устранения токсических эффектов сердечных гликозидов используют следующие методы:
- дополнительное пероральное введение К+ с целью повышения концентрации К+ в сыворотке;
- применение антиаритмических средств (прокаинамид, фенитоин) для устранения вызванной сердечными гликозидами аритмии;
- применение моноклональных антител, связывающих сердечные гликозиды;
- введение антиген-связывающего фрагмента Fab, полученного из антител, специфичных к дигоксину, при интоксикации, угрожающей жизни пациента. Высокая аффинность сердечных гликозидов к антителам предотвращает связывание с Nа+/К+-АТФазой, и лекарство выводится из сосудистой системы.
Хотя перечисленные методы в состоянии устранить токсические явления, вызванные сердечными гликозидами, их можно ослабить или предотвратить, проводя мониторинг концентрации электролитов и сердечных гликозидов в крови. Очень важным фактором риска развития интоксикации под влиянием дигоксина является функция почек. Поскольку дигоксин экскретируется в неизмененном виде главным образом почками, для пациентов с почечной недостаточностью дозу дигоксина рассчитывают соответствующим образом.
Побочные эффекты сердечных гликозидов
- Токсичность вследствие малого терапевтического индекса
- Возможность гипокалиемии и потери К+ сердца, что может способствовать возникновению опасных для жизни аритмий при одновременном приеме диуретиков
- Дискомфорт со стороны ЖКТ, рвота и анорексия
- Аритмии, для лечения которых необходима кардиоверсия, поэтому гликозиды нужно использовать крайне осторожно
Ингибиторы фосфодиэстеразы для лечения ЗСН
Ингибиторы фосфодиэстеразы (ФДЭ) применяют для лечения пациентов с ЗСН, не поддающейся терапии другими лекарственными средствами. Изоформа ФДЭ-3 обнаруживается в гладких мышцах миокарда и сосудов. Ингибирование деградации цАМФ приводит к повышению содержания цитозольного Са2+.
Существуют многие тканеспецифичные изоформы ФДЭ. Такие ингибиторы, как инамринон (известный как амринон), милринон и веснаринон, представляют собой дипиридины, повышающие уровень цАМФ путем ингибирования ФДЭ-3. Это подавление приводит к более длительному притоку Са2+ в течение сердечного потенциала действия и повышает сократимость. Расщепление цАМФ ингибируется также в гладких мышцах артерий и вен, вызывая заметное расширение сосудов.
Ингибиторы ФДЭ увеличивают минутный объем сердца, снижают давление заклинивания в легочных капиллярах (непрямое измерение давления в левом предсердии и вероятность отека легких) и уменьшают общее периферическое сопротивление, не вызывая каких-либо существенных изменений частоты сердцебиений или артериального кровяного давления.
Инамринон как ингибитор ФДЭ используют для кратковременного лечения ЗСН
Инамринон используют в клинике для кратковременного лечения пациентов с ЗСН, не отвечающей на дигиталис и диуретики. Препарат можно использовать в качестве монотерапии или в комбинации с β1агонистами, чтобы:
- улучшить сердечный выброс;
- повысить ударный (систолический) объем;
- снизить давление в правом предсердии и давление заклинивания в легочных капиллярах. Продолжительное в/в применение не приводит к отсутствию ответа, т.е. тахифилаксия не наступает, однако при этом могут возникнуть побочные эффекты. Высока частота возникновения тошноты и рвоты, но наиболее тревожны нарушения функции печени и тромбоцитопения. Эти побочные эффекты исчезают при прекращении лечения. Инамринон может вызвать также наджелудочковую и желудочковую аритмии, поэтому его можно использовать лишь при частом мониторинге ЭКГ.
Милринон является сильным ингибитором ФДЭ-3, который не используют для длительной терапии ЗСН
Милринон — аналог инамринона, но действует сильнее. Он обладает сходным с инамриноном спектром дозолимитирующих побочных эффектов и может вызвать тромбоцитопению у незначительного количества (0,4%) пациентов. При пероральном введении он раздражает ЖКТ в меньшей степени. Однако его применение ограничено вследствие возможности возникновения фатальных аритмий, поэтому инамринон не используют для длительной терапии.
То же ограничение относится к сходному препарату эноксимону. Ни одно из этих лекарственных средств не утверждено для применения в США.
Веснаринон — ингибитор ФДЭ, потенциально обладающий дополнительными полезными свойствами
Исследования показывают, что веснаринон может повышать сократимость сердца посредством дополнительных механизмов, в частности за счет активации антипортера Nа+/Са2+-обменника, что приводит к повышению содержания цитозольного Са2+ в фазу систолы. Этот эффект может быть прямым или опосредованным (вторичным по отношению к способности лекарственного средства увеличивать продолжительность сердечного потенциала действия по механизму, который, по-видимому, включает блокаду 1Кг).
Кроме того, веснаринон способен стимулировать Isi. Основным лимитирующим побочным эффектом является агранулоцитоз, возникающий у 1-3% пациентов. Однако он обратим, когда прием лекарственного средства прекращают. При длительном лечении сердечной недостаточности применение веснаринона, как и милринона, не рекомендуется вследствие дозозависимого повышения вероятности летального исхода, и в США этот препарат запрещен.
Антагонисты β1-адренорецепторов неожиданно оказались полезными для лечения ЗСН
Эти препараты неожиданно пополнили арсенал лекарственных средств, используемых для лечения ЗСН, притом что агонисты β-адренорецепторов давно использовали для лечения острой ЗСН. Предполагают, хотя это трудно доказать, что системный механизм их действия представляет собой не что иное, как антагонизм по отношению к неблагоприятным ремоделирующим эффектам повышенного тонуса симпатической иннервации (что обычно бывает при сердечной недостаточности). Вероятно, на клеточном уровне антагонисты β1-адренорецепторов, например карведилол, уменьшают понижающую регуляцию экспрессии β1адренорецепторов, которая возникает в ответ на высокий уровень симпатического тонуса. Следовательно, возможно восстановление экспрессии β1адренорецепторов, которая в большей степени совместима с нормальным статусом сердечно-сосудистой системы.
Система G-белок-связанного рецептора киназы и аррестина участвует в трансдукции десенсибилизации и понижающей регуляции β1адренорепторов миокарда. GRK2 присутствует преимущественно в клетках эндотелия сосудов, тогда как другая изоформа, GRK3, локализуется в миоцитах сердца. Однако экспрессия изоформы GRK2 в миокарде (известной также как киназа-1 β-адренорецепторов, PARK1) при ЗСН возрастает. Ингибирование активности GRK2 может противодействовать неблагоприятному эффекту сердечного ремоделирования при дилатационной кардиомиопатии и ЗСН. Хотя механизм действия остается неясным, показано, что два β1селективных антагониста, метопролол и бисо-пролол, снижают частоту летального исхода при долговременном лечении, указывая на то, что механизмом действия на молекулярном уровне является β1-антагонизм. При лечении уменьшаются и недостаточность сердечного выброса, и число случаев внезапной сердечной смерти (точная причина летального исхода неизвестна). Установлено, что другойβ1-антагонист, карведилол, также снижает частоту летального исхода у пациентов с ЗСН. Однако это лекарственное средство в дополнение к блокаде β1-адренорецепторов блокирует также β2 и a1адренорецепторы и обладает антиоксидантным действием, его молекулярный механизм действия точно неизвестен. Все эти средства способны снижать частоту сердцебиений и минутный объем сердца в начале лечения, что может ухудшать самочувствие пациентов. Но при низкой первичной дозировке это не создает проблем. По мере дальнейшего лечения сердечный выброс возрастает, и симптомы ЗСН ослабевают. Эффективность описанных выше β1блокаторов установлена для всех классов ЗСН, за исключением наиболее тяжелых (класс IV, New York Heart Association).
Дополнительные лекарственные средства, используемые при лечении ЗСН для уменьшения отеков, а также сердечной пред- и постнагрузки
- Ингибиторы АПФ (например, каптоприл)
- Сосудорасширяющие нитраты (например, в/в нитропруссид, перорально гидралазин, местно нитроглицерин)
Для лечения ЗСН обычно используют диуретики
Диуретики снижают сердечную преднагрузку, уменьшая сосудистый объем в результате повышенной экскреции Na+ почками. Эффективность сердечного насоса возрастает, уменьшается венозное давление, и, соответственно, ослабевают признаки и симптомы отека (см. рис. 13.26). Лечение тиазидами (например, гидрохлоротиазидом) и петлевыми диуретиками (например, фуросемидом) снижает внутри- и внесосудистую задержку жидкости при ЗСН и оказывает благоприятный эффект как при острой, так и при хронической ЗСН (доказать это трудно, поскольку диуретики, как правило, назначают всем пациентам, поэтому чистый контроль отсутствует; их применение оставляет хорошее впечатление, в связи с чем по этическим соображениям их получают все пациенты). Тиазиды и петлевые диуретики применяют перорально при хронической ЗСН, тогда как фуросемид вводят в/в также при острой ЗСН.
Торсемид действует в просвете толстой части восходящей петли Генле, где он ингибирует систему переноса Na+/K+/2C1~. У пациентов с ЗСН классов II—IV (New York Heart Association) пероральный прием торсемида в дозе 10-20 мг/сут вызывает гораздо большее снижение массы тела и отеков, чем у пациентов, получающих плацебо. Диуретический эффект длится около 6-8 час. Для экскреции Na+ отношение доза-ответ является линейным в диапазоне доз от 2,5 до 20 мг перорально. Важно отметить, что при дозах до 10 мг отсутствует повышение калиурии, показывая, что данный препарат в этом отношении, подобно другим петлевым диуретикам, отличается от тиазидов. Т1/2 составляет 3,5 час. Торсемид элиминируется в результате метаболизма в печени (80%) и экскреции с мочой (20%). Более 99% торсемида связывается в плазме, поэтому очень малое его количество поступает в мочу канальцев в результате клубочковой фильтрации. Почечный клиренс в основном осуществляется путем активной секреции в мочу проксимальными канальцами.
Метолазон — тиазидный диуретик, используемый для устранения отеков, сопровождающих ЗСН. При отеках, а также почечных заболеваниях его назначают перорально в дозе 5-20 мг 1 раз в день. Для пациентов, страдающих пароксизмальной одышкой во сне, могут потребоваться более высокие дозы, чтобы обеспечить более длительный диурез и салиурез на 24-часовой период.
Побочные эффекты, возникающие при диуретической терапии, обычно бывают лишь при длительном применении диуретиков. Они включают:
- активацию гормональных путей;
- изменение баланса электролитов;
- изменение обменных процессов.
Изменение баланса электролитов относится к ионам Na+, Mg2+, Са2+ и К+ в сыворотке. Особенно серьезной является потеря ионов К+, которая может вызвать желудочковую аритмию. Чтобы предотвратить потерю К+, используют калийсберегающие диуретики спиронолактон или триамтерен.
Основные возможные метаболические изменения у некоторых пациентов — это повышение концентрации глюкозы и мочевой кислоты. Необходимо проводить тщательный мониторинг у пожилых пациентов, у которых в ходе диуретической терапии нередко снижается функция почек и могут возникнуть азотемия, недержание мочи, гиповолемия и головокружение.
Взаимодействие диуретиков с другими лекарственными средствами происходит редко. Однако диуретическое действие петлевых диуретиков, например фуросемида, может стать слабее при одновременном применении аспириноподобных НПВС. Вероятным механизмом может быть ингибирование синтеза почечного простагландина под влиянием НПВС, особенно эндогенных вазодилататоров ПГ12 и ПГЕ2.
При использовании петлевых диуретиков вместе с аминогликозидными антибиотиками могут возникнуть явления ото- и нефротоксичности.
Ингибиторы АПФ используют для лечения ЗСН в качестве препаратов первой линии
Ингибиторы АПФ (табл. 13.11) впервые были использованы при ЗСН после того, как было выявлено, что в течение периода сниженной перфузии органов и увеличения объема желудочков активируется нейрогуморальная система. Ренин-ангиотензиновый каскад снижает деятельность сердца за счет продукции ангиотензина II, который повышает системное сосудистое сопротивление (сердечную постнагрузку) и высвобождает альдостерон, вызывающий задержку Na+ и воды (отек). Подавление этого каскада ингибиторами АПФ, такими как каптоприл, эналаприл и лизиноприл, снижает уровень циркулирующего ангиотензина II. В свою очередь, это уменьшает периферическое сосудистое сопротивление (сердечную постнагрузку) и предотвращает опосредованные альдостероном задержку Na+ и увеличение объема крови (т.е. снижает сердечную преднагрузку) (см. рис. 13.26). Снижается также повышенный тонус симпатической нервной системы, уровень циркулирующего эпинефрина и повышается эффективность систолического выброса (возрастает сердечный выброс). Продолжающееся использование ингибиторов АПФ может также уменьшить индуцированные ангиотензинном II гипертрофию и ремоделирование желудочков.
В ряде клинических исследованиях установлено, что ингибиторы АПФ удлиняют продолжительность жизни пациентов с ЗСН, поэтому служат основными лекарственными средствами при этом заболевании.
Ингибиторы АПФ пациенты переносят в целом хорошо. Нередко возникает гипотензия, вызывающая головокружение. Могут возникнуть почечная дисфункция и гиперкалиемия, однако эти нарушения обратимы при отмене лекарственного средства. Примерно у 10% пациентов появляется раздражающий, а порой даже изнурительный кашель. Менее часто возникающие побочные эффекты — сыпь на коже, желудочно-кишечные расстройства, нарушения вкуса и ангионевротический отек как результат накопления брадикинина (который разрушается под влиянием АПФ) и других кининов (см. рис. 13.41). При использовании ингибиторов АПФ во II и III триместрах беременности возможно повреждение и даже гибель плода, поэтому во время беременности их прием должен быть прекращен как можно скорее.
Побочные эффекты возникают при использовании ингибиторов АПФ вместе с НПВС. Одновременное применение этих средств предотвращает действие ауторегуляторного механизма ПГ-опосредованного эфферентного расширения артериол, что приводит к почечной гипертензии.
Блокада рецепторов альдостерона снижает показатели смертности от ЗСН
Эплеренон — первый блокатор рецепторов альдостерона, применение которого было разрешено благодаря улучшению выживаемости пациентов с клиническим признаками стабильной ЗСН после ОИМ и систолической дисфункции левого желудочка (фракция выброса < 40%).
В исследовании Eplerenone Post-AMI Heart Failure Efficacy and Survival Study, изучавшем эффективность эплеренона и его влияние на выживаемость пациентов с сердечной недостаточностью после ОИМ и пациентов, имевших сердечную недостаточность после инфаркта миокарда и получавшими плацебо и стандартное лечение (ингибиторы АПФ и β-блокаторы). Было установлено, что эплеренон плюс стандартная терапия снижали смертность на 15%. Лечение нужно начинать с дозы 25 мг 1 раз в день, затем ежесуточную дозу доводят до 50 мг 1 раз в день перорально. Лечение проводят преимущественно в течение 4 нед, если пациент его переносит.
Механизм действия эплеренона неясен. Он может влиять на сердечную недостаточность, действуя на уникальные рецепторы быстрого ответа (в отличие от ядерных рецепторов медленного ответа), присутствующие в мембране клеток сердца, вызывая подавление опосредованной альдостероном апоптотической гибели клеток. Активация рецепторов плазматической мембраны кардиоцитов альдостероном индуцирует следующий каскад внутриклеточных процессов:
- активацию фосфолипазы С;
- быстрый подъем уровня внутриклеточного Са2+;
- активацию протеинкиназы С и кальцинейрина (Са2+-зависимой фосфатазы);
- дефосфорилирование проапоптотического белка (BAD);
- деполяризацию митохондрий и высвобождение цитохрома С;
- активацию апоптотического фермента каспазы-3. Когда BAD дефосфорилируется в индуцированном альдостероном каскаде, он образует гетеродимеры с двумя другими белками, bcl-2 и bcl-xL, су-прессируя их действие (они генерируют сигнал, определяющий дальнейшее выживание клеток), включая стабилизацию (закрытие) пориновых каналов митохондрий (потенциал-зависимый анионный канал). Если пориновые каналы открыты, цитохром С выходит в цитозоль, где активирует каспазу-3 (рис. 13.27).
Рис. 13.27 Механизм, посредством которого альдостерон вызывает апоптотическую гибель клеток, и механизм ингибирования этого процесса эплереноном при лечении сердечной недостаточности. Активация рецепторов альдостерона ведет к активации кальцинейрина, который дефосфорилирует проапоптотический белок (BAD), образующий гетеродимеры с bcl-2 и bcl-xL. Гетеродимеры более не могут блокировать пориновый канал митохондрий, давая возможность выхода цитохрома с (cyt-c), активирующего проапоптотический фермент каспазу-В. 1Р3 — инозитол-1,4,5-трифосфат; Р1Р2 — фосфатидилинозитолдифосфат; ДАГ — диацилглицерол.
Эплеренон несколько лет использовали для лечения гипертензии, и его свойства описаны далее («Лечение гипертензии»).
Нитровазодилататоры благоприятно влияют на ЗСН, не действуя на сердце
Нитровазодилататоры — лекарственные средства различной химической структуры, обладающие сильным сосудорасширяющим эффектом за счет действия на гладкие мышцы артерий и вен. Молекулярные механизмы их действия изучены недостаточно. Однако эти препараты:
- вызывают расслабление сосудов на клеточном уровне, предположительно усиливая активность цГМФ с помощью посредника нитрозотиола;
- способны регулировать высвобождение Са2+ из саркоплазматического ретикулума, изменять тонус симпатической нервной системы и вызывать образование расслабляющих гладкие мышцы физиологически активных веществ, таких как ПГ12 и ПГЕ2;
- снижают диастолическое давление и улучшают диастолическую функцию сердца (см. рис. 13.26). Нитропруссид представляет собой стандартный нитровазодилататор, применяемый в качестве препарата первой линий при острой ЗСН, особенно у пациентов с повышенным артериальным давлением, т.к. он уменьшает как пред-, так и постнагрузку сердца. Нитропруссид снижает давление в левом желудочке, уменьшая венозный тонус и тем самым увеличивая венозную емкость, и вызывает сдвиг в распределении объема крови.
Поскольку нитропруссид не оказывает существенного прямого действия на сократимость желудочков, повышение сердечного выброса и ударного объема происходит в результате снижения сердечной постнагрузки. Увеличение сердечного выброса не сопровождается рефлекторным повышением кровяного давления или частоты сердцебиений, и нитропруссид снижает потребление кислорода миокардом.
Нитропруссид следует вводить в/в в дозе 0,1-0,2 мг/кг/мин с титрованием дозы. Препарат используют как кратковременное средство лечения острой ЗСН.
В результате метаболизма нитропруссида в печени образуется цианид, который затем выводится почками. У пациентов с почечной недостаточностью цианид может накапливаться в организме, вызывая тошноту, спутанность сознания и судороги. Нитропруссид может также разрушаться с образованием синильной кислоты, которая высоко-авидно связывается с гемоглобином. Основным побочным эффектом нитропруссида является гипотензия, которая может быть тяжелой.
Нитроглицерин (глицерила тринитрат) и изосорбида динитрат в основном уменьшают сердечную преднагрузку, однако вызывают и слабое снижение постнагрузки. К этим препаратам быстро развивается толерантность, поэтому их введение должно быть прерывистым. Интенсивного метаболизма при первом прохождении можно избежать путем сублингвального или местного введения лекарственных средств. Наиболее частый побочный эффект — гипотензия.
Было показано, что гидралазин в комбинации с нитратами способен увеличить продолжительность жизни пациентов с ЗСН, поэтому такую комбинацию используют в качестве альтернативы по отношению к ингибиторам АПФ, особенно у пациентов, которые не переносят ингибиторы.
В дополнение к снижению сердечной постнагрузки гидралазин оказывает непрямой положительный инотропный эффект, возникающий в результате усиленной активности симпатической нервной системы вследствие артериальной вазодилатации, поэтому он полезен при отмене лечения добутамином или β1-агонистами. Гидралазин повышает также почечный кровоток. Применение гидралазина в качестве монотерапии недостаточно для необходимого уменьшения венозного застоя, поэтому препарат используют в сочетании с нитроглицерином (местно) или изосорбидом динитратом (перорально). Побочные эффекты гидралазина:
- рефлекторная активация симпатической нервной системы;
- лекарственно индуцированная системная красная волчанка, возникающая редко, если дозы гидралазина составляют менее 200 мг/сут.
Гидралазин противопоказан пациентам с ЗСН, у которых присутствует ишемическая болезнь коронарных артерий, если одновременно не принимать нитраты, т.к. потребление кислорода миокардом возрастает под влиянием гидралазина вследствие усиления симпатической стимуляции сердца.
Несиритид обладает уникальным механизмом действия при ЗСН
Несиритид представляет собой очищенный рекомбинантный препарат, принадлежащий к новому классу лекарственных средств, — мозговому натрийуретическому пептиду (МНУП) В-типа. Он показан для в/в введения пациентам с острой декомпенсированной ЗСН, которые страдают одышкой в покое или при минимальной нагрузке. У этих пациентов несиритид снижает давление заклинивания в легочных капиллярах и облегчает одышку. Он связывается с гуанилилциклазой в гладких мышцах сосудов и эндотелиальных клетках, приводя к повышению внутриклеточной концентрации цГМФ и расслаблению гладкомышечных клеток (имитируя эндогенный NO; см. рис. 13.14). Несиритид вводят в/в. Рекомендуемая схема: болюсная инъекция 2 мкг/кг, затем инфузия 0,01 мкг/кг/мин. Фармакодинамический Т1/2 (3 час) продолжительнее, чем фармакокинетический Т1/2 (18 мин). При стабильном состоянии уровень МНУП в плазме возрастает от базового эндогенного уровня до 3-6-кратного, если несиритид вводят в дозах 0,01— 0,03 мкг/кг/мин.
Несиритид выводится из кровотока посредством трех механизмов (в порядке убывания значимости):
- связывания с клиренс-рецепторами клеточной поверхности, последующей клеточной интернализации и лизосомного протеолиза;
- протеолитического расщепления пептида эндопептидазами, такими как нейтральная эндопептидаза, которые присутствуют на поверхности сосудов, обращенной в их просвет;
- почечной фильтрации.
Основные побочные эффекты — гипотензия и азотемия (редко). Однако эффективность лекарственного средства недавно была поставлена под сомнение.
Побочные эффекты лекарственных средств, применяемых для лечения ЗСН
- Сердечные гликозиды имеют узкий терапевтический индекс и могут вызвать аритмии
- Кратковременное лечение ингибиторами фосфодиэстеразы способно вызвать тромбоцитопению и аритмии
- β1-Агонисты могут привести к возникновению тахиаритмий, а при длительном применении может ухудшиться функция миокарда
- Диуретики вызывают серьезные нарушения баланса электролитов, например гипокалиемию, что может стать причиной желудочковых аритмий
- Ингибиторы АПФ обладают незначительными побочными эффектами и в основном вызывают лишь гипотензию
- Нитровазодилататоры, несиритид и эплеренон, вызывают немногочисленные побочные эффекты
Левосимендан — новый препарат для лечения ЗСН
В 2004 г. было показано, что левосимендан повышает выживаемость при сердечной недостаточности (наблюдение 4 нед). Это лекарственное средство представляет потенциальный интерес, т.к. оно предположительно повышает инотропное состояние и снижает системное сосудистое сопротивление без повышения концентрации внутриклеточного Са2+ в миоцитах. Если это так, то должна быть снижена вероятность возникновения побочных эффектов в отношении сердечного ритма, что типично для других препаратов, обладающих положительным инотропным действием. Механизм действия (рис. 13.28) связывают с сенсибилизацией комбинации тропонин С-Са2+, ведущей к положительному инотропному эффекту, и активацией сосудистой Iк(атф)> которая снижает периферическое сосудистое сопротивление. Однако было показано, что в предсердиях человека левосимендан вызывает ингибирование ФДЭ-3, приводя к повышению уровня внутриклеточного Са2+. Следовательно, механизм действия левосимендана остается недоказанным.
Рис. 13.28 Предполагаемый механизм действия левосимендана. Са2+ и левосимендан связываются с тропонином С. Это изменяет конформацию тропонина С, в результате возрастает его аффинность и к Са2+, и к левосимендану. Это так называемый эффект сенсибилизатора Са2+. Связывание с Са2+ активирует тропонин С, после чего он приобретает способность предотвращать блокирующий эффект тропомиозина на связывание актина с миозином. Это облегчает связывание актин-миозин и вызывает положительную инотропную реакцию. АДФ — аденозиндифосфат; АТФ — аденозинтрифосфат.
Лечение застойной сердечной недостаточности[править | править код]
Существует множество лекарственных средств, облегчающих признаки и симптомы ЗСН, но фармакотерапия не предотвращает ухудшения функции сердца, лежащего в основе заболевания. В отдельных случаях может понадобиться хирургическая операция на клапанах (если причиной является их недостаточность) или трансплантация сердца (если причинами служат обширный инфаркт миокарда или вирусный миокардит).
Лечение острой сердечной недостаточности[править | править код]
Агонисты β1-адренорецепторов представляют собой избирательно действующие на сердце симпатомиметические средства, используемые при острой сердечной недостаточности
β1-Адренорецепторы обнаруживаются преимущественно в тканях сердца. Их агонисты вызывают повышение концентрации внутриклеточного Са2+ и цАМФ и, как следствие, положительную инотропную реакцию. Для лечения острой сердечной недостаточности избирательные β1-агонисты предпочитают неизбирательным симпатомиметикам, которые обладают нежелательной агонистической активностью по отношению к a1адренорецепторам (вызывают периферическую вазоконстрикцию).
Добутамин и дофамин — наиболее распространенные β1-агонисты, однако их применение ограничено в/в введением по неотложным показаниям.
Добутамин (рацемат) представляет собой относительно избирательный агонист сердечных β1адренорецепторов при введении в дозе менее 5 мг/кг/мин. Он обусловливает менее выраженную вазоконстрикцию по сравнению с эпинефрином. В более высоких дозах он влияет на β2- и на а1адренорецепторы (в меньшей степени). Добутамин быстро улучшает многие показатели функции сердца:
- повышает сердечный выброс;
- снижает среднее артериальное давление;
- уменьшает системное сосудистое сопротивление;
- снижает давление наполнения желудочков (давление в желудочках по мере их наполнения кровью).
Добутамин используют при неотложной терапии острой тяжелой левожелудочковой дисфункции, ассоциированной с отеком легких или шоком, которые не удается устранить обычными лекарственными средствами. Короткий Т1/2 означает, что данный препарат не подходит для длительного перорального употребления. Добутамин не увеличивает почечный кровоток. При длительном использовании постоянная активность β1-агониста действует на сердце неблагоприятно. Добутамин можно использовать для быстрого улучшения функции сердца при «стрессовой» эхокардиографии.
Дофамин является широко используемым β1агонистом, обладающим также агонистической активностью в отношении рецепторов дофамина. Его относят к нейропередатчикам, т.к. он влияет на нервную систему, но не проникает через гематоэнцефалический барьер. При в/в введении дофамин оказывает положительный инотропный эффект на сердечную мышцу в результате:
- β1агонизма (прямой эффект);
- высвобождения эндогенного норэпинефрина (опосредованный эффект, терапевтически малозначим).
Дофамин вызывает вазодилатацию почечных артериол, что повышает выход мочи и облегчает отечность. В неотложной терапии его используют для устранения кардиогенного, травматического и гиповолемического шока, когда кровяное давление снижено и ухудшен почечный кровоток.
Другие β1-агонисты, такие как изопротеренол, норэпинефрин и эпинефрин, никогда не используют при лечении острой сердечной недостаточности вследствие избыточных положительных хронотропных эффектов (всех трех препаратов) или периферической вазоконстрикции в результате a1-агонизма (норэпинефрин и эпинефрин).
Использование β1-агонистов при лечении острой сердечной недостаточности следует рассматривать исходя из фармакодинамических процессов, происходящих на уровне рецепторов. При острой сердечной недостаточности высокий симпатический тонус сердца вызывает понижающую регуляцию адренергических β1-рецепторов. Следовательно, повторное воздействие β1-агонистов на сердце может привести к тахифилаксии или утрате β1-функции в больном сердце, которая может быть результатом неучастия рецепторов в каскаде трансдукции. Таким образом,как это ни парадоксально, длительное применение селективных β1-агонистов может усилить понижающую регуляцию рецепторов и ухудшить функцию миокарда при острой сердечной недостаточности. По этой причине, а также вследствие способности β1агонистов «истощать» кислород в миокарде (продукция АТФ в процессе β1агонизма требует больше кислорода, чем в отсутствие этого процесса), вызывать аритмии и даже некроз миокарда β1агонисты никогда не используют для длительного лечения острой сердечной недостаточности, а применяют только при неотложной терапии (т.е. в острой фазе обширного инфаркта миокарда).
Гипертензия[править | править код]
Гипертензия — это состояние повышенного кровяного давления
Гипертензия — это постоянное повышенное системное кровяное давление (систолического или диастолического) выше 140/90 мм рт. ст. Изолированной систолической гипертензией называют повышенное систолическое кровяное давление (обычно выше 140-160 мм рт. ст.) в отсутствие повышения диастолического давления.
Постоянное высокое кровяное давление повышает риск поражения почек, сердца и мозга, а также риск развития сердечно-сосудистых заболеваний (например, атеросклероза). Высокое кровяное давление — это признак, а не собственно заболевание. В большинстве случаев причину, лежащую в основе повышения давления, не удается диагностировать (так называемая эссенциальная гипертензия). Легочная гипертензия — это совершенно особое заболевание.
На систему контроля нормального кровяного давления можно воздействовать лекарственными средствами. Давление контролируют совместно нервная и эндокринная системы (рис. 13.29), которые модулируют:
- объем крови;
- минутный объем сердца;
- периферическое сосудистое сопротивление. Целью терапевтического вмешательства при лечении гипертензии является снижение высокого кровяного давления. Это удается сделать с помощью лекарственных средств, действующих прямо или опосредованно на объем крови, сердечный выброс и периферическое сосудистое сопротивление. При этом ожидается, что снижение давления ограничит последующее развитие патологии органов.
Рис. 13.29 Факторы, контролирующие кровяное давление. Кровяное давление определяется сердечным выбросом, который зависит от частоты сердечных сокращений, ударного объема и периферического сопротивления. Сердечный выброс зависит от возвращаемого в сердце количества крови, которое зависит от емкостного сопротивления вен и венул (преднагрузка) и объема крови (под контролем почек). Периферическое сосудистое сопротивление определяется артериолами.
Тканевые мишени антигипертензивных средств:
- симпатические нервы, высвобождающие вазоконстриктор норэпинефрин;
- почки, которые регулируют объем крови;
- сердце, выполняющее выброс крови;
- артериолы, определяющие периферическое сосудистое сопротивление;
- эндотелиальные клетки, которые регулируют синтез или деградацию эндогенных гипертензивных и гипотензивных средств, таких как ангиотензин II и NO;
- ЦНС, воспринимающая кровяное давление и контролирующая его путем воздействия на системы, участвующие в регуляции кровяного давления.
Гипертензия
- Гипертензию обычно диагностируют, когда обнаруживают стойкое повышение диастолического давления выше 90 мм рт. ст.
- Кровяное давление повышается при увеличении сердечного выброса, повышении периферического сопротивления или увеличении объема крови
- Первичная гипертензия не имеет очевидной причины
- Вторичная гипертензия возникает в результате заболеваний, например феохромоцитомы и венозного стеноза
Гипертензию подразделяют на первичную и вторичную
Первичная (эссенциальная) гипертензия — это повышение кровяного давления без видимой причины.
Она охватывает 90-95% всех случаев и обычно появляется у взрослых, чаще всего в возрасте старше 40 лет. С первичной гипертензией ассоциируются различные факторы риска: генетическая предрасположенность, ожирение, неумеренное употребление алкоголя и отсутствие физической активности. Некоторые из этих факторов служат дополнительными мишенями для антигипертензивных препаратов.
Вторичная гипертензия составляет 5-10% всех случаев и обусловлена определенной причиной, например почечно-сосудистым заболеванием, повышающим кровяное давление в результате активации ренин-ангиотензин-альдостероновой системы (рис. 13.30). Вторичную гипертензию также могут вызвать различные эндокринные болезни (например, феохромоцитома, опухоль мозгового вещества надпочечников, секретирующая избыточное количество эпинефрина).
Рис. 13.30 Ренин-ангиотензин-альдостероновая система. Высвобождение ренина стимулирует превращение ангиотензиногена из печени в ангиотензин I, который превращается в ангиотензин II под влиянием ангиотензинпревращающего фермента. Ангиотензин II вызывает сужение сосудов, высвобождение альдостерона из коры надпочечников и задержку Na+, что повышает кровяное давление, но снижает высвобождение ренина, таким образом система сохраняет состояние гомеостаза. АПФ — ангиотензинпревращающий фермент.
Гипертензию можно классифицировать по степени сердечно-сосудистого риска и размеру повышения кровяного давления
У большинства пациентов лечение гипертензии длится всю жизнь и нацелено на снижение риска развития сердечно-сосудистой патологии. У некоторых пациентов, обычно с существенно повышенным кровяным давлением, возникает необходимость снизить кровяное давление в течение нескольких часов, т.е. оказать неотложную помощь.
Как правило, у пациентов с гипертензией кровяное давление прогрессивно повышается в течение нескольких месяцев или лет. В результате риск развития сердечно-сосудистых заболеваний медленно увеличивается (рис. 13.31). Утрата сосудистой эластичности и податливости кровеносных сосудов способствует возникновению хронической гипертензии. Отсюда следует, что терапия должна быть направлена на длительное снижение кровяного давления.
Рис. 13.31 Изменения стенки кровеносных сосудов при хронической гипертензии. Эти изменения развиваются медленно. Клетки гладких мышц среднего слоя стенки сосуда проникают в интиму, которая в результате утолщается (предоставлено Alan Stevens, Jim Lowe).
При быстро развивающейся гипертензии резкий подъем кровяного давления за короткое время может привести к опасному для жизни повреждению органов — сердца, аорты, головного мозга или почек (рис. 13.32). В этой ситуации задача состоит в том, чтобы снизить кровяное давление за несколько минут или часов. Подобные ситуации становятся все более редкими по мере совершенствования антигипертензивной терапии, однако могут возникать при неадекватной терапии, а также если пациент перестает принимать лекарство, ошибочно полагая, что у него все в порядке, или если заболевание не диагностировано и терапию не проводили. Характерными для этого состояния являются высокое и нарастающее кровяное давление и признаки повреждения того или иного органа, например энцефалопатия. Здесь важно быстро снизить кровяное давление с помощью в/в введения лекарственного средства, однако проводить эту процедуру следует осторожно и постадийно (обычно по произвольному выбору), чтобы избежать низкого цереброваскулярного давления и, следовательно, ишемии мозга (рис. 13.33).
Рис. 13.32 Изменения стенки кровеносных сосудов при острой (быстро развивающейся) гипертензии. При острой гипертензии повреждение стенки кровеносных сосудов и сосудистого эндотелия ведет к адгезии и активации тромбоцитов и высвобождению различных медиаторов (фактора, активирующего тромбоциты, тромбоксана А2, серотонина, аденозиндифосфата, тромбина) (предоставлено Alan Stevens, Jim Lowe).
Рис. 13.33 Соотношение между церебральным кровотоком и средним артериальным давлением. При тяжелой гипертензии, особенно требующей неотложной терапии, быстрое падение среднего артериального давления может вызвать избыточное снижение церебрального кровотока, церебральную ишемию и, возможно, инсульт.
Лечение гипертензии[править | править код]
В качестве терапии первой линии применяют немедикаментозное лечение
Пациентам с гипертензией предписано избегать ситуаций и факторов, предрасполагающих к возникновению сердечно-сосудистых заболеваний. Основные рекомендации:
- выполнять физические упражнения;
- снизить массу тела, если она чрезмерна;
- в некоторых случаях ограничить прием соли с пищей;
- прекратить курение;
Классы лекарственных средств, используемых для лечения гипертензии
- Диуретики
- Антагонисты β1-адренорецепторов (β-блокаторы)
- Антагонисты a1-адренорецепторов
- Агонисты β2-адренорецепторов
- Вазодилататоры, действующие прямо
- Антагонисты Са2+
- Ингибиторы АПФ
- Антагонисты ангиотензина II
- Антагонисты альдостерона
- Блокаторы адренергических нейронов и резерпин
- Антагонисты имидазолина I,
- Антагонисты дофамина D,
- ограничить употребление этанола;
- лечить расстройства липидного обмена.
Лекарственная терапия быстро развивающейся гипертензии отличается от лечения хронической гипертензии
В седьмом отчетном докладе Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (2003) представлены основные принципы предотвращения гипертензии и лечения хронической гипертензии (рис. 13.34).
Рис. 13.34 Алгоритм лечения гипертензии. АК — антагонист кальция; АПФ — ангиотензинпревращающий фермент; БРА — блокатор рецептора ангиотензина I [Chobanian AV, et al. JAMA 2003; 289: 2560-2571].
Ключевые положения доклада Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (2003 r.)
- У лиц старше 50 лет систолическое кровяное давление более 140 мм рт. ст. является гораздо более важным фактором риска развития сердечно-сосудистой патологии, чем диастолическое кровяное давление
- Риск сердечно-сосудистого заболевания начиная со 115/75 мм рт. ст. удваивается с каждым повышением кровяного давления на 20/10 мм рт. ст. Нормотензивные лица старше 55 лет на всю оставшуюся жизнь имеют 90% риск развития гипертензии
- Людей, имеющих систолическое кровяное давление от 120 до 139 мм рт. ст. или диастолическое кровяное давление от 80 до 89 мм рт. ст., следует считать прегипертензивными. Им необходимо изменить образ жизни с целью сохранения здоровья, чтобы предотвратить сердечнососудистые заболевания
- Для лекарственного лечения большинства пациентов с неосложненной гипертензией следует использовать тиазидные диуретики — либо в отдельности, либо в комбинации с препаратами других классов. В случае повышенного риска необходимо первоначально использовать антигипертензивные средства других классов (ингибиторы АПФ, блокаторы рецепторов ангиотензина, β-блокаторы, антагонисты Са2+)
- Для большинства пациентов с гипертензией требуется применение двух или более антигипертензивных средств, чтобы кровяное давление снизилось до заданной величины (< 140/90 мм рт. ст. или < 130/80 мм рт. ст. для пациентов с диабетом или хроническими заболеваниями почек)
- Если давление более чем на 20/10 мм рт. ст. выше заданного, необходимо начать лечение двумя препаратами, один из которых обычно тиазидный диуретик
- Наиболее эффективная терапия позволит устранить гипертензию только при необходимой мотивации со стороны пациента
Все антигипертензивные лекарственные средства обладают побочными эффектами, что может приводить к отказу от их приема
Хотя побочные эффекты лекарственных средств встречаются при лечении всех заболеваний, особое значение они приобретают при лечении гипертензии, поскольку у большинства пациентов симптомы заболевания отсутствуют большую часть времени (исключая случаи неотложной терапии). Лишь когда возникают вторичные осложнения, например инсульт, появляются и симптомы заболевания. Следовательно, любые побочные эффекты, какими бы тривиальными они ни были, ухудшают самочувствие пациента, поэтому пациенты неохотно принимают лекарства длительно.
Фармакотерапевтическим эффектом терапии гипертензии обладает большая группа лекарственных средств с различными механизмами действия
Выбор лекарственного средства зависит от нескольких факторов: клинической эффективности препарата, его стоимости, индивидуальной переносимости пациентом и сопутствующих заболеваний (таких как ЗСН или диабет, обусловливающий необходимость применения ингибиторов АПФ в качестве препаратов первой линии).
Для лечения гипертензии используют лекарственные средства различных классов, однако их классификация неоднородна
На выбор лекарственного средства может повлиять тип гипертензии, а также некоторые другие клинические условия.
В целом существуют лишь незначительные различия между популяциями пациентов по способности их организма отвечать быстрым снижением кровяного давления на лекарственные средства. Но некоторые группы пациентов при длительном лечении могут лучше реагировать на препараты определенного класса. Так, лица, принадлежащие к европеоидной расе, лучше, чем пациенты негроидной расы, реагируют на антагонисты адренорецепторов и ингибиторы АПФ, а пожилые люди лучше реагируют на антагонисты Са2+ и диуретики по сравнению с молодыми. Однако вариабельность ответа в большей степени зависит от индивидуальных особенностей пациента, чем от принадлежности к той или иной популяции. Конечная цель терапии состоит в снижении смертности среди пациентов с гипертензией. Установлено, что этой цели отвечают немногие лекарства, включая тиазидные диуретики и ингибиторы АПФ. Существуют опасения, что препараты некоторых классов не снижают, а повышают смертность.
Диуретики относятся к полезным антигипертензивным средствам, однако их благоприятный эффект может быть не связан с влиянием на диурез
Фармакология диуретиков подробно описана в главе 12. Для лечения гипертензии используют диуретики трех типов:
- тиазиды;
- петлевые диуретики;
- калийсберегающие средства.
Ранее полагали: диуретики снижают кровяное давление в результате повышения экскреции воды почками, что приводит к снижению объема плазмы и внеклеточной жидкости, а также уменьшает сердечный выброс. Однако существует несколько причин, заставляющих усомниться в этом, и главная из них заключается в том, что антигипертен-зивная активность целого спектра диуретических средств не является прямо пропорциональной их диуретической активности:
- тиазиды относятся к сравнительно эффективным антигипертензивным средствам, но обладают лишь умеренной активностью как диуретики;
- петлевые диуретики — относительно неэффективные антигипертензивные средства (у пациентов с нормальной функцией почек), однако принадлежат к сильным диуретикам.
Если бы антигипертензивное действие тиазидов было вызвано их диуретическим эффектом, то кривая доза-ответ должна была бы представлять производное наложения двух эффектов, чего в действительности нет (рис. 13.35). Триамтерен не является антигипертензивным средством, несмотря на то что его диуретический эффект подобен таковому антигипертензивного препарата амилорида. С другой стороны, тиазиды утрачивают эффективность у пациентов с умеренной почечной недостаточностью.
Рис. 13.35 Отношение доза-ответ для тиазидов как антигипертензивных средств (влияние на кровяное давление) и как диуретиков (влияние на экскрецию К+). Кривые не перекрываются, что указывает на независимость двух эффектов.
Таким образом, хотя диурез все еще считают ответственным за благоприятный эффект диуретиков при гипертензии, становится более очевидным, что механизм действия этих препаратов при лечении гипертензии выяснен недостаточно.
Предполагают, что диуретики (особенно тиазиды) оказывают эффект при гипертензии, модулируя активность К+-каналов. Регулируемые АТФ К+-каналы, играющие роль в сопротивлении артериол, могут быть активированы тиазидами. Этот эффект на молекулярном уровне приводит к гиперполяризации мембраны, которая противостоит поступлению Са2+ в гладкие мышцы и их сокращению, а на системном уровне — снижает периферическое сосудистое сопротивление.
Тиазиды — наиболее широко применяемые антигипертензивные диуретики
Тиазидные диуретики (например, бендрофлуметиазид, гидрохлоротиазид) и тиазидоподобные лекарственные средства, производные сульфонамида (например, хлорталидон), активно транспортируются посредством чувствительных к пробенециду секреторных механизмов в проксимальные почечные канальцы. Препараты этой группы как диуретики действуют на люминальную мембрану кортикального разводящего сегмента дистальных извитых канальцев.
Тиазиды могут вызвать половую дисфункцию у мужчин. Поскольку гипертензия (у лиц пожилого возраста) обычно связана с импотенцией, трудно определить распространенность и воздействие этого побочного эффекта. Относительно высокие дозы тиазидных диуретиков способны индуцировать гиперурикемию и неблагоприятно влияют на концентрацию липидов и глюкозы в сыворотке. Кроме хорошо известных тиазидных диуретиков, применяют менее распростаненные препараты.
Хинетазон по своим характеристикам сходен с другими тиазидами. Его можно использовать для лечения гипертензии (и уменьшения отеков при сердечной недостаточности) перорально в дозе 1-2 таблетки (по 50 мг) 1 раз в день. Поскольку он относительно долго сохраняет активность, обычно достаточно однократного суточного приема. Для некоторых пациентов может быть необходима общая дневная доза 150-200 мг. При использовании хинетазона в комбинации с другими антигипертензивными средствами доза каждого лекарства часто может быть снижена.
Метолазон был описан ранее в связи с его применением для лечения отеков, обусловленных сердечной недостаточностью. При слабой до умеренной эссенциальной гипертензии его назначают перорально в дозе 2,5-5 мг 1 раз в день. Можно использовать таблетку быстрого действия — 0,5 мг 1 раз в день, обычно утром. Если эффект недостаточен, дозу можно повысить до 1 мг/сут. Увеличение дозы свыше 1 мг не усиливает эффект.
Бензтиазид был описан ранее в связи с его применением для лечения сердечной недостаточности. В случае гипертензии его можно использовать либо в качестве монотерапии, либо для усиления эффективности других антигипертензивных средств при более тяжелых формах гипертензии. Лечение следует начать перорально с дозы 50-100 мг/сут в 2 приема. Эту дозировку можно сохранить и далее, пока не произойдет терапевтически значимое падение кровяного давления. В дальнейшем дозировка должна быть скорригиро-вана в соответствии с реакцией пациента — в сторону либо повышения до 50 мг 4 раза в день, либо снижения до минимального эффективного уровня. Также для лечения гипертензии используют метиклотиазид (5 мг) и политиазид (2 мг), принимаемые перорально 1 раз в день. Их применяют в качестве монотерапии или в комбинации с другими средствами.
Гипокалиемия может возникнуть как побочный эффект длительного лечения тиазидами
Характерным побочным эффектом тиазидов является повышение концентрации Na+ в дистальных извитых канальцах, что нарушает реабсорбцию К+, т.к. последнюю опосредует Nа+/К+-АТФаза и, следовательно, она зависит от соответствующего градиента Na+, чтобы создать возможность обмена Na+/K+. Таким образом, тиазидные диуретики могут вызвать повышение экскреции К+ (калийурез) и, возможно, гипокалиемию. Однако, если при лечении гипертензии используют низкие дозы тиазидов, эти потенциальные изменения могут не достигнуть клинической значимости. Заметная гипокалиемия, индуцированная малыми дозами тиазидных диуретиков у пациентов с гипертензией, может стать свидетельством существования первичного альдостеронизма. К счастью, максимальный антигипертензивный эффект тиазидов проявляется при очень низких дозах — 25-50 мг/сут. Если же гипокалиемия возникает, она может вызвать или усилить предсуществующие сердечные аритмии. Избежать гипокалиемии можно с помощью дополнительного назначения калия (хлорид калия перорально). С другой стороны, тиазиды можно использовать в комбинации с калийсберегающими средствами.
Тиазиды способны повышать уровень ренина в плазме (из-за повышенного удаления Na+ из крови вследствие диуреза), поэтому возрастает синтез ангиотензина II и вслед за этим высвобождение альдостерона. Альдостерон способствует выведению К+ через почки, что обусловливает гипокалиемический эффект тиазидов. Сопутствующее применение антагониста β-адренорецепторов или ингибитора АПФ снижает активность ренина или ангиотензина в плазме соответственно. Это может улучшить зависимый от альдостерона компонент гипокалиемического эффекта тиазидов. Кроме того, ингибиторы АПФ потенцируют гипотензивные эффекты тиазидов.
Индуцированной диуретиками гипокалиемии можно избежать, используя калийсберегающие диуретики
Так называемые калийсберегающие диуретики действуют на собирательный проток коркового слоя почки, где происходит обмен ионов Na+ на ионы К+ и Н+ с помощью обменного механизма, регулируемого эндогенным альдостероном:
- такие препараты, как амилорид и триамтерен, действуют на люминальную мембрану. Молекулярный механизм их действия — это блокада Na+-каналов и неконкурентный антагонизм по отношению к альдостерону;
- спиронолактон представляет собой обратимый конкурентный антагонист альдостерона по отношению к внутриклеточным рецепторам в люминальной мембране коркового собирательного протока. Спиронолактон действует как антагонист минералокортикостероидных эффектов альдостерона (рис. 13.36). В дополнение к быстрому действию на клеточные мембраны альдостерон связывается с внутриклеточными минералокортикостероидными рецепторами как в эпителиальных (например, почки), так и неэпителиальных (например, сердце, кровеносные сосуды и мозг) тканях и повышает кровяное давление путем индукции реабсорбции натрия и, возможно, другими механизмами. Этот препарат не используют для лечения первичной гипертензии вследствие его потенциально опасных побочных эффектов, особенно у пациентов мужского пола, у которых он интерферирует с синтезом и действием тестостерона.
Рис. 13.36 Яосартан и кандесартан используют для лечения гипертензии главным образом благодаря их антагонистической активности в отношении рецептора ангиотензина I (ATI). Оба средства снижают уровень альдостерона в крови и расширяют артериолы. Антигипертензивные свойства эплеренона обусловлены его блокирующим действием на рецепторы альдостерона.
Эплеренон — первое антигипертензивное средство нового класса антагонистов альдостерона
Эплеренон принадлежит к новому классу антагонистов альдостерона (см. рис. 13.36). Очень важным является тот факт, что замещение карбоксиметильной группы при атоме углерода 17 заметно снижает аффинность эплеренона к другим стероидным рецепторам по сравнению со спиронолактоном. Сниженное взаимодействие с рецепторами половых гормонов объясняет малую вероятность возникновения побочных эффектов эплеренона, в частности гинекомастии.
Рекомендуемая начальная доза эплеренона составляет 50 мг перорально 1 раз в день. Полный терапевтический эффект проявляется в течение 4 нед. Для пациентов, у которых прием препарата в дозе 50 мг/сут не дал желаемого снижения кровяного давления, дозировку следует повысить до 50 мг 2 раза в день. Дальнейшее повышение дозы не рекомендуется, т.к. это не оказывает большего эффекта, чем прием 100 мг, и возрастает риск гиперкалиемии.
В клинических исследованиях применение эплеренона в дозах 50-200 мг/сут значительно снижало систолическое и диастолическое кровяное давление, а эффективность сохранялась в течение всего интервала до очередного приема. Эффект эплеренона не зависел от возраста, пола или расы пациентов за одним исключением — при низкорениновой гипертензии снижение кровяного давления у пациентов негроидной расы было выражено в меньшей степени, чем у других пациентов в начальный период лечения.
Эплеренон можно использовать вместе с ингибиторами АПФ, антагонистами рецепторов ангиотензина II, антагонистами Са2+, β-блокаторами и гидрохлоротиазидом. Существуют многочисленные побочные эффекты эплеренона:
- головная боль;
- головокружение;
- диарея;
- желудочные боли;
- кашель;
- чрезмерная усталость;
- симптомы, сходные с гриппом;
- увеличение или повышенная чувствительность молочных желез;
- аномальное вагинальное кровотечение.
Некоторые менее частые побочные эффекты могут быть серьезными:
- боль в груди;
- онемение в руках и ногах;
- потеря мышечного тонуса;
- слабость или тяжесть в ногах;
- спутанность сознания;
- утрата сил;
- холодная, серая кожа;
- нерегулярное сердцебиение.
Эплеренон противопоказан при следующих состояниях:
- гиперкалиемия;
- диабет II типа (инсулинонезависимый) с микроальбуминурией (белок в моче);
- заболевание почек;
- одновременном приеме калия или калийсберегающих диуретиков (амилорид, триамтерен или спиронолактон).
Примерно 50% эплеренона связываются с белками плазмы. Он метаболизируется в печени главным образом посредством CYP3A4 и имеет Т1/2 равный 4-6 час, поэтому существует возможность лекарственного взаимодействия на уровне связывания с белками плазмы и метаболизма (особенно с кетоконазолом).
К другим диуретикам, используемым для лечения гипертензии, относят индапамид и торсемид. Есть сообщения, что индапамид в дозе 1,5 мг (перорально 1 раз в день) — наиболее эффективное лекарственное средство, снижающее систолическое кровяное давление на протяжении 2-3 мес с начала терапии. Это важный момент в предотвращении вторичного сердечно-сосудистого риска (т.е. инсульта) среди пациентов с гипертензией. Индапамид — прототипичный для класса индолиновых диуретиков препарат, ингибирующий карбоангидразу в почках. Подобно тиазидам, он в равной степени эффективно снижает кровяное давление и отеки, ассоциированные с ЗСН. Индапамид связывается на 79% с белками плазмы, и более 90% препарата метаболизируется перед элиминацией. Индапамид выводится главным образом почками (70%) и с фекалиями. Существует риск гипонатриемии и гипокалиемии, особенно в пожилом возрасте. У таких пациентов индапамид может усилить побочные эффекты применяемого одновременно дигиталиса. Индапамид способен повышать уровень мочевой кислоты в сыворотке, провоцируя подагру. В целом фармакология индапамида напоминает таковую тиазидов. Торсемид относят к петлевым диуретикам, подобно фуросемиду (см. ранее). Торсемид также можно использовать для лечения гипертензии.
С учетом предсказуемых побочных эффектов диуретики как антигипертензивные средства пациенты переносят хорошо, лишь 10% пациентов вынуждены прекратить их применение после длительной терапии.
Симпатолитические средства представляют собой гетерогенную группу препаратов, которые снижают кровяное давление, действуя на симпатическую нервную систему
Активность симпатической нервной системы играет важную роль в быстрой регуляции кровяного давления (см. рис. 13.30). Симпатолитические средства снижают кровяное давление, ингибируя один компонент или несколько:
- некоторые симпатолитики действуют центрально — на вазомоторный центр головного мозга, обусловливая снижение симпатического тонуса;
- другие симпатолитики действуют периферически — на адренергическую нейропередачу на пре- или постсинаптическом уровне или на рецепторы, активированные циркулирующим эпинефрином и высвобождаемым нервной системой норэпинефрином.
Многие симпатолитические средства опосредованно влияют на сердечную, сосудистую и другие ткани, действуя на нервную ткань. Другие, например антагонисты β-адренорецепторов, прямо действуют на рецепторы норэпинефрина и эпинефрина сердечно-сосудистой системы. Описание симпатолитиков далее расположено в порядке, отражающем избирательность их действия как симпатолитиков, а не частоту их использования в качестве антигипертензивных средств. Неселективные симпатолитики (например, ганглиоблокаторы и блокаторы адренергических нейронов) в настоящее время используют редко вследствие побочных эффектов.
β-Блокаторы занимают второе место после диуретиков по частоте применения в качестве антигипертензивных средств
Механизм антигипертензивного действия β-блокаторов еще недостаточно изучен. Эти препараты обладают целым спектром эффектов, и благоприятный эффект каждого из них может зависеть от его индивидуальных, специфических свойств:
- молекулярный механизм действия в основном обусловлен конкурентным антагонизмом в отношении β1адренорецепторов, хотя свой вклад может вносить также антагонизм по отношению к β2-адренорецепторам. Этот вопрос еще до конца не изучен;
- механизм действия на уровне тканей неясен. β-Блокаторы могут действовать на ЦНС, снижая симпатический тонус, на сердце, уменьшая частоту сердечных сокращений и сердечный выброс, на почки, снижая продукцию ренина. Общим признаком является уменьшение периферического сопротивления, однако его механизмы остаются невыясненными.
В клинике используют большое число различных β-блокаторов (рис. 13.37). Они различаются по способности блокировать β1адренорецепторы в сердце и ЦНС в сопоставлении с β2-рецепторами бронхов и периферических кровеносных сосудов.
Атенолол и метопролол принадлежат к относительно избирательным β1антагонистам, применяемым для лечения гипертензии
Термин «кардиоселективный» традиционно используют для описания избирательно действующих антагонистов β1рецепторов, хотя эти средства влияют на любые ткани, экспрессирующие β1адренорецепторы. Кардиоселективные β1блокаторы, такие как атенолол и метопролол, противодействуют эффектам норэпинефрина и эпинефрина в отношении частоты сердечных сокращений, однако обладают менее выраженным действием на дыхательные пути, чем неселективные β-блокаторы. Тем не менее, поскольку избирательность действия этих лекарственных средств на β2рецепторы по сравнению с β2-рецепторами лишь относительна (разница менее 8-кратной), они противопоказаны пациентам с астмой вследствие возможности развития бронхоспазма, за исключением особых случаев (например, когда другие антигипертензивные средства пациент не переносит, а необходимость какой-либо лекарственной терапии существует).
Пиндолол — частичный агонист β1-рецепторов, используемый для лечения гипертензии
Для лечения гипертензии используют избирательные частичные агонисты β1адренорецепторов, в частности пиндолол. Эти препараты ингибируют избыточную активность β1адренорецепторов, возникающую под влиянием симпатической гиперактивности, однако оказывают общий β1агонистический эффект при низком симпатическом тонусе. В свое время частичные агонисты β1адренорецеторов были описаны как β1-блокаторы с присущей им симпатомиметической активностью. Частичные агонисты β1адренорецепторов снижают кровяное давление примерно в той же степени, что и β1-блокаторы, однако вызывают менее выраженное снижение частоты сердцебиений. Это может быть полезно, если пациент получает одновременно средства, увеличивающие интервал QT, т.к. брадикардия способствует расширению QJ, что может привести к возникновению ЖТ torsades de pointes. Кроме этого эффекта клиническое значение частичного агонизма неизвестно. Не установлено также, что частичные агонисты, в отличие от β1блокаторов, оказывают благоприятное влияние в отношении предотвращения вторичного инфаркта миокарда.
Лабеталол и карведилол — неселективные антагонисты а1- и β1-адренорецепторов, используемые для лечения гипертензии
Соотношение между β1 и a1-антагонизмом, выявляемое терапевтически, для карведилола составляет 10 : 1, для лабеталола — 4:1. Подобно пиндололу, эти лекарственные средства снижают кровяное давление, уменьшая периферическое сосудистое сопротивление при отсутствии изменений частоты сердечных сокращений и минутного объема сердца. Карведилол обладает и другими эффектами, которые могут играть дополнительную роль при его использовании для лечения сердечной недостаточности.
Небиволол является относительно избирательным β1-блокатором, эффект которого при лечении гипертензии исследуют
Имеются данные, указывающие на уникальность этого препарата среди β-блокаторов как средства, обладающего дополнительным свойством вызывать зависимую от эндотелия вазодилатацию. Этот эффект обусловливает метаболит с активностью агониста β2-адренорецепторов, вызывающий NO-зависимое расширение артериол.
При лечении гипертензии β-блокаторы имеют благоприятное отношение польза-риск
Побочные эффекты β-блокаторов редко вызывают опасение, тем не менее они могут послужить причиной отказа от их применения при лечении гипертензии:
- антагонизм в отношении β1адренорецепторов может резко ухудшить симптомы ЗСН, снижая сердечный выброс, хотя при длительном лечении ЗСН антагонисты β1адренорецепторов применяют в низких дозах (см. ранее)',
- антагонизм в отношении β2-адренорецепторов (основа некардиоселективного действия) может привести к бронхоспазму (что служит противопоказанием к применению у пациентов с астмой, хотя появляются данные, указывающие на парадоксальное улучшение состояния при астме в случае длительного применения антагонистов β2-адренорецепторов; см. главу 14), а также к замедленному выходу из состояния гипогликемии у пациентов с диабетом.
Благоприятный эффект β-блокаторов как лекарственных средств, используемых для предотвращения вторичного инфаркта миокарда у пациентов с гипертензией, может превосходить риск у многих пациентов, страдающих сопутствующим обструктивным легочным заболеванием или диабетом II типа.
Внезапное прекращение приема β-блокаторов может вызвать стенокардию и ОИМ
Внезапное прекращение приема β-блокаторов может вызвать возобновление симптомов симпатической стимуляции сердца, приводя к стенокардии и ОИМ. В случае отсутствия эффекта β-блокатора или плохой переносимости рекомендуют прекращать его прием постепенно, а не делать резкого перехода к использованию другого препарата.
Антагонисты а1адренорецепторов особенно благоприятно действуют при лечении гипертензии у пациентов с доброкачественной гиперплазией предстательной железы
Празозин был первым избирательным препаратом, молекулярный механизм действия которого основан на антагонизме в отношении a1адренорецепторов. Празозин и его аналоги, такие как теразозин и доксазозин (табл. 13.12), прямо действуют на a1-адренорецепторы, которые в изобилии экспрессированы в артериолах, создающих сосудистое сопротивление, где они опосредуют сосудосуживающий ответ на циркулирующий эпинефрин и норэпинефрин, высвобождаемый адренергическими нейронами. Следовательно, антагонисты а1адренорецепторов действуют, ингибируя этот тонус и снижая периферическое сосудистое сопротивление. Празозин превосходит более старые неселективные средства, блокирующие а2- и aa1-адренорецепторы. В обычных условиях норэпинефрин ограничивает собственное высвобождение, действуя на пресинаптические а2-рецепторы (отрицательная обратная связь). Препараты, блокирующие а2-рецепторы, повышают высвобождение норэпинефрина из симпатических нервных окончаний, а неограниченное выделение норэпинефрина в сердце вызывало бы избыточную стимуляцию постсинаптических β1адренорецепторов и тахикардию. В связи с этим неселективные а-антагонисты не применяют в качестве антигипертензивных средств. Поскольку празозин избирателен в отношении a1-рецепторов, механизм отрицательной обратной связи остается интактным, означая, что терапевтическая эффективность препарата не снижается под влиянием тахикардии (рис. 13.38).
Рис. 13.38 Антагонистическое действие на постсинаптические а-адренорецепторы. Празозин (агента гон ист) предотвращает вазоконстрикцию, вызываемую норэпинефрином. Затем эффекты норэпинефрина ослабляются посредством механизма отрицательной обратной связи, т.к. празозин не блокирует пресинаптические а2-адренорецепторы и они могут взаимодействовать с норэпинефрином, активируя отрицательную обратную связь.
Антагонисты a1-адренорецепторов изменяют уровень ЛПНП и апопротеина В в плазме, в связи с чем общий уровень ЛПНП снижается, так же как уровень липопротеинов очень низкой плотности и общий уровень триглицеридов. Эти препараты повышают уровень холестерина липопротеинов высокой плотности и, следовательно, уменьшают эффект одного из факторов риска, ассоциированного с болезнью коронарных артерий. Клиническое значение этого феномена остается неизвестным.
Празозин назначают 2 раза в день, тогда как доксазозин и теразозин — 1 раз в день, что связано с их более длительным в плазме (что более удобно для пациентов).
Урапидил — антагонист a1адренорецепторов, обладающий дополнительной активностью агониста 5-НТ1А. В связи с этим его действие на ЦНС (продолговатый мозг) вызывает снижение тонуса симпатической нервной системы. Следовательно, урапидил снижает кровяное давление, не вызывая рефлекторной тахикардии, обычно возникающей при использовании других антагонистов а1адренорецепторов.
При пероральном применении эффект урапидила сопоставим с таковым большинства других антигипертензивных средств при гипертензии любой степени. В/в введение урапидила эффективно в случае гипертонического криза и при контроле гипертензии во время хирургического вмешательства.
В странах, где разрешено его использование (с 1980-х гг. оно доступно в Европе, Южной Америке и Азии, но не разрешено в США), его применяют в качестве альтернативного средства при относительных противопоказаниях в отношении других средств и у пациентов, не реагирующих на иные схемы лечения или нетолерантных к ним.
Побочные эффекты a1-антагонистов: постуральная гипотензия, головокружение, слабость, утомляемость, рефлекторная тахикардия (кроме урапидила) и головная боль, а также слабый седативный эффект, сухость во рту и отсутствие эякуляции.
|
Таблица 13.12 Празозин и его аналоги | |||||
|
Лекарственные средства |
Основные показания |
Обычные дозы п/о (мг/сут) |
Т1/2 в плазме (час) |
Метаболизм и элиминация |
Побочные эффекты |
|
Празозин |
Гипертензия ЗСН Феномен Рейно |
3-7,5 |
4 |
Метаболизм в печени, 50% при первом прохождении |
Гипотензия (редко); усиливается гипонатриемией |
|
Теразозин |
Гипертензия |
1-20 |
12 |
Метаболизм в печени, 50% при первом прохождении Элиминация с желчью/ фекалиями |
Редко головокружение, головная боль, заложенность носа |
|
Доксазозин |
Гипертензия ЗСН ДГПЖ |
2-16 |
19-22 |
Метаболизм в печени, низкий при первом прохождении Элиминация с желчью/ фекалиями |
Сходные с эффектами теразозина |
Рис. 13.39 Антагонистическое действие на пресинаптические а2-адренорецепторы. В результате предотвращается высвобождение норэпинефрина и последующий постсинаптический схгагонизм. Клонидин представляет собой селективный а2-агонист. Постсинаптическим рецептором является бета1 в сердце он опосредует тахикардию, в кровеносных сосудах — вазоконстрикцию.
Применение агонистов а2-адренорецепторов для лечения гипертензии в целом нельзя считать предпочтительным выбором
Действующие центрально агонисты a2-адренорецепторов, такие как клонидин, гуанфацин, гуанабенц и а-метилдопа, по своему действию напоминают аутоингибирующие эффекты норэпинефрина в отношении симпатической активности в отсутствие других симпатомиметических эффектов (рис. 13.39). Причина этого явления — в относительной избирательности действия на a2-рецепторы. Механизмы действия следующие:
- на молекулярном уровне — агонизм в отношении а2-адренорецепторов; в результате снижается активность вазомоторного центра в головном мозге, что приводит к падению активности симпатической нервной системы;
- снижение периферического сопротивления вследствие расслабления артериол. Однако при продолжающейся терапии доминирующими эффектами становятся снижение частоты сердцебиений и минутного объема сердца, особенно в случае применения клонидина.
Клонидин является широко используемым а2-агонистом, тогда как а-метилдопа представляет собой пролекарство, метаболизируемое в ходе двухэтапного ферментативного процесса с образованием а2-агониста метилнорэпинефрина (рис. 13.40). Поскольку при использовании ОС-метилдопы почечный кровоток поддерживается на хорошем уровне, этот препарат широко применяют при лечении гипертензии у пациентов с почечной недостаточностью или цереброваскулярным заболеванием. а-Метилдопу используют также во время беременности, т.к. препарат не оказывает вредного влияния на плод, несмотря на его переход через плацентарный барьер.
Рис. 13.40 Метаболизм метилдопы с образованием а-метилнорэпинефрина. Обратите внимание, что группа СН3 отсутствует в DOPA — эндогенном предшественнике дофамина, который метаболизируется теми же ферментами, превращаясь в норэпинефрин.
К побочным эффектам агонистов а2-адренорецепторов относят седативный эффект (в большей степени у клонидина и гуанабенца, чем у гуанфацина и гуанадрела), сухость во рту, ортостатическую гипотензию (в частности, у пожилых пациентов), сексуальную дисфункцию у мужчин и галакторею. В настоящее время (Х-метилдопу используют очень редко вследствие вызываемых этим препаратом серьезных побочных эффектов (включая диффузное паренхиматозное поражение печени, напоминающее эффекты вирусного гепатита, возможны в редких случаях лихорадка и гемолитическая анемия). Исключение — широкое применение во время беременности, когда препарат можно принимать без опасения длительный срок.
Использование клонидина пациентами с гипертензией ассоциировано с быстрым возвратом кровяного давления до уровня, которое было перед началом лечения, если терапию внезапно прекращают. Развивается синдром отмены, который характеризуется тахикардией, беспокойным состоянием и потоотделением.
Повторное повышение кровяного давления можно устранить, вернувшись к приему препатрата или используя периферически действующий антагонист a1-адренорецепторов, чтобы предотвратить опосредованную симпатической нервной системой периферическую вазоконстрикцию. Этих побочных эффектов можно избежать, снижая дозу клонидина постепенно.
Клонидин доступен в виде препарата для чрескожного применения с целью снижения кровяного давления до 7 сут с меньшей вероятностью появления побочных эффектов. Однако он может вызвать нежелательные эффекты в месте аппликации.
Алкалоиды раувольфии, в частности резерпин, блокируют адренергические нейроны, вызывая расширение артериол и снижение минутного объема сердца у пациентов с гипертензией
Резерпин транспортируется в периферические окончания симпатических нервов посредством процесса захвата 1 (механизм повторного захвата эпинефрина в нервы) и действует следующим образом:
- молекулярный механизм его действия заключается в ингибировании норэпинефринового насоса (АТФ- и Mg2+-зависимый захват), присутствующего в депо (везикулах) для эпинефрина в цитоплазме нейронов. Это снижает содержание норэпинефрина в депо и уменьшает опосредованное потенциалом действия высвобождение норэпинефрина из окончаний симпатических нервов;
- возникающие тканевый и системный эффекты заключаются в расширении артериол и уменьшении минутного объема сердца.
Подобно другим алкалоидам раувольфии, действие резерпина характеризуется медленным началом и сохраняющимися эффектами. Обычная начальная доза для пациента, не получающего других антигипертензивных средств, составляет в среднем 0,5 мг/сут перорально в течение 1-2 нед. Для поддержания эффекта дозу снижают до 0,1-0,25 мг/сут. Более высокие дозы следует применять с осторожностью, поскольку может значительно усугубляться серьезная психологическая депрессия и возрастать риск других побочных эффектов. Этого можно избежать путем тщательного подбора дозы.
Эффекты, вызванные действием резерпина на сердечно-сосудистую и нервную системы, могут персистировать какое-то время после прекращения приема лекарственного средства.
Побочные эффекты алкалоидов раувольфии как класса включают сухость во рту, заложенность носа и психологическую депрессию (реже). Противопоказан их прием вместе с ингибиторами моноаминоксидазы. С учетом этих факторов применять резерпин и родственные препараты стали реже.
Другие алкалоиды раувольфии, используемые для лечения гипертензии, включают десерпидин, раувольфию серпентина и ресциннамин. Десерпидин принимают перорально в дозе 250-500 мкг/сут в 1-2 приема. Раувольфию серпентина назначают перорально по 250-500 мг/сут в 1-2 приема. Начальная доза ресциннамина составляет 0,5 мг 2 раза в день. Поддерживающие дозы могут варьировать от 0,25 до 0,5 мг/сут. Более высокие дозы следует применять с осторожностью.
Гуанетидин обладает двумя механизмами действия на молекулярном и клеточном уровнях, которые совместно обусловливают блокаду адренергических нейронов
Гуанетидин и родственные гуанидиновые соединения, включая гуанадрел (и другие, не используемые в США терапевтические средства, в частности бетанидин и дебрисохин), подобно резерпину транспортируются в периферические окончания симпатических нервов посредством процесса захвата 1. Однако механизм их действия отличается от такового резерпина:
- первый молекулярный механизм — это конкуренция с норэпинефрином за внутриклеточный эпинефриновый насос. В адренергические везикулы поступает и депонируется преимущественно лекарственное средство, а не норэпинефрин, содержание которого в депо уменьшается;
- второй молекулярный механизм состоит в связывании лекарственного средства с внутренней поверхностью невролеммы, что препятствует ее слиянию с депо-везикулами, — действие, блокирующее адренергические нейроны. В результате уменьшается высвобождение норэпинефрина из окончаний симпатических нервов.
Резерпин и аналоги гуанидина имеют два общих побочных эффекта:
- постуральная гипотензия;
- генерализованная блокада симпатической нейропередачи.
Постуральная гипотензия (падение кровяного давления при изменении положения тела из горизонтального в вертикальное) возникает вследствие утраты рефлекса артериальной и венозной констрикции, опосредованного симпатической нервной системой. В нижних конечностях скапливается венозная кровь, уменьшая венозный возврат и сердечный выброс. По этой причине, а также в связи с доступностью новых, менее опасных лекарственных средств, гаунетидин в настоящее время используют только у пациентов с тяжелой гипертензией, которые не реагируют на другие препараты.
Для лечения гипертензии применяют антагонисты Са2+
Антагонисты Са2+ по химической структуре подразделяют на три группы (см. главу 2). Из них 1,4-дигидропиридины, нифедипин, никардипин и амлодипин обладают выраженной избирательностью в отношении сосудистой системы и являются наиболее эффективными антигипертензивными антагонистами Са2+, а фенетилалкиламин, верапамил, бензотиазепин и дилтиазем имеют меньшую избирательность в отношении сосудов и могут также влиять на АВ-узел, вызывая АВ-блокаду, поэтому применение верапамила и дилтиазема связано с проблемами проведения в сердце, особенно у пациентов, получающих антагонисты β1-адренорецепторов.
Пожилые пациенты с гипертензией хорошо реагируют на антагонисты Са2+. Однако организм лиц негроидной расы отвечает на эти препараты хуже. В целом действие антагонистов Са2+ проявляется быстро, и кровяное давление снижается в пределах 30 мин после введения.
Случайными побочными эффектами могут быть пульсирующая головная боль, учащенное сердцебиение, потоотделение, тремор и прилив крови (вследствие вазодилатации). Эти эффекты свойственны быстродействующим средствам, но почти полностью отсутствуют у медленнодействующих препаратов, которые и следует предпочесть. Основной побочный эффект при использовании верапамила — запоры, однако более важно то, что и верапамил, и дилтиазем могут оказать отрицательный инотропный эффект у пациентов с предсуществующей сердечной недостаточностью, поэтому таким пациентам эти лекарства противопоказаны. Нифедипин и амлодипин этим свойством не обладают (см. ранее).
Новые антагонисты Са2+, разрешенные в США для лечения гипертензии, — барнидипин (известный также как мепиродипин), лацидипин, лерканидипин и манидипин. Их свойства перечислены в табл. 13.4. Это препараты длительного действия, как у амлодипина, с невысоким риском побочных эффектов, в том числе отеков.
Барнидипин в дозе 20 мг перорально 1 раз в день обеспечивает 24-часовое снижение кровяного давления, эквивалентное достигаемому с помощью амлодипина и нитрендипина, однако вызывает меньше побочных эффектов, специфичных для данного класса лекарственных средств. Эффективность и безопасность барнидипина сохраняются при длительной терапии. Лацидипин имеет подобный профиль (сок грейпфрута неблагоприятно действует на его метаболизм). Лерканидипин, другое сходный препарат, по-видимому, уменьшает риск развития атеросклероза по механизму, не относящемуся к его антигипертензивному эффекту. Фармакология манидипина сходна с фармакологией лерканидипина.
Появляется все больше данных о том, что в действительности эти средства повышают смертность среди пациентов с гипертензией, что, возможно, связано с повышенным риском возникновения ОИМ, желудочно-кишечных кровотечений и рака. Если рассматривать лекарственные средства отдельно, то лишь для нифедипина можно отметить небольшое, но достоверное повышение общей смертности, а некоторые лекарственные средства (амлодипин, фелодипин, верапамил и дилтиазем), согласно опубликованным данным, не увеличивают смертность по тем же критериям. Нифедипин не следует использовать для лечения гипертензии в течение 2 нед после ОИМ.
Вазодилататоры прямого действия
Лекарственные средства, у которых молекулярный механизм расширения артериол не связан с антагонизмом в отношении a1-адренорецепторов или блокадой Са2+-каналов L-типа, традиционно называют прямо действующими вазодилататорами. Эти препараты используют для неотложной терапии гипертензии.
Гидралазин относится к препаратам третьей линии, используемым для терапии умеренной гипертензии. Это единственный прямо действующий вазодилататор, применяемый для лечения гипертензии (от слабой до умеренной степени) в качестве препарата второй или третьей линии. Вместе с тем его используют также как парентеральное средство неотложной терапии при гипертензии, а также во время беременности, поскольку в этих условиях доказана безопасность его длительного применения. Молекулярный и клеточный механизмы действия гидралазина заключаются в повышении уровня цГМФ после активации гуанилилциклазы, что приводит к расслаблению гладких мышц прекапиллярных сосудов и, соответственно, снижению кровяного давления вследствие уменьшения периферического сосудистого сопротивления (см. рис. 13.2). Гидралазин в дозах, превышающих 200 мг/сут, вызывает у некоторых пациентов волчаночноподобный синдром. Другие аспекты применения гидралазина при ЗСН описаны ранее.
Миноксидил высокоэффективно снижает кровяное давление, особенно при тяжелой гипертензии с почечной недостаточностью. Диазоксид сходен с миноксидилом, однако его используют редко (за исключением неотложных случаев) вследствие его побочных эффектов.
Миноксидил — более эффективный вазодилататор, чем гидралазин; вызывает расширение сосудов, определяющих сосудистое сопротивление. На молекулярном уровне он действует, активируя АТФ-чувствительные К+-каналы, что приводит к гиперполяризации сарколеммы гладких мышц и последующему снижению притока Са2+ через Са2+-каналы L-типа. Миноксидил принимают 1-2 раза в день, он очень эффективен у пациентов с тяжелой гипертензией и почечной недостаточностью. Подобно гидралазину, его назначают в комбинации с диуретиками и антагонистами адренорецепторов для предотвращения рефлекторного повышения сердечного выброса и задержки жидкости, которые могут быть значительными у некоторых пациентов.
Обычный побочный эффект миноксидила — рост волос на лице, что ограничивает его применение у женщин, но делает пригодным для лечения алопеции у мужчин.
Ингибиторы АПФ
Неактивный декапептид ангиотензин I под влиянием АПФ превращается в активный октапептид ангиотензин II (см. рис. 13.31). Ангиотензин II оказывает разнообразные эффекты, способствующие повышению кровяного давления (рис. 13.41): сужает артериолы и стимулирует высвобождение альдостерона из коры надпочечников. В свою очередь, альдостерон стимулирует реабсорбцию Na+ в почках (см. ранее применение спиронолактона и эплеренона). Каптоприл, снижая синтез ангиотензина II, вызывает вазодилатацию и уменьшает задержку Na+. Снижение кровяного давления может быть достигнуто блокадой либо АПФ, либо рецепторов ангиотензина II. Ингибиторы АПФ используют при всех типах гипертензии любой степени тяжести. Эти препараты снижают показатели смертности. Их классифицируют по химической структуре на основании присутствия в молекуле сульфгидрильного, карбоксильного или фосфинильного компонентов. Ингибиторы АПФ обладают следующими механизмами действия:
- молекулярный — подавление активности АПФ;
- в результате снижаются синтез ангиотензина II и метаболизм некоторых сосудосуживающих кининов (в частности, брадикинина).
Рис. 13.41 Эффекты ингибиторов ангиотензинпревращающего фермента (АПФ). Ингибиторы АПФ снижают концентрацию ангиотензина II (вазоконстриктор) и повышают концентрацию брадикинина (вазодилататор). Накопление брадикинина (нижняя часть рисунка) происходит в результате действия ингибиторов АПФ на кининазу II. Обратите внимание, что кининаза II и АПФ в действительности представляют собой один и тот же фермент (пептидилдипептидазу). ПГ — простагландин.
Ингибиторы АПФ
- Каптоприл
- Эналаприл
- Беназеприл
- Цилазаприл
- Фосиноприл
- Периндоприл
- Хинаприл
- Рамиприл
- Зофеноприл
- Моэксиприл
- Трандолаприл
Каптоприл взаимодействует с сульфгидрильными группами АПФ и является прототипичным ингибитором АПФ. Другими ингибиторами АПФ являются лизиноприл (в США его применяют чаще всего), эналаприл, беназеприл, цилазаприл, рамиприл, хинаприл (все они взаимодействуют с АПФ через его карбоксильный компонент) и фоси-ноприл (связывается с фосфинильной группой) (см. табл. 13.11). Карбоксилсодержащие ингибиторы АПФ (эналаприл, лизиноприл и т.д.) начинают действовать медленнее, чем каптоприл, но их эффект длится дольше. Многие ингибиторы АПФ представляют собой пролекарства, для обозначения их активных метаболитов добавляют суффикс «-ат». Например, эналаприл и рамиприл метаболизируются и превращаются в активные метаболиты эналаприлат и рамиприлат. Два новых ингибитора АПФ, периндоприл и зофеноприл, представляют собой пролекарства (соответственно, периндоприлат и SQ26333).
Неожиданно оказалось, что при длительном использовании ингибиторов АПФ концентрация ангиотензина II в крови восстанавливается до исходного (до лечения) уровня, однако сниженное кровяное давление сохраняется. Это указывает на существование дополнительных механизмов антигипертензивного эффекта, например изменение концентрации брадикинина в плазме. АПФ катализирует инактивацию брадикинина, являющегося эндогенным вазодилататором, поэтому фармакотерапевтические эффекты ингибиторов АПФ могут быть связаны с изменением баланса между действием ангиотензина II, брадикинина и, возможно, других кининов (см. рис. 13.41).
Ответ на ингибиторы АПФ при гипертензии заключается в:
- снижении периферического сопротивления с незначительными изменениями частоты сердечных сокращений и сердечного выброса;
- уменьшении задержки Na+, вторичном по отношению к изменению уровня альдостерона.
Ингибиторы АПФ при лечении гипертензии обладают такой же эффективностью, как диуретики или антагонисты β1адренорецепторов. Однако при одновременном применении ингибиторов АПФ и диуретиков общая терапевтическая эффективность может быть выше, чем при использовании того или другого препарата отдельно. Возможно, это частично связано с ослаблением неблагоприятного эффекта диуретиков на ренин-ангиотензиновую систему под влиянием ингибиторов АПФ.
Экспериментальные и клинические данные показывают, что снижение эфферентного артериолярного сопротивления вследствие снижения уровня ангиотензина II после лечения ингибиторами АПФ может быть полезным для пациентов с дисфункцией почек, особенно для лиц с диабетической нефропатией или общим снижением почечной функции. Это обусловлено тем, что подавление активности ангиотензина II способно вызвать существенное уменьшение перфузионного давления. В результате у таких пациентов может возникнуть почечная недостаточность.
Ингибиторы АПФ имеют мало побочных эффектов, поэтому эти препараты предпочтительны для терапии. Одним из необычных побочных эффектов является характерный кашель, предположительно обусловленный действием брадикинина, метаболизм которого подавляют ингибиторы АПФ (см. главу 14). Этот эффект наименее выражен у фосиноприла, структурно отличающегося от других ингибиторов АПФ.
Антагонисты рецепторов ангиотензина II
Прототипичный препарат саралазин оказался неподходящим для терапевтического применения, поскольку он представляет собой иммуногенный пептид и неактивен при пероральном приеме, поэтому были получены непептидные, активные при пероральном применении соединения — лосартан, кандесартан, ирбесартан и олмесартан. Лосартан был первым антагонистом ангиотензина II, использованным для лечения гипертензии. Это пролекарство, превращающееся в активный метаболит (ЕХР3174). Он представляет собой антагонист рецепторов ATI, поэтому снижает индуцированное ангиотензином II высвобождение альдостерона из коры надпочечников и вазоконстрикцию артериол (см. рис. 13.36). Лосартан хорошо переносим и столь же эффективен, как эналаприл и нифедипин. Ответ на этот препарат развивается медленно, кровяное давление снижается на протяжении нескольких недель при продолжающемся лечении. Начальная доза составляет 50 мг перорально 1 раз в день, что удобно для приема, однако возможен прием 2 раза в день. Используют также комбинацию с фиксированной дозой: 12,5 мг гидрохлоротиазида и 50 мг лосартана. В отличие от ингибиторов АПФ, лосартан и родственные препараты не влияют на деградацию брадикинина. До сих пор не установлено, способствует ли это благоприятному фармакотерапевтическому эффекту. Ингибиторы АПФ противопоказаны во время беременности, существует возможность фетотоксичности и у антагонистов ATI. Кандесартан цилексетил представляет собой пролекарство, которое после приема внутрь гидролизуется с образованием активной формы — кандесартана. Кандесартан цилексетил в дозе 2-32 мг перорально дает гипертензивный эффект через 2 нед после начального приема, полный эффект наступает через 4 нед. После однократного приема лекарства снижение кровяного давления сохраняется более 24 час. Кандесартан цилексетил дополнительно снижает кровяное давление в комбинации с гидрохлоротиазидом. При одинаковых дозах обоих лекарственных средств кандесартан действует сильнее и немного эффективнее, чем лосартан. Рефлекторная тахикардия не возникает. При длительном применении кандесартан цилексетил сохраняет свою эффективность. Избирательность его действия на рецепторы ATI более чем в 10 000 раз выше, по сравнению с ATII. Оральная биодоступность кандесартана цилексетила равна 15%, максимальная концентрация достигается через 3-4 час. Объем распределения составляет 0,13 л/кг (> 99% кандесартана связывается с белками плазмы). Препарат слабо метаболизируется в печени путем О-деэтилирования, превращаясь в неактивный метаболит. Общий клиренс плазмы составляет 0,37 мл/мин/кг, около 26% дозы экскретируется в неизмененном виде с мочой и примерно 67% — с фекалиями. Т1/2 равен « 9 час. Побочные эффекты кандесартана немногочисленны и слабо выражены. Наиболее частой причиной прекращения его приема служат головная боль (0,6%) и головокружение (0,3%).
Другой антагонист рецепторов ATI — ирбесартан. Он имеет более высокую биодоступность (60-80%), в меньшей степени связывается с белками плазмы (90%) и менее избирателен в отношении ATI по сравнению с ATII, чем кандесартан (в 8500 раз). Однократный суточный пероральный прием 150 и 300 мг вызывает статистически и клинически достоверное снижение систолического и диастолического кровяного давления.
Механизмы действия антигипертензивных средств основных классов
- Тиазидные диуретики повышают экскрецию Na+ и временно уменьшают объем крови, однако механизм, посредством которого они снижают кровяное давление, неясен
- Симпатолитики снижают способность симпатической нервной системы повышать кровяное давление
- Вазодилататоры расслабляют гладкие мышцы сосудов и уменьшают периферическое сосудистое сопротивление
- Ингибиторы АПФ снижают периферическое сосудистое сопротивление и объем крови, не оказывая влияния на частоту сердечных сокращений
Олмесартан медоксомил применяют для лечения гипертензии в дозе до 40 мг/сут однократно. Подобно кандесартану цилексетилу и лосартану, он представляет собой пролекарство. К другим антагонистам ATI, применяемым для лечения гипертензии, относят эпросартан, телмисартан и валсартан. Обычно рекомендуемая стартовая доза эпросартана месилата (в таблетках) составляет 600 мг перорально 1 раз в день при использовании в качестве монотерапевтического средства при отсутствии гиповолемии у пациентов. Препарат можно принимать 1-2 раза в день при общей суточной дозе 400-800 мг.
Антагонисты имидазолина II
Моксонидин в дозе 200 или 400 мкг перорально снижает кровяное давление посредством двух механизмов. Он является агонистом рецепторов имидазолина I1 в ростровентролатеральном отделе продолговатого мозга, тем самым снижая активность симпатической нервной системы. Предполагают также, что моксонидин агонистически действует на а2-рецепторы головного мозга, оказывая эффект, подобный вызываемому клонидином (см. рис. 13.39). Однако моксонидин более избирателен по отношению к рецепторам I1 по сравнению с a2-рецепторами, и у него отсутствует эффект подавления дыхания, который приписывают центральной а2-активации. В связи с этим моксонидин вызывает меньше побочных эффектов, чем клонидин. Снижение кровяного давления, вызываемое моксонидином, обычно сопровождается уменьшением частоты сердечных сокращений, которое имеет меньшую длительность и величину, чем падение кровяного давления. Конечный T1/2 моксонидина составляет 2 час. Элиминация осуществляется главным образом через почки. Побочные эффекты немногочисленны и слабо выражены: сухость во рту, головная боль, головокружение и утомляемость.
Антагонисты дофамина
Фенолдопан — избирательный агонист дофамина D1, вызывающий расширение сосудов, повышение почечной перфузии и усиление натрийуреза у пациентов с гипертензией. Фенолдопан действует непродолжительно вследствие короткого Т1/2, равного менее 10 мин. Его используют как средство парентеральной терапии для хирургических пациентов с гипертензией высокого риска, для периоперационного ведения пациентов при трансплантации почки и других органов, а также после введения рентгеноконтрастного вещества пациентам группы высокого риска. Это прототипичное лекарственное средство разрешено в США для применения в больничных условиях с целью кратковременного лечения (до 48 час) тяжелой гипертензии, когда необходимо получить быстрое, но легко обратимое снижение кровяного давления, включая злокачественную гипертензию с ухудшением функции периферических органов. Короткая продолжительность действия фенолдопана позволяет избежать стойкого избыточного снижения кровяного давления в условиях неотложной помощи.
Комбинированное лечение
Эффективным фармакотерапевтическим подходом при гипертензии является применение комбинации двух или более лекарственных средств. Совместное применение препаратов, обладающих различными механизмами действия, дает возможность уменьшить их дозы, тем самым ослабляя побочные эффекты. В США существует большой спектр комбинаций с фиксированным соотношением доз, разрешенных для применения (табл. 13.13), некоторые из них выпускают в готовой форме (в виде таблеток или капсул). Дозы лекарственных средств в комбинации меньше, поэтому побочные эффекты возникают реже. Кроме того, пациенту легче принимать сразу все необходимые лекарства, а не каждое в отдельности. Все комбинации включают лекарственные средства, рассмотренные в этой главе, за исключением петлевого диуретика пиретанида, который ингибирует котранспортер Na+/K+/Cl".
Антагонисты β-адренорецепторов и антагонисты Са2+ (только дигидропиридины), применяемые в комбинации, пациенты обычно хорошо переносят при условии тщательного подбора дозы. Комбинация нифедипина с антагонистами β-адренорецеп-торов способна вызвать брадикардию и сердечную недостаточность вследствие синергизма лекарственных эффектов (один из них опосредован антагонизмом в отношении β1адренорецепторов сердца, другой — в отношении Са2+-каналов L-типа желудочков).
Диуретик в комбинации с ингибитором АПФ (например, гидрохлоротиазид и периндоприл) представляют собой эффективную комбинацию для лечения гипертензии, которую хорошо переносят многие пациенты с гипертензией от слабой до умеренной степени. Достоинством комбинаций диуретиков с ингибиторами АПФ является их аддитивный эффект в снижении кровяного давления. Комбинация ингибиторов АПФ и антагонистов Са2+ также эффективно снижает кровяное давление и обычно хорошо переносима. Однако в этом случае аддитивный эффект, как правило, не возникает.
Таблица 13.13 Комбинации антигипертензивных средств с фиксированным соотношением доз
- Амилорид гидрохлорид + гидрохлоротиазид
- Амлодипин бесилат + беназеприл гидрохлорид
- Атенолол + хлорталидон
- Беназеприл гидрохлорид + гидрохлоротиазид
- Бендрофлуметиазид + надолол
- Бисопролол фумарат + гидрохлоротиазид
- Кандесартан цилексетил + гидрохлоротиазид
- Каптоприл + гидрохлоротиазид
- Хлоротиазид + метилдопа
- Хлоротиазид + резерпин
- Хлорталидон + клонидин
- Хлорталидон + резерпин
- Десерпидин + метиклотиазид
- Дилтиазем + эналаприл
- Эналаприл + фелодипин
- Эналаприл + гидрохлоротиазид
- Эпросартан месилат + гидрохлоротиазид
- Фосиноприл + гидрохлоротиазид
- Гуанетидин + гидрохлоротиазид
- Гидралазин + гидрохлоротиазид
- Гидралазин + гидрохлоротиазид + резерпин
- Гидрохлоротиазид + ирбесартан
- Гидрохлоротиазид + лизиноприл
- Гидрохлоротиазид + лосартан
- Гидрохлоротиазид + метилдопа
- Гидрохлоротиазид + метопролол
- Гидрохлоротиазид + моэксиприл
- Гидрохлоротиазид + олмесартан медоксомил
- Гидрохлоротиазид + пропранолол
- Гидрохлоротиазид + хинаприл
- Гидрохлоротиазид + резерпин
- Гидрохлоротиазид + спиронолактон
- Гидрохлоротиазид + телмисартан
- Гидрохлоротиазид + тимолол малеат
- Гидрохлоротиазид + триамтерен
- Гидрохлоротиазид + валсартан
- Гидрофлуметиазид + резерпин
- Периндоприл + индапамид
- Пиретанид (аценокумарол) + рамиприл
- Политиазид + празозин
- Политиазид + резерпин
- Резерпин + трихлорметиазид
- Трандолаприл + верапамил
Использование антагонистов β1-адренорецепторов вместе с антагонистами Са2+ (кроме дигидропиридинов) опасно
Применение антагонистов β1адренорецепторов в комбинации с антагонистами Са2+, не относящимися к дигидропиридинам (например, верапамилом), опасно, т.к. такие комбинации, по имеющимся данным, вызывают асистолию, выраженную брадикардию и гипотензию. Каждое из лекарственных средств, снижая внутриклеточный уровень Са2+ в сердце, уменьшает сократимость миокарда. Дигидропиридины, например нифедипин, не оказывают такого действия вследствие высокой избирательности по отношению к сосудам и отсутствия существенного влияния на ткани сердца.
Ингибиторы ренина снижают уровень ангиотензина II
Ингибиторы ренина представляют собой новый класс лекарственных средств, снижающих уровень ангиотензина II. Разработано несколько ингибиторов ренина с высокой активностью и продолжительным действием. Однако оральная биодоступность существующих сейчас средств слишком низка, чтобы достичь эффективной концентрации в плазме человека. Эндопептидаза 24.11 (нейтральная эндопептидаза) является ферментом, который гидролизует предсердный натрийуретический пептид (НУП). НУП обладает диуретическим, натрийуретическим и сосудорасширяющим свойствами; он высвобождается в результате изменений предсердного объема или давления и играет роль в регуляции кровяного давления. Теоретически ингибирование нейтральной эндопептидазы должно уменьшать деградацию НУП и тем самым повышать уровень циркулирующего НУП. Эта форма лекарственной терапии может оказаться благоприятной для пациентов с гипертензией. Однако прототипичный препарат омапатрилат до сих пор не получил разрешения на применение в США вследствие опасений относительно его вреда (возможность ангионевротического отека). Омапатрилат лишен избирательности, блокируя нейтральную эндопептидазу и АПФ.
Неотложная терапия гипертензии[править | править код]
Неотложная терапия необходима в ситуациях, когда повреждение органов-мишеней настолько обширное и острое, что жизнь пациента находится в непосредственной опасности. Не существует определенного уровня кровяного давления, который явился бы признаком неотложности. Ситуациями, связанными с необходимостью неотложной терапии, могут быть гипертоническая энцефалопатия, расслоение аневризмы аорты, ишемия миокарда и быстро развивающаяся почечная недостаточность вследствие гипертонической нефропатии. Применяемые лекарственные средства перечислены в табл. 13.14.
Нитропруссид натрия — непосредственно действующий вазодилататор, используемый в неотложной терапии гипертензии
Нитропруссид натрия вводят в/в для быстрого контролируемого снижения кровяного давления в неотложных случаях. Он имеет короткий Т1/2 (30-40 сек) и вызывает глубокое расширение артерий и вен (см. табл. 13.14). Его молекулярный механизм действия обусловлен NO (см. рис. 13.2). Нитропруссид натрия представляет собой пролекарство, спонтанно распадающееся с образованием NO в гладкомышечных клетках. NO повышает уровень цГМФ в гладкомышечных клетках сосудов в результате стимуляции активности цитозольной гуанилилциклазы (см. рис. 13.14).
Неотложная терапия гипертензии
- Необходима в тех случаях, когда повышенное артериальное давление представляет прямую угрозу для жизни пациента
- Эффективным средством в этих условиях является в/в введение нитропруссида натрия
Таблица 13.14 Лекарственные средства, используемые при гипертоническом кризе
|
Вазодилататоры |
Начало действия (мин) |
|
Нитропруссид натрия |
Немедленное |
|
Диазоксид |
2-4 |
|
Гидралазин |
10-20 |
|
Эналаприлат |
15 |
|
Никардипин |
10 |
|
Симпатолитики | |
|
Триметафан |
1-5 |
|
Эсмолол |
1-2 |
|
Лабеталол |
5-10 |
Нитропруссид натрия действует быстро и эффективно. Его можно использовать для быстрого снижения кровяного давления, однако важно проводить постоянный мониторинг кровяного давления, т.к. нитропруссид натрия может вызвать его резкое падение, что приведет к гипоперфузии жизненно важных органов. Доза должна быть тщательно подобрана в зависимости от реакции кровяного давления.
Ганглиоблокирующие лекарственные средства используют только в неотложной терапии гипертензии
Триметафан — антагонист никотиновых рецепторов, относительно избирательный по отношению к этим рецепторам в автономных ганглиях. Его применяют только в случаях неотложной терапии гипертензии, ассоциированной с расслоением аневризмы аорты.
При в/в введении это средство проявляет генерализованный антагонистический эффект в отношении как парасимпатических, так и симпатических ганглиев (т.е. прекращается желудочная моторика, не опорожняется мочевой пузырь и т.д.). В связи с этим триметафан не подходит для поддерживающей терапии гипертензии.
Другие способы лечения острого повышения кровяного давления
Очень высокое кровяное давление само по себе, в отсутствие острого заболевания, обычно не требует парентеральной терапии, которая может быть опасной. Если неотложная терапия не является настоятельно необходимой, лекарственные средства можно использовать перорально. Можно применять препараты любого класса, однако чаще всего используют:
- диуретики;
- антагонисты β-адренорецепторов;
- антагонисты Са2+;
- ингибиторы АПФ.
Побочные эффекты лекарственных средств на сердце[править | править код]
|
Таблица 13.15 Побочные эффекты лекарственных средств на сердце | ||
|
Лекарственные средства |
Побочные эффекты |
Примечания |
|
Доксорубицин |
Кардиопатия |
Общая доза должна быть ограничена |
|
Ибупрофен и родственные препараты |
Повышение кровяного давления |
Это не главная опасность |
|
Кокаин/амфетамины |
Повышение кровяного давления |
Опасен эффект злоупотребления |
ПАТОФИЗИОЛОГИЯ И ЗАБОЛЕВАНИЯ КРОВЕНОСНЫХ СОСУДОВ[править | править код]
Разнообразные заболевания вызывают общие или местные расстройства кровоснабжения тех или иных тканей или органов и рассматриваются здесь вместе как заболевания периферических сосудов.
Механизмы действия лекарственных средств, используемых для лечения заболеваний периферических сосудов, описаны в данной главе (например, фармакология препаратов, расширяющих артериолы см. ранее «Гипертензия», об антитромботических средствах см. ранее «Стенокардия») и в главе 10. Болезни сосудов, при лечении которых лекарственную терапию не применяют, здесь не рассматриваются.
Заболевания периферических сосудов[править | править код]
При этих заболеваниях поражаются артерии, что может быть вызвано рядом патологических процессов:
- артериосклерозом (рис. 13.42);
- дистрофической кальцификацией мышечноэластического слоя артерий, наблюдаемой при артериосклерозе Монкеберга, которая обычно развивается в крупных артериях нижних конечностей у пожилых людей и наиболее часто у пациентов с хроническим сахарным диабетом;
- кистозным медиальным некрозом или дегенерацией, что представляет собой мукоидную дегенерацию коллагена и эластической ткани среднего слоя стенки артерий, часто с кистозными изменениями, и встречается преимущественно у пожилых пациентов с гипертензией. Таким образом, заболевание периферических сосудов является показателем долго существующей гипертензии.
Рис. 13.42 Артериосклероз характеризуется утолщением и затвердением стенок артерий и артериол. Наиболее ранние изменения представляют собой небольшие жировые полоски, которые выглядят как бледные участки под эндотелием на сегменте аорты (слева). На сегменте в центре видны перламутрово-белые фибролипидные бляшки, а на сегменте справа можно видеть давние, изъязвленные бляшки с прилипшим тромбом, состоящим из фибрина и тромбоцитов (предоставлено Alan Stevens, Jim Lowe).
Для пациентов с предсуществующим заболеванием периферических сосудов эффективными средствами, замедляющими или предотвращающими формирование тромбоза, служат аспирин и дипиридамол, используемые для профилактики. Предполагается, что:
- аспирин предотвращает тромбоз при этом заболевании;
- дипиридамол предотвращает тромбоз и расширяет артериолы.
Принципы лечения заболеваний периферических сосудов
- Действие лекарственных средств должно быть направлено на устранение дефицита перфузии и вызвавшей его причины (например, сосудистого спазма), если таковая известна
- Применяют тромболитики, если перфузия нарушена вследствие тромбоза
- Артериодилататоры используют в случаях, когда причиной нарушения перфузии является сосудистый спазм
При заболевании периферических сосудов необходима местная терапия
- Лекарственные средства, которые предотвращают или устраняют тромбоз или снимают сосудистый спазм, действуют местно. Их применяют для лечения заболеваний периферических сосудов. В отличие от этого, при лечении болезни коронарных артерий (стенокардии) эффективной оказывается вазодилатация в отдаленных от сердца участках организма за счет снижения пред- или постнагрузки на сердце
Хроническая ишемия нижних конечностей и перемежающаяся хромота[править | править код]
Эта патология возникает как следствие атероматозного заболевания, захватывающего аорту, подвздошные артерии и/или другие периферические сосуды. Лечение направлено на профилактику тромбоза и включает прием низких доз аспирина (325 мг/сут) и хирургическое вмешательство.
Васкулит[править | править код]
Васкулит — это воспаление кровеносных сосудов, вызываемое отложением иммунных комплексов. В артериях, венулах или капиллярах, пораженных воспалением, возникает некроз и инфильтрация лимфоцитами и эозинофилами, приводящая к ишемии соответствующих тканей. Существуют различные формы васкулита: системный некротизирующий васкулит (например, нодозный полиартериит, аллергический ангиит), васкулит, обусловленный гиперчувствительностью (например, сывороточная болезнь, пурпура Геноха-Шонляйна), и васкулит, ассоциированный с отторжением трансплантата сердца (см. главу 15). Синдром Такаясу, редкое заболевание за пределами Японии, характеризуется васкулитом, поражающим дугу аорты, а также другие крупные артерии. Для терапии этого заболевания применяют глюкокортикостероиды, однако это не исключает возникновения сердечной недостаточности и цереброваскулярных осложнений.
Болезнь Рейно[править | править код]
При этом заболевании возникают эпизоды сильного спазма артерий, снабжающих кровью пальцы рук или ног. Обычно этот спазм вызывают холод или вибрация.
Прежде всего рекомендуется избегать воздействия холода и прекратить курить. Более тяжелые симптомы требуют применения вазодилататоров. Используемые лекарственные средства вызывают расширение артериол, хотя их эффективность при данном заболевании может быть умеренной.
Для уменьшения спазма применяют антагонисты a1-адренорецепторов, например празозин, однако препараты этой группы не обладают избирательностью в отношении спазма и могут вызвать нежелательное падение кровяного давления. Используют также прямо действующие вазодилататоры (например, нитроглицерин и нитраты; см. рис.13.14) и антагонисты Са2+ (например, дилтиазем и нифедипин).
Молекулярный механизм действия дилтиазема и нифедипина заключается в блокировании Са2+-каналов L-типа, и клеточным ответом на это воздействие является уменьшение притока Са2+ и подавление каскада процессов, ведущих к вазоконстрикции (см. ранее «Гипертензия»).
В четырех отдельных клинических исследованиях изучали эффективность применения нифедипина при болезни Рейно. У большинства пациентов было отмечено симптоматическое улучшение. Нифедипин эффективнее празозина, препарат можно принимать перорально до воздействия холода, чтобы избежать приступа. Ингибиторы АПФ и простациклин также можно использовать для лечения болезни Рейно, т.к. они вызывают вазодилатацию.
Варикозное расширение вен[править | править код]
Одним из основных заболеваний периферических сосудов, поражающие вены, является варикозное расширение вен. Вторым из основных заболеваний периферических сосудов является тромбоз вен (включая тромбофлебит), который развивается в результате утраты их эластичности и переполнения кровью. Лечение проводят с помощью инъекций склерозирующих средств или хирургического вмешательства. Для склеротерапии применяют тетрадецилсульфат натрия. Он вызывает воспаление интимы сосудов и образование тромба, обычно закрывающего вену. В результате последующего образования фиброзной ткани вена полностью закрывается и затем пропадает.
Тромбоз вен («красные сгустки»)[править | править код]
Венозные тромбы состоят преимущественно из свернувшейся крови и в меньшей степени из агрегированных тромбоцитов. Поверхностный тромбофлебит представляет собой местное поверхностное воспаление стенки вен с вторичным тромбозом вен. Терапию поверхностного тромбофлебита проводят с помощью НПВС, включая аспирин, поскольку главной мишенью для терапевтического воздействия служит воспалительный процесс.
Гиалуронидазу применяют для улучшения кровотока при поверхностном тромбофлебите
Гиалуронидазу называют ферментом «распространения» или «диффузии», поскольку она повышает проницаемость соединительной ткани, гидролизуя гиалуроновую кислоту. Это временно снижает вязкость клеточного цемента и способствует диффузии введенной жидкости или местных транссудатов и экссудатов.
При тромбозе глубоких вен тромбы образуются обычно в глубоко расположенных венах нижних конечностей. Любое воспаление является вторичным, и здесь необходимо в первую очередь воспрепятствовать образованию тромба, а не лечить вторичное воспаление. Важная последующая задача лечения состоит в том, чтобы предотвратить легочную эмболию, которую могут вызвать венозные тромбы, попадающие в легочный кровоток.
Для профилактики тромбоза вен в течение 1 нед — 3 мес можно применять большие дозы антикоагулянта гепарина (или НМГ, например эноксапарина).
Тромбоз вен и его лечение
- Заболевание периферических вен характеризуется сосудистым воспалением и тромбозом
- Лечение поверхностного тромбофлебита направлено на борьбу с воспалением, для чего используют НПВС
- Лечение и профилактика заболевания глубоко расположенных вен направлены на предупреждение тромбоза
- Средством профилактики тромбоза служат гепарин и варфарин
- Стрептокиназу используют для разрушения образовавшихся тромбов
Гепарин обладает антикоагулянтной активностью, однако его действие кратковременно
Гепарин ингибирует реакции, ведущие к свертыванию крови и образованию фибринового сгустка. В комбинации с антитромбином III он подавляет тромбоз путем инактивации активирующего фактора X и препятствует превращению протромбина в тромбин. Гепарин не разрушает уже образовавшиеся тромбы.
Оральные антикоагулянты, например варфарин, назначают в тех случаях, когда венозный тромб остается локализованным. Варфарин является другим профилактическим препаратом, ингибирующим способность витамина К стимулировать синтез факторов свертывания II, VII, IX и X (см. главу 10). Однако его антикоагулянтный эффект проявляется по меньшей мере через 49-72 час. Гепарин и варфарин могут вызвать ненужное кровотечение, поэтому следует тщательно определить их эффективные дозы, не дающие этого нежелательного эффекта.
Стрептокиназу (или различные формы tPA) используют в лечении тромбов, затем проводят антикоагулянтную профилактику для предупреждения рецидивов
Стрептокиназа взаимодействует с плазминогеном, образуя активирующий комплекс, который превращает плазминоген в плазмин. Плазмин разрушает фибриновые сгустки, а также расщепляет фибриноген и другие белки плазмы.
Ксимелагатран, препарат для лечения венозной тромбоэмболии, проходит клинические исследования
Ксимелагатран применяют перорально как пролекарство мелагатрана. Мелагатран обратимо связывается с тромбином, как связанным с фибрином, так и свободно циркулирующим. После перорального приема ксимелагатран быстро ингибирует активность тромбина, а также замедляет и супрессирует образование тромбина.
Препарат обладает антикоагулянтным, антитромбоцитарным и профибринолитическим эффектами, лишь незначительно удлиняя время капиллярного кровотечения. При пероральном приеме ксимелагатран имеет стабильный и предсказуемый фармакокинетический профиль и низкий потенциал взаимодействия с другими лекарственными средствами. Он экскретируется почками главным образом в виде мелагатрана.
В клинических исследованиях оценивали эффект перорального применения ксимелагатрана в следующих ситуациях: предотвращение венозной тромбоэмболии (включая тромбоз глубоких вен с легочной эмболией или без нее) после заместительной хирургии тазобедренного или коленного суставов; лечение и длительная вторичная профилактика венозной тромбоэмболии; предотвращение инсульта и других системных эмболических процессов, ассоциированных с неклапанной предсердной фибрилляцией; профилактика сердечнососудистых осложнений после ОИМ. Результаты этих исследований показали, что отношение польза-риск при фиксированной дозе в отсутствие мониторинга коагуляции сопоставимо в положительном смысле с аналогичным показателем при использовании современной стандартной терапии, например эноксапарина/варфарина при лечении тромбоза глубоких вен с легочной эмболией или без нее. Однако вследствие повышенного уровня ферментов печени, отмеченного у 9,6% пациентов, получавших лечение ксимелагатраном, необходим регулярный мониторинг.
Ревипарин представляет собой НМГ, используемый для лечения тромбоэмболии
Ревипарин в дозе 1750 ME анти-ХА при п/к введении оказался столь же эффективным, как и не-фракционированный гепарин, в предупреждении тромбоза глубоких вен при хирургических вмешательствах с умеренным риском (как общих, так и на брюшной полости) и существенно снижал частоту тромбоза глубоких вен у пациентов с аппаратной иммобилизацией нижних конечностей.
В суточной дозе 4200 ME анти-Ха ревипарин был таким же эффективным, как нефракционированный гепарин или эноксапарин, при профилактике тромбоза глубоких вен после ортопедических операций высокого риска. То же самое было отмечено при его использовании для предупреждения тромбоза глубоких вен и/или легочной эмболии, а также смертности при ортопедических операциях высокого риска.
У пациентов с острой венозной тромбоэмболией ревипарин был эффективнее, чем нефракционированный гепарин, в снижении частоты тромбозов и по крайней мере столь же эффективным, как и нефракционированный гепарин, в предотвращении клинических рецидивов тромбоза глубоких вен и/или легочной эмболии. Применение ревипарина ассоциировано с подобной или более низкой частотой возникновения кровотечений, как и при использовании нефракционированного гепарина.
Тинзапарин также является ингибитором тромбина. При п/к введении 4500 ME анти-Ха его Т1/2 составляет 3,4 час. Среднее соотношение активности анти-Ха и активности анти-Па равно 2,8; оно выше, чем у нефракционированного гепарина (примерно 1,2). При лечении острого симптоматического тромбоза глубоких вен с легочной эмболией или без нее тинзапарин вводят только п/к, если его применяют вместе с варфарином. Рекомендуемая доза составляет 175 ME анти-Ха на 1 кг массы тела, 1 раз в день, в течение по меньшей мере 6 сут, пока в полной мере не проявится антикоагулянтный эффект варфарина. Лечение варфарином должно быть начато в соответствующий срок (обычно через 1-3 сут после начала применения тинзапарина).
Существуют и другие ингибиторы тромбина, которые применяют в настоящее время, например НМГ данапароид.
Атеротромбоз[править | править код]
Атеротромбоз — это острый тромбоз, возникающий на фоне хронического атеросклероза. Гемодинамические последствия атеротромбоза периферической сосудистой системы не коррелируют достаточно явно со степенью дисфункции (хромота). Факторы, предположительно способствующие развитию данного вида патологии, включают повреждение эндотелия, повышение вязкости крови, поражение мышечных волокон, нарушение ДНК митохондрий мышц и изменение мышечного метаболизма.
Простагландины и ишемия нижних конечностей
Простагландины десятилетиями используют для лечения ишемии нижних конечностей в критических ситуациях, однако проведенные недавно исследования не выявили какой-либо роли этих средств в лечении атеротромботической хромоты.
Пропионил-L-карнитин применяют в терапии атеротромбоза
Накопление ацилкарнитинов, особенно во время физической нагрузки, по-видимому, способствует развитию симптомов и прогрессированию заболевания, и захват кислорода на пике линейно и обратно пропорционально коррелирует с содержанием короткоцепочечного ацилкарнитина в мышцах. Карнитин ингибирует продукцию ацилкарнитина, конкурируя с ацетил-КоА за карнитинпальмитоилтрансферазу. Это снижает содержание ацилкарнитина в мышцах, а также увеличивает количество субстрата (ацетил-КоА) для цикла Кребса. Про-пионил-L-карнитин представляет собой пролекарство для карнитина. При пероральном приеме в дозе 2 г/сут он существенно увеличивает время, в течение которого пациент может ходить, и со временем (на протяжении 6-12 мес) прогрессивно снижает боли в нижних конечностях. Каких-либо побочных эффектов при сравнении с плацебо не отмечено.
Эффект статинов при лечении атеротромбоза исследуют
Было обнаружено, что статины снижают риск развития ишемии и улучшают симптомы хромоты.
Цилостазол в терапии атеротромбоза
Цилостазол является ингибитором ФДЭ-3, который в дозе 100 мг 2 раза в день перорально улучшает состояние пациентов при перемежающейся хромоте. Механизмы его действия окончательно не выяснены. Ингибируя ФДЭ-3, цилостазол и некоторые его метаболиты уменьшают деградацию цАМФ, вследствие чего возрастает его содержание в кровеносных сосудах и тромбоцитах, приводя к вазодилатации и подавлению агрегации тромбоцитов соответственно. По сравнению с плацебо цилостазол в дозе 50 или 100 мг 2 раза в день улучшает способность пациента ходить, причем этот эффект появляется в пределах 2 нед от начала лечения. Побочные эффекты возникают нечасто и включают головную боль, сердцебиение и диарею. Цилостазол интенсивно метаболизируется ферментами системы цитохрома Р-450 печени, в основном ЗА4, метаболиты экскретируются главным образом с мочой. Один из них, 3,4-дегидроцилостазол, по-видимому, обусловливает по меньшей мере 50% фармакологической активности (ингибирование ФДЭ-3). Цилостазол на 95-98% связывается с белками. препарата и его метаболитов составляет около 11-13 час. Цилостазол противопоказан пациентам с ЗСН любой степени тяжести (ингибиторы ФДЭ-3, например веснаринон, повышают вероятность летального исхода у пациентов с ЗСН).
ИНФЕКЦИИ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ[править | править код]
Общие принципы лечения инфекций описаны в главе 6. Здесь основное внимание уделено аспектам лечения инфекций, относящимся к сердечнососудистой системе.
Инфекционный эндокардит[править | править код]
Это заболевание поражает эндокард или сосудистый эндотелий и представляет собой наиболее распространенную инфекцию сердечно-сосудистой системы. Чаще всего ее возникновение связано с употреблением наркотиков, а также с недостаточностью сердечных клапанов. Иногда заболевание принимает форму острой инфекции, однако чаще протекает незаметно, как подострый бактериальный эндокардит (рис. 13.43).
Инфекционный эндокардит в Великобритании и США встречается редко (6-7 случаев на 100 000 населения), но распространен в развивающихся странах. Обычно мишенью для инфекции являются сердечные клапаны, измененные под влиянием ревматического заболевания или имеющие врожденные дефекты, а также пролабированный митральный клапан и аортальный клапан при кальцифицирующем его заболевании. Однако могут быть поражены и нормальные клапаны, особенно после инъекции нестерильных лекарственных средств. Возбудителями инфекционного эндокардита могут быть практически любые микроорганизмы, включая грибы, риккетсии и хламидии. В большинстве случаев обнаруживают широко распространенные микроорганизмы Streptococcus viridans, Streptococcus faecalis и Staphylococcus aureus.
Лечение инфекционного эндокардита[править | править код]
Если возбудителями заболевания служат S. viridans или S. faecalis, для лечения используют пенициллин G и гентамицин. В случае S. aureus применяют флоксациллин и либо фузидовую кислоту, либо гентамицин. Инфекционный эндокардит может развиться после стоматологических операций в результате попадания бактерий из полости рта в кровоток. Чтобы предотвратить эту опасность, используют профилактическое введение пенициллина за 7 сут до операции.
Инфекционный миокардит (в том числе болезнь Чагаса)[править | править код]
Это заболевание представляет собой воспаление сердечной мышцы, характеризующееся лихорадкой и сердечной недостаточностью. Возбудителями являются вирусы, бактерии или паразиты. Вслед за лейкоцитарной инфильтрацией миокарда могут возникнуть неишемический некроз или дегенера
ция миоцитов. Предполагают, что большинство случаев вирусного миокардита вызывают энтеровирусы (Коксаки, гриппа, краснухи, полиомиелита, аденовирусы, эховирусы), которые с трудом поддаются лекарственной терапии. Однако миокардит могут вызвать и бактериальные инфекции (экзотоксины, продуцируемые Corynebacterium, Rickettsia, Chlamydia, Coxiella) и простейшие (Trypanosoma cruzi, Toxoplasma gondii).
Болезнь Чагаса (американский трипаносомоз) вызывает внутриклеточный паразит Т. cruzi. Возникающий миокардит является наиболее частой причиной сердечной недостаточности в Бразилии и соседних странах. Паразит передается различными кровососущими клопами семейства Triatominidae. Вслед за повреждением в месте укуса возникают паразитемия и лихорадка. Поражение сердца вызывают токсины, высвобождаемые паразитом, а также воспалительные клетки.
Существует две клинически различающиеся формы заболевания:
- острая форма — поражает главным образом детей и в большинстве случаев имеет слабые клинические проявления. Повреждение сердца возникает в результате прямой инвазии клеток миокарда паразитом и последующих воспалительных изменений;
- хроническая форма — характеризуется повреждением сердечной мышцы в результате аутоиммунной реакции, индуцированной Т. cruzi и опосредованной цитотоксическими Т-клетками.
80% пациентов с острой формой заболевания и несколько больше с хронической формой удается вылечить.
Нифуртимокс представляет собой препарат выбора для лечения острой формы болезни Чагаса
Нифуртимокс обладает трипаноцидным действием за счет образования свободных радикалов, которые реагируют с молекулярным кислородом, образуя анионы супероксида, пероксид водорода и гидроксильные свободные радикалы.
Трипаносомы чувствительны к этим реакционноспособным метаболитам (вызывающим перекисное окисление липидов и ДНК), поскольку у них отсутствуют каталаза и глутатионпероксидаза, инактивирующие эти токсическое продукты.
Примахин устраняет тканевую инфекцию и предотвращает развитие паразита в крови (эритроцитарных форм). Бензнидазол, другой препарат, эффективен против Т. cruzi, резистентных к нифуртимоксу.
Побочные эффекты бензнидазола и нифуртимокса включают желудочно-кишечные расстройства и сыпь. Нифуртимокс высокотоксичен для клеток человека, однако обладает некоторой избирательностью, поскольку скорость образования радикалов гораздо ниже в клетках человека по сравнению с трипаносомами. Нифуртимокс может также вызывать анорексию, тремор, парестезию, полиневрит и преходящую лейкопению. Побочные эффекты примахина относятся преимущественно к желудочно-кишечному тракту.
Инфекционный перикардит[править | править код]
Перикардит — это воспаление перикарда, покрывающего поверхность эпикарда сердца. Воспаление перикарда обычно носит вторичный характер по отношению к различным заболеваниям сердца, системным расстройствам или метастазам опухолей, возникающим в отдаленных местах организма. Заболевание имеет множественную этиологию, но чаще всего причиной служит вирус Коксаки.
Для лечения симптомов инфекционного перикардита используют НПВС перорально — аспирин, напроксен или индаметацин. Однако если перикардит тяжелый или рецидивирующий, необходима системная терапия глюкокортикостероидами.
Болезнь Кавасаки[править | править код]
Это генерализованный васкулит, вызывающий обширное поражение сосудов сердца с возможным летальным исходом. Этиология болезни неизвестна, но имеющиеся данные позволяют полагать, что это не аутоиммунное, а индуцированное заболевание предположительно вирусом. В течение острой фазы болезнь Кавасаки характеризуется артериитом средних и крупных сосудов, артериальными аневризмами, вальвулитом и миокардитом. Особое значение имеют аневризмы коронарных артерий, которые могут стать причиной тромбоза или разрыва. При этом заболевании очевидна активация лимфоцитов и макрофагов.
Экспериментальные исследования показали присутствие антител, способных вызывать гибель эндотелиальных клеток, предварительно обработанных интерлейкином-1 или фактором некроза опухолей. Функция этих антител при данном заболевании неясна: они могут служить либо просто маркерами заболевания, либо иметь патогенетическое значение.
Лечение болезни Кавасаки[править | править код]
Пациентов с болезнью Кавасаки можно классифицировать на 5 уровней по относительному риску ишемии миокарда. До уровня 3 терапия не показана. При уровне 3 имеют место одиночные, от малой до средней величины, аневризмы коронарной артерии, в этом случае назначают аспирин. Уровень 4 характеризуется присутствием одной (или нескольких) крупной артериальной аневризмы или множественных аневризм, от мелких до средних, без обструкции. Для лечения используют только аспирин или аспирин с добавлением варфарина. Пациенты с наивысшим риском возникновения инфаркта миокарда имеют признаки обструкции коронарной артерии. Этих пациентов относят к уровню 5 и лечат аспирином (с варфарином или без него), а также антагонистами Са2+ для уменьшения потребности миокарда в кислороде.
В проведенных недавно исследованиях установлено, что в/в введение гамма-глобулина до 10 сут от начала болезни снижает заболеваемость и частоту возникновения поражений коронарных артерий. Гамма-глобулин содержит антитела к различным вирусам. Антитела направлены против оболочки вирусов и способны нейтрализовать некоторые из них, предотвращая их связывание с клетками организма-хозяина.
Ревматическая лихорадка[править | править код]
Ревматическая лихорадка представляет собой воспалительное заболевание, возникающее у детей и взрослых молодых людей и оставляющее длительные последствия. Заболевание наиболее распространено в странах Среднего Востока, Дальнего Востока и Восточной Европы. Оно возникает у небольшой части лиц (имеющих высокий уровень антител к стрептококкам) через несколько недель после фарингеальной инфекции, вызванной стрептококками группы А. На этой стадии определяют аутоантитела к антигенам сердца (рис. 13.44).
Установлено, что углеводные антигены стрептококков перекрестно реагируют с антигенами клапанов сердца и миокарда. В связи с этим предполагают, что ревматическая лихорадка возникает как результат аномальной клеточной и гуморальной реакции иммунной системы организма, индуцированной стрептококками группы А. Возможно, что такая реакция на стрептококки обусловлена генетическими особенностями иммунной системы индивида.
Лечение ревматической лихорадки[править | править код]
Лечение направлено на устранение инфекции и ее эффектов
Прежде всего необходимо избавиться от остаточной стрептококковой инфекции. С этой целью применяют однократную в/м инъекцию бензатинпенициллина или феноксиметилпенициллин перорально 4 раза в день в течение 1 нед. Высокие дозы салицилатов ингибируют активность ЦОГ. Назначают предельно переносимые дозы, выше которых у пациентов появляется звон в ушах. Если присутствует кардит, применяют системное лечение глюкокортикостероидами. Рецидивы — обычное явление при наличии персистирующих повреждений сердца. Их предотвращают постоянным ежедневным применением феноксиметилпенициллина (перорально) или ежемесячными инъекциями бензатин-пенициллина до возраста 20 лет или в течение 5 лет после последнего рецидива.
Рис. 13.44 Патогенетические последствия и основные морфологические признаки острого ревматического заболевания сердца. Острая ревматическая лихорадка часто вызывает митральный вальвулит, характеризующийся линейным расположением вегетаций вдоль линии смыкания створок клапанов.
Читайте также[править | править код]
- Неотложные состояния
- Синдром спортивного сердца
- Физиологическая гипертрофия миокарда
- Патологическая гипертрофия миокарда
- Острое и хроническое перенапряжение сердца
- Спортивное сердце (лечение)
- Сердечно-сосудистая система и спорт
- Сердечно-сосудистая система
- Лечение сердечных заболеваний спортсменов
- Хроническая сердечная недостаточность
- Гипотония (пониженное артериальное давление)
Литература[править | править код]
- Ashrafian Н, Violaris AG. Beta-blocker therapy of cardiovascular diseases in patients with bronchial asthma or COPD: The pro viewpoint. Pri Care Resp J 2005; 14: 236-241.
- ASSENT-2 Investigators. Single-bolus tenecteplase compared with front-loaded alteplase in AMI: the ASSENT-2 double-blind randomised trial. Lancet 1999; 354: 716-722.
- Baguet J-P, Robitail S, Boyer L, Debensason D, Auquier P. A meta-analytical approach to the efficacy of antihypertensive drugs in reducing blood pressure. Am J Cardiovasc Drugs 2005; 5: 131-140.
- Blasi F, Tarsia P, Cosentini R, Valenti V. Newer antibiotics for the treatment of respiratory tract infections. Curr Opin Pulm Med 2004; 10: 189-196.
- Braunwald E, Antman EM, Beasley JW et al. ACC/AHA guideline update for the management of patients with unstable angina and non-ST-segment elevation myocardial infarction-2002: summary article: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on the Management of Patients With Unstable Angina). Circulation 2002; 106:1893-1900.
- Brown NJ. Eplerenone. Circulation 2003; 107: 2512-2518.
- Chieffo A, Stankovic G, Bonizzoni E et al. Early and mid-term results of drug-eluting stent implantation in unprotected left main. Circulation 2005; 111: 791-795.
- Cleophas TJ, Zwinderman AH. Beta-blockers and heart failure: meta-analysis of mortality trials. Int J Clin Pharm Ther 2001; 39: 383-388. [An appraisal of the topic.]
- Chobain AV, Bakris GL, Black HR et al. Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. The Seventh Report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. JAMA 2003; 289: 2560-2572.
- Connolly SJ. Meta-analysis of antiarrhythmic drug trials. The American Journal of Cardiology 1999; 84(Suppl 1): 90-93.
- Domanski MJ et al. Effect of angiotensin converting enzyme inhibition on sudden cardiac death in patients following AMI. A meta-analysis of randomized clinical trials. J Am Coll Cardiol 1999; 33: 598.
- Eikelboom JW, Quinlan DJ, Mehta SR et al. Unfractionated and low-molecular-weight heparin as adjuncts to thrombolysis in aspirin-treated patients with ST-elevation acute myocardial Infarction: a meta-analysis of the randomized trials. Circulation 2005; 112: 3855-3867.
- Fiessinger JN, Huisman MV, Davidson BL et al. THRIVE Treatment Study Investigators. Ximelagatran vs low-molecular-weight heparin and warfarin for the treatment of deep vein thrombosis: a randomized trial. JAMA 2005; 293: 736-739.
- Freedman JE. Molecular regulation of platelet-dependent thrombosis. Circulation 2005; 1 12: 2725-2734. [Biology of current and future putative drug targets.]
- Caziano ТА. Cardiovascular disease in the developing world and its cost-effective management. Circulation 2005; 112: 3547-3553.
- Cluckman TJ, Sachdev M, Schulman SP, Blumenthal RS. A simplified approach to the management of non-ST-segment elevation acute coronary syndromes. JAMA 2005; 293: 349-357.
- Goldschmidt-Clermont PJ, Creager MA, Lorsordo DW, et al. Atherosclerosis 2005: Recent Discoveries and Novel Hypotheses. Circulation 2005 1 12: 3348-3353
- Healey JS, Baranchuk A, Crystal E et al. Prevention of atrial fibrillation With angiotensin-converting enzyme inhibitors and angiotensin receptor blockers: a meta-analysis. J Am Coll Cardiol 2005; 45: 1832-1839.
- Heidenreich PA et al. Meta-analysis of trials comparing beta-blockers, Ca2+ antagonists, and nitrates for stable angina. JAMA 1999; 281: 1927.
- Hiatt WR. Treatment of disability in peripheral arterial disease: new drugs. Current drug Targets. Cardiovasc Hematolog Disord 2004; 4: 227-231.
- Jabbour S, Young-Xu Y, Craboys ТВ et al. Long-term outcomes of optimized medical management of outpatients with stable coronary artery disease. Am J Cardiol 2004; 93: 294-299.
- La Rosa JC et al. Effect of statins on risk of coronary disease: a meta-analysis of randomized controlled trials. JAMA 1999; 282: 2340.
- Lawes CMM, Bennett DA, Feigin VL, Rodgers A. Blood pressure and stroke: an overview of published reviews. Stroke 2004; 35: 1024.
- LoscalzoJ. Clinical trials in cardiovascular medicine in an era of marginal benefit, bias, and hyperbole. Circulation 2005;112: 3026-3029. [An opinion on how to assimilate cardiovascular clinical trial data.]
- Martino E, Bartalena L, Bogazzi F, Braverman LE. The effects of amiodarone on the thyroid. Endocrine Rev 2001; 22: 240-254.
- Mebazaa A, Barraud D, Welschbillig S. Randomized clinical trials with levosimendan. Am J Cardiol 2005; 96(Suppl 1): 74-79 [Update on an emerging drug.]
- Patrono С, Garcia Rodriguez LA, Landolfi R, Baigent C. Drug therapy: low-dose aspirin for the prevention of atherothrom-bosis. N Engl J Med 2005; 353: 2373-2383.
- Peng H, Carretero OA, Vuljaj N et al. Angiotensin-converting enzyme inhibitors: a new mechanism of action. Circulation 2005; 1 12: 2436-2445. [An animal study that reveals a possible new explanation for some of the long term benefit with this class of drug on the heart in hypertensive patients.]
- Pitt B, White H, Nicolau J et al. Eplerenone reduces mortality 30 days after randomization following acute myocardial infarction in patients with left ventricular systolic dysfunction and heart failure. J Am Coll Cardiol 2005; 46: 425-431.
- Prandoni P. Emerging strategies for treatment of venous thromboembolism. Expert Opin Emerg Drugs 2005; 10: 87-94.
- Roccaforte R, Demers C, Baldassarre F, Teo KK, Yusuf S. Effectiveness of comprehensive disease management programmes in improving clinical outcomes in heart failure patients. A meta-analysis. Eur J Heart Failure 2005; 7: 11 33— 1144.
- Silber S. When are drug-eluting stents effective? A critical analysis of the presently available data. Z Kardiol 2004; 93: 649-663.
- Taylor AL, Wright JT Jr, Cooper RS, Psaty BM. Importance of race/ethnicity in clinical trials: lessons from the African-American Heart Failure Trial (A-HeFT), the African-American Study of Kidney Disease and Hypertension (AASK), and the Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). Circulation 2005; 112: 3654-3666.
- Teerlink JR. Overview of randomized clinical trials in acute heart failure syndromes. Am J Cardiol 2005; 96(Suppl 1): 59-67.
- Williams B. Recent hypertension trials: implications and controversies. J Am Coll Cardiol 2005; 45: 813-827.
- Yan AT, Yan RT, Liu PP. Narrative review: pharmacotherapy for chronic heart failure: evidence from recent clinical trials. Ann Intern Med 2005; 142: 132-145.
- YusufS, Mehta SR, Xie С et al; CREATE Trial Group Investigators. Effects of reviparin, a low-molecular-weight heparin, on mortality, reinfarction, and strokes in patients with AMI presenting with ST-segment elevation. JAMA 2005; 293: 427-435.