Антибактериальные средства
Источник: «Наглядная фармакология».
Автор: X. Люльман. Пер. с нем. Изд.: М.: Мир, 2008 г.
Содержание
Антибактериальные средства
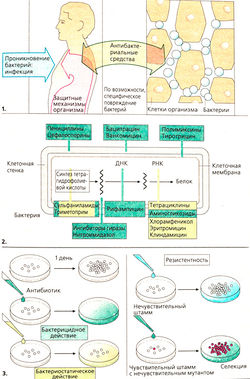
В результате проникновения бактерий через кожные или слизистые барьеры может возникнуть бактериальное инфекционное заболевание. Чаще всего иммунная система организма справляется с возбудителем, и заболевание не развивается. Некоторые микроорганизмы, однако, выработали тонкую стратегию «борьбы» с лекарством. Эти возбудители попадают в клетки хозяина в результате фагоцитоза. Дальнейшее слияние фагосом и лизосом предотвращается, а, следовательно, невозможен распад бактериальных клеток. В подобной вакуоле, стенка которой проницаема для необходимых возбудителю питательных веществ (аминокислоты, сахара), микроорганизмы размножаются, пока клетка не погибнет; вышедшие из клетки бактерии проникают в другую клетку — нового хозяина. Такую стратегию применяют хламидии, туберкулезные микобактерии, Legionella pneumophila, Toxoplasma gondii, представители родов Salmonella и Leishmania. Терапия одним препаратом в этих случаях малоэффективна, так как лекарство сначала должно проникнуть в клетку хозяина, а затем через мембрану вакуоли, где находятся бактерии. Если бактерии размножаются быстро и защитные силы организма не справляются с инфекцией, то инфекционное заболевание проявляется в виде воспаления, например, раневая инфекция или инфекция мочевыводящих путей. Для лечения применяются вещества, уничтожающие бактерий или препятствующие их размножению и при этом не затрагивающие собственные клетки организма (1).
Специфическое повреждение клеток бактерий возможно в том случае, если лекарственное вещество вовлекается в обменные процессы, характерные только для микроорганизмов. Специфическое действие оказывают вещества, блокирующие синтез клеточной стенки бактерий, так как клетки человека не имеют клеточной стенки. Направления действия антибактериальных препаратов представлены на схеме (2).
Полимиксины и тиротрицин не описываются в данной книге, так как из-за плохой переносимости они применяются только местно.
Действие антибиотиков можно продемонстрировать in vitro (3), когда бактерии размножаются в определенной питательной среде. На среде с антибактериальным веществом можно наблюдать два эффекта:
1) бактерицидный -— гибель бактерий;
2) бактериостатический — бактерии выживают, но прекращают размножаться. Все препараты классифицируются в соответствии с основным лечебным эффектом (разные цвета на рис. 2), несмотря на то что в зависимости от условий применения могут наблюдаться некоторые различия в их действии.
Если антибактериальная терапия неэффективна, то говорят о резистентности бактерий. Причиной резистентности могут быть особенности метаболизма бактерий, благодаря которым они становятся нечувствительными к действию антибиотика (естественная резистентность). Антибиотик может быть эффективным лишь против нескольких видов бактерий — антибиотик узкого спектра действия (например, пенициллин G) или очень многих видов — антибиотик широкого спектра действия (например, тетрациклины). Первоначально чувствительные к антибиотикам бактерии могут мутировать под влиянием препарата, превращаясь в нечувствительные штаммы (приобретенная резистентность), в результате чего бактерии со случайными мутациями выживают и продолжают размножаться, тогда как обычные штаммы погибают. Чем чаще назначается определенный препарат, тем больше вероятность развития резистентности к нему (например, множественная резистентность к возбудителям больничных инфекций).
Резистентность может также передаваться при участии плазмид (плазмидная резистентность), при этом ДНК, ответственная за устойчивость к антибиотику, передается от одной бактерии к другой путем конъюгации или трансдукции.
Ингибиторы синтеза клеточной стенки
Большинство клеток бактерий окружены клеточной стенкой, которая, как плотная капсула, защищает их от внешних воздействий и высокого внешнего осмотического давления. Прочность клеточной стенки обусловлена наличием мурей н-пептидо-гликанового остова — большой макромолекулы с сетчатой структурой. Мономерные звенья этой макромолекулы состоят из аминосахара N-ацетил глюкозамина и N-ацетилмурамовой кислоты, содержащей пептидную цепь. Эти вещества синтезируются бактерией и транспортируются через клеточную мембрану наружу. Фермент транспептидаза связывает пептидные цепи двух соседних аминосахаров.
Ингибиторы синтеза клеточной стенки действуют только на бактерии, так как клетки человеческого организма не имеют клеточной стенки. Эти препараты обладают бактерицидной активностью в отношении растущих и размножающихся микроорганизмов. Таков механизм действия бета-лактамных антибиотиков — пенициллинов и цефалоспоринов, а также бацитрацина и ванкомицина.
Пенициллины
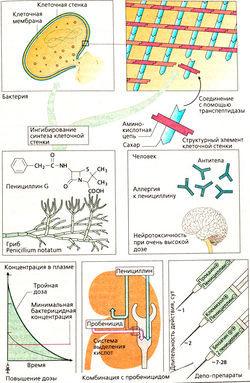
Родоначальник этой группы антибиотиков — пенициллин G (бензилпенициллин). Его получают из культур плесневых грибов (первоначально — из Penicillium notatum). Структурной основой пенициллина G, как и других пенициллинов, является 6-аминопенициллиновая кислота (6-АПК) с четырехчленным β-лактамным кольцом. Сама 6-АПК не обладает антибактериальным действием. Пенициллины препятствуют синтезу клеточной стенки путем ингибирования транспептидазы. Если бактерии находятся в фазе роста или размножения, то пенициллины вызывают их гибель (бактерицидное действие): при дефекте клеточной стенки целостность бактерий нарушается.
Препараты пенициллинов очень хорошо переносятся. Суточная доза пенициллина G составляет от 0,6 г в/м (106 ЕД) до 60 г инфузионно. Основным побочным эффектом пенициллина является аллергическая реакция (возникает в 5% случаев), проявляющаяся в разных формах — от кожных высыпаний до анафилактического шока (менее 0,05%). При аллергии на пенициллин введение препаратов этой группы противопоказано. Из-за возможной аллергической реакции их также не применяют местно. Нейротоксическое действие, проявляющееся чаще всего в виде судорог, встречается при применении особенно высоких концентраций, быстром внутривенном введении больших доз или при прямом введении в ликвор.
Пенициллин G выводится почками очень быстро (Т1/2 из плазмы 30 мин) в неизмененной форме.
Увеличение продолжительности действия достигается несколькими путями.
- Введение в повышенной дозе: при одинаковом периоде полувыведения t1/2 концентрация препарата, превышающая минимально эффективную, сохраняется более длительное время.
- Комбинация с пробеницидом: выведение пенициллина почками осуществляется при помощи анионообменной (кислотной) системы секреции в проксимальных канальцах (СООН-группа 6-АПК). Кислота пробеницид конкурирует на этом пути с пенициллином и задерживает его выведение.
- Внутримышечное введение в виде депо-препарата: пенициллин G в анионной форме (—СОО") образует малорастворимые соли с веществами, содержащими положительно заряженные аминогруппы (прокаин, антигистаминное средство клемизол, двухзарядный катион бензатина). Из различных депо-препаратов пенициллин высвобождается за разное время.
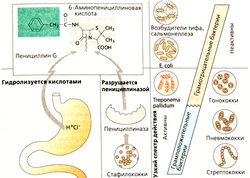
Пенициллин G очень хорошо переносится, однако недостатки (А) ограничивают его терапевтическое применение.
- Поскольку желудочный сок расщепляет β-лактамное кольцо, инактивируя пенициллин, его вводят только инъекционно.
- β-Лактамное кольцо расщепляется также бактериальными ферментами (β-лактамазами). Так, пенициллиназа, продуцируемая в основном стафилококками, расщепляет пенициллин и вызывает развитие резистентности к антибиотику.
- Узкий антибактериальный спектр действия: он эффективен против многих грамположительных бактерий, грамотрицательных кокков, возбудителя сифилиса, однако не в отношении многих других грамотрицательных бактерий.
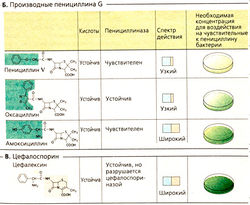
Производные пенициллина с заместителями в 6-аминопенициллиновой кислоте имеют следующие преимущества (Б).
- Кислотоустойчивость позволяет принимать препараты перорально (при возможности их всасывания в кишечнике). Производные, представленные на рисунке, назначают перорально. Пенициллин /(феноксиметилпенициллин) имеет такие же антибактериальные свойства, как пенициллин G.
- Устойчивые к пенициллиназе изоксазолил-пенициллины (оксациллин, диклоксациллин, флуклоксациллин) применяют перорально при инфекциях, вызванных стафилококками, продуцирующими пенициллиназу.
- Расширенный спектр действия. Амино-пенициллин амоксициллин влияет на многие грамотрицательные бактерии, например колиформы, тифозную сальмонеллу. Для защиты от разрушения пенициллиназой препарат комбинируют с ингибитором пенициллиназы (клавулановая кислота, сульбакгам, тазобактам).
Близкий по структуре ампициллин (не имеет 4-гидроксигруппы) проявляет схожий спектр действия, однако плохо всасывается (< 50%), нарушает развитие флоры кишечника (вызывает диарею) и должен вводиться инъекционно.
Широким спектром действия (активны против псевдомонад) обладают карбоксипеницилпин (тикарциллин) и аципаминопенициллин (мезлоциллин, азлоциллин, пипера-циллин), однако они разрушаются кислотой и пенициллиназой.
Цефалоспорины — β-лактамные антибиотики; продуцируются грибами; бактерицидное действие основано на ингибировании транспептидазы. На рисунке изображен цефалексин (серым цветом выделена 7-аминоцефалоспориновая кислота, входящая в состав всех цефалоспоринов). Цефалоспорины кислотоустойчивы, однако многие из них плохо всасываются. Поэтому большинство препаратов применяют парентерально в стационаре. Цефалексин принимают перорально. Цефалоспорины устойчивы к действию пенициллиназы, однако существуют бактерии, продуцирующие цефалоспориназы. Некоторые производные устойчивы и к этой β-лактамазе. Цефалоспорины имеют широкий спектр действия. Новые производные (цефатоксим, цефменоксим, цефтриаксон, цефтазидим) эффективны против тех возбудителей, которые резистентны к действию многих антибактериальных препаратов. Цефалоспорины чаще всего хорошо переносятся. Однако все эти препараты могут вызывать аллергические реакции. Некоторые нефротоксичны, несовместимы с алкоголем, могут провоцировать кровотечения (антагонизм с витамином К).
Другие препараты, нарушающие синтез клеточной стенки. Антибиотики бацитрацин и ванкомицин влияют на мембранный транспорт веществ, необходимых для построения клеточной стенки. Они воздействуют только на грамположительные бактерии. Бацитрацин представляет собой смесь полипептидов, очень нефротоксичен и применяется только местно. Гликопептид ванкомицин (применяется перорально) является средством выбора для лечения кишечной инфекции, возникающей в результате антибактериальной терапии (псевдомембранозный энтероколит, возбудитель Clostridium difficile). Препарат не всасывается в кишечнике. Ванкомицин может применяться для лечения инфекции, вызванной грамположительными кокками, устойчивыми к действию других, лучше переносимых препаратов. Среди побочных эффектов — возможная потеря слуха.
Ингибиторы синтеза тетрагидрофолиевой кислоты
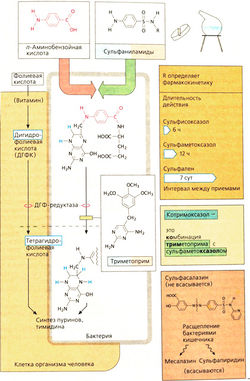
Тетрагидрофолиевая кислота (ТГФК) играет роль кофермента в синтезе пуриновых оснований и тимидина. Эти соединения в свою очередь являются структурными элементами для построения ДНК и РНК. При недостатке ТГФК тормозится клеточное деление. ТГФК образуется из дигидрофолиевой кислоты (ДГФК); эта реакция катализируется дигидрофолатредуктазой. Структурной основой ДГФК является фолиевая кислота, которая не может синтезироваться в организме человека, а поступает с пищей как витамин. Большинство бактерий не нуждаются в фолиевой кислоте, поскольку они могут синтезировать ее самостоятельно. Нарушение синтеза ТГФК в клетках бактерий достигается с помощью сульфаниламидов и три-метоприма.
Сульфаниламиды имеют структурное сходство с пара-аминобензойной кислотой (ПАБК) — одним из соединений, необходимых для синтеза ДГФК бактериями. Сульфаниламиды, являясь аномальными субстратами, конкурируют с ПАБК и таким образом тормозят синтез ДГФК. Поскольку большинство бактерий не могут получать фолиевую кислоту извне, происходит их обеднение ДГФК. Сульфаниламиды действуют бактериостатически на широкий спектр микроорганизмов. Сульфаниламиды — синтетические препараты; их общая структурная формула представлена на рис. А.
Фармакокинетическое поведение действующего вещества определяет остаток R. Большинство сульфаниламидов всасывается при пероральном приеме, частично метаболизируется и выводится почками. Скорость выведения и продолжительность действия могут значительно различаться. Побочные эффекты: аллергические реакции, иногда с тяжелыми поражениями кожи, вытеснение других препаратов из комплексов с белками плазмы или вытеснение непрямого билирубина у новорожденных (опасность желтухи, противопоказаны женщинам на поздних сроках беременности и новорожденным). В настоящее время сульфаниламиды применяются довольно редко из-за большой вероятности развития резистентности. Эти препараты были первыми химиотерапевтическими средствами (применяются с 1935 г.).
Триметоприм ингибирует дигидрофолатредуктазу бактерий. Человеческий фермент более устойчив к действию препарата. Однако иногда в результате приема три-метоприма наблюдается угнетение костного мозга. Триметоприм (2,4-диаминопири-дин) является химиотерапевтическим препаратом с бактериостатическим действием по отношению к широкому спектру микроорганизмов. Чаще всего используется в составе котримоксазола.
Котримоксазол — комбинированный препарат, состоящий из триметоприма и сульфаниламида сульфаметоксазола. Препарат последовательно воздействует на две ступени синтеза ТГФК и поэтому более эффективен, чем оба лекарства по отдельности: реже возникает устойчивость, может проявляться бактерицидное действие. Побочные эффекты такие же, как у каждого препарата в отдельности.
Сульфасалазин (салазосульфапири-дин) -^средство для лечения язвенного колита и болезни Крона. Бактерии кишечника расщепляют препарат с образованием сульфаниламида сульфапиридина и месалазина (5-аминосапициловой кислоты). Последняя в больших концентрациях, возможно, обладает противовоспалительным действием (ингибирование синтеза лейкот-риенов?) Сульфасалазин всасывается только после расщепления в нижних отделах кишечника и может вызывать побочные эффекты, типичные для сульфаниламидов (см. выше). Препараты месалазина высвобождаются на протяжении длительного времени и позволяют избежать использования сульфаниламидов.
Сульфасалазин ранее применялся для лечения ревматоидного артрита.
Ингибиторы синтеза ДНК
Дезоксирибонуклеиновая кислота (ДНК) служит матрицей для синтеза нуклеиновых кислот. Рибонуклеиновая кислота (РНК) необходима для синтеза белков и роста клетки. Синтез ДНК предшествует клеточному делению. Вещества, блокирующие считывание информации с матрицы ДНК, нарушают клеточный метаболизм. Описанные ниже препараты применяются в качестве антибактериальных средств, поскольку они не повреждают клетки человека.
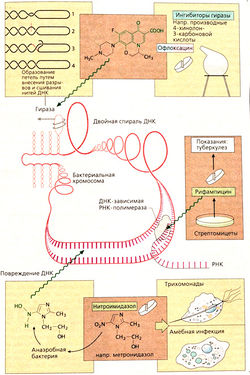
Ингибиторы гиразы. Фермент гираза (топоизомераза II) осуществляет упорядоченную укладку бактериальной хромосомы, длина которой составляет около 1000 мкм; размер самой бактериальной клетки всего лишь 1 мкм. Хромосома представляет собой двойную скрученную спираль ДНК. Нити хромосом образуют петли, длина которых уменьшается в результате скручивания. Гираза закручивает петли путем внесения разрывов и сшивания концов без вращения всей нити.
Ингибиторами бактериальной гиразы являются производные 4-хинолон-З-карбоновой кислоты (в молекуле офлоксацина структура этой кислоты выделена зеленым цветом). Эти соединения препятствуют сшиванию нитей ДНК и тем самым оказывают бактерицидное действие. Препараты всасываются при пероральном приеме. Один из первых препаратов этой группы палидиксовая кислота влияет только на грамотрицательные бактерии и достигает терапевтической концентрации только в моче; используется для лечения инфекций мочевыводящих путей. Норфлоксацин имеет широкий спектр действия. Офлоксацин, ципрофлоксацин, эноксацин и другие препараты этой группы применяются при инфекциях внутренних органов.
Побочными действиями, помимо нарушений работы желудочно-кишечного тракта и аллергических реакций, часто являются поражения ЦНС (например, спутанность сознания, замешательство, галлюцинации, судороги). Препараты противопоказаны при беременности, кормлении грудью и в период роста, так как повреждают хондроциты эпифизов и хрящевую ткань. Возможны разрывы сухожилий, особенно у пожилых или принимающих глюкокортикоиды пациентов. Кроме того, препараты гепатотоксичны, удлиняют интервал QT, способствуя развитию аритмий.
Производные нитроимидазола, например метронидазол, повреждают ДНК, образуя комплексы или вызывая разрывы цепи. У облигатных анаэробов, т. е. бактерий, растущих в бескислородной среде, происходит образование реакционноспособных метаболитов (как изображенный на рис. А гидроксиламин), повреждающих ДНК. Препараты оказывают бактерицидное действие. По схожему механизму они убивают простейших Trichonomas vaginalis (возбудитель инфекции мочеполовых путей) и Entamoeba histolytica (возбудитель заболевания толстой кишки — амебной дизентерии — и абсцессов печени). Метронидазол хорошо всасывается в желудочно-кишечном тракте, а также применяется внутривенно и местно (вагинально). Возможно, он обладает тератогенным действием, поэтому противопоказан при беременности и кормлении грудью. Метронидазол не следует применять более десяти дней. Тинидазол эквивалентен по действию метронидазолу.
Рифампицин ингибирует фермент, осуществляющий транскрипцию в бактериях. Действует бактерицидно на грамположительные и грамотрицательные бактерии, а также на микобактерий (туберкулез, проказа). Препарат применяют только для лечения туберкулеза и проказы, что связано с высоким риском развития резистентности при частом применении.
Противопоказан в первом триместре беременности и в период кормления грудью.
Рифубутин схож с рифампицином, эффективен при устойчивости к рифампицину.
Ингибиторы синтеза белка
Белковый синтез представляет собой перевод (трансляцию) наследственной информации с мРНК в белковую цепь. Связывание аминокислот (АК) в белковую цепь происходит на рибосомах. Доставку АК к мРНК осуществляют транспортные молекулы тРНК. К определенной тРНК подходят только соответствующие участки мРНК (кодоны, состоящие из трех нуклеотидных остатков).
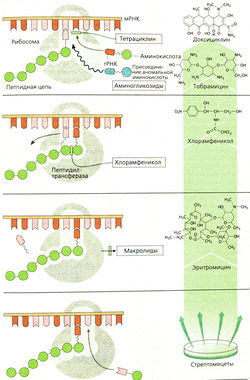
Включение АК в пептидную цепь обычно состоит из следующих этапов (А):
- Рибосома фиксирует два соседних кодона мРНК. Один из них (левый) содержит уже связанный комплекс тРНК-АК, а АК является частью пептидной цепи. Другой кодон (правый) готов для присоединения следующего комплекса тРНК-АК.
- После его присоединения происходит связывание аминокислот соседних комплексов тРНК-АК. Это осуществляет фермент пептидилтрансфераза, которая отщепляет АК от тРНК в первом комплексе.
- Освободившаяся тРНК отходит от мРНК. Рибосома может двигаться по мРНК к следующему кодону.
- Правый комплекс тРНК-АК сдвигается влево, а справа может присоединяться следующий комплекс.
Отдельные этапы этого процесса можно заблокировать различными антибиотиками. Некоторые из антибиотиков первоначально были выделены из представителей стрептомицетов, отдельные аминогликозиды — из микромоноспоровых бактерий.
1. а) Тетрациклины ингибируют присоединение к рибосоме тРНК-АК-комплекса и обладают бактериостатическим действием, направленным на широкий спектр микроорганизмов.
б) Аминогликозиды вызывают присоединение неподходящего тРНК-АК-комплекса, что приводит к синтезу аномального белка. Обладают бактерицидным действием, в основном направленным на грамотрицательные бактерии. Стрептомицин и канамицин используют преимущественно для лечения туберкулеза. Окончание “mycin” в названии препарата происходит от вида стрептомицетов (Streptomyces), а окончание “micin” имеют антибиотики, происходящие из других видов микроорганизмов, например, гентамицин (gentamicin) из Micromonospora.
2. Хлорамфеникол ингибирует пептидил-трансферазу. Имеет широкий спектр бактериостатического действия. В настоящее время его получают химическим синтезом; молекула имеет простую структуру.
3. Макролиды препятствуют продвижению рибосомы. Оказывают преимущественно бактериостатическое действие, в основном на грамположительные возбудители. Воздействуют и на внутриклеточные микроорганизмы, такие как хламидии и микоплазмы. Макролиды применяются перорально. Главным представителем группы является эритромицин. Он хорошо переносится. Применяется как замена пенициллина при аллергии или резистентности к нему. Производные эритромицина кларитромицин, рокситромицин, азитромицин имеют аналогичный механизм действия, однако дольше выводятся, поэтому их принимают в меньших дозах и не так часто. Возможны повреждения желудочно-кишечного тракта. Из-за ингибирования CYP-изоферментов (CYP3A4) возникает опасность наложения эффектов лекарственных средств. Телитромицин — полусинтетический макролид с модифицированной структурой («кетолид»). Устойчивость к препарату объясняется его взаимодействием с другим участком рибосомы. Линкозамиды. Клиндамицин обладает схожим с эритромицином антибактериальным действием. Оказывает бактериостатический эффект на грамположительные аэробные и анаэробные бактерии. Клиндамицин является полусинтетическим хлорза-мещенным аналогом линкомицина, образуемого стрептомицетами. Клиндомицин всасывается лучше линкомицина, обладает более сильным антибактериальным действием и поэтому чаще применяется. Оба препарата хорошо проникают в костную ткань.
4. Оксазолидиноны (например, линезолид) созданы недавно. Они блокируют начало синтеза полипегтгидной цепи в момент соединения рибосомы, мРНК и стартового тРНК-АК-комплекса. Оказывают бактериостатическое действие на грамположительные бактерии. Сообщалось о случаях подавления развития костного мозга (угнетение кроветворения) Необходим контроль формулы крови.
Тетрациклины хорошо всасываются из желудочно-кишечного тракта. Доксициклин и миноциклин всасываются практически полностью. Внутривенное введение показано крайне редко. Наиболее частыми побочными эффектами являются нарушения функции желудочно-кишечного тракта (тошнота, рвота, понос), что обусловлено 1) прямым раздражающим действием на слизистую и 2) нарушением активности естественной микрофлоры кишечника (как при приеме очень многих антибиотиков!) с последующим заселением патогенной флорой, например представителями рода Candida. Однако одновременный прием антацидов или молока для уменьшения раздражения желудка нецелесообразен, так как тетрациклины образуют нерастворимые комплексы с многозарядными катионами металлов (например, Са2+, Mg2+, А!3+, Ре2+/з+) и теряют активность. Именно комплексообразованием Са2+ с тетрациклином объясняется накопление этого препарата в костях и зубах во время их роста, в результате чего зубы становятся желто-коричневыми (необратимо), а рост костей тормозится (обратимо). Поэтому тетрациклины противопоказаны женщинам с 3 месяцев беременности и детям до 8 лет. Другими побочными эффектами являются повышенная фотосенсибилизация кожи, а также нарушения функции печени, чаще при внутривенном введении.
Хлорамфеникол — антибиотик очень широкого спектра действия; он полностью всасывается при пероральном приеме, равномерно распределяется по организму, преодолевая диффузионные барьеры, в том числе гематоэнцефалический. Несмотря на преимущества, хлорамфеникол применяется редко (инфекции ЦНС), так как способен повреждать костный мозг. Возможно развитие двух форм угнетения кроветворения: 1) дозозависимая — токсическая и обратимая; 2) латентная; развивается через несколько недель после лечения, не зависит от дозы, часто — летальный исход. Даже при местном назначении хлорамфеникола (в виде глазных капель) следует помнить об опасности нарушения кроветворения.
Аминогликозидные антибиотики состоят из аминосахаров, соединенных глико-зидными связями (см. гентамицин С1а — один из компонентов смеси, называемой гентамицином). В молекулах аминогликозидов имеется несколько гидрокси- и аминогрупп, способных связывать протоны. Поэтому эти соединения сильно полярны и очень плохо проникают через мембраны. Не всасываются из кишечника. Неомицин и паромомицин применяют перорально для уничтожения флоры кишечника (операции на кишечнике, уменьшение образования аммиака при печеночной коме). Для системного лечения инфекционных заболеваний аминогликозиды назначают парентерально (например, гентамицин, тобрамицин, амикацин, нетилмицин). Местно для лечения инфекций костей и мягких тканей применяются средства, высвобождающие гентамицин. Препараты проникают внутрь бактерий, используя их транспортные системы. Они проникают в почки через клетки проксимальных канальцев по транспортной системе обратного захвата олигопептидов. Аминогликозиды могут повреждать канальцевые клетки (нефротоксичность, в основном обратимая), а также чувствительные клетки органов равновесия и слуха (ототоксичность, иногда необратимая).