Нейростимуляторы и нейропротекторы в спортивном питании: научный обзор
Содержание
- 1 Нейростимуляторы и нейропротекторы в спортивном питании
- 2 Производные холина и аналоги
- 3 Фосфатидил-серин - Phosphatidylserine (PS)
- 4 Кофеин и кофеин-содержащие источники
- 5 Позиция Международного Общества Спортивного Питания (ISSN) по кофеину
- 6 Полифенолы
- 7 L-Теанин (L-theanine)
- 8 Другие вещества с потенциальным нейротропным действием
- 9 Читайте также
- 10 Ссылки
Нейростимуляторы и нейропротекторы в спортивном питании[править | править код]
Авторы: д.м.н. Александр Дмитриев, врач-эндокринолог Алексей Калинчев
Процессы мышления, памяти, скорость визуальной и моторной реакции, одним словом все, что принято включать в оценку состояния мозговых функций, имеет огромное значение в спорте. Оптимальное состояние центральной (ЦНС) и периферической (ПНС) нервной системы обеспечивает адекватную реакцию исполнительных органов, включая скелетную мускулатуру, гормональную и биохимическую адаптацию организма к физическим нагрузкам. Степень адаптации определяет и дальнейшие процессы: скорость развития утомления (снижение способности воспроизводить те же движения, что и в начале тренировки, падение реакции и координации и т.д.); длительность периода восстановления; способность на том же уровне проводить следующий цикл тренировок и многое другое. С возрастом адаптационные возможности снижаются, и у спортсменов старшей возрастной группы требуются дополнительные усилия для сохранения концентрации и реакции на внешние стимулы, большее время на принятие оптимальных решений. Снижение когнитивных функций отражается и на способности переносить нагрузки: чем точнее оценка ситуации, выше скорость выполнения упражнений, тем меньше (экономнее) энергозатраты спортсмена и больше потенциальный объем выполняемой работы. Иными словами, умный и быстро мыслящий спортсмен имеет преимущество перед спортсменом с затуманенным сознанием и вялой реакцией. Можно ли противостоять развитию нейромышечной усталости и снижению когнитивных функций, сохранив свежесть ума и реакции на протяжении длительного периода, и быть полностью готовым к полноценным тренировкам и соревнованиям уже на следующий день? Разрешенные к применению в спорте (не входящие в список WADA) нейротропные БАДы включают вещества как быстрого (немедленного) действия (специфические), так и с отсроченным (метаболически обусловленным) эффектом. Последний (проявляется через дни, недели и месяцы применения и, в большинстве случаев, носит неспецифический характер. Международное Общество Спортивного Питания (ISSN) в течение нескольких лет прицельно анализирует БАДы, которые применяются в спортивной медицине как профессиональными спортсменами, так и просто любителями занятий в фитнес-центрах, с целью улучшения параметров умственной деятельности и других функций ЦНС.
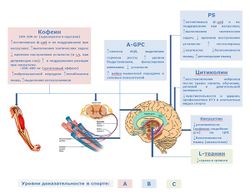
Согласно публикации Krissy Kendall (“Bodybuilding.com”, 25 мая 2016) существует несколько групп БАДов, которые потенциально способны улучшать функции мозга у тренирующихся лиц (с очень разной доказательной базой): 1) производные холина и аналоги (цитиколин; альфа-глицерил-фосфорилхолин – A-GPC); 2) фосфатидил-серин – PS), естественный метаболит организма, выполняющий целый ряд функций, включая улучшение памяти, внимания, поддержание реакции и торможение развития усталости; 3) производные пурина – кофеин и природные источники, его содержащие; 4) полифенолы (ресвератрол, Гинкго Билоба и др.); 5) L-теанин (L-theanine) – небелковая аминокислота листьев зеленого чая; снижает реакцию мозга на экстремальные стрессорные воздействия; 6) хуперцин А (huperzine A) – популярный растительный ноотроп – повышает уровень ацетилхолина в мозге, и некоторые другие.
Указанные группы разрешенных к применению стимуляторов мозговой деятельности имеют различный доказательный уровень – от категории «А» (высшая степень доказательности) до категории «С» и «D» (самый низкий уровень доказательности). Далее в этой главе мы подробно рассмотрим доказательную базу для каждой группы веществ.
С практической точки зрения, улучшение когнитивных функций достоверно обеспечивают и другие известные вещества и пищевые добавки, такие как креатин, дипептиды L-глутамина, омега-3 ПНЖК и некоторые другие. Однако, их действие на функциональное состояние мозговой ткани является, скорее всего, вторичным и, главное, не основным в общем спектре фармакологической активности. Их свойства описаны в отдельных главах настоящего «Руководства по спортивной нутрициологии» и не являются предметом рассмотрения в настоящей статье.
Следует также отметить, что достаточно мощные нейрогенные стимуляторы природного и синтетического происхождения запрещены для применения в спорте и входят в соответствующие списки WADA (см. лист запрещенных субстанций на 2017 год): группа S6 (стимуляторы неспецифические и специфические); S8 – каннабиноиды. Особое внимание следует обратить на вещество оксилофрин (Метилсинефрин - группа S6 – специфические стимуляторы), которое до 2016 года, несмотря на запрет WADA, входило в состав ряда продуктов спортивного питания в США. Продукты с оксилофрином производились, распространялись и применялись в различных видах спорта, что послужило предметом специального разбирательства в официальных регулирующих органах (FDA, Сенат США и др.). Этот вопрос, как и ряд других, рассмотрен в специальной главе настоящего Руководства «Проблемное спортивное питание».
Другой, не менее значимой группой веществ, являются нейропротекторы. Нейропротекторы повышают устойчивость мозговой ткани к травмирующим стрессорным воздействиям в таких контактных видах спорта как бокс, американский футбол, регби, ряд других силовых единоборств, в которых могут возникать острые или хронические травмы головного мозга с ближайшими или отдаленными последствиями. Зачастую такими нейропротективными свойствами обладают и стимуляторы мозговой деятельности из вышеописанных групп. Включение нейропротекторов в состав комплексной НМП является целесообразной мерой и должно производиться на основе имеющихся научных и клинических исследований эффективности и безопасности.
Производные холина и аналоги[править | править код]
Основополагающим веществом этой группы является холин [(2-гидроксиэтил)триметиламмоний], катион 2-гидроксиэтилтриметиламмония, [(CH3)3N+CH2CH2OH] X−.
Относится к водорастворимым витаминам группы В (В4). В организме из холина под влиянием холин-ацетилтрансферазы образуется ацетилхолин, являющийся передатчиком (нейромедиатором) нервных импульсов в ЦНС и ПНС. Функционирование холинергических систем мозга в совокупности с другими нейромедиаторными системами, определяет все основные параметры деятельности мозга.
Сам по себе холин является добавкой, разрешенной к применению в большинстве стран мира в составе лекарственных препаратов и БАДов. Научная точка зрения на холин в Европе определена документом Европейского Общества по безопасности пищи» (EFSA) с длинным названием «Scientific Opinion on the substantiation of health claims related to choline and contribution to normal lipid metabolism (ID 3186), maintenance of normal liver function (ID 1501), contribution to normal homocysteine metabolism (ID 3090), maintenance of normal neurological function (ID 1502), contribution to normal cognitive function (ID 1502), and brain and neurological development (ID 1503) pursuant to Article 13(1) of Regulation (EC) No 1924/2006». Согласно этому документу, Европейской Комиссией для холина признаны с точки зрения доказательной медицины следующие направления: нормализация метаболизма липидов; поддержание нормальной функции печени; оптимизация обмена аминокислоты гомоцистеина; нормализация неврологических функций организма; улучшение когнитивных функций; стимуляция развития мозговых структур. Специально для влияния холина на функции нервной системы выделены следующие показания (выписка из документа):
Таблица 1. Свойства холина как составной части пищевых продуктов в плане регуляции нервной деятельности
| Направленность действия | Предлагаемые формулировки для продукции, содержащей холин |
|---|---|
| Когнитивные функции, память, неврологические показатели Повышение функциональной активности мозга за счет улучшение передачи импульсов между нейронами мозга. Входит в состав нейромедиаторов. Улучшает память, способность к обучению и концентрацию внимания. Предотвращает нейродегенеративные процессы в ЦНС под влиянием стрессорных и патогенных факторов. |
- Холин поддерживает нормальное функционирование нервной системы - Холин поддерживает передачу нервных импульсов - Холин поддерживает когнитивные функции - Холин помогает поддерживать память и функции мозга |
| Суточная доза для спортсменов – 100 мг; для обычных людей 45 мг (15% от минимальной терапевтической дозы 300 мг); минимальная суточная доза 20 мг. | |
| Развитие Незаменимый нутриент для функции мозговой ткани и периферической нервной системы. Стимулирует развитие ЦНС и памяти (входит в группу витаминов В). Несмотря на синтез в небольшом количестве в организме, должен поступать с пищей для поддержания здоровья. |
- Холин является незаменимым нутриентом для нормального развития, особенно мозга и нервной системы |
| Суточная доза для этапа развития ЦНС и ПНС 20 мг; содержание в функциональной пище – не менее 20 мг | |
Цитиколин[править | править код]
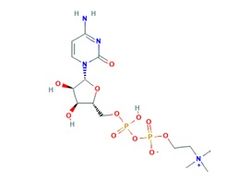
Цитиколин – (CDP-холин; цитидин 5’-ди-фосфохолин) природное вещество, широко применяемое в различных странах в качестве БАДа (пищевой добавки). Экзогенное введение цитиколина влияет на клеточный метаболизм мозга, улучшая когнитивные функции и оказывая нейропротекторное действие как в доклинических, так и в клинических исследованиях (J.J.Secades, J.L.Lorenzo, 2006; R.Ozay и соавт., 2007; V. Parisi и соавт., 2008). Сочетая в структуре холин и цитидин, цитиколин участвует в синтезе фосфолипидов клеточных мембран, восстанавливая их структуру (J.J.Secades, J.L.Lorenzo, 2006; R.Conant, A.G.Schauss, 2004) и обеспечивая источник холина для образования нейромедиатора ацетилхолина (AЦХ) и синтеза фосфатдихолина (I.H.Ulus и соавт., 1989; J.J.Secades, J.L.Lorenzo, 2006).
Фармакокинетика и метаболизм цитиколина[править | править код]
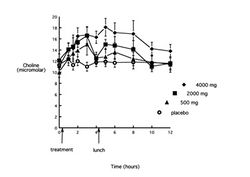
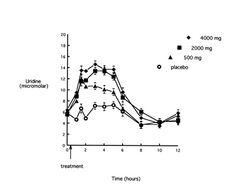
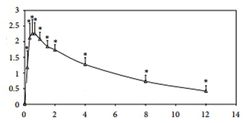
Подробное исследование фармакокинетики цитиколина у человека при пероральном введении в различных дозах выполнено R.J.Wurtman и соавторами (2000). Цитиколин принимался натощак в дозах 500, 2000 и 4000 мг (в сравнении с плацебо). Образцы крови на содержание холина, уридина и цитидина брались через 1, 1.5, 2, 3, 4, 5, 6, 8, 10 и 12 часов после приема цитиколина.
Цитиколин после приема внутрь абсорбируется практически полностью и достаточно быстро. Он метаболизирует в печени с образованием холина и цитидина, однако у человека основными метаболитами при энтеральном приеме цитиколина в процессе абсорбции в кишечнике являются холин и уридин, которые и служат циркулирующими в крови главными маркерами при исследовании фармакокинетики цитиколина. Как видно из рис.2, прием цитиколина приводит к значимому (P<0,05) дозо-зависимому увеличению площади под кривой «концентрация холина-время» (AUC). Пик концентрации холина наблюдался через 2-3 часа после приема дозы 500 мг и через 5 часов после приема других доз. Величина возрастания была 23, 32 и 43% для доз 500, 2000 и 4000 мг, соответственно (P<0.001), а продолжительность повышения для дозы 500 мг составила 4 часа, 2000 мг – 6-8 часов, 4000 мг – 8-10 часов. Прием цитиколина достоверно (P<0,001) увеличивает AUC под кривой «концентрация уридина-время» при использовании всех дозировок вещества (рис.3), однако увеличение дозы с 2000 мг до 4000 мг не сопровождается дальнейшим ростом данного показателя. Пик концентрации уридина отмечается через 1,5 часа после дозы 500 мг, и через 3 часа – после других доз, составляя 101, 136 и 134% от базовых значений соответственно возрастающей дозе. Повышение сохраняется 5–6 часов при всех дозировках. И если прием пищи (обед) несколько замедляет спад концентраций холина (рис.2), то на динамику концентраций уридина он не влияет. Циркулирующие в крови метаболиты цитиколина в значительной степени распределяется в структурах головного мозга, с быстрым внедрением фракций холина в структурные фосфолипиды. Уридин, после проникновения через ГЭБ, превращается в уридин-5’-трифосфат, который в дальнейшем может метаболизировать до цитидин-трифосфата и CDP-холина. Только 15 % введенной дозы цитиколина выводится из организма человека; менее 3 % - почками и около 12 % - с выдыхаемым СО2. Менее 1% цитиколина выделяется с фекалиями.
Таким образом, исходя из фармакокинетики цитиколина, для создания относительно равномерной эффективной концентрации вещества и его метаболитов в плазме крови необходимо применение внутрь в дозе 500 мг 3 раза в день, или 2000 мг 2 раза в день. Повышение дозировки нецелесообразно из-за отсутствия дополнительного прироста концентрации активных метаболитов (холина и уридина) в крови.
Фармакодинамика цитиколина[править | править код]
Влияние цитиколина на нейромедиаторные процессы в мозге[править | править код]
Ряд исследований показал, что пищевые добавки цитиколина увеличивают содержание в мозге холин-содержащих веществ, повышающих биоэнергетику. Так, S.M.Babb и соавторы (1996), применив метод протонной магниторезонансной спектроскопии (MRS) in-vivo, выявили, что однократная доза CDP-холина увеличивает концентрацию холина в плазме крови как у молодых, так и у пожилых лиц через 3 часа после приема. Продолжая это исследование, в более поздней публикации те же авторы (S.M.Babb и соавт., 2002) методом MRS измерили изменения биохимии мозга у здоровых лиц после 6 недель приема 500 мг цитиколина. Они обнаружили повышение в структурах мозга фосфодиэфиров, которое коррелировало с клиническими признаками улучшения памяти. М.М.Silveri и соавторы (2008) с помощью MRS-метода оценили уровни метаболитов мозга у лиц в возрасте 40 – 60 лет, получавших постоянно пищевые добавки цитиколина в течение 6-и недель в дозах 500 или 2000 мг/день. Наблюдалось достоверное повышение уровней фосфокреатина в передней части поясной извилины коры головного мозга, что подтверждает предположение об улучшении биоэнергетики и поддержании функции фосфолипидов клеточных мембран мозга во фронтальной коре. Результаты исследований на животных оказались комплементарны данным, полученным в исследованиях у человека, и подтвердили потенциальную роль цитиколина в регуляции нейротрансмиттерных процессов мозга: 28-дневное введение крысам цитиколина увеличивало высвобождение дофамина в стриатуме (J.Agut и соавт., 2000).
Влияние цитиколина на показатели умственной деятельности[править | править код]
Необходимо подчеркнуть, что большинство работ по оценке влияния цитиколина на когнитивные функции выполнено у лиц старше 40 лет, в основном у пожилых. В этой возрастной группе получены достоверные данные об улучшении внимания, памяти, времени реакции и других показателей (A.Agnoli и соавт., 1989; A.Davalos, J.Secades, 2011; Е.McGlade и соавт., 2012). Были установлены параметры курсового применения цитиколина в этой возрастной группе (включая, в первую очередь, лиц с перенесенными инсультами) – 500-2000 мг в сутки в течение 6-и недель с нарастанием эффекта при увеличении дозы. В результате усиливается фокусировка внимания, рабочая память и точность выполнения поставленных задач как у здоровых лиц старше 40 лет, так и у лиц пожилого возраста с нейрокогнитивными нарушениями. Причинами положительного действия цитиколина на сегодняшний день считаются усиление допаминергической передачи (повышение уровня допамина в мозге, чувствительности допаминовых рецепторов) и возмещение нейромедиаторной недостаточности в мозге. Наиболее полная оценка влияния цитиколина на когнитивные функции людей с различными нарушениями мозговой деятельности дана в систематическом обзоре N. Cano-Cuenca и соавторов (2015). В ней сделан достаточно важный для потенциального применения цитиколина в медицине вывод: достоверно доказана эффективность цитиколина в улучшении когнитивных функций у лиц, перенесших острый инсульт, но для вывода о влиянии на возрастные заболевания (болезнь Альцгеймера или васкулярная деменция) нужны дополнительные исследования.
На сегодняшний день нет экспериментальных и клинических подтверждений способности цитиколина в диапазоне терапевтических доз улучшать когнитивные функции у молодых здоровых лиц без признаков нарушения функционального состояния мозга, которые бы служили основанием для применения в составе НМП спортсменов.
Влияние цитиколина на функции поврежденного мозга и устойчивость мозга к повреждениям[править | править код]
С точки зрения практики спортивной медицины нейропротективное действие препарата или БАДа оценивается по его способности: а) снижать реакцию мозга на потенциально опасное травматическое воздействие (проявляется при превентивном, профилактическом назначении вещества) и, тем самым, минимизировать последствия; б) ускорять восстановление после перенесенной черепно-мозговой травмы. Обе эти ситуации имеют место в контактных видах спорта (и не только), а последствия хорошо известны и часто укорачивают продолжительность жизни и снижают ее качество у спортсменов. На протяжении многих лет цитиколин считался одним из наиболее перспективных веществ в комплексном лечении последствий черепно-мозговой травмы (ЧМТ). До 2009 года выполнен целый ряд экспериментальных исследований эффектов цитиколина при ЧМТ. Установлено, что цитиколин оказывает нейропротективное действие (С.Е.Dixon и соавт., 1997; М.К.Baskaya и соавт., 2000; R.J.Dempsey, V.L.Raghavendra Rao, 2003): достоверно предотвращает потерю нейронов в гиппокампе, вызванную ЧМТ, снижает величину контузии коры головного мозга и улучшает неврологическое восстановление. Кроме того, цитиколин дозо-зависимо снижает хронический моторный и пространственный дефицит, увеличивает внеклеточный уровень ацетилхолина – ключевого медиатора процессов памяти (C.E.Dixon и соавт., 1997). Эти факты свидетельствуют в пользу способности цитиколина усиливать холинергическую передачу и ликвидировать хронический функциональный дефицит при ЧМТ. Другой фактор действия цитиколина – ослабление процесса падения уровня допамина, развивающегося после травмы (B.M.Ross и соавт., 2001; R.Rejdak и соавт., 2002; J.J.Secades, G.Frontera, 1995), что способствует восстановлению. Рандомизированные клинические исследования цитиколина при ЧМТ показали ускорение функционального восстановления при наличии фокального моторного дефицита у пациентов с сильной ЧМТ (F.Cohadon и соавт., 1982), восстановление воспоминаний, объема памяти (H.S.Levin, 1991), снижение пост-контузионной симптоматики при ЧМТ слабой выраженности, снижение времени пребывания в больнице и потребности в повторной госпитализации (V.Calatayud Maldonado и соавт., 1991). Цитиколин также усиливал мозговой кровоток: после введения вещества пациентам с ЧМТ и выраженной потерей памяти устранялась гипоперфузия нижней левой височной области коры головного мозга (J.Leon-Carrion и соавт., 2000).
Однако, выполненное в 2009 году крупное рандомизированное двойное-слепое плацебо-контролируемое мультицентровое исследование эффектов 90-дневного применения цитиколина («COBRIT», R.Zafonte и соавторы, 2009, 2012) в отношении функционального состояния пациентов после ЧМТ разной величины (слабая, средняя, сильная) поставило под сомнение целесообразность использования цитиколина после ЧМТ. Авторами этой большой работы было сделано заключение, что эффективность цитиколина у пациентов с ЧМТ в остром и пост-остром периоде при 90-дневном применении не превышает действия плацебо.
Опровержение данного заключения было сделано сразу в двух не менее серьезных работах: R.M.Adibhata (2013) и J.J. Secades (2014). J.J. Secades (2014) выполнил т.н. кумулятивный мета-анализ на основе работ, опубликованных на протяжении последних 35 лет и имеющихся в базах данных Medline, Embase и Ferrer (последняя компания осуществляет маркетинг цитиколина в ряде стран), которые касались сравнительных исследований цитиколина в острой фазе повреждения мозга. В таблице 2 приведены сведения по таким отобранным работам с указанием тяжести повреждения мозга и схем применения цитиколина.
Таблица 2. Характеристика исследований, включенных в мета-анализ влияния цитиколина на острое повреждение мозга (J.J.Secades, 2014)
| Автор | n | ВПМ | Дозировки |
|---|---|---|---|
| Misbach 1978 | 80 | СР-СИ | 300 мг в/в 14 дней |
| Espagno 1979 | 46 | СИ | 250 мг в/в или в/м 20 дней |
| Richer 1980 | 60 | СИ | 750 мг в/в или в/м 20 дней |
| Cohadon 1982 | 60 | СИ | 750 мг в/в или в/м 20 дней |
| Lecuire 1982 | 25 | СР-СИ | 750 мг в/в 10 дней |
| Lecuire 1985 | 40 | СР-СИ | 750 мг в/в 10 дней |
| Ogashiwa 1985 | 101 | СИ | 1000 мг в/в 7 дней |
| Raggueneau 1988 | 921 | СИ | 500-750 мг в/в 20 дней |
| Calatayud 1991 | 216 | СР-СИ | 3-4 г в/в 4 дня 2 г п/о 26 дней |
| Lozano 1991 | 78 | СР-СИ | 3-6 г в/в 14 дней |
| Aniruddha 2009 | 62 | СЛ | 1 г п/о 30 дней |
| Zafonte 2012 | 1070 | СЛс, СР-СИ | 2 г п/о 90 дней |
Примечания: ВПМ – выраженность повреждения мозга: СЛ – слабое; СЛс – слабое с осложнениями; СР – средней тяжести; СИ – сильное. n – число участников исследования; в/в – внутривено; в/м – внутримышечно; п/о – перорально (внутрь)
Полученные в результате мета-анализа данные четко показывают положительные свойства цитиколина в отношении ЧМТ и, в отличие от исследования COBRIT, сфокусированы именно на цитиколине (при таком подходе действие цитиколина не «растворено» в эффектах других компонентов комплексного лечения ЧМТ, как в COBRIT).
Таким образом, положительное действие цитиколина обусловлено, в первую очередь, ускорением восстановления мозговых функций после травматических повреждений, сокращением сроков реабилитации, более полной реставрацией памяти и способности к обучению, речевой и двигательной активности. Это имеет и фармако-экономический эффект – снижение затрат на восстановительные процедуры и возвращение к тренировочной и соревновательной практике. В настоящее время цитиколин дистрибьютируется в 60 странах мира по ряду показаний, среди которых ЧМТ и ее последствия.
Полученные результаты открывают дорогу сразу для двух направлений применения цитиколина: 1) в клинической медицине – для лечения последствий спортивной ЧМТ разной степени тяжести (к спортивной нутрициологии не относится, и является чисто клинической задачей) и 2) превентивного курсового применения цитиколина как БАДа с нейропротективным действием в контактных видах спорта в составе комплексной НМП для повышения устойчивости мозга к постоянным (хроническим) травмирующим воздействиям и снижения последствий такой хронической травматизации.
Второе направление соответствует задачам спортивной нутрициологии, т.к. подразумевает составление таких схем НМП, где стрессо-устойчивость мозговой ткани формируется последовательно на протяжении месяцев целенаправленных пищевых интервенций.
Потенциальные возможности превентивного применения цитиколина в контактных видах спорта. Целый ряд фармакодинамических свойств цитиколина, в первую очередь нейропротективное действие при профилактическом назначении, заставляют специалистов в области спортивной медицины рассматривать это вещество как перспективный компонент в составе спортивного питания в таких контактных видах спорта, как бокс, борьба, другие виды единоборств, футбол, хоккей. В этих специальных дисциплинах микроповреждения головного мозга в результате сотрясений и ударов, постепенно (или однократно) накапливаясь, могут приводить к серьезным ближайшим или отдаленным нарушениям высшей нервной деятельности. Повышение устойчивости к травмирующим мозг внешним воздействиям, предотвращение развития хронической травматической энцефалопатии (ХТЭ) – важная задача спортивного врача.
Хроническая травматическая энцефалопатия (ХТЭ) в спорте[править | править код]
Несмотря на то, что впервые термин ХТЭ (Chronic Traumatic Encephalopathy - CTE) появился в медицинской литературе в 1960-х годах прошлого столетия применительно к категории спортсменов-боксеров, проблема остается актуальной и трудно решаемой и в наше время и в других видах спорта (А.С.McKee и соавт., 2009; B.I.Omalu и соавт., 2005, 2006). ХТЭ – нейродегенеративное заболевание, причиной которого, по крайней мере частично, являются повторяющиеся травмы мозга, включающие как сильные, так и слабые воздействия. Последствиями таких многократно повторяющихся повреждений мозга являются: нарушение исполнительных функций; снижение памяти; депрессия и суицидальные настроения; апатия; слабый контроль импульсивных реакций и, в конечном счете, деменция. Ранние симптомы ХТЭ у спортсменов приведены в таблице 3.
Таблица 3. Ранние симптомы ХТЭ у спортсменов в контактных видах спорта (С.М. Baugh и соавт., 2012)
| Категория | Симптомы |
|---|---|
| Когнитивные | Нарушение памяти. Дисфункция процессов организации и оценки тренировочных задач (проблемы с планированием, постановкой задач и последовательностью их исполнения, критической оценкой результатов и четкостью суждений) |
| Изменение настроения | Депрессия, апатия, раздражительность, суицидальные мысли |
| Поведенческие | Проблемы с импульсивным контролем (например, быть вспыльчивым, легко выходить из себя, «заводиться с пол-оборота»). Снятие тормозных ограничений. Злоупотребление алкоголем и/или наркотиками, а также другие виды зависимости. Агрессия, склонность к насильственным действиям. |
Достаточно детальный анализ этиологии и патогенеза ХТЭ у боксеров сделано в работе Н.Е. Полищук и А.В. Муравского (2009). В этом обзоре дана эпидемиология ЧМТ, механизмы развития повреждений, патанатомия и патофизиология ХТЭ, клинические и неврологические симптомы, критерии оценки степени нарушений и постановка диагноза, тестирование спортсменов. Однако в небольшом разделе «Профилактика травматической энцефалопатии боксеров» рекомендации сводятся к выявлению групп риска. Применение нейропротекторов и антиоксидантов в лечении и предупреждении ХТЭ обозначено в качестве пожеланий для дальнейшего изучения без какой-либо детализации, что свидетельствует об отсутствии данных такого рода в отечественной литературе.
Поскольку получение хронических травмирующих мозг воздействий во многих видах контактного спорта является неизбежным, встает вопрос профилактики с целью смягчения реакции на макро- и микроповреждения и минимизации их последствий. Определенную роль может играть включение в состав комплексной НМП нейропротекторных средств природного происхождения. Частичным подтверждением этого положения могут служить данные о компенсаторном повышении содержания холина у атлетов, имеющих в анамнезе повторяющиеся травмы мозга, по сравнению со спортсменами аналогичного возраста без истории получения таких травм (A.Lin и соавт., 2010). Защитное действие цитиколина при превентивном применении также может быть обусловлено повышением уровня глутатиона в мозге (R.M.Adibhatla и соавт., 2001; М.Barrachina и соавт., 2003; J.P.De la Cruz и соавт., 2000), обладающего мощным антиоксидантным эффектом. Кроме того, цитиколин может снижать апоптоз и предотвращать клеточную смерть в эксперименте (J.Krupinski и соавт., 2002; C.Mir и соавт., 2003), что, по мнению J.Erdman и соавторов (2011) в совокупности может служить основанием для рутинного применения пищевых добавок цитиколина в составе НМП при повторяющихся травмах головного мозга.
Хотя на сегодняшний день и недостаточно данных для отнесения цитиколина и других производных холина к спортивным добавкам категории «А» (высшая степень доказательности), тем не менее они входят в качестве перспективных БАДов во многие классификации (S. Potgieter, 2013; M.H.Williams, 2004), и могут, с нашей точки зрения, быть отнесены по уровню доказательности к категории «В» Учитывая высокий профиль безопасности цитиколина, и высокую научную обоснованность его использования в качестве нейропротектора, в практической работе целесообразно курсовое назначение цитиколина спортсменам в контактных видах спорта в дозах 500-1000 мг 2 раза в день в течение 4-8 недель с перерывами 1-1,5 месяца.
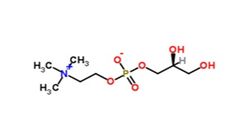
Альфа-глицерил-фосфорил-холин (alpha-Glyceryl-phosphoryl-choline – A-GPC)[править | править код]
Альфа-глицерил-фосфорил-холин (A-GPC) – вещество, которое может потенциально повысить физическую готовность спортсмена за счет сочетания центрального и периферического (усиления нервно-мышечной передачи) стимулирующих эффектов. Особенности фармакокинетики A-GPC заключаются в том, что он обеспечивает в 12 раз большую концентрацию холина в сыворотке крови, чем неорганические соли холина, и на гораздо большее время (12 часов против 30 минут) (M.J.Hirsch и соавт., 1978; R.J.Wurtman и соавт.,1977). Доказан хороший профиль безопасности A-GPC в средних и высоких дозах (L.Parnetti и соавт., 20007; A.M.Brownawell и соавт., 20011). После приема внутрь и всасывания в кишечнике A-GPC превращается в организме в фосфатидил-холин – мощный источник холина (S.H.Zeisel, 2012). A-GPC в эксперименте повышает концентрацию ацетилхолина в нейронах ЦНС (E.Traini и соавт., 2013), усиливает выделение гормона роста в ответ на постоянные тренировки (T.Ziegenfuss и соавт., 2008) и препятствует падению скорости реакции у человека в процессе изматывающих тренировок (J.R.Hoffman и соавт., 2010). В лаборатории J.R.Hoffman исследовали эффект однократного (острого) и хронического (курсового) 4-х недельного приема комбинированной пищевой добавки под названием CRAM на показатели реакции и субъективные показатели (заполнение опросников) усталости (утомляемости), способности фокусироваться, готовности к действиям по сравнению с плацебо у спортсменов-любителей (студенты). В рандомизированном исследовании приняло участие 19 человек (17 мужчин и две женщины) в возрасте 21±0,6 года, масса тела 81±9 кг. Тестирование показателей при однократном приеме CRAM проводилось за время исследования дважды с интервалом в 4-е недели. Добавка CRAM включала разовую порцию (3 капсулы), содержащую: A-GPC 150 мг, холина битартрат 125 мг, фосфатидил-серин (PS) 50 мг, ниацин (витамин B3) 30 мг, пиридоксин HCl (витамин B6) 30 мг, метилкобаламин (витамин B12) 0,06 мг, фолиевая кислота 4 мг, L-тирозин 500 мг, кофеин безводный 60 мг, ацетил-L-карнитин 500 мг и нарингин 20 мг. Прием капсул запивался 300 мл воды. Тестирование включало 4-минутный тест на реакцию (PRE), а через 10 минут – тренировка до истощения с последующим повторением теста на реакцию. Тренировочный истощающий период состоял из 30-секундного Wingate-анаэробного теста на мощность, максимального числа отжиманий в течение 1-ой минуты, затем максимального числа приседаний за 1 минуту. Курсовой прием CRAM в той же суточной дозе ежедневно продолжался 4-е недели для CRAM и затем плацебо для всех участников с «отмывочным» периодом 4 недели. На рис.5. представлены эффекты CRAM на показатели реакции испытуемых как при однократном, так и курсовом приеме.
Как видно из диаграммы, лица, получавшие однократно пищевые добавки CRAM, были способны поддерживать хорошие показатели реакции после нагрузки, в отличие от группы плацебо. В то же время, CRAM не влиял на регистрируемые показатели реакции при курсовой приеме, а также на показатели мощности и выносливости. Анализ данных визуальной аналоговой шкалы показали, что СRAM способствует поддержанию субъективного чувства бодрости, предупреждает возникновение чувства усталости, сохраняет способность к фокусировке внимания у спортсменов-любителей. С другой стороны, нельзя с уверенностью утверждать, что положительный эффект пищевой добавки CRAM обусловлен исключительно содержанием в ней A-GPC, т.к. и другие компоненты (PS, кофеин, карнитин) обладают определенным нейротропным эффектом, о чем будет сказано ниже.
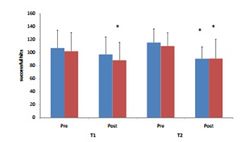
В более поздней работе D.Bellar и соавторов (2015) оценивалось влияние A-GPC уже «в чистом виде» в качестве донатора холина для усиления функции ацетилхолина как медиатора нервно-мышечной передачи (периферический аспект нейрогенного действия производных холина) при физических нагрузках. Отправной гипотезой исследования было предположение, что высокая биодоступность холина в составе A-GPC обеспечит восстановление уровней холина после тренировок, что положительно скажется на результатах тестирования. В рандомизированное двойное-слепое плацебо-контролируемое перекрестное исследование с «отмывочным» периодом одна неделя были включены 13 здоровых студентов-мужчин (возраст 21,9 ± 2,2 года, рост 180,3 ± 7,7 см, вес 87,6 ± 15,6 кг, VO2 max 40,1 ± 7.2 млO2кг/мин, жировая масса тела 17,5 ± 4,6 %). Испытуемыми осуществлялся прием A-GPC (AlphaSize®, ChemiNutra, Austin, TX) в капсулах утром и вечером (по 300 мг, суммарная доза в сутки 600 мг) или плацебо в течение 6-и дней. Тестирование параметров физической формы проводилось до и после 6-дневного приема БАДа или плацебо (у тех же испытуемых с недельным «отмывочным» перерывом) и включало: изометрический тест тяги фиксированного грифа штанги от середины бедра («золотой стандарт» глобальной оценки силы - isometric mid-thigh pull test - IMTP) с автоматизированным компьютерным анализом показателей; изометрический тест для мышц верхней части тела (upper body isometric test - UBIST). Острый эффект оценивался через 1 час после приема 600 мг A-GPC в первый раз, хронический – через 6 дней приема. При однократном (остром) приеме не выявлено никаких отличий в группе с БАДом по сравнению с плацебо. При 6-дневном (хроническом, курсовом) приеме препаратов выявлены достоверные различия и разная направленность изменений показателей в обоих изометрических тестах для A-GPC и плацебо (рис. 6).

Как видно из графиков, A-GPC значительно увеличивает показатели силы при изометрическом мышечном напряжении во всех группах мышц (68% и 86% для IMTP и UBIST, соответственно), в то время как в группе с плацебо отмечена тенденция к снижению показателей.
Кроме уже приведенных исследований имеются данные A.R.Jagim и соавторов (2015) о способности мульти-ингредиентных добавок, содержащих A-GPC, повышать среднюю мощность в спринтерских тестах (максимальной интенсивности) на беговой дорожке в зале без изменения пика и средней мощности прыжковых движений. A.G.Parker и соавторы (2015) при однократном приеме A-GPC в дозах 200 мг или 400 мг отметили недостоверную тенденцию к увеличению мощности прыжков. Также однократный прием большей дозы 600 мг A-GPC повышает показатели в жиме лежа у тренированных мужчин.
Потенциальными механизмами действия A-GPC являются: 1) повышение биодоступности холина для нейронов и усиление в них синтеза ацетилхолина; 2) опосредованное увеличение секреции гормона роста за счет стимуляции высвобождения катехоламинов; 3) хроническое увеличение концентрации гормона роста в организме при курсовом применении A-GPC (более 7 дней), что сказывается уже на активации анаболических процессов в мышцах.
Таким образом, A-GPC является эффективной пищевой добавкой для курсового применения сроком от 6 недель в дозе 300 мг на прием два раза в день (утром и вечером, суммарная суточная доза 600 мг), или однократно в дозе 600 мг за 30-90 минут до тренировки или соревнования, для улучшения нейро-мышечной передачи и повышения силовых показателей спортсменов. Результаты экспериментальных и клинических исследований эффективности и безопасности позволяют рекомендовать тренерам и спортивным врачам включение A-GPC как универсального стимулятора нейро-мышечной передачи в состав комплексной НМП в большинстве видов спорта для повышения показателей силы и мощности.
Фосфатидил-холин (Лецитин) (Phosphatidyl Choline, Lecithin)[править | править код]
В соответствии с позицией Международного Общества Спортивного Питания (ISSN, R.B.Kreider и соавт., 2010), основанной на изучении научной литературы за последние 10 лет, несмотря на теоретическую обоснованность потенциала этого вещества как стимулятора нервно-мышечной передачи, нет данных клинических исследований у человека даже в плане контроля веса и состояния нервно-мышечной системы.
Фосфатидил-серин - Phosphatidylserine (PS)[править | править код]
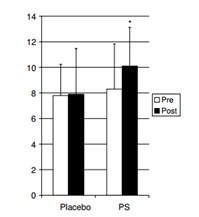
Хотя фосфатидил-серин (PS) и не является производным холина, его рассмотрение в данном разделе является вполне уместным в связи со следующими обстоятельствами: 1) в большинстве смесей, содержащих производные холина, включен и PS; 2) спектр фармакологической активности включает способность регулировать функции возбудимых мембран клеток головного мозга, улучшать когнитивные функции; 3) по механизму действия PS является фосфолипидом, который включается в клеточные мембраны структур с высокой метаболической активностью, таких как мозг, сердце, легкие, печень и скелетная мускулатура (A.Blokland и соавт., 1999; M.A.Starks и соавт., 2008), что может при совместном приеме с производными холина оказывать синергичное положительное действие в условиях предельных физических нагрузок и снижения нейрогуморальной регуляции. Ряд исследований показал, что PS может снижать воспаление (P.Monteleone и соавт., 1990; M.L.Huynh и соавт., 2002) и действовать как антиоксидант(S.Lactorraca и соавт., 1993; C.D.Dacaranhe, J. Terao, 2001). Эти предпосылки привели к исследованиям способности PS улучшать показатели физической силы и восстановление после физических нагрузок. Группа исследователей Калифорнийского Университета в 1998 году (T.D.Fahey и соавторы) впервые показала эффективность PS у тяжелоатлетов. Как видно из рисунка 8, PS достоверно и значительно снижает посттренировочную болезненность мышц и улучшает самочувствие спортсменов (по субъективным шкалам оценки – опросники).
Дальнейшие исследования подтвердили способность PS при приеме внутрь улучшать восстановление, увеличивать объем выполняемой работы, а возможными механизмами этих эффектов являются опосредованное возрастание тестостерона и снижение уровней кортизола в плазме крови. Таким образом, гормональный баланс смешается в сторону анаболических процессов при торможении катаболических.
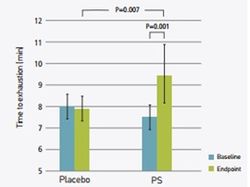
В работах, выполненных в Великобритании (M.Kingsley и соавт., 2005,2006), изучалось влияние PS на выносливость. В двойном-слепом плацебо-контролируемом исследовании у 14 здоровых и тренированных мужчин изучены эффекты перорального приема 750 мг/день PS или плацебо в течение 10 дней. Тестирование производилось на велотренажере до и после периода приема добавок. Выносливость определялась на велоэргометре при 85% VO2max. PS увеличивал время наступления истощения на 25% (с 7,51 до 9,51 мин), в контрольной группе изменений не отмечено (рис.9).
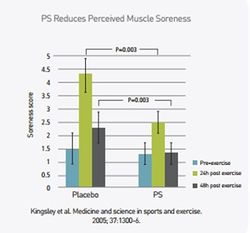
В другом двойном-слепом плацебо-контролируемом исследовании тех же автороов (M.Kingsley и соавт., 2005) 16 футболистов получали 750 мг/день PS или плацебо в течение 10 дней. Увеличение времени истощения составило в группе PS 4,2%, в то время как в группе плацебо оно уменьшилось по сравнению с исходными показателями на 3,7%. Прием PS способствует снижению болезненности мышц. Так, на основе опросников (шкала субъективной оценки), M.Kingsley и соавторы (2005) обнаружили снижение субъективных болезненных ощущений в разных группах мышц, наблюдавшиеся обычно на 2-3 день после интенсивной тренировки, под влиянием PS, по сравнению с плацебо (рис.10).
М.А.Starks и соавторы (2008) сообщили о снижении стрессорного ответа на циклические упражнения средней интенсивности (65% - 85% VO2max) после 10 дней приема 600 мг/день пищевых добавок PS, что проявилось снижением уровней выделения кортизола, повышением тестостерона и сдвигом соотношения тестостерон/кортизол в пользу тестостерона в ответ на физическую нагрузку (рис.11)
Однако, имелись и отрицательные результаты. Так, М.Kingsley и сотрудники (2006) не подтвердили улучшение восстановления у отдельных лиц после цикла упражнений на беговой дорожке. В целом, количество исследований PS и его комбинаций с другими фармаконутриентами весьма ограничено, особенно в плане регуляции мощности и времени реакции на стрессорные стимулы.
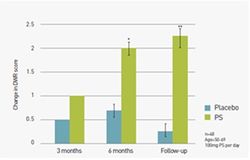
Влиянию PS на когнитивные функции человека посвящено более 30 публикаций. Суммарный анализ подтвердил значительное улучшение памяти, снижение времени и правильности принятия решений, большую умственную гибкость при отсутствиии заметных побочных эффектов. PS – единственный на сегодня БАД, одобренный FDA для улучшения когнитивных функций. PS при курсовом назначении оказывает долгосрочный положительный эффект в отношении мозговых клеточных структур. Одной из иллюстраций свойств PS служит график из работы А.Kato-Kataoka и соавторов (2010), где доза PS 100 мг/день в течение 6-и месяцев достоверно и дозозависимо (практически линейно) уже через 3 месяца улучшает когнитивные функции (возрастание показателей в 2 раза). Эффект нарастает к концу 6-го месяца (еще в 2,5 раза) и сохраняется на достигнутом уровне в течение 3-х месяцев после окончания курса (рис.12).
Исследование R.Jäger и соавторов (2007) у молодых гольфистов не выявило достоверного снижения уровня стресса, но количество точных ударов достоверно возрастало (рис.13), что также указывает на положительное влияние курсового применения PS в дозе 200 мг/день в течение 42 дней на высшую нервную деятельность. С другой стороны, эта дозировка существенно меньше той, которая применялась в других работах.
Таким образом, PS может применяться в качестве ежедневной пищевой добавки в дозе 100-200 мг/день курсами 2-6 месяцев для предупреждения снижения когнитивных функций и повышения точности выполнения заданий в условиях интенсивных физических нагрузок в тренировочный и соревновательный период. Помимо этого, пищевые добавки PS в более высоких дозах (600-800 мг/день) у лиц, занимающихся спортом, оказывают следующие эффекты: увеличивают время наступления истощения; повышают уровень тестостерона (анаболическое опосредованное влияние); снижают уровень кортизола (опосредованный антикатаболический эффект); увеличивают соотношение тестостерон/кортизол (улучшение репаративных процессов); редуцируют болезненность мышц; улучшают самочувствие. PS активирует mTor, что способствует увеличению размеров мышц и мышечной силы, и усиливает регенерацию мышечной ткани. Рекомендованные дозы для спортсменов для этих целей 400-800 мг/день курсами 10-42 дня. PS прочно вошел в ассортимент спортивного питания в виде компонента белковых продуктов, напитков, батончиков и др., а также в виде самостоятельной добавки.
На прошедшей в США в 2016 году международной конференции по пищевым добавкам в спорте A-GPC и PS названы в числе наиболее перспективных новых веществ недопингового плана для повышения физической готовности спортсменов.
Кофеин и кофеин-содержащие источники[править | править код]
Кофеин относится к группе фармаконутриентов с высокой доказательной базой (категория «А») по всем известным международным классификациям БАДов, разрешенных к применению в спорте. Однако, надо помнить, что до 2004 года он входил в список запрещенных к употреблению в спорте веществ (стоп-лист WADA), и только после ожесточенных споров был вычеркнут из него. Эти дискуссии не затихают до сих пор (см. далее раздел «Контроль за применением кофеина и кофеин-содержащих составов в спорте»).
Фармакокинетика кофеина при экзогенном введении[править | править код]
Кофеин-бензоат натрия при пероральном приеме всасывается в кишечнике практически на 100%. Время достижения максимальной концентрации в плазме крови (Tmax) составляет 30-60 минут, быстро распределяется во всех органах и тканях организма, проникает через гематоэнцефалический барьер и плаценту (U.Gundert-Remy, 2015). Объем распределения – 0,67 л/кг веса тела. Не обладает специфичностью распределения по органам и тканям. Период полувыведения составляет - 3,9-5,3 ч (иногда до 10 ч). Связь с белками крови (альбуминами) - 15%. Метаболизму в печени подвергается более 90% введенного кофеина. Основная часть 70-80% деметилируется в печени c образованием параксантина (1,7-диметилксантин). Другими первичными метаболитами являются теофиллин и теобромин. Выведение кофеина и его метаболитов осуществляется почками (10% - в неизменном виде, остальные количества, в основном, в виде параксантина, теофиллина и теобромина).
Отдельное, весьма важное с практической точки зрения исследование, выполнено для фармакокинетики кофеина в составе кофейного напитка. В работе S.Teekachunhatean и соавторов (2013) проведено исследование на 11 мужчинах-добровольцах, которые выпивали 180 мл кофе с содержанием кофеина 96,34±1,39 мг/180 мл, после чего у них определялись концентрации кофеина в плазме крови в течение 12 часов (образцы крови). Динамика концентраций представлена на рис.14.
Как видно из графика, максимальная концентрация в плазме (Сmax) составила 2,5±0,4 мкг/мл, время ее достижения (Tmax) – 0,44±0,1 часа, площадь под кривой «время-концентрация» (AUC) - 13±2 мкг/час/мл, время полужизни – 4,9±1,4 часа. Эти данные практически полностью совпадают с фармакокинетикой кофеина при приеме в виде чистого вещества в дозе 100 мг.
Создана специальная форма кофеина в составе жевательной резинки и защечных таблеток для рассасывания в полости рта с дипазоном доз 50-200 мг в одной порции для удобства применения в процессе выполнения тренировочных задач. Важным свойством такой формы является быстрое всасывание (в отличие от приема внутрь) уже в полости рта, что обеспечивает первичное наступление эффекта через 5-15 минут (при меньшей величине концентрации в плазме крови), и поддержание достигнутой концентрации кофеина по мере необходимости (G.H.Kamimori и соавт., 2002).
Фармакодинамика кофеина[править | править код]
Хотя кофеин обладает многими эффектами в организме, основным механизмом считается его конкуренция с аденозином в местах связывания с соответствующими рецепторами (L.L.Spriet, M.J.Gibala, 2004; B.Sokmen и соавт., 2008). В частности, за счет блокады центральных и периферических аденозиновых рецепторов и торможения активности фосфодиэстераз, способствует накоплению цАМФ и цГМФ. Ингибирует фосфодиэстеразу цАМФ (не только в ЦНС, но и в сердце, гладкомышечных органах, жировой ткани, скелетных мышцах). Стабилизирует передачу в дофаминергических синапсах (психостимулирующие свойства), бета-адренергических синапсах гипоталамуса и продолговатого мозга (повышение тонуса сосудодвигательного центра), холинергических синапсах коры (активация корковых функций) и продолговатого мозга (возбуждение дыхательного центра), норадренергических синапсах (усиление физической активности, анорексия). Таким образом, эффекты кофеина, в первую очередь, нейрональные и локализованы в ЦНС, что важно понимать при дальнейшей оценке его эргогенных свойств. К собственным механизмам действия кофеина добавляются и эффекты теофиллина и параксантина, как его метаболитов, на ЦНС (B.B.Fredholm и соавт., 1999). Кроме влияния на ЦНС, кофеин в процессе физических нагрузок способствует утилизации питательных субстратов. В частности, смещает упор с накопления гликогена на повышение мобилизации свободных жирных кислот (Essig D. И соавт., 1980; L.L.Spriet и соавт., 1992). Усиливается внутримышечное окисление жиров при циклических нагрузках. Правда такие метаболические эффекты кофеина проявляются только в средних и высоких дозах – 5-9 мг/кг (350-630 мг на спортсмена весом 70 кг), по сравнению с диапазоном психотропных доз. Еще одним механизмом потенциального эргогенного влияния кофеина может быть наблюдаемое в процессе физических нагрузок повышение выносливости за счет увеличение выделения бета-эндорфинов. Так, D.Laurent и соавторы (2000) показали, что прием кофеина в дозе 6 мг/кг увеличивает концентрацию в плазме бата-эндорфинов после 2-х часового теста на велотренажере на уровне пика потребления 65% VO2. Известно, что повышенное выделение в организме бета-эндорфинов при физических нагрузках за счет своего анальгетического эффекта способно снижать болевую чувствительность (A.Grossman, J.R.Sutton, 1985).
Сочетание кофеина с углеводами[править | править код]
Наряду с прямым центральным эргогенным эффектом, кофеин способен усиливать липолиз и снижать процесс утилизации гликогена, оказывая опосредованное метаболическое эргогенное действие. Как показали исследования у тренированных велосипедистов (J.L.Ivy и соавт.,1979), кофеин в дозах 250 мг и 500 мг за час до физической нагрузки увеличивает объем выполняемой работы на 7,4%.по сравнению с контролем, и на 5,3% - по сравнению с глюкозой. Хорошо известны положительные эффекты самой глюкозы и других «быстрых» углеводов как энергетических субстратов в плане обеспечения потребностей организма при всех видах физических нагрузок. Однако работы по сочетанному применению кофеина и углеводов на сегодняшний день не дали весомых доказательств синергичности в плане повышения физической готовности спортсменов.
Предтренировочные комплексы с кофеином[править | править код]
Предтренировочные комплексы, включающие кофеин, отличаются чрезвычайным разнообразием компонентов, что резко затрудняет оценку вклада каждого компонента в конечный результат. С другой стороны, не так много доказательных работ в данном направлении. Приведем лишь некоторые из них, выполненные в лабораториях, пользующихся авторитетом в мире спортивной медицины. В работе A.E.Smith и соавторов (2010), опубликованной в журнале ISSN, проведено рандомизированное одиночное-слепое плацебо-контролируемое параллельное исследование влияния предтренировочного комплекса на показатели трехнедельной высокоинтенсивной интервальной тренировки (HIIT) при аэробной и анаэробной беговой нагрузке, объем выполненной работы и состав тела. В исследовании приняло участие 24 спортсмена среднего уровня подготовки (средние показатели: возраст 21 год, рост 172 см, масса тела 66 кг, VO2max 3,2 л/мин, жировая масса 19%). Пищевая порошкообразная добавка весом 18 г (Game Time®, Corr-Jensen Laboratories Inc., Aurora, CO) содержала 40 ккал и включала whey-протеин, «cordyceps sinensis» (род грибов класса аскомицетов), креатин, цитруллин, женьшень и кофеин. Эта смесь, предварительно растворенная в 250 мл воды, принималась внутрь за 30 мин до тестирования и тренировочной сессии. Тестирование показателей осуществлялось до и после тренировочной программы. Использовался также кардиоваскулярный фитнесс (VO2max) с оценкой спирометрически. Результаты показали достоверные улучшения VO2max, аэробной и анаэробной способности, состава тела, повышение тощей массы тела (ТМТ) в условиях сочетания комплексной добавки и HIIT.
N.Martinez и соавторы (2016) в своей работе отмечают, что использование предтренировочных комплексов как в развлекательных, так и в конкурентных видах спорта, в последние годы растет драматическими темпами. Примерно 70% молодых взрослых людей по крайней мере один раз пробовали такие комплексы, а 30% потребляют их на регулярной основе. В их собственной работе исследовались эффекты однократного (острого) применения кофеин-содержащего пред-тренировочного комплекса на показатели физической готовности, включая анаэробную мощность, мощность верхних и нижних мышечных групп, общую силу у мужчин, тренирующихся для своего удовольствия. В исследовании приняло участие 13 мужчин (средний возраст 24 года, рост 180 см, масса тела 80-90 кг). Состав комплекса: 1 ложка 14,5 г содержала 10 ккал, 3 г углеводов, 0% жира, 2 г бета-аланина, экстракт свеклы 1,5 г, ВСАА+нитраты 2 г, кофеин из расчета 4 мг/кг и др. Авторы доказали, что пред-тренировочный комплекс достоверно повышает анаэробный пик и среднюю анаэробную мощность по сравнению с плацебо и исходными показателями. Однако, эти данные не дают никакой ясности, за счет чего именно улучшаются показатели физической готовности.
Позиция Международного Общества Спортивного Питания (ISSN) по кофеину[править | править код]
Эта позиция изложена в статье E.R.Goldstein и соавторов (2010) и сводится к следующим основным положениям:
- Кофеин проявляет свои эргогенные свойства в наибольшей степени при применении в безводной форме (капсулы, порошки, таблетки и др.) по сравнению с кофейным напитком.
- В большинстве работ применялись протоколы на основе приема кофеина за 60 минут до физической нагрузки для достижения максимальной абсорбции, однако достаточно выраженный эффект наблюдается уже через 15-30 минут после его приема.
- Кофеин эффективен для повышения физической готовности к разного рода нагрузкам в низких и средних дозировках (3-6 мг/кг). Более того, превышение этих доз (более 9 мг/кг) не дает дополнительных преимуществ.
- В условиях депривации сна (например, у военнослужащих) кофеин может действовать как мобилизующий фактор (усиливает фокусировку внимания, реакцию на визуальные и слуховые стимулы).
- Кофеин оказывает эргогенное действие при нагрузках, требующих максимальной выносливости, и повышает переносимость (время) таких нагрузок.
- Кофеин может усиливать ресинтез гликогена в период восстановительной фазы тренировок.
- Кофеин является пищевой добавкой выбора при высокоинтенсивных продолжительных нагрузках, например, в командных видах спорта (футбол, хоккей и др.).
- Менее ясны факты в отношении влияния кофеина на силу и мощность в некоторых спортивных дисциплинах. Данные противоречивы и требуются дальнейшие исследования.
- Более четкими являются данные о положительном влиянии кофеина на силу и мощность у женщин.
- Научные исследования не подтверждают способность кофеина усиливать диурез в процессе тренировок. Более того, не выявлено усиления на фоне приема кофеина потоотделения, потерь воды, изменений водно-солевого баланса в организме по сравнению с их обычными вариациями в ходе тренировок.
Позиция Ирландского Совета по Спорту относительно кофеина (Caffeine. Technical Document Developed by INDI/SNIG for the Irish Sports Council, 2014)
Суммарно преимущества кофеина при приеме внутрь сводятся к следующему:
- Обладает эргогенными эффектами как при однократных, так и пролонгированных тренировках.
- Снижает усталость при повторяющихся высокоинтенсивных спринтах у велосипедистов.
- Удлиняет время наступления усталости и снижает необходимое время для выполнения фиксированных задач при приеме до и во время тренировок на выносливость.
- Снижает болевые ощущения у спортсменов, возникающие при физических нагрузках.
- Улучшает настроение, поддерживает время реакции, мышечную мощь и энергичность в спортивных единоборствах и при постоянных тренировках.
- Повышает когнитивные функции.
- Может увеличивать силу мышечных сокращений при приеме до и во время нагрузок.
- Повышает уровень бодрствования во время напряженных многодневных соревнований за счет активации ЦНС.
- Ослабляет падение профессиональных спортивных и военных навыков, обусловленных депривацией сна.
Рекомендуемые схемы дозирования[править | править код]
2-3 мг/кг веса тела за 60 минут до тренировки или соревнования. При необходимости – до 3-6 мг/кг, что требуется далеко не всегда. Для спортсменов в видах спорта, требующих выносливости, прием кофеина может быть приближен к началу старта соревнования (за 5-10 минут). Желательно обеспечить точность дозирования, т.е. использовать такие формы (напитки, таблетки, капсулы, гели, жевательные резинки и пр.), которые позволяют определять дозу и время поступления кофеина в организм.
Предосторожности при использовании кофеина[править | править код]
Кофеин увеличивает частоту сердечных сокращений и повышает тонкий моторный контроль, что может негативно отразиться в ситуациях, требующих управления механизмами и приборами. Необоснованные избыточные дозы кофеина могут нарушить сон, восстановление и подготовку к выступлению. Необходимо проверять индивидуальную чувствительность спортсмена к кофеину, учитывать потенциальное взаимодействие с другими пищевыми добавками.
Полифенолы[править | править код]
Самая большая группа полифенолов – флавоноиды. Существует 6 групп флавоноидов: 1) флавоны (например, апигенин, лютеолин), которые содержатся в петрушке и сельдерее; 2) флаваноны/флавонолы (например, гесперетин, нарингенин/астильбин, энгелетин), которые содержатся в основном в цитрусовых, травах (орегано) и вине; 3) изофлавоны (например, даидзеин, генистеин, глицитин), содержащиеся в сое и ее продуктах; 4) флавонолы (например, кемпферол, кверцетин), содержащиеся в луке, луке-порее и брокколи); 5) флаванолы (например, (+)-катехин, (−)-эпикатехин, эпигаллокатехин и эпигаллокатехин галлат (EGCG), который преобладает в зеленом чае, красном вине и шоколаде; 6) антоцианидины (например, пеларгонидин, цианидин и мальвидин) из красного вина и ягод. Существует также два класса полифенолов, которые не относятся к флавоноидам: 1) феноловые кислоты (гидроксибензойные кислоты и гидроксикоричные кислоты); 2) стильбены. Кофейная кислота – наиболее распространенная феноловая кислота (содержится в сливах, киви, яблоках и чернике). Главным представителем стильбенов является ресвератрол (resveratrol), который существует в двух формах – цис- и транс-изомерической (содержится в вине, ананасах и грейпфруте).
Механизмами защитного (нейропротективного) действия флавоноидов являются: 1) повышение устойчивости нейронов к чрезмерному возбуждающему действию нейромедиаторов; 2) снижение реакции на окислительный стресс; 3) ускорение восстановления нейроной сети после физических и психических нагрузок. Так, экстракты Гинко Билоба (Ginkgo biloba) защищают нейроны гиппокампа от нейротоксического воздействия ряда химических соединений (Y.Luo и соавт., 2002).
На сегодняшний день считается, что полифенолы обладают хорошим потенциалом в плане улучшения когнитивных функций (память, обучаемость и т.д.). Большинство работ затрагивает вопросы снижения мнестических и иных функций ЦНС в процессе старения. Тем не менее, накоплен определенный материал по отдельным представителям полифенолов в спортивной медицине.
L-Теанин (L-theanine)[править | править код]
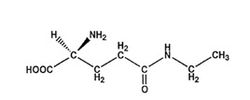
L-теанин (гамма-глутамил-этиламид) – аминокислота, содержащаяся в разных видах зеленого чая (Camellia sinensis), а также в грибах Xerocomus badius. Содержание L-теанина колеблется в пределах 1%-2% в высушенных листьях, а одна чашка зеленого чая содержит около 25 мг вещества. L-теанин также получают синтетическим путем. Максимальная суточная доза, допускаемая FDA США составляет 1200 мг.
- Читайте основную статью L-Тианин (L-Теанин)
Прямых исследований изолированного применения L-теанина в дозах 50-250 мг/день в плане спортивной подготовки не проводилось (L.Baker, 2013). Таким образом, на сегодняшний день имеются лишь теоретические предпосылки для применения L-теанина в спорте, не подкрепленные клиническими доказательствами. Несмотря на это, L-теанин не только включен в состав многих комплексных смесей для бодибилдеров, но и рекомендован для практического применения рядом спортивных ассоциаций.
Другие вещества с потенциальным нейротропным действием[править | править код]
Чрезвычайно важную роль в поддержании мозга, когнитивных функций, восстановлении ЦНС и ПНС после физических нагрузок, играют омега-3 ПНЖК. Результаты исследований влияния EPA и DHA на высшую нервную деятельность, нервно-мышечную передачу, процессы восстановления нервной ткани после прекращения действия физического и психологического стресса, подробно изложены в соответствующем разделе данного «Руководства», посвященном семейству омега-ЖК и их роли в спортивной подготовке. Сходным образом, нейротропные свойства креатина, также повышающего когнитивные функции спортсменов.
Что касается других веществ, упоминаемых, в той или иной степени, во многих пособиях по нутритивной поддержке в спорте как нейро- и психотропные, то, как справедливо отмечено в обзоре L.Baker (2013), данные по таким веществам как ВСАА, флаванолы какао, женьшень, гуарана, тирозин, родиола розовая, изофлавоны сои, ацетил-L-карнитин, хуперцин А, либо противоречивы, либо недостаточны, либо дают отрицательный результат.
Примечания: на схеме не указаны омега-3 ПНЖК, которые при курсовом назначении повышают когнитивные функции и оказывают защитное действие в отношении нейрональной и мышечной ткани. Эти аспекты рассмотрены в соответствующей главе настоящего «Руководства». Это же касается креатина, активно участвующего в нейрональном метаболизме, глутамина и его дипептидов, а также донаторов оксида азота. А, В, С – уровни доказательности эффективности в спорте от высшего (А) к низшему (С).
Читайте также[править | править код]
- Бета-аланин: научный обзор
- Глутамин: научный обзор
- HMB: научный обзор
- Донаторы оксида азота: научный подход
- Креатин: научный обзор
- Спортивные напитки: научный обзор
- Препараты витамина D в спортивной медицине: научный обзор
Ссылки[править | править код]
- Полищук Н.Е., Муравский А.В. Черепно-мозговая травма у боксеров. Обзор литературы. Нейрохирургия, 2009, 3:80-88.
- Adibhatla R.M., Hatcher J. F., Dempsey R. J. Effects of citicoline on phospholipid and glutathione levels in transient cerebral ischemia. Stroke, 2001, 32(10):2376–2381.
- Adibhatla R.M. Citicoline in stroke and TBI clinical trials. Nat Rev Neurol., 2013, 9: 173.
- Agnoli A., Bruno G., Fioravanti M. Therapeutic Approach to Senile Memory Impairment: A Double-Blind Clinical Trial with CDP Choline, Alzheimer’s Disease: Proceedings of the 5th Meeting of the Interna-tional Study Group on the Pharmacology of Memory Disorders Associated with Aging, Birkhauser, Boston, 1989.
- Agut J., Ortiz J., Wurtman R. Cytidine (5')Di- phosphocholine Modulates Dopamine K(+)-Evoked Re-lease in Striatum Measured by Microdialysis,” Annals of the New York Academy of Sciences, 2000, 920: 332- 335.
- Aniruddha T.J., Pillai S., Devi B.I. et al. Role of citicoline in the management of mild head injury. Indian J Neurotrauma, 2009, 6:49-52.
- Babb S.M. et al. Differential Effect of CDP-Choline on Brain Cytosolic Choline Levels in Younger and Older Subjects as Measured by Proton Magnetic Resonance Spectroscopy, Psychopharmacology, 1996, 127, 2: 88-94.
- Babb S.M. et al. Chronic Citicoline Increases Phos-phodiesters in the Brains of Healthy Older Subjects: An in Vivo Phosphorus Magnetic Resonance Spectroscopy Study, Psychopharmacology, 2002, 161, 3: 248-254.
- Baker L. Effects of dietary constituents on cognitive and motor skill performance in sports. Sports Science Exchange, 2013, 26, 119: 1-6.
- Barrachina M., Dominguez I., Ambrosio S. et al. Neuroprotective effect of citicoline in 6-hydroxydopamine-lesioned rats and in 6-hydroxydopamine-treated SH-SY5Y human neuroblastoma cells. J.Neurol.Sci., 2003, 215(1–2):105–110.
- Baskaya M.K., Dogan A., Rao A.M., Dempsey, R.J. Neuroprotective effects of citicoline on brain edema and blood-brain barrier breakdown after traumatic brain injury. J. Neurosurg., 2000, 92: 448–452.
- Baugh Ch.M., Stamm J.M., Riley D.O. et al. Chronic traumatic encephalopathy: neurodegeneration following repetitive concussive and subconcussive brain trauma. Brain Imaging and Behavior, 2012, DOI 10.1007/s11682-012-9164-5.
- Bellar D.М., LeBlanc N.R., Campbell B. The effect of 6 days of alpha glycerylphosphorylcholine on isometric strength. J.Intern.Soc.Sports Nutr., 2015, 12:42-48.
- Blokland A., Honig W., Browns F., Jolles J. Cognition-enhancing properties of subchronic phosphatidylserine (ps) treatment in middle-aged rats: comparision of bovine cortex ps with eggs ps and soybean ps. Nutrition,1999, 15:778-783.
- Brownawell A.M., Carmines E.L., Montesano F. Safety assessment of AGPC as a food ingredient. Food Chem. Toxicol., 2011, 49(6):1303–1315.
- Calatayud Maldonado V., Calatayud Perez J.B., Aso Escario J. Effects of CDP-choline on the recovery of patients with head injury. J. Neurol. Sci., 1991, 103(Suppl.): S15–S18.
- Cano-Cuenca N., Solís-García del Pozo J., Jordán J. Citicoline efficiency on cognitive function: A systematic review. J Aging Res. Clin. Practice, 2015, 4(4):240-246.
- Cohadon F., Richer E., Poletto B. (). [A precursor of phospholipids in the treatment of severe traumatic comas]. Neurochirurgie, 1982, 28: 287–290.
- Conant R., Schauss A.G. Therapeutic Applications of Citicoline for Stroke and Cognitive Dysfunction in the Elderly: A Review of the Literature, Alternative Medi-cine Review, 2004, 9, 1: 17-31.
- Dacaranhe C.D., Terao J. A unique antioxidant activity of phosphatidylserine on iron-induced lipid peroxidation of phospholipid bilayers. Lipids, 2001, 36:1105-1110.
- Davalos A., Secades J. Citicoline Preclinical and Clinical Update 2009-2010, Stroke, 2011, 42, 1: S36-S39.
- De la Cruz J. P., Pavia J., Gonzalez-Correa J. A. et al. Effects of chronic administration of s-adenosyl-l-methionine on brain oxidative stress in rats. Naunyn-Schmiedebergs Archives of Pharmacology, 2000, 361(1):47–52.
- Dempsey R.J., Raghavendra Rao V.L. Cytidinediphosphocholine treatment to decrease traumatic brain injuryinduced hippocampal neuronal death, cortical contusion volume, and neurological dysfunction in rats. J. Neurosurg., 2003, 98: 867–873.
- Dixon C.E., Ma X., Marion D.W. Effects of CDPcholine treatment on neurobehavioral deficits after TBI and on hippocampal and neocortical acetylcholine release. J. Neurotrauma, 1997, 14: 161–169.
- Erdman J., Oria M., Pillsbury L. Nutrition and Traumatic Brain Injury. Improving Acute and Subacute Health Outcomes in Military Personnel. The National Acad.Press, Washington, 2011.
- Espagno J., Tremoulet M., Gigaud M., Espagno Ch. Etude de l’action de la CDPcholine dans les troubles de la vigilance post-traumatique. La Vie Médicale,1979, 3: 195-196.
- Essig D., Costill D.L., Van Handel P.J. Effects of caffeine ingestion on utilisation of muscle glycogen and lipid during leg ergometer exercise. Int.J.Sports Med., 1980, 1:86-90.
- Fahey T.D., Pearl M.S. The Hormonal and Perceptive effects of phosphatidylserine administrtion during twо weeks of resistive exercise induced overtraining. Biology of sport, 1998,15:136-144.
- Fredholm B.B., Battig K., Holmen J., Nehlig A., Zvartau E.E. Actions of caffeine in the brain with special reference to factors that contribute to its widespread use. Pharmacol.Rev., 1999, 51:83-133.
- Goldstein E.R., Ziegenfuss T., Kalman D. et al. International society of sports nutrition position stand: caffeine and performance. J.Intern.Soc.Sports Nutr., 2010, 7:5-20.
- Grossman A., Sutton J.R. Endorphins: What are they? How are they measured? What is their role in exercise?. Med.Sci.Sports Exerc., 1985,17:74-81.
- Gundert-Remy U. Pharmacokinetic and Pharmacodynamic Effects of Caffeine. EFSA Stakeholders Meeting on the safety of caffeine. Brussels, 5 March 2015.
- Hirsch M.J., Growdon J.H., Wurtman R.J. Relations between dietary choline or lecithin intake, serum choline levels, and various metabolic indices. Metabolism, 1978, 27:953-960.
- Hoffman J.R., Ratamess N.A., Gonzalez A. et al. The effects of acute and prolonged CRAM supplementation on reaction time and subjective measures of focus and alertness in healthy college student. J. Int. Soc. Sport Nutr., 2010,7:39-47.
- Huynh M.L., Fadok V.A., Henson P.M. Phosphatidylserine-dependent ingestion of apoptotic cells promotes tgf-β1 secretion and the resolution of inflammation. J.Clin.Invest., 2002, 109:41-50.
- Jäger R., Purpura M., Geiss K-R. et al. The effect of phosphatidylserine on golf performance. J.Intern.Soc.Sports Nutr., 2007, 4:23-28.
- Jajim A.R., Wright G., Schultz K. et al. Effects of acute ingestion of a mult-ingredient pre-workout supplement on lower body power and anaerobic sprint performance. J.Int.Soc.Sport Nutr., 2015, 12 Suppl 1:49.
- Kamimori G.H., Karyekar C.S., Otterstetter R et al: The rate of absorption and relative bioavailability of caffeine administered in chewing gum versus capsules to normal healthy volunteers. Int.J.Pharm., 2002, 234:159-167.
- Kato-Kataoka A., Sakai M., Ebina R. et al. Soybean-Derived Phosphatidylserine Improves Memory Function of the Elderly Japanese Subjects with Memory Complaints. J. Clin. Biochem. Nutr., 47, 246–255.
- Kingsley M., Wadsworth D., Kilduff L.P. et al. Effects of phosphatidylserine on oxidative stress following intermittent running. Med.Sci.Sports Exerc., 2005, 37:1300-1306.
- Kingsley M., Miller M., Kilduff L.P., McEneny J. Benton D: Effects of phosphatidylserine on exercise capacity during cycling in active males. Med.Sci.Sports Exerc., 2006, 38:64-71.
- Kingsley M., Kilduff L.P., McEneny J. et al. Phosphatidylserine supplementation and recovery following downhill running. Med.Sci.Sports Exerc., 2006, 38:1617-1625.
- Krupinski J., Ferrer I., Barrachina M. et al. CDP-choline reduces procaspase and cleaved caspase-3 expression, nuclear DNA fragmentation, and specific PARP-cleaved products of caspase activation following middle cerebral artery occlusion in the rat. Neuropharmacology, 2002, 42(6):846–854.
- Lactorraca S., Piersanti P., Tesco G. et al. Effect of phosphatidylserine on free radical susceptibility in human diploid fibroblasts. J.Neural.Transm.Park Dis.Dement.Sect., 1993, 6:73 77.
- Laurent D., Schneider K.E., Prusaczyk W.K. et al. Effects of caffeine on muscle glycogen utilization and the neuroendocrine axis during exercise. J.Clin.Endocrinol.Metab., 2000, 85:2170-175.
- Lecuire J., Duplay J. Double-blind trial of citicoline versus meclofenossato in patients with head injury. Giorn. Ital. Searches Clin. Terapeut., 1982, 3: 51-55.
- Lecuire J. Traumatismes craniens: Etude comparative Piracetam- CDPcholine. C R Ther. Pharmacol. Clin., 1985, 3: 3-7.
- Leon-Carrion J., Dominguez-Roldan J.M., Murillo-Cabezas, F. et al. The role of citicoline in neuropsychological training after traumatic brain injury. NeuroRehabilitation, 2000, 14:33–40.
- Levin H.S. (1991). Treatment of postconcussional symptoms with CDP-choline. J. Neurol. Sci., 1991, 103(Suppl.), S39–S42.
- Lin A., Ramadan S., Box, H. et al. Neurochemical changes in athletes with chronic traumatic encephalopathy. Chicago: Radiological Society of North America. 2010.
- Lozano R. CDP-choline in the treatment of cranio-encephalic traumata. J. Neurol. Sci., 1991, 103 Suppl: S43-47.
- Luo Y., Smith J., Paramasivam V. et al. Inhibition of amyloid-beta aggregation and caspase-3 activation by the Ginkgo biloba extract EGb761. Proc. Natl. Acad. Sci. USA 99? 2002: 12197-12202.
- Martinez N., Campbell B., Franek M. et al. The effect of acute pre-workout supplementation on power and strength performance. J.Intern.Soc.Sports Nutr., 2016, 13:29-36.
- McGlade E., Locatelli A., Hardy J. et al. Improved Attentional Performance Following Citicoline Administration in Healthy Adult Women. Food and Nutrition Sciences, 2012, 3, 769-773.
- McKee A. C., Cantu R. C., Nowinski C. J. et al. Chronic traumatic encephalopathy in athletes: progressive tauopathy after repetitive head injury. J.Neuropathol.Exper. Neurol., 2009, 68(7): 709–735.
- Meeusen R. Nutrition and neurogenesis. Sports Science Exchange (2015) 28, 149: 1-5.
- Ozay R. et al. Citicoline Improves Functional Recovery, Promotes Nerve Regeneration, and Reduces Postoperative Scarring after Peripheral Nerve Surgery in Rats. Surg. Neurol., 2007, 68, 6: 615-622.
- Mir C., Clotet J., Aledo R. et al. CDPcholine prevents glutamate-mediated cell death in cerebellar granule neurons. Journal of Molecular Neuroscience, 2003, 20(1):53–59.
- Misbach J., Andradi S., Harahap T.P. et al. Doubleblind trial of Nicholin (CDP-choline) on the patients with severe head injury. Biannual Meeting of Neurology, Psychiatry and Neurosurgery, Surabaya (Indonesia). 1978.
- Monteleone P., Beinat L., Tanzillo C. et al. Effects of phosphatidylserine on the neuroendocrine response to physical stress in humans. Neuroendocrinology, 1990, 52:243-248.
- Ogashiwa M., Sano K., Manaka S. et al.) Effectiveness of CDPcholine on disturbance of consciousness (DOC). Novel biochemical, pharmacological and clinical aspects of cytidinediphosphocholine. Elsevier Science Publ Co NY. 1985.
- Omalu B. I., DeKosky S. T., Minster R. L. et al. Chronic traumatic encephalopathy in a National Football League player. Neurosurgery, 2005, 57: 128–134.
- Omalu B. I., DeKosky S. T., Hamilton R. L. et al. Chronic traumatic encephalopathy in a national football league player: part II. Neurosurgery, 2006, 59:1086–1092.
- Parisi V. et al. Evidence of the Neuroprotective Role of Citicoline in Glaucoma Patients. Progress in Brain Research, 2008, 173: 541-554.
- Parker A.G., Byars A., Purpura M., Jäger R. The effect of alphaglycerylphosphorylcholine, caffeine or placebo on markers of mood, cognitive function, power, speed and agility. J.Int.Soc. Sport Nutr., 2015, 12 Suppl 1:41.
- Parnetti L., Mignini F., Tomassoni D. et al. Cholinergic precursors in the treatment of cognitive impairment of vascular origin: Ineffective or need for re-evalulation? J.Neuro.Sci., 2007, 257:264–269.
- Potgieter S. Sport nutrition: A review of the latest guidelines for exercise and sport nutrition from the American College of Sport Nutrition, the International Olympic Committee and the International Society for Sports Nutrition. S. Afr. J. Clin. Nutr., 2013, 26(1):6-16.
- Raggueneau J.L., Jarrige B. National Survey result in serious head injuries: Analysis of 219 injuries treated with CDP-choline [ National inquiry on the outcome of severe head injuries : analysis of 921 Injured Patients Treated with CDP-choline ]. Agressologie. 1988, 29: 439-443.
- Rejdak R., Toczolowski J., Solski, J. et al. Citicoline treatment increases retinal dopamine content in rabbits. Ophthalmic Res., 2002, 34: 146–149.
- Richer E., Cohadon F. Therapeutic trial of a precursor phospholipids on the treatment of severe traumatic comas. International Symposium: Suffering and cerebral phospholipid precursors Paris. Paris. 1980.
- Ross B.M., Mamalias N., Moszczynska A. et al. Elevated activity of phospholipid biosynthetic enzymes in substantia nigra of patients with Parkinson’s disease. Neuroscience, 2001, 102: 899–904.
- Scientific Opinion on the substantiation of health claims related to choline and contribution to normal lipid metabolism (ID 3186), maintenance of normal liver function (ID 1501), contribution to normal homocysteine metabolism (ID 3090), maintenance of normal neurological function (ID 1502), contribution to normal cognitive function (ID 1502), and brain and neurological development (ID 1503) pursuant to Article 13(1) of Regulation (EC) No 1924/2006», Parma, Italy. EFSA Journalб 2011б 9(4):2056-2079.
- Secades J.J., Frontera G. CDP-choline: pharmacological and clinical review. Methods Find. Exp. Clin. Pharmacol., 1995, 17(Suppl. B), 1–54.
- Secades J.J., Lorenzo J.L. Citicoline: Pharmacological and Clinical Review, 2006 Update. Methods & Findings in Experimental & Clinical Pharmacology, 2006, 28, Suppl. B: 1-56.
- Secades J.J. Citicoline for the Treatment of Head Injury: A Systematic Review and Meta-analysis of Controlled Clinical Trials. J. Trauma Treat., 2014, 4:1-4.
- Silveri M.M. et al. Citicoline Enhances Frontal Lobe Bioenergetics as Measured by Phosphorus Magnetic Resonance Spectroscopy,” NMR in Biomedicine, 2008, 21,10:1066-1075.
- Sokmen B., Armstrong L.E., Kraemer W.J. et al. Caffeine use in sports: Considerations for the athlete. J.Strength Cond.Res., 2008, 22:978-986.
- Smith A.E., Fukuda D.H., Kendall K.L., Stout J.R. The effects of a pre-workout supplement containing caffeine, creatine, and amino acids during three weeks of high-intensity exercise on aerobic and anaerobic performance. J.Intern.Soc.Sports Nutr., 2010, 7:10-21.
- Spriet L.L., MacLean D.A., Dyck D.J. et al. Caffeine ingestion and muscle metabolism during prolonged exercise in humans. Am.J.Physiol., 1992, 262:E891-898.
- Spriet L.L., Gibala M.J. Nutritional strategies to influence adaptations to training. J.Sports Sci., 2004, 22:127-141.
- Starks M.A., Starks S.L., Kingsley M. et al. The effects of phosphotidylserine on endocrine response to moderate intensity exercise. J. Inter. Soc. Sports Nutr., 2008, 5:11.
- Teekachunhatean S., Tosri N., Rojanasthien N. Pharmacokinetics of Caffeine following a Single Administration of Coffee Enema versus Oral Coffee Consumption in Healthy Male Subjects. ISRN Pharmacology, 2013, Article ID 147238, 7 pages.
- Traini E., Bramanti V., Amenta F. Choline alphoscerate (alpha-glycerylphosphorylcholine) and old choline-containing phospholipid with a still interesting profile as cognition enhancing agent. Curr Alzheimer Res., 2013,10(10):1070–1079.
- Ulus I.H. et al. Choline Increases Acetylcholine Re-lease and Protects against the Stimulation-Induced De-crease in Phosphatide Levels within Membranes of Rat Corpus Striatum, Brain Research, 1989, 484, 1-2: 217-227.
- WADA: The world anti-doping code international standard. Prohibited list. Jan. 2017.
- Williams M.H. Dietary Supplements and Sports Performance: Introduction and Vitamins. J. Intern. Soc.Sports Nutr., 2004, 1(2):1-6.
- Wurtman R.J., Hirsch M.J., Growdon J.H. Lecithin consumption raises serumfree-choline levels. Lancet, 1977, 2:68-69.
- Wurtman R. J., Regan M., Ulus I., Yu L. Effect of Oral CDP-Choline on Plasma Choline and Uridine Levels in Humans. Biochemical Pharmacology, 2000, 60, 7: 989- 992.
- Zafonte R., Friedewald W.T., Lee S.M. et al. The Citicoline Brain Injury Treatment (COBRIT) Trial: Design and Methods. J.Neurotrauma, 2009, 26:2207–2216.
- Zafonte R.D., Bagiella E., Ansel B.M. et al. Effect of citicoline on functional and cognitive status among patients with traumatic brain injury: Citicoline Brain Injury Treatment Trial (COBRIT). JAMA, 2012, 308(19):1993-2000.
- Ziegenfuss T., Landis J, Hofheins J: Acute supplementation with alpha glycerylphosphorylcholine augments growth hormone response to, and peak force production during, resistance exercise. J Int Soc Sports Nutr., 2008, 5(Suppl 1):P15.
- Zeisel S.H. A brief history of choline. Ann.Nutr.Metab., 2012, 61(3):254–258.