Функции почек
Содержание
Почки. Солевой и водный баланс[править | править код]
Функции[править | править код]
Почки регулируют выведение из организма воды и солей с целью поддержания постоянного объема внеклеточной жидкости и осмоляльности, помогают поддерживать кислотно-основной гомеостаз; удаляют конечные продукты метаболизма и чужеродные вещества; предотвращают выведение полезных веществ (например, глюкозы) путем реабсорбции; продуцируют гормоны (например, эритропоэтин) и активаторы гормонов (ренин); выполняют метаболические функции (катаболизм белков и пептидов, глюконеогенез и т. д.).
Экскреция органических веществ[править | править код]
Пища поставляет необходимые питательные вещества, но в ней есть и вредные компоненты. Организм обычно способен отсортировать их сразу же во время еды по запаху и вкусу, или, если они уже съедены, путем расщепления специфическими ферментами и с помощью абсорбирующих механизмов в кишечнике (например, D-глюкоза и (.-аминокислоты всасываются, а D-аминокислоты и L-глюкоза нет). Похожие механизмы работают и при выведении через печень (желчь - стул): полезные желчные кислоты почти полностью всасываются в кишечнике при помощи специальных транспортеров, тогда как отходы метаболизма, такие как билирубин, в основном удаляются с фекалиями. Подобным же образом, почки плохо реабсорбируют все бесполезные или вредные вещества (включая конечные продукты, например креатинин). Важные же вещества (такие как D-глюкоза и L-аминокислоты) реабсорбируются при помощи специальных транспортеров и, таким образом, избегают экскреции.
Печень и почки также способны модифицировать эндогенные отходы и инородные компоненты (ксенобиотики), лишая их токсичности (если они токсичны) и подготавливая их к быстрому выведению. В незаряженной форме или после ферментативного присоединения групп ОН или СООН эти вещества объединяются с глюкуроновой кислотой, сульфатом, ацетатом или глутатионом и формируют конъюгаты. Конъюгированные вещества затем секретируются в желчь и в просвет проксимальных канальцев (с дальнейшей метаболической обработкой или без таковой).
Канальцевая секреция[править | править код]
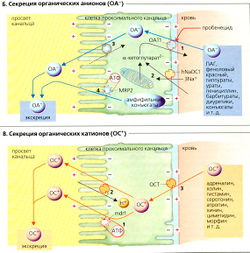
Проксимальные канальцы используют механизмы активного транспорта для секреции многочисленных отходов и ксенобиотиков. Это осуществляется при помощи переносчиков органических анионов (ОА-) и органических катионов (ОС+). Секреция этих веществ позволяет поднять их клиренс выше клиренса инулина и, таким образом, увеличить их фракцию экскреции (ФЭ) выше 1 (100%) для более эффективного удаления (А, ср. красную и синюю кривые). Секреция осуществляется переносчиками и, следовательно, подчиняется кинетике насыщения. В отличие от реабсорбируемых веществ, таких как D-глюкоза, фракция экскреции органических анионов и катионов снижается с ростом их концентрации в плазме (А, кривая секреции ПАГ достигает плато, а наклон кривой экскреции ПАГ снижается). Некоторые органические анионы (например, ураты и оксалаты) и катионы (например, холин) и секретируются, и реабсорбируются (двунаправленный транспорт), что приводит к суммарной реабсорбции (ураты, холин) или секреции (оксалаты).
К секретируемым органическим анионам (OА~) относятся индикаторы, такие как ПАГ (л-аминогиппурат) и феноловый красный; эндогенные вещества, такие как ураты, оксалаты, гиппураты; лекарства: пенициллин G, барбитураты и многочисленные диуретики; а также конъюгированные вещества (см. выше), содержащие глюкуронат, сульфат или глутатион. Пробенецид, по причине большой аффинности к транспортным системам, является потенциальным ингибитором секреции 0А~.
Активная стадия секреции ОА- (Б) осуществляется через базолатеральную мембрану клеток проксимальных канальцев и аккумулирует в клетках органические анионы, чтобы преодолеть отрицательный внутренний потенциал. Мембрана имеет переносчик с широкой специфичностью (ОАТ1 - транспортер органических анионов 1-го типа), который транспортирует ОА- из крови в клетки канальцев в обмен на дикарбоксилат, например сукцинат2- или а-кетоглуторат2- (Б1). Последнее вещество происходит из клеточного метаболизма глутамина; переносчик Na+-дикарбоксилата у человека hNADC-1 также проводит дикарбоксилат (вместе с 3Na+) в клетку путем вторичного активного транспорта (Б2). Поэтому транспорт ОА- называется третичным активным транспортом. Выход ОА- в просвет канальца происходит пассивно (облегченная диффузия; БЗ). Для секреции амфифильных конъюгатов, таких как связанные с глутатионом липофильные токсины, также используется АТФ-зависимый конъюгатный насос (MRP2 = белок, отвечающий за мультимедикаментозную резистентность 2-го типа) в мембране просвета канальцев (Б4).
К секретируемым органическим катионам (ВС+) относятся эндогенные вещества (адреналин, холин, гистамин, серотонин и т. д.) и лекарственные вещества (атропин, морфин, хинин и т. д.).
В противоположность секреции ОА- активная стадия секреции OС+ происходит через люминальную мембрану клеток проксимальных канальцев (аккумуляция в просвете происходит после преодоления отрицательного мембранного потенциала внутри клетки). Мембрана содержит: (а) прямые АТФ-зависимые переносчики органических катионов (mdr1; первичный активный транспорт 0С+; В1); (б) мультиспецифический антипортер OС+/Н+ (третичный активный транспорт; В2). Катионы OС+ пассивно диффундируют из крови в клетку при помощи мультиспецифического транспортера органических катионов ГОСТ; ВЗ).
Диурез и диуретики[править | править код]
Увеличение выделения мочи свыше 1 мл/мин (диурез) может иметь следующие причины:
- Водный диурез: Снижение осмоляльности плазмы и/или увеличение объема крови ведут к уменьшению уровня АДГ и, следовательно, к удалению «свободной воды» . * •
- Осмотический диурез происходит, когда в почечные канальцы попадает активное вещество, нереабсорбируемое осмотически (например, маннит). Эти вещества удерживают воду в просвете канальца, после чего она выводится. Осмотический диурез может также иметь место в том случае, если концентрация реабсорбируемого вещества (например, глюкозы) превышает абсорбционную емкость канальцев, что приводит к гипергликемии. Глюкозурия при сахарном диабете, следовательно, сопровождается диурезом и вторичным увеличением жажды. Гипербикарбонатурия по этой же причине может приводить к осмотическому диурезу.
- Прессорный диурез развивается в том случае, если осмоляльность в мозговом веществе почки снижается при увеличении кровотока, что имеет место чаще всего при повышенном кровяном давлении.
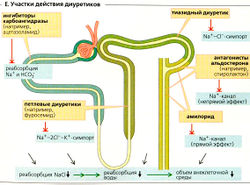
- Диуретики (Е) - это лекарства, индуцирующие диурез. Большинство из них (кроме осмотических диуретиков наподобие маннита) действует в основном путем ингибирования реабсорбции NaCI (салуретики) и уже потом путем снижения реабсорбции воды. Терапия диуретиками, например, при лечении отеков и повышенного давления вызывает понижение объема внеклеточной жидкости.
Несмотря на то что диуретики в основном ингибируют транспорт NaCI по всему телу, они имеют большую почечную «специфичность», поскольку действуют из просвета канальцев, где становятся очень концентрированными благодаря секреции и реабсорбции воды в канальцах. Таким образом, дозировки, не вызывающие нежелательных системных эффектов, являются терапевтически эффективными в просвете канальцев.
Диуретики типа ингибиторов карбоангидразы (например, ацетазоламид, бензоламид) снижают обмен Na+/H+ и реабсорбцию HCO3 в проксимальных канальцах. Степень развивающегося диуреза незначительна, поскольку дистальные сегменты канальцев реабсорбируют NaCI, не реабсорбируемый выше, а также потому, что происходит снижение СКФ благодаря канальцево-клубочковой обратной связи. В добавление к этому, повышенная экскреция HCO3 также ведет к нереспираторному (метаболическому) ацидозу. Следовательно, этот тип диуретиков используется только для пациентов с сопутствующим алкалозом.
Петлевые диуретики (например, фуросемид и буметанид) высокоэффективны. Они ингибируют буметанидчувствительный котранспортер BSC, Na+-2К+-симпорт-переносчик в толстом сегменте восходящего колена (ТСВК) петли Генле. Это не только снижает реабсорбцию NaCI, но также блокирует «мотор» механизма концентрирования мочи. Поскольку положительный люминальный трансэпителиальный потенциал (ЛПТП) в ТСВК падает, парацеллюляр-ная реабсорбция Na+, Са2+ и Мg2+ также ингибируется. Так как количество нереабсорбируемого Na+, поступающего в собирательную трубочку, увеличивается, секреция К+ растет, одновременная потеря Н+ ведет к гипокалиемии и гипокалиемическому алкалозу.
Петлевые диуретики ингибируют BSC в плотном пятне, таким образом «обманывая» юкстагломерулярный аппарат (ЮГА), заставляя его «поверить», что в просвете канальцев нет больше NaCI. Затем СКФ увеличивается по механизму канальцево-клубочковой обратной связи, что, в свою очередь, вызывает диурез.
Тиазидные диуретики ингибируют резорбцию в дистальных канальцах. Подобно петлевым диуретикам, они увеличивают реабсорбцию в нижних сегментах канальцев, что приводит к потерям К+ и Н+.
Калийсберегающие диуретики. Амилорид блокирует Na+-каналы в главных клетках соединительных канальцев и собирательной трубочки, что ведет к уменьшению выделения К+. Антагонисты альдостерона (например, спиролактон), которые блокируют цитоплазматические рецепторы альдостерона, также оказывают калийсберегающий эффект.
Тубулогломерулярная обратная связь, ренин-ангиотензиновая система[править | править код]
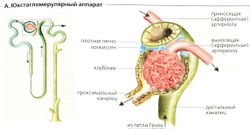
Юкстагломерулярный аппарат (ЮГА) состоит из (а) юкстагломерулярных клеток приносящей артериолы (включая ренинсодержащие и симпатически иннервируемые гранулярные клетки) и выносящей артериолы, (б) клеток плотного пятна толстого сегмента восходящего колена петли Генле и (в) юкстагломерулярных мезангиальных клеток (полкиссен, А) нефрона (А).
Функции ЮГА: (1) локальное проведение тубулогло-мерулярной обратной связи (механизм саморегуляции) в своем собственном нефроне при помощи ангиотензина II (ATII) и (2) системная продукция ангиотензина II как части ренин-ангиотензиновой системы (РАС).
Тубулогломерулярная обратная связь (механизм саморегуляции). Поскольку через почки ежедневно проходит в 10 раз больше жидкости, чем общий объем внеклеточной жидкости, выведение воды и соли должно точно соответствовать их поглощению. Резкие изменения в СКФ отдельного нефрона (СФН) и количества NaCI, фильтруемого в единицу времени, могут происходить по нескольким причинам. Повышение значения СФН ассоциируется с риском того, что дистальные механизмы реабсорбции NaCI перегружены, и слишком много NaCI и НгО будет потеряно с мочой. Заниженный показатель СФН означает, что слишком много NaCI и НдО удерживается. Степень реабсорбции NaCI и Н2О в проксимальных канальцах определяет, как быстро канальцевая моча проходит по петле Генле. Когда меньшее количество абсорбируется в верхней части, моча быстрее проходит по толстому сегменту восходящего колена петли, что приводит к уменьшению степени разбавления мочи и большей концентрации NaCI в плотном пятне, [NaCI]MD. Если величина [NaCI]MD становится слишком большой, гладкие мышцы стенки приносящей артериолы сокращаются, чтобы не изменилась СКФ через данный нефрон в течение 10 с, и наоборот (отрицательная обратная связь). Механизм регуляции неясен, но рецепторы ангиотензина II типа 1А (АТ1A) играют в этом ведущую роль.
Однако, если изменения [NaCI]MD обусловлены хроническими изменениями общего количества NaCI в организме и связанными с этим изменениями объема внеклеточной жидкости через механизм саморегуляции (обратной связи), нарушения зависимости СФН от [NaCI]MD могут иметь фатальные последствия. Поскольку увеличение в течение длительного времени объема внеклеточной жидкости уменьшает реабсорбцию NaCI в проксимальных канальцах, [NaCl]MD будет возрастать, приводя к снижению СКФ и дальнейшему увеличению объема внеклеточной жидкости. В обратной ситуации объем внеклеточной жидкости уменьшается. Для предотвращения таких эффектов зависимость [NaCl]MD/СФН может быть смещена в соответствующем направлении с помощью определенных веществ. Оксид азота (N0) смещает кривую при увеличении объема внеклеточной жидкости (увеличение СФН при прежнем значении [NaCI]MD), а (только локально эффективный) ангиотензин II сдвигает кривую в противоположном направлении при уменьшении объема.
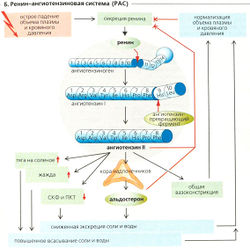
Ренин-ангиотензиновая система (РАС). Если среднее артериальное давление в почках внезапно падает ниже 90 мм рт. ст., почечные барорецепторы запускают высвобождение ренина, таким образом увеличивая общую концентрацию ренина в плазме. Ренин - это пептидаза, которая катализирует отщепление ангиотензина от субстрата ренина ангио-тензиногена (выделяемого печенью). Примерно через 30-60 мин после падения артериального давления ангиотензинпревращающий фермент (АПФ), который синтезируется в легких и других органах, отщепляет две аминокислоты от ангиотензина I с образованием ангиотензина II (Б).
Регуляция РАС (Б). Порог артериального давления для высвобождения ренина увеличивается при помощи а1-адренорецепторов, а базальная секреция ренина увеличивается при помощи бета1-адренорецепторов. Ангиотензин II и альдостерон являются наиболее важными эффекторами РАС. Ангиотензин II стимулирует высвобождение альдостерона корой надпочечников (см. далее). Оба гормона прямо (срочное действие) или косвенно (отложенное действие) ведут к новому увеличению артериального давления (Б), и высвобождение ренина, таким образом, снижается до нормы. Кроме того, оба гормона ингибируют высвобождение ренина (отрицательная обратная связь).
Если средний кровоток снижается только в одной почке (например, в результате стеноза поврежденной почечной артерии), то поврежденная почка начинает высвобождать больше ренина, что, в свою очередь, приводит к почечной гипертензии в остальной системе кровообращения.
Эффекты ангиотензина II. Помимо действия на миокард и кровеносные сосуды (в основном посредством АТд-рецепторов), ангиотензин II имеет следующие срочные или отложенные эффекты, опосредованные рецепторами АТ1 (А).
- Сосуды. Ангиотензин II имеет потенциальное вазоконст-рикторное и гипертензивное действие, что (посредством эндотелина) влияет на артериолы (срочное действие).
- ЦНС. Ангиотензин II оказывает действие на гипоталамус, что приводит (через циркуляторный центр) к вазоконст-рикции (быстрое действие). Он также увеличивает секрецию АДГ в гипоталамусе, что стимулирует жажду и потребность в соли (отложенное действие).
- Почки. Ангиотензин II играет основную роль в регуляции почечного кровообращения и СКФ путем сужения приносящих и/или выносящих артериол (отложенное действие, ср. саморегуляция). Он прямо стимулирует реабсорбцию Na+ в проксимальных канальцах (отложенное действие).
- Надпочечники. Ангиотензин II стимулирует синтез альдостерона в коре надпочечников (отложенное действие) и ведет к высвобождению адреналина в мозговом веществе надпочечников (срочное действие).