Физиология сердца и сердечно-сосудистой системы
Содержание
- 1 Сердечно-сосудистая система
- 2 Кровеносные сосуды и кровоток
- 3 Сердечный цикл
- 4 Генерация и проведение сердечного импульса
- 5 Зависимость «давление-объем» для желудочков сердца
- 6 Регуляция ударного объема
- 7 Венозный возврат
- 8 Обменные процессы в эндотелии
- 9 Гипертензия
- 10 Циркуляторный шок
- 11 Кровообращение в организме плода и новорожденного
- 12 Читайте также
Сердечно-сосудистая система[править | править код]
Общие сведения[править | править код]
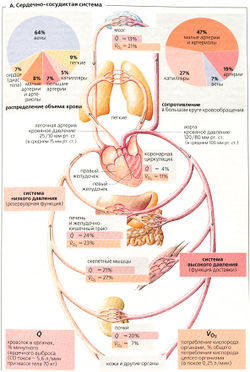
Кровь выталкивается из левого желудочка, по артериям системного (или большого) круга кровообращения поступает в капиллярное (микроциркулярное, терминальное) русло периферической сети и возвращается по венам в правое предсердие. Далее она выталкивается из правого желудочка в легочный (или малый) круг кровообращения, откуда возвращается в левый желудочек (А).
Общий объем крови составляет примерно 4-5 л (—7% массы тела, не считая жировых тканей). Около 80% крови циркулирует по венам, правому сердцу и легочным сосудам, которые называются системой низкого давления (А, справа). Эти очень эластичные емкостные сосуды служат резервуарами крови, где кровь хранится и высвобождается в случае необходимости при помощи венозной вазоконстрикции. Когда объем крови увеличивается, например, при переливании крови, более 99% объема донорской крови остается в системе низкого давления (высокоемкостная система) и только менее 1 % циркулирует в артериальной системе высокого давления (низкоемкостная система). И наоборот, снижение объема крови отразится в первую очередь на запасах крови в системе низкого давления. Центральное венозное давление (в правом предсердии или вблизи него 4-12 см вод. ст.), у людей с нормально работающими легкими и сердцем является удобным показателем для оценки объема крови (и объема внеклеточной жидкости).
Минутный сердечный выброс (или объем, СО). Минутный сердечный выброс вычисляется как произведение сердечного ритма (СР) и ударного объема (УО). В покое СО в норме составляет примерно 70 [мин-1] • 0,08 [л] = 5,6 л/мин, или, точнее, в среднем 3,4 л/мин на м2 поверхности тела (сердечный индекс). Увеличение СР (до 180 мин-1) и/или УО может увеличить СО до 15-20 л/мин.
Распределение крови по организму происходит в большом круге кровообращения единовременно (А, величина О) и определяется функциональной приоритетностью органов (жизненно важные органы) и текущими потребностями организма. Поддержание необходимого кровоснабжения мозга (примерно 13 % СО покоя) является самым главным приоритетом не только потому, что мозг- главный жизненно важный орган, но и потому, что он очень чувствителен к гипоксическим повреждениям. Важное значение имеет также перфузия миокарда коронарными артериями (примерно 4% СО покоя), поскольку любые нарушения насосной функции сердца подвергают опасности всю систему кровообращения. Примерно 20-25% СО распределяется между почками. Это очень много, если принять во внимание малую массу почек (только 0,5% массы тела). Почечный кровоток в основном используется для поддержания экскреторной (выделительной) и регуляторной функций почек. Поэтому в почках кровоток может быть временно снижен в пользу кровоснабжения сердца и мозга, например при угрозе шока. При интенсивной физической нагрузке СО увеличивается, и кровь распределяется в больших количествах по скелетным мышцам. При переваривании пищи достаточно большую фракцию СО забирает желудочно-кишечный тракт. Естественно, что все органы не могут получать слишком большой объем крови одновременно. Кровоток к коже (примерно 10% СО покоя) в основном служит для теплоотдачи. Кожный кровоток возрастает в ответ на увеличение выработки тепла организмом (физическая работа) и/или при высокой внешней температуре, а в некоторых случаях снижается (возникает бледность) в пользу жизненно важных органов (например, при шоке).
Весь СО проходит через легочный (малый) круг кровообращения, так как малый и большой круги кровообращения организованы последовательно (А). Бедная кислородом венозная кровь по легочным артериям поступает в легкие, где насыщается кислородом, т. е. «артериализуется». Сравнительно небольшое дополнительное количество насыщенной кислородом крови из большого круга кровообращения достигает легких через бронхиальную артерию. Вся кровь легочного круга кровообращения поступает в сердце по легочным венам.
Общее периферическое сопротивление. Сопротивление кровотока в легочном круге кровообращения составляет только 10% общего периферического сопротивления (ОПС) всех сосудов большого круга кровообращения. Поэтому среднее давление в правом желудочке (примерно 15 мм рт. ст. = 2 кПа) значительно ниже, чем в левом желудочке (100 мм рт. ст. = 13,3 кПа). Поскольку сопротивление в малых артериях и артериолах составляет около 50% ОПС (А, вверху справа), они называются резистивными сосудами.
Кровеносные сосуды и кровоток[править | править код]
В большом круге кровообращения кровь выталкивается из левого желудочка в аорту и возвращается в правое предсердие по полой вене (А). При этом среднее кровяное давление падает от 100 мм рт. ст. в аорте до 2-4 мм рт. ст. в полой вене [А2], что создает разницу давлений (ΔР) примерно в 97 мм рт. ст. (легочный круг кровообращения). По закону Ома,
ΔР (мм рт. ст.] = Q*R, [8.1]
где Q - интенсивность кровотока (мин • л-1), а R- сопротивление кровеносного русла (мм рт. ст. • л • мин-1]. Уравнение [8.1] можно использовать для расчета кровотока в конкретном органе [R - сопротивление органа), а также во всей кровеносной системе, где Q - минутный выброс (объем) сердца (СО) и R- общее периферическое сопротивление кровотока (ОПС). ОПС в покое составляет около 18 мм рт. ст. • мин • л-1.
Аорта и крупные артерии распределяют кровь по периферическим сосудам. При этом они выступают в роли компрессионных камер (амортизирующий эффект), поскольку (благодаря своей высокой эластичности, характеризуемой растяжимостью, ΔV/ΔPtm) они превращают пульсирующий ток крови от сердца в практически равномерный капиллярный кровоток. Высокое систолическое давление при выталкивании крови вызывает растяжение стенок этих эластических сосудов, и часть выталкиваемой крови «хранится» в расширенном просвете сосудов. Благодаря релаксации напряжения стенок сосудов после закрытия клапана аорты поддерживает кровоток во время диастолы. Эластичность (растяжимость) артериальных сосудов снижается с возрастом.
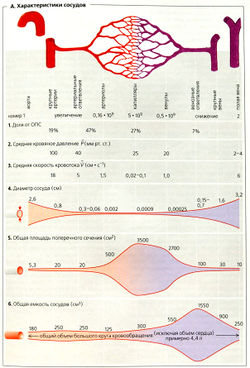
Скорость (V) и интенсивность (Q) кровотока. Площадь поперечного сечения аорты составляет 5,3 см2, общая площадь поперечного сечения всех артерий системы кровообращения - 20 см2 (А5), тогда среднюю скорость кровотока покоя V (во время систолы и диастолы) можно рассчитать из СО покоя (5,6 л/мин): средняя скорость кровотока равна 18 см/с в аорте и 5 см/с в артериях (АЗ). Так как аорта получает кровь только во время периода изгнания, максимальные значения покоя для 1? и 0 у корня аорты во время этого периода гораздо выше (V = 95 см/с, Q = 500 мл/с).
По уравнению Хагена-Пуазейля R = 8 • l • η/(π • r4) [8.2]
сопротивление потока [R] в трубке известной длины (l) зависит от вязкости (η) жидкости и внутреннего радиуса трубки в четвертой степени (г4).
Уменьшение радиуса всего на 16% достаточно для удвоения сопротивления.
Малые артерии и артериолы отвечают почти за 50% ОПС (резистивные сосуды, А1 ), поскольку их малый радиус имеет гораздо большее влияние на общее периферическое сопротивление (ОПС; R ~ 1/r4), чем их большое общее поперечное сечение ПСА (R ~ г2). Следовательно, в этих сосудах кровяное давление значительно снижается. Таким образом, любые изменения радиуса малых артерий и артериол имеют решающее влияние на ОПС. Их ширина (просвет), а также радиус прекапиллярного сфинктера определяют количество крови, попадающей в капиллярное русло (где и происходит газообмен).
Хотя капилляры имеют еще меньший радиус (и гораздо большее сопротивление, чем артериолы), их общий вклад в ОПС составляет лишь около 27%, поскольку их общее попереченое сечение очень велико (А1). Обмен жидкостью и растворенными веществами происходит через стенки капилляров и посткапиллярных венул. Оба этих типа сосудов хорошо подходят для этой задачи, так как (а) V в них очень мала (0,02-0,1 см/с; АЗ) (благодаря большой общей площади поперечного сечения), (б) они имеют очень большую общую площадь обменной поверхности (примерно 1000 м2), (в) их стенки могут быть очень тонкими, а внутренний радиус очень маленьким (4,5 мкм) (закон Лапласа, см. далее).
Трансмуральное (пристеночное) давление наполнения Pfm [Н/м2], т. е. разность давлений по разные стороны стенки полых органов (внутреннее давление минус внешнее давление), вызывает растяжение стенки. Материал эластической стенки, следовательно, должен быть способен противостоять этому растяжению. Результирующее (тангенциальное, пристеночное) трансмуральное давление Т [Н/м] является функцией внутреннего радиуса г [м] данного органа. По уравнению Лапласа для цилиндрических (или сферических) полых тел
Ptm = T/r (или Ptm = 2T w/r). [8.3а/б]
Здесь Т— общее трансмуральное (пристеночное) давление, которое не зависит от толщины стенки. При одном и том же Рtm толстая стенка более эффективна, чем тонкая. Для определения напряжения на единицу площади поперечного сечения стенки (требование к устойчивости ее материала, Н/м2) должна учитываться толщина стенки (w). Уравнение [8.3а/б], следовательно, преобразуется:
Ptm = T* w/r (или Ptm = 2T* w/r). [8.4а/б]
Кровь собирается в вены, которые могут накапливать большие объемы жидкости (АБ). Эти емкостные сосуды служат резервуарами крови.
Сердечный цикл[править | править код]
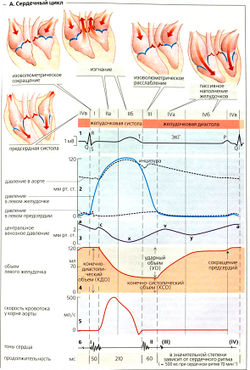
Сердечный ритм (СР) покоя составляет 60-80 ударов в минуту. Сердечный цикл (А], таким образом, занимает примерно 1 с. В сердечном цикле выделяют четыре периода (фазы): фаза I - изоволюметрического сокращения: фаза II - период изгнания (I и II происходят в систолу); фаза III - период изоволюметрического расслабления; фаза IV - период наполнения (III и IV происходят в диастолу). В конце IV фазы сокращаются предсердия (фаза IVb). Сокращению предшествует электрическое возбуждение предсердий и желудочков.
Сердечные клапаны определяют направление кровотока внутри сердца, например из предсердия в желудочек (фаза IV) или из желудочка в аорту или легочную артерию (фаза II). Все сердечные клапаны закрыты во время фаз I и III (А, вверху). Открывание и закрывание клапанов контролируется давлением с двух сторон клапана.
Сердечный цикл. К концу диастолы синоатриальный узел (СА-узел) желудочков испускает электрические импульсы - на ЭКГ начало зубца Р (фаза IVb, А1). Это приводит к сокращению предсердий (ДА), затем следует возбуждение желудочков (комплекс QRS) - давление в желудочках начинает расти (А2, синяя линия) до тех пор, пока не превысит предсердное давление, клапаны (митральный и трехстворчатый) закрываются сразу после предшествующей продуктивной фазы сердечных тонов. Это означает конец диастолы. Конечно-диастолический объем крови (КДО) в желудочке в среднем составляет около 120 мл (А4) или, более точно, 70 мл/м2 поверхности тела.
Вслед за этим начинается период изоволюмического сокращения (фаза I, примерно 50 мс). Желудочки теперь сокращаются при закрытых клапанах, производя первый тон сердца (А6) - давление в желудочках при этом быстро увеличивается. Наклон этой восходящей кривой давления дает максимальную скорость развития давления (максимум dP/dt). Полулунные клапаны (аорты и легочной вены) теперь открыты, поскольку давление в левом желудочке (А2, синяя линия) больше, чем в аорте (черная прерывистая кривая), примерно на 80 мм рт. ст., а давление в правом желудочке больше, чем в легочной артерии, примерно на 10 мм рт. ст.
Период изгнания (фаза II; в покое примерно 210 мс). Во время этой фазы давление в левом желудочке и аорте достигает максимума и составляет примерно 120 мм рт. ст. (систолическое давление). В начале периода изгнания (Па, или фазы быстрого изгнания) быстро выталкивается большая фракция ударного объема (УО) (А4) и кровоток достигает максимума (А5). Вслед за этим возбудимость миокарда снижается (зубец Т, А1), снижается также давление в желудочках (остающаяся фракция УО изгоняется медленно, фаза 116) до тех пор, пока не падает ниже давления в аорте или легочной артерии соответственно. Это ведет к закрыванию полулунных клапанов - второй сердечный тон (А6). Фракция УО покоя в среднем составляет 80 мл или, более точно, 47 мл/м2 поверхности тела. Фракция выброса (УО/КДО) покоя в среднем составляет 0,67. Конечно-систолический объем (КСО) крови, остающийся в желудочках к концу периода изгнания, составляет примерно 40 мл (А4).
Затем начинается первая фаза желудочковой диастолы, или изоволюмического расслабления (фаза III; примерно 60 мс). Предсердия тем временем наполняются, в основном благодаря засасывающему эффекту, создаваемому при опускании плоскости клапанов во время фазы изгнания. В результате центральное венозное давление (ЦВД) снижается (АЗ, падение от с до х). Желудочковое давление теперь быстро снижается, заставляя атриовентрикулярные клапаны опять открыться под действием недостаточного предсердного давления.
Вслед за этим начинается период наполнения (фаза IV; в покое примерно 500 мс). Кровь быстро переходит из предсердий в желудочки, что приводит к падению ЦВД (АЗ, точка у). Поскольку желудочки за первую четверть диастолы наполняются на 80%, эта фаза называется фазой быстрого желудочкового наполнения (IVa, А4). Желудочковое наполнение замедляется (фаза IV6), вслед за этим происходит систола предсердий (фаза IVb) и обратный пик ЦВД (А2,3). При нормальном сердечном ритме сокращение предсердий дает около 15% объема желудочков. Когда сердечный ритм возрастает, продолжительность сердечного цикла снижается в основном за счет диастолы, и вклад сокращения предсердий в наполнение желудочков увеличивается.
Биение сердца создает пульс (волны давления), который проходит по артериям с характерной скоростью пульса (СП): в аорте СП составляет 3-5 м/с, а в лучевой артерии - 5-12 м/с. СП гораздо выше скорости кровотока (РЭ, которая достигает пика в 1 м/с в аорте и увеличивается пропорционально (а) снижению эластичности (растяжимости) стенок аорты и артерий и (б) увеличению кровяного давления.
Генерация и проведение сердечного импульса[править | править код]
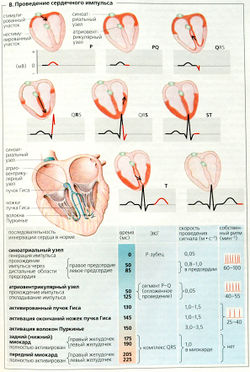
Сердце содержит мышечные клетки, которые генерируют электрические импульсы (клетки водителя ритма), проводят их (система проведения) и отвечают на эти стимулы [рабочий миокард). Сердечные импульсы генерируются внутри сердца (спонтанно; это свойство называется автоматизмом). Частота и регулярность работы клеток водителя ритма (пейсмекеров) тоже является (внутренним) свойством сердца (ритмические сокращения). Мышцы сердца (миокарда) образуют функциональный (не анатомический) синцитий, поскольку клетки соединены щелевыми контактами - вставочными дисками; так же осуществляется предсердно-желудочковый контакт. Импульс, возникающий в любом отделе сердца, ведет к полному сокращению обоих желудочков и предсердий или полному отсутствию сокращения (ответ по типу «все или ничего»).
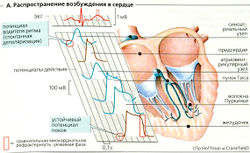
Сердечное сокращение в норме стимулируется импульсами синоатриального узла (СА-узла), который также называется водителем ритма первого порядка. Импульсы проводятся (А) через предсердие к предсердно-желудочковому (атриовентрикулярному) узлу (АВ-узлу). Пучок Гиса является началом специализированной проводящей системы, включающей также правую и левую ножки пучка Гиса и волокна Пуркинье, которые проводят импульсы далее в миокард желудочков, где эти импульсы перемещаются изнутри наружу и от вершины к основанию сердца. Эту электрическую активность можно регистрировать in vivo (В) - электрокардиограмма.
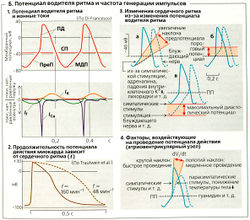
Потенциал водителя ритма (Б1, вверху). Клеточный потенциал СА-узла называется потенциалом водителя ритма. Эти клетки не имеют устойчивого потенциала покоя. Вместо этого, они медленно деполяризуются сразу после каждой реполяризации, наиболее отрицательное значение которой называется максимальным диастолическим потенциалом (МДП, примерно -70 мВ). Медленная диастолическая деполяризация, или предпотенциал (ПреП), преобладает до тех пор, пока снова не будет достигнут пороговый потенциал (ПП). Таким образом, запускается следующий потенциал действия (ПД).
Потенциал водителя ритма (Б1, внизу) подвергается разнообразным присущим ему изменениям ионной проводимости (g) и ионного тока (Л через плазматическую мембрану. Начинаясь с МДП, запускаемые гиперполяризацией увеличение ионселективной проводимости и приток катионов (//) в клетки ведут к медленной деполяризации (ПреП). По достижении ПП быстро растет gCа и наклон потенциала водителя ритма увеличивается, что вызывается усилением притока Са2+ (ICа). Когда потенциал доходит до положительных значений, резко возрастает, что приводит к притоку К+ (IK), и клетки водителя ритма реполяризуются до МДП.
Каждый потенциал действия в синоатриальном узле обычно генерирует один удар сердца. Сердечный ритм, следовательно, определяется частотой генерации импульсов водителя ритма. Частота генерации импульсов снижается (БЗ, прерывистая линия), если (а) уменьшается наклон ПреП (БЗа); (б) ПП становится менее отрицательным (БЗб); (в) МДП становится более отрицательным, что приводит к началу спонтанной деполяризации нижних (более удаленных, дистальных) уровней проводящей системы (БЗв); (г) реполяризация после потенциала действия происходит медленнее (наклон становится более пологим).
Первые три условия увеличивают время, необходимое для достижения порогового потенциала (ПП).
Все компоненты проводящей системы могут деполяризоваться спонтанно, но синоатриальный узел является естественным, или номотопным (нормально расположенным), водителем ритма (синусовый ритм обычно составляет от 60 до 100 мин-1). Собственный ритм других водителей медленнее, чем синусовый ритм, поскольку наклон их ПреП и реполяризация более пологие (см. выше). Потенциал действия, возникающий в синоатриальном узле, наступает, следовательно, на более удаленных (более низких) уровнях проводящей системы до того, как спонтанная деполяризация достигает ПП. Собственный ритм низших компонентов проводящей системы [эктопические, или смещенные, водители ритма) начинает играть роль (а) при увеличении собственной частоты; (б) когда более быстрые водители ритма подавлены; (в) проводимость сино-атриального узла нарушена. Сердечные удары при атриовентрикулярном ритме (от 40 до 55 мин-1), или даже при более медленном ритме (от 25 до 40 мин-1), в этом случае контролируются (желудочковыми) водителями ритма третьего порядка.
Угнетение при перевозбуждении. Автоматизм клеток, более удаленных от водителей ритма (например, АВ-узла или волокон Пуркинье), временно подавляется после эксплуатации при высокой частоте сердечных сокращений. Это ведет к увеличенному притоку Na+ и, следовательно, к увеличению активности Na+-К+-АТФазы. Поскольку это электрогенный фермент, клетки гиперполяризуются, и для достижения порогового потенциала требуется больше времени, чем без предшествующего высокочастотного воздействия (БЗв).
Клетки рабочего миокарда содержат потенциалзависимые быстрые Na+-каналы, которые осуществляют кратковременный, но быстрый приток Na+ в начале потенциала действия. Наклон их потенциалов действия, таким образом, увеличивается быстрее, чем для потенциала водителя ритма (А). Потенциал покоя преобладает над потенциалом действия (ПД), т. е. в рабочем миокарде в норме спонтанная деполяризация не возникает. Длительный миокардиальный потенциал действия имеет характерное плато. Таким образом, участки миокарда, стимулируемые первыми, все еще находятся в стадии рефрактерности в тот момент, когда ПД достигает участков миокарда, получивших стимул в последнюю очередь. Это предотвращает циклическое наступление ПД в миокарде. Данное условие выполняется вне зависимости от того, является ли сердечный ритм быстрым или очень медленным, поскольку продолжительность ПД варьирует в соответствии с сердечным ритмом (Б2).
Роль Са2+. Наступающий ПД открывает потенциалзависимые Са2*-каналы (ассоциированные с дигид-ропиридиновыми рецепторами) в сарколемме клеток миокарда, запуская приток Са2+ из внеклеточного пространства. Это вызывает локальное увеличение цитоплазматической концентрации Са2+ (Сa2+-«вспышки»), что в свою очередь запускает открытие лигандзависимых, рианодинчувствительных Са2* -каналов в саркоплазматическом ретикулуме (депо Са2+). Приток Са2+ в цитоплазму приводит к электромеханическому сопряжению и сокращению миокарда. Концентрация Са2+ в цитоплазме определяется активным транспортом ионов Са2+ назад: (а) в депо Са2+ при помощи Са2+-АТФазы ISERCA), которая стимулируется фосфоламбаном, (б) во внеклеточное пространство. Это осуществляется с помощью Са2+-АТ-Фазы и обменника 3Na+/2Ca?+, который работает за счет электрохимического градиента Na+, устанавливаемого Na+-К+-АТФазой.
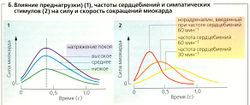
Несмотря на то что сердце сокращается автономно, существуют эфферентные сердечные нервы, отвечающие в основном за модуляцию сердечной деятельности в соответствии с меняющимися потребностями. Автономная нервная система (и адреналин в плазме] может воздействовать на следующие аспекты сердечной деятельности: (а] скорость генерации импульсов водителями ритма и, следовательно, сердечный ритм (хронотропное действие); (б) скорость проведения импульса, особенно в атриовентрикулярном узле (дромотропное действие);(в) сократимость сердца, т. е. силу сокращения сердечной мышцы при заданной начальной длине волокна (инотропное действие).
Эти изменения в работе сердца индуцируются ацетилхолином (АХ), высвобождаемым в парасимпатической нервной системе - в блуждающем нерве (связывается с Мg-холинорецепторами клеток водителя ритма), норадреналином (НА) в симпатической нервной системе и адреналином плазмы крови (А). НА и А связываются с -адренорецепторами. Частота запуска СА-узла увеличивается под действием НА и А (положительный хронотропный эффект) и снижается под действием АХ (отрицательный хронотропный эффект), так как эти вещества могут вызывать изменение наклона ПреП и МДП в клетках СА-узла (БЗа и в). Под влиянием АХ наклон ПреП становится меньше (уплощается), МДП становится более отрицательным, а растет. И обратно, наклон и амплитуда ПреП растут под влиянием А или симпатических стимулов (высокий If) благодаря росту катионной проводимости (Na+) и, при некоторых условиях, снижению дк. Только НА и А имеют хронотропные эффекты на проксимальные компоненты проводящей системы. От них зависит, будут ли участвовать в процессе атриовентрикулярный узел или водители ритма третьего порядка.
АХ (левая ветвь блуждающего нерва) снижает скорость проведения импульса в атриовентрикулярном узле, тогда как НА и А ее увеличивают благодаря отрицательному и положительному дромо-тропным эффектам соответственно. В основном это достигается через изменения амплитуды и наклона в конце ПД (БЗв и Б4), что вызывается изменениями проводимостей и дса.
При положительном инотропном эффекте НА и А воздействуют непосредственно на рабочий миокард. Результирующее увеличение сократимости основано на увеличении притока ионов Саг+ из внеклеточного пространства, запускаемом β1-адренорецепторами, что приводит к увеличению концентрации Са2+ в цитоплазме. Этот приток Са2+ можно ингибировать введением блокаторов Са2+-каналов (антагонистов Са2+). Другие факторы, увеличивающие сократимость миокарда, - это увеличение продолжительности ПД, приводящее к увеличению продолжительности притока Са2+, и ингибирование Na+ -К+ -АТФазы (например, сердечными гликозидами дигиталисом и строфантином). Последствия этого процесса таковы: пологий градиент Na+ на клеточной мембране → снижение движущей силы для 3Na+/Са2+-переносчика → снижение притока Са2+→ увеличение концентрации Са2+ в цитоплазме.
При низком сердечном ритме приток Са2+ также низкий (несколько ПД в единицу времени) - между отдельными ПД остается достаточно много времени для опока Са2+. Средняя концентрация Са2+ в цитоплазме, следовательно, понижена, и сократимость также низкая. Только при помощи этого косвенного механизма нейроны симпатической нервной системы способны вызывать отрицательный инотропный эффект (частотный инотропизм). НА и А могут оказывать свой положительный инотропный эффект или косвенно, или прямо при помощи β1-адренорецепторов рабочего миокарда.
Зависимость «давление-объем» для желудочков сердца[править | править код]
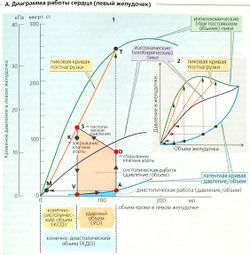
Соотношение между объемом (длиной) и давлением (напряжением) желудочка связано с зависимостью между длиной мышцы и силой ее сокращения с учетом специфики сердца. Диаграмма работы сердца может быть получена при нанесении на график изменений давления в желудочке и его объема за время одного полного сердечного цикла (А1, точки A-D-S-V-A, значения давления для левого желудочка).
Для построения диаграммы работы желудочков можно использовать следующие кривые «давление-объем»:
- Латентная (в покое) кривая «давление-объем»: показывает давление, которое пассивно (без мышечного сокращения) возникает при различных объемных нагрузках на желудочек (А1, 2; синяя кривая).
- Изоволюмическая пиковая кривая (А1, 2, зеленая кривая): построена по экспериментальным данным - измерения на изолированном сердце. Данные получены для различных объемных нагрузок путем измерения пикового давления в желудочках при постоянном объеме во время сокращения. Следовательно, сокращение изоволюмическое (при одном и том же объеме), и выброса при этом не происходит (А2, вертикальные стрелки).
- Изотоническая (изобарная) пиковая кривая (А1, 2, фиолетовая кривая): также основана на экспериментальных измерениях, сделанных при разных объемных нагрузках при изотонических (изобарных) условиях, т. е. выброс контролируется таким образом, что желудочковое давление остается постоянным при уменьшении объема (А2, горизонтальные стрелки).
- Постнагрузочная пиковая кривая (А1, 2, оранжевая кривая): систола состоит из фазы изоволюмического сокращения (А1, А-D), за которой следует ауксотоническая фаза выброса (объем снижается, в то время как давление продолжает расти) (А1, D-S и с. 199А, фаза II). Этот тип смешанного сокращения называется постнагрузочным сокращением (см. с. 73Б). При данной объемной нагрузке (преднагрузка) (А1, точка А) значение постнагрузочного пика меняется (А1, точка S) в зависимости от аортального давления конца диастолы (А1, точка D). Все значения пиковых постнагрузок лежат на прямой, соединяющей изотонические и изоволюмические пики для каждой объемной нагрузки (точка А) (А1, точки Т и М).
Диаграмма работы желудочков. Соотношение «давление-объем», наблюдаемое в течение сердечного цикла, можно представить в виде диаграммы работы, например, левого желудочка (А1): конечно-диастолический объем (КДО) составляет 125 мл (А1, точка А). Во время фазы изоволюметрического сокращения давление в левом желудочке возрастает (все клапаны закрыты) до тех пор, пока не будет достигнуто диастолическое аортальное давлении (80 мм рт. ст. в данном случае) (А1, точка D). Затем аортальный клапан открывается. Во время периода изгнания объем желудочка уменьшается на ударный объем (УО), тогда как давление вначале продолжает расти (закон Лапласа, уравнение [8.46]: Ptm↑, поскольку r↓ и w↑). Как только достигается максимальное (систолическое) давление (А1, точка S), объем остается практически постоянным, а вот давление немного падает до тех пор, пока не опустится ниже аортального, заставляя закрыться аортальный клапан (А1, точка К). Во время фазы изоволюмического расслабления давление быстро снижается практически до О (А1, точка V). Желудочки теперь содержат только конечно-систолический (резервный) объем (КСО), который равен в данном примере 60 мл. Давление желудочков слегка возрастает во время фазы наполнения (пассивная кривая «давление-объем»).
Работа и мощность сердца[править | править код]
Поскольку работа (Дж = Н • м) эквивалентна произведению давления (Н • м-2 = Па) на объем (м3), участок внутри диаграммы работы сердца (А1, розовый участок) характеризует работу, совершаемую левым желудочком во время систолы (13,333 Па • 0,00008 м3 = 1,07 Дж; правый желудочек: 0,16 Дж). В систоле миокард совершает работу в основном путем активного сокращения, а гораздо меньшая доля работы связана с пассивным эластичным сопротивлением желудочка - его растяжением при наполнении. Это - работа наполнения в диастоле (А1, синий участок под синей кривой) миокарда желудочка (опосредованно), миокарда предсердия, а также дыхательных и скелетных мышц (венозный возврат).
Общая работа сердца. Кроме работы, выполняемой правым и левым желудочками в систоле (примерно 1,2 Дж в покое), сердце должно генерировать еще 20% энергии (0,24 Дж) для пульса. Для движения крови в покое требуется лишь небольшое количество энергии (1% общей работы сердца), но энергетические требования возрастают вместе с сердечным ритмом. Общая мощность сердца (работа/время) в покое (70 мин-1 = 1,17 с-1) составляет примерно 1,45 Дж • 1,17 с-1 = 1,7 Вт.
Регуляция ударного объема[править | править код]
Механизм Франка-Старлинга (МФС): сердце автономно отвечает на изменения объема желудочков или нагрузки аортального давления, корректируя ударный объем (УО) по сердечной преднагрузке (напряжение покоя). МФС также поддерживает эквивалентные значения УО в обоих желудочках для предотвращения нарушений в легочном (малом) или системном (большом) кругах кровообращения.
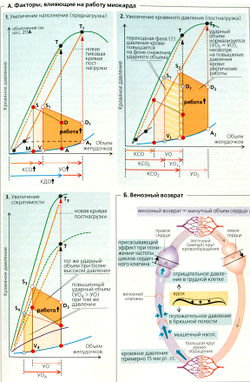
Преднагрузочные изменения. Когда объемная нагрузка (преднагрузка) возрастает, начало изоволюмического сокращения сдвигается вправо по латентной P-V-кривой (А1, от точки А до точки А1). Это увеличивает конечно-диастолический объем (КДО), ударный объем (УО), работу сердца и конечно-систолический объем (КСО) (А).
Постнагрузочные изменения. Когда нагрузка аортального давления (постнагрузка) возрастает, аортальный клапан не открывается до тех пор, пока давление в левом желудочке не увеличится соответствующим образом (А2, точка Dt). Так, УО во время короткой переходной фазы (У0() снижается, и КСО возрастает (KCOt). Вслед за этим начало изоволюмического сокращения сдвигается вправо по латентной Р-V-кривой (А2, точка Ад). УО затем нормализуется (УО2). несмотря на увеличенное аортальное давление (D2), что приводит к сравнительно большому увеличению КСО (КСОд).
Преднагрузочные или независимые постнагрузочные изменения силы сердечных сокращений обсуждаются в терминах сократимость или инотропный эффект. Сила сердечных сокращений увеличивается в ответ на норадреналин (НА) и адреналин (А), а также на увеличение сердечного ритма (опосредованный р^-адренорецепторами, положительный инотропный эффект и частотный инотропный эффект соответственно). Это вызывает несколько эффектов, в особенности увеличение пиков изоволюмического давления (АЗ, зеленая кривая). Сердце, таким образом, может качать кровь против увеличивающегося уровня давления (АЗ, точка D3) и/или выталкивать больший ударный объем УО (за счет КСО) (АЗ, У04).
В то время как изменения преднагрузки воздействуют на силу сокращения, изменения сократимости также воздействуют на скорость сокращения. В клинической практике как мера сократимости используется увеличение изоволюмического давления в единицу времени (максимум dP/dt). dP/dt увеличивается под действием НА и А и снижается при брадикардии или при параличе сердца.
Венозный возврат[править | править код]
Кровь из капилляров собирается в вены и возвращается в сердце. Механизмы, способствующие венозному возврату (Б): (a) vis a tergo (т. е. посткапиллярное кровяное давление, КД) (примерно 15 мм рт. ст.); (б) присасывающий эффект АВ-перегородки сердца, возрастающий при снижении частоты циклов работы сердечного клапана в систолу; (в) давление, оказываемое на вены при сокращении скелетных мышц (мышечный насос) клапаны вен препятствуют обратному току крови; (г) увеличенное брюшное давление вместе со сниженным внутригрудным давлением во время вдоха (Ppl), что ведет к дилатации грудных вен и засасыванию крови из соседних сосудов.
Ортостатический рефлекс[править | править код]
При вставании из положения лежа на спине в вертикальное положение (ортостатическое изменение) кровеносные сосуды в ногах подвергаются дополнительному гидростатическому давлению кровяного столба. Результирующая вазодилатация увеличивает объем крови в венах ног (примерно на 0,4 л). Поскольку эта кровь берется из общего циркулирующего объема крови, т. е. в основном из легочных сосудов, венозный возврат в левое предсердие снижается, что приводит к снижению ударного объема и минутного сердечного выброса. Для предотвращения избыточного падения артериального давления происходит рефлекторное увеличение (ортостатический рефлекс) сердечного ритма и периферического сопротивления; при этом может произойти ортостатический коллапс. Уменьшение кровяного давления более резко выражено в положении стоя, чем при ходьбе, что обусловлено насосной функцией мышц. И наоборот, давление в венах, расположенных выше уровня сердца, например в церебральных венах, снижается, когда человек находится в положении стоя в течение длительного времени. Поскольку венозное давление чуть ниже диафрагмы остается постоянным, несмотря на изменение положения тела, это положение называется точкой гидростатической нейтральности.
Центральное венозное давление (ЦВД) измеряется в правом предсердии (норма: 0-12 см водн. ст. или 0-9 мм рт. ст.). Поскольку ЦВД зависит главным образом от объема крови, в клинической практике с помощью монитора, записывающего ЦВД, контролируют объем крови (например, при переливании крови). Повышенное значение ЦВД (> 20 см водн. ст. или 15 мм рт. ст.) может быть патологическим (например, из-за паралича сердца или других болезней, связанных с дисфункцией сердечного насоса) или физиологическим (например, при беременности).
Обменные процессы в эндотелии[править | править код]
Питательные вещества и продукты метаболизма обмениваются через стенки капилляров и посткапиллярных венул (обменные сосуды). Их эндотелий имеет малые (примерно 2-5 нм) или большие (20-80 нм, особенно в почках и печени) функциональные поры: проницаемые внутриклеточные щели или эндотелиальные поры соответственно. Степень эндотелиальной проницаемости сильно варьирует в разных органах. Теоретически эндотелий любого сосуда должен пропускать воду и неорганические ионы, но большинство непроницаемо для клеток крови и больших молекул белков. Транспорт некоторых больших молекул осуществляется путем трансцитоза и с помощью переносчиков.
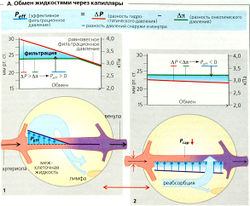
Фильтрация и реабсорбция. Около 20 л жидкости в день фильтруется в межклеточное пространство из обменных сосудов (исключая сосуды почек) организма. Ежедневно около 18 л этой жидкости реабсорбируется в посткапиллярных венулах. Остающиеся 2 л в день приходятся на лимфу и возвращаются в кровоток (А). Фильтрационный, или реабсорбционный, уровень Qf является функцией эндотелиального коэффициента фильтрации Kf (гидравлическая проницаемость к • обменная площадь А) и эффективного фильтрационного давления Peff[Qf= Kf * *Peff). Peff вычисляется как разность изменения гидростатического давления АР и изменения онкотического давления Ал) (по разные стороны капиллярной стенки) (соотношение Старлинга, А), где ΔР - капиллярное давление (Рcaр) минус интерстициальное (межклеточное) давление [Pint, в норме 0 мм рт. ст.). На уровне сердца АР на артериальном конце капилляров системного круга кровообращения составляет примерно 30 мм рт. ст. и снижается примерно до 22 мм рт. ст. на венозном конце. Поскольку Δπ (πсар - %t) (=» 24 мм рт. ст., А) противодействует АР, изначально высокий уровень фильтрации [Peff = + 6 мм рт. ст.) падает по ходу капилляров и при Peff = 0 полностью останавливается (равновесное давление фильтрации). Кратковременное (<1 мин) падение Peff до 0 приводит к реабсорбции в просвет капилляров и венул. Как только АР в легких становится ниже 10 мм рт.ст., пульмонарное Peff становится отрицательным и, таким образом, фильтрация не происходит.
В частях тела, расположенных ниже сердца, эффекты гидростатического давления столба крови увеличивают давление в просвете капилляров (в ногах —90 мм рт. ст.). Уровень фильтрации в этих участках, следовательно, возрастает, особенно в положении стоя. Этому противодействуют два механизма «саморегуляции»: (1) отток воды приводит к увеличению концентрации белков в просвете (и, таким образом, Δπ) по ходу капилляров (что обычно происходит в клубочковых капиллярах,); (2) повышенная фильтрация приводит к увеличению Pint и последующему снижению АР.
Отеки. Если объем фильтруемой жидкости выше, чем ее количество, возвращаемое в кровь, жидкость аккумулируется в интерстициальном пространстве (внеклеточные отеки), воротной вене (перитонеальный выпот, асцит) и легочных межклеточных пространствах (отек легких).
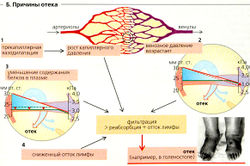
Причины отеков (Б):
- Увеличенное капиллярное давление (Б1) из-за прекапиллярной вазодилатации (Рсар↑), особенно в том случае, когда проницаемость капилляров для белков также увеличивается (σprot↓ и Δπ↓), например, из-за инфекции или в случае анафилаксии (гистаминовой и т. д.). Гипертензия в воротной вене ведет к асциту.
- Увеличенное венозное давление (Рсар↑, Б2), например, по причине венозного тромбоза или сердечной недостаточности.
- Сниженная концентрация белков плазмы, особенно альбумина, ведущая к падению Δπ (БЗ), например из-за белковой потери (протеинурия), сниженного синтеза белков в печени (например, при циррозе печени) или из-за повышенного распада белков плазмы для удовлетворения энергетических потребностей (голодные отеки).
- Сниженный лимфодренаж, например из-за компрессии лимфатических протоков (опухоли), разрывов (при операциях), зарастания (облитерации) (радиотерапия) или непроходимости (бильгарциоз), может вести к местным отекам (Б4).
- Увеличенное гидростатическое давление способствует развитию отеков в нижних частях тела (например, в коленях, Б)__
Диффузия. Растворенные частицы могут захватываться и проходить через капиллярные стенки вместе с фильтруемой и реабсорбируемой водой (захват растворителем), однако гораздо большую роль в обмене растворенными веществами играет диффузия. Чистая диффузия вещества (например, О2, CО2) имеет место в том случае, если концентрации этого вещества в плазме и внеклеточном пространстве различны.
Гипертензия[править | править код]
Гипертензия - хроническое увеличение артериального давления в большом круге кровообращения. Основным критерием диагностики гипертензии является стойкое увеличение кровяного давления в покое при систоле и диастоле до >140 мм рт. ст. и/или >90 мм рт. ст. соответственно. В отсутствие или при неадекватном лечении гипертензия приводит к повышенной нагрузке и компенсаторной гипертрофии левого желудочка, что в конечном счете может развиться в недостаточность левого сердца. Люди с гипертензией подвержены также риску атеросклероза и его последствий (инфаркт миокарда, инсульт, почечная недостаточность и т. д.). Таким образом, гипертензия существенно укорачивает продолжительность жизни многих людей.
Основной причиной гипертензии являются: (а) увеличение объема внеклеточной жидкости при увеличении венозного возврата и, следовательно, увеличении минутного сердечного выброса («объемная» гипертензия), (б) увеличение общего периферического сопротивления (резистентная гипертензия). Поскольку гипертензия всегда означает сосудистые изменения, приводящие к увеличению периферического сопротивления, гипертензия типа (а) в итоге превращается в гипертензию типа (б), которая вне зависимости оттого, как она начиналась, заканчивается порочным кругом.
Увеличение объема внеклеточной жидкости происходит в том случае, когда абсорбируется (всасывается) больше NaCI (и воды), чем секретируется. Обычно большое потребление соли с пищей может повлиять на развитие первичной артериальной гипертензии (эссенциальной гипертензии], наиболее распространенного типа гипертензии, по крайней мере у пациентов, чувствительных к соли. Гиповолемическая (объемная гипертензия может даже развиться при относительно небольшом, но несбалансированном потреблении соли. Это происходит при почечной недостаточности или в случае, когда опухоль в корковом веществе надпочечников продуцирует неконтролируемое количество альдостерона, что приводит к удерживанию Na+.
Другой важной причиной гипертензии является феохромоцитома, опухоль, секретирующая адреналин и норадреналин, и таким образом увеличивающая СО и ОПС. Почечная гипертензия может развиться из-за стеноза почечной артерии и заболеваниях почек. Это приводит к повышенной секреции ренина, который, в свою очередь, поднимает кровяное давление через ренин-ангиотензин-альдостероновую (РАА) систему.
Циркуляторный шок[править | править код]
Циркуляторный шок характеризуется острой (или близкой к острой) прогрессирующей генерализованной недостаточностью кровообращения с нарушением микроциркуляции и неспособностью поддерживать адекватный кровоток в жизненно важных органах. В большинстве случаев минутный сердечный выброс (СО) недостаточен по различным причинам, которые объясняются ниже.
- Гиповолемический шок характеризуется понижением центрального венозного давления и уменьшением венозного возврата, что приводит к изменению ударного объема (механизм Франка-Старлинга). Объем крови может уменьшиться из-за кровотечения (геморрагический шок) или каких-либо других условий, связанных с потерей жидкости через желудочно-кишечный тракт (например, при сильной рвоте, хронической диарее), почки (например, при сахарном диабете, несахарном диабете, при применении высоких доз диуретиков) или кожу (ожоги, чрезмерное потоотделение без потребления жидкости). Может произойти также внутренняя потеря крови, например, из-за кровотечения в мягких тканях, в средостении, в плевральном или абдоминальном пространстве.
- Кардиогенный шок: острая сердечная недостаточность может быть вызвана острым инфарктом миокарда, острой декомпенсацией сердечной недостаточности или ухудшением сердечного наполнения, например при тампонаде перикарда. Центральное венозное давление выше, чем при гиповолемическом шоке.
- Шок может случиться по гормональным причинам, например при адренокортикальной недостаточности, диабетической коме или передозировке инсулина (гипогликемический шок).
- Вазогенный шок: уменьшение минутного сердечного выброса также может произойти из-за периферической вазодилатации и, в итоге, результирующего уменьшения венозного возврата. Это происходит при грамположительной септицемии [септический шок), анафилактическом шоке, немедленной реакции гиперчувствительности (пищевая или лекарственная аллергия, укус/ужаление насекомого), при которых высвобождаются вазоактивные вещества (например, гистамин).
Симптомы. Гиповолемический и кардиоваскулярный шок характеризуются сниженным кровяным давлением (слабый пульс), увеличенным сердечным ритмом, бледностью с холодным потом (не наблюдается при шоке, вызываемом вазодилатацией), сниженной продукцией мочи (олигурией) и сильной жаждой.
Шоковый индекс 1 отношение пульса (удары/мин) к систолическому кровяному давлению (мм рт. ст.); шоковый индекс позволяет сделать грубую оценку потери объема крови. Индекс до 0,5 - норма (<10% кровопотеря); до 1,0 - это кровопотеря <20-30% и надвигающийся шок; до 1,5 — явный шок, кровопотеря >30-50%.
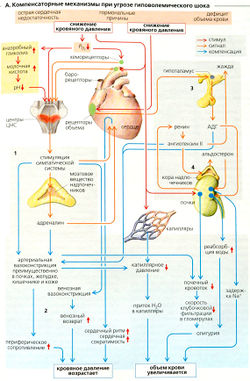
Большинство описанных симптомов организм отражает с помощью контррегуляторных мер во время непрогрессирующей фазы шока с целью предотвращения прогрессирующего шока (А). К ним относятся как быстродействующие механизмы повышения кровяного давления, так и медленно действующие механизмы компенсации потери объема.
Компенсация кровяного давления (А, слева). Снижение кровяного давления увеличивает симпатический тонус (А1). При артериальной вазоконст-рикции (отсутствует при шоке из-за вазодилатации) понижается минутный сердечный выброс и кровь не поступает к коже (бледность), в брюшные органы и почки (олигурия), а направляется к жизненно важным органам, таким как коронарные артерии и мозг. Это явление известно как централизация кровотока (А2). Симпатическое сужение венозных емкостных сосудов (которые увеличивают наполнение желудочков), тахикардия и положительный инотропный эффект ограниченно увеличивают заниженный минутный сердечный выброс.
Компенсация дефицита объема (А, справа). Когда шок становится неотвратимым, кровяное давление снижается и возникает вазоконстрикция периферической кровеносной сети, что ведет к снижению капиллярного фильтрационного давления и позволяет межклеточной жидкости попадать в кровоток. Рецепторы растяжения предсердий определяют уменьшение объема внеклеточной жидкости (низкое наполнение предсердий) и проводят сигналы, прекращающие секрецию предсердиями атриопептина и запускающие секрецию антидиуретического гормона (АДГ) задней долей гипофиза (рефлекс Гаера-Генри). АДГ индуцирует вазоконстрикцию (V1-рецепторы) и удерживание жидкости (V2-рецепторы). Падение почечного кровяного давления вызывает увеличение секреции ренина и активацию ренин-ангиотензин-альдостероновой системы (РАА). Если эти меры по предотвращению надвигающегося шока успешны, потерянные эритроциты позже возмещаются (посредством повышенной секреции эритропоэтина почками, с. 94), а концентрация белков в плазме крови нормализуется за счет повышения их синтеза в печени.
Проявленный (прогрессирующий) шок развивается в том случае, если эти компенсаторные механизмы гомеостаза не способны предотвратить наступление шока, и пациент не получает необходимого лечения (переливание донорской крови и т. д.). Серьезное понижение давления (гипотензия) (< 90 мм рт. ст. - систолическое кровяное давление или < 60 мм рт. ст. - среднее кровяное давление) может продолжаться в течение длительного времени, даже несмотря на возмещение объема крови. В результате развивается гипоксия, что ведет к повреждению многих органов и множественной органной недостаточности, что в конечном счете приводит к необратимому шоку и смерти.
Кровообращение в организме плода и новорожденного[править | править код]
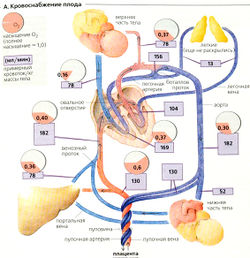
Плацента. Материнская плацента выступает в качестве «кишки» (абсорбция питательных веществ), «почки» (удаление отходов) и «легких» плода (снабжение О2, удаление СО2). Хотя кривая диссоциации комплекса 02-гемоглобин у плода сдвинута вправо по сравнению с тем, как наблюдается для взрослого человека, только 60% (0,6) плацентарного гемоглобина насыщено О2 (А).
Кровь плода распределяется в соответствии с потребностями. Неактивные и слабоактивные органы получают мало крови. Минутный сердечный выброс сердца плода (обоих предсердий) составляет 0,2 л/мин на килограмм массы плода. Сердечный ритм плода возрастает от начального в 65 мин-1 (5-я неделя) до 130-160 мин-1 в последующие недели. Примерно 50% крови, изгоняемой из сердца, протекает через плаценту, а другая половина снабжает тело (35%) и легкие (15%) плода. Это обеспечивается правым и левым сердцем, которые функционируют в основном параллельно вплоть до рождения.
Кровообращение у плода. Кровь проходит через тело плода следующим образом (А): после того как кровь артериализируется в плаценте, она попадает в организм плода по пупочной вене и часть крови проходит через венозный проток (аранциев проток) в обход печени. Входя в нижнюю полую вену, кровь смешивается с венозной кровью из нижней части тела. Направляемая специальными клапанами полой вены, смешанная кровь попадает прямо в правое предсердие через отверстие в предсердной перегородке (овальное отверстие). Из левого предсердия она затем попадает в левый желудочек. Находясь в правом предсердии, кровь смешивается с венозной кровью из верхней полой вены (незначительное смешивание), которую получает правый желудочек. Лишь около 1/3 этой крови достигает легких (из-за высокого сопротивления потоку крови, поскольку легкие еще не расправлены, а также из-за вазоконстрикции сосудов). Остальные 2/3 объема крови проходят по артериальному протоку (боталлову протоку) в аорту (сброс крови справа налево). Благодаря низкому периферическому сопротивлению (плацента) кровяное давление в аорте относительно низкое, лишь около 65 мм рт. ст. к концу беременности.
Артерии сердца и верхней части тела снабжаются частично артериализованной кровью из левого желудочка (А). Это важно, поскольку ткани мозга чувствительны к гипоксии. Оставшаяся кровь покидает аорту и смешивается с венозной из боталлова протока. В результате кровь, поступающая в нижнюю половину тела, имеет сравнительно низкую концентрацию О2 (насыщение кислородом = 0,3; А). Основная часть этой крови возвращается к плаценте по пупочной артерии, где снова насыщается кислородом.
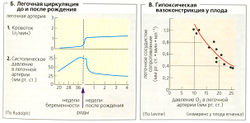
Кровообращение у плода во время родов. Обмен кислородом, СО2, питательными веществами и продуктами жизнедеятельности через плаценту внезапно прекращается при родах. Это ведет к повышению PCО2 в крoви- чтo активирует хеморецепторы, индуцирующие сильный дыхательный рефлекс. Этот рефлекс вызывает движение вдоха, которое создает отрицательное давление в грудной полости, что вытесняет кровь из плаценты и пупочной вены (плацентарная трансфузия) и раскрывает легкие. Раскрытие легких и подъем альвеолярного давления PО2 снижает сопротивление легочного кровообращения, и кровоток возрастает одновременно со снижением давления (Б1, 2). Тем временем сопротивление большого круга кровообращения возрастает из-за окклюзии (сжатия) пуповины. Это изменяет направление кровотока в боталловом протоке, что приводит к сбросу крови слева направо. Легочный круг кровообращения таким образом несколько дней после рождения получает кровь из аорты. Объем наполнения правого предсердия снижается из-за нехватки плацентарной крови, тогда как объем наполнения левого предсердия возрастает благодаря увеличению легочного кровотока. Благодаря возникающему градиенту давления между левым и правым предсердиями и снижению уровня простагландинов, оказывающих сосудорасширяющий эффект, овальное отверстие обычно закрывается в течение примерно двух недель после рождения. Артериальный (боталлов) и венозный (аранциев) протоки также закрываются, и большой и малый круги кровообращения теперь работают последовательно. Закрытие артериального протока вызывается повышением РО2 в крови (митохондриальный О2-сенсор производит Н2О2 → блокада К+-каналов → деполяризация →открытие Са2+-каналов L-типа →вазоконстрикция).
В том случае, когда овальное отверстие или артериальный или венозный протоки остаются открытыми, образуются шунты, создающие нагрузку для сердца. При проходимости овального отверстия (дефект предсердной перегородки) кровь течет из левого предсердия в правое предсердие (сброс крови слева направо), далее в правый желудочек (перегрузка объемом), оттуда в легкие и из них - в левый желудочек. При проходимости боталлова протока кровь течет из аорты в легочную артерию (сброс крови слева направо), далее в легкие (перегрузка давлением), а затем в аорту.