Механический фактор роста: комбинации
Содержание
Механический фактор роста: комбинации[править | править код]
Роль ИФР в системе МФР (пролиферация/дифференциация)[править | править код]
С практической точки зрения понимание роли и места инсулиноподобного фактора роста – 1 в системе механического фактора роста имеет существенное значение. По сути, если МФР применяется с целью восстановления поврежденных тренировкой мышц, то особо вникать в систему ИФР/МФР и не стоит. Но подозреваю, что у многих из вас цель не только восстановление, а еще и увеличение тренированных мышц, поэтому давайте постараемся разобраться.
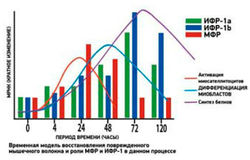
ИФР-1 является именно тем фактором, который заканчивает построение нового волокна. Механический фактор роста активирует миосателлитоцит, и он начинает делиться (пролиферация), а ИФР-1 заставляет миосателлитоцит преобразоваться в миобласт и из колонии миобластов создать миотрубку (дифференциация). По времени эти процессы стартуют практически одновременно, но в дальнейшем МФР и пролиферация обгоняют (что вполне логично) ИФР и дифференциацию. Этот цикл условно можно представить следующим образом:
- повреждение мышечного волокна;
- спустя 4–7 часов – увеличение активации миосателлитоцитов;
- 24–30 часов после повреждения – пик пролиферации и активности мфр;
- 30–48 часов – снижение до минимума мфр и, соответственно, снижение пролиферации;
- 48 часов после повреждения – пик дифференциации и воздействия на миосателлиты ифр;
- 120–130 часов после повреждения – снижение до минимума ифр и, соответственно, снижение дифференциации в миобласты;
- 72 часа после повреждения – пик синтеза сократительных и др. белков в поврежденной мышце;
- 200 часов после повреждения;
- снижение до минимума синтеза белков.
Нагляднее эти процессы продемонстрированы на схеме. Необходимо обратить внимание на то, что, вопреки досужему мнению, ИФР и МФР не являются синергистами, т. е. их одновременное взаимодействие не способно улучшить эффект друг друга. Однако без одного из этих элементов не будет желаемого эффекта от другого. Т. е. если МФР будет недостаточно, то деление миосателлитоцитов будет не настолько обильным, чтобы преодолеть стадию восстановления и перейти в стадию роста; с другой стороны, если ИФР слишком рано вступит в процесс деления, то он (ИФР) заставит те клетки, которые уже разделились, преобразиться в миобласты, что тоже позволит восстановить мышцу, но не позволит ее увеличить. Конечно, у вас может возникнуть вопрос, когда именно нужно ввести ИФР, чтобы запустить преобразование клеток- сателлитов в миобласты? Отвечу. Не стоит беспокоиться и бежать на «черный рынок» за ИФР, т. к. ваш организм об этом уже позаботился. Вы ведь помните, что тренировка, а также сон, провоцируют секрецию гормона роста, который в свою очередь стимулирует секрецию ИФР? Так вот, ИФР вы получите и так, и получите его порциями (после тренировки, после сна), что в течение последующих «послетренировочных» суток позволит несколько преобразовать клетки- сателлиты в миобласты. Другой вопрос, будет ли достаточно эндогенного ИФР, чтобы справиться с обилием «наплодившихся» клеток-сателлитов? Решением этой задачи может быть применение экзогенного гормона роста, ИФР, релизинг-пептидов и/или аналогов соматолиберина, но об этом немного позже.
Запасы миосателлитоцитов[править | править код]
Хотя многие из «пептидных юзеров» крайне редко (а вернее, практически никогда) не задумываются о таких мелочах, как количество клеток- сателлитов (в основном всех интересует, насколько вырастет бицепс, сколько наберут на курсе, сколько сольют после курса, не усохнут ли яички и не заболеют ли раком), но данный аспект крайне важен в случае применения механического фактора роста.
Во время развития эмбриона часть клеток-сателлитов формирует мышцы, а часть остается «про запас». На протяжении всей жизни количество миосателлитоцитов меняется, и меняется в основном в зависимости от двигательной активности (ну а также от болезней, связанных с повреждениями мышечных волокон). В ходе неоднократных исследований группами ученых, которые занимаются разными направлениями (изучением стероидных и белково-пептидных гормонов), отмечалось, что с возрастом у людей с большей двигательной активностью количество миосателлитоцитов снижается, а у людей с меньшей двигательной активностью клеток- сателлитов остается больше. Но при этом более подвижные и активные старички имели значительно менее хрупкую мускулатуру и большую мышечную массу, чем их менее подвижные «коллеги».
Если вы помните, в первой части повествования про МФР я говорил о наличии двух взглядов на вопрос количества клеток-сателлитов. Одна теория гласит, что количество миосателлитов отмерено от рождения и невосполнимо. Другая, наоборот, указывает на то, что клетки-сателлиты могут самообновляться. Так вот, на данный момент (что особо приятно) существенный перевес имеет именно точка зрения о восстановлении пула клеток-сателлитов. И этот перевес вполне обоснованный и подтвержденный в ходе исследований.
В 2003 году группой американских ученых в ходе 20-недельного эксперимента, в котором принимали участие 61 мужчина в возрасте от 18 до 35 лет, удалось продемонстрировать, что продолжительные высокие дозы тестостерона (600 мг тестостерона энантата в неделю), совместно с полным подавлением естественной секреции тестостерона (при помощи инъекций гонадолиберина) и периодическими тренировками, способны существенно увеличивать количество миосателлитоцитов в тренируемой мышце. Было замечено, что в группе, к которой применяли энантат в дозировке 600 мг, количество клеток-сателлитов на 1 мм мышечного волокна равняется трем- четырем. Кто-то, конечно, может улыбнуться такому пустяку, но, поверьте, это серьезное количество по сравнению с «группой 300 мг», у которых клеток- сателлитов насчитали всего 1-2 штуки на 1 мм, и по сравнению с «группой 125 мг», у которых в 1 мм не удалось найти ни одной клеточки. Конечно, учеными был сделан вывод о стимулирующей способности тестостерона, однако следует заметить, что ими не уделялось внимания таким факторам, как соматотропин, инсулиноподобный фактор роста и механический фактор роста. Хотя стоит отметить, что в рамках данного исследования был замечен интересный феномен, который заключается в том, что длительное применение ААС (6–12 лет) не приводило к постоянному прогрессивному увеличению количества клеток- сателлитов, что пока объясняют как ослабление влияния андрогенов на клетку-сателлит. Именно этот факт пока дает возможность говорить о положительном влиянии тестостерона на увеличение клеток-сателлитов. Согласитесь, интересное свойство.
Не стоит также снимать со счетов и теорию обновления естественных резервов, которая заключается в том, что не все клетки-сателлиты преобразовываются в миобласт, благодаря чему в резерве всегда остается более-менее постоянное количество миосателлитоцитов.
Комбинирование МФР с другими разновидностями фармакологических продуктов[править | править код]
Итак, мы с вами перешли к самому любопытному, с точки зрения «химиков- практиков», разделу, а именно к рассмотрению вариантов комбинирования МФР с другими продуктами современного рынка спортивной фармы. Однако из этических соображений я не буду указывать примеры и дозировки конкретных курсов, поскольку пептиды (и в том числе МФР) не предназначены для использования человеком, а другие лекарственные препараты предназначены для лечения, и их применение без контроля лечащего врача может существенно навредить здоровью.
МФР + андрогенно-анаболические стероиды[править | править код]
Механический фактор роста в такой комбинации будет выполнять роль «поставщика строительного материала». При этом ААС будут стимулировать производство сократительных белков как в старых, так и во вновь созданных волокнах (что позволит этим волокнам максимально быстро адаптироваться к рабочему процессу), а также (как в случае с энантатом) будут стимулировать увеличение количества миосателлитоцитов.
МФР + инсулин[править | править код]
Многих подобная комбинация может удивить, но она (комбинация) по своей эффективности может лишь уступать МФР + ААС. Инсулин (при грамотном применении) в данном случае позволит длительное время поддерживать интенсивный синтез белков (ну и конечно, гипогликемия простимулирует секрецию ГР), а МФР без помех поддержит обильное деление миосателлитоцитов. При этом ИФР, как выключатель деления миосателлитоцитов, тоже придет вовремя, а именно после секреции ГР. Т. е. к этому времени ИФР уже будет материал для формирования миотрубок.
МФР + инсулиноподобный фактор роста – 1[править | править код]
С одной стороны, не самая удачная комбинация, поскольку ИФР-1 не будет давать нормально разойтись пролиферации клеток-сателлитов, но, с другой стороны (вернее, в случае применения «длинных» форм), весьма эффективная связка. Если комбинировать с обычным рекомбинантным ИФР-1 либо с более мощным DES (1–3) ИФР-1, то применять можно любые формы МФР, при этом инъекции МФР и ИФР-1 лучше разделить по времени так, чтобы ИФР-1 был введен в конце как спусковой механизм для формирования миобластов и миотрубок. Если есть желание экспериментировать с IGF-1 LR3 или с pIGF720, то придется применять только пролонгированную форму рMGF720.
МФР + рекомбинантный гормон роста[править | править код]
Данная комбинация вполне эффективна, поскольку гормон роста позволит увеличить синтез белков, в т. ч. и коллагена, запустить липолиз, стимулировать гиперплазию иммунных желез. Однако не стоит забывать про «родного сына» гормона роста – ИФР-1, который, помимо всех положительных эффектов, запустит дифференциацию миосателлитоцитов. Не скажу, что этого следует бояться, и что это существенно снизит эффективность МФР, но, тем не менее, под эту комбинацию лучше выбрать либо «короткий» (обычный) МФР либо «длинный» рMGF720, который будет поддерживать деление клеток- сателлитов на достаточно высоком уровне, вне зависимости от продолжительного бомбардирования ИФР-1.
МФР + релизинг-пептиды и аналоги соматолиберинов[править | править код]
Знаю, что многие сейчас ухмыльнуться, но это зря. Релизинг-пептиды и аналоги соматолиберинов со своей способностью резко и высоко поднимать концентрацию ГР, при этом несильно поднимать концентрацию ИФР-1, как раз и являются одними из самых привлекательных продуктов в плане эффективного комбинирования с МФР. Причем абсолютно нормально «себя будут чувствовать» как короткие, так и длинные формы МФР.
Заключение[править | править код]
МФР может занять свое место во время так называемой послекурсовой терапии, либо на какой-то период стать альтернативой ААС при подготовке к соревнованиям с допинг- контролем, или стать неплохим терапевтическим средством при восстановлении натруженных мышц. Про самостоятельное использование не упоминаю, т. к. это само собой разумеющееся. Диапазон невелик? Ну ничего. Еще все впереди…
Данный класс продуктов относительно молодой, и белых пятен пока достаточно (например, не решен вопрос с родным МФР-рецептором у клетки- сателлита, либо нет единого мнения по оптимальным дозировкам), но с развитием науки и расширением индустрии (которые друг друга в чем-то подпитывают) я не нахожу такую ситуацию драматичной. Каждый день делаются открытия. И если раньше многие статьи повествовали о каких-то «неизученных» влияниях андрогенных гормонов, гормона роста, соматомедина С на скелетную мышцу, то в последнее время довольно часто в обширных трудах научных деятелей, которые работают в разных «гормональных классах» и проводят эксперименты с добровольцами, все чаще и чаще можно увидеть упоминания о механическом факторе роста, как о непосредственном медиаторе того или иного процесса в отдельной клетке и в организме в целом.
Источник: Железный мир 2013 №10