Омега-7 жирные кислоты: научный обзор
Содержание
- 1 Омега-7 мононенасыщенные жирные кислоты – новый класс фармаконутриентов в спортивном питании для контроля веса и обмена липидов
- 2 Структура и физико-химические свойства омега-7 МНЖК
- 3 Источники получения омега-7 МНЖК и их характеристика
- 4 Метаболизм Омега-7 МНЖК в организме
- 5 Результаты экспериментальных исследований in vitro и in vivo
- 6 Результаты клинических исследований
- 7 Заключение
- 8 Читайте также
- 9 Ссылки
Омега-7 мононенасыщенные жирные кислоты – новый класс фармаконутриентов в спортивном питании для контроля веса и обмена липидов[править | править код]
Авторы: д.м.н. Александр Дмитриев, врач-эндокринолог Алексей Калинчев
Введение[править | править код]
Открытие в 2008 году исследователями Гарварда (H.Cao и соавторы, Department of Genetics and Complex Diseases, Harvard School of Public Health, Boston, Lipomics Technologies, West Sacramento, США) нового липокина жировой ткани – омега-7 МНЖК (C16:1n7) – пальмитолеиновой кислоты (ПОК), дало толчок экспериментальным и клиническим исследованиям этого соединения в качестве потенциального средства лечения метаболического синдрома. В экспериментах на мышах с обычной и высокожировой диетой H.Cao и соавторы проанализировали содержание в плазме большого количества жирных кислот в норме и в условиях развития ожирения. При ожирении отмечается нарастание уровней свободных жирных кислот, что приводит к развитию инсулинорезистентности и накоплению липидов в печени. Как известно, нарушение метаболизма липидов, повышение концентрации свободных жирных кислот рассматриваются как важный фактор патогенеза инсулинорезистентности, возникновения избыточного веса и ожирения (D.B.Savage и соавт., 2007).
ПОК стимулирует действие инсулина, снижает инсулинорезистентность тканей, уменьшает отложение жиров и препятствует развитию ожирения. По мнению авторов, ПОК является важным элементом поддержания системного метаболического гомеостаза и осуществляет связь между адипозной тканью и системным метаболизмом.
ПОК, в отличие от омега-3 ПНЖК, синтезируется в организме в печени и жировой ткани. Экзогенное поступление ПОК происходит в составе очень многих продуктов, причем в количественном отношении ПОК далеко не доминирующая кислота. Поэтому сформировалась актуальная задача выделения ПОК из источников, ее содержащих, для детальной оценки влияния на липидный и углеводный обмен. Среди источников с наибольшим процентным содержанием ПОК выделяют растительные масла (облепиховое, орехов макадамии) и рыбий жир. Облепиховое масло содержит большое количество пальмитиновой кислоты (ПК), считающейся веществом с высоким атерогенным потенциалом, что требует удаления ПК из состава масла для получения концентрата ПОК. Рыбий жир отличается высоким содержанием омега-3 ПНЖК (эйкозапентаеновой – ЕРА и докозагексаеновой – DHA кислот), которым последние 40 лет придается большое значение в нормализации липидного и углеводного обмена в группах пациентов высокого риска развития заболеваний сердечно-сосудистой системы и печени (см. Омега-3 жирные кислоты: научный обзор). Имеются данные, что механизмы действия этих двух классов омега-ЖК принципиально различаются, причем их совместное введение сопровождается синергичным эффектом.
Данный обзор посвящен анализу структурных и физико-химических особенностей ПОК (омега-7 МНЖК), ее роли в метаболических процессах, развитии нарушений липидного и углеводного обмена, влиянию экзогенного введения ПОК в составе растительных и животных масел и в виде очищенных концентратов in vivo и in vitro на показатели метаболизма, а также перспективам применения в спортивной медицине, включая фитнес, программы снижения веса, регулирование состава тела в бодибилдинге, профессиональном конкурентном спорте.
Структура и физико-химические свойства омега-7 МНЖК[править | править код]
Наименования омега-7 МНЖК и их обозначения как химических веществ и липидов приведены в таблице 1.
Таблица 1. Класс омега-7 МНЖК
| Генерическое наименование | Обозначение как липида | Химическое наименование |
|---|---|---|
| нет | 12:1ω7 | 5-додеценовая к-та (5-dodecenoic acid) |
| нет | 14:1ω7 | 7-тетрадеценовая к-та (7-tetradecenoic acid) |
| Пальмитолеиновая к-та (Palmitoleic acid) | 16:1ω7 | 9-гексадеценовая к-та (9-hexadecenoic acid) |
| Вакценовая к-та (Vaccenic acid) | 18:1ω7 | 11-октадеценовая к-та (11-octadecenoic acid) |
| Пауллиниевая к-та (Paullinic acid) | 20:1ω7 | 13-эйкозеновая к-та (13-eicosenoic acid) |
| нет | 22:1ω7 | 15-докозеновая к-та (15-docosenoic acid) |
| нет | 24:1ω7 | 17-тетракозеновая к-та (17-tetracosenoic acid) |
Все омега-7 ЖК являются мононенасыщенными соединениями. Наибольшее значение как с научной, так и клинической точки зрения имеют две ЖК (табл.2):
Таблица 2. Химическая характеристика наиболее важных омега-7 МНЖК
| Генерическое наименование | Химическое наименование | Брутто формула | IUPAC формула (с метильного конца) | IUPAC формула (с карб. конца) | Рациональная полуразвернутая формула |
|---|---|---|---|---|---|
| цис-Пальмитолеиновая к-та (cis-Palmitoleic acid) |
цис-9-гексадеценовая к-та (cis-9-hexadecenoic acid) | С15Н29СOOH | 16:1ω7 | 16:1Δ9 | СН3-(СН2)5-СН=СН-(СН2)7-СООН |
| цис-Вакценовая к-та (cis-Vaccenic acid) |
11-октадеценовая к-та (cis-11-octadecenoic acid) | С17Н33СOOH | 18:1ω7 | 18:1Δ11 | СН3-(СН2)5-СН=СН-(СН2)9-СООН |
| транс-Вакценовая к-та (trans-Vaccenic acid) |
11-октадеценовая к-та (trans-11-octadecenoic acid) | С17Н33СOOH | 18:1ω7 | 18:1Δ11 | СН3-(СН2)5-СН=СН-(СН2)9-СООН |
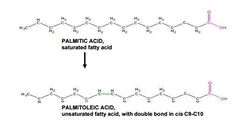
Пальмитолеиновая кислота (ПОК) – мононенасыщенная ЖК, которая входит в состав триглицеридов адипозной ткани млекопитающих, молочных продуктов, рыбьего жира, масла орехов макадамии, облепихового масла и ряда других. Синтезируется в организме из пальмитиновой кислоты под действием дельта-9 десатуразы (рис.1).
Вакценовая кислота (ВК) в виде природного транс-изомера содержится в жирах многих животных, молоке, масле и йогуртах. В организме ВК метаболизирует с образованием румениковой кислоты – полиненасыщенной ЖК (n-6).
Источники получения омега-7 МНЖК и их характеристика[править | править код]
С целью создания фармаконутриентов на основе ПОК используются источники животного и растительного происхождения: рыбий жир (перуанские анчоусы, коммерческое наименование 50% концентрата ПОК – Провинал – Provinalтм), при этом подавляющее большинство существующих форм рыбьего жира содержит омега-7 МНЖК в значительно меньшей концентрации; масло орехов макадамии с содержанием ПОК 15-21%; масло плодов облепихи с содержанием ПОК около 30% и выше. Суммарные данные о составе основных жирных кислот этих источников представлены в таблице 3.
Таблица 3. Состав преобладающих (наиболее важных) жирных кислот (ЖК) в различных источниках получения омега-7 МНЖК (в % от общего количества ЖК)
| ЖК | Масло облепихи | Масло макадамии | Рыбий жир перуанских анчоусов |
|---|---|---|---|
| Насыщенные ЖК: | |||
| Миристиновая (С14:0) | 0,8-1 | 0,8-1 | 7,5 |
| Пальмитиновая (С16:0) | 28-36 | 8-9 | 14-17 |
| Стеариновая (С18:0) | 1-2,5 | 3-4 | 4-5 |
| Арахидоновая (С20:0) | 0,5-1 | 2,5-3 | - |
| Мононенасыщенные: | |||
| Пальмитолеиновая (С16:1n7) | 30-36 | 18-20 | 8-9 |
| Олеиновая (С18:1n9) | 5-13 | 52-56 | 12-13 |
| Вакценовая (С18:1n7) | 5-6 | 3-4 | - |
| Полиненасыщенные | |||
| Линолевая (С18:2n6) | 12-24 | 1,5-2 | - |
| Эйкозапентаеновая (20:5n3) | - | 0,3-0,5 | 13-14 |
| Докозагексаеновая (22:6n3) | - | - | 17-19 |
Получение ПОК из рыбьего жира – многоступенчатый и затратный вариант, что, в сочетании с низким содержанием ПОК в сырье, существенно удорожает процесс производства и конечный продукт. Менее затратным считается получение ПОК из облепихового масла из-за ее высокой (30% и выше) исходной концентрации в сырье. Существуют способы обогащения, позволяющие довести концентрацию ПОК до 80% от общего количества жирных кислот (концентрат омега-7 МНЖК), однако на фармацевтическом рынке такие обогащенные формы отсутствуют. Доминирующее положение занимает 50% концентрат ПОК из рыбьего жира, в котором количество пальмитиновой кислоты (ПК) снижено до уровня 1-2,5%. С другой стороны, широко представлены необогащенные формы облепихового масла высшего качества из Финляндии, где содержание ПОК исходно составляет 35-37%, что, по мнению производителей, достаточно для позиционирования таких продуктов как омега-7 МНЖК (Мембразин, Омега-7 кардио и т.д.).
Пальмитолеиновая кислота (ПОК) – основной представитель омега-7 МНЖК. Подавляющее большинство экспериментальных и все клинические исследования в настоящее время выполнены с использованием ПОК. Считается установленным, что цис- и транс-формы вакценовой кислоты не обладают свойствами, характерными для ПОК. ПОК – 16-и углеродная МНЖК, которая присутствует в природе в виде цис-изомера (C16:1n-7, cis-9-hexadecenoic acid) и транс-изомера ((C16:1n-7, trans-9-hexadecenoic acid).
Метаболизм Омега-7 МНЖК в организме[править | править код]
Фармакокинетика ПОК[править | править код]
ПОК, поступающая с пищей, быстро абсорбируется (примерно через 30-40 минут), однако специальных исследований абсорбции выделенной из источника ПОК при пероральном введении нами не обнаружено. Она является мононенасыщенной ЖК и в этом смысле подобна олеиновой кислоте (ОК - омега-9 ЖК). Однако, ОК составляет 90% всех МНЖК, поступающих с пищей (содержится в оливковом масле и других растительных жирах), в то время как значимые количества ПОК содержатся только в отдельных пищевых продуктах. ПОК, поступающая с пищей, покрывает менее 4% от общей потребности в энергии.
Фармакокинетика ПОК (Провинал, ProvinalTM, 52,5% концентрат ПОК) при внутривенном введении в эксперименте на овцах с ожирением изучена в работе S.K.Duckett и соавт. (2014). Препарат вводился в виде инфузии два раза в день в течение 28 дней в дозах 5 и 10 мг/кг веса тела. Образцы крови для подробного биохимического анализа брались через 5 минут после окончания каждой инфузии в дни: 0; 7-ой; 14-ый и 21-й. Базовый уровень ПОК (C16:1 cis-9) в сыворотке крови составил в среднем 8,9 мкг/мл, через 5 минут после в/в инфузии он повышался до 11,7 мкг/мл (+31,5%) в дозе 5 мг/кг, и до 14,3 мкг/кг (+60,7%) в дозе 10 мг/кг (P<0,05). Параллельно достоверно (Р<0,001) линейно дозозависимо увеличивались концентрации в сыворотке арахидоновой (C20:4) и эйкозапентаеновой (EPA, омега-3, C20:5) кислот. Повышение EPA составило 10% в дозе ПОК 5 мг/кг, и 30,7% в дозе 10 мг/кг. Указанные изменения в крови быстро проходили в течение 50 минут (N.M.Long и соавт., 2014).
Ежедневная двукратная в/в инфузия ПОК в течение 28 дней сопровождается следующими кумулятивными изменениями профиля жирных кислот в сыворотке: увеличение ПОК (до 60%) и вакценовой кислоты (другая омега-7 МНЖК) с 5 до 11 мкг/мл (более, чем вдвое). Эти изменения содержания отдельных ЖК определили линейное возрастание в течение периода исследования общего содержания МНЖК и ПНЖК n-6 в сыворотке крови (P<0,05). При этом соотношение ПОК/ПК также линейно возрастало в процессе исследования.
Метаболизм ПОК[править | править код]
В отличие от омега-3 ЖК, ПОК может синтезироваться в организме как продукт липогенеза. Первичный процесс синтеза происходит в печени с помощью десатуразы стероил-коэнзима-А (stearoyl-coenzyme-A desaturase (SCD). Затем ПОК идет на образование триглицеридов (ТГ), включаясь в формирование липопротеидов очень низкой плотности (ЛОНП - VLDL), а также секретируется в кровь. Кроме того, ПОК может синтезироваться в адипозной ткани. Хотя ПОК считается «малой» ЖК, по распространенности в организме она находится на пятом месте в большинстве тканей и фракций липидов крови. В процессе метаболизма ПОК может конвертироваться в ряд других ЖК семейства омега-7, в частности, пальмитолиноленовую кислоту (palmitolinoleic acid (16:2n7) и румениевую кислоту (rumenic acid (18:2n7), и поэтому рассматривается как «родительская» ЖК для других кислот данного класса (V.J.Barthet, 2008).
Пальмитолеиновая кислота (ПОК) против пальмитиновой кислоты (ПК)[править | править код]
Существует принципиальная разница между ПОК и ее прекурсором ПК (16:0) – насыщенной ЖК, которая является самой распространенной ЖК в живых организмах. Однако, ферменты десатуразы, которые превращают ПК в ПОК, имеют слабый аффинитет к ПК, что обусловливает очень небольшие количества ПОК, обнаруживаемые в организме. Соотношение ПОК/ПК в плазме крови обозначается как десатурационный индекс.
ПК содержится в большинстве жиров и масел, включая пальмовые продукты (например, пальмовое масло), мясо, сыр, масло и др. Это продукт, наиболее часто используемый при приготовлении пищи. Потребление ПК и других насыщенных ЖК имеет тенденцию к ограничению из-за отрицательного влияния на обмен жиров и возрастанию риска кардиометаболических нарушений, атерогенности многих продуктов, содержащих насыщенные ЖК. Отмечено снижение окисления жиров и возрастание ежедневного расхода энергии, которые ведут к ожирению. Повышенное потребление ПК ассоциируется с воспалением и развитием инсулинорезистентности (V.J.Barthet, 2008; S.C.Benoit и соавт., 2009; M.Garaulet и соавт., 2011). С практической точки зрения представляется важным тот факт, что природные источники ПОК могут одновременно содержать и высокие концентрации ПК. Например, облепиховое масло содержит очень высокие концентрации ПОК (32-42%), но в то же время, не менее высокие концентрации ПК (34-41%) от общего количества ЖК. Поэтому при оценке состава коммерческих готовых форм, содержащих ПОК, следует обращать внимание и на содержание ПК, если этот источник ЖК не подвергался предварительной технологической обработке. Источник, содержащий одновременно высокие концентрации ПОК и ПК не может рассматриваться как препарат омега-7 МНЖК
Роль стереоизомерии[править | править код]
В пищевых продуктах содержатся цис- и транс-формы ПОК. В рыбьем жире, масле орехов макадамии, облепиховом масле и адипозной ткани млекопитающих (включая жировую ткань печени, где происходит синтез ПОК) присутствует цис-изомер (cis-Palmitoleic acid; 9-cis-Hexadecenoic acid). Большинство основных клинических доказательств положительного действия пищевой интервенции ПОК на профиль липидов, С-реактивный белок, контроль гликемии и инсулиночувствительность также получено для цис-изомера ПОК (A.M.Bernstein и соавт., 2014 и др.). Соответственно, предлагаемые на фармацевтическом рынке варианты ПОК, содержат цис-изомер этой МНЖК. Транс-изомер ПОК (trans-Palmitoleic acid; 9-trans-Hexadecenoic acid. содержится в молочных продуктах.
С другой стороны, имеются достаточно серьезные доказательства исследователей Гарварда, что пищевые источники, содержащие транс-форму ПОК, оказывают сходное действие, по крайней мере, в отношении воспаления и риска развития диабета (D.Mozaffarian и соавт., 2010). Таким образом, на сегодняшний день нет оснований выделять какую-либо стереоформу (цис- или транс-) в плане перспектив исследования и клинического использования. Тем не менее, требуются дальнейшие расширенные исследования в этом направлении, в частности, выделенных (очищенных) форм транс-ПОК.
Результаты экспериментальных исследований in vitro и in vivo[править | править код]
В настоящее время выполнен достаточно большой объем экспериментальных исследований как самой ПОК, так и ряда источников, ее содержащих (суммарные данные представлены в табл. 4 и 5).
Фундаментальным событием, давшим начало более детальным исследованиям ПОК, явилось открытие ученых Гарвардского Университета (H.Cao и соавт., 2008) проведших скрининг более 400 жирных кислот. Они установили, что ПОК функционирует как липокин-липид с гормоноподобной биологической активностью (на молекулу получен патент в соответствии с видом активности). Они также выдвинули гипотезу, что эстерифицированная форма ПОК, циркулирующая в крови, обеспечивает коммуникационную связь с отдаленными органами и осуществляет регуляцию метаболического гомеостаза. Исследователи предположили, что ПОК является единственной ЖК, которая может регулировать состав жирных кислот сыворотки крови в точном соответствии с имеющимися повреждениями (нарушениями) метаболизма липидов в жировой ткани.
В экспериментальных исследованиях на животных получены данные о положительном влиянии ПОК на функцию печени и профиль липидов плазмы крови (Z.H.Yang и соавт., 2011; S.Shiba и соавт., 2011). Н.Cao и соавторы (2008) в экспериментах на мышах выявили отчетливое стимулирующее действие ПОК на активность инсулина в скелетных мышцах и подавление гепатостеатоза. В другом исследовании использовалось пероральное введение 300 мг/кг ПОК ежедневно в течение 4-х недель (альтернативная группа – 300 мг/кг пальмитиновой кислоты – ПК) мышам (специальная экспериментальная модель исследования ожирения при диабете II типа с низкой чувствительностью к инсулину) (Z.H.Yang и соавт., 2011). ПОК останавливала рост веса тела, снижала развитие гипергликемии и гипертриглицеридемии, а также повышала чувствительность к инсулину. Кроме того, в группе с ПОК (по сравнению с группой с ПК) отмечалось меньшее накопление жира в печени, более низкий уровень триглицеридов печени и ее веса. После введение ПОК крысам наблюдалось повышение поступления глюкозы в скелетные мышцы, усиление ее окисления и образования гликогена (N.Dimopoulos и соавт., 2006).
ПОК при внутривенном введении в условиях экспериментального ожирения[править | править код]
Комплексная оценка влияния ПОК (ProvinalTM, 50% концентрат ПОК) на состав липидов сыворотки крови, уровни инсулина, инсулинорезистентность, внутримышечное содержание липидов и размеры адипоцитов при внутривенном введении (дважды в сутки в дозах 5 и 10 мг/кг) в течение 28 дней в эксперименте на овцах с ожирением изучена в работе S.K.Duckett и соавт. (2014). Все наблюдаемые изменения носили дозо-зависимый линейный характер и были наиболее выражены в дозе 10 мг/кг. К 28 дню исследования значительно возрастали в сыворотке крови уровни омега-7 МНЖК (ПОК и вакценовая кислота, на 60% и 120%, соответственно), увеличивались концентрации МНЖК и ПНЖК n-6, соотношение ПОК/ПК (P<0,05), что расценено в качестве положительных сдвигов.

Как видно из рис.2А, если в начале исследования в группе с дозой ПОК 10 мг/кг исходные показатели уровней инсулина были выше, то на 14-ый и 28-ой день исследования они достоверно и очень существенно снижались по сравнению с другими группами (Р<0,05). В дозе 5 мг/кг уровни инсулина на 14 день не отличались от контроля, но на 28 день были достоверно ниже. Уровень глюкозы плазмы под влиянием ПОК не изменялся и составил 95±19 мг/дл. Показатель инсулинорезистентности (Homeostatis Model Assessment-Insulin Resistance (HOMA-IR) в целом показал сходную динамику с изменениями уровней инсулина, при этом достоверное снижение инсулинорезистентности по сравнению с контролем носило дозозависимый характер и наблюдалось к 28 дню исследования как в дозе 5 мг/кг, так и в дозе 10 мг/кг (Р<0,05). Отдельно оценивались изменения концентрации ЖК в скелетных мышцах, подкожной и мезентериальной жировой ткани и тканях печени. Отмечено дозо-зависимое (от вводимой дозы ПОК) линейное возрастание в этих тканях омега-7 МНЖК (ПОК и вакценовой кислоты), ЕРА и докозапентаеновой кислоты в процессе 28-дневного наблюдения (Р<0,05). В целом концентрации омега-6 и омега-3 ПНЖК линейно и дозо-зависимо от введенной ПОК возрастали. Весьма важно, что также линейно возрастало и соотношение ПОК/ПК.
Биохимические изменения в плазме крови сопровождались достоверным снижением прироста веса экспериментальных животных (на 77%, Р<0,01). При этом достоверных изменений антропометрических данных, размеров жировых отложений не выявлено. Таким образом, ПОК при 28-дневном в/в введении оказывает отчетливое положительное влияние на основные параметры липидного и углеводного обмена в условиях ожирения, снижает инсулинорезистентность тканей. Совокупность дозо-зависимых линейных положительных изменений важнейших показателей липидного и углеводного обмена при введении ПОК доказывает принадлежность ПОК к фармаконутриентам, сочетающих свойства нутриентов и фармакологических агентов.
Суммируя результаты экспериментальных исследований, можно сделать следующие выводы:
- ПОК антагонизирует негативное влияние ПК и высоких концентраций глюкозы на бета-клетки поджелудочной железы, предотвращая фрагментацию ДНК и торможение процесса пролиферации (K.Maedler и соавт., 2003).
- ПОК способствует транспорту глюкозы в клетках обычных и инсулинорезистентных скелетных мышц и увеличивает в 2 раза ее концентрацию, усиливает окисление глюкозы и образование гликогена, антагонизируя действие ПК (N.Dimopoulos и соавт., 2006).
- ПОК на клеточном уровне угнетает липоапоптоз, вызываемый стресс-ответом эндоплазматического ретикулюма после воздействия ПК (Y.Akazawa и соавт., 2010).
- При 4-х недельном введении мышам с диабетом введение ПОК повышает чувствительность к инсулину, снижает уровни глюкозы и инсулина в плазме и ТГ в плазме и печени. ПОК подавляет mРНК-экспрессию провоспалительных генов адипокинов (TNF-α, резистин) в белой жировой ткани и генов липогенеза (SREBP-1, FAS, SCD-1) в печени (Z.H.Yang и соавт., 2011).
- ПОК повышает уровни холецистокинина и потребление пищи (Z.H.Yang и соавт., 2013).
- Экзогенное введение омега-7 МНЖК при экспериментальном ожирении увеличивает концентрацию циркулирующей ПОК и снижает прирост массы тела и размер внутримышечных адипоцитов (S.K.Duckett и соавт., 2013).
- По данным экспериментальных исследований Cleveland Clinic Foundation (2013) экзогенное введение ПОК снижает уровень ТГ, LDL и общего холестерола плазмы, повышает HDL.
- Омега-7 МНЖК снижают воспаление жировой ткани, реакцию перитонеальных макрофагов и гипертрофию адипоцитов, вызываемые высокожировой диетой (E.A.Lima и соавт., 2014).
Сравнительное экспериментальное исследование омега-7 МНЖК и омега-3 ПНЖК[править | править код]
До недавнего времени считалось, что положительные эффекты рыбьего жира в отношении обмена липидов в организме ограничиваются двумя полиненасыщенными омега-3 ЖК (ПНЖК) – эйкозапентаеновой (EPA) и докозагексаеновой (DHA). Позже было обнаружено, что относительно высокое содержание в жире некоторых рыб омега-7 мононенасыщенной ЖК (пальмитолеиновой кислоты) также вносит свой вклад в нормализацию липидного обмена при его нарушениях (D.D.Hong и соавт., 2003; T.Ide и соавт., 2004; T.Higuchi и соавт., 2008). В более поздней работе S.Shiba и соавторов (2011) исследовано влияние потребления линейными мышами (С57BL/6J) двух вариантов диеты с заданными параметрами (39% - углеводы, 40% - жир, 21% - белок, с равной калорийностью): 1) жировой компонент – рыбий жир; 2) жировой компонент – свиное сало (насыщенные транс-жирные кислоты (Н-транс-ЖК). После 10 недель такой диеты мыши второй группы (потреблявшие Н-транс-ЖК) были разделены на три группы: 1-ая – с добавлением перорально Н-транс-ЖК (30 мг/сутки один раз); 2-ая – Н-транс-ЖК 10 мг/сутки+EPA 20 мг/сутки, один раз; 3-я – Н-транс-ЖК 10 мг/сутки+ПОК 20 мг/сутки, один раз. Такие варианты диеты сохранялись в течение последующих 2-х недель. Группа мышей, находившаяся на диете с рыбьим жиром в течение 10 недель, продолжала ее получать также еще две недели. Основные результаты исследования: 1) различия между группами, получавшими только Н-транс-ЖК и рыбий жир после 12 недель диеты сводились к значительно более высокому уровню ТГ в плазме и липидов в печени в группе с Н-транс-ЖК; 2) уровень ТГ в плазме в группах с добавлением EPA и ПОК к Н-транс-ЖК был примерно равным и занимал среднее положение между группой с потреблением Н-транс-ЖК и рыбьего жира; 3) уровень липидов печени был наиболее низким в группах с добавлением к Н-транс-ЖК ПОК и ЕРА не только по сравнению с группой мышей, получавших Н-транс-ЖК, но и по сравнению с группой, получавшей рыбий жир. Таким образом, ЕРА и ПОК оказывают отчетливое защитное действие в отношении метаболизма липидов в печени. В то же время, анализ своих результатов и исследований других авторов, позволил сделать вывод о различных механизмах защитного действия омега-3 ПНЖК и омега-7 МНЖК (ПОК), связанных с влиянием на разные ферментативные системы в печени, что создает основу для комбинированного использования этих двух классов ненасыщенных ЖК для синергичного усиления гепатопротективного эффекта. Важно, что положительные эффекты омега-7 МНЖК проявляются уже при кратковременном 2-х недельном введении.
Результаты клинических исследований[править | править код]
Уровень ПОК в организме как прогностический фактор риска развития метаболических нарушений[править | править код]
В работе D.Mozaffarian и соавторов (2010) исследовалась взаимосвязь между фосфолипидами плазмы крови, содержащими транс-ПОК, и метаболическими факторами риска и инцидентами возникновения диабета II типа у 3736 взрослых лиц (Cardiovascular Health Study (CHS) при наблюдении в течение года. На основании своих ранее проведенных экспериментальных исследований, авторы предположили, что непеченочные источники ПОК могут подавлять синтез жиров печени и, таким образом, улучшать метаболизм. В исследовании использованы пищевые источники (молочные продукты), содержащие транс-изомеры ПОК. На основании результатов множественного корреляционного анализа установлено, что повышенное поступление транс-ПОК (и, соответственно, повышенная ее концентрация в организме) способствует уменьшению ожирения, повышению HDL-холестерола, понижению ТГ, общего холестерола, инсулинорезистентности и трехкратному снижению риска развития диабета. Описаны количественные показатели этого процесса в динамике, показана независимость выявленных закономерностей от демографических показателей, образа жизни, других пищевых факторов. Отсутствие связи с другими пищевыми факторами и изменениями других фосфолипидов, подчеркивает именно специфическое действие транс-ПОК в уменьшении метаболических рисков, в т.ч. развития диабета. В работе N.Stefan и соавторов (2010) циркулирующая ПОК определена как строгий и независимый предиктор инсулиночувствительности у человека.
Суммарные данные экзогенного введения ПОК и ПОК-содержащих источников в клинических исследованиях приведены в таблицах 7 и 8.
Исследование клинической эффективности и безопасности концентрата ПОК из рыбьего жира (ProvinalTM)[править | править код]
Начальные клинические данные опубликованы в 2012 году (J.Green, Tersus Pharmaceuticals, LLC). Исследуемые лица были рандомизированы соответственно суточной дозе ПОК: 210 мг/день (n=13) или 840 мг/день (n=14). Показатели изменений в группах были следующими (табл. 4 и 5):
- Снижение LDL-холестерола
- на 12-19% в дозе 210 мг ПОК
- на 3.9-30% в дозе 840 мг ПОК
- Снижение общего холестерола
- на 3-15% в дозе 210 мг ПОК
- на 3.9-30% в дозе 840 мг ПОК
- Тенденция к понижению не-HDL-холестерола.
Не отмечено изменений уровней глюкозы. Обе дозы ПОК хорошо переносились без каких-либо побочных эффектов. При проведении отдельного анализа в подгруппах, у лиц с высоким исходным уровнем C-реактивного белка (hsСRP) отмечено его значительное (в среднем на 73%) снижение при введении ПОК в дозе 210 мг/день. Среди исследуемых лиц половина имела исходный уровень холестерола >200 мг/дл. Анализ в этой подгруппе показал (табл.5) значимое снижение общего, не-HDL, LDL холестерола и ТГ при применении обеих доз ПОК. Следует отметить, что все субъекты с исходно высоким LDL-холестеролом одновременно находились на терапии статинами и/или фибратами, и, тем не менее, показали более, чем 10% снижение общего и LDL холестерола. Исходя из этого, исследователи предполагают возможность комплементарного механизма действия между статинами и ПОК.
Таблица 4. Изменения профиля липидов при различных дозах ПОК (J.Green,2012, цит. по обзору Metagenics, Inc., 2013)
|
Показатель |
Изменение |
210 мг (п=13) |
840 мг (п=14) | ||||
|
Исходное значение |
Через 4 недели |
Среднее изменение |
Исходное значение |
Через 4 недели |
Среднее изменение | ||
|
ТГ |
1 |
128 |
118 |
-1,1% |
146 |
130 |
-11,0% |
|
LDL |
1 |
118 |
112 |
-5,1% |
118 |
109 |
-7,6% |
|
не-HDL |
1 |
143 |
136 |
-4,9% |
147 |
135 |
-8,2% |
|
TChol |
1 |
199 |
189 |
-5.0% |
195 |
182 |
-6.7% |
Примечания: ТГ – триглицериды; LDL – липопротеиды низкой плотности; не-HDL – липопротеиды, исключая высокой плотности; TChol – общий холестерол
Таблица 5. Анализ данных в подгруппах с исходным уровнем ТСhol˃200 мг/дл (J. Green, 2012, цит. по обзору Metagenics, Inc., 2013)
|
Показатель |
Изменение |
210 мг (п=6) |
840 мг (п=7) | ||||
|
Исходное значение |
Через 4 недели |
Среднее изменение |
Исходное значение |
Через 4 недели |
Среднее изменение | ||
|
ТГ |
1 |
100 |
93 |
-7,0% |
180 |
153 |
-15,0% |
|
LDL |
1 |
141 |
125 |
-11,3% |
134 |
117 |
-12,7% |
|
не-HDL |
1 |
161 |
143 |
-4,9% |
170 |
147 |
-8,2% |
|
TChol |
1 |
232 |
208 |
-10.3% |
219 |
190 |
-13.2% |
Примечания: ТГ – триглицериды; LDL – липопротеиды низкой плотности; не-HDL – липопротеиды, исключая высокой плотности; TChol – общий холестерол
Результаты предварительных клинических исследований были отражены во внутренних отчетах Института Здоровья клиники Кливленда (Wellness Institute, Cleveland Clinic, Lyndhurst, Огайо, США) и Медицинского Института в Пуэрто-Рико (Xyrion Medical Institute, Ponce, США) в 2013 году. Они представляют собой две последовательные работы (открытое исследование и двойное-слепое рандомизированное плацебо-контролируемое исследование - L Martinez, 2013a,b). Рандомизированное исследование включало 60 лиц с повышенным исходным hsCRP (от 3 до 10 мг/л), но без диагностированных кардиометаболических нарушений. Пациенты получали (без изменения обычного режима питания) 420 мг очищенного препарата омега-7 МНЖК (содержащего 210 мг ПОК) или плацебо один раз в день в течение 30 дней. В группе с плацебо изменений не выявлено, а в группе с ПОК наблюдались следующие изменения (табл.6): снижение hsCRP (высокочувствительного С-реактивного белка); снижение ТГ, LDL, не-HDL и общего холестерола; повышение HDL холестерола.
Таблица 6. Изменение профиля липидов при введении 210 мг ПОК (L.Martinez, 2013a,b)
|
Показатель |
Изменение |
Открытое исследование (п=16) |
Плацебо-контролируемое исследование (п=60) |
|
Средние изменения за 30 дней в % |
Средние изменения за 30 дней в % | ||
|
hs-CRP |
↓ |
-64 |
-50 |
|
ТГ |
↓ |
-36 |
-17 |
|
LDL |
↓ |
-10 |
-7 |
|
HDL |
↑ |
+4 |
+3 |
|
He-HDL |
↓ |
-17 |
-9 |
|
TChol |
↓ |
-13 |
-7 |
Примечания: hs-CRP – высокочувствительный С-реактивный белок; ТГ – триглицериды; LDL – липопротеиды низкой плотности; HDL – липопротеиды высокой плотности; не-HDL – липопротеиды, исключая липопротеиды высокой плотности; TChol – общий холестерол. Изменения достоверны по сравнению с плацебо (Р<0,01).
Дальнейшее обобщение и анализ результатов двойного-слепого рандомизированного плацебо-контролируемого исследования подробно представлены в 2014 году в «Журнале клинической липидологии» (A.M.Bernstein и соавт., 2014). В окончательный анализ включались лица от 17 до 70 лет (в среднем 45 лет; 37% мужчин и 63% женщин), уровнем высокочувствительного С-реактивного белка (hs-CRP) в интервале от 2 до 5 мг/л. Критериями исключения были: ИМТ≥45, резкое изменение веса за последние 2 недели (≥3 кг), нефротическая протеинурия (≥3 г/день), онкологические заболевания в анамнезе, долгосрочный (более 6 мес.) прием антигипертензивных или антидиабетических препаратов, средств для снижения веса и некоторые другие. Рандомизация осуществлялась в две группы (n=30 в каждой): 1) экспериментальная группа с ежедневным в течение 30 дней однократным пероральным назначением (в составе пищи) концентрата цис-ПОК в дозе 220,5 мг (Провиналтм, 52,5% концентрат из рыбьего жира перуанских анчоусов с предварительным удалением всех омега-3 ПНЖК, включая ЕРА и DHA, и снижением содержания ПК до уровня <1%; 2) контрольная группа (ежедневный однократный пероральный в течение 30 дней прием плацебо с 1000 мг МСТ, которые не изменяли по результатам биохимического анализа крови ни липидный состав крови, ни уровень hs-CRP). В исходных показателях обеих групп отмечались: дислипидемия (LDL≥100 мг/дл) и повышение CRP (≥3 мг/л), но без явлений гипертензии (систолическое АД 117±8, диастолическое - 68±6 мм рт.ст.). Исходные показатели липидного обмена, CRP и их изменения через 30 дней приема препарата и плацебо представлены в таблице 9.
Таблица 7. Суммарные данные экспериментальных и клинических исследований влияния базовых источников омега-7 МНЖК (ПОК) - масла орехов макадамии и облепихового масла (без выделения омега-7 МНЖК - ПОК) - на метаболизм липидов и глюкозы
| Авторы, год | Краткое содержание, результаты и выводы работы |
|---|---|
| J.D.Curb и соавт., 2000 | Рандомизированное перекрестное исследование влияния трех различных 30-дневных диет у человека (n=30, 18-53 лет): высокое содержание НЖК (37% общей энергии от жиров); рекомендованная АНА диета (30% энергии от жиров); диета, базирующаяся на МНЖК из макадамии (37% энергии из жиров). Оценка в сыворотке общего холестерола, HDL и ТГ. Вывод: диета на основе МНЖК макадамии, также как и диета с пониженным содержанием НЖК, оказывают положительное влияние на регистрируемые показатели липидного обмена по сравнению с высокожировой диетой. |
| J.Hiraoka-Yamamoto и соавт., 2004 | Исследование в Японии у молодых здоровых японских женщин с 3-х недельным потреблением орехов макадамии, кокоса и сливочного масла. В группах с потреблением орехов макадамии и кокоса отмечено значимое снижение концентрации в сыворотке общего холестерола, LDL, а также снижение общего веса и ИМТ в группе макадамии. В группе с употреблением сливочного масла таких положительных изменений не отмечено. |
| A.E.Griel и соавт., 2008 | Рандомизированное перекрестное контролируемое 5-недельное сравнительное исследование (n=25, 15 женщин, 10 мужчин) двух диет: 1) обогащенная орехами макадамии (42.5 г./8.79 MJ (2100 ккал) - 33% общего жира (7% НЖК, 18% МНЖК, 5% ПНЖК); 2) средняя американская диета (33% общего жира (13% НЖК, 11% МНЖК, 5% ПНЖК). Оценивались: профиль липидов, общий холестерол, LDL, HDL и ТГ. Вывод: Диета с макадамией снижает ТГ, улучшает профиль липидов, повышает HDL, что позволяет рекомендовать данную диету для снижения риска развития сердечно-сосудистых заболеваний. |
| P.S.Larmo и соавт., 2008 | Объемное клиническое исследование влияния натуральной облепихи на течение общей неспецифической инфекции, инфекции ЖКТ и мочевыводящих путей, уровень С-реактивного белка (CRP) в сыворотке крови у 233 пациентов. Существенных различий в клинической картине инфекционных процессов между группой, принимавшей облепиху, и контролем не выявлено. Однако уровень CRP был существенно ниже в группе, принимавшей облепиху. |
| N.R.Matthan и соавт., 2009 | Экспериментальное исследование на хомяках с 12-недельным введением стандартной диеты (10% жира, 0,1% холестерола) диеты в следующих вариантах: 1) обогащение макадамией (МНЖК); 2) пальмовым маслом (НЖК); 3) рапсовым маслом (МНЖК); 4) саффлоровым маслом (ПНЖК). Изучалось влияние диет на профиль липидов и накопление аортального холестерола. В группе с диетой на макадамии по сравнению с группами с диетой на пальмовом и кокосовом масле были ниже концентрации не-HDL-холестерола и ТГ, и выше – HDL по сравнению со всеми другими группами животных. Концентрации аортального холестерола не изменялись при всех типах диет. |
| Yan-Jun Xu и соавт., 2011 | Обзор исследований влияния облепихи на липидный обмен и функции сердечно-сосудистой системы за период до 2011 года. Вывод: кардиопротективный и другие положительные метаболические эффекты связаны с комплексом флавоноидов, антиоксидантов и витаминов. ПОК и другие ЖК не рассматривались. |
| P.S Larmo и соавт., 2013 | Клиническое рандомизированное перекрестное исследование 80 женщин с избыточным весом. 30-дневная пищевая интервенция: сухих ягод облепихи (SBs); облепихового масла (SBo); экстракта ягод в смеси с мальтодекстрином (1:1); мороженных ягод. Оценивался метаболический профиль сыворотки крови с помощью 1H ЯМР спектроскопии. Вывод: Все виды интервенции умеренно улучшают метаболический профиль, снижая LDL и ТГ, повышая HDL. Действие имеет прямую корреляционную зависимость от выраженности исходного профиля кардиометаболического риска. |
| E.A.Lima и соавт., 2014 | Экспериментальное исследование у мышей влияния добавок масла орехов макадамии (2 г/кг в день, три раза в неделю в течение 12 недель) на инсулиночувствительность, воспаление, профиль липидов и размер адипоцитов в условиях высокожировой диеты, вызывающей ожирение. Выводы: высокожировая диета вызывает воспаление жировой ткани, реакцию перитонеальных макрофагов и гипертрофию адипоцитов. Добавки масла макадамии уменьшают эти явления. |
| М. Sayegh и соавт., 2014 | Обзор потенциального использования облепихи в лечении сердечно-сосудистых заболеваний и в других областях медицины за период до 2014 года. Отмечено положительное влияние на профиль липидов и снижение воспаления, однако большинство исследований у человека и в эксперименте носят ограниченный характер, недостаточную доказательную силу. Трактовка полученных данных затруднена из-за множества активных компонентов состава облепихи, обладающих по отдельности разнонаправленным эффектом. Вопрос роли омега-7 МНЖК не рассматривался. |
| Примечания | ПОК – пальмитолеиновая кислота; ПК – пальмитиновая кислота. Облепиховое масло – первый по процентному содержанию ПОК источник (26-36% от общего количества ЖК). Проблема облепихового масла состоит в равном количестве ПОК и ее антагониста в плане влияния на метаболизм липидов и глюкозы – атерогенной ПК (примерно 1:1).Масло орехов макадамии – второй по процентному содержанию ПОК источник (65% олеиновой кислоты (C18:1) и 18% ПОК (C16:1) от общего содержания ЖК, содержание ПК составляет 8-9%. АНА – Американская Кардиологическая Ассоциация. НЖК – насыщенные ЖК. МНЖК – мононенасыщенные ЖК. ПНЖК – полиненасыщенные ЖК. ТГ – триглицериды. HDL – липопротеиды высокой плотности, LDL – липопротеиды низкой плотности. ИМТ – индекс массы тела. |
Таблица 8. Суммарные данные экспериментальных и клинических исследований омега-7 МНЖК – ПОК (50% концентрат)
| Авторы, год | Краткое содержание, результаты и выводы работы |
|---|---|
| K.Maedler и соавт., 2003 | Исследование на культуре бета-клеток поджелудочной железы человека. 4-х дневная экспозиция ПК и высокой концентрации глюкозы вызывает апоптоз бета-клеток, снижает их пролиферацию и повреждает функцию. ПОК стимулирует пролиферацию бета-клеток и антагонизирует эффекты ПК и высокой концентрации глюкозы. Вывод: ПОК – антагонист ПК по влиянию на углеводный обмен. |
| N.Dimopoulos и соавт., 2006 | Сравнение у крыс влияния ПОК и ПК на действие инсулина и утилизацию глюкозы. ПОК способствует транспорту глюкозы в клетках скелетных мышц и увеличивает в 2 раза ее концентрацию, усиливает окисление глюкозы и образование гликогена. ПК оказывает антагонистическое д-е по отношению к ПОК. Вывод: диета с ПОК ускоряет обмен глюкозы в обычных и инсулин-резистентных скелетных мышцах. |
| H.Cao и соавт., 2008 | Изучение метаболизма липидов и глюкозы в жировой ткани мышей в норме и в условиях их нарушения, и действия инсулина. Вывод: ПОК является специфическим липидным гормоном (липокином) адипозной ткани, который стимулирует д-е инсулина в мышцах, снижает уровень печеночных ТГ, подавляет экспрессию цитокинов в адипоцитах, снижает экспрессию печеночных ферментов, имеющих отношение к формированию инсулиночувствительности. |
| Y.Akazawa и соавт., 2010 | Исследования с инкубацией изолированных первичных гепатоцитов, клеток Huh-7 и Hep 3B человека и мышей в питательных средах с добавлением ПК и ПОК. Вывод: ПОК редуцирует липоапоптоз, вызываемый ПК у всех видов печеночных клеток, снижает стресс-ответ эндоплазматического ретикулюма на ПК, угнетает дисрегулирующее влияние ПК на ряд ферментных систем печени. |
| Z.H.Yang и соавт., 2011 | Исследование хронического введения ПОК на инсулинорезистентность и накопление липидов в печени у мышей с генетическим диабетом II. ПОК предупреждает увеличение веса тела, значительно увеличивает чувствительность к инсулину (преодолевает инсулинорезистентность), предотвращает апоптоз бета-клеток, снижает накопление липидов в печени. Вывод: ПОК снижает гипергликемию и гипертриглицеридемию за счет повышения чувствительности к инсулину, подавления экспрессии провоспалительных генов и улучшения метаболизма липидов в печени у мышей с диабетом. |
| S.Shiba и соавт., 2011 | Экспериментальное 2-х недельное исследование на мышах перорального введения ПОК (омега-7 МНЖК) и EPA (омега-3 ПНЖК), полученных из рыбьего жира. Выявлено существенное снижение уровней липидов в печени и плазме крови как при введении ПОК, так и EPA. Вывод: ПОК и EPA даже при краткосрочном (2 недели) применении обладают синергичным положительным влиянием на липидный обмен при ожирении, что может быть основанием для создания комбинированных форм этих ЖК с целью клинического использования. в условиях высокожировой диеты, вызывающей ожирение. |
| Z.H.Yang и соавт., 2013 | Продолжение исследований 2011 года на крысах при пероральном краткосрочном введении ПОК. ПОК снижает (по сравнению с ПК и омега-9 олеиновой кислотой) потребление пищи, в том числе – и в составе ТГ. Оливковое масло таким эффектом не обладало. ПОК дозо-зависимо накапливается в тонком кишечнике и повышает уровни холецистокинина. ПОК не влияет на экспрессию PPARα, а антагонисты PPARα не влияют на насыщающий эффект ПОК. Вывод: пероральное введение ПОК вызывает эффект насыщения, в механизме которого не принимает участие PPARα, что отличает ПОК от статинов и фибратов. |
| T.A.Burns и соавт., 2013 | Исследование влияния ПОК (в/в инфузия в дозе 5 мг/кг веса тела, средний вес = 87 кг, общая доза около 450 мг) у овец с ожирением на эффект в/в введения глюкозы (0,25 г/кг) и инсулина (0.02 μU/кг). Через 2 мин после введения уровень ПОК в плазме возрастал в 10 раз, а через 30 мин возвращался к исходной величине. Вывод: ПОК повышает чувствительность к инсулину у животных с ожирением. |
| S.K.Duckett и соавт., 2014 | Влияние в/в инфузии ПОК (5-10 мг/кг/день в течение 28 дней) овцам с ожирением на липогенез и уровни циркулирующего в крови инсулина. Концентрация ПОК в крови возрастала линейно в процессе исследования с параллельным линейным увеличением концентрации других омега-ЖК: VA, EPAи DHA. ПОК снижала прирост веса тела на 77%, уменьшала в дозе 10 мг/кг/день размеры внутримышечных адипоцитов, снижала уровни инсулина на 14-ы и 21-ый дни инфузии, общий уровень липидов в мышцах и мезентериальной адипозной ткани в дозах 5 и 10 мг/кг/день. Вывод: в/в инфузия ПОК в течение 28 дней тормозит прирост веса тела, уменьшает размеры внутримышечных адипоцитов, общее содержание липидов и уровни циркулирующего инсулина. Эти изменения могут опосредоваться нарушением экспрессии генов, регулирующих поступление глюкозы и окисление ЖК, особенно в мышцах. |
| A.Bolsoni-Lopes и соавт., 2014 | Исследование на культуре первичных адипоцитов и T3-L1 клеток мышей. Сравнение эффектов ПОК, ПК и олеиновой ЖК, предварительно вводимых системно (300 мг/кг/день) в течение 10 дней. ПОК (но не другие ЖК) увеличивает инсулин-индуцированное поступление глюкозы в клетки и уровень в них белка. ПОК повышает окисление глюкозы (аэробный гликолиз), конверсию в лактат (анаэробный гликолиз) и включение в глицерол-TAG, но снижает de novo синтез ЖК из глюкозы и ацетата и активность липогенных ферментов глюкозы-6-фосфат дегидрогеназы и АТФ-цитрат лиазы. Вывод: ПОК обладает несколькими механизмами: снижает продукцию глюкозы в печени; стимулирует поступление глюкозы в клетки скелетной мускулатуры; усиливает поступление глюкозы и ее метаболизм в адипоцитах; снижает синтез ЖК за счет активации AMPK. |
| M.I.Alonso-Vale и соавт., 2015 | ПОК продуцируется и выделяется адипоцитами, и оказывает влияние на распределение глюкозы. ПОК снижает проявления гепатостеатоза у мышей, защищает бета-клетки поджелудочной железы от повреждающих эффектов ПК и улучшает профиль липидов. ПОК – модулятор липолиза в адипоцитах и содержания главных липаз - ATGL и HSL через PPARα – механизмы in vivo и in vitro. Вывод: ПОК стимулирует липолиз, митохондриальное окисление ЖК, что может вносить вклад в повышение расхода энергии адипоцитами. |
| N.Morse, 2015a | Обзор результатов доклинических и эпидемиологических исследований у человека ПОК (цис-форма). Анализ доказательств наличия противовоспалительного и липидопонижающего действия, связанных с предотвращением метаболического синдрома, включая сердечно-сосудистые заболевания и инсулинорезистентность при диабете и ожирении. |
| J.Green, 2012 | Клиническое исследование на пациентах с высоким риском нарушений липидного обмена. Вывод: ПОК снижает уровни высокочувствительного С-реактивного белка, ТГ, LDL, не-HDL и общего холестерола, уменьшая риск развития сердечно-сосудистых метаболических нарушений. |
| L.Martinez, 2013a | Открытое клиническое исследование ПОК. Показано снижение уровней липидов и С-реактивного белка, снижение веса. Предварительные данные (внутренний отчет). Подробные результаты в публикации этой группы авторов (A.M.Bernstein и соавт., 2014) |
| L.Martinez, 2013b | Двойное-слепое рандомизированное плацебо-контролируемое клиническое исследование ПОК. Показано снижение уровней липидов и высоко-чувствительного С-реактивного белка. Предварительные данные (внутренний отчет). Подробные результаты в публикации этой группы авторов (A.M.Bernstein и соавт., 2014) |
| A.M.Bernstein и соавт., 2014 | Двойное-слепое рандомизированное плацебо-контролируемое 30-дневное клиническое исследование ПОК в разовой суточной дозе 220,5 мг у взрослых пациентов (старше 21 года, n=60) с дислипидемией и умеренным системным воспалением (hs-CRP – 2-5 мг/л). Результаты: снижение hs-CRP (на 44%), ТГ (на 15%) и LDL (на 8%), возрастание HDL (на 5%). Подробнее в тексте обзора (прим. авторов). |
| N.Morse, 2015b | Обзор результатов исследований ПОК у человека за последние несколько лет. Хотя имеющиеся данные позволяют предполагать революционный характер сделанного открытия положительных свойств ПОК (цис-форма) в отношении регуляции липидного и углеводного обмена, требуются дополнительные расширенные исследования, соответствующие международным стандартам, особенно в лечении метаболического синдрома. |
| Примечания | ЖК – жирные кислоты; ПОК – пальмитолеиновая кислота; ПК – пальмитиновая кислота; VA – вакценовая кислота; EPA – эйкозапентаеновая кислота; DHA – докозагексаеновая кислота; ТГ – триглицериды; PPARα - рецептор, активируемый пероксисомными пролифераторами (рeroxisome proliferator-activated receptors) – звено в механизме действия фибратов и статинов; LDL – липопротеиды низкой плотности; HDL – липопротеиды высокой плотности; hs-CRP – высокочувствительный С-реактивный белок; ATGL – липаза HSL – липаза; AMPK - 5'АМФ-активируемая протеинкиназа - клеточная протеинкиназа, контролирующая энергетический баланс клетки. Активируется при значительном потреблении энергии клетки (например, при физической нагрузке) и нарастании внутриклеточного уровня АМФ. В результате активации АМФК клетка переходит в энергосберегающее состояние (в том числе блокирует синтез жирных кислот и активирует их окисление). |
Таблица 9. Показатели липидного обмена и С-реактивного белка плазмы крови до и после 30-дневного однократного перорального приема ПОК в дозе 220,5 мг и плацебо в исследовании A.M.Bernstein и соавторов (2014)
| Показатель | ПОК (n=30) | Плацебо (n=30) | Абсолютные изменения* | Р |
|---|---|---|---|---|
| CRP (мг/л) Исходное значение Через 30 дней |
4,3±0,2 2,1±0,2 |
4,3±0,1 4,0±0,2 |
-1,9 (-2,3 до 1,4) | <0,0001 |
| ТГ (мг/дл) Исходное значение Через 30 дней |
202,4±11,9 170,3±9,6 |
210,6±11,0 207,2±10,7 |
-30,2 (-40,2 до -25,3) | <0,0001 |
| LDL холестерол (мг/дл) Исходное значение Через 30 дней |
114,1±4,3 105,8±3,7 |
119,6±4,9 119,2±4,3 |
-8,9 (-12,0 до -5,8) | <0,0001 |
| HDL-холестерол (мг/дл) Исходное значение Через 30 дней |
45,7±1,0 47,1±0,9 |
43,3±1,0 42,7±0,9 |
+1,4 (1,5-3,3) | <0,0001 |
*- эффект абсолютных изменений устанавливался по математической модели с учетом сдвигов в обеих группах.
Как видно из таблицы 9, между двумя группами не было значимых различий в исходных показателях. Через 30 дней в группе с ПОК отмечено существенное снижение уровней СRP (44%), ТГ (15%) и LDL (8%), и умеренное повышение HDL (5%). По мнению авторов, полученные данные свидетельствуют о снижении показателей двух факторов риска (дислипидемии и системного воспаления) под влиянием омега-7 МНЖК (пальмитолеиновой кислоты - ПОК). Это позволяет рассматривать ПОК в качестве нового перспективного вещества для коррекции метаболических нарушений в условиях умеренной дислипидемии и системного воспаления.
Заключение[править | править код]
Проведенные экспериментальные и клинические исследования омега-7 МНЖК в виде выделенного из рыбьего жира концентрата пальмитолеиновой кислоты (ПОК), а также, в меньшей степени, ряда источников с повышенным содержанием этой кислоты (масло макадамии, некоторых форм облепихового масла) позволяют предположить, что ПОК может рассматриваться как эндогенный регулятор липидного обмена.
ПОК синтезируется в организме в печени и жировой ткани и, выделяясь в кровоток, повышает чувствительность клеток тканей к инсулину, уменьшает инсулинорезистентность при патологических состояниях, нормализует профиль липидов (повышение липопротеидов высокой плотности, снижение липопротеидов низкой плотности, триглицеридов и общего холестерола), снижает уровень маркера системного воспаления – С-реактивного белка. Гарвардская школа (H.Cao и соавт., 2008) рассматривают ПОК как гормон (липокин) адипозной ткани млекопитающих и связующее звено между жировой тканью и другими органами, регулирующий обмен липидов и углеводов и оказывающий защитное действие при метаболическом синдроме. Этот механизм принципиально отличает ПОК, как омега-7 МНЖК, от широко изученных и используемых омега-3 ПНЖК.
В экспериментальных исследованиях in vitro и in vivo ПОК способствует транспорту глюкозы в клетках обычных и инсулинорезистентных скелетных мышц и увеличивает в 2 раза ее концентрацию; усиливает окисление глюкозы и образование гликогена; антагонизирует действие атерогенной пальмитиновой кислоты (ПК) и предотвращает негативное влияние ПК и высоких концентраций глюкозы на бета-клетки поджелудочной железы; снижает концентрации липопротеидов низкой плотности, триглицеридов и общего холестерола и повышает липопротеиды высокой плотности в плазме при ожирении; снижает продукцию провоспалительных цитокинов; снижает прирост массы тела, размеры внутримышечных адипоцитов и воспалительные реакции жировой ткани; снижает образование атеросклеротических бляшек.
В клинических исследованиях, пока еще очень малочисленных, получены первые доказательства улучшения профиля липидов плазмы крови и снижения уровней С-реактивного белка при системном воспалительном процессе, которое достигает очень существенных величин (более 50%). Это может иметь прикладное значение для снижения микроповреждений скелетной мускулатуры и болезненности мышц после физических нагрузок, и ускорения восстановления спортсменов.
На основании этих данных омега-7 МНЖК (ПОК) может рассматриваться в качестве фармаконутриента, сочетающего свойства нутриента (сродство эндогенному активному соединению, участие в построении фосфолипидов клеточных мембран, образовании энергии и т.д.) и фармакологического агента с присущей последним дозо-зависимостью эффекта, диапазоном терапевтического действия, специфичностью воздействия на конкретные звенья регуляции обмена, антагонизм по отношению к атерогенной пальмитиновой кислоте. К особенностям клинического действия ПОК можно отнести: малую величину эффективных доз (200-220 мг/день; в 2,5-3 раза меньше доз омега-3 ПНЖК); однократный прием для достижения клинического результата при приеме в течение 30 дней; чрезвычайно выраженное снижение (на 50% и более) маркеров системного воспаления (С-реактивный белок); быстрое развитие положительных изменений показателей липидного обмена и системного воспаления (2 недели применения); синергизм с действием омега-3 ПНЖК при совместном использовании, что служит основанием для их комбинирования в клинической практике; наличие ряда доказательств различий в биохимическом механизме действия этих двух классов ЖК на уровне клеток организма.
Таким образом, исследования in vitro и in vivo, а также клинические исследования дают достаточно оснований для применения ПОК в качестве биологически активного вещества для профилактики (в группах риска) и лечения нарушений липидного обмена и/или ожирения (избыточного веса) без или в сочетании с признаками системного воспаления. В рутинной клинической практике ПОК уже применяется в ряде клиник Северной Америки и Великобритании.
В настоящее время нет данных об эргогенных свойствах омега-7 МНЖК. Однако, с точки зрения спортивной нутрициологии, имеется достаточно клинических доказательств для включения разных форм омега-7 МНЖК в программы снижения веса при занятиях фитнессом и других видах физических нагрузок, что уже имеет место в США и Канаде. Комбинирование ПОК с омега-3 и омега-5 ПНЖК также может оказаться эффективным в этом плане, как и сочетание с другими фармакологическими препаратами для контроля веса. С научной точки зрения, интересны исследования у профессиональных спортсменов при направленном изменении состава тела (повышение ТМТ при снижении жировой массы).
Читайте также[править | править код]
- Бета-аланин: научный обзор
- Глутамин: научный обзор
- HMB: научный обзор
- Донаторы оксида азота: научный подход
- Креатин: научный обзор
- Нейростимуляторы и нейропротекторы в спортивном питании: научный обзор
- Омега-3 жирные кислоты: научный обзор
- Омега-5 жирные кислоты: научный обзор
- Спортивные напитки: научный обзор
- Препараты витамина D в спортивной медицине: научный обзор
Ссылки[править | править код]
- Горемыкина Н.В., Верещагин А.Л., Бычин Ю.А., Кошелев Ю.А. Сравнение триглицеридного состава облепихового масла алтайского края методом дифференциальной сканирующей калориметрии. Техника и технология пищевых производств. 2015. Т. 37. № 2, 104-109.
- Akazawa Y., Cazanave S., Mott J.L. et al. Palmitoleate attenuates palmitate-Induced Bim and PUMA up-regulation and hepatocyte lipoapoptosis. J.Hepatol. 2010, 52:586-593.
- Alonso-Vale M.I., Cruz M., Bolsoni-Lopes A., de Sá R. de Andrade P. Palmitoleic Acid (C16:1n7) Treatment Enhances Fatty Acid Oxidation and Oxygen Consumption in White Adipocytes. The FASEB Journal, 2015, vol. 29 no. 1, Supplement 884.25
- Barthet V.J. (n-7) and (n-9) cis-Monounsaturated fatty acid contents of 12 Brassica species. Phytochemistry. 2008, 69(2):411-417.
- Benoit S.C., Kemp C.J., Elias C.F., et al. Palmitic acid mediates hypothalamic insulin resistance by altering PKC-θ subcellularlocalization in rodents. J. Clin. Invest. 2009, 119(9):2577-2589.
- Bernstein A.M., Roizen M.F., Martinez L. Purified Palmitoleic Acid for the Reduction of High Sensitivity C-Reactive Protein and Serum Lipids: A double-blinded, randomized, placebo controlled study. J.Clin.Lipidology, 2014, 8, 612-617.
- Bolsoni-Lopes A., Festuccia W.T., Chimin P. et al. Palmitoleic acid (n-7) increases white adipocytes GLUT4 content and glucose uptake in association with AMPK activation. Lipids in Health and Disease 2014, 13:199-209.
- Burns T.A., Long N.M., Alende G. et al. Palmitoleic (C16:1) acid alters glucose and insulin metabolism in obese lambs. J. Anim. Sci. 2013.v. 91 (E-Suppl. 2), J. Dairy Sci. v. 96 (E-Suppl. 1): 391 (abstr. W279).
- Cao H., Gerhold K., Mayers J.R. et al. Identification of a lipokine, a lipid hormone linking adipose tissue to systemic metabolism. Cell. 2008, 134(6):933-944.
- Curb J.D., Wergowske G., Dobbs J.C. et al. Serum lipid effects of a high-monounsaturated fat diet based on macadamia nuts. Archives of Internal Medicine, 2000, v.160, 8, 1154–1158.
- Dimopoulos N., Watson M., Sakamoto K., Hunda H.S. Differential effects of palmitate and palmitoleate on insulin action and glucose utilization in rat L6 skeletal muscle cells. Biochem. J. 2006, 399:473-481.
- Duckett S.K. et al. Effect of palmitoleic acid on body composition and adipocyte cell size in obese sheep. J. Anim. Sci. Vol. 91 (E-Suppl. 2)/J. Dairy Sci. Vol. 96 (E-Suppl. 1): 391 (abstr. W278). 2013.
- Garaulet M., Hernandez-Morante J.J., Tebar F.J., Zamora S. Relation between degree of obesity and site-specific adipose tissue fatty acid composition in a Mediterranean population. Nutrition. 2011, 27(2):170-176.
- Green J.A. Effect of two levels of Provinal™ (purified Palmitoleic Acid; C16:1n7; Omega 7) on serum lipid and C-reactive protein(CRP) profiles in humans. Tersus Pharmaceuticals, LLC: 2012
- Griel A.E., Cao Y., Bagshaw D. D. et al. A Macadamia nut-rich diet reduces total and LDL-cholesterol in mildly hypercholesterolemic men and women. Journal of Nutrition, 2008, v.138, 4, 761–767.
- Higuchi T., Shirai N., Saito M., Suzuki H., Kagawa Y. Levels of plasma insulin, leptin and adiponectin, and activities of key enzymes in carbohydrate metabolism in skeletal muscle and liver in fasted ICR mice fed dietary n-3 polyunsaturated fatty acids. J.Nutr.Biochem. 2008, 19, 577-586.
- Hiraoka-Yamamoto J., Ikeda K., Negishi H. et al., “Serum lipid effects of a monounsaturated (palmitoleic) fatty acid-rich diet based on macadamia nuts in healthy, young japanese women,”
- Clin. Exper. Pharmacol. Physiol., 2004, v.l, 31, suppl. 2, pp. S37–S38.
- Hong D.D., Takahashi Y., Kushiro M., Ide T. Divergent effects of eicosapentaenoic and docosahexaenoic acid ethyl esters, and fish oil on hepatic fatty acid oxidation in the rat. Biochem.Biophys.Acta. 2003, 1635, 29-36.
- Ide T., Hong D.D., Ranasinghe P., Takahashi Y. et al. Interaction of dietary fat types and sesamin on hepatic fatty acid oxidation in rats. Biochim Biophys Acta. 2004, 1682:80–91.
- Larmo P.S., Alin J., Salminen E., Kallio H., Tahvonen R. Effects of sea buckthorn berries on infections and inflammation: a double-blind, randomized, placebo-controlled trial. Eur. J. Clin. Nutr. 2008, 62:1123–1130.
- Larmo P.S., Kangas A.J., Soininen P. et al. Effects of sea buckthorn and bilberry on serum metabolites differ according to baseline metabolic profiles in overweight women: a randomized crossover trial. Am. J. Clin. Nutr. 2013, 1-11.
- Lima E.A., Silveira L.S., Masi L.N. et al. Macadamia Oil Supplementation Attenuates Inflammation and Adipocyte Hypertrophy in Obese Mice. Hindawi Publishing Corporation Mediators of Inflammation, v.2014, Article ID 870634, 9 pages.
- Long N.M., Burns T.A., Volpi Lagreca G. et al. Palmitoleic Acid Infusion Alters Circulating Glucose and Insulin Levels. J.Metabolic.Syndr., 2014, 3:3,1-6.
- Maedler K., Oberholzer J., Bucher P., Spinas G.A., Donath M.Y. Monounsaturated fatty acids prevent the deleterious effects of palmitate and high glucose on human pancreatic β-cell turnover and function. Diabetes. 2003, 52:726-733.
- Martinez L. Lipid and CRP reductions observed with the administration of purified palmitoleic acid: an open label trial. Proprietary research report, 2013a.
- Martinez L. Provinal (R) in the reduction of CRP: A double blinded, randomized, placebo controlled study.Provinal purified omega 7. Vol: Tersus Pharmaceuticals; 2013b.
- Matthan N.R., Dillard A., Lecker J. L. et al. Effects of dietary palmitoleic acid on plasma lipoprotein profile and aortic cholesterol accumulation are similar to those of other unsaturated fatty acids in the golden Syrian hamster. The Journal of Nutrition, 2009, v.139, 2, 215–221.
- Morse N. Lipid-lowering and anti-inflammatory effects of palmitoleic acid: Evidence from preclinical and epidemiological studies. Lipid Technology 05/2015a; 27(5).
- Morse N. Lipid‐lowering and anti‐inflammatory effects of palmitoleic acid: Evidence from human intervention studies. Lipid Technology 07/2015b; 27(7).
- Mozaffarian D., Cao H., King I.B. et al. Circulating palmitoleic acid and risk of metabolic abnormalities and new-onset diabetes. Am. J. Clin. Nutr. 2010, 92(5):1350-1358.
- Savage D.B., Petersen K.F., Shulman G.I. Disordered lipid metabolism and the pathogenesis of insulin resistance. Physiol.Rev., 2007, 87, 507-520.
- Sayegh М., Miglio С., Ray S. Potential cardiovascular implications of Sea Buckthorn berry consumption in humans. Int. J Food Sci. Nutr.,2014, 1-8.
- Shiba S., Tsunoda N., Wakutsu M. et al. Regulation of lipid metabolism by palmitoleate and eicosapentaenoic acid (EPA) in mice fed a high fat diet. Biosci. Biotechnol. Biochem. 2011, 75:2401–2403.
- Stefan N., Kantartzis K., Celebi N. et al. Circulating palmitoleate strongly and independently predicts insulin sensitivity in humans. Diabetes Care. 2010, 33:405-407.
- Xu Y-J., Kaur M., Dhillon R.S. et al. Health benefits of sea buckthorn for the prevention of cardiovascular diseases. J.Functional Food, 2011, 3: 2-12.
- Yang Z.H., Miyahara H., Hatanaka A. Chronic administration of palmitoleic acid reduces insulin resistance and hepatic lipid accumulation in KK-Ay Mice with genetic type 2 diabetes. Lipids Health Dis. 2011, 10:120.
- Yang Z.H., Takeo J., Katayama M. Oral administration of omega-7 palmitoleic acid induces satiety and the release of appetite-related hormones in male rats. Appetite. 2013, 65:17.