Метаболический синдром — различия между версиями
Marta (обсуждение | вклад) (→Роль ожирения в развитии метаболического синдрома) |
Sint (обсуждение | вклад) |
||
| (не показано 11 промежуточных версий 3 участников) | |||
| Строка 5: | Строка 5: | ||
=== История === | === История === | ||
| − | В 1922 г. Г.Ф. Ланг в своих трудах отмечал наличие ассоциации артериальной гипертензии и [[Ожирение|ожирения]], нарушений обмена углеводов и подагры, об этой связи доложили на Х съезде терапевтов его сотрудники А.Л. Мясников | + | ''В 1922 г.'' Г.Ф. Ланг в своих трудах отмечал наличие ассоциации артериальной гипертензии и [[Ожирение|ожирения]], нарушений [[Углеводный обмен (наглядная биохимия)|обмена углеводов]] и [[Лечение подагры|подагры]], об этой связи доложили на Х съезде терапевтов его сотрудники А.Л. Мясников и Д.М. Гротель. |
| − | 1923 г. шведский исследователь E.Kylin. впервые указал связь [[Гипертония и спорт (повышенное артериальное давление)|артериальной гипертензии]] (АГ) с [[Сахарный диабет - действие инсулина|гипергликемией]] и гиперурикемией. | + | ''1923 г.'' шведский исследователь E.Kylin. впервые указал связь [[Гипертония и спорт (повышенное артериальное давление)|артериальной гипертензии]] (АГ) с [[Сахарный диабет - действие инсулина|гипергликемией]] и гиперурикемией. |
| − | В 1948 г. выдающийся клиницист Е.М. Тареев отмечал: « Представление о гипертонике наиболее часто ассоциируется с ожирелым гиперстеником, с возможным нарушением белкового обмена, с засорением крови продуктами неполного метаморфоза- | + | ''В 1948 г.'' выдающийся клиницист Е.М. Тареев отмечал: « Представление о гипертонике наиболее часто ассоциируется с ожирелым гиперстеником, с возможным нарушением белкового обмена, с засорением крови продуктами неполного метаморфоза-[[холестерин]]ом, мочевой кислотой». |
| − | В 1966 г. связь сахарного диабета и атеросклероза описал Л.С. Шварц. В это же время J.Camus назвал сочетание у одного и того же больного сахарного диабета, дислипидемии и поражения суставов ''метаболическим трисиндромом''. | + | ''В 1966 г.'' связь сахарного диабета и атеросклероза описал Л.С. Шварц. В это же время J.Camus назвал сочетание у одного и того же больного сахарного диабета, дислипидемии и поражения суставов ''метаболическим трисиндромом''. |
| − | В 1968 г. H.Mehnert и H. Kuhlman обозначили сочетание нарушения обменов как ''« синдром изобилия»''. | + | ''В 1968 г.'' H.Mehnert и H. Kuhlman обозначили сочетание нарушения обменов как ''« синдром изобилия»''. |
| − | M. Hannefeld и W. Leonard в 1981 г. впервые сделали подробное описание ''метаболического синдрома''. В силу существования в эпоху «холодной войны» политической тенденциозности, труды исследователей из России и стран «Восточного блока» замалчивались медицинской общественностью Запада. | + | M. Hannefeld и W. Leonard ''в 1981 г.'' впервые сделали подробное описание ''метаболического синдрома''. В силу существования в эпоху «холодной войны» политической тенденциозности, труды исследователей из России и стран «Восточного блока» замалчивались медицинской общественностью Запада. |
| − | В 1988 г. G. Reaven в своей Бантингской лекции, обобщив эпидемиологические, клинические и экспериментальные данные, выдвинул концепцию, в которой указал, что резистентность к [[инсулин]]у, абдоминальное ожирение, АГ, дислипидемия и [[Сердечно-сосудистая патология|коронарная болезнь сердца]] являются проявлением единого патологического состояния, обозначенного им как ''« Синдром Х»''. | + | ''В 1988 г.'' G. Reaven в своей Бантингской лекции, обобщив эпидемиологические, клинические и экспериментальные данные, выдвинул концепцию, в которой указал, что резистентность к [[инсулин]]у, абдоминальное ожирение, АГ, дислипидемия и [[Сердечно-сосудистая патология|коронарная болезнь сердца]] являются проявлением единого патологического состояния, обозначенного им как ''« Синдром Х»''. |
| − | А. Regenauer | + | А. Regenauer ''в 1988 г.'', описывая прогностические аспекты МС, назвал его «good life syndrome», то есть ''« синдром благополучия»'' (сытости). |
| − | В 1989 г. N. Kaplan привел данные популяционных исследований, свидетельствующие о неблагоприятном жизненном и трудовом прогнозе у больных с сочетанием ожирения, сахарного диабета, АГ и коронарной болезни сердца, назвав симптомокомплекс ''«смертельным квартетом»''. | + | ''В 1989 г.'' N. Kaplan привел данные популяционных исследований, свидетельствующие о неблагоприятном жизненном и трудовом прогнозе у больных с сочетанием ожирения, сахарного диабета, АГ и коронарной болезни сердца, назвав симптомокомплекс ''«смертельным квартетом»''. |
| − | В последние годы в исследовательской и практической медицине укоренился термин | + | В последние годы в исследовательской и практической медицине укоренился термин «метаболический синдром», сущность его постепенно расширялась, так как стали выявляться ранее неизученные нарушения, наблюдавшиеся у части больных. |
| − | А.И.Мартынов в 2000 отнес к ним повышенное содержание фибриногена, уровня «малых» липопротеинов, [[Ингибитор активатора плазминогена-1|ингибитора-1 активатора плазминогена]] и микроальбуминурию<ref>Колопкова Т. А. и др. МЕТАБОЛИЧЕСКИЙ СИНДРОМ Х-ПАНДЕМИЯ XXI ВЕКА //Саратовский научно-медицинский журнал. – 2008. – Т. 4. – №. 3.</ref>. | + | А.И.Мартынов ''в 2000 г.'' отнес к ним повышенное содержание фибриногена, уровня «малых» липопротеинов, [[Ингибитор активатора плазминогена-1|ингибитора-1 активатора плазминогена]] и микроальбуминурию<ref>Колопкова Т. А. и др. МЕТАБОЛИЧЕСКИЙ СИНДРОМ Х-ПАНДЕМИЯ XXI ВЕКА //Саратовский научно-медицинский журнал. – 2008. – Т. 4. – №. 3.</ref>. |
Результатом совместной работы ведущих международных организаций по изучению МС явилось создание нового определения. В настоящее время для установления диагноза необходимо наличие трех из пяти нижеперечисленных критериев. | Результатом совместной работы ведущих международных организаций по изучению МС явилось создание нового определения. В настоящее время для установления диагноза необходимо наличие трех из пяти нижеперечисленных критериев. | ||
| Строка 44: | Строка 44: | ||
Выделяют два типа ожирения, различающихся по локализации скоплений [[Жировая ткань|жировой ткани]], - андроидный и гиноидный. | Выделяют два типа ожирения, различающихся по локализации скоплений [[Жировая ткань|жировой ткани]], - андроидный и гиноидный. | ||
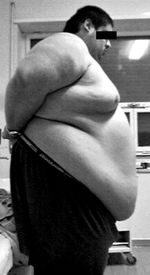
[[Image:Androidnoe.jpg|150px|thumb|left|Андроидное (висцеральное) ожирение у мужчины]] | [[Image:Androidnoe.jpg|150px|thumb|left|Андроидное (висцеральное) ожирение у мужчины]] | ||
| − | *''Абдоминальное (висцеральное) ожирение'' — один из основных клинических симптомов метаболического синдрома, которое является важным фактором риска сердечно-сосудистых и других заболеваний (рис. 1), сахарного диабета II типа и ранних проявлений атеросклероза<ref>Ruderman N., Flier J. S. Chewing the Fat--ACC and Energy Balance //Science. – 2001. – Т. 291. – №. 5513. – С. 2558-2559.</ref>. Андроидный тип характеризуется гипертрофией адипоцитов и обычно наблюдается у лиц зрелого возраста. Избыточное отложение жира происходит в области верхней половины туловища, живота. Растет масса висцерального жира. Этот тип ожирения обычно называют центральным или абдоминальным, а также «яблочным». | + | *''Абдоминальное ('''висцеральное''') ожирение'' — один из основных клинических симптомов метаболического синдрома, которое является важным фактором риска сердечно-сосудистых и других заболеваний (рис. 1), сахарного диабета II типа и ранних проявлений атеросклероза<ref>Ruderman N., Flier J. S. Chewing the Fat--ACC and Energy Balance //Science. – 2001. – Т. 291. – №. 5513. – С. 2558-2559.</ref>. Андроидный тип характеризуется гипертрофией адипоцитов и обычно наблюдается у лиц зрелого возраста. Избыточное отложение жира происходит в области верхней половины туловища, живота. Растет масса висцерального жира. Этот тип ожирения обычно называют центральным или абдоминальным, а также «яблочным». |
Kissebah A. и Bjorntorp P. показали<ref>Kissebah A. H., Krakower G. R. Regional adiposity and morbidity //Physiological Reviews. – 1994. – Т. 74. – №. 4. – С. 761-811.</ref>, что при одинаковом показателе [[Индекс массы тела|индекса массы тела]] (ИМТ) абдоминальное ожирение сопровождается более высоким риском развития сопутствующих заболеваний, чем периферическое ожирение.Именно поэтому выраженность осложнений ожирения является более высокой у мужчин, чем у женщин<ref>БО Ш., САВЕЛЬЕВА Л. В. КОМПЛЕКСНЫЙ ПОДХОД К ЛЕЧЕНИЮ ОЖИРЕНИЯ И МЕТАБОЛИЧЕСКОГО СИНДРОМА У МУЖЧИН //Ожирение и метаболизм. – 2009. – №. 4.</ref>. | Kissebah A. и Bjorntorp P. показали<ref>Kissebah A. H., Krakower G. R. Regional adiposity and morbidity //Physiological Reviews. – 1994. – Т. 74. – №. 4. – С. 761-811.</ref>, что при одинаковом показателе [[Индекс массы тела|индекса массы тела]] (ИМТ) абдоминальное ожирение сопровождается более высоким риском развития сопутствующих заболеваний, чем периферическое ожирение.Именно поэтому выраженность осложнений ожирения является более высокой у мужчин, чем у женщин<ref>БО Ш., САВЕЛЬЕВА Л. В. КОМПЛЕКСНЫЙ ПОДХОД К ЛЕЧЕНИЮ ОЖИРЕНИЯ И МЕТАБОЛИЧЕСКОГО СИНДРОМА У МУЖЧИН //Ожирение и метаболизм. – 2009. – №. 4.</ref>. | ||
| − | *При ''гиноидном типе ожирения'' | + | *При ''гиноидном типе ожирения ('''периферическое''')'' происходит гиперплазия жировых клеток, так как он обычно развивается в детстве и наблюдается в течение всей жизни. Гиноидный тип характеризуется преимущественным отложением жира в области ягодиц и бедер, поэтому его называют ягодично - бедренным, или грушевидным. |
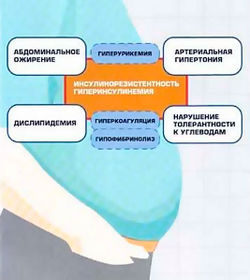
[[Image:Insulinorezistentnoct'.jpg|250px|thumb|right|Рис.2. Компоненты метаболического синдрома. Пунктиром обозначены вторичные проявляния МС]] | [[Image:Insulinorezistentnoct'.jpg|250px|thumb|right|Рис.2. Компоненты метаболического синдрома. Пунктиром обозначены вторичные проявляния МС]] | ||
| − | |||
| − | |||
При развившемся андроидном ожирении с возрастом больного повышается активность центров гипоталамуса и снижается их чувствительность к влияниям с периферии. Последовательность развития нарушений, составляющих метаболический синдром, представляется следующим образом: ожирение - инсулинорезистентность - гиперинсулинемия - артериальная гипертензия - атеросклероз - коронарная болезнь сердца - сахарный диабет II типа<ref>ДЗГОЕВА Ф. Х. Висцеральное ожирение-ключевое звено метаболического синдрома //Ожирение и метаболизм. – 2004. – №. 1.</ref>. | При развившемся андроидном ожирении с возрастом больного повышается активность центров гипоталамуса и снижается их чувствительность к влияниям с периферии. Последовательность развития нарушений, составляющих метаболический синдром, представляется следующим образом: ожирение - инсулинорезистентность - гиперинсулинемия - артериальная гипертензия - атеросклероз - коронарная болезнь сердца - сахарный диабет II типа<ref>ДЗГОЕВА Ф. Х. Висцеральное ожирение-ключевое звено метаболического синдрома //Ожирение и метаболизм. – 2004. – №. 1.</ref>. | ||
=== Инсулинорезистентность в развитии метаболического синдрома === | === Инсулинорезистентность в развитии метаболического синдрома === | ||
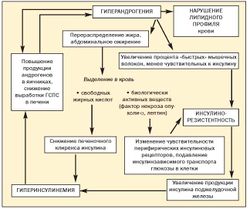
[[Image:Fat4.jpg|250px|thumb|right|Рис.3. Роль гиперандрогении в развитии метаболического синдрома]] | [[Image:Fat4.jpg|250px|thumb|right|Рис.3. Роль гиперандрогении в развитии метаболического синдрома]] | ||
| − | + | Развитие гипертрофического ожирения провоцирует снижение чувствительности периферических тканей к действию инсулина. Именно развитие хронического избытка инсулина в крови большинство исследователей считают “пусковой кнопкой” для возникновения всех заболеваний, входящих в понятие "метаболический синдром"<ref>Благосклонная Я. В., Шляхто Е. В., Красильникова Е. И. Метаболический сердечно-сосудистый синдром //Рус. мед. журн. – 2001. – Т. 9. – №. 2. – С. 67œ70.</ref>(рис.2). | |
| + | |||
| + | До настоящего времени не прекращается дискуссия о первичности или вторичности инсулинорезистентности и гиперандрогении при метаболическом синдроме (рис. 3)<ref>Оганов М. Эпидемиологические аспекты метаболического синдрома. – 2004.</ref>. | ||
| + | |||
| + | ==== Первая гипотеза ==== | ||
| + | |||
| + | ИР — полигенная патология, в развитии которой могут иметь значение '''мутации генов''' субстрата инсулинового рецептора (IRS-1 и IRS-2), β3-адренорецепторов, разобщающего протеина (UCP-1), а также молекулярные дефекты белков сигнального пути [[инсулин]]а (глюкозные транспортеры). Особую роль играет снижение чувствительности к инсулину в мышечной, жировой и печеночной тканях, а также в надпочечниках. | ||
| + | |||
| + | В миоцитах нарушаются поступление и утилизация глюкозы, в жировой ткани развивается резистентность к антилиполитическому действию [[инсулин]]а. Интенсивный [[липолиз]] в висцеральных адипоцитах приводит к выделению большого количества свободных жирных кислот (СЖК) и глицерина в портальный кровоток. Поступая в печень, СЖК, с одной стороны, становятся субстратом для формирования атерогенных липопротеидов, а с другой — препятствуют связыванию инсулина с гепатоцитом, потенциируя ИР. ИР гепатоцитов ведет к снижению синтеза [[гликоген]]а, активации гликогенолиза и [[глюконеогенез]]а. Долгое время ИР компенсируется избыточной продукцией инсулина, поэтому нарушение гликемического контроля манифестирует не сразу. Но, по мере истощения функции β-клеток поджелудочной железы, наступает декомпенсация углеводного обмена, сначала в виде нарушенных гликемии натощак и толерантности к глюкозе (НТГ), а затем и сахарного диабета 2 типа (Т2СД). Дополнительное снижение секреции инсулина при МС вызывается длительным воздействием высоких концентраций СЖК на β-клетки (так называемый липотоксический эффект). При имеющихся генетически обусловленных дефектах секреции инсулина развитие Т2СД значительно ускоряется<ref>Мамедов М. Н. Метаболический синдром: практические аспекты диагностики и лечения в амбулаторных условиях //Москва. – 2005.</ref>. | ||
| − | + | ==== Вторая гипотеза ==== | |
| − | + | Согласно другой гипотезе, ведущую роль в развитии и прогрессировании инсулинорезистентности играет '''[[жировая ткань]]''' абдоминальной области. Особенность висцеральных адипоцитов — высокая чувствительность к липолитическому действию [[Катехоламины|катехоламин]]ов и низкая к антилиполитическому действию инсулина. | |
| − | + | Помимо веществ, непосредственно регулирующих липидный обмен, жировая клетка продуцирует [[эстрогены]], [[Иммунная система|цитокины]], ангиотензиноген, [[ингибитор активатора плазминогена-1]], липопротенлипазу, адипсин, [[Адипонектин|адинопектин]], [[интерлейкин-6]], [[Фактор некроза опухоли-альфа|фактор некроза опухолей-α]] (ФНО-α), трансформирующий фактор роста В, [[лептин]] и др. | |
| − | + | ФНО-α способен воздействовать на инсулиновый рецептор и транспортеры глюкозы, потенциируя инсулинорезистентность, и стимулировать секрецию лептина. Лептин («голос жировой ткани») регулирует [[пищевое поведение]], воздействуя на [[Гормоны голода и насыщения|гипоталамический центр насыщения]]; повышает тонус симпатической нервной системы; усиливает термогенез в адипоцитах; подавляет синтез инсулина; воздействует на инсулиновый рецептор клетки, снижая транспорт глюкозы. При [[Ожирение|ожирени]]и наблюдается лептинорезистентность. Полагают, что гиперлептинемия оказывает стимулирующее действие на некоторые гипоталамические релизинг-факторы (РФ), в частности на [[Гипоталамо-гипофизарно-надпочечниковая система|АКТГ-РФ]]. Так, при МС часто отмечается легкий гиперкортицизм, который играет определенную роль в патогенезе МС<ref>Адашева Т. В., Демичева О. Ю. Метаболический синдром–основы патогенетической терапии //Лечащий врач. – 2003. – Т. 10. – С. 24-28.</ref>. | |
| − | + | === Лечение метаболического синдрома === | |
| − | + | ''Читайте основную статью:'' [[Лечение метаболического синдрома]] | |
| − | + | == Читайте также == | |
| − | + | * [[Лептин]] | |
| + | * [[Грелин]] | ||
| + | * [[Диета для похудения]] | ||
| + | * [[Типы ожирения]] | ||
| + | * [[Тренировки для похудения]] | ||
== Источники == | == Источники == | ||
Текущая версия на 09:50, 2 июня 2021
Содержание
Метаболический синдром[править | править код]
Метаболический синдром («полиметаболический синдром», «синдром изобилия», «синдром Х», «смертельный квартет», «гормональный метаболический синдром», «синдром инсулинорезистентности», «смертельный секстет», «метаболический сосудистый синдром», «дисметаболический синдром», «гипертриглицеридемическая талия», «кардиометаболический синдром»)[1] — это сочетание нарушенного углеводного обмена, абдоминального ожирения, дислипидемии и гипертензии, и связан с развитием сахарного диабета 2 типа и сердечно-сосудистых заболеваний [2].
История[править | править код]
В 1922 г. Г.Ф. Ланг в своих трудах отмечал наличие ассоциации артериальной гипертензии и ожирения, нарушений обмена углеводов и подагры, об этой связи доложили на Х съезде терапевтов его сотрудники А.Л. Мясников и Д.М. Гротель.
1923 г. шведский исследователь E.Kylin. впервые указал связь артериальной гипертензии (АГ) с гипергликемией и гиперурикемией.
В 1948 г. выдающийся клиницист Е.М. Тареев отмечал: « Представление о гипертонике наиболее часто ассоциируется с ожирелым гиперстеником, с возможным нарушением белкового обмена, с засорением крови продуктами неполного метаморфоза-холестерином, мочевой кислотой».
В 1966 г. связь сахарного диабета и атеросклероза описал Л.С. Шварц. В это же время J.Camus назвал сочетание у одного и того же больного сахарного диабета, дислипидемии и поражения суставов метаболическим трисиндромом.
В 1968 г. H.Mehnert и H. Kuhlman обозначили сочетание нарушения обменов как « синдром изобилия».
M. Hannefeld и W. Leonard в 1981 г. впервые сделали подробное описание метаболического синдрома. В силу существования в эпоху «холодной войны» политической тенденциозности, труды исследователей из России и стран «Восточного блока» замалчивались медицинской общественностью Запада.
В 1988 г. G. Reaven в своей Бантингской лекции, обобщив эпидемиологические, клинические и экспериментальные данные, выдвинул концепцию, в которой указал, что резистентность к инсулину, абдоминальное ожирение, АГ, дислипидемия и коронарная болезнь сердца являются проявлением единого патологического состояния, обозначенного им как « Синдром Х».
А. Regenauer в 1988 г., описывая прогностические аспекты МС, назвал его «good life syndrome», то есть « синдром благополучия» (сытости).
В 1989 г. N. Kaplan привел данные популяционных исследований, свидетельствующие о неблагоприятном жизненном и трудовом прогнозе у больных с сочетанием ожирения, сахарного диабета, АГ и коронарной болезни сердца, назвав симптомокомплекс «смертельным квартетом».
В последние годы в исследовательской и практической медицине укоренился термин «метаболический синдром», сущность его постепенно расширялась, так как стали выявляться ранее неизученные нарушения, наблюдавшиеся у части больных.
А.И.Мартынов в 2000 г. отнес к ним повышенное содержание фибриногена, уровня «малых» липопротеинов, ингибитора-1 активатора плазминогена и микроальбуминурию[3].
Результатом совместной работы ведущих международных организаций по изучению МС явилось создание нового определения. В настоящее время для установления диагноза необходимо наличие трех из пяти нижеперечисленных критериев.
![]() Критерии метаболического синдрома: IDF, NHLBI, AHA, WHF, IAS, IASO, 2009 г.
Критерии метаболического синдрома: IDF, NHLBI, AHA, WHF, IAS, IASO, 2009 г.
Любые 3 из перечисленных:
- Абдоминальное ожирение (данные, специфичные для отдельных стран и популяций)
- Триглицериды 1,7 ммоль/л (150 мг/дл) или медикаментозная терапия гипертриглицеридемии
- Снижение ЛПВП: у мужчин: <1,0 ммоль/л (40 мг/дл), у женщин: <1,3 ммоль/л (50 мг/дл) или медикаментозная терапия дислипидемии
- Повышенный уровень АД 130/85 мм рт. ст. или прием антигипертензивной терапии пациентом с артериальной гипертензией в анамнезе
- Повышенный уровень гликемии натощак 100 мг/дл или прием сахароснижающей терапии.
Роль ожирения в развитии метаболического синдрома[править | править код]
По материалам Фремингемского исследование было установлено, что у больных с артериальной гипертонией отмечена значительная частота метаболических нарушений: гиперхолестеринемия и гиперинсулинемия (80% обследованных), гиперурикемия (25%), сахарный диабет (15%). Было также отмечено, что у одного и того же больного часто наблюдается сочетание ожирения, артериальной гипертонии и сахарного диабета II типа[4] . Кроме того, указанное исследование позволило выделить ожирение как независимый фактор риска сердечно-сосудистых заболеваний, для которых характерна высокая смертность, особенно женщин[5].
Выделяют два типа ожирения, различающихся по локализации скоплений жировой ткани, - андроидный и гиноидный.
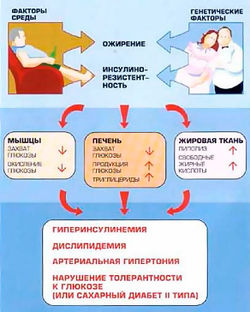
- Абдоминальное (висцеральное) ожирение — один из основных клинических симптомов метаболического синдрома, которое является важным фактором риска сердечно-сосудистых и других заболеваний (рис. 1), сахарного диабета II типа и ранних проявлений атеросклероза[6]. Андроидный тип характеризуется гипертрофией адипоцитов и обычно наблюдается у лиц зрелого возраста. Избыточное отложение жира происходит в области верхней половины туловища, живота. Растет масса висцерального жира. Этот тип ожирения обычно называют центральным или абдоминальным, а также «яблочным».
Kissebah A. и Bjorntorp P. показали[7], что при одинаковом показателе индекса массы тела (ИМТ) абдоминальное ожирение сопровождается более высоким риском развития сопутствующих заболеваний, чем периферическое ожирение.Именно поэтому выраженность осложнений ожирения является более высокой у мужчин, чем у женщин[8].
- При гиноидном типе ожирения (периферическое) происходит гиперплазия жировых клеток, так как он обычно развивается в детстве и наблюдается в течение всей жизни. Гиноидный тип характеризуется преимущественным отложением жира в области ягодиц и бедер, поэтому его называют ягодично - бедренным, или грушевидным.
При развившемся андроидном ожирении с возрастом больного повышается активность центров гипоталамуса и снижается их чувствительность к влияниям с периферии. Последовательность развития нарушений, составляющих метаболический синдром, представляется следующим образом: ожирение - инсулинорезистентность - гиперинсулинемия - артериальная гипертензия - атеросклероз - коронарная болезнь сердца - сахарный диабет II типа[9].
Инсулинорезистентность в развитии метаболического синдрома[править | править код]
Развитие гипертрофического ожирения провоцирует снижение чувствительности периферических тканей к действию инсулина. Именно развитие хронического избытка инсулина в крови большинство исследователей считают “пусковой кнопкой” для возникновения всех заболеваний, входящих в понятие "метаболический синдром"[10](рис.2).
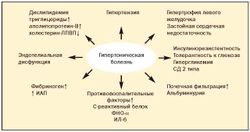
До настоящего времени не прекращается дискуссия о первичности или вторичности инсулинорезистентности и гиперандрогении при метаболическом синдроме (рис. 3)[11].
Первая гипотеза[править | править код]
ИР — полигенная патология, в развитии которой могут иметь значение мутации генов субстрата инсулинового рецептора (IRS-1 и IRS-2), β3-адренорецепторов, разобщающего протеина (UCP-1), а также молекулярные дефекты белков сигнального пути инсулина (глюкозные транспортеры). Особую роль играет снижение чувствительности к инсулину в мышечной, жировой и печеночной тканях, а также в надпочечниках.
В миоцитах нарушаются поступление и утилизация глюкозы, в жировой ткани развивается резистентность к антилиполитическому действию инсулина. Интенсивный липолиз в висцеральных адипоцитах приводит к выделению большого количества свободных жирных кислот (СЖК) и глицерина в портальный кровоток. Поступая в печень, СЖК, с одной стороны, становятся субстратом для формирования атерогенных липопротеидов, а с другой — препятствуют связыванию инсулина с гепатоцитом, потенциируя ИР. ИР гепатоцитов ведет к снижению синтеза гликогена, активации гликогенолиза и глюконеогенеза. Долгое время ИР компенсируется избыточной продукцией инсулина, поэтому нарушение гликемического контроля манифестирует не сразу. Но, по мере истощения функции β-клеток поджелудочной железы, наступает декомпенсация углеводного обмена, сначала в виде нарушенных гликемии натощак и толерантности к глюкозе (НТГ), а затем и сахарного диабета 2 типа (Т2СД). Дополнительное снижение секреции инсулина при МС вызывается длительным воздействием высоких концентраций СЖК на β-клетки (так называемый липотоксический эффект). При имеющихся генетически обусловленных дефектах секреции инсулина развитие Т2СД значительно ускоряется[12].
Вторая гипотеза[править | править код]
Согласно другой гипотезе, ведущую роль в развитии и прогрессировании инсулинорезистентности играет жировая ткань абдоминальной области. Особенность висцеральных адипоцитов — высокая чувствительность к липолитическому действию катехоламинов и низкая к антилиполитическому действию инсулина.
Помимо веществ, непосредственно регулирующих липидный обмен, жировая клетка продуцирует эстрогены, цитокины, ангиотензиноген, ингибитор активатора плазминогена-1, липопротенлипазу, адипсин, адинопектин, интерлейкин-6, фактор некроза опухолей-α (ФНО-α), трансформирующий фактор роста В, лептин и др.
ФНО-α способен воздействовать на инсулиновый рецептор и транспортеры глюкозы, потенциируя инсулинорезистентность, и стимулировать секрецию лептина. Лептин («голос жировой ткани») регулирует пищевое поведение, воздействуя на гипоталамический центр насыщения; повышает тонус симпатической нервной системы; усиливает термогенез в адипоцитах; подавляет синтез инсулина; воздействует на инсулиновый рецептор клетки, снижая транспорт глюкозы. При ожирении наблюдается лептинорезистентность. Полагают, что гиперлептинемия оказывает стимулирующее действие на некоторые гипоталамические релизинг-факторы (РФ), в частности на АКТГ-РФ. Так, при МС часто отмечается легкий гиперкортицизм, который играет определенную роль в патогенезе МС[13].
Лечение метаболического синдрома[править | править код]
Читайте основную статью: Лечение метаболического синдрома
Читайте также[править | править код]
Источники[править | править код]
- ↑ Бурова СА. Метаболический синдром: патогенез, клиника, диагностика, подходы к лечению. РМЖ 2001;2(9):56—62.
- ↑ Метаболический синдром: аргументы «за» и «против» Учамприна В.А.1, Романцова Т.И., Калашникова М.Ф.ГБОУ ВПО Первый Московский государственный медицинский университет им. И.М. Сеченова 2012г
- ↑ Колопкова Т. А. и др. МЕТАБОЛИЧЕСКИЙ СИНДРОМ Х-ПАНДЕМИЯ XXI ВЕКА //Саратовский научно-медицинский журнал. – 2008. – Т. 4. – №. 3.
- ↑ Hubert H. B. et al. Obesity as an independent risk factor for cardiovascular disease: a 26-year follow-up of participants in the Framingham Heart Study //Circulation. – 1983. – Т. 67. – №. 5. – С. 968-977.
- ↑ Колопкова Т. А. и др. МЕТАБОЛИЧЕСКИЙ СИНДРОМ Х-ПАНДЕМИЯ XXI ВЕКА //Саратовский научно-медицинский журнал. – 2008. – Т. 4. – №. 3.
- ↑ Ruderman N., Flier J. S. Chewing the Fat--ACC and Energy Balance //Science. – 2001. – Т. 291. – №. 5513. – С. 2558-2559.
- ↑ Kissebah A. H., Krakower G. R. Regional adiposity and morbidity //Physiological Reviews. – 1994. – Т. 74. – №. 4. – С. 761-811.
- ↑ БО Ш., САВЕЛЬЕВА Л. В. КОМПЛЕКСНЫЙ ПОДХОД К ЛЕЧЕНИЮ ОЖИРЕНИЯ И МЕТАБОЛИЧЕСКОГО СИНДРОМА У МУЖЧИН //Ожирение и метаболизм. – 2009. – №. 4.
- ↑ ДЗГОЕВА Ф. Х. Висцеральное ожирение-ключевое звено метаболического синдрома //Ожирение и метаболизм. – 2004. – №. 1.
- ↑ Благосклонная Я. В., Шляхто Е. В., Красильникова Е. И. Метаболический сердечно-сосудистый синдром //Рус. мед. журн. – 2001. – Т. 9. – №. 2. – С. 67œ70.
- ↑ Оганов М. Эпидемиологические аспекты метаболического синдрома. – 2004.
- ↑ Мамедов М. Н. Метаболический синдром: практические аспекты диагностики и лечения в амбулаторных условиях //Москва. – 2005.
- ↑ Адашева Т. В., Демичева О. Ю. Метаболический синдром–основы патогенетической терапии //Лечащий врач. – 2003. – Т. 10. – С. 24-28.