Бета-аланин: научный обзор
Содержание
Бета-Аланин в спортивной медицине
Авторы: д.м.н. Александр Дмитриев, врач-эндокринолог Алексей Калинчев
В последние годы в мире возрос интерес к бета-Аланину (β-Аланин, β-Alanine, БА) как биологически активной аминокислоте, применяемой в качестве фармаконутриента с целью повышения физической готовности как спортсменов, так и обычных лиц, занимающихся физкультурой или подверженных повышенным физическим нагрузкам. В период с 2007 по 2015 год выполнено большое количество исследований у разных категорий лиц: профессиональных спортсменов, военных, обычных тренированных и нетренированных лиц, - для определения эффективности бета-аланина, дозировок и схем использования. На основании этих работ сформулированы рекомендации для однократного (острого) и курсового применения β-аланина, сочетания с другими макро-, микро- и фармаконутриентами. В то же время, в отечественной литературе крайне мало работ, посвященных данному вопросу, что затрудняет практическое применение β-аланина. Данный обзор предназначен для восполнения пробела в этом плане и создания основы для будущих российских рекомендаций.
Структура и физико-химические свойства β-Аланина (БА)
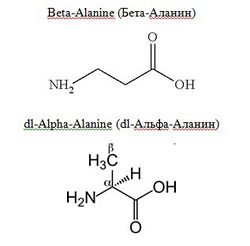
Бета-Аланин (3-аминопропионовая кислота; бета-аминопропионовая кислота; 3-Aminopropionic acid; Beta-Aminopropionic acid) имеет молекулярный вес 89,1 г/моль, чрезвычайно высокую растворимость в воде 545 г/л (при 25оС). Растворимость в воде L-Аланина (альфа-Аланина) при той же температуре - 166 г/л.
Альфа- и бета-Аланин – изомеры, имеют одинаковую формулу С3Н7NO2, но молекулярная структура у них разная. У альфа-Аланина амидная группа прикреплена к центральному углеродному атому, в то время как у бета-Аланина – к концевому углеродному атому. Это обусловливает различные химические свойства. В частности, температура плавления альфа-Аланина – 314°С, бета-Аланина – 196°С.
Экзогенное введение β-Аланина и метаболические процессы в организме
Фармакокинетика
В работе R.C.Harris и соавторов[1] на 28 здоровых молодых мужчинах (возраст 33,5±9,9 года; вес 80,2±17,1 кг) исследовалась динамика концентрации бета-аланина в плазме крови после перорального его введения в нескольких вариантах.
- Исследование 1. Однократное введение бета-аланина (n=6): A) БА в виде дипептида с гистидином (эквивалентно 40 мг/кг веса тела) в курином бульоне; B) 10 мг/кг веса тела, C) 20 мг/кг веса тела и D) 40 мг/кг веса тела в виде препарата Карнозин (CarnoSyn, NAI, USA, бета-Аланин-L-Гистидин).
- Исследование 2. Двухнедельное введение бета-аланина (n=6) в дозе 10 мг/кг веса тела 3 раза в день (три приема БА с 9.00 утра с интервалом 3 часа).
- Исследование 3. Четырехнедельное введение бета-аланина или Карнозина (n=16) 4 раза в день по 800 мг БА или плацебо для оценки влияния хронического введения БА на биохимические и гематологические показатели крови.
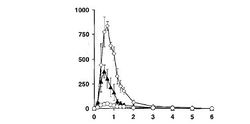
В исследовании 1 с однократным введением различных доз бета-аланина выявлено, что доза 40 мг/кг β-аланина вызывает побочные эффекты в виде покраснения и покалывания, которые развиваются через 20 мин после перорального применения и продолжаются в течение 1 часа, после чего бесследно исчезают. Эти проявления возникают первично на ушах, лбе, коже черепа, и распространяются далее на нос, руки, спину и ягодицы. Аналогичные, но гораздо менее интенсивные и кратковременные проявления, отмечены и в дозе 20 мг/кг веса тела, и достаточно редко – в дозе 10 мг/кг (ориентировочная фиксированная средняя доза 800 мг на прием). Пики концентраций бета-аланина (рис.1) для всех исследуемых доз наблюдались в интервале 30-40 минут, при этом максимальная концентрация β-аланина в плазме отмечалась в дозе 40 мг/кг (833,5±42,8 мкмол/л на 40-ой минуте), что в 2,2 раза превышает максимальную концентрацию в дозе 20 мг/кг. Эффект дозы 10 мг/кг был очень мал. Затем концентрация БА в плазме быстро снижается в течение часа в дозе 20 мг/кг, и 1,5-2 часов – в дозе 40 мг/кг. Время полужизни (Т1/2) для всех введенных доз составляет около 25 минут. Результаты показали, что имеются существенные различия в абсорбции и динамике содержания бета-аланина в плазме между пероральным введением бета-аланина в чистом виде или в растворе куриного бульона (рис.2).
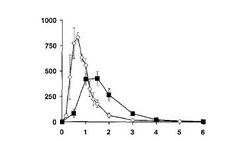
Из графиков видно, что куриный бульон замедляет всасывание бета-аланина, снижает пик его концентрации в плазме крови, но пролонгирует время повышения концентрации. Так, пик концентрации в плазме при введении бета-аланина в составе куриного бульона примерно в два раза ниже, чем при введении бета-аланина в чистом виде (427,9±66,1 мкмол/л на 90-ой минуте, и 833,5±42,8 мкмол/л на 40-ой минуте, соответственно).
В исследовании 1 оценивалась также потеря введенного перорально бета-аланин с мочой в зависимости от дозы. Потери составили 0,6±0,09%, 1,5±0,4% и 3,6±0,5% для доз 10, 20 и 40 мг/кг, соответственно.

В исследовании 2 с двухнедельным введением бета-аланина в дозе 10 мг/кг веса тела 3 раза в день (три приема бета-аланина с 9.00 утра с равными интервалами в 3 часа) и примерной разовой дозой 800 мг выявлено (рис.3), что концентрация бета-аланина в плазме после каждого приема препарата успевала вернуться к исходным значениям (через 3 часа) перед следующим приемом. Побочные эффекты, характерные для более высоких доз и, частично, для данной дозы при первом применении, при повторных приемах уже не проявлялись. Пик концентрации бета-аланина в плазме после приема дозы 10 мг/кг составлял такую же величину, что и в исследовании 1.
В исследовании 3 с 4-х недельным введением бета-аланина (4 раза в день по 800 мг, т.е. примерно 10 мг/кг веса) не выявлено каких-либо изменений биохимических и гематологических показателей в плазме крови, а также проявлений побочных эффектов. Параллельно в течение 4-х недель приема препарата происходило нарастание содержания карнозина в мышечной ткани с исходных 22,7±1,1 ммол/кг/дм до 33,4±4,0 ммол/кг/дм к концу 4-ой недели (в среднем +47%). Это расценивается в качестве положительного эффекта в плане регуляции рН мышечных клеток, обеспечения нормального перехода мышц из состояния отдыха в рабочее (тренировочное) состояние, и наоборот, а также снижения лактата.
В связи с выявленным снижением выраженности и частоты побочных эффектов бета-аланина при замедлении всасывания в кишечнике, были созданы ретардные формы с постепенным высвобождением бета-аланина (таблетки, порошки). Изучению фармакокинетики и связанных побочных эффектов одной из таких форм бета-аланина в виде таблеток (slow-release - SR) c постепенным выделением β-аланина посвящена работа J.Decombaz и соавторов[2]. В рандомизированном одиночном-слепом исследовании на 11 здоровых добровольцах сравнивались основные фармакокинетические параметры однократного утреннего введения обычного водного раствора бета-аланина и ретардных таблеток в дозе 1,6 г (табл.1).
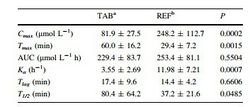
Как видно из таблицы 1, величина пика концентрации (Сmax) при приеме ретардных таблеток была примерно в три раза ниже, чем в случае водного раствора, а время его достижения (Тmax) – в два раза дольше (1 час против 0,5 часа). В то же время не выявлено различий в площадях под кривыми «концентрация/время», снижались потери β-аланина с мочой (202 против 663 мкмол, Р<0,0001) и повышалось удержание бета-аланина в организме (98.9% против 96.3%, Р<0.001). Побочные эффекты, описанные ранее как покраснение и покалывание в определенных участках кожи, и соответствующие по времени максимуму концентрации β-аланина в плазме крови, были значительно менее выражены при приеме ретардных таблеток (Р<0,001), а по частоте возникновения приближались к эффекту плацебо. Таким образом, применение ретардных форм, обеспечивающих замедленное высвобождение бета-аланина в кишечнике, позволяет избежать побочных эффектов неретардированных форм бета-аланина при сохранении величины основного показателя (для хронического применения вещества) – площади под кривой «концентрация-время». Эти факторы обеспечивают, по крайней мере для тех спортсменов, которые болезненно реагируют на покраснение кожи и парестезии при применении повышенных доз бета-аланина, несомненные преимущества SR-форм.
Метаболизм
Особенности метаболизма β-аланина обусловлены его химической структурой. На рисунке 4 представлено сходство бета-аланина с некоторыми другими аминокислотами и процесс образования карнозина в скелетных мышцах.
Бета-аланин – непротеиногенная аминокислота (не участвует в синтезе белков) и продуцируется в самом организме в процессе распада пиримидинов, декарбоксилирования кишечной микрофлорой L-аспартата и трансаминирования при взаимодействии 3-оксопропаната и L-аспартата[3]. Синтез бета-аланина происходит в печени в процессе необратимой деградации тимина, цитозина и урацила. После синтеза β-аланина транспортируется в мышечные клетки, проникает в сарколемму за счет натрий и хлор-зависимой транспортной системы, которая может быть универсальной для сходных по химической структуре аминокислот (рис.4). Аналогичный процесс происходит и в ЦНС, где БА играет роль нейропередатчика и нейромодулятора, имеет идентифицированные места связывания с рецепторами ГАМК, NMDA и глицина в гиппокампе и некоторых других структурах, участвующих в формировании когнитивных функций.
Внутри возбудимых клеток β-аланин может формировать дипептидную связь с гистидином в процессе АТФ-зависимой реакции и действия фермента карнозин-синтетазы, образуя карнозин (рис.4). Синтез карнозина регулируется величиной поступления β-аланина внутрь мышечных волокон[4], уровнем активности карнозин-синтетазы и, в отсутствие достаточного поступления бета-аланина с пищей, печеночным синтезом бета-аланина и его транспортом в скелетные мышцы[5]. Нормальный уровень внутриклеточного карнозина 20-30 ммол/кг-1 сухого веса тела, у мужчин он выше, чем у женщин, с возрастом понижается в среднем на 47% к 70 годам по сравнению с 20-летними лицами. Существует прямая корреляционная связь возрастного снижение β-аланина и тестостерона. Карнозин, как и бета-аланин, выполняет множество функций: снижение окисления липидов и протеинов; повышение АТФ-азной активности; регуляция функции макрофагов; защита клеточных мембран; образование хелатов двухвалентных катионов и др., в том числе, связанных с процессом старения. Важным аспектом является участие в нейрогенной регуляции, особенно, в процессах памяти.
Фармакодинамика (механизм действия)
Карнозин (β-Аланил-L-Гистидин) – естественный дипептид организма, образующийся, как уже отмечалось выше, в результате соединения бета-аланина и Гистидина при помощи карнозин-синтетазы. Депо карнозина находится в скелетных мышцах. Распад этого соединения происходит под влиянием фермента карнозиназы, которая локализуется в сыворотке крови и ряде тканей, но отсутствует в мышечной ткани[6]. Поэтому пероральное введение карнозина – неэффективный метод повышения содержания уровня внутримышечного карнозина, т.к. поступающий через кишечник карнозин в конечном счете полностью метаболизируется перед попаданием в мышцы[7]. Роль Карнозина как внутриклеточного протонного буфера впервые была выявлена еще в 1953 году в СССР С.Е.Севериным[8], который показал, что отсутствие карнозина приводит к быстрому развитию усталости и ацидоза. По показателю логарифма константы диссоциации (pKa) равному 6.83 и высокой концентрации в мышцах карнозин представляется более эффективным буфером, чем два других физико-химических буфера - бикарбонат (pKa 6.3) или неорганический фосфат (pKa 7.2), при превышении физиологического диапазона рН. Предварительные данные показывают, что вклад карнозина в буферизационную способность мышц составляет от 7 до 40%. Данные о способности пищевых добавок β-аланина увеличивать внутримышечную концентрацию карнозина и снижать посттренировочную редукцию рН (ацидоз, вызванный физической нагрузкой), подтверждают концепцию о значительной роли карнозина в буферных системах мышечной ткани.
Потенциальная физиологическая роль карнозина не ограничивается функцией протонного буфера. В процессе повышенных физических нагрузок образуется большое количество реактивных кислородных радикалов, которые вносят существенный вклад в развитие утомляемости и мышечных повреждений. Карнозин препятствует действию этих субстанций, выступая в роли антиоксиданта[9], а также связывая в виде хелатных соединений ионы таких металлов как медь и железо.
Пищевые добавки бета-аланина и физическая подготовка военнослужащих
В процессе интенсивных физических тренировок военных и повышения их боеготовности часто отмечается снижение физической формы. Применение специальных пищевых добавок с целью избежать подобных спадов физической формы – обычная практика в армиях многих стран. В частности, в США частота применения БАДов достигает 30-40% в зависимости от рода войск и характера выполняемых задач. Следует подчеркнуть, что в армейской подготовке военнослужащих западных стран, как и в спортивной подготовке спортсменов, проявляется четкая тенденция к смещению акцента с применения фармакологических средств на использование нутритивных методов повышения физической готовности. Так, ряд членов Медицинской Корпорации армии США высказал необходимость исследования нефармакологических (недопинговых) альтернатив снижения утомляемости военнослужащих в процессе тренировки выносливости и выполнения тактических задач[10].
Β-Аланин (БА) очень популярная добавка[11][12], используемая для повышения мышечной силы и мощности у тренированных спортсменов. Однако, до настоящего времени отсутствовали исследования влияния бета-аланина на функциональную подготовку солдат, выполняющих специфические оперативные задачи. Проблема заключалась в том, что военные врачи при назначении бета-аланина руководствовались результатами исследований на спортсменах и экстраполировали их в отношении военных, без учета специфики стоящих перед ними задач, адаптации к специальным тренировочным программам. Считалось, что результаты, полученные в конкурентных видах спорта, автоматически можно переносить на армию без анализа влияния бета-аланина на выполнение тактических заданий.
Первая работа по специальной оценке эффективности бета-аланина у военнослужащих была опубликована только в 2014 году R.Ko и соавторами[13]. В этом обзоре, сделанном по заказу Министерства обороны, анализируется безопасность и эффективность бета-аланина и его комбинаций с другими фармаконутриентами в процессе физической подготовки, снижения усталости, восстановления после упражнений у военнослужащих в целом на основе 13 баз данных. Чрезвычайная вариабельность исследованных групп лиц, доз бета-аланина, их комбинаций, отсутствие привязки к выполнению физических упражнений и многие другие факторы не позволили дать положительное заключение об эффективности бета-аланина.
Исследования, проведенные J.R.Hoffman и соавторами[11][12][14] позволили более детально оценить эффективность бета-аланина при выполнении специфических военных заданий с повышенной физической нагрузкой, требующих решения тактических задач.
В исследовании 2014 года J.R.Hoffman и соавторы[14] показали, что прием бета-аланина (6 г/день) в течение 4-х недель молодыми здоровыми солдатами элитного военного подразделения армии Израиля увеличивает мощность физических движений (прыжков), точность стрельбы и скорость поражения цели. Эти улучшения в подготовке выявляются после 4 недель высокоинтенсивных тренировок и однократного бега (4 км) на выносливость. В то же время не выявлено улучшений когнитивных функций под влиянием бета-аланина в условиях повышенных нагрузок и утомления. Авторы объясняют этот факт возможной неадекватностью используемого теста в данных условиях для оценки изменений когнитивных функций.
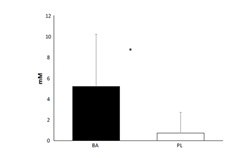
В последующих работах J.R.Hoffman и соавторы[11][12] на солдатах этого же элитного подразделения сил самообороны Израиля исследовали влияние ежедневного приема бета-аланина в дозе 6 г/день в течение 30 дней на содержание карнозина в мышцах и мозге методом магнитно-резонансной спектроскопии (МРС – MRS – диагностический метод исследования, основанный на использовании явления ядерного магнитного резонанса для получения биохимического профиля тканей). Оценивалась также физическая готовность и когнитивные функции, но уже с помощью другого теста, более адекватного специфике задач данного подразделения. Через 30 дней отмечено значительное увеличение содержания карнозина в мышцах (рис.7), совпадающее с изменениями, наблюдаемыми ранее у спортсменов, но без изменения уровня карнозина в мозге.
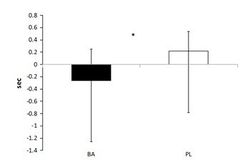
Улучшение физической готовности носило выборочный характер и касалось, в основном, однократного кратковременного (в интервале 60-360 секунд) упражнения (переноска пострадавшего на 50 метров) (рис.8).
С помощью нового теста удалось выявить достоверное улучшение когнитивных функций на фоне приема бета-аланина, что проявлялось не только повышением точности стрельбы, но и способностью сохранять фокусировку в условиях массированного огня. Этот факт расценен авторами как результат антистрессорного опосредованного действия бета-аланина.
Бета-аланин как потенциальный протектор посттравматических стрессовых нарушений
По данным Американской Ассоциации Психиатров стресс, перенесенный вследствие травмы, в ряде случаев служит причиной значительных поведенческих изменений, включая боязнь высоких нагрузок, потерю концентрации, неадекватность реакций на события и др. Имеются основания предполагать, что повышение уровня карнозина в мозге оказывает антидепрессанто-подобное действие[15]. J.R.Hoffman и соавторами[16] выполнена экспериментальная работа, которая создает основу для еще одного направления применения бета-аланина в спортивной медицине – нутритивно-метаболической терапии (НМТ) и предотвращения развития посттравматического стресс-синдрома, ускорения процесса адаптации спортсменов после травм. В опытах на крысах 30-дневное пероральное введение бета-аланина в дозе 100 мг/кг значительно уменьшало поведенческие реакции, характерные для посттравматического состояния. Нормализация поведения сопровождалась повышением концентрации карнозина в гиппокампе.
Читайте также
- Бета-аланин
- Бета-аланин (научный обзор)
- Бета-аланин в спорте
- Действие бета-аланина
- Применение бета-аланина
- L-карнитин: научный обзор
- Глутамин: научный обзор
- HMB: научный обзор
- Донаторы оксида азота: научный подход
- Креатин: научный обзор
- Омега-3 жирные кислоты: научный обзор
- Спортивные напитки: научный обзор
- Препараты витамина D в спортивной медицине: научный обзор
Источники
- ↑ Harris R.C., Tallon M.J., Dunnett M. et al. The absorption of orally supplied beta-alanine and its effect on muscle carnosine synthesis in human vastus lateralis. Amino Acids. 2006, 30(3):279–289.
- ↑ Decombaz J., Beaumont M., Vuichoud J. et al. Effect of slow-release b-alanine tablets on absorption kinetics and paresthesia. Amino Acids. 2012, 43:67–76.
- ↑ Tiedje K.E., Stevens K., Barnes, S., Weaver D.F. β-Alanine as a small molecule neurotransmitter. Neurochem. Int. 2010, 57, 177–188.
- ↑ Derave W., Everaert I., Beeckman S., Baguet A. Muscle carnosine metabolism and beta-alanine supplementation in relation to exercise and training. Sports Med. 2010, 1, 40(3):247-263.
- ↑ Harris, R.C., Wise, J.A., Price, K.A. et al. Determinants of muscle carnosine content. Amino Acids 2012, 43, 5–12.
- ↑ Sale C, Saunders B, Harris RC. Effect of beta-alanine supplementation on muscle carnosine concentrations and exercise performance. Amino Acids. 2010, 39(2):321–333.
- ↑ Gardner M.L., Illingworth K.M., Kelleher J., Wood D. Intestinal absorption of the intact peptide carnosine in man, and comparison with intestinal permeability to lactulose. J. Physiol. 1991, 439(1):411–422.
- ↑ Severin S.E., Kirzon M.V., Kaftanova T.M. Effect of carnosine and anserine on action of isolated frog muscles. Dokl. Akad. Nauk SSSR.1953, 91(3):691–694.
- ↑ усталости Klebanov G.I., Teselkin Yu. O., Babenkova I.V. et al. Effect of carnosine and its components on free-radical reactions. Membr Cell Biol. 1998, 12(1):89–99.
- ↑ Russo M.B., Arnett M.V., Thomas M.L., Caldwell J.A. Ethical use of cogniceuticals in the militaries of democratic nations. Am. J. Bioeth. 2008, 8:39–49.
- ↑ 11,0 11,1 11,2 Hoffman J.R., Stout J.R., Harris R.C., Moran D.S. β‑Alanine supplementation and military performance. Amino Acids. 2015a, 47: 2463-2474.
- ↑ 12,0 12,1 12,2 Hoffman J.R., Landau G., Stout J.R. et al. β-Alanine ingestion increases muscle carnosine content and combat specific performance in soldiers. Amino Acids. The Forum for Amino Acid, Peptide and Protein Research. 2015b, 47(3): 627-636.
- ↑ Ko R., Low Dog T., Gorecki D.K. et al. Evidence-based evaluation of potential benefits and safety of beta-alanine supplementation for military personnel. Nutr. Rev. 2014, 72:217–225.
- ↑ 14,0 14,1 Hoffman J.R., Landau G., Stout J.R. et al. β-alanine supplementation improves tactical performance but not cognitive function in elite special operation soldiers. J. Int. Soc. Sports Nutr. 2014, 11:15.
- ↑ Tomonaga S., Yamane H., Onitsuka E. et al. Carnosine-induced anti-depressant-like activity in rats. Pharmacol. Biochem. Behav. 2008, 89:627–632.
- ↑ Hoffman J.R., Ostfeld I., Stout J.R. et al. β‑Alanine supplemented diets enhance behavioral resilience to stress exposure in an animal model of PTSD. Amino Acids, 2015c, 47:1247–1257.