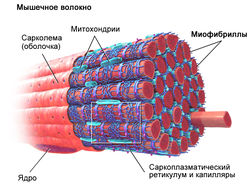
Гипертрофия мышц
Источник:
Эндокриная система, спорт и двигательная активность.
Перевод с англ./под ред. У.Дж. Кремера и А.Д. Рогола. - Э64
Издательство: Олимп. литература, 2008 год.
Содержание
Механизмы гипертрофии скелетных мышц[править | править код]
Гипертрофия скелетных мышц (греч. hyper – больше и греч. trophe – питание, пища) – это адаптационное увеличение объема или массы скелетной мышцы. Уменьшение объема или массы скелетной мышцы называется атрофией. Уменьшение объема или массы скелетной мышцы в пожилом возрасте называется саркопенией.
Гипертрофия - это адаптация мышц к нагрузке[править | править код]
Гипертрофия обуславливает скорость сокращения скелетной мышцы, максимальную силу, а также способность противостоять утомлению, — все это важные физические качества, имеющие непосредственное отношение к спортивным показателям. Благодаря высокой вариативности различных характеристик мышечной ткани, таких, как размер и состав мышечных волокон, а также степень капилляризации ткани, скелетные мышцы способны быстро приспосабливаться к изменениям, возникающим в ходе тренировочного процесса. В то же время характер адаптации скелетных мышц к силовым упражнениям и упражнениям на выносливость будет отличаться, что свидетельствует о существовании различных систем реагирования на нагрузку.
Таким образом, приспособительный процесс скелетных мышц к тренировочным нагрузкам можно рассматривать как совокупность согласованных локальных и периферических событий, ключевыми регуляторными сигналами к которым являются гормональные, механические, метаболические и нервные факторы. Изменения в скорости синтеза гормонов и ростовых факторов, а также содержание их рецепторов являются важными факторами регуляции приспособительного процесса, позволяющего скелетным мышцам удовлетворить физиологические потребности различных видов двигательной активности.
Подробнее читайте: Адаптация мышц к нагрузке.
Типы гипертрофии мышечных волокон[править | править код]
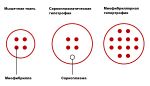
Можно выделить два крайних типа гипертрофии мышечных волокон[1][2]: миофибриллярную гипертрофию и саркоплазматическую гипертрофию.
- Миофибриллярная гипертрофия мышечных волокон – увеличение объема мышечных волокон за счет увеличения объема и числа миофибрилл. При этом возрастает плотность укладки миофибрилл в мышечном волокне. Гипертрофия мышечных волокон ведет к значительному росту максимальной силы мышцы. Наиболее предрасположены к миофибриллярной гипертрофии быстрые (IIB тип) мышечные волокна[1] и в меньшей степени IIА типа.
- Саркоплазматическая гипертрофия мышечных волокон – увеличение объема мышечных волокон за счет преимущественного увеличения объема саркоплазмы, т. е. несократительной их части. Гипертрофия этого типа происходит за счет повышения содержания в мышечных волокнах митохондрий, а также: креатинфосфата, гликогена, миоглобина и др. Наиболее предрасположены к саркоплазматической гипертрофии медленные (I) и быстрые окислительные (IIА) мышечные волокна[1]. Саркоплазматическая гипертрофия мышечных волокон мало влияет на рост силы мышц, но зато значительно повышает способность к продолжительной работе, т. е. увеличивает их выносливость.
В реальных ситуациях гипертрофия мышечных волокон представляет собой комбинацию двух названных типов с преобладанием одного из них. Преимущественное развитие того или иного типа гипертрофии мышечных волокон определяется характером тренировки. Упражнения со значительными внешними отягощениями (более 70%-от максимума), способствуют развитию миофибриллярной гипертрофии мышечных волокон. Такой тип гипертрофии характерен для силовых видов спорта (тяжелая атлетика, пауэрлифтинг). Длительное выполнение двигательных действий, развивающих выносливость, с относительно небольшой силовой нагрузкой на мышцы вызывает, главным образом, саркоплазматическую гипертрофию мышечных волокон. Такая гипертрофия свойственна бегунам на средние и длинные дистанции. Спортсменам, занимающихся бодибилдингом, свойственна как миофибриллярная, так и саркоплазматическая гипертрофия мышечных волокон[3].
Нередко к гипертрофии относят и гиперплазию мышцы (увеличение количества волокон), однако последние исследования[4] показали, что вклад гиперплазии в объем мышцы составляет менее 5% и носит более существенный характер только при использовании анаболических стероидов. Гормон роста при этом не вызывает гиперплазии. Таким образом, люди склонные к гипертрофии, как правило, имеют большее количество мышечных волокон. Общее число волокон заложено генетически и практически не меняется в течение жизни без применения специальной фармакологии.
Методика оценки степени гипертрофии[править | править код]
Для того, чтобы оценить степень гипертрофии скелетной мышцы, необходимо измерить изменение её объема или массы. Современные методы исследования (компьютерная или магнито-резонансная томография) позволяют оценить изменение объема скелетных мышц человека и животных. С этой целью выполняются многократные «срезы» поперечного сечения мышцы, что позволяет вычислить её объем. Однако, до настоящего времени о степени гипертрофии скелетных мышц достаточно часто судят по изменению максимального значения поперечного сечения мышцы, полученного посредством компьютерной или магниторезонансной томографии.
В бодибилдинге гипертрофию мышц оценивают измеряя охваты рук (на уровне предплечья и бицепса), бедер, голеней, грудной клетки с помощью метровой ленты.
Показатели, определяющие объем скелетных мышц[править | править код]
Основным компонентом скелетных мышц являются мышечные волокна, которые составляют приблизительно 87% от её объема[5]. Этот компонент мышцы называют сократительным, так как сокращение мышечных волокон позволяет мышце изменять свою длину и перемещать звенья опорно-двигательного аппарата, осуществляя движение звеньев тела человека. Остальной объем мышцы (13%) занимают несократительные элементы (соединительно-тканные образования, кровеносные и лимфатические сосуды, нервы, тканевая жидкость и др.).
В первом приближении[6] объем всей мышцы (Vм) можно выразить формулой:
Vм = Vмв × Nмв +Vнс
Влияние тренировки на параметры, определяющие объем скелетных мышц[править | править код]
Доказано, что под влиянием силовой тренировки и тренировки на выносливость возрастает объем мышечных волокон (Vмв) и объем несократительной части мышцы (Vнс). Не доказано увеличения количества мышечных волокон (гиперплазии мышечных волокон) у человека под влиянием силовой тренировки, хотя у животных (млекопитающих и птиц) гиперплазия мышечных волокон доказана[7].
Механизмы гипертрофии скелетных мышц[править | править код]
В основе миофибриллярной гипертрофии мышечных волокон лежит интенсивный синтез и уменьшенный распад мышечных белков. Существует несколько гипотез миофибриллярной гипертрофии:
- гипотеза ацидоза;
- гипотеза гипоксии;
- гипотеза механического повреждения мышечных волокон.
Гипотеза ацидоза предполагает, что пусковым стимулом для повышенного синтеза белка в скелетных мышцах является накопление в них молочной кислоты (лактата). Увеличение лактата в мышечных волокнах вызывает повреждение сарколеммы мышечных волокон и мембран органелл, появление в саркоплазме мышечных волокон ионов кальция, что вызывает активизацию протеолитических ферментов, расщепляющих мышечные белки. Увеличение синтеза белка в этой гипотезе связано с активацией и последующим делением клеток-сателлитов.
Гипотеза гипоксии предполагает, что пусковым стимулом для повышенного синтеза белка в скелетных мышцах является временное ограничение поступления кислорода (гипоксия) к скелетным мышцам, что происходит при выполнении силовых упражнений с большими отягощениями. Гипоксия и последующая реперфузия (восстановление притока кислорода к скелетным мышцам) вызывает повреждение мембран мышечных волокон и органоидов, появление в саркоплазме мышечных волокон ионов кальция, что вызывает активизацию протеолитических ферментов, расщепляющих мышечные белки. Увеличение синтеза белка в этой гипотезе связано с активизацией и последующим делением клеток-сателлитов.
Гипотеза механического повреждения мышечных волокон предполагает, что пусковым стимулом для повышенного синтеза белка является большое мышечное напряжение, что приводит к сильным повреждениям сократительных белков и белков цитоскелета мышечного волокна. Доказано[8], что даже однократная силовая тренировка может привести к повреждению более 80% мышечных волокон. Повреждение саркоплазматического ретикулума вызывает увеличение в саркоплазме мышечного волокна ионов кальция и последующим процессам, описанным выше.
Согласно вышеописанным гипотезам повреждение мышечного волокна вызывает запаздывающие болезненные ощущения в мышцах (DOMS), что связывается с их воспалением.
Очень важную роль в регуляции объема мышечной массы, в частности в развитии гипертрофии мышц, играют андрогены (мужские половые гормоны). У мужчин они вырабатываются половыми железами (семенниками) и в коре надпочечников, а у женщин - только в коре надпочечников. Соответственно у мужчин количество андрогенов в организме больше, чем у женщин.
Возрастное развитие мышечной массы идет параллельно с увеличением продукции андрогенных гормонов. Первое заметное увеличение объема мышечных волокон наблюдается в 6-7-летнем возрасте, когда усиливается образование андрогенов. С наступлением полового созревания (11 – 15 лет) начинается интенсивный прирост мышечной массы у мальчиков, который продолжается и после периода полового созревания. У девочек развитие мышечной массы в основном заканчивается с периодом полового созревания.
В опытах на животных установлено, что введение препаратов андрогенных гормонов (анаболиков) вызывает значительную интенсификацию синтеза мышечных белков, в результате чего увеличивается масса тренируемых мышц и как результат – их сила. Вместе с тем гипертрофия скелетных мышц может происходить и без участия андрогенных и других гормонов (гормона роста, инсулина и тиреоидных гормонов).
Влияние тренировки на композицию и гипертрофию мышечных волокон различных типов.
Доказано[9][10][11], что силовая тренировка и тренировка на выносливость не изменяют соотношения в мышцах медленных (I тип) и быстрых (II тип) мышечных волокон. Вместе с тем эти виды тренировки способны изменять соотношение двух видов быстрых волокон, увеличивая процент мышечных волокон IIA типа и соответственно уменьшая процент мышечных волокон IIB типа.
В результате силовой тренировки степень гипертрофии быстрых мышечных волокон (II типа) значительно больше, чем медленных волокон (I типа), тогда как тренировка направленная на выносливость ведет к гипертрофии в первую очередь медленных волокон (I типа). Эти различия показывают, что степень гипертрофии мышечного волокна зависит, как от меры его использования в процессе тренировок, так и от его способности к гипертрофии.
Силовая тренировка связана с относительно небольшим числом повторных максимальных или близких к ним мышечных сокращений, в которых участвуют как быстрые, так и медленные мышечные волокна. Однако и небольшого числа повторений достаточно для развития гипертрофии быстрых волокон, что указывает на их большую предрасположенность к гипертрофии (по сравнению с медленными волокнами). Высокий процент быстрых волокон (II типа) в мышцах служит важной предпосылкой для значительного роста мышечной силы при направленной силовой тренировке. Поэтому люди с высоким процентом быстрых волокон в мышцах имеют более высокие потенциальные возможности для развития силы и мощности.
Тренировка выносливости связана с большим числом повторных мышечных сокращений относительно небольшой силы, которые в основном обеспечиваются активностью медленных мышечных волокон. Поэтому при тренировке на выносливость более выражена гипертрофия медленных мышечных волокон (I типа) по сравнению с гипертрофией быстрых волокон (II типа).
Факторы гипетрофии[править | править код]
Синтез сократительных белков[править | править код]
Усиление синтеза сократительных белков является безоговорочным условием увеличения размера мышечных клеток в ответ на тренировочную нагрузку. В процессе роста скелетных мышц изменяется не только интенсивность синтеза белка, но и скорость его деградации[12]. У человека усиление синтеза белка выше уровня покоя происходит очень быстро, в течение 1 — 4 ч после завершения разового тренировочного занятия[13]. В начале мышечной гипертрофии усиление синтеза белка коррелирует с ростом активности РНК [14]. Передача мРНК облегчается теми факторами, активность которых, как известно, регулируется путем их фосфорилирования[15]. Параллельно с этими изменениями после тренировочного занятия происходит усиление транспорта аминокислот в мышцы, подвергавшиеся нагрузке. С теоретической точки зрения это увеличивает доступность аминокислот для белкового синтеза[16].
Рибонуклеиновая кислота (РНК)[править | править код]
Ряд данных свидетельствует о том, что после этого первоначального этапа необходимым условием продолжения гипертрофии мышц является увеличение уровня РНК(в отличие от увеличения активности РНК, происходившего вначале). Здесь возросшее количество мРНК может быть обусловлено либо усилением генной транскрипции в клеточных ядрах, либо увеличением количества ядер. Мышечные волокна взрослого человека содержат сотни ядер и каждое ядро осуществляет синтез белка в каком-то ограниченном объеме цитоплазмы, получившем название "ядерный компонент”[17]. Важно отметить, что хотя ядра мышечной клетки прошли митоз, они способны обеспечивать увеличение фибрилл лишь до определенного предела, после которого становится необходимым привлечение новых ядер. Это предположение подтверждается результатами исследований человека и животных, демонстрирующими, что гипертрофия скелетных мышечных волокон сопровождается значительным увеличением количества ядер[18]. У хорошо тренированных людей, например у тяжеловесов, количество ядер в гипертрофированной фибрилле скелетной мышцы больше, чем у лиц, ведущих малоподвижный образ жизни. Установлено существование линейной зависимости между количеством ядер и площадью поперечного сечения миофибриллы[19]. Появление новых ядер в увеличившейся миофибрилле играет роль в поддержании постоянного ядерно-цитоплазматического соотношения, т. е. стабильного размера ядерного компонента. О появлении новых ядер в гипертрофирующихся миофибриллах сообщалось для лиц разного возраста[20].
Гиперплазия (клетки-сателлиты)[править | править код]
Наряду с гипертрофией (увеличением объема клеток) под влиянием физических тренировок наблюдается процесс гиперплазии - рост числа волокон за счет деления клеток-сателлитов. Именно гиперплазия обеспечивает развитие мышечной памяти.
Клетки-сателлиты или спутниковые клетки
Функции спутниковых клеток это облегчение роста, обеспечение жизнедеятельности и восстановление поврежденной скелетной (не сердечной) мышечной ткани Эти клетки называются клетками-сателлитами, потому что расположены на наружной поверхности мышечных волокон, между сарколеммой и базальной пластинкой (верхний слой базальной мембраны) мышечного волокна. Спутниковые клетки имеют одно ядро, занимающее большую часть их объема. Обычно эти клетки находятся в состоянии покоя, но они активируются, когда мышечные волокна получают любую травму, например, от силовых тренировок. Спутниковые клетки затем размножаются и дочерние клетки притягиваются к поврежденному участку мышц. Затем они сливаются с существующим мышечным волокном, жертвуя свои ядра, которые помогают регенерировать мышечные волокна. Важно подчеркнуть, что этот процесс не создает новые скелетные мышечные волокна (у людей), но увеличивает размер и количество сократительных белков (актина и миозина) в пределах мышечного волокна. Этот период активации сателлитных клеток и пролиферации длится до 48 часов после травмы или после сессии силовых тренировок[21].
Влияние андрогенных анаболических стероидов[править | править код]
Результаты исследований, проведенных на животных, показали, что использование андрогенных анаболических стероидов сопровождается значительным увеличением размера мышц и мышечной силы[22]. Применение тестостерона в концентрациях, превышающих физиологические, у мужчин с различным уровнем физической подготовленности на протяжении 10 недель сопровождалось существенным увеличением мышечной силы и поперечного сечения четырехглавой мышцы бедра[23]. Известно, что андрогенные анаболические стероиды увеличивают интенсивность синтеза белка и способствуют росту мышц как in vivo, так и in vitro[24]. У человека прием анаболических стероидов на протяжении длительного времени усиливает степень гипертрофии мышечных волокон у хорошотренированных тяжелоатлетов[25]. Скелетные мышцы тяжелоатлетов, принимавших анаболические стероиды, характеризуются экстремально большим размером мышечных волокон и большим количеством ядер в мышечных клетках[26]. Подобную картину наблюдали на животных моделях, в частности, было обнаружено, что андрогенные анаболические стероиды опосредуют свое миотрофное воздействие путем увеличения количества ядер в мышечных волокнах и увеличения количества мышечных волокон[27]. Таким образом, анаболические стероиды способствуют увеличению количества ядер с целью обеспечения белкового синтеза в чрезвычайно гипертрофированных мышечных волокнах[28]. Основным механизмом, посредством которого андрогенные анаболические стероиды индуцируют мышечную гипертрофию, является активация и индукция пролиферации миосателлитоцитов, которые впоследствии сливаются с уже существующими мышечными волокнами или между собой, формируя новые мышечные волокна. С таким выводом согласуются результаты иммуногистохимической локализации рецепторов андрогенов в культивируемых клетках-спутниках, демонстрирующие возможность непосредственного воздействия анаболических стероидов на миосателлитоциты[29].
Влияние инсулина, аминокислот и физических упражнений на гипертрофию[править | править код]
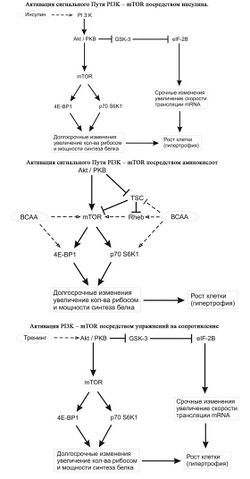
Инсулин, аминокислоты и упражнения на сопротивление - все эти факторы приводят к усилению синтеза белка в скелетных мышцах[30]. Несмотря на то, что инсулин, аминокислоты и упражнения по отдельности активируют несколько путей передачи сигнала в скелетных мышцах, один путь, PI3K – mTOR (фосфатидилинозитол-3-киназа – мишень рапамицина млекопитающих), является целью для всех трех. Активация пути передачи сигнала PI3K – mTOR имеет в результате и срочный (от нескольких минут до нескольких часов) и пролонгированный (от часов до нескольких дней) эффект регуляции синтеза белка через модуляцию нескольких этапов, включающих инициацию трансляции мРНК и, как следствие, биосинтез на рибосомах. Общей конечной точкой в передаче сигналов от каждого из стимулов является протеинкиназа mTOR. Ингибирование mTOR рапамицином или посредством генетических методов (к примеру, через РНК-интерференции в культивированных клетках) предотвращает увеличение синтеза белка, вызванные любым из трех обозначенных стимулов. Более того, рапамицин резко ослаблял гипертрофию, наблюдаемую в модели синергетической абляция при упражнениях на сопротивление. По факту, в обоих типах клеток – и в культивированных, и у животных in vivo ингибирование mTOR приводило к уменьшенному фенотипу клеток. В целом, имеющиеся данные строго обозначают центральную роль mTOR в контроле клеточного роста. Теперь, когда важность роли mTOR в процессе гипертрофии была идентифицирована, будущие исследования должны в ближайшее время предоставить более детальную информацию относительно механизмов, с помощью которых аминокислоты и физические упражнения способствуют продвижению сигналлинга через эту киназу. Кроме того, изучение находящихся после mTOR реакций, активируемых ей, и приводящих к экспрессии генов также должно быть адресовано к последующим исследованиям. Вместе такие исследования, направленные как на сигналлинг на входе mTOR, так и на выходе приведут к лучшему пониманию, как инсулин, аминокислоты и упражнения на сопротивления увеличивают белковый синтез и гипертрофию в скелетных мышцах.
Прочие анаболические агенты[править | править код]
- Гормон роста
- Инсулин
- Механический фактор роста
- Факторы роста фибробластов
- Инсулиноподобные факторы роста и их рецепторы
- Спортивное питание для роста мышц
Читайте также[править | править код]
- Рост мышц
- Типы мышечных волокон
- Креатин
- Фармакологическое сопровождение спортивной деятельности
- Анаболическое окно
Источники[править | править код]
- ↑ 1,0 1,1 1,2 Коц Я.М. Спортивная физиология Учебник для институтов физической культуры. — М.: Физкультура и спорт, 1998.
- ↑ Солодков А.С., Сологуб Е.Б. Физиология человека. Общая. Спортивная. Возрастная: Учебник. — М.: Терра-Спорт, Олимпия пресс, 2001.
- ↑ Солодков А.С., Сологуб Е.Б. Физиология человека. Общая. Спортивная. Возрастная: Учебник. — М.: Терра-Спорт, Олимпия пресс, 2001.
- ↑ Kraemer, William J.; Zatsiorsky, Vladimir M. (2006). Science and practice of strength training. Champaign, IL: Human Kinetics. p. 50. ISBN 0-7360-5628-9.
- ↑ MacDougall J.D., Sale D.G., Alway S.E., Sutton J.R. Muscle fiber number in biceps brachii in bodybuilders and control subjects // Journal Applied Physiology, 1984. V 57. № 5. P. 1399-1403.
- ↑ Самсонова А.В. Гипертрофия скелетных мышц человека: Учебное пособие. — 3-е изд. — СПб.: Политехника, 215.
- ↑ MacDougall J. D. Hypertrophy and Hyperplasia // In: The Encyclopedia of Sport Medicine. Strength and Power in Sport. — Bodmin, Cornwall: Blackwell Publishing, 2003.
- ↑ Gibala, M.J., MacDougall J.D., Tarnopolsky M.A., Stauber W.T., Elorriaga A. Changes in human skeletal muscle ultrastructure and force production after acute resistance exercise // Journal of Applied Physiology. — 1995. — С. 702-708.
- ↑ MacDougall J.D., Elder G.C.B., Sale D.G., Moroz J.R. & Sutton, J.R. Effects of strength training and immobilization on human muscle fibers // European Journal of Applied Physiology. — 1980. — № 43. — С. 25–34.
- ↑ Язвиков В.В. Влияние спортивной тренировки на состав мышечных волокон смешанных скелетных мышц человека // Теория и практика физической культуры. — 1988. — № 2. — С. 48-50.
- ↑ Язвиков В.В., Морозов С.А., Некрасов А.Н. Корреляция между содержанием медленных волокон в наружной широкой мышце бедра и спортивными результатами // Физиология человека. — 1990. — Т. 16, № 4. — С. 167-169.
- ↑ Goldbeig et al., 1975
- ↑ Wong, Booth, 1990; Chcsley ct al., 1992; Biolo ct al., 1995; Philips ct al., 1997
- ↑ Laurent et al., 1978; Wong, Booth, 1990
- ↑ Frederickson, Sonebcig, 1993; Wada ct al., 1996
- ↑ Biolo et al., 1997
- ↑ Cheek, 1985; Hall, Ralston, 1989; Allen ct al., 1999
- ↑ Goldberg et al., 1975; Cabric, James, 1983; Winchester, Gonyea, 1992; Allen et al., 1995; Kadi, 2000
- ↑ Kadi et al., 1999а; Kadi, 2000
- ↑ Hikida et al., 1998; Kadi, Tomcll, 2000
- ↑ Hawke, T.J., and D. J. Garry. Myogenic satellite cells: physiology to molecular biology. Journal of Applied Physiology. 91: 534-551, 2001.
- ↑ Egginton, 1987; Salmons, 1992
- ↑ Basin et al., 1996
- ↑ Powers, Florini, 1975; Rogozkin, 1979
- ↑ Kadi et al., 1999b
- ↑ Kadi et al., 1999b
- ↑ Galavazi, Szirmai, 1971; Sassoon, Kelley, 1986; Joubcrt, Tobin, 1989; Joubert, Tobin, 1995
- ↑ Kadi et al., 1999b
- ↑ Doumit et al., 1996
- ↑ Douglas R. Bolster, Leonard S. Jefferson and Scot R. Kimball. Regulation of protein synthesis associated with skeletal muscle hypertrophy by insulin-, amino acid- and exercise-induced signaling. Department of Cellular and Molecular Physiology, The Pennsylvania State University College of Medicine, PO Box 850, Hershey, PA 17033, USA