Переваривание и усвоение жиров
Содержание
Переваривание и усвоение жиров[править | править код]
Среднее потребление жиров(масло животное и растительное, маргарин, молоко, мясо, сосиски, яйца, орехи и т. д.) составляет примерно 60-100 г в сутки, но существуют большие индивидуальные вариации (10-250 г в сутки). Большинство жиров в пище (90%) - это нейтральные жиры, или триацилглицериды (триглицериды). Остальные жиры -это фосфолипиды, эфиры холестерина и жирорастворимые витамины (витамин A, D, Е и К). Более 95% липидов обычно всасываются в тонком кишечнике.
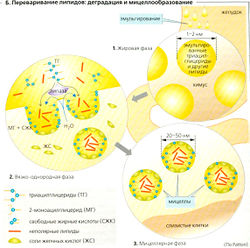
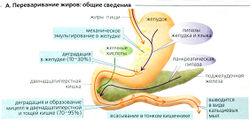
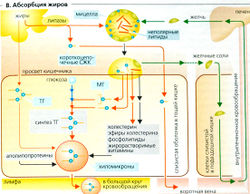
Переваривание жиров (А). Липиды плохо растворяются в воде, и поэтому для их переваривания в водной среде желудочно-кишечного тракта и для последующего всасывания и транспорта в плазму крови требуются специальные механизмы. Хотя недеградированные триацилглицериды могут всасываться в небольших количествах, жиры пищи должны быть гидролизованы ферментами перед тем, как они смогут эффективно всосаться. Для оптимальной ферментативной активности требуется предварительная механическая эмульгация жиров (в основном в дистальной части желудка), поскольку липидные капли в эмульсии (1-2 мкм; Б1) имеют гораздо большую (относительную к массе жиров) поверхность для работы липаз.
Липазы - ферменты, растворяющие жиры, вырабатываются железами языка, дна желудка (главные клетки и слизистые клетки шейки) и поджелудочной железы (А). Примерно 10-30% пищевых жиров гидролизуется в желудке, а остальные 70-90% расщепляется в двенадцатиперстной кишке и верхней части тощей кишки. Липазы из языка и желудка имеют кислый оптимум pH, а липазы поджелудочной железы - pH 7-8. Липазы становятся активными в области контакта жира (масла) с водой (Б). Панкреатическая липаза (триацилглицеролгидролаза) проявляет липолитическую активность (максимальная скорость липолиза 140 г жира/мин) в присутствии колипаз и Са2+. Проколипазы из сока поджелудочной железы, будучи активированы трипсином, образуют липазы. В большинстве случаев панкреатические липазы расщепляют триацилглицериды (ТГ) по первой и третьей сложноэфирной связи. Этот процесс требует присутствия воды и приводит к образованию свободных жирных кислот (СЖК) и 2-моно-ацилглицерида.
При этом вокруг фермента формируется вязко-однородная фаза с водной и гидрофобной зонами (Б2). Избыток Са2+ или дефицит моноацилглицерида приводит к превращению жирных кислот в кальциевые мыла, которые потом выводятся.
Фосфолипаза А2 (образуется из профосфолипазы А3 панкреатического сока при активации трипсином) расщепляет вторую сложноэфирную связь фосфолипидов (в основном фосфатидилхолина = лектина), содержащихся в мицеллах. Для этой реакции требуется присутствие желчных солей и Са2+.
Неспецифичная карбоксилэстераза (= неспецифичная липаза = гидролаза эфиров холестерина) из панкреатического секрета воздействует на эфиры холестерина в мицеллах, а также на все три эфирные связи ТГ и эфирные связи витаминов A, D, Е.
Эта липаза также присутствует в женском грудном молоке (но не в коровьем), и поэтому вскормленные грудью младенцы получают пищеварительные ферменты, требующиеся для расщепления молочного жира вместе с молоком матери. Поскольку ферменты чувствительны к теплу, пастеризация грудного молока значительно уменьшает способность младенцев переваривать молочные жиры.
2-Моноацилглицериды, длинноцепочечные свободные жирные кислоты и другие липиды агрегируют с желчными кислотами и спонтанно формируют мицеллы в тонком кишечнике (БЗ). (Поскольку короткоцепочечные жирные кислоты более полярны, они могут всасываться непосредственно и не нуждаются в желчных кислотах или мицеллах.) Диаметр мицелл составляет всего 20-50 нм, отношение поверхность/объем у них примерно в 50 раз больше, чем у липидных капель в эмульсии. Они облегчают плотный контакт между продуктами расщепления жиров и стенкой тонкого кишечника и, следовательно, важны для всасывания липидов. Полярный конец участвующих в процессе веществ (в основном конъюгированных желчных кислот, 2-моноацилглицерида и фосфолипидов) обращен в водную среду, а неполярная - внутрь мицелл. Полностью неполярные липиды (например, эфиры холестерина, жирорастворимые витамины и липофильные яды) находятся внутри мицелл. Таким образом, неполярные липиды во время всех этих процессов остаются в липофильном окружении до тех пор, пока не достигают липофильной щеточной каймы (микроворсинок) мембран эпителия. Там они абсорбируются клетками слизистой путем либо растворения в мембране, либо пассивного транспорта (например, в случае свободных жирных кислот при помощи переносчиков). Хотя всасывание жиров завершается к тому моменту, когда химус достигает конца тощей кишки, желчные кислоты, высвобождающиеся из мицелл, абсорбируются только в конце подвздошной кишки и затем рециркулируют (внутрипеченочная циркуляции).
Распределение и хранение жиров[править | править код]
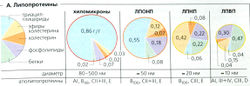
Липиды в крови транспортируются в виде липопротеинов, ЛП (А), представляющих собой агрегаты молекул (микроэмульсии) с центральной частью из сильногидрофобных липидов, таких как триацилглицерид (ТГ) и сложные эфиры холестерина (СНО-эфиры), окруженных слоем амфипатических липидов (фосфолипиды, холестерин). Липопротеины содержат также некоторые типы белков, называемых аполипопротеинами. Липопротеины различны по размеру молекул, плотности, липидному составу, а также участкам синтеза и составу аполипопротеинов. Аполипопротеины (Аро) функционируют в качестве структурных элементов липопротеинов (например, АроАII и АроВ48), лигандов рецепторов липопротеинов (АроВ100, АроЕ и т. д.) на мембране клеток-мишеней липопротеинов и активаторов ферментов (например, ApoAI и АроСII).
Хиломикроны транспортируют липиды (в основном триацилглицериды, ТГ) из кишечника на периферию (при помощи кишечной лимфы и большого круга кровообращения; Г), где их АроСII активируют эндотелиальную липазу липопротеинов (ЛЯП), которая отщепляет свободные жирные кислоты (СЖК) от ТГ. В основном СЖК абсорбируется миоцитами и жировыми клетками (Г). При помощи АроЕ хиломикронные остатки доставляют остальные триацилглицериды, холестерин и сложные эфиры холестерина в гепатоциты при помощи рецептор-опосредованного эндоцитоза (Б, Г).
Холестерин и ТГ, импортируемые из кишечника, а также синтезированные в печени, экспортируются как фракция ЛПОНП (липопротеины очень низкой плотности) из печени на периферию, где они при помощи АроСII также активируют ЛПСП, приводя к высвобождению СЖК (Г). Это приводит к потерям АроСН и экспозиции АроЕ. Остатки ЛПОНП или ЛПСП (липиды средней, или промежуточной плотности) остаются. Примерно 50% ЛПСП возвращается в печень (в основном в связанном виде - с АроЕ на рецепторах ЛПНП; см. далее), где ЛПСП репроцессируются и экспортируются из печени в виде ЛПОНП (Б).
Другие 50% ЛПСП превращаются в ЛПНП (липопротеины низкой плотности) после контакта с липазой печени (что приводит к потерям АроЕ и экспозиции АроВ100). Две трети ЛПНП доставляют холестерин и эфиры холестерина в печень, а другая треть - во внепеченочные ткани (Б). Связывание АроВ100 с рецепторами ЛПНП необходимо для обоих процессов.
Липопротеины высокой плотности (ЛПВП) обменивают некоторые апопротеины на хиломикроны и ЛПОНП и абсорбируют излишний холестерин из внепеченочных клеток и крови (Б). Вместе с АроА1 они активируют плазматические лецитин-холестеролацилтрансферазы (ЛХАТ), которые ответственны за частичную этерификацию холестерина. ЛПВП также доставляют холестерин и его эфиры в печень и железы, продуцирующие стероидные гормоны и имеющие рецепторы ЛПВП (яичники, семенники, кора надпочечников).
Триацилглицериды (ТГ)[править | править код]
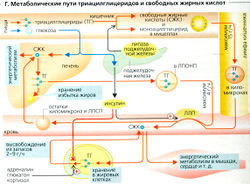
Триацилглицерины, поступающие с пищей, расщепляются на свободные жирные кислоты (СЖК) и 2-моноацилглицерид (МГ) в желудочно-кишечном тракте (В). Поскольку короткоцепочечные свободные жирные кислоты растворимы в воде, они могут быть абсорбированы и транспортированы в печень по воротной вене. Длинноцепочечные жирные кислоты и 2-моноацилглицерин нерастворимы в воде. Они в клетках слизистой оболочки вновь превращаются в ТГ (В). (СЖК, необходимые для синтеза ТГ, переносятся СЖК-связывающими белками от клеточной мембраны к участкам синтеза, т. е. к гладкому эндоплазматическому ретикулуму.) Поскольку ТГ нерастворимы в воде, вслед за этим они включаются в хиломикроны, которые, в свою очередь, экзоцитируются во внеклеточную жидкость, затем проходят в кишечную лимфу (снова проходя через печень), откуда, в итоге, попадают в большой круг кровообращения (В, Г). (Плазма крови становится мутной примерно через 20-30 мин после принятия жирной пищи из-за присутствия в ней хило-микронов.) Печень также синтезирует ТГ, забирая необходимые СЖК из плазмы или синтезируя их из глюкозы. ТГ с ЛПОНП (см. ранее) после этого сек-ретируются в плазму (Г).
Поскольку экспортная емкость этого механизма ограничена, избыток СЖК или глюкозы (Г) может привести к аккумуляции ТГ в печени (жирная печень).
Свободные жирные кислоты (СЖК) представляют собой высокоэнергетические субстраты, используемые для энергетического метаболизма. Жирные кислоты, циркулирующие в крови, существуют в основном в форме ТГ (в составе липопротеинов), а СЖК плазмы образуют комплексы с альбумином. Жирные кислоты удаляются из ТГ хиломикронов и ЛПОНП липазой липопротеинов (ЛЛП) на стороне просвета эндотелия капилляров многих органов (в основном в жировой ткани и мышцах) (Г). АроСН на поверхности ТГ и ЛПОНП активируют ЛЛП. Инсулин, секретируемый после еды, индуцирует ЛЛП (Г), что способствует быстрой деградации реабсорбированых пищевых ТГ. ЛЛП также активируются гепарином (из эндотелиальной ткани, из тучных клеток и т. д.), что позволяет удалить хиломикроны из мутной плазмы; и поэтому он также называется фактором просветления плазмы. СЖК в составе комплексов с альбумином в плазме в основном транспортируются в мишени (Г).
- В сердечную мышцу, скелетную мышцу, почки и другие органы, где они окисляются до СО2 и Н2О в митохондриях (β-окисление) и используются как источник энергии.
- В жировые клетки (Г), которые либо хранят СЖК, либо используют их для синтеза ТГ. При возрастании энергетических потребностей либо снижении поставки СЖК в жировых клетках они отщепляются из триацилглицеридов (липолиз) и транспортируются в те участки, где необходимы (Г). Липолиз стимулируется адреналином, глюкагоном и кортизолом и ингибируется инсулином.
- В печень, где СЖК окисляются или используются для синтеза ТГ.
Холестерин (СНО)[править | править код]
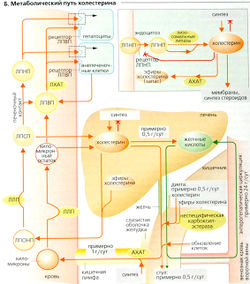
Сложные эфиры холестерина (СНО-эфиры), как и триацилглицериды (ТГ), представляют собой неполярные молекулы. В водной среде организма они могут транспортироваться лишь в составе липопротеинов (или связанными с белками) и могут быть использованы в обмене веществ только после превращения в холестерин, который более полярен (Б). СНО-эфиры служат запасными веществами и в некоторых случаях как транспортная форма СНО. СНО-эфиры присутствуют во всех липопротеинах, но наиболее распространены в ЛПНП (42%) (А).
Холестерин - важный компонент клеточной мембраны. Более того, он предшественник желчных солей (Б), витамина D и стероидных гормонов. В сутки примерно 0,6 г холестерина теряется с фекалиями (в виде копростерина) и выводится через кожу. Количество желчных кислот, теряемых за сутки, составляет около 0,5 г. Эти потери (без учета потребления холестерина с пищей) должны компенсироваться путем постоянного ресинтеза холестерина в желудочно-кишечном тракте и печени (Б). Холестерин, поступающий с пищей, частично усваивается сам по себе, а частично - в этерифицированной форме (Б, справа внизу). До того как он реабсорбируется, эфиры холестерина расщепляются неспецифической панкреатической карбоксилэстеразой до холестерина, который всасывается в верхней части тонкого кишечника (Б, внизу). Клетки слизистой желудка содержат ацил-КоА-холестеринацилтрансферазу (АХАТ) - фермент, реэтерифицирующий всасываемый холестерин, так что и холестерин, и его эфиры могут быть интегрированы в хил омикроны (А). Холестерин и его эфиры СНО в остатках хиломикронов (см. ранее) транспортируются в печень, где ли-зосомальные кислые липазы снова расщепляют эфиры до холестерина. Этот холестерин, а также холестерин из других источников (ЛПНП, ЛПВП) покидают печень (Б) различными способами: 1) путем экскреции в желчь; 2) путем превращения в желчные соли, которые также потом поступают в желчь; 3) путем включения в ЛПОНП — липопротеины печени, экспортирующие липиды в другие ткани. Под действием ЛЛП (см. далее) ЛПОНП преобразуются в ЛПСП и позже в ЛПНП (Б, слева). ЛПНП транспортируют холестерин и его эфиры в клетки с рецепторами ЛПНП (печеночные и внепеченочные клетки; Б, вверху). Плотность рецепторов на поверхности клеток колеблется в соответствии с потребностями в холестерине. Как и печеночные клетки (см. выше), внепеченочные клетки поглощают ЛПНП посредством рецептор-опосредованного эндоцитоза, и лизосомальные кислые липазы переводят эфиры холестерина в холестерин (Б, справа вверху). Затем клетки могут встраивать холестерин в клеточные мембраны или использовать его для синтеза стероидов. Избыток холестерина вызывает (а) ингибирование синтеза холестерина в клетках (З-НМG-СоА-редуктаза) и (б) активацию АХАТ - фермента, зтерифицирующего и запасающего холестерин в форме его эфиров.
Гиперлипопротеинемия[править | править код]
Избыток липидов в крови может отражать увеличение уровня триацилглицеридов и/или холестерина (> 2,0-2,2 г/л сыворотки, этот показатель обнаруживается у примерно каждого пятого жителя западных стран). В наиболее серьезной форме семейная гиперлипопротеинемия (генетический дефект) вызывает увеличенную концентрацию холестерина в крови с самого рождения, что может привести к инфаркту миокарда в юношеском возрасте. Болезнь вызывается генетическим дефектом высокоаффинных рецепторов ЛПНП. Уровень холестерина в сыворотке повышается, поскольку клетки поглощают небольшие количества богатых холестерином липопротеинов низкой плотности (ЛПНП). Внепеченочные ткани синтезируют большие количества холестерина, поскольку З-НМG-СоА-редуктаза не может ингибировать синтез холестерина по причине пониженного всасывания ЛПНП. В результате все больше ЛПНП связывается с низкоаффинными рецепторами, опосредующими всасывание и запасание холестерина в макрофагах, кожных покровах и кровеносных сосудах. Таким образом, гиперхолестеринемия увеличивает риск атеросклероза и коронарной болезни сердца.