Кетоаналоги аминокислот
Содержание
- 1 Кетоаналоги ВСАА (ВСКА) и других аминокислот в спортивной медицине (научный обзор)
- 2 Накопление продуктов азотистого обмена
- 3 Экзогенное поступление кетоаналогов аминокислот (ВСКА) как стратегия уменьшения образования продуктов азотистого обмена при интенсивных и продолжительных тренировках
- 4 Заключение
- 5 Читайте также
- 6 Ссылки
Кетоаналоги ВСАА (ВСКА) и других аминокислот в спортивной медицине (научный обзор)[править | править код]
Авторы: д.м.н. Александр Владимирович Дмитриев, врач-эндокринолог Алексей Александрович Калинчев
Как известно, интенсивные пролонгированные тренировки вызывают катаболические процессы, проявляющиеся распадом белков мышечной ткани, а образующиеся при этом аминокислоты идут на получение энергии. Параллельно драматически растет в крови и в мышцах уровень аммиака. Эти изменения сохраняются более часа после окончания физической нагрузки. Накопление аммиака – негативный фактор, снижающий переносимость тренировок, повышающий усталость и, как следствие, снижающий спортивные результаты. Включение альфа-кетоаналогов аминокислот (ВСКА) в состав НМП спортсменов высшей квалификации с целью замещения части незаменимых аминокислот для снижения образования азотистых «отходов» метаболизма - одно из новых перспективных направлений повышения выносливости и переносимости тяжелых и продолжительных тренировок.
Накопление продуктов азотистого обмена[править | править код]
- Более подробно основная статья: Гипераммониемия при физических нагрузках
Проблема нарастающего накопления продуктов азотистого обмена (ПАО) в крови, мозге и мышцах в процессе больших физических нагрузок является предметом пристального внимания еще с начала 1960-х годов. Аккумуляция аммиака рассматривается в качестве одной из существенных причин усталости нейрогенного происхождения («теория центральной усталости») в спорте, снижающего переносимость нагрузок и результаты выступлений[1][2][3]. Исследования выявили очень важную в теоретическом и практическом плане зависимость уровня накопления аммиака в плазме крови от интенсивности физической нагрузки: минимальные изменения концентрации при интенсивности ниже 50-60% VO2, но быстрое нарастание концентраций при увеличении нагрузок, особенно, на уровне истощения[4][5]. Однако, не только интенсивность, но и продолжительность физической нагрузки определяет нарастание концентрации аммиака. Продолжительные (более 1 часа) субмаксимальные тренировки (60–75% VO2max) способствуют накоплению аммиака за счет разрушения ВСАА в мышцах для получения дополнительной энергии. Существует прямая зависимость физической нагрузки, развития усталости и накопления азотистых продуктов метаболизма на периферии и в ЦНС. Высокие концентрации аммиака повышают скорость наступления усталости, риск развития мышечных судорог, снижают сократительную способность скелетных мышц, замедляют восстановление после нагрузки. Источником избыточного аммиака являются аминокислоты, а для мышечной ткани, в первую очередь, - BCAA, - как доминирующий пул аминокислот. Под воздействием трансаминаз ВСАА теряют аминогруппы, способствуя образованию азотистых продуктов обмена веществ и гипераммониемии.
Экзогенное поступление кетоаналогов аминокислот (ВСКА) как стратегия уменьшения образования продуктов азотистого обмена при интенсивных и продолжительных тренировках[править | править код]
Экспериментальные и клинические исследования показали, что кетоаналоги аминокислот имеют такой же эффект в отношении азотистого баланса, несмотря на то, что содержат меньше азота. Поэтому в формуле ВСКА целесообразно соблюдать те же пропорции, что и при использовании ВСАА, т.е. в соответствии с потребностями организма в незаменимых аминокислотах.
Фармакокинетика и метаболизм кетоаналогов аминокислот при пероральном приеме[править | править код]
У здоровых людей возрастание в плазме кетоаналогов аминокислот отмечается через 10 минут после приема внутрь[6]. Эти уровни примерно в 5 раз выше, чем до начала приема препарата. Пик концентраций приходится на 20-60 минуты, а нормализация уровней наблюдается через 90 минут, но кривые изменений и их величина различны для каждой аминокислоты и ее кетоаналога. В плазме крови отмечается сходное увеличение уровней кетоаналогов и соответствующих аминокислот, показывающих, что процесс трансаминирования кетоаналогов очень быстрый. Таким образом, экзогенное поступление ВСКА приводит к их ускоренной интеграции в естественные процессы метаболизма. Трансаминирование кетоаналогов демонстрируется возрастанием плазменных уровней соответствующих аминокислот. Судьба кетоаналога тесно связана с двойной направленностью активности аминотрансферазы в клетках:
Кетоаналог<> Аминокислота Аминотрансфераза
Активность фермента в направлении кетоаналог>аминокислота ускоряется, когда поступление аминокислоты снижается, а поступление энергии адекватно. Если эти условия не соблюдаются, вместо трансаминирования происходит процесс декарбоксилирования кетоаналогов. Декарбоксилирование необратимо и катализируется специфической дегидрогеназой. Вещества, образующиеся в процессе декарбоксилирования, будут включаться в метаболические пути цикла трикарбоновых кислот, где они используются как субстраты для продукции энергии или сохраняются в форме гликогена и жиров. Важно отметить, что уровни этих двух ферментов низки в печени, в то время как в мышечной ткани они присутствуют в большом количестве. У кетоаналогов и аминокислот, которые имеют разветвленную углеродную структуру, трансаминирование и декарбоксилирование происходят преимущественно в мышцах. Поэтому, по крайней мере часть этих веществ, вводимых перорально, поступает через кровяное русло в мышцы. Фармакокинетические исследования показали, что оптимальная эффективность активности трансаминазы проявляется в условиях значимого снижения поступления незаменимых аминокислот с диетой.
Фармакодинамика (механизм действия) кетоаналогов аминокислот[править | править код]
Кетоаналоги аминокислот (кетокислоты) поддерживают, как и соответствующие АК, нормальный синтез белка в организме (анаболическое действие). Такая компенсация ведет к уравновешиванию позитивного азотистого баланса. Экспериментальные и клинические исследования показали, что кетоаналогов аминокислот имеют такой же эффект в отношении азотистого баланса, что и ВСАА, несмотря на то, что не содержат аминогруппу. Поэтому при формировании формулы кетоаналогов аминокислот количества и пропорции кетоаналогов целесообразно устанавливать в соответствии с потребностями организма в незаменимых аминокислотах, а потребность определять из необходимого количества белка в сутки (ВСКА включаются в общий расчет потребности).
- Отличия по сравнению с незаменимыми аминокислотами. Альфа-кетокислоты имеют сходные углеродные цепочки при отсутствии аминогруппы. Эти аналоги не содержат азот и не образуют азотистые продукты обмена. Альфа-кетокислоты являются акцепторами аминогрупп и могут восстанавливаться в соответствующие аминокислоты в организме. В реакции трансаминирования, которая ведет к такой трансформации, мочевино-образующие аминокислоты, такие как глутамин и аланин, используются как доноры аминогрупп. Таким способом эти аминокислоты уводятся с их мочевино-образующего метаболического пути. Этот процесс вовлекает аминогруппы во вторичную переработку и поддерживает постоянство количества азота. Такой механизм делает возможным захват азота в количестве примерно 35.6 мг на 322 мг ВСКА.
- Специфические свойства некоторых кетоаналогов.
Сохранение азота из-за перехода аминогрупп к кетоаналогам ассоциируется с прямым торможением образования мочевых продуктов. Это торможение особенно свойственно кетолейцину. Угнетение уреагенеза устойчиво сохраняется в течение 8 дней.
- Стимулирование синтеза белка.
Кетолейцин и, возможно лейцин, могут увеличивать синтез белка. Эти вещества вызывают усиление агрегации полирибосом.
- Торможение нарушений белкового обмена.
Кетоаналоги могут задерживать процесс разрушения белков, и, таким образом, оказывать антикатаболическое действие. Кроме того, снижение экскреции белка с мочой вносит вклад в увеличение альбумина сыворотки крови и поддержание нутритивного статуса в нормальных границах.
- Влияние на фосфорно-кальциевый обмен. Применение кальциевых солей кетоаналогов аминокислот позволяет обходиться без дополнительного приема препаратов кальция. Это удобно при параллельном курсе приема витамина D.
- Влияние на нарушения углеводного и жирового обмена. Кетоаналоги повышают чувствительность тканей к инсулину.
- Влияние на метаболический ацидоз. Метаболический ацидоз, возникающий в процессе интенсивных и продолжительных тренировок, играет значительную отрицательную роль в изменениях метаболизма белка, толерантности к глюкозе и обмене в костной ткани. Кетоаналоги аминокислот при хроническом приеме уменьшают проявления ацидоза.
- Антиоксидантные эффекты. Кетоаналоги аминокислот имеют положительное влияние на перекисное окисление липидов мембран эритроцитов, которое возрастает при физических нагрузках, и отражает возрастание продукции окислительных свободных радикалов.
- Влияние на нарушения обмена липидов. ВСКА снижают уровни триглицеридов.
Экспериментальные и клинические исследования кетоаналогов аминокислот при физических нагрузках[править | править код]
В экспериментальном исследовании R.D.de Almeida и соавторов[7] оценивалось влияние однократного (острого) введения кетоаналогов аминокислот на показатели биохимии крови в ответ на физическую нагрузку. Проведена рандомизация животных (крысы) в 4 группы: 1) альфа-кетоаналоги незаменимых аминокислот - ВСКА (коммерческий препарат Кетостерил 0,1 г в 0,5 мл воды, исходя из дозы 0,3 г/кг) без тренировок; 2) тренировки (ежедневно в течение 6 дней); 3) ВСКА + тренировки; 4) контрольная (без ВСКА и тренировок). Тренировки увеличивали содержание аммиака во всех группах, однако на фоне ВСКА оно составило 40%, в то время как в группе без ВСКА – 100%. Параллельно кетоаналоги аминокислот снижали уровень мочевины в крови и усиливали клиренс креатинина, при увеличении содержания лактата крови. Таким образом, однократный прием кетоаналогов аминокислот непосредственно перед физической нагрузкой значительно (в 2,5 раза) снижает гипераммониемию, уровень мочевины в плазме крови. Однако, этого недостаточно для выводов о положительном эргогенном влиянии ВСКА при однократном применении.
В клинической работе E.S.Prado и соавторов[8], которая явилась логическим продолжением экспериментальных исследований этих же авторов, описанных выше, изучалось однократное (острое) применение кетоаналогов аминокислот на физическую готовность профессиональных велосипедистов (n=13) в условиях гипераммониемии, вызванной нагрузками. Необходимо отметить, что все участники в течение 2-х дней до тестирования и день после него находились на кетогенной диете с пониженным содержанием углеводов: 35% общей потребляемой энергии – от протеинов, 55% - от жиров, и 10% - от углеводов. Тренировочные нагрузки составляли в день в среднем 70 км. Объем нагрузок и кетогенная диета применялись с целью снижения запасов мышечного гликогена и получения более высокого уровня аммониемии. В день тестирования участники сдавали лабораторные тесты на пустой желудок и затем получали завтрак и легкий ланч. Через час после ланча участники получали либо 5 таблеток ВСКА (Кетостерил - Ketosteril®; Fresenius, Bad Homburg, Germany), либо 5 таблеток по 200 мг лактозы (контрольная группа) рандомизированным двойным-слепым методом. Суммарное количество компонентов в назначенной дозе Кетостерила составило: альфа-кетоаналог изолейцина 335 мг, альфа-кетоаналог лейцина 505 мг, альфа-кетоаналог фенилаланина 430 мг, альфа-кетоаналог валина 340 мг, альфа-гидроксианалог метионина 295 мг; аминокислоты - L-лизина ацетат 75 мг, L-треонин 265 мг, L-триптофан 115 мг, L-гистидин 190 мг, L-тирозин 150 мг.
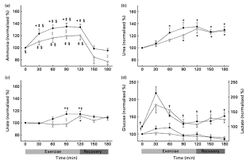
Исследование начиналось через час после приема пищевых добавок и включало физическую нагрузку на велотренажере в течение 2-х часов при нормальной температуре окружающей среды и влажности (23 ± 2°C и 60 ± 5 %, соответственно). Регистрировались стандартные показатели функционального состояния (75–85 % от максимальной ЧСС, в среднем 156 ударов/мин). Как видно из верхнего правого графика на рис.1, в контрольной группе отмечалось нарастание концентрации аммиака с 30-ой минуты тестирования, с достижением максимума на 60-90 минуте и его сохранением до 120 минуты. В группе с кетоаналогами АК, изменения развивались позже и не превышали (максимум на 120 минуте) 17% от исходных значений. Таким образом, уровень аммониемии в процессе физической пролонгированой нагрузки снижался на фоне ВСКА почти в два раза по сравнению с контролем. Окончание нагрузки приводило к быстрому снижению уровня аммиака в течение часа. Сходные различия отмечались и в отношении уровней мочевины в крови: ВСКА замедляли нарастание ее концентрации, хотя, в отличие от концентраций аммиака, в период отдыха не происходило нормализации показателей мочевины. Не отмечено различий между двумя группами в динамике концентраций глюкозы и лактата крови. Сопоставление результатов экспериментальных и клинических эффектов применения кетоаналогов аминокислот, позволяет сделать вывод о безусловной способности кетоаналогов аминокислот при однократном (остром) приеме уменьшать гипераммониемию, вызываемую физическими нагрузками, особенно при израсходовании глюкозы в плазме крови и запасов депо гликогена в печени и мышцах. Однако, признаков эргогенного действия ВСКА при однократном применении не наблюдается. Наиболее вероятным биохимическим механизмов снижения образования аммиака при приеме ВСКА на фоне физических нагрузок является связывание кетоаналогами аммиака (образование хелатных соединений) или прямое включение кетоаналогов в цикл Кребса. Кроме того, кетоаналоги аминокислот могут повышать биодоступность глюкозы через глюконеогенез (что менее вероятно, учитывая отсутствие изменений динамики концентраций в крови под действием ВСКА).
В исследовании S.R.Camerino и соавторов[9] у 16 профессиональных велосипедистов показано, что употребление кетоаналогов аминокислот (препарат «Кетостерил» (12-24 таблеток в день; содержание ВСКА в одной таблетке: альфа-кетоаналог изолейцина 67 мг; альфа-кетоаналог лейцина 101 мг; альфа-кетоаналог валина 86 мг; альфа-кетоаналог фенилаланина 68 мг) в течение 2-х дней, предшествующих тренировочному заезду, полностью устраняет повышение уровней аммиака по сравнению с плацебо-группой (+70% в плазме крови в течение 2-х часового интенсивного непрерывного тренинга при максимальной нагрузке на велотренажере). Только к концу теста в группе с кетоаналогов аминокислот отмечена тенденция к возрастанию концентрации уратов в крови. В обеих группах отмечалось одинаковое накопление лактата. Однако, в данной работе этот факт не отразился на когнитивных и моторных функциях спортсменов.
В рандомизированном двойном-слепом плацебо-контролируемом (РДСПК) клиническом исследовании у 33 молодых мужчин[10] уже при курсовом (4-х недельном) приеме кетоаналогов аминокислот с разветвленной цепью в дозе 0,2 г/кг/день выявлено значительное увеличение переносимости тренировок, повышение основных показателей физической готовности (эргогенный эффект) и стрессоустойчивости. Каждая тренировочная сессия состояла из двух частей: 30-минутный бег на выносливость с последующими тремя спринтами по 3 минуты (с максимальной скоростью для участников на беговой дорожке , ЧСС ? 95%). Эта интенсивность тренировки на выносливость была установлена в соответствии с ЧСС на уровне индивидуального анаэробного порога (IAT), определяемого в тесте на беговой дорожке (см.ниже). Тренировочная программа продолжалась в течение 4-х недель с пятью сессиями каждую неделю под врачебным контролем. После фазы тренировки участники получали неделю на восстановление. В ходе восстановительной фазы не проводились специальные тренировки, а участники вели обычный активный образ жизни. В работе использовались три вида пищевых добавок (в соответствии с группами рандомизации) в виде гранулята (диаметр гранул около 2 мм), растворяемого в воде перед употреблением. Раствор гранулята принимался весь период исследования от момента начала тренировок до окончания периода восстановления (5 недель) два раза в день – за 2 часа до и через 2 часа после тренировки. Смесь N1 (группа 1) содержала: альфа-кетоглутарат (AKG, 0,2 г/кг веса/день; смесь Na-AKG 144,66 мг/кг/день, что соответствует 127,6 мг/кг/день AKG, и 91,33 мг/кг/день Ca-AKG, что соответствует 72,4 мг/кг/день AKG). Смесь N2 (группа 2) содержала три альфа-кетоаналога ВСАА (BCKA) в дозе 0,2 г/кг/день: ?-кетоизокапроат (?-ketoisocaproate, KIC) - 47.4%; ?-кетоизовалериат (?-ketoisovalerate, KIV) - 30.0% и ?-кетометилвалериат (?-ketomethylvalerate, KMV) - 22.6%). Смесь N3 (группа 3) содержала плацебо, эквивалентное смесям 1 и 2 по энергетической ценности, содержанию натрия и кальция. Все параметры фиксировались трижды (рис.6, схема исследования): перед тренировкой (Тест 1) – исходные значения); после 4-х недель тренировок (Тест 2); в конце 1-ой недели восстановления (Тест 3).
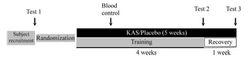
Время тренировок за неделю рассчитывалось как сумма времени бега на выносливость и времени спринтов, соответственно протоколу (рис.2). На велоэргометре определялось VO2max (тест «до истощения») и максимальная мощность (Pmax). Беговая готовность оценивалась в стандартном тесте на беговой дорожке (наклон 1,5%; начальная скорость 6 км/час с увеличением на 2 км/час каждые 3 минуты) до истощения. Готовность рассчитывалась, исходя из взаимосвязи регистрируемой мощности и изменениями концентрации лактата. Изометрический максимальный вращающий момент (Tmax_ISM) и изокинетическая максимальная готовность (Pmax_ISK) четырехглавой мышцы бедра доминирующей ноги определялись на динамометре (Isokinetic BIODEX Dynamometer (Biodex Medical Systems, USA); максимальные величины брались из трех попыток. Показатели стресса и восстановления определялись на основе специального опросника (RESTQ-Sport, шкала от 0 до 5) еженедельно. Диета для всех трех групп была одинаковой (выравнивание диет – обязательное условие проведения исследований такого рода): 2509±115 ккал/день; 49,2% углеводов, 30,3% жиров; остальное – протеины. Примерно одинаковыми были и другие регистрируемые показатели: ИМТ, жировая масса (16%), концентрации в плазме крови глюкозы (4,7 ммол/л), холестерола (4,3 ммол/л), триглицеридов (1,6 ммол/л) и С-реактивного белка (0,8 мг/л). В течение первых двух недель тренировок между группами не отмечалось различий в регистрируемых показателях. Однако, начиная с третьей недели в контрольной группе все временные показатели начинали снижаться, оставаясь неизменными в группах с AKG и ВСКА (рис.3). Суммарный объем работы, выполняемый контрольной группой во второй половине исследования был достоверно ниже, чем в группах с альфа-кетоаналогами аминокислот. Во всех группах в процессе тренировок возрастал VO2max без достоверных отличий в ходе трех тестирований. В группах с кетоаналогами Рmax после периода восстановления достоверно возрастала, но в контрольной группе достоверных изменений не выявлено. Изометрический максимальный крутящий момент не изменялся в контрольной группе после тренировки и восстановления, но достоверно увеличивался после периода восстановления в группах с AKG и ВСКА (рис.4). Сходные изменения получены и в отношении производительности мышц по результатам изокинетических измерений (рис.5).
Рис.3. Суммарное время способности выполнения тренировочного задания (ось ординат, минуты; подробные объяснения в тексте) в исследовании Y.Liu и соавторов (2012) в контрольной группе (левые столбики), в группе, принимавшей AKG (средние столбики) и в группе, принимавшей ВСКА (правые столбики). Светлые столбики – 1-ая неделя исследования; столбики с точками – 2-ая неделя исследования; столбики со штриховкой – 3-я неделя; темные столбики – 4-ая неделя
Рис.4. Величины пика изометрического крутящего момента (ось ординат) в различные фазы выполнения тренировочного задания в исследовании Y.Liu и соавторов (2012) в контрольной группе (левые столбики), в группе, принимавшей AKG (средние столбики) и в группе, принимавшей ВСКА (правые столбики). Светлые столбики – перед тренировкой; столбики с точками – после тренировки; столбики со штриховкой – после периода восстановления.
Рис.5. Величины пика изокинетической производительности мышц (ось ординат) в различные фазы выполнения тренировочного задания в исследовании Y.Liu и соавторов (2012) в контрольной группе (левые столбики), в группе, принимавшей AKG (средние столбики) и в группе, принимавшей ВСКА (правые столбики). Светлые столбики – перед тренировкой; столбики с точками – после тренировки; столбики со штриховкой – после периода восстановления.
По данным RESTQ-Sport-анализа уровень стресса существенно возрастал в контрольной группе в течение третьей недели тренировок, но не изменялся в ВСКА- и AKG-группах. Очень похожим образом, эмоциональные (субъективные) показатели усталости достигали максимальных значений на 3-ей неделе тренировок в контрольной группе, но достоверно не изменялись в группе, принимавшей ВСКА. В AKG-группе отмечено умеренное повышение данных показателей во все периоды тренировок, а также в фазе отдыха.
Авторы делают заключение, что 4-х недельные пищевые интервенции альфа-кетоаналогов незаменимых аминокислот в составе диеты в дозе 0,2 г/кг/день (соответствует 14 г аминокислот/белка на 70 кг веса тела) оказывают, начиная с третьей недели тренировок, достоверное и выраженное положительное влияние на объем выполняемой тренировочной работы, максимальную мощность и общее функциональное состояние мышц, снижает субъективные негативные эмоциональные ощущения от физической нагрузки и чувство усталости, и ускоряет восстановление. Все эти факторы улучшают переносимость максимальных тренировочных нагрузок.
Таким образом, кратковременное применение альфа-кетоаналогов аминокислот (ВСКА) устраняет гипераммониемию, но не оказывает эргогенного действия при физических нагрузках. Курсовое назначение (4 недели и более) не только купирует гипераммониемию, но и оказывает отчетливое эргогенное действия, проявляющееся в повышении силы и выносливости.
На сегодняшний день альфа-кетоаналоги аминокислот (ВСКА) более известны своими положительными эффектами в нефрологии (препарат Кетостерил), где они применяются уже много лет у пациентов с хронической болезнью почек (ХБП) в сочетании с малобелковой диетой для усиления противоазотемического эффекта диетотерапии, торможения процесса накопления аммиака и отдаления потребности в диализной терапии. Теперь спектр действия этой группы нутритивно-метаболической поддержки (НМП) расширился за счет спортивной нутрициологии.
Тем не менее, исследования ВСКА в профессиональном спорте находятся только в начальной стадии. Требуются исследования в других видах спорта, в различных тренировочных режимах и условиях, сочетания с другими макро- и фармаконутриентами. Важно определить, какая суммарная доля белка (включая аминокислоты) может быть заменена на ВСКА для максимизации эргогенного эффекта протеиновой составляющей в диете.
Заключение[править | править код]
Включение альфа-кетоаналогов незаменимых аминокислот в состав НМП (замещение ими части незаменимых аминокислот, в первую очередь, ВСАА в дневном рационе) спортсменов высшей квалификации - одно из перспективных направлений повышения выносливости и переносимости тяжелых и продолжительных тренировок. Идея замены ВСАА их кетоаналогами с целью снижения нагрузки организма азотистыми «отходами» принадлежит нефрологам. Альфа-кетоаналоги лейцина изолейцина и валина (коммерческий продукт «Кетостерил»), лишенные аминогруппы, имеют ту же ценность в плане синтеза белка, что и ВСАА, но не только не способствуют образованию аммиака и других азотистых продуктов, но и связывают аминогруппы других аминокислот (процесс обратного трансаминирования). В нефрологии эти свойства альфа-кетоаналогов (ВСКА) позволяют остановить прогрессию хронической болезни почек (ХБП), отсрочить начало диализной терапии. ВСКА используются по этому показанию уже не первый десяток лет во многих странах мира. Принципиальным отличием ситуации в нефрологии от спорта является сочетание ВСКА с низкобелковой и очень низкобелковой диетой при лечении ХБП. В спорте мы имеем дело с повышенным потреблением белка и заменой части этой усиленной протеиновой диеты добавками ВСКА при сохранении общего объема потребления протеинов.
В спортивной медицине исследование ВСКА ведется всего несколько лет. Экспериментальные и клинические исследования показали, что ВСКА имеют такой же эффект в отношении азотистого баланса, несмотря на то, что содержат меньше азота. Поэтому при формировании формулы ВСКА количества и пропорции кетоаналогов целесообразно устанавливать в соответствии с потребностями организма в незаменимых аминокислотах, а потребность определять из необходимого количества белка в сутки (ВСКА включаются в общий расчет потребности). Однократный прием ВСКА непосредственно перед физической нагрузкой значительно (в 2,5 раза) снижает гипераммониемию, уровень мочевины в плазме крови, но не оказывает эргогенного действия. В то же время, как показало рандомизированное двойное-слепое плацебо-контролируемое (РДСПК) клиническое исследование Y.Liu и соавторов[10], при курсовом (4-х недельном) приеме ВСКА в дозе 0,2 г/кг/день наблюдается не только купирование гипераммониемии, но и значительное увеличение переносимости тренировок, повышение основных показателей физической готовности (эргогенный эффект) и стрессоустойчивости. Таким образом, на сегодняшний день предлагается следующая схема применения ВСКА: 4-6-х недельные пищевые интервенции альфа-кетоаналогов незаменимых аминокислот (коммерческий вариант «Кетостерил») в составе регулярной диеты в дозе 0,2 г/кг/день (соответствует 14 г аминокислот/белка на 70 кг веса тела; примерно 10% общей потребности в белке в сутки), разделенной на 2 или 4 приема (до и после тренировки).
Надо учитывать, что исследования ВСКА в профессиональном спорте находятся только в начальной стадии. Требуются анализ эффективности в разных спорта при различных тренировочных режимах (аэробные и анаэробные нагрузки), в условиях сочетания с другими макро- и фармаконутриентами, и многое другое. Важно определить, какая суммарная доля белка (включая аминокислоты) может быть заменена на ВСКА (насколько больше 10%) для максимизации эргогенного эффекта протеиновой составляющей в диете.
Читайте также[править | править код]
- BCAA: научный обзор
- L-карнитин: научный обзор
- АТФ: научный обзор
- Бета-аланин: научный обзор
- Глутамин: научный обзор
- HMB: научный обзор
- Донаторы оксида азота: научный подход
- Креатин: научный обзор
- Нейростимуляторы и нейропротекторы в спортивном питании: научный обзор
- Омега-3 жирные кислоты: научный обзор
- Омега-5 жирные кислоты: научный обзор
- Омега-7 жирные кислоты: научный обзор
- Спортивные напитки: научный обзор
- Препараты витамина D в спортивной медицине: научный обзор
- Протеолитические ферменты
Ссылки[править | править код]
- ↑ Lowenstein J.M. Ammonia production in muscle and other tissues: the purine nucleotide cycle. Physiol.Rev., 1972, 52:382-414.
- ↑ Much B.J.C., Banister E.W. Ammonia metabolism in exercise and fatigue; a review. Med.Sci.Sports Exerc., 1983, 15(1):41-50.
- ↑ Brouns F., Beckers E., Wagenmakers A.J.M., Saris W.H.M. Ammonia accumulation during highly intensive long-lasting cycling: individual observations. Int.J.Sports Med., 1990, 11(Suppl.2): S78-S84.
- ↑ Babij P., Matthews S., Rennie M. 1983. Changes in blood ammonia, lactate and amino acids in relation to workload during bicycle ergometer exercise in man. Eur.J Appl.Physiol., 1983, 50: 405–411.
- ↑ Buono M.J., Clancy T.R., Cook J.R. Blood lactate and ammonium ion accumulation during graded exercise in humans. J. Appl. Physiol., 1984, 57, 135–139.
- ↑ Schauder P. Pharmacokinetic and metabolic interrelationships among branched-chain keto and amino acids in humans. J.Lab.Clin.Med., 1985, 106(6):701-707.
- ↑ de Almeida R.D., Prado E.S., Llosa C.D. et al. Acute supplementation with keto analogues and amino acids in rats during resistance exercise. Br.J.Nutr., 2010, 104(10):1438-1442.
- ↑ Prado E.S., de Rezende Neto J.M., de Almeida R.D. et al. Keto analogue and amino acid supplementation affects the ammonaemia response during exercise under ketogenic conditions. Br.J.Nutr., 2011, 105:1729–1733.
- ↑ Camerino S.R., Lima R.C., Franca T.C. et al. Keto analogue and amino acid supplementation and its effects on ammonemia and performance under thermoneutral conditions. Food Funct., 2016, 7(2):872-880.
- ↑ 10,0 10,1 Liu Y., Lange R., Langanky J. et al. Improved training tolerance by supplementation with ?-Keto acids in untrained young adults: a randomized, double blind, placebo-controlled trial. J. Intern.Soc.Sports Nutr., 2012, 9:37-46.



